Introducción
COVID-19 simplifica el término “enfermedad por coronavirus 2019”. La enfermedad cambió su nombre oficialmente a COVID-19 (coronavirus disease) el 11 de febrero del presente año. Esta es una patología causada por el virus llamado SARS-COV-2, del inglés severe respiratory acute syndrome 21,2. La COVID-19 fue descrita a finales de diciembre de 2019 en pacientes de la ciudad de Wuhan, provincia Hubei, China. El 9 de enero del presente año, el Centro Chino para el Control y la Prevención de Enfermedades (CDC), informó el descubrimiento del nuevo coronavirus, y el 12 de enero dieron a conocer la secuencia genómica del nCoV-2019 3,4. En menos de tres meses fue declarada pandemia debido a su rápida expansión mundial. El día 11 de marzo, la OMS la declaró como una pandemia mundial 5.
El SARS-COV-2 no se considera una zoonosis, ya que su transmisión es principalmente de humano a humano a través de gotas respiratorias y/o contacto cercano. Esto ocurre cuando una persona infectada tose, estornuda, habla cerca de otra, le da la mano, la abraza, etc. La transmisión fecal-oral también se ha sugerido, así como un mecanismo de transmisión vertical (cada vez más en duda). De igual forma, también es posible contagiarse al tocar una superficie en la que se encuentre el virus y luego tocarse la boca, la nariz o los ojos 6,7. Por consiguiente, el virus se puede contagiar por contacto directo (con una persona infectada) o de forma indirecta (por contacto con superficies contaminadas). Es posible detectar el SARS-COV-2 hasta pasadas 3 horas en aerosoles, 4 en cobre, 24 en cartón y hasta 2 o 3 días en acero inoxidable y en plástico 8. Su periodo de incubación tiene una mediana de 5 a 6 días (rango de 0 a 24 días) 9,10. Aunque en China, con los primeros 425 casos, la media fue de 7,5 ± 3,4 días (IC 95 % 5,3-19) 11.
El promedio del tiempo desde el inicio de los síntomas hasta la recuperación es de 2 semanas en enfermedad leve y de 3 a 6 semanas en casos graves o enfermedad crítica. A su vez, el tiempo entre el inicio de la sintomatología hasta la instauración de los síntomas graves es de alrededor de 1 semana. Mientras que, para llegar a la muerte, riesgo que aumenta con la edad, transcurren 2 a 8 semanas 9. En el diagnóstico, el método de elección para la detección del SARS-COV-2 es la reacción en cadena de polimerasa con transcriptasa reversa en tiempo real (rtRT-PCR, por sus siglas en inglés) 12.
En la actualidad no se dispone de un tratamiento específico para la COVID-19, excepto por las medidas de soporte y la adaptación a las condiciones de cada persona y sus comorbilidades 13. En los casos leves se ofrece el cuidado común a otras infecciones respiratorias virales, además del aislamiento estricto de los infectados. La tasa de letalidad oscila entre el 2,3 y 7,2 %, dependiendo de la edad, el sexo y el estado clínico comórbido de las personas infectadas 14,15.
El objetivo de este artículo se centra en realizar una búsqueda bibliográfica acerca del abordaje (epidemiología, factores de riesgo, fisiopatología, manifestaciones clínicas, diagnóstico y tratamiento) de la enfermedad por COVID-19 en pacientes embarazadas.
Metodología
Se realizó una búsqueda sistemática de la literatura entre enero y junio de 2020 a través de las siguientes bases de datos: EMBASE (Elsevier), Lilacs (Biblioteca Virtual en Salud-Bvs, interfaz iAHx), Medline (PubMed), Science Direct, Cochrane Database of Systematic Reviews (Wiley), dare (Database of Abstracts of Reviews of Effects, Wiley), CENTRAL (Cochrane Central Register of Controlled Trials, Ovid), WHO, ICTRP (International Clinical Trials Registry Platform, ICTRP portal) y Clinical Trials. En la búsqueda se incluyeron artículos originales, reportes de casos, artículos de revisión y ensayos clínicos aleatorizados fase III que testuvieran disponibles completamente para su evaluación y revisión. Se utilizaron los siguientes términos MeSH: “Coronavirus” AND “Pregnancy” AND “Pneumonia” AND “Infectious Disease Transmission, Vertical”. De un total de 471 escritos, se hizo la selección por título y luego por abstract, eligiendo finalmente los artículos incluidos en esta revisión.
Definición
La COVID-19 (enfermedad por coronavirus 2019) es una nueva patología de rápido incremento de infectados y defunciones 16, que se ha convertido en una emergencia de salud pública mundial. Es una patología zoonótica, por lo cual puede transmitirse de animales a humanos. Los coronavirus que infectan a los humanos (HCoV) suelen producir cuadros clínicos variables. Desde el resfriado común hasta otros más catastróficos y graves como los producidos por los virus del Síndrome Respiratorio Agudo Grave (por sus siglas en inglés, SARS) y del Síndrome Respiratorio de Oriente Próximo (MERS-CoV) 17. A pesar de que la información disponible a la fecha acerca de los efectos en las gestantes y su descendencia sigue siendo escasa, la información con la que se cuenta con relación a las consecuencias en las vías respiratorias sirve de guía sobre cómo podría afectar esta enfermedad a la embarazada y al feto en desarrollo 18.
Epidemiología
Se cree que el virus tiene un origen zoonótico y los murciélagos han sido considerados como los directamente responsables 19. En un comienzo, se informó que los casos estaban asociados con la exposición al mercado de mariscos en Wuhan 17,20,21.
En comparación con el SARS y el MERS, el 2019- CoV parece tener una mayor infectividad, pero con una tasa de mortalidad más baja 18, en comparación con el brote de SARS (2002-2003) que tuvo una tasa de letalidad cercana al 10 %, o del MERS que mató al 34,4 % de las personas con la enfermedad (2012 y 2019) 22,23.
La infección se produce cuando una persona enferma tose o estornuda y expulsa partículas del virus (pueden viajar de 1 a 2 metros y depositarse en las superficies) que entran en contacto con otras personas en el entorno. Por lo tanto, el SARS-COV-2 se obtiene respirando las gotas o tocando las superficies contaminadas y luego tocando la nariz, la boca y los ojos. Las personas pueden ser contagiosas mientras los síntomas continúen e incluso después de una mejoría clínica. El virus puede permanecer viable en las superficies durante varios días, si las condiciones ambientales le son adecuadas o favorables, pero se destruye en menos de un minuto por desinfectantes regulares (hipoclorito de sodio y el peróxido de hidrógeno) 24,25.
Los reportes epidemiológicos de mujeres embarazadas con SARS, resultan de publicaciones con pequeñas series. En un estudio publicado por Chen et al. 26 se informó de 9 mujeres diagnosticadas con COVID-19 durante el tercer trimestre del embarazo. Una segunda serie fue publicada por Zhu et al. 27 e incluyó 9 gestantes con 10 bebés (1 embarazo gemelar). Es claro que los informes de mujeres embarazadas diagnosticadas con COVID-19 resultan limitados, por lo tanto existen muy pocos datos disponibles al respecto.
Factores de riesgo
La COVID-19 es una patología nueva, por lo que existe limitada información sobre los factores de riesgo. Se han identificado varias causas que generan mayor peligro, con base en la información actualmente disponible. Los adultos mayores y las personas con afecciones subyacentes graves (de cualquier edad) tienen mayor susceptibilidad de enfermarse delicadamente. A la fecha de hoy, seguimos aprendiendo acerca de la COVID-19. Entre los factores de riesgos más frecuentes, se destacan los detallados en la tabla 1 6,10,28,29.
Tabla 1. Factores de riesgo de enfermedad por COVID-19
| Factores de riesgo en la enfermedad por SARS-COV-2 (COVID-19) | |
|---|---|
| Afecciones cardíacas graves. | Infección VIH (< 350 CD4). |
| Asma. | Inmunosupresión. |
| Diabetes. | Personas que viven en asilos de ancianos. |
| Edad mayor 0 igual a 65 años. | Personas que viven en establecimientos de cuidados a largo plazo. |
| Enfermedad hepática. | Sobrepeso/obesidad. |
| Enfermedad pulmonar obstructiva crónica. | Trastornos de la hemoglobina. |
| Enfermedad renal crónica en diálisis. | Tratamientos inmunosupresores. |
Fuente: Elaboración propia
Fisiopatología
Los coronavirus (COVS) corresponden a un grupo de virus que causan un alto porcentaje de resfriados comunes en humanos. Se les denomina coronavirus por la corona de puntas que se le observa alrededor, en imágenes de microscopía electrónica (la apariencia de la partícula vírica o virión es la de una corona solar). Las puntas corresponden a las glicoproteínas espiga (S), distribuidas en toda la superficie del virus 30,31. El SARS-COV-2 es un virus ARN de cadena sencilla, no segmentado- monocatenario, de polaridad positiva (+SSRNA), de aproximadamente 30.000 pares de bases, de origen zoonótico y perteneciente a la familia Coronaviridae del género betacoronavirus envuelto, subgénero de sarbecovirus, subfamilia Orthocoronavirinae, del orden Nidovirales 30,32. El periodo de incubación suele ser de 4 días, mostrando un rango de 2 a 7 días (IC 95 %: 4,5-5,8 días), extendiéndose hasta 14 días 33, aunque algunas personas pueden tener una incubación más prolongada 34.
El virus SARS-COV-2 ingresa a la célula del huésped, a través de la adherencia de la glicoproteína S a los receptores celulares de la enzima convertidora de angiotensina 2 (ECA). Este receptor se expresa principalmente en células epiteliales del pulmón, corazón, intestino, estómago, vejiga, esófago, riñón y vasos sanguíneos 31. La glicoproteína espiga (S) utiliza sus dos subunidades funcionales para la unión: la subunidad S1 es responsable de la unión con el receptor de la célula hospedero, y la subunidad S2 es responsable de la fusión del virus con las membranas celulares 35,36.
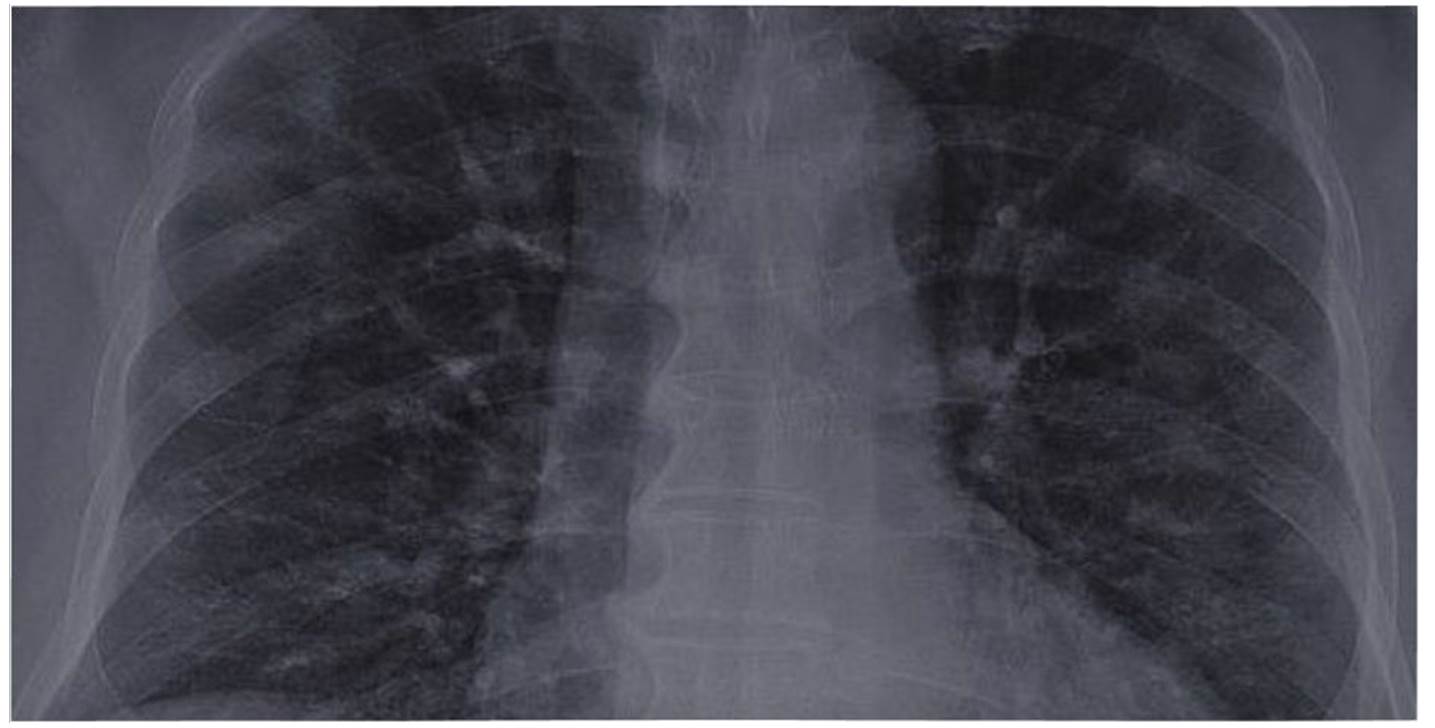
El objetivo principal de la infección por COVID-19 es el tracto respiratorio inferior, causando neumonía grave combinada con evidencias radiológicas de opacidades en vidrio esmerilado 17,37. En la figura 1 se describe una neumonía por COVID-19. Las partículas del virus se propagan a través de la mucosa respiratoria, infectando otras células, e induciendo una tormenta de citoquinas a nivel sistémico, lo cual genera una serie de respuestas inmunes y causan cambios en los leucocitos periféricos (linfocitos) 1.
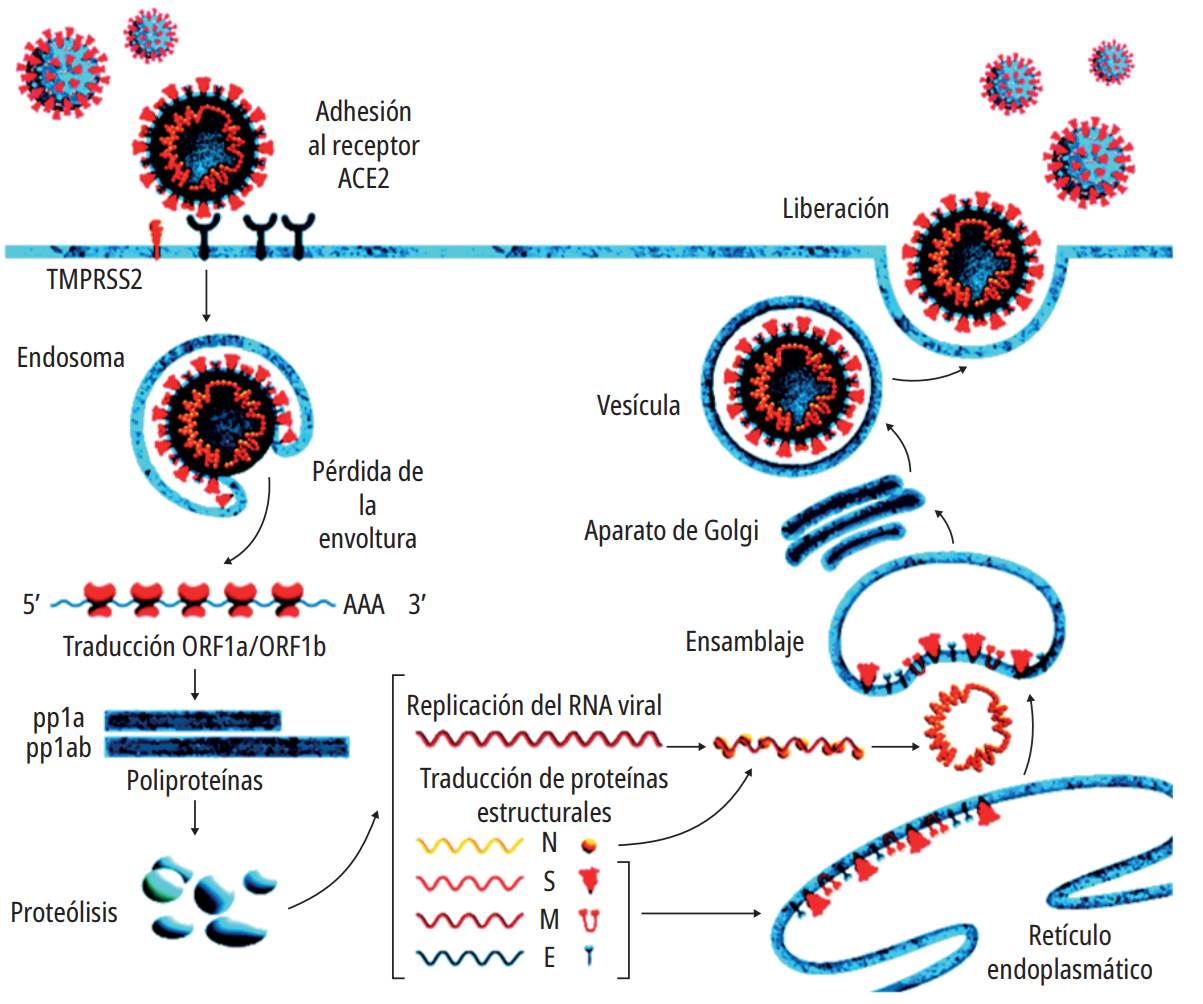
Al finalizar la fusión virus-membrana celular, el ARN genómico viral se libera y permite la formación de las poliproteínas 1a y 1ab, la transcripción de los ARNS subgenómicos y replicación del genoma viral. Los viriones emergen y son trasportados al complejo de Golgi. Donde se ensamblan junto con la nucleocápside para producir nuevas partículas víricas, las que serán exportadas hacia la membrana plasmática celular en forma de vesículas, produciéndose así la liberación del virus por la célula. Posteriormente, este procede a infectar nuevas células en un ciclo repetitivo que culmina con la recuperación o con la muerte de la persona 38,39. La figura 2 resume la replicación del SARS-COV-2.
El SARS-COV-2 causa una respuesta inflamatoria sistémica que se inicia con una tormenta de citosinas (síndrome de “tormenta citoquínica”). La cual consiste en una liberación de grandes cantidades de citocinas pro inflamatorias (IFN-A, IFN-G, IL-1B, IL-6, IL-12, IL-18, IL-33, TNF-a, TGFb, etc.) y quimiocinas (CCL2, CCL3, CCL5, CXCL8, CXCL9, CXCL1O) 23,24. Esto representa un violento ataque del sistema inmune, causando daño alveolar difuso, insuficiencia orgánica múltiple y en los casos graves, la muerte 40.
La unión de SARS-COV-2 a los receptores ECA2 localizados en la superficie de las células alveolares tipo n (AT2), es de vital importancia, debido a que desencadena la cascada inflamatoria en las vías respiratorias inferiores, ocasionando un síndrome de dificultad respiratoria aguda 17,41. En síntesis, el daño alveolar difuso es la lesión patológica pulmonar clásica del Síndrome de Dificultad Respiratoria Aguda, fenómeno que ha sido observado en pacientes fallecidos por neumonía grave por COVID-19 40,42,43.
Manifestaciones clínicas
Se diferencian tres fases en la enfermedad: la fase I, en la que el virus se replica en la mucosa respiratoria y se da la viremia. Se caracteriza por los síntomas de la infección respiratoria (tos seca), viremia (fiebre) y, en el caso de la COVID-19, la gastroenteritis (vómitos y/o diarrea). También suele aparecer linfopenia. En la fase 11, la infección se localiza en el pulmón, pero persisten la tos y la fiebre; la neumonía puede ser leve o cursar con taquipnea e hipoxia (signos de gravedad). Además, se acentúa la linfopenia y ocurre elevación en los niveles de dímero D. A partir de este momento, la evolución puede ser hacia la mejoría, con eliminación del virus y desaparición paulatina de los síntomas; o por el contrario el paciente puede progresar al estado crítico que caracteriza a la fase m: dificultad respiratoria severa (requiere respiración asistida) y signos de respuesta inflamatoria sistémica (SIRS, de Systemic Imflammatory Response Syndrome), con su constelación de signos (fiebre o hipotermia, taquipnea, taquicardia e hipotensión) hasta llegar un shock séptico 44,45. En la figura 3 se resume la gravedad de la enfermedad según la línea de tiempo.
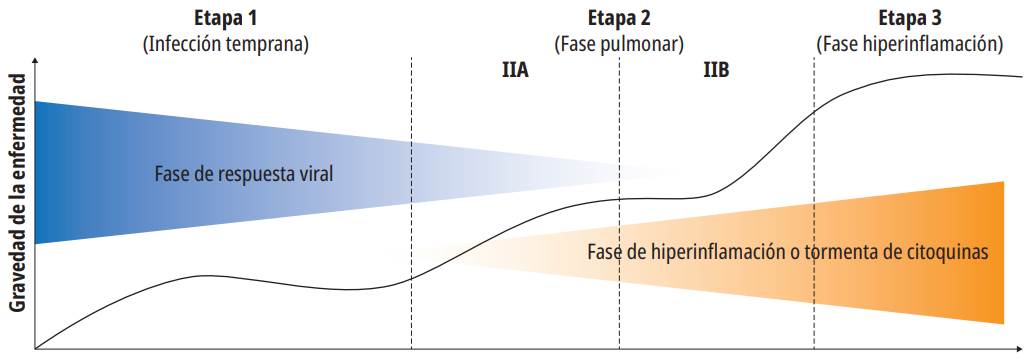
Fuente: modificado de 45.
Figura 3. Gravedad de la enfermedad por COVID-19, según la línea de tiempo.
En el 98 % de los casos, el desarrollo de la sintomatología se toma 11.5 días en promedio (IC 95 %: 8,2-15,6 días). Solo el 1 % de la población desarrolla síntomas posterior a un aislamiento de 14 días. Los síntomas y signos más frecuentes incluyen: fiebre mayor 38° C (83-98 %), tos seca (76-82 %), disnea (31-55 %), astenia (38,1 %), expectoración (33,4 %), dolor de garganta (13,9 %), cefalea (13,6 %), mialgia o artralgia (14,8 %), escalofríos (11,4 %), náuseas o vómitos (5 %), congestión nasal (4,8 %), diarrea (3,7 %), hemoptisis (0,9 %) y congestión conjuntival (0,8 %). La mortalidad oscila entre el 2 a 3 % y hasta un 10 % de los infectados pueden presentar manifestaciones graves 46,47,48. Los reportes acerca de las alteraciones del olfato (anosmia) son variables, pero alrededor del 33,9 % refiere alteración del olfato o del gusto (ageusia) con el 33,3 %, mientras que 18,6 % refieren ambas 49,50. La definición de asintomático, leve, moderado, severo y crítico se resume en la tabla 2.
Tabla 2. Clasificación de los pacientes con COVID-19
Fuente: elaboración propia.
Las mujeres gestantes parecen no tener mayor susceptibilidad para contraer la infección por COVID-19, ni para presentar mayores complicaciones graves. Sin embargo, los datos existentes en la actualidad siguen siendo limitados.
Diagnóstico
El método de elección para la detección del SARS-COV-2 es la reacción en cadena de polimerasa con transcriptasa reversa en tiempo real (rtRT-PCR, por sus siglas en inglés: Quantitative Reverse Transcription Polymerase Chain Reaction). No obstante, también se disponen de pruebas rápidas y simples (con alta sensibilidad y precisión), que pueden realizarse a gran escala 51.
Existen tres tipos de pruebas para el diagnóstico de laboratorio del SARS-COV-2:
Pruebas de detección de ácidos nucleicos (reacción en cadena de la polimerasa o PCR).
Pruebas de detección de antígeno.
Pruebas de detección de anticuerpos (IgG, IgM).
La PCR detecta casos aún en fase asintomática. Mientras que las pruebas serológicas de anticuerpos son más sencillas y económicas que la PCR, destacándose por su gran utilidad epidemiológica y diagnóstica 52,53. La mediana de detección de anticuerpos IgM es de 5 días (rango entre 3 y 6 días). Por su parte, la IgG se detecta a los 14 días (rango entre 10 y 18 días) después del inicio de los síntomas 54.
El protocolo utilizado en Colombia para la detección del virus y diagnóstico de la enfermedad COVID-19 se realiza siguiendo la guía del Ministerio de Salud y Protección Social 55, publicada el 19 de marzo del presente año. Es uno de los autorizados por la OMS, y el recomendado por la Organización Panamericana de la Salud (OPS) 56,57.
Para la toma de laboratorios, ultrasonografía o estudios radiológicos en una gestante con sospecha de infección por COVID-19, esta se ha de conducir con mascarilla y sin acompañante a la zona de aislamiento establecido por la institución donde se encuentre, y el profesional asistencial la atenderá siguiendo el protocolo de protección establecido.
Infección por COVID-19 en las embarazadas
El embarazo es un estado fisiológico que predispone a las mujeres a complicaciones respiratorias. Debido a los cambios fisiológicos en sus sistemas inmunitario y cardiopulmonar, las gestantes tienen más probabilidades de desarrollar una enfermedad grave después de la infección por virus respiratorios 58. En el año 2009, las embarazadas representaron el 1 % de los pacientes infectados con el virus de la influenza A subtipo H1N1, pero representaron el 5 % de todas las muertes relacionadas con H1N1 59.
Actualmente, se sabe que el SARS-COV y el MERS-COV son responsables de complicaciones graves durante el embarazo. Incluida la necesidad de intubación endotraqueal, ingreso a una unidad de cuidados intensivos (UCI), insuficiencia renal y muerte 60,61. Se ha publicado que alrededor del 50 % de las mujeres embarazadas con SARS fueron ingresadas a UCI, 33 % requirieron ventilación mecánica, y la tasa de mortalidad fue tan alta como el 25 % 60. No obstante, a la fecha de hoy, no hay evidencia científica de que las embarazadas sean más susceptibles a la infección por COVID-19 o que aquellas con infección por COVID-19 sean más propensas a desarrollar neumonía grave o complicaciones relacionadas con la infección 62,63. De hecho, las características clínicas de estas pacientes suelen ser similares a las de las no embarazadas con infección por COVID-19 17.
Por otro lado, se ha descrito la fiebre como el síntoma predominante en las gestantes, aunque en algunos casos no se hizo presente sino hasta después del parto (vaginal o cesárea) 62,63. La mayor parte de las mujeres gestantes, de forma usual, no termina en neumonía grave ni requiere UCI 26,64,65,66, e incluso se les ha dado de alta sin complicaciones severas.
En relación a la morbilidad obstétrica, se ha descrito mayor riesgo de aborto espontáneo (32,1 %), parto pretérmino (24,3 %), ruptura prematura de membranas (20,7 %), preeclampsia (16,2 %), restricción del crecimiento fetal (11,7 %), pérdida de bienestar fetal intraparto y muerte perinatal (11,1 %) 26,27,63,67,68. Pero no ha sido detectado la COVID-19 en las placentas de las mujeres analizadas 64,65. De hecho, ninguna mostró cambios sugestivos de corioamnionitis 64.
Por otra parte, se ha descrito que la complicación obstétrica más frecuente es el parto pretérmino con un 41,1 % (IC 95 %: 25,6-57,6), presentando una tasa de mortalidad perinatal del 7 % (IC 95: 1,4-16,3) 63. No obstante, es casi improbable que la infección esté asociada a defectos congénitos.
En opinión de los expertos, es poco probable que el feto esté expuesto a la infección durante el embarazo 26,61,63. En un estudio realizado por Chen et al. 26, las muestras de líquido amniótico, sangre de cordón umbilical, leche materna y de hisopo oro-faríngeo de los neonatos fueron negativas. De igual modo, Li et al. 66 reportaron muestras negativas de líquido amniótico, sangre de cordón umbilical, placenta y leche materna en un estudio realizado en una gestante positiva a SARS-COV-2.
En ese sentido, son muchos los autores que coinciden en reportar la ausencia de transmisión vertical 26,27,64,65,66. No obstante, cabe notar que es probable que la transmisión de la infección, madre-hijo ocurra durante el periodo neonatal. Por ello, se recomienda mantener distancia entre los recién nacidos y sus progenitoras durante los primeros días, para lo que se sugiere que sean alimentados por personas no infectadas, con calostro y leche materna, extraída de la madre 69.
Recomendaciones para el abordaje y tratamiento de las mujeres embarazadas con infección por COVID-19 70,71,72 (algoritmo 1 y 2)
Las unidades de medicina materno-fetal deben organizar lo que será el manejo de gestantes con COVID-19 o sospechosas de la infección. Tanto en el servicio de urgencias obstétricas, como en la zona de preparto/partos, zona de recuperación y/o área de hospitalización de alto riesgo obstétrico y puerperio. Las decisiones deben ser consensuadas entre los equipos de medicina interna, infectología, obstetricia, neonatología y los que sean necesarios.
Las gestantes con síntomas respiratorios deben cumplir con las recomendaciones de asilamiento respiratorio: usar máscara facial, higiene frecuente de manos y esperar en un área apartada, separada y bien ventilada, al menos a 2 metros de distancia de otras personas.
Los casos confirmados y sospechosos de COVID-19 deben confinarse lo antes posible en una sala de aislamiento de infección aérea (sala con medidas de apartamiento correspondiente). Si esta no está disponible, se debe considerar traslado a un hospital con sala de hermetismo de infección aérea.
El embarazo debe considerarse una condición de riesgo, potencialmente mayor y monitorearse de cerca, incluida la frecuencia cardíaca fetal y el monitoreo de la actividad contráctil.
Se ha de considerar la oxigenoterapia temprana (Sa02 ≥95% y/o pO2 70 mmHg).
Usar líquidos intravenosos de manera conservadora a menos que exista inestabilidad cardiovascular.
Se deben investigar otras infecciones respiratorias virales e infecciones bacterianas, debido al riesgo de coinfecciones.
Se ha de tener en cuenta la terapia antimicrobiana empírica, debido al riesgo de infecciones bacterianas superpuestas. Considerando el escenario de una NAC (neumonía adquirida en la comunidad) para definir qué antibióticos se deben iniciar.
Se debe considerar el tratamiento empírico para la influenza en caso de fuerte sospecha de infección, si se tiene un panel viral confirmatorio de neumonía por influenza, o mientras se esperan los resultados de las pruebas de diagnóstico.
No se debe utilizar corticosteroides de rutina. El uso de esteroides para promover la maduración pulmonar fetal, ante inminencia de parto prematuro, se debe individualizar (su uso no produce efectos perjudiciales maternos, sin embargo, existe la controversia respecto a que pueden alterar el despeje del virus). Su aplicación es una decisión consensuada con el infectólogo y el neonatólogo. Es indiscutible que su administración o no, nunca debe demorar la necesidad de finalización del embarazo ante la presencia de una causa materna.
Si se sospecha shock séptico, se ha de instaurar un manejo rápido y dirigido. La paciente debe ser trasladada a una unidad de cuidados intensivos, a fin de brindarle soporte ventilatorio y/o vasopresor en caso de necesitarlo.
Se recomienda la trombo-profilaxis de acuerdo al escenario, balanceando riesgo de sangrado versus trombosis, al momento del embarazo y/o a la fase del trabajo de parto en que se encuentre la paciente.
Las decisiones sobre el parto y la interrupción del embarazo deben basarse en la edad gestacional, la condición materna, la estabilidad fetal y el deseo materno. La infección por COVID-19, no es indicación para finalizar la gestación, a menos que haya necesidad de mejorar la oxigenación materna.
Aunque las series reportadas de gestantes con neumonía e infección por COVID-19 arrojan una tasa de cesárea del 94 % 73, la mayoría realizadas por sospecha de alteraciones del bienestar fetal. No existen estudios donde se demuestre que la cesárea mejore los parámetros ventilatorios al compararla con el parto vaginal.
Siempre que sea posible, la vía del parto debe ser la vaginal. Lo anterior, para disminuir el tiempo del trabajo de parto, con acortamiento del expulsivo, a fin de evitar el agotamiento materno y eventuales complicaciones quirúrgicas innecesarias 74.
El shock séptico, la disfunción orgánica múltiple o el estado fetal insatisfactorio son indicaciones de cesárea o de terminación del embarazo antes de la viabilidad 75.
En las gestantes con trabajo de parto pretérmino espontáneo, no se recomienda la tocolisis para retrasar el parto con el objeto de administrar corticoides 76.
A fin de disminuir el riesgo de transmisión del virus de la madre al neonato, se debe considerar la separación temporal de la madre confirmada o bajo sospecha, permaneciendo aislada hasta que las precauciones de transmisión viral le sean levantadas.
El neonato hijo de madre confirmada con COVID-19 o sospechosa debe ser considerado “persona bajo vigilancia”, y ser protegido para evitar su contagio.
Si no fue posible el aislamiento temporal, la madre confirmada o sospechosa debe realizar higiene de manos y usar mascarilla cada vez que vaya a atender o amamantar a su neonato. En la habitación se debe considerar la mayor separación que sea posible entre la cuna y la cama de la madre.
Recomendaciones para la atención durante el trabajo de parto 70,71,72
El trabajo de parto y la atención del parto en mujeres con infección por COVID-19 se ha de realizar en una sala en aislamiento (con la mínima cantidad de profesionales de la salud); todo el personal que intervenga debe utilizar equipo de protección personal (EPP).
La parturienta debe utilizar mascarilla durante todo el proceso.
Es mandatario la monitorización fetal continua, además del control seriado de signos vitales (frecuencia respiratoria y saturación de oxígeno en forma horaria).
La analgesia neuroaxial no se contraindica. Sin embargo, la anestesia general se ha de evitar a toda costa.
Es útil el clampeo precoz del cordón umbilical y el aislamiento del neonato de la madre. El contacto cercano con la madre puede favorecer el contagio del recién nacido, a pesar de la implementación de medidas de cuidado.
La recuperación postparto inmediata se ha de realizar en la sala de aislamiento.
La analgesia postparto se hará de manera similar a cualquier puérpera.
A la fecha, no existe evidencia de paso de SARS-COV-2 por la leche materna, por eso no se desaconseja la lactancia.
El puerperio debe estar en una unidad dispuesta para hospitalización de pacientes con diagnóstico o sospecha de COVID-19, con el propósito de disminuir la exposición de otras pacientes y recién nacidos.
En mujeres con infecciones asintomáticas o leves, el alta se hará según indicación obstétrica institucional, educándolas sobre las medidas de aislamiento domiciliario y del recién nacido. Se hará el seguimiento vía telefónica, 48 a 72 horas después, y luego a la semana.
Finalmente, la evidencia disponible sugiere que la mayoría de las gestantes pueden pasar la infección por COVID-19, de forma leve o asintomática 77,78. Se ha publicado que un alto porcentaje son asintomáticas (87,9 %) 79, y que la proporción de mujeres embarazadas con enfermedad grave, es similar a la de la población general adulta (86 % leve, 9 % grave y 5 % crítica) 80. Por lo tanto, las gestantes pasarían la enfermedad de forma leve o asintomática, tal como ocurre en el 80 % de la población general. La OMS recomienda la lactancia exclusiva durante los primeros 6 meses de vida, incluso en aquellos casos donde la madre presente la infección por el coronavirus SARS-COV-2 81.
Es enfático recordar que, en relación a la vía del parto, autoridades y sociedades profesionales, como el English Royal College of Obstetricians and Gynaecologists74, y la Society for Maternal-Fetal Medicine63, han adoptado la postura de que la COVID-19 no es una contraindicación para el parto vaginal, aconsejándose el acortamiento del expulsivo.
En mujeres con embarazo menor a 24 semanas la enfermedad se maneja similar a una mujer no gestante, pero se ha de considerar la interrupción del embarazo en caso de que este condicione el manejo de la paciente.
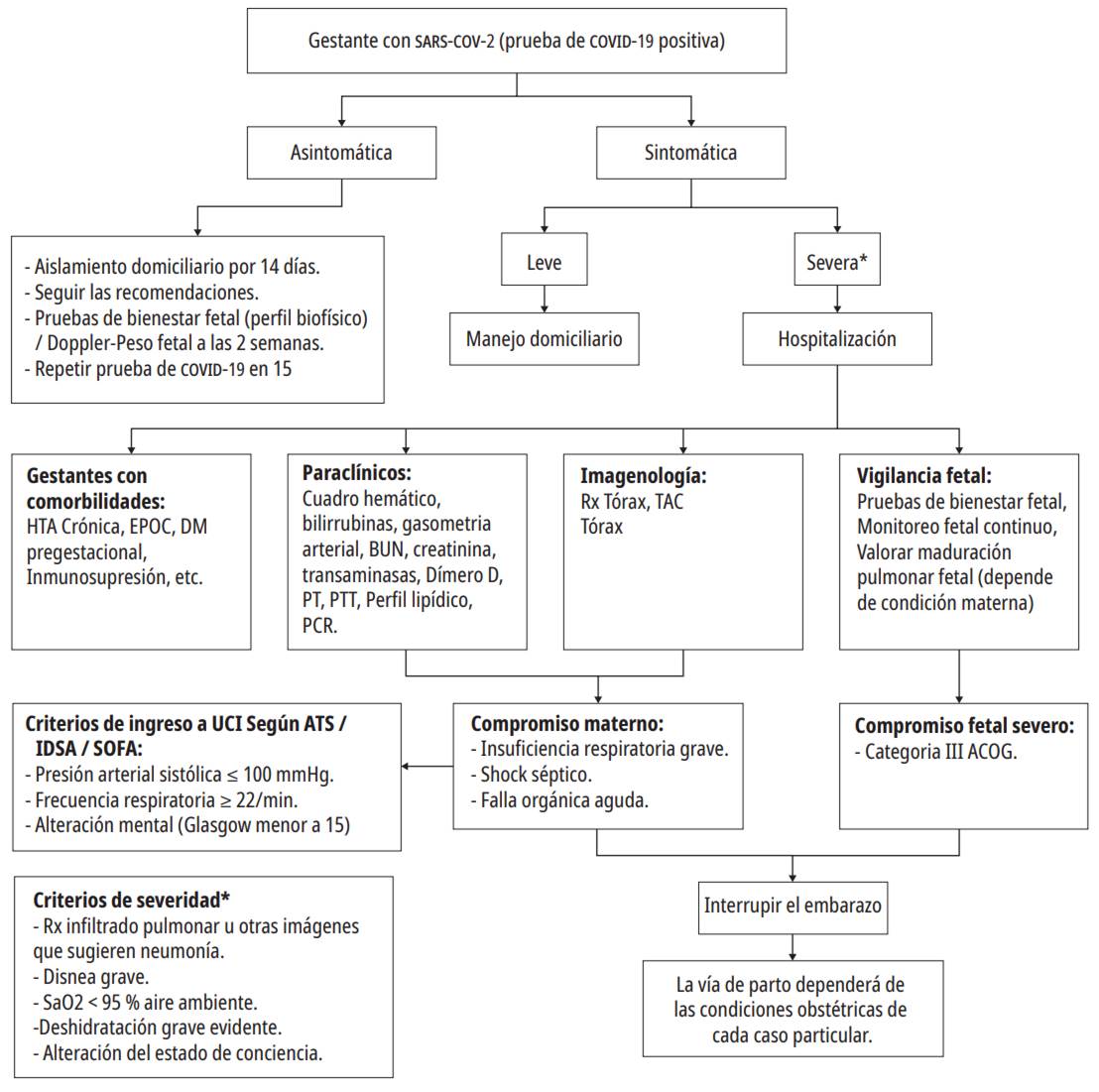
En las figuras 4 y 5 se resume el abordaje de las mujeres embarazadas con sospecha de infección por COVID-19.
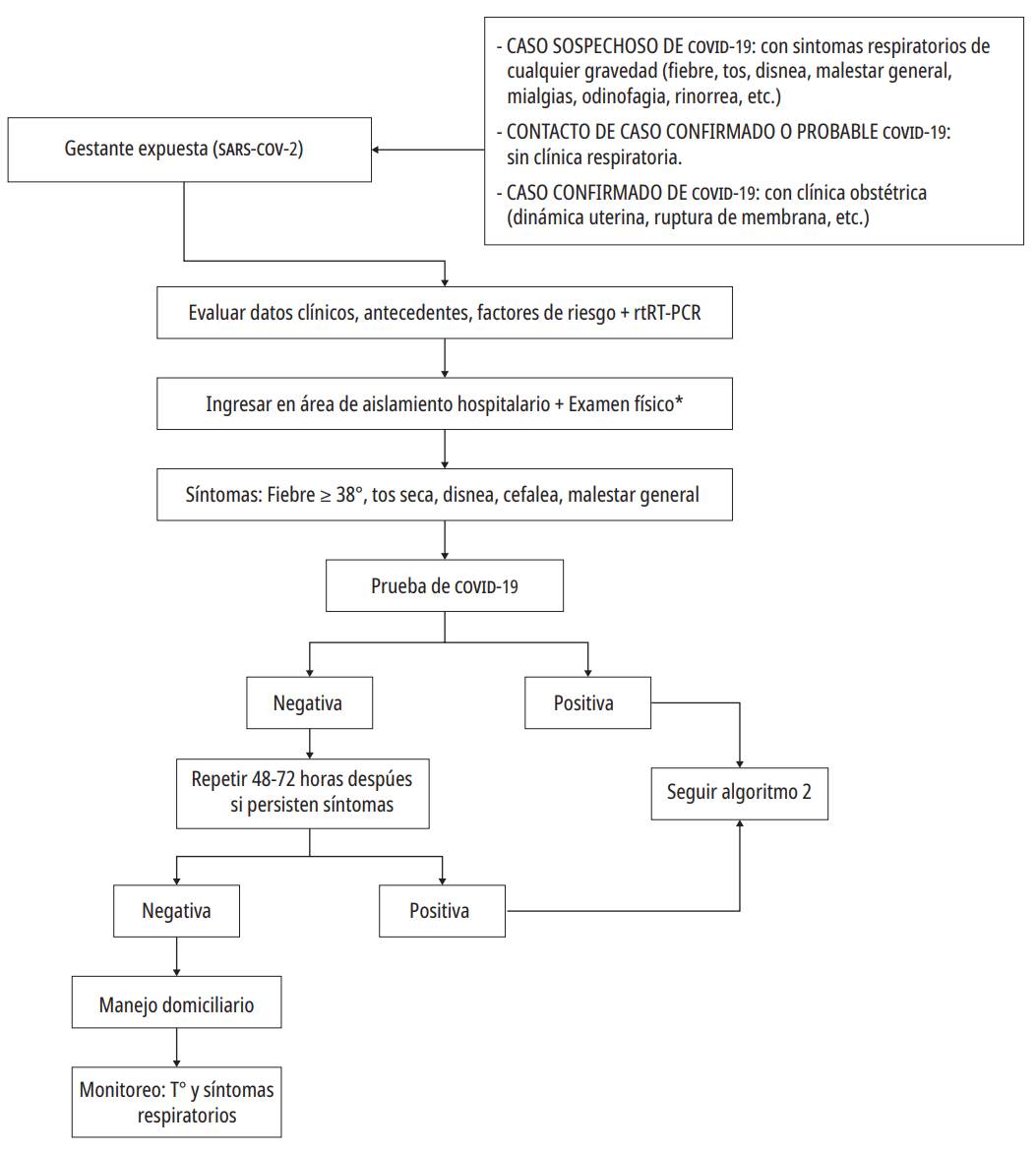
Fuente: elaboración propia.
Figura 4. Algoritmo 1. Manejo de gestante expuesta a infección por COVID-19. Nota: Utilizar los EPP (Equipos de Protección Personal) acorde a protocolo institucional.
Conclusiones
Las mujeres gestantes deben ser consideradas de alto riesgo por sumayor susceptibilidad y debido su respuesta inmune alterada, en especial durante el segundo trimestre. No obstante, parecen tener un curso clínico que no difiere significativamente de la población general. A pesar de que lo hasta ahora descrito se muestra prometedor y favorable, lo que más conviene es la precaución. Por lo tanto, no se deben subestimar los riesgos fetales y maternos frente a la infección materna por COVID-19.
El momento del parto depende de las condiciones de la gestante, la edad gestacional y las condiciones fetales; siendo la vía vaginal la elección predilecta del parto, ya que la transmisión vertical no ha sido documentada, al menos cuando la infección ocurre entre las 25 y 39 semanas de embarazo.
El manejo que se le debe dar a este tipo de pacientes son los tratamientos sintomáticos y de sostén. Se ha de adoptar un enfoque multidisciplinario con el objetivo de hacer una adecuada oxigenación materna; garantizando el equilibrio entre los parámetros necesarios para asegurar el paso de oxígeno a través de la placenta; asegurando una adecuada perfusión útero/placentaria y un óptimo contenido de oxígeno arterial materno. Cabe notar que para esto deben contarse con las medidas de protección adecuadas para los trabajadores de la salud.
Aún hoy, no se ha podido diferenciar si las complicaciones observadas durante la gestación en mujeres con la infección por SARS-COV-2 se debían a la presencia del virus o a complicaciones propias del embarazo. Pero, las características clínicas de las gestantes con infección por COVID-19 durante la última etapa del embarazo son similares a las reportadas por no embarazadas que presentan la infección.
La transmisión de la madre al neonato, en los casos en que ha sucedido, se produce de forma usual, por el contacto estrecho entre ellos después del nacimiento.
Es importante que futuros estudios proporcionen información más detallada sobre las condiciones maternas y fetales, así como la justificación de las intervenciones obstétricas.