Introducción
La intoxicación por medicamentos es un motivo frecuente de consulta en urgencias en el mundo. Los analgésicos no opioides, como el acetaminofén, son un causal destacado para este tipo de intoxicación. Su fácil acceso y bajo costo ocasiona una baja percepción de riesgo. A pesar de que el acetaminofén tiene un amplio rango de seguridad, las intoxicaciones no solo se pueden presentar por el consumo de dosis tóxicas, pues algunos estudios han identificado que incluso con la dosis terapéutica máxima (4g en 24 horas) puede darse la elevación discreta de las enzimas hepáticas. El consumo de estas dosis por más de 4 días puede producir lesión hepática aguda. Asimismo, la ingesta concomitante de otros fármacos que inducen el metabolismo del acetaminofén por vía cyp450 pueden incrementar su toxicidad 1,2.
Los efectos de la ingestión de dosis tóxicas de acetaminofén dependen de factores extrínsecos e intrínsecos del paciente como la dosis consumida, la presencia de comorbilidades, la edad, el tiempo transcurrido entre la ingestión y la administración del tratamiento, entre otros 1,3. El objetivo del presente artículo es transmitir los aspectos importantes para el diagnóstico y tratamiento de la intoxicación por acetaminofén al personal de salud en los servicios de atención primaria.
Metodología de búsqueda
Se realizó una revisión narrativa mediante la búsqueda de artículos a través de las bases de datos Pubmed, Clinical key, Scielo, Google académico, Access medicine y Science direct, utilizando los descriptores: “Acetaminophen” AND “Pharmacology”, “Acetaminophen” AND “poisoning”, “Acetaminophen poisoning” AND “emergency treatment” e “Intoxicación por acetaminofén y Tratamiento farmacológico”. Adicionalmente, se consultaron libros de texto de farmacología y toxicología. Para la búsqueda bibliográfica, se encontraron un total de 5.378 artículos publicados desde el año 2005, de los cuales se obtuvieron 1.486 publicaciones con acceso a texto completo. Finalmente, se tomaron 49 referencias bibliográficas relacionadas con atención primaria en urgencias y 2 publicaciones previas al 2005, debido a que incluían información relacionada con consideraciones especiales en la intoxicación por acetaminofén.
Epidemiología
Según el Sistema de Vigilancia Epidemiológica (SIVIGILA), del Instituto Nacional de Salud de Colombia, entre los años 2008 a 2020 se reportaron 348.302 casos de intoxicación por sustancias químicas. De los cuales 99.631 se relacionaron con medicamentos, con un promedio de 7.663 casos por año, ocupando el primer lugar de consulta. Sin embargo, nuestro país no cuenta con un reporte consolidado de los casos de intoxicación por acetaminofén. La figura 1 resume las consultas a urgencias por intoxicaciones según los grupos de sustancias químicas relacionados 4.
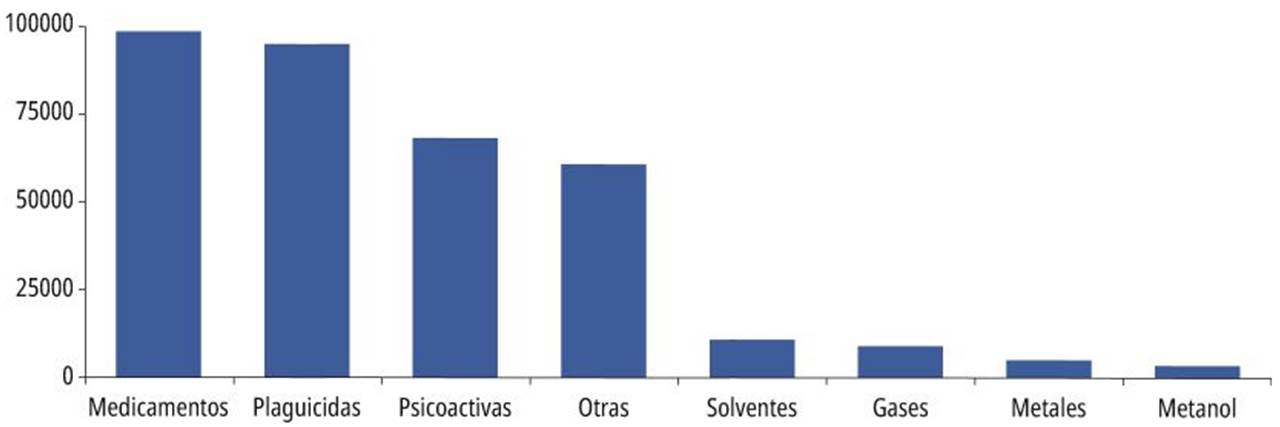
Fuente: elaboración propia
Figura 1. Intoxicaciones por sustancias químicas según tipo de agente causal, Colombia. 2008-2020.
Características generales y farmacología del acetaminofén
El acetaminofén, conocido también como paracetamol o por su nombre químico N-acetil para aminofenol, es un medicamento analgésico con más de 100 años de historia, muy utilizado en el mundo para el control del dolor agudo leve según la escala analgésica de la Organización Mundial de la Salud.
Mecanismo de acción farmacológica
El acetaminofén ha sido categorizado como un medicamento analgésico y antipirético con poca actividad antiinflamatoria. Su mecanismo de acción aún es poco claro. No obstante, se ha descrito que su acción se basa en un mayor efecto inhibidor de las COX-1 y 2 en el sistema nervioso central, así como en el bloqueo preferente sobre COX-3. Resultando en una disminución en la producción de prostaglandinas, responsables de la producción de fiebre, dolor y menor medida de la inflamación. Algunos autores le han atribuido acción analgésica central mediante interferencia con las vías serotoninérgicas descendentes del dolor por interacción con los receptores espinales de 5-hidroxitriptamina tipo 3 (5-HT 3), mecanismo observado en algunos estudios en animales y en humanos. 5,6,7,8.
Características cinéticas
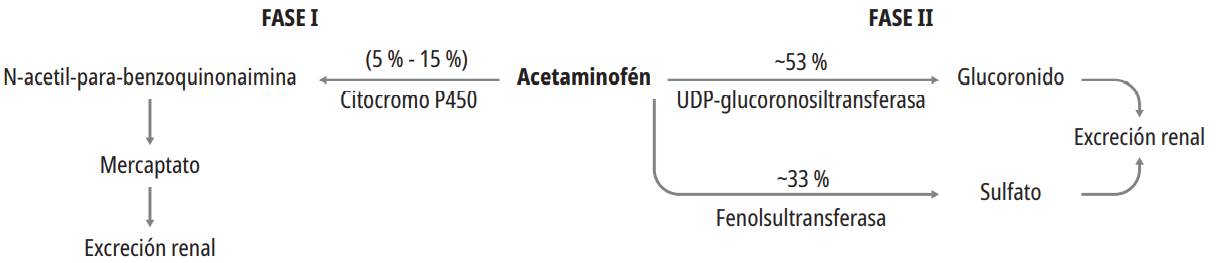
El acetaminofén se absorbe por vía oral con una buena biodisponibilidad, alcanzando la concentración sérica máxima entre 30 a 60 minutos, aproximadamente. Su volumen de distribución es de 0,95 L/kg y la unión a proteínas es del 25 %, circunstancias que facilitan su eliminación renal. El metabolismo de este medicamento es hepático, principalmente mediante conjugación con ácido glucurónico y sulfatos (85-90 %) que posteriormente se eliminan en su mayoría por vía renal. Mientras el 10 % a 15 % se metaboliza por acción de las isoenzimas 2E1, 3A4, 1A2 Y 2B6 del CYP450 mediante la unión con cisterna y ácido mercaptúrico (por N hidroxilación). Resultando en la producción de N-acetil-p-benzoquinonaimina o acetimidoquinona (NAPQI), un metabolito tóxico que en condiciones normales es detoxificado por medio de la conjugación con glutatión y grupos sulfidrilos, proceso que se muestra en la figura 2 9,10,11,12. La vida media de eliminación del acetaminofén en dosis terapéuticas es de 2 %, aunque tras la ingestión de dosis tóxicas puede prolongarse hasta las 12 horas 13.
Mecanismo de toxicidad
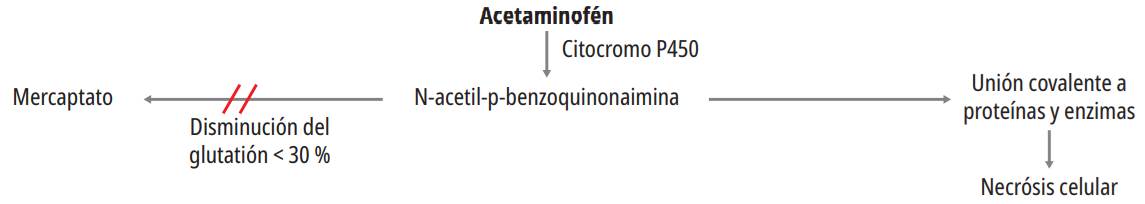
En la figura 3 se evidencia cómo tras el consumo de dosis supraterapéuticas, con el aumento de la producción de N-acetil-benzoquinoneimina (NAPQI), las reservas de glutatión se agotan dejando libre gran parte del tóxico que, al acumularse, induce estrés oxidativo, alteración en la síntesis de ATP y daño mitocondrial, causando necrosis centrolobulillar (por una mayor proporción de CYP450 en esta zona) con la posterior liberación de las enzimas hepáticas 14,15,16,17.
Dosis tóxica
En el caso de los niños, la dosis de acetaminofén a partir de la cual se genera hepatotoxicidad es cerca de 10 veces mayor a la terapéutica. En adultos es 6 veces superior a la máxima permitida en cada toma. La tabla 1 muestra las dosis terapéuticas y tóxicas para niños y adultos según las recomendaciones actuales de la FDA 18,19.
Tabla 1. Dosis terapéuticas y tóxicas en niños y adultos.
| Grupo etario | Dosis terapéutica | Dosis tóxica |
|---|---|---|
| Niños | 10-15 mg/kg/ dosis (60 mg/kg/día) | ≥ 150 mg/kg |
| Adultos | 1 g dosis (máximo 4 g/día) | ≥7.5 g* |
Fuente: elaboración propia.
Nota: Las dosis tóxicas referidas corresponden a ingestiones agudas únicas. Sin embargo, diferentes autores han recomendado que en casos de uso de dosis supraterapéuticas se considere dosis tóxica cuando la dosis diaria supera los 6 g en un periodo de 24 horas 20.
Debido a la potencial toxicidad hepática, es necesario que en los casos de ingestión de dosis tóxicas el paciente sea hospitalizado para inicio de terapia con N acetilcisteína (NAC) y se realicen los estudios de laboratorio pertinentes 20,21,22,23. Es importante tener en cuenta que los valores de toxicidad pueden ser inadecuadamente altos para los pacientes considerados de alto riesgo, razón por la que cada caso debe ser analizado individualmente a partir de la recopilación de los datos completos de la historia clínica 24.
Factores de riesgo
Entre los factores de riesgo relacionados a una mayor severidad del cuadro clínico y progresión a hepatotoxicidad en el paciente que ha ingerido acetaminofén se encuentran 20,25:
Bajas reservas de glutatión.
Consumo de medicamentos o sustancias inductoras de CYP450.
Hepatopatía previa.
Ingestión concomitante de fármacos que compiten por la conjugación con el glutatión.
En la tabla 2 se describen los diferentes factores de riesgo y los mecanismos que predisponen a un mayor daño hepático.
Tabla 2. Factores de riesgo para el desarrollo de hepatotoxicidad en intoxicación por acetaminofén.
| Factores de riesgo | Ejemplos |
|---|---|
| Baja reserva de glutatión (menor disponibilidad de glutatión para el metabolismo del NAPQI). |
|
| Consumo de medicamentos o sustancias inductoras de CYP450 (incremento en la producción de NAPQI). |
|
| Hepatopatías previas (mayor susceptibilidad de los hepatocitosal daño por alteración mitocondrial previa y menor disponibilidad de reacciones de conjugación). |
|
| Uso de fármacos que compiten por la conjugación con el glutatión (disminución de la capacidad de depuración del NAPQI). |
|
| Edad (inmadurez funcional hepática en niños y disminución de la capacidad funcional hepática asociada con la edad y el uso de agentes hepatotóxicos en adultos). |
|
Fuente: elaboración propia.
Nota: UBE: Unidades de Bebida Etílica estándar (1 cerveza comercial = 1 copa de vino tinto = 1 copa de whisky = 1 UBE), establecida por la Organización Mundial de la salud 20,28,29,30,31.
Presentación clínica
El cuadro clínico de intoxicación aguda por acetaminofén se divide en cuatro fases:
Primera fase: Se presenta durante las primeras 24 horas postingesta. El cuadro se caracteriza por manifestaciones inespecíficas, predominantemente gastrointestinales, tales como: malestar general, náuseas, vómito y dolor abdominal. Otros síntomas presentes son: palidez, diaforesis y reacciones de hipersensibilidad. Durante esta fase, algunos pacientes permanecen asintomáticos. Los laboratorios no suelen encontrarse alterados, pero puede existir elevación de enzimas hepáticas con valores de AST o ALT mayores a 1 000 U/L, siendo más alta la elevación de la AST que la ALT 18,20,32.
Segunda fase: Se presenta de 24 a 72 horas postingesta. Aunque los síntomas mencionados pueden mejorar, la lesión hepática progresiva se puede manifestar con dolor en hipocondrio derecho, hepatomegalia, y elevación de enzimas hepáticas, las cuales comienzan a aumentar de 24 a 36 horas después de una sobredosis. Adicionalmente, puede evidenciarse elevación de la bilirrubina total, alargarse el tiempo de protrombina y se pueden manifestar anormalidades en la función renal 9,13,20.
Tercera fase: Se presenta de 72 a 96 horas postingesta. Es en esta fase donde las anormalidades en la función hepática llegan al pico máximo caracterizado por necrosis centrolobulillar hepática. Lo cual se expresa clínicamente con la aparición de ictericia, coagulopatía y encefalopatía. En ese sentido, se puede evidenciar una marcada elevación de las transaminasas, pudiendo mostrar valores hasta de 30.000 UI/L, hiperamonemia, prolongación de pt y del INR (mayor riesgo de sangrado), hipoglucemia, acidosis láctica y una concentración total de la bilirrubina mayor a 4 con predominio de la indirecta. Dada la disfunción multiorgánica presentada, es en esta etapa donde ocurre la mayoría de muertes 18,20,33.
Fase de resolución: Esta fase ocurre de 4 a 7 días posteriores a la intoxicación, si el paciente recibió tratamiento adecuado. Aunque el proceso puede prolongarse 3 semanas o más y la recuperación histológica puede tomar hasta tres meses 18,20.
La velocidad de aparición de estas fases depende de la cantidad de acetaminofén ingerida, la combinación con otros hepatotóxicos y los factores de riesgo del paciente.
Diagnóstico
En este tipo de intoxicación es fundamental el reconocimiento temprano para reducir el riesgo de morbimortalidad. De la misma forma, es primordial la adecuada indagación al paciente y a los testigos (familiares, amigos, personas a cargo), en busca de la causa de la ingesta, ya sea accidental o voluntaria, y la presencia de factores de riesgo o circunstancias que incrementan la gravedad del evento, como ya se mencionó anteriormente 21,34.
En estos pacientes se deben realizar pruebas de función hepática (glucosa, tiempo de protrombina, INR, transaminasas y bilirrubinas), función renal (nitrógeno ureico (BUN), creatinina y electrolitos), gases arteriales y, si hay disponibilidad, se debe determinar la concentración de acetaminofén, 4 horas después de la ingesta debido a que es el tiempo de distribución del medicamento.
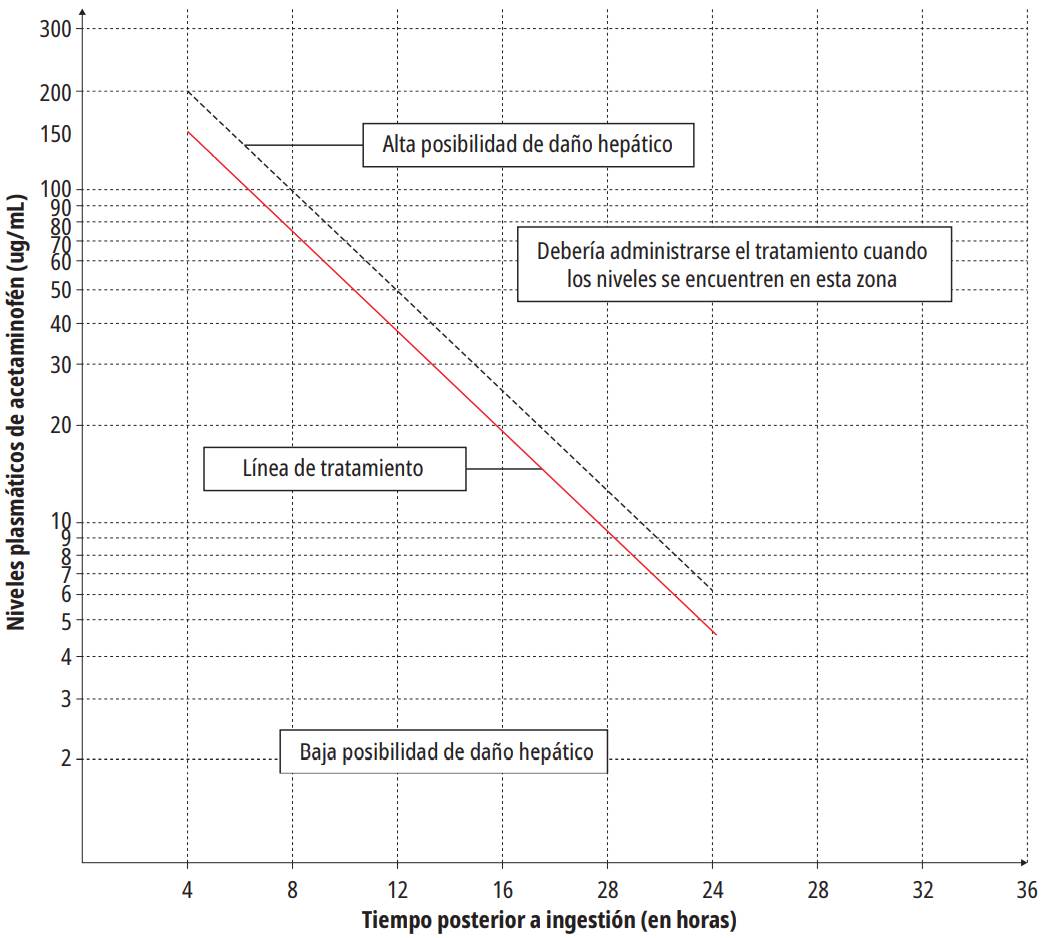
El valor de los niveles séricos de acetaminofén obtenidos puede graficarse en el nomograma de Rumack-Matthew, el cual se puede observar en la figura 4. Además, estos niveles pueden correlacionarse directamente con la severidad de la intoxicación, el riesgo de hepatotoxicidad y la indicación de manejo con NAC en el caso de intoxicación por ingesta única de acetaminofén. Sin embargo, su uso suele verse limitado por la no disponibilidad de este paraclínico en los servicios de urgencias de atención primaria 21,22,23,26.
En los pacientes sin evidencia de daño hepático 72 horas después de una ingestión peligrosa de acetaminofén es muy poco probable que se presente daño hepático grave 24.
Tratamiento
El manejo inicial del paciente con sospecha o confirmación de intoxicación por acetaminofén influye directamente en la reducción del riesgo de hepatotoxicidad. Este se basa en la estabilización del paciente según su grado de compromiso sistémico, disminución de la absorción del medicamento, tratamiento específico con el antídoto, detección y manejo de posibles complicaciones 9.
Manejo general
Identificar situaciones de riesgo vital e iniciar el soporte básico y/o avanzado según sea necesario (ej. Paciente en paro respiratorio por ingestión de acetaminofén combinado con opioides).
Tomar las muestras necesarias para valorar función hepática, función renal, marcadores de coagulación, electrolitos, glucemia, etc., y determinar la presencia de niveles séricos del tóxico si están disponibles, sin que ello retarde el inicio de la antidototerapia.
Descontaminación gastrointestinal:
Carbón activado: actualmente está consensuado como el mejor descontaminante del tubo digestivo al unirse al acetaminofén en el estómago para así disminuir la absorción gastrointestinal y las concentraciones del mismo. Se recomienda el uso carbón activado dentro de un periodo de 1 a 4 horas después de la ingesta de dosis tóxicas de acetaminofén. Se ha asociado a una disminución del 45 % en los niveles séricos, reduciendo la tasa de absorción, incluso en pacientes con ingestiones masivas (> 30 gr) del medicamento y su hepatotoxicidad 1,26,35,36. La dosis recomendada es 1 g/kg vía oral o por sonda orogástrica (ej. Paciente inconsciente con tubo endotraqueal), preparado al 20 % (5 cc de agua por cada gramo de carbón activado). Puede presentarse emesis, en cuyo caso se podrá administrar una nueva dosis de carbón activado a 0,5 g/kg si se produce antes de 30 minutos posteriores a la administración del carbón. Se puede considerar el uso de antieméticos mientras el paciente esté hidratado y no existan contraindicaciones o riesgo de efectos adversos. El efecto secundario más frecuente es el estreñimiento y, raramente, broncoaspiración secundaria a la emesis 22. Su uso está contraindicado si hay posible compromiso de vía aérea o ausencia de ruidos intestinales 20,23.
Lavado gástrico: este procedimiento tiene como función extraer la mayor cantidad posible del medicamento antes de que se absorba. Es útil si la ingestión del medicamento lleva menos de 1 hora 23,26. Sin embargo, un ensayo clínico aleatorizado encontró que el carbón activado puede ser más efectivo que el lavado gástrico para prevenir la absorción de acetaminofén 26.
Tratamiento específico
La N-Acetilcisteína (NAC) es el antídoto con mayor evidencia de efectividad. Especialmente cuando se administra en las primeras 6 a 8 horas postingesta 18,36. Por este motivo, diferentes meta-análisis y revisiones sistemáticas la consideran de elección para este tipo de intoxicaciones (nivel de recomendación I para la vía intravenosa y II para la vía oral) 26. Este medicamento previene la lesión hepática, principalmente porque restablece las reservas de glutatión al actuar como su precursor, sustituyendo las reservas depletadas por el metabolito tóxico NAPQI. Adicionalmente, disminuye la formación de NAPQI por aumento de la conjugación con sulfato para producir metabolitos no tóxicos. Asimismo, el grupo cisteína se une e inactiva el metabolito tóxico producido a través de la oxidación de enzimas de la CYP450, principalmente la CYP2E1, favoreciendo la formación de conjugados de ácido mercaptúrico y derivados cisteínicos que propician su excreción. Disminuyendo así la producción de radicales libres y favoreciendo la producción de energía mitocondrial 18.
Igualmente, en pacientes con falla hepática, ayuda a mejorar el equilibrio hemodinámico, la función respiratoria y el edema cerebral. Aunque no se conoce con certeza el mecanismo de estos efectos 18,21. La NAC desarrolla hepatotoxicidad solo en el 5 a 10 % de los pacientes que han ingerido una dosis tóxica severa. Mientras que, para los casos en los que los pacientes han desarrollado insuficiencia hepática, ha reducido la mortalidad en un 20-30 % 20. En Colombia, para el tratamiento de esta intoxicación se encuentran disponibles las presentaciones en sobres de 100,200,300 y 600 mg para uso oral (las cuales se utilizan diluyendo cada sobre en 100 mi de agua), y ampolletas para uso intravenoso de 300 mg/3 mL 23.
Indicaciones
Pacientes que hayan ingerido dosis tóxicas de acetaminofén con o sin síntomas de hepatotoxicidad.
Ingestión de dosis tóxicas de acetaminofén con presencia de elevación de transaminasas, incluso en ausencia de síntomas.
Pacientes con factores de riesgo que hayan consumido dosis supraterapéuticas de acetaminofén 23.
Dosis
La administración oral de NAC se realiza de la siguiente manera:
Este régimen de tratamiento tiene una duración total de 72 horas 21,23,24,37.
Cuando se presenta intolerancia a la vía oral, hay alteración del estado de conciencia o falla hepática, el medicamento se administra por vía intravenosa 34, según el protocolo tradicional de tres fases basado en el método Prescott de esta forma:
Dosis de carga de 150 mg/kg diluidos en 200 mi de dextrosa al 5 % en agua destilada (menores de 20 kg: 3cc/kg de dad 5 %), para pasar en 15 a 60 minutos.
Dosis de mantenimiento de 50 mg/kg diluidos en 500 mi dextrosa al 5 % en agua destilada (menores de 20 kg: 7cc /kg de dad 5 %) en 4 horas.
100 mg/kg diluidos en 1000 cc de dextrosa al 5 % en agua destilada (menores de 20 kg: 14 cc/ kg de DAD 5 %) las siguientes 16 horas 21,23,26,28.
Aunque se considera que la mayor efectividad del tratamiento con NAC para reducir el riesgo de lesión hepática se alcanza cuando se inicia antes de las 8 horas post ingestión de acetaminofén, diferentes estudios han demostrado la utilidad de su uso hasta las 24 horas postingesta, o si el paciente evoluciona hacia un mayor riesgo de toxicidad hepática 26,37,38.
Las reacciones adversas al tratamiento con NAC ocurren con frecuencia e intensidad variable dependiendo de la vía de administración. En el caso de la administración del antídoto por vía oral, se han reportado principalmente alteraciones gastrointestinales como náuseas, emesis, dolor abdominal, rinorrea, opresión torácica y broncoconstricción (efecto poco frecuente en pacientes asmáticos).
Las reacciones que pueden presentarse con la administración endovenosa son rash, prurito, urticaria, rubor e, incluso, eventos graves como reacciones anafilactoides o anafilaxia en el 10 a 20 % de los tratados. En estos casos es necesario realizar las intervenciones para el tratamiento de estas reacciones según su gravedad incluyendo:
Antihistamínicos: recomendables para el tratamiento de las reacciones de hipersensibilidad leve y moderada, y como coadyuvantes en el tratamiento de la anafilaxia.
Glucocorticoides: antiinflamatorios que permiten reducir la respuesta inflamatoria asociada con las reacciones de hipersensibilidad.
Epinefrina: intervención de primera línea para el tratamiento específico de las reacciones anafilácticas.
Es probable que las reacciones sistémicas con la primera dosis puedan relacionarse con la velocidad de infusión. Rara vez llegan a producir la muerte 34,39,40,41.
Dado que la presentación de las reacciones adversas se asocia a la concentración y velocidad de administración, se han propuesto diferentes esquemas con el fin de reducir tales efectos y disminuir el riesgo de reacciones anafilácticas. Entre ellos, el protocolo modificado de 12 horas, que consiste en un método de administración corta en dos fases: 100 mg/kg en 200 cc DAD 5 % para 2 horas y 200 mg/kg en 1000 cc de DAD 5 % para 10 horas. También conocido como régimen SNAP (Scottish and Newcastle Antiemetic Pretreatment Paracetamol Poisoning Study Regim) que podría disminuir el vómito y la necesidad de antieméticos (36 % vs 65 %, respectivamente) y de anafilaxis (5 % vs 31 %, respectivamente) 18,42,43.
Un importante estudio multicéntrico de corte retrospectivo que comparó el uso oral e intravenoso de NAC, examinó los datos de un total de 4.048 pacientes. 2.086 de ellos recibieron tratamiento intravenoso y 1.962 pacientes tratamiento oral. Esta investigación concluyó que el protocolo intravenoso (20 horas) fue efectivo cuando se administró antes de las 12 horas desde la ingesta, y el protocolo de administración oral fue efectivo, incluso cuando se administró más de 18 horas después de una sobredosis (protocolo de 72 horas). Los investigadores no hallaron diferencias estadísticamente significativas entre los dos tratamientos. En ambos casos la eficacia del antídoto disminuye más allá de las 8 horas posteriores a la ingestión 24,35.
Seguimiento, pronóstico y complicaciones
Según la evidencia científica disponible, los pacientes intoxicados con acetaminofén que reciben tratamiento oportuno tienen un riesgo de muerte menor al 2 % y evolucionan hacia la recuperación completa sin secuelas. Sin embargo, es recomendable tener en cuenta en qué casos se puede tratar y cuando requiere remisión, como se evidencia en la tabla 3. Con respecto a la edad, se ha descrito que los niños menores de 6 años tienen un mejor pronóstico en comparación con los adultos. Esto debido a su mayor capacidad de detoxificación del acetaminofén 44.
Tabla 3. Criterios de remisión a nivel especializado 23,45.
| Criterios para remisión |
|---|
| Signos o síntomas de insuficiencia hepática aguda. |
| Encefalopatía o deterioro clínico progresivo. |
| Prolongación del tiempo de protrombina (>1.8 veces el control). |
| Necesidad de trasplante hepático. |
| Hipoglucemia. |
| No contar con el antídoto específico. |
| Elevación progresiva de los niveles de transaminasas. |
| Hipertensión endocraneana. |
| Alteración de la función renal (creatinina sérica mayor a 2 mg/dL). |
Fuente: elaboración propia.
Hospitalización
Aunque el paciente que consulta en forma temprana después de la ingestión se encuentre asintomático o sin signos de toxicidad, puede permanecer hospitalizado durante el tratamiento para ejercer una estricta vigilancia dada posibilidad de progresión a toxicidad hepática.
Interconsulta y valoración por toxicología
En todos los casos de sospecha o ingestión de dosis tóxicas de acetaminofén o ante cualquier duda por parte del equipo tratante en urgencias, deberá establecerse comunicación inmediata con el centro de información y asesoría toxicológica asignado (ej. Línea Nacional de Toxicología de Colombia 018000916012 o 1-2886012) o con el servicio de toxicología de referencia en la zona correspondiente, con el fin de verificar el manejo adecuado y establecer las necesidades de remisión para tratamiento por parte de los especialistas en toxicología clínica. Especialmente, en los casos de ingestión de dosis potencialmente letales o en los pacientes que cursan con alteraciones clínicas o de laboratorio que sugieran riesgo de deterioro 23,45.
Seguimiento con ALT (alanina aminotransferasa)
Se debe realizar la monitorización de los niveles de transaminasas, especialmente ALT en los pacientes con intoxicación por acetaminofén cada 12 a 18 horas 46,47,48.
Ingreso a unidad de cuidados intensivos (UCI)
Los pacientes con signos de hepatotoxicidad (coagulopatía, encefalopatía, alteraciones metabólicas), falla renal o disfunción de otros órganos, se deberán ingresar a la unidad de cuidados intensivos, pues requieren evaluación neurológica frecuente, monitorización continua de sus signos vitales y pueden necesitar procedimientos invasivos. En la tabla 4 se muestran los criterios de ingreso a UCI 21,49.
Tabla 4. Criterios de necesidad de ingreso a UCI 21,45.
| Criterios de ingreso a UCI |
|---|
| Coagulopatía grave y sostenida (INR ≥ 6.5). |
| Encefalopatía. |
| Disfunción orgánica. |
| Acidosis metabólica: pH menor de 7,3 (independientemente del grado de encefalopatía). |
| Hipotensión a pesar de adecuada reposición de líquidos.. |
| Necesidad de trasplante hepático o diálisis renal. |
| Hipoglucemia grave. |
| Hiperbilirrubinemia. |
Fuente: elaboración propia.
Consideraciones en mujeres gestantes
Aunque el acetaminofén se considera un medicamento seguro durante el embarazo (clasificación B) y la dosis máxima recomendada es la misma que en no gestantes (4 gr./día), este medicamento es una de las sustancias más comúnmente asociadas con intoxicaciones durante el embarazo 50. Dado el paso a través de la barrera placentaria, en dosis tóxicas el acetaminofén puede lesionar tanto los hepatocitos maternos como los fetales 51. En caso de sobredosis con acetaminofén en el primer trimestre del embarazo, se aumenta el riesgo de aborto. Esto podría deberse a la toxicidad directa sobre el embrión, aunque aún no se ha esclarecido el mecanismo.
Entre tanto, si la intoxicación ocurre en el último trimestre del embarazo, algunos autores recomiendan finalizar el embarazo en caso de encontrar niveles tóxicos en la madre, en presencia o no de hepatotoxicidad. Por esta razón, en los casos de ingestión de dosis tóxicas en mujeres gestantes es indispensable la remisión al nivel especializado en el que se pueda realizar la valoración conjunta por toxicología y ginecobstetricia 51,52,53. Actualmente, el tratamiento con NAC en gestantes se recomienda por su aparente capacidad para atravesar la barrera placentaria, reducir el riesgo de hepatotoxicidad en el feto 51,52,53 y su perfil de seguridad durante la gestación (clasificación B FDA).
Otras consideraciones
En el paciente en el que se identifique ingestión voluntaria de acetaminofén con fines suicidas, se deberá considerar la interconsulta del servicio de psiquiatría una vez finalizado el tratamiento de la intoxicación.
Criterios de alta clínica
Finalización del esquema de tratamiento con NAC sin complicaciones.
Paciente asintomático y sin alteración de las pruebas de laboratorio posterior al tratamiento 23.
Conclusión
La intoxicación por acetaminofén es común tanto en población pediátrica como adulta y su adecuado reconocimiento y manejo es determinante en la evolución clínica del paciente. El tratamiento de este tipo de intoxicación está orientado a reducir el riesgo de complicaciones relacionadas con la hepatotoxicidad. 20
La NAC es un pilar fundamental para el manejo de los pacientes con alta sospecha o confirmación de la ingestión de dosis tóxicas de acetaminofén, debido a que restaura las reservas de glutatión a nivel hepático, disminuyendo así la posibilidad de desarrollo de lesión de este órgano. Según la evidencia científica disponible, es posible utilizar este antídoto por vía oral o endovenosa con eficacia similar. 18,26.
Es necesario que el personal de salud tenga claros los conceptos relativos a la toxicidad del acetaminofén y el abordaje terapéutico general y específico adecuado. Además de los criterios generales de remisión, siempre es importante solicitar el apoyo de los centros de información toxicológica (ej. Línea nacional de toxicología 018000916012 o (57) 1-2886012) o los especialistas en toxicología. Todo con el fin de brindar la mejor atención para mejorar el pronóstico de los pacientes.