Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Hacia la Promoción de la Salud
Print version ISSN 0121-7577
Hacia promoc. Salud vol.16 no.2 Manizales July/Dec. 2011
ASSESMENT OF A TEST THAT MEASURES ENAMEL SUSCEPTIBILITY TO DENTAL CAVITIES
AVALIAÇÃO DE UM TESTE QUE MIDE A SUSCETIBILIDADE DO ESMALTE A CARIES DENTAL
María del Pilar Cerezo Correa**
* Odontóloga, Especialista en Investigación y Docencia Universitaria, Especialista en Gerencia en Servicios de Salud. Universidad Autónoma de Manizales. Colombia. Correo electrónico: sonríe@autonoma.edu.co
** Odontóloga, Especialista en Salud Pública y en Auditoria en Salud, Universidad Autónoma de Manizales. Colombia. Correo electrónico: mapice@autonoma.edu.co
Objetivo: correlacionar los resultados de la prueba colorimétrica con la historia de caries de los pacientes adultos jóvenes, para determinar la posibilidad de usarla como indicador de la susceptibilidad del esmalte adulto a la disolución en ácidos, propios de la placa dental o de factores erosivos externos. Metodología: estudio analítico correlacional, determinación del tamaño de la muestra con nivel de confianza del 95%, poder del 80%, razón 1:1, razón de riesgo 1:5. Muestra: 87 personas en el grupo con historia de caries y 83 en el de sanos, selección aleatoria de instituciones de educación para adultos de la ciudad de Manizales. Criterios de inclusión: tener entre 18 y 20 años y dientes anteriores superiores. Se firmó el consentimiento informado. Aplicación de técnica colorimétrica en ambos grupos, se utilizaron discos de 2,8 mm de papel absorbente impregnados en una solución de cristal violeta; un ácido grabador (ácido clorhídrico a un pH de 1,9) y una escala colorimétrica de pH. Se aplicaron la prueba de Kappa, sensibilidad y especificidad. Resultados: resistente según la prueba: 55%, y no resistente: 45%. Según la prueba Kappa, la concordancia entre la prueba y la susceptibilidad del esmalte son bajas (IC: 0,59 - 1,47 Kappa 0,1). La sensibilidad (36%) y el valor predictivo positivo (40%) fueron bajos. La especificidad (45%) y el valor predictivo negativo (40%) también fueron bajos. Conclusiones: no hay concordancia entre la susceptibilidad a la disolución ácida del esmalte según la prueba utilizada en esta investigación y la experiencia pasada de caries en adultos jóvenes.
Esmalte dental, susceptibilidad a caries dentarias, disolución, grupos vulnerables. (Fuente: DeCS, BIREME).
Objective: to correlate the results of the colorimetric test with the cavities history of young adult patients to determine the possibility to use this test as an indicator of susceptibility of the adult enamel compared to acid dissolution from dental plaque or extrinsic erosive factors. Method: correlational analytic study with sample size determination and a 95% confidence interval, 80% 1:1 rate , 1:5 risk rate. Sample: 87 people with cavities history in the group and 83 people in the healthy group in an at random selection at Educational Institutions for Adults in Manizales. Inclusion criteria: being 18 -20 years old and having upper anterior teeth. They signed an informed consent. Colorimetric technique was applied in both groups. 2.8mm absorbent paper discs impregnated with a violet crystal solution were used as well as an acid etching (chloridric acid, 1.9 pH) and a pH colorimetric scale ., Sensitivity and specificity Kappa tests were applied. Results: resistance according to the test was 55% and non-resistance was 45%. According to Kappa's test the concordance between the test and enamel susceptibility is low (IC: 0.59 - 1.47 Kappa 0.1). Sensitivity (36%) and positive predictive value (40%) were low. Specificity (45%) and negative predictive value (40%) were also low. Conclusions: no concordance was found between enamel susceptibility to acid dissolution according to the test used in this research project and the past experience of cavities in young adults.
Dental enamel, dental cavity susceptibility, dissolution, risk groups. (Source: MeSH, NLM)
Objetivo: co-relacionar os resultados do teste colorimétrico com a historia de caries dos pacientes adultos jovens, para determinar a possibilidade de usar- a como indicador da suscetibilidade do esmalte adulto à dissolução em ácidos próprios da placa dental ou de fatores erosivos externos. Metodologia: estudo analítico co-relacional, determinação do tamanho da amostra com nível de confiança de 95%, poder de 80%, ração 1:1, ração de risco 1:5. Amostra: 87 pessoas no grupo com historia de caries e 83 no de saudáveis, seleção aleatória de instituições de educação para adultos da cidade de Manizales. Critérios de inclusão: ter entre 18 e 20 anos e dentes anteriores superiores. Firmou se o consentimento informado. Aplicação de técnica colorimétrica nos dois grupos utilizou se discos de 2,8 mm de papel absorvente impregnados em uma solução de cristal violeta; um acido gravador (ácido clorídrico a um pH de 1,9) e uma escada colorimétrica de pH. Aplicaram se o teste de Kappa, sensibilidade e especificidade. Resultados: resistentes segundo o teste: 55% e não resistente: 45%. Segundo o teste de Kappa, a concordância entre o teste e a suscetibilidade do esmalte é baixa (IC: 0,59 - 1,47 Kappa 0,1). A sensibilidade (36%) e o valor preditivo positivo (40%) foram baixos. A especificidade (45%) e o valor preditivo negativo (40%) também foram baixos. Conclusões: não há concordância entre a suscetibilidade à dissolução ácida do esmalte segundo ao teste utilizado nesta pesquisa e a experiência passada de caries em adultos jovens.
Esmalte dental, suscetibilidade a caries dentarias, dissolução, grupos vulneráveis. (Fonte: DeCS, BIREME)
La caries dental es una enfermedad multifactorial prevenible, pero en Colombia, específicamente en Caldas, ocupa el cuarto lugar de consulta (1). Durante años se han realizado esfuerzos para disminuir esta patología, actualmente el Plan Nacional de Salud Pública 2007-2010 contempla entre sus objetivos mejorar la salud oral de la población mediante acciones de promoción de la salud y prevención de la enfermedad (2).
Entre los factores que intervienen en la producción de la caries dental se encuentra la resistencia del esmalte a la disolución ácida (3). La disolución del esmalte dental por sustancias acídicas puede aparecer como resultado de caries o de erosión, aunque estas dos patologías muestran un agente etiológico común, en este caso el ácido, y su patogénesis difiere notablemente respecto a la dinámica del proceso de disolución.
La caries involucra una exposición a largo término a los ácidos orgánicos débiles originados en la placa bacteriana, resultando en periodos alternativos de remineralización y desmineralización (4). La composición química del esmalte es un factor que resulta importante en la susceptibilidad a la disolución ácida. El mayor contenido de carbonato y de magnesio determina una velocidad de disolución en los ácidos más rápida; en cambio, el contenido de iones trazas de estroncio, molibdeno y otros disminuye esta susceptibilidad (5). En la aparición de lesiones cariosas, el factor más importante es que se logre en la superficie del esmalte, de forma persistente, un acúmulo ácido con el nivel de pH requerido para iniciar su disolución. La resistencia del esmalte juega un carácter pasivo, que puede modificar únicamente la velocidad de su disolución en una unidad de tiempo.
Lo deseable es un esmalte resistente que permita limitar el daño y que ante ataques discontinuos tal como sucede con la presencia de la placa bacteriana cariogénica en superficies lisas, pueda dar lugar a un equilibrio biodinámico entre los procesos agresivos y la reposición iónica ejercida por la saliva entre los periodos consecutivos de agresión, de tal manera que impida el avance de la lesión o permita su total remineralización.
El interés para el desarrollo de métodos que identifiquen grupos y pacientes con riesgo de presentar caries dental ha sido demostrado por la literatura científica. La predicción correcta de la posibilidad de que se presente caries dental o erosión en un paciente, sería beneficioso por varias razones: a) daría orientación sobre las necesidades de prevención; b) aumentaría la efectividad de los procedimientos preventivos; c) permitiría una aplicación apropiada de los niveles de prevención, y d) daría eficiencia económica y permitiría controlar los costos de una rehabilitación para la caries o la erosión dental (6).
Los estudios realizados mediante la aplicación de la técnica colorimétrica RM a partir de 1984, que sobrepasan las 10.000 aplicaciones, demuestran que los niños con esmalte poco resistente desarrollan significativamente más caries en el periodo de un año que los niños restantes (7). Esta prueba ha sido utilizada también para valorar la capacidad individual de remineralización del esmalte dental (8).
La prueba se fundamenta en que todo ácido colocado sobre el esmalte dental puede producir desmineralización. Los iones calcio y fosfatos liberados, al incorporarse al ácido, elevan progresivamente el pH, y si la solución ácida tiene un indicador de pH, pueden observarse los cambios en sus tonalidades.
Determinar si la velocidad de la disolución ácida del esmalte se correlaciona con la "historia pasada de caries" representaría la posibilidad de poder aplicar una prueba de riesgo objetiva en cada paciente, para obtener el grado posible de resistencia de su esmalte a la caries (en pacientes niños) y muy posiblemente a la erosión dental (en el caso de los pacientes adultos) permitiendo la aplicación de medidas preventivas en forma individualizada.
Los estudios relacionados con esta prueba colorimétrica se han realizado en escolares. El objetivo de esta investigación es correlacionar los resultados de la prueba colorimétrica con la historia de caries de los pacientes adultos jóvenes, para determinar la posibilidad de usarla como indicador de la susceptibilidad del esmalte adulto a la disolución en ácidos propios de la placa dental o de factores erosivos externos.
Esta investigación de tipo analítico correlacional consideró un nivel de confianza (1-alfa) del 95%, un poder (1-Beta) del 80%, con una razón 1:1, y una razón de riesgo de 1.5 (1.5 más veces de probabilidad de tener caries y posible susceptibilidad a la erosión) en los pacientes con disolución del esmalte alta, la muestra registró 84 pacientes con caries o experiencia pasada de caries y 84 en el grupo de sanos o sin caries, ni experiencia pasada de caries. Finalmente, se examinaron 87 pacientes en el grupo con historia de caries y 83 en el grupo de sanos. Los pacientes fueron seleccionados en forma aleatoria de institutos para la educación de adultos de la ciudad de Manizales, que firmaron el consentimiento informado. Con el fin de garantizar la homogeneidad de la muestra se consideraron los siguientes criterios de inclusión: tener entre 18 y 20 años, pertenecer al estrato socioeconómico 3, determinado mediante la dirección de la residencia según clasificación de la "Dependencia de Valorización" del municipio de la ciudad, y presentar en la boca los dientes anteriores superiores. La investigación cumplió con todo lo requerido por la norma 8430 del Ministerio de la Protección Social de Colombia.
Se realizó una valoración clínica para identificar los pacientes sanos y los pacientes con presencia de caries o experiencia pasada de caries, que se asignó a cada uno de los grupos. La valoración la realizó uno de los investigadores con experiencia en la toma de índices de caries dental. Para el diagnóstico de caries y experiencia pasada de caries se tuvieron en cuenta los criterios del índice COP (caries actual: caries cavitacional y dientes con extracción indicada por caries; experiencia de caries: dientes obturados por caries y dientes extraídos por caries), la valoración se realizó en la misma institución con luz natural, se utilizaron un espejo bucal y una sonda OMS y se aplicó el protocolo de bioseguridad.
Para la aplicación de la prueba colorimétrica, se utilizaron discos de 2,8 mm de papel absorbente impregnados previamente en una solución de cristal violeta, la cual es un iniciador que a un pH 2,0 es amarillo ocre y que al elevarse el pH ofrece una gama de diferentes colores; un ácido grabador (ácido clorhídrico a un pH de 1,9), una escala colorimétrica de pH, que consta de 14 colores, donde el color 1 es amarillo ocre y el color 14 es violeta intenso con una gama de colores intermedios según el pH que registre el disco.
La prueba se realizó en los incisivos centrales superiores porque se ha reportado que son los que registran el promedio ponderado de todos los dientes a la resistencia del esmalte a la disolución ácida (9). El protocolo aplicado fue el siguiente: se limpió con agua destilada la superficie del esmalte de uno de los incisivos centrales superiores, se aisló el campo operatorio con algodón en rollo y se secó la superficie del diente. En una caja de cristal se depositó una pequeña gota de ácido clorhídrico, con una pinza de punta fina se tomó el disco de papel absorbente y se sumergió en el ácido, hasta observar el cambio de coloración, desde el violeta intenso hasta el amarillo ocre. Se escurrió el contenido de ácido del disco en el borde de la caja de cristal y se procedió a colocar el disco sobre la superficie vestibular del diente, cerca de su borde incisal. Utilizando un cronómetro, a los 60 segundos se identificó el color que tomó el disco y se comparó con la escala colorimétrica estandarizada. Se lavó el diente con agua y se realizó una topicación con fluoruro de sodio al 2%. La prueba fue aplicada por un investigador diferente al que realizó la valoración inicial, de tal modo que no conociera el grupo al que pertenecía el paciente.
Interpretación de los resultados: si el disco presentaba los colores numerados con 1, 2, 3, 4 o 5, se consideró que el esmalte era resistente a la disolución ácida, y si la coloración del disco alcanzaba los colores entre 6 y 14 se consideró que el esmalte era poco resistente; estos valores se anotaron en una hoja de registro.
La información fue procesada en el programa SPSS versión 16. Se aplicaron la prueba de Kappa, sensibilidad, valor predictivo positivo, especificidad y valor predictivo negativo.
Para efecto de análisis, los resultados de la prueba se agruparon en dos categorías: resistentes y no resistentes, quedando como frecuencias relativas las siguientes:
Resistentes según la prueba: 94 dientes que corresponden al 55%, y no resistentes según la prueba: 77 dientes que corresponden al 45%.La prueba Kappa es la diferencia entre la concordancia observada y la esperada como fracción de la diferencia máxima. Como el valor máximo I0 es 1, esto da: K = Io-Ie / 1-Ie donde: Io es incidencia en el grupo no expuesto: Io = a+d/n, y donde: Ie es incidencia en el grupo expuesto. Ie = (a+c)(a+b) + (b+d)(c+d) / n².
Los cálculos indicaron que la concordancia entre la prueba colorimétrica y la susceptibilidad era baja según la prueba Kappa (tabla 1).

Sensibilidad = a/a+c: positivos verdaderos/positivos verdaderos + falsos negativos x 100.
La sensibilidad es el porcentaje de personas con la enfermedad correctamente clasificadas como enfermas.
Valor predictivo positivo = a/a +b: positivos verdaderos/positivos verdaderos + falsos negativos.
El valor predictivo positivo es la probabilidad de tener la enfermedad cuando el resultado de la prueba es positivo.
La sensibilidad de la prueba es baja. El instrumento calificó al 36% de las personas con caries en el grupo de riesgo alto. Según el valor predictivo positivo, de 100 personas clasificadas en riesgo alto, el 40% tiene historia de caries. La prueba colorimétrica tuvo un valor bajo de sensibilidad y un bajo valor predictivo positivo (tabla 2).

Especificidad: d/b+d: negativos verdaderos/falsos negativos + negativos verdaderos x 100.
La especificidad es el porcentaje de personas sin la enfermedad correctamente clasificadas como sanos.Valor predictivo negativo = d/c + d: negativos verdaderos/falsos negativos + negativos verdaderos.
El valor predictivo negativo es la probabilidad de no tener la enfermedad cuando el resultado de la prueba es negativo.
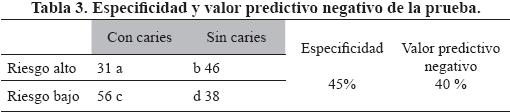
La especificidad de la prueba fue baja, de 100 personas sanas solo 45 eran clasificadas en riesgo bajo. El valor predictivo negativo registró que de 100 personas clasificadas en riesgo bajo, el 40% estaban sanas. La prueba colorimétrica tuvo un valor bajo de especificidad y un bajo valor predictivo negativo (tabla 3).
El Ministerio de Salud de Cuba ha realizado investigaciones (10) sobre la relación de la prueba que mide la susceptibilidad a la disolución ácida del esmalte con la actividad cariogénica, considerando muestras de hasta 869 niños; en sus conclusiones manifiesta no haber encontrado relación entre la prueba colorimétrica y la experiencia de caries en la dentición permanente. Estos resultados coinciden con lo hallado en este trabajo. Una explicación de la razón por la que esta investigación tampoco encontró un valor alto de correlación, sensibilidad y especificidad entre la prueba de la disolución ácida con la experiencia pasada de caries podría estar fundamentada en la diferencia de la reacción del esmalte de dientes temporales y dientes permanentes ante los ácidos. El examen del microscopio de escaneo electrónico (SEM) ha mostrado que la desmineralización se inicia en el núcleo (centro de los cristales) y en la interfase de la pared (vaina del prisma). Durante la disolución, los cristales se vuelven más pequeños y eventualmente se observan cristales de nano tamaño que se adhieren a la superficie del esmalte de los dientes temporales o se escapan dentro de la solución.
Después de la disolución inicial, las paredes del esmalte de los temporales tienden a fracturarse, mientras que las paredes del esmalte de los permanentes se mantienen intactas. Se ha observado que casi todos los componentes orgánicos del esmalte se localizan en las paredes (11,12). Después de un tiempo largo de reacción (1 o 2 semanas) las partículas de apatita de nano tamaño procedentes de la solución por filtración, son protegidas cinéticamente contra la disolución, inclusive cuando la solución se mantiene insaturada.
El promedio del rango de disolución del esmalte de los dientes permanentes y temporales durante la etapa lineal inicial de disolución es 1,5 +/- 0,5 x 1010 mol mm-2 min-1 y de 2,6 +/- 0,5 x 1011 mol mm-2 min-1, respectivamente. La disolución de los cristales de fosfato de calcio es altamente dependiente del grado de saturación. Como la composición y la estructura de los tejidos del esmalte no son homogéneos y cambian con el desarrollo de la lesión, el proceso de desmineralización es complejo. Considerando los diferentes rangos de disolución del esmalte temporal y permanente, se asume que las diferencias en este rango aparecen relacionadas con la diferencia de su estructura (13, 14). El promedio de la profundidad de las lesiones está asociado con la densidad de la unión prismática y la fracción de volumen del esmalte interprismático, valores ambos que son significativamente más grandes en el esmalte de los dientes temporales.
El volumen del poro en el esmalte desmineralizado influye parcialmente en la distribución de la pérdida mineral subsecuente. El efecto puede ser mediado por los cambios en el trasporte iónico, inducidos por los coeficientes de difusión local, cambiando la porosidad (15) y el contenido mineral relativo (16). El contenido mineral reportado es del 81,3% - 94,2 % para el esmalte temporal (17,18), mientras que el esmalte permanente está cerca del 97%, con un restante de agua y matriz orgánica (19). Las proteínas de la matriz son removidas durante la maduración del esmalte (12). Típicamente los componentes orgánicos inhiben la disolución de los cristales (20). Sin embargo, hay estudios in vitro en los que el esmalte temporal con mayor cantidad de contenido orgánico se disuelve considerablemente más rápido que el esmalte permanente. La desmineralización del esmalte permanente y temporal en un medio acídico muestra diferencias significativas con un esmalte primario que registra una susceptibilidad mayor a la desmineralización (21).
Al igual que en la investigación realizada por Sánchez y col. (9) en este proyecto no se encontró una relación entre la prueba y la historia de caries. Una posible explicación para estos resultados podría ser relacionada con la adsorción de los componentes salivares que reducen los rangos de disolución ácida del carbonato de apatita. La película adquirida ha mostrado ser altamente efectiva en la inhibición de la disolución, lo cual sugiere que la maduración de esta película aumenta la protección contra la disolución ácida en pruebas in vivo e in vitro, de tal manera que esta maduración permite la formación de una cubierta ácido resistente de sitios químicos activos en la superficie de apatita, altamente efectiva para obstaculizar la difusión de iones hidrógeno a la superficie de apatita y de iones de calcio y fosfato de los minerales del diente (22).
La película adquirida se forma por una adsorción selectiva de proteínas salivares y glicoproteínas a la superficie del diente. La formación de la película es un proceso complejo y los lípidos (23) y carbohidratos (24) también son incorporados en esta película durante la maduración. No es muy claro cuál de los componentes o combinaciones son responsables por la acción protectora en la superficie del diente. Se ha encontrado que la formación de la película adquirida in vivo es rápida dentro de la primera hora, y no cambia en cantidad considerable después de este tiempo. Es posible que ocurran cambios cualitativos en el tiempo y que, por lo tanto, se aumente la protección mineral de la apatita contra en ataque ácido (22).
La falta de concordancia entre los resultados de la prueba aplicada en este estudio y la presencia o ausencia de caries en los pacientes puede relacionarse con lo registrado en pruebas de susceptibilidad del esmalte a la caries dental realizadas en adultos, que han concluido que las diferencias entre los grupos de pacientes con alta y baja experiencia de caries se encuentran en los conteos de lactobacilos y en la habilidad para la producción de ácido (Test de Snyder). Adicionalmente, hay una diferencia en el rango del flujo salivar y la habilidad para neutralizar los ácidos que es estadísticamente significativa (25). Esto implicaría pensar que una prueba aislada como la de la disolución ácida en el caso de los adultos no es suficiente para predecir fenómenos tan complejos y multifactoriales como la caries o la erosión dental.
Otros estudios sobre la susceptibilidad del esmalte a la disolución han determinado que existen inhibidores del proceso como el ión flúor; sin embargo, existe otra familia de inhibidores de la disolución del esmalte como es el grupo de los bifosfonatos. La mayor parte de la atención en la literatura se ha centrado en el EHDP (Etano-1-hidroxi-1,1 difosfonato) y en el MHDP (mentono-hidroxi-difosfonato) (26, 27). Tan pronto como ocurre la inhibición de la disolución de los componentes de apatita del esmalte, el comportamiento de los dos componentes (EHDP y MHDP) es similar. Pero en investigaciones in vitro se ha observado que una substancia que actúa como un inhibidor de la desmineralización del tejido duro está presente en una concentración tan alta que es suficiente para formar una concentración significativa de complejos con el enrejado de iones disueltos; de esta manera, se disminuiría el efecto de la inhibición sobre la disolución. Hay al menos dos razones para que esto ocurra: a) que la concentración de un inhibidor puro, no complejo, esté disminuida, y b) que al menos una concentración de un enrejado de iones no complejos esté también disminuida. El segundo efecto sería importante en el desarrollo de la caries dental, particularmente en sistemas en los cuales los iones de calcio son complejos (28). Una reducción de la concentración de calcio a un valor constante de pH produce un efecto grande sobre el rango de disolución de la hidroxiapatita que produce a su vez una reducción similar en la concentración de fosfatos (29).
En esta investigación no se encontró una concordancia entre la prueba y la susceptibilidad del esmalte a la disolución ácida. Tanto la naturaleza de la lesión del esmalte como el rango de tiempo en que se forma son altamente dependientes de la composición y de las propiedades de la solución desmineralizante. El rango de desmineralización es inversamente proporcional al pH de la solución y del DS (radio del promedio del producto de la actividad iónica de la hidroxiapatita en solución, a su producto de solubilidad constante). Bajo condiciones experimentales, con valores relativamente altos de pH, no se forman lesiones subsuperficiales en el esmalte; sin embargo, estas lesiones aparecen consistentemente en soluciones con valores de pH inferiores a 5,5.
La desmineralización del esmalte ocurre en dos fases, una fase inicial de desmineralización que es seguida por una fase subsecuente que corresponde a la porción mayor de pérdida mineral. La fase inicial lenta de desmineralización puede estar relacionada con las propiedades de la superficie del esmalte o con el desarrollo de una capa superficial altamente mineralizada en una lesión subsuperficial en formación. Todo esto lleva a relacionar la actividad de la caries con un factor que determina el potencial cariogénico. Este factor es el potencial del fluido de la placa dental (30).
Para evaluar el potencial relativo de desmineralización in vivo (en términos de predecir las tasas de desmineralización del esmalte) se deben considerar ambos, el DS y la actividad acídica total presentes en los fluidos de la placa bajo las condiciones de producción ácida (por ejemplo, después de la de la exposición a carbohidratos fermentables). El pH del fluido de la placa desciende bruscamente (de pH 7 a 5) como resultado de un aumento en la concentración de ácido láctico total/(de 2 mmol/l a más de 30 mmol/l). Otros ácidos orgánicos (por ejemplo, ácido acético y propiónico) están presentes en concentraciones apreciables (30 mmol/l) antes y después de la producción de ácido láctico (30).
Estos ácidos también deben ser tenidos en consideración como lo han establecido previamente otros investigadores (31). El potencial de desmineralización de cualquier medio que incluye fluido de placa dental es altamente dependiente del DS; por ejemplo, la tasa de desmineralización predictiva en una solución de ácido láctico (65 mmol/l, pH 5) con un DS de 0,28 será aproximadamente 18 veces mayor que lo que se predice para una solución de ácido láctico de la misma concentración y pH con un DS de 0,38. Los estudios in vitro sugieren que inclusive diferencias relativamente pequeñas de DS encontradas en los fluidos de la placa pueden resultar en diferencias muy significativas en la tasas de desmineralización del esmalte in vitro (30).
El protocolo de la prueba estandarizada aplicada en esta investigación no incluye la información acerca del DS del ácido empleado para poder haberlo comparado con el DS de los ácidos que se producen en placa dental, pero queda expuesta la posibilidad de que la reacción del esmalte adulto a un ácido esté relacionada con el DS y que de ello dependa la susceptibilidad a disolverse.
Muchos métodos han sido propuestos con el fin de lograr una correcta predicción de la susceptibilidad del esmalte a la disolución ácida, algunos individuales y otros que combinan varias alternativas, incluyendo test microbiológicos y pruebas en saliva (32-34).
Alaluusua y col. (35) han mostrado que en las pruebas individuales la experiencia pasada de caries es más sensible y específica que las pruebas microbiológicas de saliva como predictor de un aumento de caries futura. En general, las lesiones incipientes de caries (36) y la historia pasada de caries (37-40) son los mejores predictores de la susceptibilidad a la aparición de nuevas caries dentales. El inicio del proceso carioso no se puede atribuir a una sola causa, pues para su desarrollo se requiere la interacción de tres factores principales: agresión al esmalte de gran magnitud, insuficiente resistencia del esmalte a la disolución ácida y ausencia de los mecanismos de remineralización (41).
No hay concordancia entre la susceptibilidad a la disolución ácida del esmalte y la experiencia pasada de caries en adultos jóvenes según la prueba colorimétrica RM.
1. Dirección Territorial de Salud de Caldas. Perfil epidemiológico 2008. Caldas: Dirección Territorial de Salud de Caldas; 2008. [ Links ]
2. Ministerio de la Protección Social de Colombia. Decreto 3039 de 2007. Plan Nacional de Salud Pública 2007-2010. Ministerio de la Protección Social de Colombia;2007. [ Links ]
3. Rodríguez Miro, MJ. Etiopatogenia de la caries dental. Actualidad en estomatología, serie Inf Tem 3 1979; 1. En: Rodríguez M, Gispert E, Rodríguez J, Fonte M, Vega D, Rojas G, Rodríguez A, Cantillo E, Ávila L. Resistencia del esmalte a la disolución ácida: su relación con la actividad cariogénica. Rev Cubana Estomatol 1989;26(1-2):57-69. [ Links ]
4. Jenkins GN. Some physiological aspects of dental caries: physiology and biochemistry of the mouth. Blacwell scientific publications 1978; 9:255-269. In: Tucker K, Adams M, Shaw L, Smith AJ. Human enamel as a substrate for in vitro acid dissolution studies: Influence of tooth surface and morphology. Caries Res 1998;32:135-40. [ Links ]
5. Curzon ME et al. Strontium in drinking water and dental caries. J Dent Res (Spec Issue 1977) Abstrac 167,A 84. [ Links ]
6. Isokangas P, Alanen P, Tiekso J. The clinician's ability to identify caries risk subjects without saliva tests - a pilot study. Community Dent Oral Epidemiol 1993; 21:8-10. [ Links ]
7. Boletín Informativo. Cooperación técnica entre países del área Andina, Centroamérica y Caribe Hispano. Centro Nacional de Materiales Dentales (CNMD) Dr. Hugo Paolini Ricci. Universidad Central de Venezuela 1991; 4 [ Links ]
8. Gisper E, Cantillo E, Rivero A, Cruz M. Remineralización in vivo del esmalte desmineralizado artificialmente. Rev Cub Estomatol 2001;38(1):5-9. [ Links ]
9. Sánchez TL, Sáenz LP, Gómez ME, Pérez J. Resistencia del esmalte a la disolución ácida y su correlación con la caries dental. Rev Salud Pub Méx 1995;37(3):224-31. [ Links ]
10. Rodríguez MJ, Gispert E, Gallego J, Fonte M, Vega D, Rojas Rodríguez A, Cantillo E, Rodríguez A, Ávila LE. La resistencia del esmalte a la disolución ácida: su relación con la actividad criogénica. Rev Cub Estomatol 1989;26(1-2)57-69. [ Links ]
11. Pelton AR, Gronsky R, Williams DB. Images of materials. Oxford: Oxford University Press;1991. In: Wang LJ, Tang R, Bonstein T, Bush P, Nancollas GH. Enamel demineralization in primary and permanent teeth. J Dent Res 2006;85(4):359-63. [ Links ]
12. Veis A. Mineralization in organic matrix frameworks. In: Dove PM, De Yoreo JJ, Weiner S, editors. Biomineralization. Reviews in mineralogy and geochemistry. Washington, DC: The Mineralogical Society of America; 2003. p. 249-89. [ Links ]
13. Shellis RP. Relationship between human enamel structure and the formation of caries-like lesions in vitro. Arch Oral Biol 1984;29:975-81. [ Links ]
14. Sonju Clasen AB, Ogaard B, Duschner H, Ruben J, Arends J, Sonju T. Caries development in fluoridated and non-fluoridated deciduous and permanent enamel in situ examined by microradiography and confocal laser scanning microscopy. Adv Dent Res 1997;11:442-7. [ Links ]
15. Dowker SE, Elliott JC, Davis GR, Wassif HS. Longitudinal study of the three-dimensional development of subsurface enamel lesions during in vitro demineralization. Caries Res 2003; 37:237-45. [ Links ]
16. Naujoks R, Schade H, Zelinka F. Chemical composition of different areas of the enamel of deciduous and permanent teeth (the content of Ca, P, CO2, Na and N2). Caries Res 1967;1:137-43. [ Links ]
17. Angker L, Nockolds C, Swain MV, Kilpatrick N. Quantitative analysis of the mineral content of sound and carious primary dentine using BSE imaging. Arch Oral Biol 2004;49:99-107. [ Links ]
18. Cuy JL, Mann AB, Livi KJ, Teaford MF, Weihs TP. Nanoindentation mapping of the mechanical properties of human molar tooth enamel. Arch Oral Biol 2002;47:281-91. [ Links ]
19. Le Geros RZ. (1991). Calcium phosphates in oral biology and medicine. Basel: Karger. In: Wang LJ, Tang R, Bonstein T, Bush P, Nancollas GH. Enamel demineralization in primary and permanent teeth. J Dent Res 2006; 85(4):359-63. [ Links ]
20. Weiner S, Dove PM. (2003). An overview of biomineralization processes and the problem of the vital effect. In: Dove PM, De Yoreo JJ, Weiner S, editors. Biomineralization. Reviews in mineralogy and geochemistry. Washington, DC: The Mineralogical Society of America;2003. p. 1-29. [ Links ]
21. Wang LJ, Tang R, Bonstein T, Bush P, Nancollas GH. Enamel demineralization in primary and permanent teeth. J Dent Res 2006;85(4):359-63. [ Links ]
22. Kautsky MB, Featherstone JDB. Effect of salivary components on dissolution rates of carbonated apatites. Caries Res 1993;27:373-77. [ Links ]
23. Slominay BL, Murty VLN, Zdebska E, Slomiany A, Gwodzinsky K, Mande IE. Tooth surface pellicle lipids and their role in the protection of dental enamel against acid lactic diffusion in man. Arch oral boil 1986;31:187-91. [ Links ]
24. Fischer SJ, Prakophol A, Kajisa L, Murray PA. External radiolabellin of components of pellicle on human enamel and cementum. Arch oral Biol 1987;32:509-17. [ Links ]
25. Rovelstad GH, Geller JH, Cohen AH. Caries susceptibility tests, hyaluronidase activity of saliva and dental caries experience. J Dent res 1958;32(2):306-11. [ Links ]
26. Ellliot K, Fitzsimons DW, editors. Hard tissue Growth, repair and remineralization. CIBA oundation Symposium No. 11. Amsterdam: Elsevier: 57-990. In: Christoffersen J, Cristoffersen MR, Ruben J, Arends J. The effect of EHDP concentration on enamel demineralization in vitro. J Dent Res 1991;70(2):123-26. [ Links ]
27. Featherstone JDB, Duncan JF, Cutress TW. Amechanism for dental caries base don chemical processes and diffusion phenomena during in vitro caries simulation on human tooth enamel. Arch Oral Biol 1979;24:101-12. [ Links ]
28. Christoffersen J, Cristoffersen MR, Ruben J, Arends J. The effect of EHDP concncetration on enamel demineralization in vitro. J Dent Res 1991;70(2):123-26. [ Links ]
29. Christoffersen J, Cristoffersen MR. Kinetics of dissolution of calcium hidroxyapatyte II.dissolution in non-stoichiometric solutions at constant pH. J Crystal Growtrh 1979;47:671-79. [ Links ]
30. Margolis HC, Zhang YP, Lee CY, Kent RL, Moreno EC. Kinetics of enamel demineralization in vitro. J Dent Res 1999;78(7):1326-55. [ Links ]
31. Featherstone JD, Rodgers BE. Effect of acetic, lactic and other organic acids on the formation of artificial carious lesions. Caries Res 1981;15:377-85. [ Links ]
32. Johnson NW, editor. Risk markers for oral diseases. Volume I, Dented Caries, Markers of high and low risk groups and individuals. Cambridge: Cambridge University Press;1991. In: Isokangas P, Alanen P, Tiekso J. The clinician's ability to identify caries risk subjects without saliva tests - a pilot study. Community Dent Oral Epidemiol 1993;21:8-10. [ Links ]
33. Bader JD, editor. Risk and assessment in dentistry. Chapel Hill: University of North Carolina Dental Ecology; 1990. In: Isokangas P, Alanen P, Tiekso J. The clinician's ability to identify caries risk subjects without saliva tests - a pilot study. Community Dent Oral Epidemiol 1993:21:8-10. [ Links ]
34. Stamm JW, Disney JA, Graves RC, Bohannan HM, Albernathy JR. The University of North Carolina caries risk assessment study. 1: Rationale and content. J Public Heallh Dent 1988;48:225-232. In: Isokangas P, Alanen P, Tiekso J. The clinician's ability to identify caries risk subjects without saliva tests - a pilot study. Community Dent Oral Epidemiol 1993;21:8-10. [ Links ]
35. Alaluusua S, Kleemola -Kujala E, Gronross L, Evalahti M. Salivary caries-related tests as predictors of future caries increment in teenagers. A three-year longitudinal study. Oral Microhiot Immunol 1990;5-77-81. [ Links ]
36. KlocK B, Krasse B. A comparison between different methods for prediction of caries activity. Scand J Dent Res 1979; H7:129-39. [ Links ]
37. Birkeland JM, Broch L, Jorkjen J L.Caries experience as predictor for caries incidence. Community Dent Oral Epidemiol 1976;4:66-9. [ Links ]
38. Seppa L, Haussen H. Frequency of initial caries lesions as predictor of future caries increment in children. Scand J Dent Res 1988;96: 9-13. [ Links ]
39. Seppa L, Hausen H, Pollanen L, Helasjharju K, Karkkainen S. Past caries recording made in Public Dental Clinics as predictors of caries prevalence in early adolescence. Community Dent Oral Epidemiol 1989;17:277-81. [ Links ]
40. López OP, Cerezo MP, Paz AL. Puesta a prueba de un instrumento que predice el riesgo de caries dental. Rev Col de investigación en odontología [serie en línea] 2010 [citado 2011 Mar 17];1(2). Disponible en URL: http://rcio.org/index.php/rcio/article/viewArticle/23 [ Links ]
41. Silverstone LM. The histopathology of enamel lesions produced in vitro previously exposing to calcifying fluids. Caries Res, 1970;4:31-48. In: Sánchez TL, Sáenz LP, Gómez MA, Pérez J. Resistencia del esmalte a la disolución ácida y su correlación con la caries dental. Salud Pública Mex 1995;37:224-31. [ Links ]














