Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO  Similars in Google
Similars in Google
Share
Revista Colombiana de Reumatología
Print version ISSN 0121-8123
Rev.Colomb.Reumatol. vol.13 no.2 Bogotá June 2006
Presentación de caso y revisión de la literatura
Carlos Jaime Velásquez Franco1, Luis Alberto Ramírez Gómez2
1Médico Internista, Residente de Reumatología, Universidad de Antioquia.
2Profesor Titular y Jefe de la Sección de Reumatología, Hospital Universitario San Vicente de Paúl, Universidad de Antioquia, Medellín, Colombia.
Resumen
Se presenta el caso de un paciente de 26 años, con síndrome de falla cardíaca, síntomas respiratorios persistentes, fibrilación auricular y muerte súbita por taquicardia ventricular no sostenida; con evidencia ecocardiográfica de insuficiencia mitral severa y confirmación histológica e imaginológica pulmonar de sarcoidosis.
Palabras clave: sarcoidosis, falla cardíaca, insuficiencia mitral, fibrilación auricular.
Summary
The following case presents a 26 year-old man with heart failure, persistent respiratory symptoms, atrial fibrillation and sudden death due to non-sustained ventricular tachycardia with echocardiografic evidence of severe mitral insufficiency and histologic and imagenologic pulmonary evidence of sarcoidosis.
Key words: sarcoidosis, heart failure, mitral insufficiency, atrial fibrillation.
Introducción
La sarcoidosis es una enfermedad multisistémica de etiología desconocida, descrita inicialmente en 1877 por Jonathan Hutchinson, quien informó el caso de un paciente europeo con múltiples lesiones cutáneas en parches, violáceas y levantadas(1). En la actualidad, la sarcoidosis se define como una enfermedad granulomatosa crónica que se caracteriza por un gran número de macrófagos y de linfocitos T activados. El granuloma está compuesto por la confluencia de varias células epiteliodes sin necrosis de caseificación. Para el diagnóstico de esta entidad, se deben excluir, en primera instancia, enfermedades granulomatosas de etiología definida. La sarcoidosis tiene una distribución global, con predilección por la raza negra y el género femenino. Es más prevalente en ciertas áreas geográficas. Todos los órganos pueden estar comprometidos, pero los granulomas y los cambios radiológicos ocurren, con mayor frecuencia, en los pulmones, hasta en el 90% de los pacientes(2). Los hallazgos pulmonares más frecuentes son: linfadenopatías hiliares bilaterales, infiltrados pulmonares y alteraciones espirométricas obstructivas o restrictivas. El compromiso de otros órganos oscila entre un 25 y un 70%(3,4).
Se presenta el caso de un paciente con sarcoidosis cardíaca, que es una presentación poco frecuente de esta entidad, asociada a sarcoidosis pulmonar estadio IV (fibrosis pulmonar).
Reporte de caso
Resumen historia clínica
Paciente masculino de 26 años, natural y residente en Quibdó (Chocó), peluquero. Con cuadro clínico de seis meses de evolución: dolor torácico opresivo y difuso refractario al consumo de analgésicos, disnea progresiva, edema de miembros inferiores de predominio vespertino, con ortopnea y disnea paroxística nocturna. El paciente presentó pérdida subjetiva de peso, astenia, adinamia e hiporexia. Hace un mes inicia con tos que, al comienzo, era seca y, a las dos semanas, se tornó productiva blanquecina y luego amarillenta de manera intermitente, con episodios de hemoptisis. Ningún antecedente personal relevante. Examen físico de ingreso al Hospital Universitario San Vicente de Paúl: regular estado general, caquéctico, disneico. Pulso: 100/minuto; frecuencia cardíaca: 140/minuto; arrítmica; presión arterial de 100/70; FR 24/minuto. Auscultación cardíaca con ritmo de galope S3 y soplo holosistólico mitral III/VI; auscultación pulmonar con crépitos difusos de predominio bibasal, hepatomegalia dolorosa 5 cm. por debajo del reborde costal derecho a la palpación abdominal; no esplenomegalia. Reflujo hepatoyugular positivo. Ingurgitación yugular grado III. Presencia de adenopatía supraclavicular izquierda, de 3 cm. de diámetro, bordes irregulares, consistencia pétrea, no dolorosa y ausencia de adenopatías en alguna otra cadena ganglionar. En anasarca. Se inicia manejo médico con restricción hídrica, diuréticos, digitálicos endovenosos y vasodilatadores, sin mejoría.
Resultados de paraclínicos relevantes
Hemograma con recuento de linfocitos de 1352/mm3 (2000-4000); hemoglobina: 14 g/dL (13,5-17,5); eritrosedimentación: 22 mm/3 (0-17); proteína C reactiva: 1,51 mg% (0-1); creatinina: 1,5 mg% (0,5-1); calcio sérico: 10,8 mg% (9-10); AST 52 U/L (0-35), ALT 74 U/L (0-35); estudios microbiológicos negativos, tuberculina con 0 mm de induración; factor reumatoide: 25 UI (menor de 20 UI); ecocardiografía transtorácica con prolapso valvular mitral e insuficiencia moderada, hipertrofia de ventrículo izquierdo con severa disfunción sistólica (fracción de eyección del 15%) y severa dilatación de la aurícula izquierda (área de 4,6 cm.).
Se toma EKG con evidencia de fibrilación auricular con respuesta ventricular rápida (Figura 1).
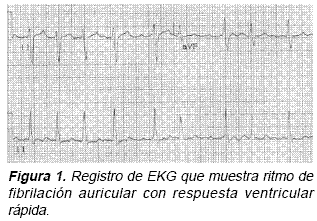
También se toman: radiografía del tórax PA y lateral izquierda (Figura 2) y TAC del tórax simple y contrastado (Figura 3).
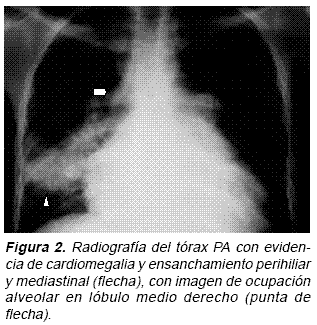
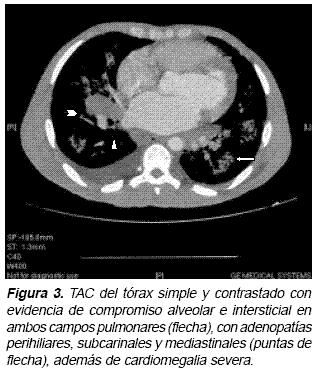
El paciente presenta compensación paulatina del síndrome de falla cardíaca con manejo médico (furosemida 80 mg IV, captopril en dosis crecientes desde 12,5 mg hasta 50 mg/día, metoprolol a dosis bajas desde 6,25 mg hasta 25mg/día) y control adecuado de la respuesta ventricular con beta metildigoxina 0,1 mg/día y anticoagulación con warfarina. Se le practica biopsia excisional de adenopatía supraclavicular izquierda, que se envía para estudio de anatomía patológica y microbiológico. Las coloraciones para hongos, bacterias y micobacterias, al igual que los cultivos para estos microorganismos fueron negativas y la anatomía patológica reportó reacción granulomatosa crónica no caseificante compatible con sarcoidosis (Figura 4).
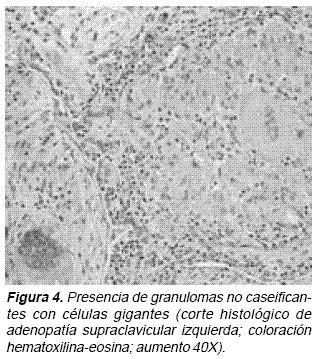
Se inicia tratamiento inmunosupresor concomitante con prednisolona 1mg/kg/día y metotrexate 10 mg IM semanal, con mantenimiento de la compensación del síndrome de falla cardíaca y control adecuado de la respuesta ventricular.
A la semana siguiente, el paciente presenta aumento de la tos e incremento de los infiltrados pulmonares, por lo cual es evaluado por Neumología, quien decide llevarlo a fibrobroncoscopia para toma de estudios microbiológicos para descartar proceso infeccioso concomitante. Durante el procedimiento, sin documentarse hipoxemia y en total compensación de la falla cardíaca, presenta episodio de taquicardia ventricular con colapso hemodinámico, refractario a reanimación cardiopulmonar avanzada y cardioversión eléctrica. El paciente fallece. La familia del paciente no acepta el procedimiento de necropsia.
Discusión
El primer caso de sarcoidosis cardíaca se informó en 1929 cuando Bernstein describió la presencia de granulomas sarcoides que comprometían pericardio(5). En 1977, Roberts informó el resultado de 113 necropsias realizadas a estos pacientes, encontrando que la ubicación más frecuente de granulomas fue la pared libre ventricular izquierda, seguida del septum interventricular. Silverman analizó los resultados de 84 autopsias consecutivas de pacientes con sarcoidosis, con edad promedio de 46 años; el 61% eran mujeres. El 27% de estos pacientes presentó granulomas miocárdicos; el 35% fue clínicamente silente y el resto tenía historia de falla cardíaca o trastornos de la conducción. Cuatro pacientes presentaron muerte súbita y en solo dos de ellos existió la sospecha clínica premortem de sarcoidosis(6). En un estudio retrospectivo de 18 mujeres y 23 hombres con sarcoidosis cardíaca, la edad promedio al momento del diagnóstico de compromiso cardíaco fue 38 años. El 73% de los pacientes eran caucásicos. Todos los pacientes tenían evidencia extracardíaca de compromiso por sarcoidosis. El 63% de los pacientes presentaron anormalidades estructurales (evidentes en la ecocardiografía en el 70%) y el 22%, alteraciones eléctricas(7).
Desde entonces, se han descrito varias clases de compromiso cardíaco por esta enfermedad, incluyendo anormalidades en el sistema de conducción, insuficiencia mitral, insuficiencia cardíaca, aneurismas ventriculares, derrame y taponamiento pericárdicos, pericarditis, arritmias ventriculares y muerte súbita. En este paciente que se informa, se presentaron: trastornos del ritmo supraventriculares y ventriculares, insuficiencia mitral, insuficiencia cardíaca, muerte súbita y evidencia histopatológica de sarcoidosis, hallazgos que confirman el compromiso cardíaco por sarcoidosis.
El compromiso cardíaco ocurre en el 20 a 27% de los pacientes con sarcoidosis en Estados Unidos; se ha descrito una frecuencia hasta del 58% en pacientes japoneses. La evidencia clínica de sarcoidosis cardíaca solo se presenta en el 5% de los casos(8). Las manifestaciones clínicas específicas dependen de la localización y extensión del miocardio comprometido. Con respecto al compromiso cardíaco evidenciado en este paciente, las arritmias supraventriculares se presentan en un 19% de los casos; se atribuyen, como causas probables, la dilatación auricular secundaria a disfunción ventricular izquierda o a cor pulmonale o por el compromiso directo auricular como foco de ritmo ectópico. También se describe, como en este paciente, disfunción valvular en sarcoidosis cardíaca; la insuficiencia mitral (aguda o crónica) es el hallazgo más frecuente; parece explicarse con compromiso directo de los músculos papilares; se presenta en el 68% de los casos(5,6).
Otra manifestación de sarcoidosis cardíaca es el síndrome de falla cardíaca, que es la segunda causa de muerte en estos pacientes, luego de la muerte súbita. Por la infiltración de sarcoide, puede presentarse rigidez ventricular (disfunción diastólica o disminución severa de la contractilidad y posterior disfunción sistólica). Fahy estudió 50 casos de sarcoidosis pulmonar, donde el 14% de ellos presentó disfunción diastólica e insuficiencia mitral concomitantes. Puede ocurrir la presentación clínica de cardiomiopatía restrictiva o dilatada. La presencia de falla cardíaca implica un pobre pronóstico, con una importante disminución de la sobrevida a corto y a largo plazo (3-5 años), cuando la fracción de eyección es menor del 50% (en el paciente informado, la fracción de eyección fue del 15%). Con respecto a la presencia de arritmias ventriculares, la más frecuente es la taquicardia ventricular (TV) sostenida o no sostenida, que se detecta en el 23% de los pacientes y es la segunda presentación cardíaca más frecuente, luego de los bloqueos AV. Se presume que la TV es la causa de muerte súbita en estos pacientes. La fisiopatología de este trastorno del ritmo consiste en un mecanismo de reentrada alrededor de la infiltración por sarcoide. Existe una alta frecuencia de recurrencia de TV en estos pacientes y de muerte súbita, como es el caso del paciente(5,6).
Con respecto al tratamiento de las sarcoidosis cardíacas, éste debe ir dirigido a aliviar los síntomas, controlar el proceso inflamatorio, prevenir el deterioro posterior de la función miocárdica y prevenir la muerte súbita. Por tanto, el tratamiento debe instaurarse una vez hecho el diagnóstico, sin esperar el desarrollo de los síntomas. El pilar fundamental es el uso de corticosteroides, independiente de la presentación clínica. Estos medicamentos han demostrado mejorar el pronóstico a largo plazo y revertir las anormalidades de conducción, además de mejorar las pruebas de perfusión miocárdica. También existe evidencia imaginológica de disminución de los granulomas miocárdicos por resonancia magnética luego de la terapia esteroidea; ésta no tiene mucho impacto una vez establecida la disfunción ventricular(9). En casos refractarios o de importantes efectos adversos causados por los corticosteroides, existen alternativas terapéuticas, como: metotrexate, ciclosporina o ciclofosfamida(10). También debe mencionarse, como parte del manejo de la sarcoidosis cardíaca, el tratamiento de la falla cardíaca. El papel de los antiarrítmicos no está claramente definido, por la neumonitis y fibrosis pulmonar asociadas a su utilización (especialmente la amiodarona) y por la alta tasa de recurrencia y de muerte súbita pese a su utilización. En casos de bloqueo AV avanzado, está indicado el uso de marcapasos, hecho que ha disminuido la frecuencia de muerte súbita y mejorado el pronóstico. Con respecto al trasplante cardíaco, éste podría tener un papel en los pacientes con clase funcional NYHA IV, con mejoría de la calidad de vida y en los cuales la sarcoidosis esté limitada al corazón, pero con probabilidad de recurrencia(11).
Pese a no disponer de la demostración histológica del compromiso cardíaco en este paciente, no hubo evidencia de otras enfermedades que explicaran el cuadro clínico descrito; por ello se piensa y se confirma el caso de un paciente con sarcoidosis cardíaca con compromiso pulmonar estadio IV.
Referencias
1. Nagai S. Pulmonary sarcoidosis: pathogenesis and population differences. Intern Med 1995; 34: 833-838. [ Links ]
2. Cox CE, Davis-Allen A, Judson MA. Sarcoidosis. Med Clin North Am 2005; 89: 817-828. [ Links ]
3. Koyama T, Ueda H, Togashi K, Umeoka S, Kataoka M. Radiologic Manifestations of Sarcoidosis in Various Organs. RadioGraphics 2004; 24: 87-104. [ Links ]
4. Lynch JP, Kazerooni EA, Gay SE. Pulmonary Sarcoidosis. Clin Chest Med 1997; (4): 755-785. [ Links ]
5. Bargout R, Kelly RF. Sarcoid heart disease: clinical course and treatment. Int J Cardiol 2004; 173-182. [ Links ]
6. Silverman KJ, Hutchins GM, Bulkley BH. Cardiac sarcoid: a clinicopathologic study of 84 unselected patients with systemic sarcoidosis. Circulation 1978; 58: 1204-1211. [ Links ]
7. Chapelon-Abric C, de Zuttere D, Duhaut P, Veyssier P, Wechsler B. Cardiac Sarcoidosis: A Retrospective Study of 41 Cases. Medicine 2004; 83: 315-334. [ Links ]
8. Giuffrida TJ, Kerde FA. Sarcoidosis. Dermatol Clin 2002; 20: 435-447. [ Links ]
9. Ishikawa T, Kondoh H, Nakagawa S, Koiwaya Y, Tanaka K. Steroid therapy in cardiac sarcoidosis. Increased left ventricular contractility concomitant with electrocardiographic improvement after prednisolone. Chest 1984; 85: 445-447. [ Links ]
10. Lower EE, Baughman RP. The use of low dose methotrexate in refractory sarcoidosis. Am J Med Sci 1990; 299: 153-157. [ Links ]
11. Donsky AS, Escobar J, Capehart J, Roberts WC. Heart transplantation for undiagnosed cardiac sarcoidosis. Am J Cardiol 2002; 89: 1447-1450. [ Links ]














