Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Reumatología
Print version ISSN 0121-8123
Rev.Colomb.Reumatol. vol.35 no.3 Bogotá July/Sept. 2007
Presentación de caso y Revisión de la literatura
Síndrome de Sjögren primario con neumonía intersticial linfocítica y enfermedad quística pulmonar
Primary Sjögren's syndrome with lymphocitic interstitial pneumonia and cystic pulmonary disease
Jimi Mejía-Vallejo1, Jorge Carrillo-Bayona2, Antonio Iglesias-Gamarra3, Federico Rondón4, Álvaro Sánchez Contreras4, José Félix Restrepo5
1. Residente I de Reumatología
2. Profesor Asociado de Radiología Universidad Nacional de Colombia
3. Profesor Titular de Medicina Interna y Reumatología. Universidad Nacional de Colombia
4. Profesor Asociado de Medicina Interna y Reumatología. Universidad Nacional de Colombia
5. Profesor Titular de Medicina Interna y Reumatología. Universidad Nacional de Colombia. Coordinador Unidad de Reumatología.
Recibido para publicación: julio 27/2007 Aceptado en forma revisada: agosto 31/2007
Resumen
El síndrome de Sjögren primario (SSP) es una exocrinopatía autoinmune crónica caracterizada por infiltración linfocítica de tejido glandular y extraglandular; el compromiso pulmonar es heterogéneo; el objetivo del presente estudio es informar el primer caso en Colombia de SSP con neumonía intersticial linfocítica y enfermedad quística pulmonar, plantear diagnósticos diferenciales, abordaje diagnóstico y alternativas terapéuticas.
Palabras clave: síndrome de Sjögren primario, enfermedad pulmonar quística, neumonía intersticial linfocítica.
Summary
The primary Sjögren's syndrome (PSS) is a chronic autoimmune exocrinopathy characterized by lymphocytic infiltration of glandular and extraglandular tissue, the lung involvement is heterogeneous; the aim of this study is report the first case in Colombia of PSS with lymphocytic intersticial pneumonia and cystic pulmonary disease discuss differential diagnosis and the initial diagnostic and therapeutic work up.
Key words: primary Sjögren's syndrome, cystic lung disease, lymphocytic interstitial pneumonia.
Introducción
El síndrome de Sjögren es una exocrinopatía autoinmune crónica caracterizado por infiltración linfocítica glandular y extraglandular asociado a producción de autoanticuerpos1. Sus criterios diagnósticos incluyen queratoconjuntivitis sicca y xerostomia más la presencia de un criterio autoinmune2. Diferentes manifestaciones pulmonares han sido descritas en el síndrome de Sjögren las cuales incluyen compromiso de la vía aérea superior, compromiso de la vía aérea inferior, enfermedad pulmonar intersticial, quistes pulmonares, infiltrado nodular focal o difuso (linfoma3, pseudolinfoma, amiloidosis, hiperfuncionalidad de tejido linfoide asociado a bronquios)4. Aquí se describe el primer caso en Colombia de síndrome de Sjögren primario con múltiples quistes pulmonares asociado a un patrón imagenológico de neumonía intersticial linfocítica.
Caso
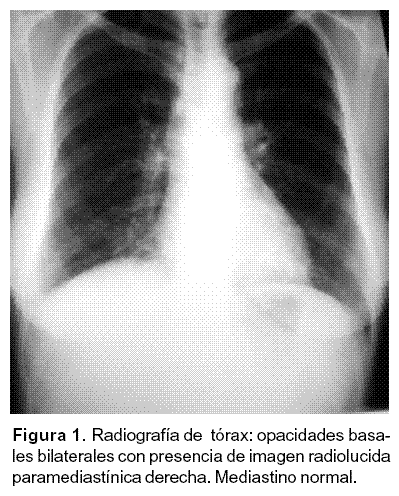
Paciente de 66 años de edad, sexo femenino, valorada en abril de 2007 por xeroftalmia, xerostomía, xeromicteria, xerodermia, fatiga, tos seca y disnea clase funcional II de dos años de evolución; con fenómeno de Raynaud, artralgia en muñeca izquierda, prurito de predominio nocturno, pérdida de peso de 12 kg en dos años; sin antecedentes ginecoobstétricos relevantes y con exposición a humo de combustión vegetal por 10 años; presión arterial de 100/60 mm Hg, frecuencia cardíaca 100 por minuto, frecuencia respiratoria 18 respiraciones minuto, peso de 43 kg, inyección conjuntival leve bilateral, exploración cardiopulmonar normal, hipocratismo digital leve. El laboratorio muestra leucocitos 3700 x mm3 (neutrófilos 43%, linfocitos 30%, monocitos 26%, basófilos 0,3%, eosinófilos 0,3%), hemoglobina 17,5 g/dl, hematocrito 54%, VCM 98 /fl, plaquetas 148000 uL, VSG 1 mm/h, ANAS positivos (patrón homogéneo 1/640), anticuerpos anti-La positivo 23 (positividad índice mayor de 15); anticuerpos anti-Ro negativos, factor reumatoide negativo; radiografía del tórax con infiltrados intersticiales reticulonodulares bibasales e imagen radiolúcida parahiliar derecha (Figura 1) y TAC de tórax de alta resolución con imágenes quísticas múltiples en ambos campos pulmonares, la de mayor tamaño paramediastínica derecha con diámetro mayor de 4,5 cm, con presencia de patrón imaginológico de neumonía intersticial linfocítica (Figura 2), biopsia de glándula salival menor conclusiva de sialoadenitis autoinmune. Teniendo como base las características clínicas, inmunológicas e histológicas se establece el diagnóstico de síndrome de Sjögren primario con compromiso monoarticular y pulmonar. Se solicitó fibrobroncoscopia con lavado broncoalveolar que mostró negatividad para malignidad, investigación de BK negativos; se inició tratamiento con prednisolona 0,5 mg/kg/día, cloroquina 250 mg día, lágrimas artificiales; la sección de cirugía de tórax determinó no realizar biopsia pulmonar debido a la alta correlación entre los hallazgos imaginológicos y patológicos; persistió disnea y marcada xeroftalmía en controles posteriores, ante lo cual se decidió iniciar rituximab.
Discusión
El síndrome de Sjögren ha sido caracterizado como una epitelitis autoinmune y, de otra forma, como una exocrinopatía autoinmune ante la presencia de adenitis focal, presencia de anticuerpos autoreactivos, y su compleja inmunopatogénesis que incluye linfoproliferación e infiltración de linfocitos T y B en tejido glandular y extraglandular (pulmones, páncreas, tracto gastrointestinal, sistema hepatobiliar, riñones, piel y médula ósea)5-6. La historia natural del compromiso respiratorio incluye disnea, taquipnea, tos como manifestación de xerotráquea y aclaración ciliar defectuosa, disfonía, sinusitis, dolor toráxico, hiperreactividad bronquial, neumonías recurrentes, sintomatología que usualmente se establece de forma temprana en el curso de la enfermedad predominantemente en pacientes con anticuerpos anti Ro7, 8.
Diversas manifestaciones pulmonares han sido descritas en pacientes con síndrome de Sjögren, formas severas progresivas de compromiso pulmonar intersticial, con una gran variedad de patrones histológicos entre los que se encuentran: neumonía intersticial no específica, neumonía organizada criptogénica, neumonía intersticial usual, neumonía intersticial linfocítica, linfoma pulmonar primario, amiloidosis intersticial difusa9-11; el compromiso de la vía aérea incluye disección traqueobronquial, enfermedad pulmonar obstructiva, bronquitis y bronquiolitis folicular linfocítica, quistes pulmonares; el compromiso pleural también ha sido documentado (Tabla 1)12. En este informe se presenta un caso de síndrome de Sjögren primario con anticuerpos anti-La con múltiples quistes pulmonares y un patrón radiológico de neumonía intersticial linfocítica.
La neumonía intersticial linfocítica está presente en el 0,9% a 42% de pacientes con SSP13, es un desorden linfoproliferativo benigno caracterizado por proliferación intersticial difusa de linfocitos y células plasmáticas, ocurre en pacientes con síndrome de Sjögren primario, tiroiditis autoinmune, síndrome de inmunodeficiencia adquirida y enfermedad de Castleman; su historia natural es altamente variable, su comportamiento es progresivo en una tercera parte de los pacientes; su asociación con linfoma aún no está definida14.
Entre la gran variedad de manifestaciones pulmonares que presenta este síndrome la enfermedad quística pulmonar es infrecuente (11 casos publicados oficialmente en la literatura mundial); en Colombia se informó un caso de síndrome de Sjögren primario con múltiples quistes pulmonares sin compromiso intersticial6, 15.
Todos los pacientes informados han sido mujeres (incluyendo el actual), con hallazgos histopatológicos similares en donde prevalece infiltrado linfocítico y linfoplasmocítico peribronquial y peribronquiolar; la amiloidosis pulmonar estuvo en el 40% de los pacientes y se ha documentado un paciente con neumonía intersticial linfocítica; la formación de quistes en el síndrome de Sjögren parece ser generada por atrapamiento aéreo secundario al extenso infiltrado inflamatorio linfoplasmocítico de la pared bronquiolar que ejerce un efecto de válvula impidiendo una adecuada espiración, apoyado lo anterior por el marcado infiltrado de linfocitos CD4 en la mucosa bronquial; existe hiperfuncionalidad del tejido linfoide asociado a los bronquios; histológicamente estos quistes consisten en tejido pulmonar comprimido o una membrana fibrosa delgada tapizada por epitelio columnar o células epiteliales cuboidales y material hialino similar al amiloide6, 16.
Ante la evidencia clara de un síndrome de Sjögren primario las alternativas diagnósticas de quistes pulmonares síndrome incluyen el granuloma eosinofílico (un subtipo de la histiocitosis de células de Langerhans), el cual puede causar bullas como resultado de cavitación de lesiones nodulares o atrapamiento aéreo distal a bronquiolos que han sido reducidos en su luz por infiltración celular de su pared, tienden a ser numerosos y a presentarse en historia previa de tabaquismo12; diferentes tipos de enfisema pulmonar, linfangioleiomiomatosis, bronquiectasias y bronquiolitis obliterante6; la presencia de quistes pulmonares y nódulos debe hacer sospechar linfoma no Hodgkin de células B presente en el 5-10% de los pacientes con SSP teniendo en consideración la naturaleza policlonal de esta patología asociada a hipergamaglobulinemia; la neumonía intersticial linfocítica puede generar quistes pulmonares o presentarse como un patrón en vidrio esmerilado en la TAC de pulmón9,12,17; la gangrena pulmonar con necrosis masiva también ha sido informada como causa de cavitación pulmonar en SSP18. Entre las lesiones quísticas no relacionadas con el síndrome de Sjögren se encuentran las fúngicas (coccidioides, aspergillus, pneumocystys), bacterianas (staphylococcus, mycobacterium), parasitarias (paragonimus, echinococcus) que deben ser consideradas teniendo presente el compromiso inmunológico en estos pacientes12.
Las pruebas de función pulmonar muestran una combinación de patrón restrictivo y obstructivo, con predominio de este último; hay pocos cambios en la difusión de monóxido de carbono; la fibrobroncoscopia con lavado broncoalveolar es una herramienta diagnóstica útil en la diferenciación de alveolitis neutrofílica característica de fibrosis pulmonar y alveolitis por células T típica del síndrome de Sjögren; sin embargo, estos tres últimos junto con la radiografía del tórax son exámenes orientativos de poco rendimiento diagnóstico; la TAC pulmonar de alta resolución genera una orientación diagnóstica profunda en la cual se puede inferir el compromiso temprano de las vías aéreas, pleura e intersticio pulmonar, orientación que será confirmada de forma definitiva por biopsia pulmonar; sin embargo, existe buena correlación histo-radiológica 12, 19-20.
El tratamiento está basado en la administración de broncodilatadores, corticoides con disminución en el volumen de los quistes en controles tomográficos ulteriores, sin embargo su eficacia no ha sido absoluta; ante la infrecuencia de enfermedad quística pulmonar en SSP y teniendo en consideración la presencia de linfocitos B en un 20% del total del infiltrado linfoplasmocítico, y el incremento en su actividad, la alternativa basada en la hipótesis de depleción de linfocitos B con fármacos biológicos como rituximab podría ser una alternativa de tratamiento útil en el afán de evitar complicaciones potencialmente letales ante la refractariedad a tratamientos convencionales como lo hicimos en este caso6, 21.
Conclusión
Se describe el primer caso clínico en Colombia de SSP con compromiso respiratorio representado por enfermedad pulmonar quística múltiple, asociado a patrón de neumonía intersticial linfocítica; esta patología rara por su coexistencia plantea un dilema diagnóstico en el cual se debe descartar otra enfermedad reumatológica asociada que incremente el espectro diagnóstico y considerar al paciente con SSP como un individuo con compromiso inmunológico y susceptible a adquirir infecciones oportunistas que se manifiesten con quistes pulmonares; esta patología posee una aproximación terapéutica aún no completamente establecida, en donde el tratamiento convencional con esteroides no es totalmente exitoso, y sólo existe la perspectiva de utilidad de depleción de linfocitos B CD20.
Referencias
1. Larché M. A short review of the pathogenesis of Sjögren's syndrome. Autoimmunity Rev 2006; 5: 132-135. [ Links ]
2. Vitali C, Bombardieri S, Jonsson R, Moutsopoulos HM, Alexander EL, Carsons SE, et al. Classification criteria for Sjögren's syndrome: a revised version of the European criteria proposed by the American-European Consensus Group. Ann Rheum Dis 2002; 61(6): 554-558. [ Links ]
3. Pérez MT, Castillo A, Restrepo JF, Peña M, Iglesias A, Méndez O. Linfoma primario del pulmón asociado a síndrome de Sjögren primario. Acta Med Colomb 1991; 16: 222-226. [ Links ]
4. Cain HC, Noble PW, Matthay RA. Pulmonary manifestation of Sjögren's syndrome. Clin Chest Med 1998; 19: 687-699. [ Links ]
5. Konttinen YT, Porola P, Konttinen L, Laine M, Poduval P. Immunohistopathology of Sjögren's syndrome. Autoimmunity Rev 2006; 6: 16-20. [ Links ]
6. Osamu S, Naoki S, Makoto A, Hirotsugu K, Moritaka S, Masayuky. Two cases of Sjögren's syndrome with multiple bullae. Inter Med 2002; 41(2): 124-128. [ Links ]
7. Ramos-Casals M, Tzioufas A, Font J. Primary Sjögren's syndrome: new clinical and therapeutic concepts. Ann Rheum Dis 2005; 64: 347-358. [ Links ]
8. Lahdensuo A, Korpela M. Pulmonary findings in patients with primary Sjögren's syndrome. Chest 1995; 108: 316-319. [ Links ]
9. Parambil J, Myers J, Lindell R, Matteson E, Ryu J. Intersticial lung disease in primary Sjögren syndrome. Chest 2006; 130: 1489-1495. [ Links ]
10. Strange C, Highland K. Interstitial lung disease in the patient who has connective tissue disease. Clin Chest Med 2004; 25: 549-559. [ Links ]
11. Delèvaux I, Andre M, Amoura Z, Kémény J, Piette J, Aumaître O. Concomitant diagnosis of primary Sjögren's syndrome and systemic amyloidosis. Ann Rheum Dis 2001; 60: 694-695. [ Links ]
12. Scully R, Mark E, McNeely W, Shepard J, Ebeling S, Ellender S, et al. Case record of the Massachusetts General Hospital. N Engl J Med 2001; 344(22): 1701-1708. [ Links ]
13. Rockall A, Rickards D, Shaw PJ. Imaging of the pulmonary manifestations of systemic disease. Postgrad Med J 2001; 77: 621-638. [ Links ]
14. Johkoh T, Müller N, Pickford H, Hartman T, Ichikado K, Akira M, et al. Lymphocytic Interstitial Pneumonia: Thin-Section CT Findings in 22 Patients. Radiol 1999; 212: 567-572. [ Links ]
15. Rojas A, Méndez P, Iglesias-Gamarra A, Rondón F, Sánchez A, Restrepo JF. Enfermedad quística pulmonar y síndrome de Sjögren. Rev Colomb Reumatol 2002; 9(2): 131-139. [ Links ]
16. Kobayashi H, Matsuoka R, Kitamura S, Tsunoda N, Saito K. Sjögren's Syndrome with multiple bullae and pulmonary nodular amyloidosis. Chest 1988; 94: 438-440. [ Links ]
17. Sutcliffe N. Sjögren syndrome. Medicine 2006; 34(11): 476-479. [ Links ]
18. Pérez-Castrillón J, González-Castañeda C, Del Campo F, González J, Martín-Escudero J, Herreros V. Cavitary lung lesion in patient with Sjögren syndrome. Postgrad Med J 1999; 75: 765-766. [ Links ]
19. Matsuyama N, Ashizawa K, Okimoto T, Kadota J, Amano H, Hayashi K. Pulmonary lesions associated with Sjögren's syndrome: radiographic CT findings. Brit J Radiol 2003; 76: 880-884. [ Links ]
20. Ito I, Nagal S, Kitaichi M, Nicholson A, Johkoh T, Noma S, et al. Am J Respir Crit Care Med 2005; 171: 632-638. [ Links ]
21. Seror R, Sordet C, Guillevin L, Hachulla E, Masson C, Ittah M, et al. Tolerance and efficacy of rituximab and changes in serum cell biomarkers in patients with systemic complication of primary Sjögren's syndrome. Ann Rheum Dis 2007; 66: 351-357. [ Links ]