Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Reumatología
Print version ISSN 0121-8123
Rev.Colomb.Reumatol. vol.15 no.1 Bogotá Jan./Mar. 2008
las manifestaciones dermatológicas
Silvia Catalina Díaz Paúl1, Carlos Jaime Velásquez Franco2, Luis Fernando Pinto Peñaranda2, Javier Darío Márquez2
1RIII Dermatología, Universidad CES. Hospital Pablo Tobón Uribe, Medellín, Colombia.2Docente Reumatología HPTU. Hospital Pablo Tobón Uribe, Medellín, Colombia.
Recibido para publicación: noviembre 23/2007. Aceptado en forma revisada: febrero 29/2008
Resumen
El síndrome de Sjögren (SS) es una enfermedad autoinmune sistémica caracterizada por la presencia de xeroftalmía y xerostomía debido a un infiltrado linfoide de las glándulas exocrinas. El SS puede ocurrir aislado (SS primario) o asociado con diferentes enfermedades autoinmunes (SS secundario). Dentro de las glándulas exocrinas las salivares y lagrimales son las más afectadas, desencadenando consecuencias objetivas severas y manifestaciones subjetivas importantes. Como resultado, las manifestaciones cutáneas han sido minimizadas a pesar de ser relativamente frecuentes. Estas manifestaciones van desde xerosis hasta complicaciones por vasculitis. El objetivo de esta revisión es delinear los posibles hallazgos en la piel de este síndrome.
Palabras clave: síndrome de Sjögren, dermatología, piel.
Summary
Sjögren's syndrome (SS) is a systemic autoimmune disease characterized by xeropthalmia and xerostomia due to lymphocytic infiltrates of exocrine glands. SS may occur alone (primary SS) or in association with several autoimmune diseases (secondary SS). Among exocrine glands the lachrymal and salivary are the foreground, owing the severity of the objective consequences and the importance of the subjective manifestations. As a result, cutaneous manifestations are minimized, albeit relatively common. These manifestations range from drynessness to complications for vasculitis. The objective of this review is to outline the possible skin findings of this syndrome.
Key words: Sjögren's syndrome, dermatology, skin.
Historia
La primera descripción del SS se atribuye a Johann Mikulicz quien en 1892 publicó el caso de un granjero de 42 años que presentó un aumento difuso de las glándula parótidas y lagrimales asociado con un infiltrado de células redondas pequeñas1. El término Síndrome de Mikulicz cayó en desuso porque se refería a múltiples causas de aumento del tamaño glandular3.
En 1930, el oftalmólogo suizo Henrik Sjögren informó hallazgos clínicos y patológicos compatibles con SS en 19 mujeres, 13 con diagnóstico probable de artritis reumatoide (AR); además introdujo el término queratoconjuntivis sicca para distinguir el ojo seco de este síndrome de la xeroftalmía producida por la deficiencia de vitamina A3.
En 1953 Morgan y Castleman4 presentaron un caso de un paciente con SS en una conferencia clínica-patológica y despertaron de nuevo el interés en esta condición. Pero fue hasta 1956 que Bloch et al.5 reconocieron la forma florida del SS.
Epidemiología
El SS primario es la forma de presentación en el 50% de los pacientes, tiene una prevalencia aproximada de 0.5-1% en la población general, siendo la segunda enfermedad inflamatoria más frecuente después de la AR, sin contar con que un porcentaje alto de los casos pasa desapercibido; el SS es nueve veces más frecuente en mujeres que en hombres y tiene dos picos de presentación: el primero en la tercera década de la vida y el segundo luego de la menopausia durante la quinta6,7.
El SS secundario es más frecuente asociado a AR, entidad a la que se sobrepone entre el 20 y el 50% de los casos; también puede encontrarse asociado a lupus eritematoso sistémico (LES), esclerosis sistémica progresiva (ESS), cirrosis biliar primaria (CBP) y dermatomiositis (DM)8.
Criterios diagnósticos
Hasta hace poco existían múltiples propuestas de criterios diagnósticos para el SS primario; la discrepancia entre las mismas conducía a confusión en la práctica clínica y en la investigación. Los criterios de uso actual son los del "European American Consensus Group Modification of the Community Criteria for SS" (Tabla 1).

Para el diagnóstico de SS primario se requieren cuatro de seis criterios, incluyendo la biopsia de glándula salival menor o los anticuerpos Anti SS-A/SS-B. Los criterios de exclusión para el diagnóstico de SS son: antecedente de radioterapia para linfoma de cabeza y cuello, sarcoidosis, infección por virus hepatitis C (VHC), síndrome de inmunodeficiencia adquirida (SIDA), enfermedad injerto vs huésped y medicamentos anticolinérgicos.
El diagnóstico del SS secundario no ha sido unificado todavía por el European American Consensus Group Modification of the Community Criteria for SS.
Anatomía patológica
La toma de la biopsia de glándulas salivares menores se debe hacer bajo ciertas normas técnicas para obtener una muestra adecuada y evitar la lesión de las fibras que inervan el labio inferior. La muestra no debe ser tomada de un sitio de la mucosa oral que se encuentre inflamado ya que podría dar un reporte falsamente positivo. En general la muestra se obtiene del labio inferior a un lado de la línea media, previa infiltración con Xylocaína se procede a realizar una incisión en sentido vertical, luego se disecan las glándulas salivales menores y con una tijera se toman cinco lóbulos glandulares. La herida se sutura con seda o con materiales absorbibles9.
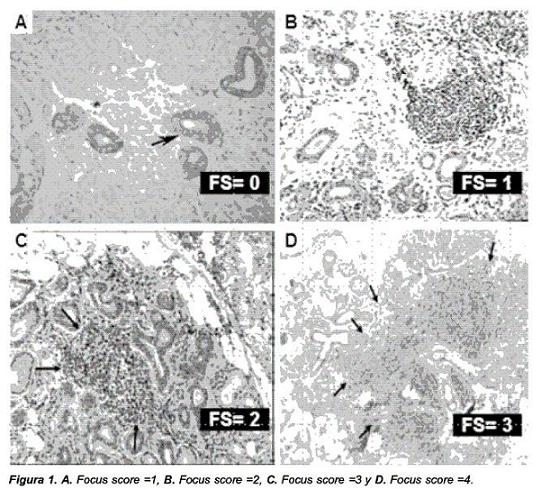
Los aspectos fundamentales al momento de analizar la biopsia incluyen una adecuada cantidad de lóbulos (mínimo cuatro) y la determinación del focus score (FS) (Tabla 2) mediante el conteo de agregados de por lo menos 50 linfocitos e histiocitos por 4 mm² de tejido glandular. Un resultado positivo es determinado por la presencia de sialoadenitis focal con mínimo un agregado de linfocitos10.

La mayoría de patólogos no tienen experiencia en leer este tipo de biopsias; así lo demuestra un estudio11 en el que 50% de biopsias clasificadas como SS fueron reclasificadas cuando las examinó un patólogo experimentado. En la Figura 1, se muestra un ejemplo de biopsia de glándula salival con focus score de cero a tres.
Inmunología y genética
Además de los hallazgos histológicos, manifestaciones como el factor reumatoide, los anticuerpos antinucleares, la hipergamaglobulinemia policlonal y autoanticuerpos como anti SSA/Ro y anti SSB/La son claros indicadores del carácter autoinmune del SS12,13.
Los autoanticuerpos contra el Ro y el La son marcadores de manifestaciones extraglandulares, en especial vasculitis. La presencia de estos anticuerpos se asocia con diferentes HLA-DR14,15.
Aproximadamente el 60% de los pacientes con SS primario expresan anticuerpos Anti SS-A y por lo menos la mitad de estos pacientes expresan Anti SS-B. Es poco común expresar Anti SS-B en ausencia de Anti SS-A16-18.
Patogénesis
A pesar de los múltiples estudios realizados la patogénesis de este síndrome es desconocida9. Se considera que el SS es una enfermedad multifactorial en la que interactúan factores ambientales que desencadenan la inflamación en individuos genéticamente predispuestos. Este proceso comprende diferentes pasos.
- El paso inicial se cree que corresponde a defectos intrínsecos de las células del epitelio glandular y de las células dendríticas que llevan a un proceso de apoptosis anormal lo que genera productos apoptóticos y a la expresión de epítopes crípticos19.
- Luego factores ambientales como procesos virales e infecciones recurrentes estimulan a las células glandulares y dendríticas a activar el sistema de inmunidad innata por medio del HLA; este sistema usa receptores Toll para reconocer patrones moleculares que son compartidos por los microorganismos causantes de estas infecciones y por los productos apoptóticos lo que conlleva a respuesta contra antígenos propios debido a un "error inmune por mimetismo molecular"20.
- Estos cambios conducen a la liberación de citoquinas que regulan de forma positiva la migración de linfocitos y células dendríticas hacia el tejido glandular21.
- La activación de los linfocitos B y T ocurre como consecuencia de la presentación de antígenos mediante el HLA-DR y otras moléculas coestimulatorias, lo que perpetúa la respuesta inmune con linfocitos de memoria, interferón tipo I y autoanticuerpos22.
- Se cree que la destrucción glandular ocurre mediante mecanismos perforina/granzyma-A y Fas/ Fas ligando23. Esta destrucción es parcial, pero la producción local de citoquinas, autoanticuerpos y metaloproteinasas conduce a disfunción del tejido glandular residual24.
Manifestaciones cutáneas
El compromiso cutáneo se observa al menos en la mitad de los pacientes con diagnóstico de SS25; las lesiones pueden ser divididas en vasculíticas y no vasculíticas26-55 (Tabla 3).
La púrpura hipergammaglobulinémica se presenta en 15% de los pacientes con SS8, se manifiesta con lesiones no palpables de coloración ocre o violácea de bordes serpiginosos y que al resolver dejan hiperpigmentación residual; puede acompañarse de neuropatía periférica56 y está frecuentemente asociada a la presencia de títulos altos factor reumatoide (especialmente el subtipo IgM) y crioglobulinas57,58. La electroforesis de proteínas muestra hipergamaglobulinemia policlonal y la biopsia de piel muestra ruptura de los vasos sanguíneos y depósito de complemento.
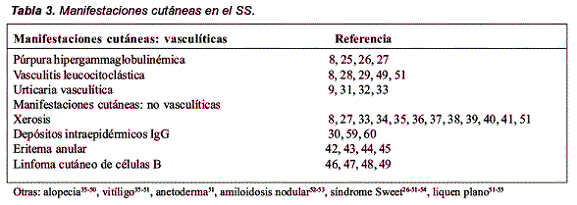
La vasculitis leucocitoclástica (Figura 2) se presenta en 11% de los pacientes con SS8, su principal manifestación es la púrpura palpable, también puede presentarse como petequias o equimosis diseminadas51. La morfología de las lesiones depende del tipo de vaso comprometido. La implicación pronóstica de esta manifestación fue descrita por Ioannidis y col.49 quien reportó
un grupo de 723 pacientes a quienes siguió durante 20 años, en el cual encontró dos subtipos de pacientes: el tipo I cuyos pacientes debutaban con púrpura palpable, hipocomplementemia a expensas de C4 y con el tiempo tenían mayor probabilidad de presentar compromiso del sistema nervioso central o pulmonar; en oposición en el tipo II los pacientes presentaban un curso clínico no complicado.
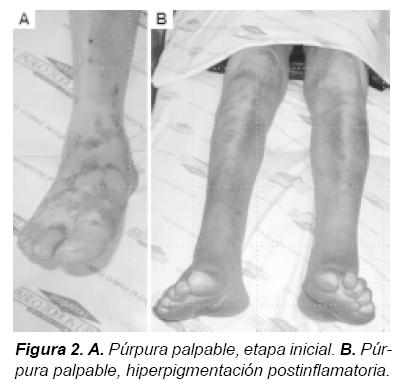
La urticaria vasculítica (Figura 3) es la forma de presentación en 21% de los pacientes con vasculitis9, su principal diferencia con la urticaria convencional radica en el tiempo de duración de los habones (mayor a 24 horas), en la presencia de dolor y ardor más que prurito y de hiperpigmentación postinflamatoria. La histopatología muestra una vasculitis leucocitoclástica clásica con necrosis fibrinoide de la pared del vaso o un patrón de infiltrado linfoide, además edema de la dermis profunda31.
La xerosis es la manifestación más importante del SS; se presenta hasta en 66% de los pacientes8, los síntomas clásicos de esta patología son inespecíficos, pero se asocian a signos objetivos como piel áspera, inelástica y descamativa. Las glándulas sebáceas constituyen la principal fuente humectante de la piel; sin embargo, las glándulas sudoríparas parecen estar implicadas debido al papel homeostático de los lactatos presentes en el sudor51. Katayama y col.37 evaluaron la capacidad de sudoración en 49 sujetos con SS y encontraron una reducción estadísticamente significativa de la tasa de sudoración de estos sujetos frente a controles sanos. Además de la franca disminución en la cantidad del sebo27,34-36 existe la posibilidad de producción de sebo anormal33,39-41; esto explicaría la presencia de pelo seco y deslustrado y de descamación y prurito del conducto auditivo externo (por la disminución de cerumen) en estos pacientes.
Otro hallazgo interesante es la presencia de depósitos intercelulares de IgG en la epidermis en 66% de los pacientes con SS primario y solo en 13% de los pacientes con SS secundario. Dos hipótesis han sido propuestas para explicar este fenómeno: la primera sugiere que la presencia de IgG intercelular sea secundaria a la presencia de complejos inmunes en esta misma localización, pero esto es improbable dada la ausencia de signos histopatológicos de inflamación a este nivel; la segunda hipótesis sugiere que la IgG se encuentra en esta localización unida a receptores de la células de Langerhans30,59. Velthius y col.60 resaltaron la asociación entre los depósitos de IgG y la presencia de Anti SS-A/SS-B circulantes.
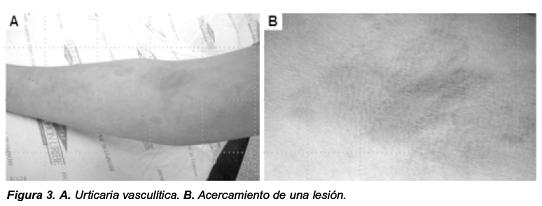
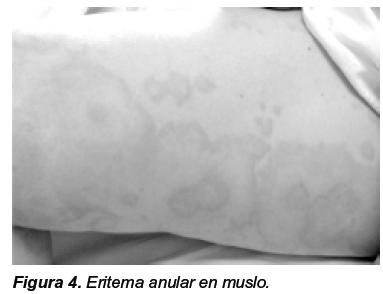
Entre los pacientes asiáticos con SS, el eritema anular (Figura 4) ha sido informado en una proporción significativa43,44; se presenta como una placa eritematoedematosa de borde elevado y centro pálido en la cara; los hallazgos histopatológicos incluyen edema marcado de la dermis superior e infiltrado linfocítico perivascular y entre los haces de colágeno42. A diferencia de las lesiones del lupus cutáneo subagudo, en estas lesiones no se observa depósito de IgG a lo largo de la membrana basal.
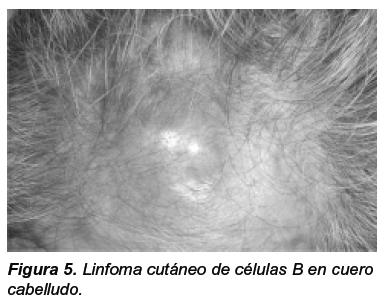
El linfoma cutáneo de células B (Figura 5) es la complicación más temida de los pacientes con SS primario, la incidencia exacta de esta patología se desconoce debido a que la mayoría de estudios existentes son cohortes de pequeño tamaño. El riesgo de desarrollar linfomas no Hogkin en pacientes con SS primario o secundario fue estimado por Kassan y col.46 quienes observaron un riesgo 44 veces mayor en estos pacientes, comparados con población normal. Se debe sospechar un linfoma de células B en pacientes con adenomegalias, infiltrados pulmonares nodulares, crecimiento parotídeo persistente y asimétrico, pico monoclonal u oligoclonal en la electroforesis de proteínas y negativización del factor reumatoide. Resultados similares han sido informados por otros autores47-49.
Otras manifestaciones no vasculíticas informadas han sido: alopecia35,50, vitíligo35,51, anetoderma51, amiloidosis nodular52,53, síndrome Sweet26,51,54, líquen plano51,55.
Manifestaciones oculares
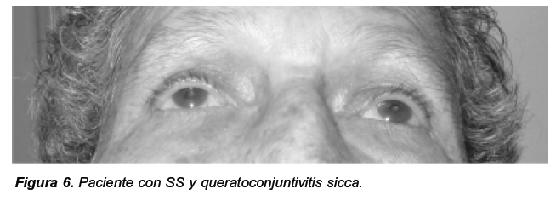
El principal hallazgo oftalmológico en pacientes con SS es la queratoconjuntivitis sicca (Figura 6) secundaria a la destrucción de las glándulas lagrimales. A pesar que el ojo seco es una manifestación prominente, muchos de los pacientes no están al tanto de los síntomas con los que se presenta. Así mismo el médico al evaluar el paciente debe determinar signos objetivos usando métodos para verificar la integridad de la superficie corneal y la producción de lágrimas (Tabla 4).
Las tintas vitales como el Rosa de Bengala, la fluoresceína y el verde de lissamina son útiles para detectar erosiones epiteliales en la córnea y células mucosas desvitalizadas en la superficie conjuntival.
En el test de Schirmer, se coloca una tirilla de papel de filtro en el saco conjuntival inferior de ambos ojos del paciente, se pide al paciente que mantenga los ojos cerrados durante 5 minutos y posteriormente se mide la migración de las lágrimas sobre el papel: un paciente joven y sano humedece al papel unos 15 mm mientras que un paciente con SS humedece el papel menos de 5 mm. La sensibilidad y la reproducibilidad del test de Schirmer son bastante bajas. Todo paciente con SS requiere una evaluación oftalmológica periódica61.
En el diagnóstico diferencial de las queratoconjuntivitis sicca hay que tener en cuenta algunas entidades como las blefaritis, queratitis herpética, conjuntivitis, blefaroespasmo, sarcoidosis, infecciones por VIH y virus de la hepatitis C, hipotiroidismo, estados hipoestrogénicos, hipotiroidismo y uveítis anterior. También es importante que los síntomas de ojo seco se exacerban con medicamentos anticolinérgicos, la ansiedad y la depresión62.
Manifestaciones orales
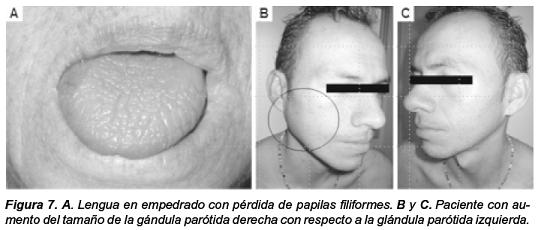
En contraste con la queratoconjuntivitis sicca los pacientes refieren de forma directa los síntomas asociados a xerostomía y el médico puede identificar con la inspección general algunos de los signos objetivos (Tabla 5 y Figura 7).
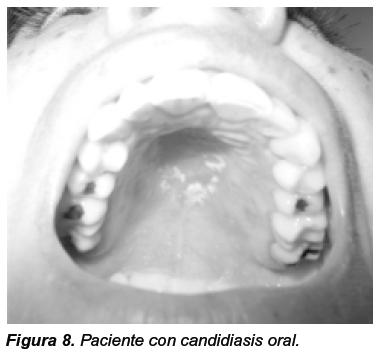
La saliva cumple papel en la deglución mecánica de los alimentos y en la protección antimicrobiana; es por esto que los pacientes con SS tienen un mayor riesgo de enfermedad periodontal e infecciones mucosas como la candidiasis (Figura 8)9.
Existen diversos métodos para la evaluación de los pacientes con compromiso oral: la sialometría cuantifica el flujo de saliva durante 15 minutos63; la sialografía parotidea evalúa la distorsión de los ductos salivales y la gamagrafía salival puede mostrar disminución en la captación del trazador65. Otras ayudas diagnósticas importantes en el diagnóstico diferencial del SS son la tomografía computarizada de alta resolución, la resonancia magnética con sustracción de tejido adiposo y la ecografía parotídea en manos experimentadas64,66. La biopsia de parótida se descartó por el alto riesgo de fístulas sialocutáneas. En caso de sospecha de linfoma de parótida se debe hacer resección biopsia de la glándula.
Un factor adicional en estos pacientes es la presencia de reflujo gastroesofágico (RGE) e incluso reflujo traqueal que puede simular infecciones respiratorias. Por lo tanto se recomienda medidas rigurosas para prevenir y tratar el RGE en estos pacientes67.
Manifestaciones sistémicas
La enfermedad extraglandular (Tabla 6) se subdivide en no visceral (sistema músculo-esquelético) y en visceral (pulmón, corazón, tracto gastrointestinal, riñón, sistema nervioso, endocrino y hematológico).
La presentación de artralgias/artritis en los pacientes con SS es similar a la de los pacientes con diagnóstico de LES70,71. Las mialgias y otros síntomas de debilidad muscular pueden presentarse en estos pacientes de forma aislada o en asociación con polimiositis, polimialgia reumática, miositis por cuerpos de inclusión, miopatía por corticoesteroides, procesos paranoplásicos o fibromialgia72,73.
La neumonitis intersticial y la xerotráquea constituyen las manifestaciones pulmonares más frecuentes del SS74. En la clasificación de la neumonitis intersticial se reconocen varios subtipos: neumonitis intersticial linfocítica, bronquiolitis obliterans, neumonía organizada y neumonitis no específica. Es importante descartar otras causas de infiltrados intersticiales como: toxicidad o hipersensibilidad por metotrexate, infliximab o rituximab e infecciones oportunistas75-77.
Dentro de las manifestaciones cardiovasculares las más comunes son la pericarditis y la hipertensión pulmonar68; sin embargo, estos pacientes pueden presentar otras alteraciones que sugieren presencia de neuropatía autonómica en respuesta a múltiples estímulos78.
Las manifestaciones renales incluyen la nefritis intersticial, la acidosis tubular renal, la parálisis hipocalémica, los cálculos renales y la osteomalacia79-81. Si se presenta deterioro súbito de la función renal, debe prestarse especial cuidado al uso de antiinflamatorios no esteroideos (AINES) y hierbas chinas82. El desarrollo de glomerulonefritis (GMN) puede sugerir amiloidosis, enfermedad por depósito de complejos inmunes o LES83. Se pueden presentar síntomas vesicales severos que se exacerban por el consumo exagerado de líquidos típico de estos pacientes84.
La disfagia en los pacientes con SS se debe en parte a la xerostomía y en parte a la dismotilidad esofágica. Los pacientes con síntomas de gastritis se deben examinar en busca de Helicobacter pylori ya que este agente ha sido asociado con linfomas MALT en los pacientes con SS85.
Los pacientes con SS tienen una posibilidad 40 veces mayor de presentar linfomas que la población general86. La mayoría de linfomas que se presentan son linfomas de células B de la zona marginal. La presencia de parótidas persistentemente inflamadas, linfadenopatías, hepatoesplenomegalia, infiltrados pulmonares, vasculitis o hipergammaglobulinemia; asociadas a caída del hematocrito, velocidad de sedimentación globular (VSG) elevada o crioglobulinas monoclonales debe despertar sospecha de linfoma en estos pacientes9.
Las manifestaciones neurológicas han sido informadas en 20% de estos pacientes; las neuropatías periféricas son las más frecuentes, seguidas por neuropatías craneales y enfermedades desmielinizantes del sistema nervioso central87. También han sido descritos cuadros psiquiátricos que preceden el diagnóstico de la enfermedad autoinmune88, y cambios en la función cognitiva con mala memoria y falta de concentración89.
Diagnóstico diferencial
Es crucial diferenciar el SS de otras enfermedades autoinmunes. El área más común de confusión es con el LES. La sobreposición más frecuente se presenta en los pacientes con LES sin GMN pero con artritis y erupciones cutáneas; estos individuos frecuentemente expresan HLA-DR3 y anticuerpos Anti SS-A.9; se debe sospechar LES de base en pacientes con síndrome seco y artropatía tipo Jaccoud, erupciones características y proteinuria importante. Es particularmente difícil el diagnóstico diferencial entre LES y síndrome de Sjögren en ancianos ya que la primera cursa con xerostomía y xeroftalmía en este grupo etario, además de menor frecuencia de nefropatía y mayor frecuencia de enfermedad pulmonar intersticial; en esta situación es importante el análisis completo de autoanticuerpos.
La sobreposición clínica con esclerodermia sistémica y la asociación con AR es considerable; sin embargo, existen diferencias en los patrones de anticuerpos, la presentación clínica, los HLA asociados y las biopsias de tejidos que permiten diferenciarlos; en estas dos entidades la histología predominante es la atrofia glandular9.
Existen otras enfermedades sistémicas que pueden imitar el SS al causar edema glandular y sequedad; estas deben ser descartadas mediante los paraclínicos necesarios (Tabla 7).
Tratamiento
Terapia cutánea
El manejo de la xerosis es similar al instaurado en otras condiciones:
- Aplicar humectante libre de fragancia mínimo dos veces el día; debe ser aplicado después del baño sobre la piel húmeda para evitar la evaporación de agua de la piel.
- Deben evitarse los baños largos con agua caliente y los limpiadores con fragancias fuertes.
- Si hay prurito se deben aplicar tópicos con pramoxina, lidocaína o mentol. Los antihistamínicos orales deben ser usados con precaución debido a su efecto anticolinérgico.
- Se recomienda el uso diario de protector solar (filtros físicos) en las zonas que no cubre la ropa; sin embargo, la protección solar más efectiva radica en el uso de prendas con UPF (factor de protección ultravioleta) y en evitar la exposición solar directa entre las 10 AM y las 2 PM.
Con respecto al manejo de las manifestaciones vasculíticas cabe anotar:
- El tratamiento de la púrpura hipergammaglobulinémica se realiza con Hidroxicloroquina (5-7 mg/kg) ya que ayuda a disminuir la hiperglobulinemia y el desarrollo subsecuente de neuropatía. El uso concomitante de altas dosis de corticosteroides y otros inmunosupresores dependerá de la gravedad el caso25.
- El tratamiento de los pacientes con vasculitis leucocitoclástica debe ser más agresivo requiriendo dosis altas de corticoides o incluso ciclofosfamida29.
Terapia ocular
Lubricantes
- Lágrimas artificiales libres de preservativos, mínimo tres veces al día y preferiblemente cada 30 a 60 minutos.
- Ung&uulm;entos lubricantes y metilcelulosa en la noche.
- Escudos laterales para el marco de las gafas para reducir la evaporación de las lágrimas; las gafas de natación son bastante eficaces para disminuir la evaporación, pero las consideraciones sociales limitan su uso.
- Uso de humidificadores en la habitación del paciente.
Oclusión del punto lagrimal inferior
- Es el tratamiento de elección debido a que 90% de las lágrimas drenan por este punto; existen múltiples tapones; los intracanaliculares no protuyen a la superficie corneal, razón por la cual son preferidos sobre los otros90.
Gotas oftálmicas
- Para casos de xeroftalmía grave se recomienda la Ciclosporina emulsión 0,05% con múltiples estudios que soportan su uso2,4,91; los síntomas se resuelven hacia el tercer mes de uso y su efecto adverso más frecuente es el ardor local; no se han descrito complicaciones sistémicas de la Ciclosporina en esta forma de administración.
- Tacrólimus en suspensión al 0,02%, puede ser benéfico en pacientes con respuesta inadecuada a la cilosporina tópica92.
Terapia sistémica
- La complicación más preocupante del compromiso de la mucosa oral es la pérdida dental, por eso es de extrema importancia el uso de seda dental luego de cada comida al igual que asistir al odontólogo para tratamientos de higiene dental y flúor mínimo cada tres meses93.
- Los sustitutos de saliva son una opción para estos pacientes; sin embargo, suelen ser mal tolerados94.
- En los pacientes con síntomas persistentes está indicado el tratamiento con secretagogos que estimulan los receptores muscarínicos; hay dos agentes disponibles: la pilocarpina y la cevimelina. Ambos han demostrado en estudios clínicos controlados94-96 incrementos significativos en la tasa de salivación (Tabla 8).
- Las manifestaciones articulares pueden manejarse con antiinflamatorios no esteroides, dosis baja de prednisolona y antimaláricos; en casos resistentes a este manejo se puede utilizar el metotrexate por períodos cortos para evitar el riesgo de neoplasia que confiere este medicamento en una entidad que de por sí cursa con un mayor riesgo de linfomas; ninguna de estas conductas tiene respaldo de un ensayo clínico controlado.
- Para casos graves de síndrome de Sjögren, con manifestaciones vasculíticas, parotidomegalia persistente, pseudolinfomas o linfomas se describe el uso de Rituximab97.
Referencias
Mikulicz JH. Uber eine eigenartige symmetrische Erkrankung der Tranen-und Mundspeicheldrusen. In: Billroth GT, editor. Beitr Chir Fortschr; 1892. p. 610-630 [Stuttgart]. [ Links ]
2. Daniels TE, Fox PC. Salivary and oral components of Sjogren's syndrome. Rheum Dis Clin North Am 1992; 18: 571-589. [ Links ]
3. Rehman HU. Sjögren's syndrome. Yonsei Med J 2003; 44(6): 947-954. [ Links ]
4. Morgan W, Castleman B. A clinicopathologic study of Mikulicz's disease. Am J Pathol 1953; 29: 471-503. [ Links ]
5. Bloch KJ, Buchanan WW, Wohl MJ, Bunim JJ. Sjögren syndrome: a clinical, pathological and serological study of 62 cases. Medicine (Baltimore) 1956; 44: 187-231. [ Links ]
6. Bowman SJ, Ibrahim GH, Holmes G, et al. Estimating the prevalence among Caucasian women of primary Sjogren's syndrome in two general practices in Birmingham, UK. Scand J Rheumatol 2004; 33: 39-43. [ Links ]
7. Pillemer SR, Matteson EL, Jacobsson LT, et al. Incidence of physician-diagnosed primary Sjogren syndrome in residents of Olmsted County, Minnesota. Mayo Clin Proc 2001; 76: 593-599. [ Links ]
8. Carsons S. A Review and Update of Sjögren's Syndrome: Manifestations, Diagnosis, and Treatment. Am J Manag Care 2001; 7: S433-S443. [ Links ]
9. Fox RI, Liu AY. Sjögren's syndrome in dermatology. Clin Dermatol 2006; 24(5): 393-413. [ Links ]
10. Dankof A, Morawietz L, Feist E. Labial salivary gland biopsy in Sjögren's syndrome. Pathologe 2006; 27(6): 416-421. [ Links ]
11. Vivino FB, Gala I, Hermann GA. Change in final diagnosis on second evaluation of labial minor salivary gland biopsies. J Rheumatol 2002; 29: 938-944. [ Links ]
12. Chan EKL, Sullivan KF, Fox RI, et al. Sjogren's syndrome nuclear antigen B (La): cDNA cloning, structural domains, and autoepitopes. J Autoimmun 1989; 2: 321-327. [ Links ]
13. Ben-Chetrit E, Fox RI, Tan EM. Dissociation of immune responses to the SS-A (Ro) 52-kd and 60-kd polypeptides in systemic lupus erythematosus and Sjögren syndrome. Arthritis Rheum 1990; 33: 349-355. [ Links ]
14. Fei HM, Kang H-I, Scharf S, et al. Specific HLA-DQA and HLA-DRB1 alleles confer susceptibility to Sjogren's syndrome and autoantibody SS-B production. J Clin Lab Anal 1991; 5: 382-391. [ Links ]
15. Lightfoot R. Cost effective use of laboratory tests in rheumatology. Bull Rheum Dis 1997; 46: 1-3. [ Links ]
16. Harley JB, Alexander EL, Bias WB, et al. Anti-Ro (SS-A) and Anti-La (SS-B) in patients with Sjogren's syndrome. Arthritis Rheum 1986; 29: 196-206. [ Links ]
17. Hamilton RG, Harley JB, Bias WB, et al. Two Ro (SS-A) autoantibody responses in systemic lupus erythematous. Arthritis Rheum 1988; 31: 446-505. [ Links ]
18. Sestak AL, Harley JB, Yoshida S, et al. Lupus/Sjogren's autoantibody specificities in sera with paraproteins. J Clin Invest 1987; 80: 138-144. [ Links ]
19. Tapinos NI, Polihronis M, Tzioufas AG, et al. Sjogren's syndrome. Autoimmune epithelitis. Adv Exp Med Biol 1999; 455: 127-134. [ Links ]
20. Takeda K, Kaisho T, Akira S. Toll-like receptors. Annu Rev Immunol 2003; 21: 335-376. [ Links ]
21. Jonsson R, Gordon TP, Konttinen YT. Recent advances in understanding molecular mechanisms in the pathogenesis and antibody profile of Sjogren's syndrome. Curr Rheumatol Rep 2003; 5: 311-316. [ Links ]
22. Sawalha AH, Potts R, Schmid WR, et al. The genetics of primary Sjogren's syndrome. Curr Rheumatol Rep 2003; 5: 324-332. [ Links ]
23. Bolstad AI, Eiken HG, Rosenlund B, et al. Increased salivary gland tissue expression of Fas, Fas ligand, cytotoxic T lymphocyte–associated antigen 4, and programmed cell death 1 in primary Sjogren's syndrome. Arthritis Rheum 2003; 48: 174-185. [ Links ]
24. Konttinen YT, Kasna-Ronkainen L. Sjogren's syndrome: viewpoint on pathogenesis. One of the reasons I was never asked to write a textbook chapter on it. Scand J Rheumatol Suppl 2002; 15-22. [ Links ]
25. Kyle R, Gleich G, Bayrid E, et al. Benign hyperglobulinemic purpura of Waldenstrom. Medicine (Baltimore) 1971; 50: 113-123. [ Links ]
26. Bernacchi E, Amato L, Parodi A, et al. Sjogren's syndrome: a retrospective review of the cutaneous features of 93 patients by the Italian Group of Immunodermatology. Clin Exp Rheumatol 2004; 22: 55-62. [ Links ]
27. Bloch KJ, Buchanan WW, Wohlmj, Bunim JJ. Sjögren's syndrome: a clinical, pathological and serological study of sixty two cases. Medicine (Baltimore) 1965; 44: 187-231. [ Links ]
28. Ramos-Casals M, Cervera R, Yague J, et al. Cryoglobulinemia in primary Sjogren's syndrome: prevalence and clinical characteristics in a series of 115 patients. Semin Arthritis Rheum 1998; 28: 200-205. [ Links ]
29. Alexander E, Provost TT. Sjfgren's syndrome. Association of cutaneous vasculitis with central nervous system disease. Arch Dermatol 1987; 123: 801-810. [ Links ]
30. Oxholm P, Oxholm A, Manthorpe R. Epidermal IgG deposits in patients with chronic inflammatory connective tissue diseases: diagnostic value and correlation to clinical and immunological parameters in patients with primary Sjögren's syndrome. Clin Exp Rheumatol 1987; 5: 5-9. [ Links ]
31. O'Donnell B, Black AK. Urticarial vasculitis. Int Angiol 1995; 14: 166-174. [ Links ] 32. Alexander E, Provost T. Sjögren's syndrome. Arch Dermatol 1987; 123: 801-810. [ Links ]
33. Provost TT, Watson R. Cutaneous manifestations of Sjögren's syndrome. Rheum Dis Clin North Am 1992; 18: 609-616. [ Links ]
34. Markusse HM, Oudkerk M, Vroom TM, et al. Primary Sjögren's syndrome: clinical spectrum and mode of presentation based on an analysis of 50 patients selected from a department of rheumatology. Neth J Med 1992; 40: 125-134. [ Links ]
35. Fye K, Talal N. Skin manifestations of Sjögren's syndrome. In: Dermatology in General Medicine. Fitzpatrick TB, Eisen AZ and Wolff K (Eds.), 2nd ed., Maidenhead, McGraw Hill, 1979: 1883-1887. [ Links ]
36. Whaley K, Williamson J, Chisholm DM, et al. Sjogren's syndrome. Sicca components. Q J Med 1973; 166: 279-304. [ Links ]
37. Katayama I, Yokozeki H, Nishioka K. Impaired sweating as an exocrine manifestation in Sjögren's syndrome. Br J Dermatol 1995; 133: 716-720. [ Links ]
38. Mitchell J, Greenspan J, Daniels T, et al. Anhidrosis in Sjögren's syndrome. J Am Acad Dermatol 1987; 16: 233-235. [ Links ]
39. Feuerman EJ. Sjögren's syndrome presenting as recalcitrant generalized pruritus. Some remarks about its relation to collagen diseases and the connection of rheumatoid arthritis with the sicca syndrome. Dermatologica 1968; 137: 74-86. [ Links ]
40. Thiers H, Moulin G, Cuffia C, et al. Syndrome de Gougerot- Sjögren associé à une dermatose de type parapsoriasis lichenoide. Bull Soc Fr Dermatol Syphiligr 1966; 73: 326-327. [ Links ]
41. Henkinri T, Larson AL, Mattern CF, et al. Abnormalities of taste and smell in Sjögren's syndrome. Ann Intern Med 1972; 76: 375-383. [ Links ]
42. Teramoto N, Katayama I, Arai H, et al. Annular erythema: a possible association with primary Sjögren's syndrome. J Am Acad Dermatol 1989; 20: 596-601. [ Links ]
43. Ruzicka T, Faes J, Bergner T, et al. Annular erythema associated with Sjogren's syndrome: a variant of systemic lupus erythematosus. J Am Acad Dermatol 1991; 25: 557-560. [ Links ]
44. Katayama I, Yamamoto T, Otoyama K, et al. Clinical and immunologica analysis of annular erythema associated with Sjögren syndrome. Dermatology 1994; 189(Suppl 1): 14-17. [ Links ]
45. Miyagawa S, Iida T, Fukumoto T, et al. Anti-Ro/SSAassociated annular erythema in childhood. Br J Dermatol 1995; 133: 779-782. [ Links ]
46. Kassan SS, Thomas TL, Moutsopoulos HM, et al. Increased risk of lymphoma in sicca syndrome. Ann Intern Med 1978; 89: 888-893. [ Links ]
47. Selva O'Callaghan A, Perez Lopez J, Solans Laque R, et al. Primary cutaneous large B-cell lymphoma of the legs in a patient with primary Sjögren's syndrome. Clin Exp Rheumatol 2003; 21: 672-672. [ Links ]
48. Royerb, Cazals Hatem D, Sibilia J, et al. Lymphomas in patients with Sjögren's syndrome are marginal zone B-cell neoplasms, arise in diverse extranodal and nodal sites, and are not associated with viruses. Blood 1997; 90: 766-775. [ Links ]
49. Ioannidis JP, Vassilio UVA, Moutsopoulos HM. Long-term risk of mortality and lymphoproliferative disease and predictive classification of primary Sjögren's syndrome. Arthritis Rheum 2002; 46: 741-747. [ Links ]
50. Humbert P, Dupond JL, Vuitton D, et al. Dermatological autoimmune diseases and the multiple autoimmune syndromes. Acta Derm Venereol 1989; 148: 2-8. [ Links ]
51. Roguedas AM, Misery L, Sassolas B, et al. Cutaneous manifestations of primary Sjögren's syndrome are underestimated. Clin Exp Rheumatol. 2004; 22(5): 632-636. [ Links ]
52. Pablos JL, Cogolludo V, Pinedo F, et al. Subcutneous nodular amyloidosis in Sjfgren's syndrome. Scand J Rheumatol 1993; 22: 250-251. [ Links ]
53. Yoneyama K, Tochigi N, Oikawa A, et al. Primary localized cutaneous nodular amyloidosis in a patient with Sjogren's syndrome: a review of the literature. J Dermatol 2005; 32: 120-123. [ Links ]
54. Foster EN, Nguyen KK, Sheikh RA, et al. Crohn's disease associated with Sweet's syndrome and Sjogren's syndrome treated with infliximab. Clin Dev Immunol 2005; 12: 145-149. [ Links ]
55. Collete, Dalac S, Brichon P, Lorc Erieb, et al. Association lichen plan et syndrome de Gougerot-Sjögren primitif. Ann Dermatol Venereol 1989; 116: 483-486. [ Links ]
56. Gemignani F, Marbini A, Pavesi G, et al. Peripheral neuropathy associated with primary Sjogren's syndrome. J Neurol Neurosurg Psychiatry 1994; 57: 983-986. [ Links ]
57. Fox RI, Carson DA, Chen P, et al. Characterization of a cross reactive idiotype in Sjfgren's syndrome. Scand J Rheumatol 1986; 561: 83-88. [ Links ]
58. Fox RI, Chen PP, Carson DA, et al. Expression of a cross reactive idiotype on rheumatoid factor in patients with Sjfgren's syndrome. J Immunol 1986; 136: 477-483. [ Links ]
59. Oxholm A, Manthorpe R, Oxholm P. Immunoglobulin deposits in the epidermis of patients with primary Sjögren's syndrome. Rheumatol Int 1984; 4: 9-12. [ Links ]
60. Velthuis PJ, Nieboer C, Kater L, et al. A prospective immunofluorescence study of immune deposits in the skin of primary Sjögren's syndrome. Acta Derm Venerol 1989; 69: 487-491. [ Links ]
61. Fox RI. Sjögren's syndrome. Lancet 2005; 366(9482): 321-331. [ Links ]
62. Pflugfelder SC. Differential diagnosis of dry eye conditions. Adv Dent Res 1996; 10: 9-12. [ Links ]
63. Bergdahl J, Bergdahl M. Environmental illness: evaluation of salivary flow, symptoms, diseases, medications, and psychological factors. Acta Odontol Scand 2001; 59: 104-110. [ Links ]
64. Yousem DM, Kraut MA, Chalian AA. Major salivary gland imaging. Radiology 2000; 216: 19-29. [ Links ]
65. Tonami H, Higashi K, Matoba M, et al. Comparative study between MR sialography and salivary gland scintigraphy in the diagnosis of Sjogren syndrome. J Comput AssistTomogr 2001; 25: 262-268. [ Links ]
66. Salaffi F, Argalia G, Carotti M, et al. Salivary gland ultrasonography in the evaluation of primary Sjogren's syndrome. Comparison with minor salivary gland biopsy. J Rheumatol 2000; 27: 1229-1236. [ Links ]
67. Belafsky PC, Postma GN. The laryngeal and esophageal manifestations of Sjogren's syndrome. Curr Rheumatol Rep 2003; 5: 297-303. [ Links ]
68. Gyongyosi M, Pokorny G, Jambrik Z, et al. Cardiac manifestations in primary Sjogren' syndrome. Ann Rheum Dis 1996; 55: 450-454. [ Links ]
69. D'Arbonneau F, Ansart S, Le Berre R, et al. Thyroid dysfunction in primary Sjogren's syndrome: a long-term follow-up study. Arthritis Rheum 2003; 49: 804-809. [ Links ]
70. Manoussakis MN, Georgopoulou C, Zintzaras E, et al. Sjögren's syndrome associated with systemic lupus erythematosus: clinical and laboratory profiles and comparison with primary Sjogren's syndrome. Arthritis Rheum 2004; 50: 882-891. [ Links ]
71. Pease CT, Shattles W, Barrett NK, et al. The arthropathy of Sjogren's syndrome. Br J Rheumatol 1993; 32: 609-613. [ Links ]
72. Lindvall B, Bengtsson A, Ernerudh J, Eriksson P. Subclinical myositis is common in primary Sjogren's syndrome and is not related to muscle pain. J Rheumatol 2002; 29: 717-725. [ Links ]
73. Bonafede RP, Downey DC, Bennett RM. An association of fibromyalgia with primary Sjogren's syndrome: a prospective study of 72 patients. J Rheumatol 1995; 22: 133-136. [ Links ]
74. Quismorio Jr FP. Pulmonary involvement in primary Sjogren's syndrome. Curr Opin Pulm Med 1996; 2: 424- 428. [ Links ]
75. Kim EA, Lee KS, Johkoh T, et al. Interstitial lung diseases associated with collagen vascular diseases: radiologic and histopathologic findings. Radiographics 2002; 22(Spec No): S151-S165. [ Links ]
76. Chatterjee S. Severe interstitial pneumonitis associated with infliximab therapy. Scand J Rheumatol 2004; 33: 276-277. [ Links ]
77. Swords R, Power D, Fay M, et al. Interstitial pneumonitis following rituximab therapy for immune thrombocytopenic purpura (ITP). Am J Hematol 2004; 77: 103-104. [ Links ]
78. Andonopoulos AP, Christodoulou J, Ballas C, et al. Autonomic cardiovascular neuropathy in Sjogren's syndrome. A controlled study. J Rheumatol 1998; 25: 238-258. [ Links ]
79. Gamron S, Barberis G, Onetti CM, et al. Mesangial nephropathy in Sjogren's syndrome. Scand J Rheumatol 2000; 29: 65-67. [ Links ]
80. Siamopoulos KC, Elisaf M, Moutsopoulos HM. Hypokalaemic paralysis as the presenting manifestation of primary Sjögren's syndrome. Nephrol Dial Transplant 1994; 9: 1176-1178. [ Links ]
81. Fulop M, Mackay M. Renal tubular acidosis, Sjogren syndrome, and bone disease. Arch Intern Med 2004; 164: 905-909. [ Links ]
82. Nishimagi E, Kawaguchi Y, Terai C, et al. Progressive interstitial renal fibrosis due to Chinese herbs in a patient with calcinosis Raynaud esophageal sclerodactyly telangiectasia (CREST) syndrome. Intern Med 2001; 40: 1059-1063. [ Links ]
83. Dabadghao S, Aggarwal A, Arora P, et al. Glomerulonephritis leading to end stage renal disease in a patient with primary Sjögren syndrome. Clin Exp Rheumatol 1995; 13: 509-511. [ Links ]
84. Shibata S, Ubara Y, Sawa N, et al. Severe interstitial cystitis associated with Sjogren's syndrome. Intern Med 2004; 43: 248-252. [ Links ]
85. Raderer M, Osterreicher C, Machold K, et al. Impaired response of gastric MALT-lymphoma to Helicobacter pylori eradication in patients with autoimmune disease. Ann Oncol 2001; 12: 937-939. [ Links ]
86. Kassan SS, Thomas TL, Moutsopoulos HM, et al. Increased risk of lymphoma in sicca syndrome. Ann Intern Med 1978; 89: 888-892. [ Links ]
87. Delalande S, de Seze J, Fauchais AL, et al. Neurologic manifestations in primary Sjogren syndrome: a study of 82 patients. Medicine (Baltimore) 2004; 83: 280-291. [ Links ]
88. Van Dam AP, Wekking EM, Callewaert JA, et al. Psychiatric symptoms before systemic lupus erythematosus is diagnosed. Rheumatol Int 1994; 14: 57-62. [ Links ]
89. Belin C, Moroni C, Caillat-Vigneron N, et al. Central nervous system involvement in Sjogren's syndrome: evidence from neuropsychological testing and HMPAOSPECT [In Process Citation]. Ann Med Interne (Paris) 1999; 150: 598-604. [ Links ]
90. Hamano T. Lacrimal duct occlusion for the treatment of dry eye. Semin Ophthalmol 2005; 20: 71-74. [ Links ]
91. Tatlipinar S, Akpek EK. Topical ciclosporin in the treatment of ocular surface disorders. Br J Ophthalmol 2005; 89: 1363-1367. [ Links ]
92. Berdoulay A, English RV, Nadelstein B. Effect of topical 0.02% tacrolimus aqueous suspension on tear production in dogs with keratoconjunctivitis sicca. Vet Ophthalmol 2005; 8: 225-232. [ Links ]
93. Papas AS, Joshi A, MacDonald SL, et al. Caries prevalence in xerostomic individuals. J Can Dent Assoc 1993; 59: 171- 174, 177-179. [ Links ]
94. Papas AS, Fernandez MM, Castano RA, et al. Oral pilocarpine for symptomatic relief of dry mouth and dry eyes in patients with Sjogren's syndrome. Adv Exp Med Biol 1998; 438: 973-978. [ Links ]
95. Katelaris CH. Pilocarpine for dry mouth and dry eye in Sjögren's syndrome. Curr Allergy Asthma Rep 2005; 5: 321-321. [ Links ]
96. Petrone D, Condemi JJ, Fife R, et al. A double-blind, randomized, placebo-controlled study of cevimeline in Sjögren's syndrome patients with xerostomia and keratoconjunctivitis sicca. Arthritis Rheum 2002; 46: 748-754. [ Links ]
97. Pijpe J, Van Imhoff GW, Spijkernet FKL, et al. Rituximab treatment in patient with primary Sjogren Syndrome. An open label fase I-II study. Arthritis Rheum 2005; 52: 740-750. [ Links ]