Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Reumatología
Print version ISSN 0121-8123
Rev.Colomb.Reumatol. vol.18 no.4 Bogotá Oct./Dic. 2011
ARTÍCULO DE REVISIÓN
1MD internista, residente de Reumatología, Universidad de Antioquia, Medellín, Colombia.
2MD, DSc, profesora sección de Reumatología, Universidad de Antioquia, Medellín, Colombia.
Correspondencia, Dra. Gloria María Vásquez: glomavas@gmail.com
Los autores declaran no presentar ningún conflicto de interés al momento de la redacción del manuscrito.
Recibido: 11 de febrero de 2011 Aceptado: 2 de octubre de 2011
Resumen
La esclerodermia es una enfermedad caracterizada por la acumulación excesiva de tejido fibroso que lleva a alteración en la estructura y función de la piel y de órganos internos. La principal citoquina involucrada en este proceso es el factor transformante de crecimiento beta y sus funciones se realizan principalmente a través de la señalización intracelular mediada por las proteínas Smad. Se han desarrollado estrategias para bloquear los efectos del factor transformante de crecimiento beta y la identificación de la vía de transmisión de señales proporciona nuevas herramientas para la investigación de futuras terapias, pero son necesarios más estudios en modelos animales y en humanos que logren reproducir en forma satisfactoria y segura los resultados.
El propósito de este artículo es analizar la función del factor transformante de crecimiento beta en la fisiopatología de la esclerodermia profundizando en la vía de señalización mediada por Smad; además, revisar los estudios que involucran estas proteínas como blanco terapéutico de moléculas y medicamentos como posibles tratamientos para la esclerodermia.
Palabras clave: esclerodermia sistémica, TGF-beta, proteínas Smad, imatinib.
Summary
Scleroderma is a disease characterized by excessive accumulation of fibrous tissue that leads to alteration in the structure and function of the skin and internal organs. The main cytokine involved in this process is the transforming growth factor beta and their functions are carried out mainly through intracellular signaling mediated by Smad proteins. Several strategies have been developed to block the effects of the transforming growth factor beta and understanding the signaling pathway provides new tools for the investigation of future therapies, but more studies are needed in animal models and humans to get the replication of the results in a satisfactory and safe manner.
The purpose of this paper is to analyze the role of the transforming growth factor beta in the pathophysiology of scleroderma emphasizing the signaling pathway mediated by Smad; it is also to review some studies involving these proteins as therapeutic targets of molecules and drugs that could become potential treatments for scleroderma.
Key words: systemic scleroderma, TGF-beta, Smad proteins, imatinib.
Introducción
La esclerodermia se identifica por la presencia de fibrosis tisular que causa alteración de la arquitectura de la piel, de los vasos sanguíneos y de órganos como los pulmones lo cual finalmente lleva a su disfunción y falla. De acuerdo con la afectación o no de órganos internos (pulmones, corazón, tracto gastrointestinal, riñones), la esclerodermia se clasifica en localizada o sistémica (SSc) y según la extensión del compromiso cutáneo se divide en SSc limitada (lcSSc) o difusa (dcSSc)1.
La particularidad de esta entidad es la producción no controlada de colágeno y de otras proteínas de la matriz extracelular que llevan a la acumulación excesiva de tejido fibroso y a la presencia de un número abundante de fibroblastos que exhiben un fenotipo activado distintivo caracterizado por el aumento en la expresión de los genes que codifican para las proteínas colágeno tipo I, colágeno tipo III, fibronectina, la expresión de actina de músculo liso alfa (a-SMA). Además está reducida la expresión de los genes que codifican para las enzimas que degradan la matriz extracelular. Las células que expresan este fenotipo se denominan miofibroblastos2,3. Hallazgos recientes discrepan con el concepto de que este proceso de fibrosis patológica es irreversible. Este cambio de paradigma tiene implicaciones trascendentales principalmente en el diseño y desarrollo de nuevos tratamiento dirigidos directamente a evitar, retardar o reversar la fibrosis4.
Factor transformante de crecimiento beta (TGF-β)
El TGF-β es un factor pleiotrópico sintetizado por muchas células en el organismo. Se considera como la citoquina que orquesta el proceso tanto fisiológico (cicatrización de heridas y reparación tisular) como patológico de fibrogénesis; además de ser un agente inmunosupresor potente ha emergido como un objetivo terapéutico importante en las enfermedades fibróticas5. Se caracteriza por ser quimiotáctico para fibroblastos, estimula su proliferación y su diferenciación en miofibroblastos, los cuales, a su vez, son la mayor fuente de TGF-β durante el proceso fibrótico, activándose de forma autocrina y paracrina induciendo la activación de otros fibroblastos6. El TGF-β también incrementa la síntesis de proteínas de la matriz extracelular mediante el aumento de la producción de colágeno tipo I, III, V y VI, al igual que de proteínas tales como fibronectina y alfa-SMA (marcador molecular de miofibroblastos activados); disminuye además la síntesis de metaloproteinasas que degradan colágeno. Los linfocitos T y fagocitos mononucleares activados sintetizan principalmente TGF-β17.
Familia de las Smad
Las proteínas Smad constituyen una familia de segundos mensajeros, conservada evolutivamente y que participa en la propagación de las señales intracelulares activadas por TGF-β indispensables para muchas de las acciones de esta citoquina, entre ellas, las profibróticas8. El nombre "Smad" se deriva de la contracción de los nombres de las proteínas similares inicialmente identificadas en la Drosophila melanogaster (MAD o Mothers against decantaplegic, donde "decan-tapléjico" se refiere a una proteína de la mosca homóloga a la proteína morfogénica ósea humana, la cual participa en el desarrollo del eje dorso-ventral durante la formación del organismo, y la expresión "mothers against" adicionada como un apunte de humor puesto que las madres usualmente forman organizaciones oponiéndose a varios asuntos) y la proteína del nemátodo Caenorhabditis elegans (SMA o "small body size", que corresponde a genes mutados que alteran el tamaño corporal)9.
En los mamíferos existen ocho Smad agrupadas en tres subfamilias10:
-
Smad reguladas por el receptor (R-Smad):
Smad1, Smad2, Smad3, Smad5 y Smad8. -
Smad mediadora común (Co-Smad):
Smad4. -
Smad inhibitorias (I-Smad): Smad6 y Smad7.
Smad1, Smad5 y Smad8 transmiten señales propias del receptor de la proteína morfogénica ósea (BMP) mientras que Smad6 es inhibitoria para BMP; Smad2 y Smad3 son específicas en la transmisión de señales desde el receptor TGF-β junto con el mediador común Smad4; Smad7 interactúa con el receptor TGF-β y bloquea la transducción de la señal dependiente de Smad11.
Las R-Smad y Smad4 contienen MH1 y MH2 (dominios de homología MAD) separados por una región de unión rica en prolina, de tamaño variable y la cual es diferente en cada una de ellas. Solo el dominio MH2 está conservado en las tres subfamilias de Smad. El dominio MH1 les confiere actividad de localización nuclear, unión al DNA y unión a factores de transcripción. El dominio MH2 es el principal efector, responsable de la unión al receptor, activación transcrip-cional y oligomerización entre Smad. El dominio MH1 media la autoinhibición por su interacción con el dominio MH2 previniendo su fosforilación en la ausencia de ligando12. La región de unión rica en prolina facilita la interacción de Smad con el sistema de degradación proteosómico; igualmente contiene un número de sitios de fosforilación que median la señalización cruzada entre la vía de las Smad y otros mecanismos de señalización13. Las R-Smad tienen en su extremo carboxilo terminal un motivo rico en serina (SXS) que es el sitio de fosforilación para su activación. En células no estimuladas por TGF-β, las R-Smad y Smad4 permanecen en el citoplasma14.
1. Señalización a través de Smad (Figura 1)
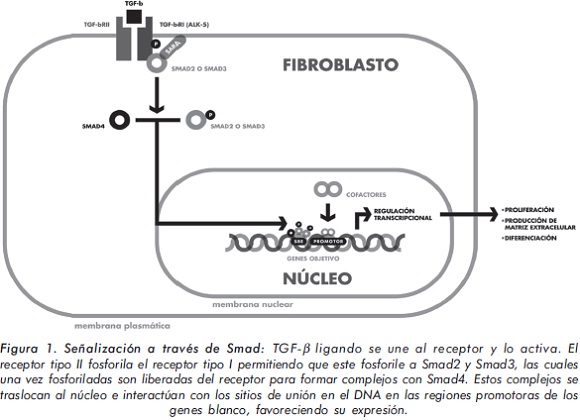
El receptor de TGF-β1 (TbR) está formado por dos proteínas transmembrana diferentes con dominios de serina/treonina cinasa, la cinasa 5 similar al receptor de activina o receptor tipo I (ALK5 o TbRI) y el receptor tipo II (TbRII). El TGF-β ligando se une al receptor y lo activa. Smad 2 y 3 son reclutadas al receptor tipo I activado por medio de una proteína de anclaje de Smad para la activación del receptor (SARA)15,16. El receptor tipo II, que es constitutivamente activo, fosforila el receptor tipo I en el dominio glicina/serina, permitiendo que el receptor tipo I fosforile a Smad2 y Smad3 en su motivo SXS. Smad2 y Smad3 una vez fosforiladas son liberadas del receptor para formar complejos homodiméricos o heterodiméricos con Smad4, los cuales se traslocan al núcleo e interactúan con los sitios de unión en el DNA (SBE o smad binding element, que contiene cinco pares de bases: 5'-CAGAC-3') en las regiones promotoras de los genes blanco favoreciendo su expresión; con la ayuda de proteínas intracelulares con las que interactúa Smad4, que funcionan como cofactores (como Sp1, factor de transcripción sinérgico requerido para la respuesta del gen del colágeno al TGF-β y el coactivador acetilasa de histona p300)17-19. Esto ocurre, por ejemplo, en el promotor del gen para la síntesis de la cadena alfa 2 del colágeno (Col1α2)20-22.
2. Regulación de la señalización
Smad7, localizado en las balsas lipídicas de las membranas celulares, es reclutado hacia el TbRI por la proteína adaptadora asociada al receptor cinasa de serina/treonina (STRAP) donde previene la incorporación y fosforilación de Smad2 y Smad3; igualmente atrae las ligasas de ubicuitina Smurf1 y Smurf2 (Smad ubiquiti-nation regulatory factors 1 y 2) hacia el TbRI con la subsecuente internalización, ubiquitinación y degradación del receptor por el proteasoma23-26. La síntesis de Smad7 es inducida por TGF-β en muchos tipos celulares a través de señalización mediada por Smad3 y Smad4, sirviendo como retroalimentación negativa27-30.
Además de su interacción con factores de transcripción activadores, Smad4 interactúa con co-represores transcripcionales como TGIF, c-ski y SNON. Estos reguladores negativos interfieren con la unión del dominio MH2 al coactivador transcripcional CBP/p300, reclutando deace-tilasas de histonas y compitiendo con Smad2 y Smad3 por la unión a Smad431. En el núcleo, una fosfatasa puede remover los grupos fosfatos del extremo carboxiloterminal de Smad2 y Smad3 y entonces junto con Smad 4 son regresadas al citoplasma. Este flujo constante dependiente del estado de fosforilación es llevado a cabo a través de receptores para la importación nuclear de proteínas (CRM-1 o "chromosome region maintenance", más conocido como XPO-1 o exportina)32. Se ha postulado igualmente la degradación en el núcleo de Smad2 fosforilada por una proteína llamada Arkadia33.
Señalización independiente de Smad
Aunque la vía de señalización por medio de Smad es el mediador intracelular principal de las señales provenientes del TbR, existen vías alternas independientes de Smad que involucran cinasas de proteínas (PKA y C, cinasa II independiente de calmodulina, MAPK, JNK); TAK1, PI3K, calcineurina (fosfatasa dependiente de calcio), cinasa de tirosina c-Abelson (c-Abl); GTPasas Ras y Rho. Estas vías interactúan unas con otras y también con Smad, creando complejas redes intracelulares de señalización34,35. Sin embargo, los mecanismos que permiten la interacción de las cascadas de señalización intracelular del TbR activado, su importancia en la mediación de las respuestas específicas de TGF-β y su papel en la fibrosis fisiológica y patológica aún no se han aclarado por completo36.
Normalmente Smad1 sirve como sustrato para los receptores de BMP, sin embargo existe evidencia de su papel en la estimulación de los genes del colágeno y del factor de crecimiento del tejido conectivo (CTGF) dependiente de TGF-β, en modelos in vitro de fibrosis renal37. En un estudio realizado por Pannu et al, en cultivos de fibroblastos de biopsias de piel de individuos normales y de pacientes con SSc demostraron la fosforilación de Smad1 por c-Abl llevando a la activación del promotor del gen CCN2 y del gen del CTGF38.
Aproximación terapéutica
En esclerodermia se ha demostrado que existen alteraciones en las vías de señalización mediadas por Smad, entre ellas el aumento de receptores para TGF-β en los fibroblastos de pacientes con esclerodermia, la regulación positiva de Smad3, la fosforilación constitutiva de Smad3 y la deficiencia de Smad721,39.
1. Interferencia con TGF-β
Se han desarrollado varias estrategias para bloquear los efectos de TGF-β que incluyen fragmentos solubles del receptor, anticuerpos neutralizantes de TGF-β, inhibidores de cinasa de treonina, inhibidores de la expresión del RNA, RNA de interferencia, etc. Sin embargo, a pesar de la investigación in vitro y en modelos animales de fibrosis, y algunos estudios en humanos, estos acercamientos o no han sido efectivos o están aún en las etapas experimentales/ensayos clínicos, por lo que no están disponibles actualmente para su uso40-42.
Existe la preocupación de que la inhibición de la actividad de TGF-β se asocie con eventos adversos como fenómenos de autoinmunidad o displasia celular y progresión a cáncer. Sin embargo, ninguno de estos efectos ha sido observado en los estudios pre-clínicos, posiblemente por la incapacidad de estas moléculas para bloquear completamente su función. Lo que sí se ha descrito es el desarrollo de aterosclerosis acelerada con el uso de anticuerpos neutralizantes anti-TGF-β en ratones deficientes de apo-E.43,44.
- a. Anticuerpos monoclonales
Yu et al., usando un modelo animal de glome-rulonefritis, señalaron cómo el bloqueo simultáneo de angiotensina II con enalapril, combinado con el bloqueo de TGF-β con un anticuerpo monoclonal neutralizante de ratón (1D11), reducía la fibrosis en una magnitud mayor que cada uno por separado45. Se desarrolló un anticuerpo monoclonal humano contra el TGF-β1 (CAT-192) y se realizó un estudio fase I/II para su uso en etapas tempranas de esclerodermia difusa cutánea sin encontrarse eficacia46.
- b. SM305
Ishida et al. demostraron cómo al bloquear la función de ALK5 con SM305 (molécula pequeña inhibidora de cinasa) en fibroblastos dérmicos normales, se abolieron la fosforilación inducida por ligando, la importación nuclear y la unión al DNA de Smad2/3 y Smad4; y se inhibieron las respuestas transcripcionales dependientes de Smad2/3, al interrumpir la expresión de genes de proteínas de la matriz extracelular, la producción de citoquinas y la diferenciación en miofibroblastos. Igualmente en ratones transgé-nicos para el gen del col1a2, SM305 previno la fosforilación inducida por TGF-β de Smad2/347.
- c. Oligonucleótidos señuelo (oligodecoys u ODN)
Son secuencias pequeñas de nucleótidos ("señuelos") que contienen el elemento de transcripción del TGF-β y unen las proteínas transac-ivadoras previniendo la unión a los elementos de transcripción reales, inhibiendo así la síntesis de colágeno y de otras proteínas de la matriz extracelular. Sin embargo, en pacientes con SSc a quienes se les administró, al compararlos con placebo, no hubo cambios en el puntaje de gravedad del compromiso cutáneo (puntaje de Rodnan) ni en los niveles de citoquinas48.
2. Agonismo con I-Smad
La transferencia génica de Smad7 ha demostrado revertir la fibrosis pulmonar, renal y peritoneal en modelos animales. Aunque estos compuestos no han sido probados en pacientes, podrían representar tratamientos futuros contra la SSc49-52.
3. Interferencia con R-Smad
- a. Halofunginona
Es un alcaloide de origen vegetal que inhibe la fosforilación de Smad3 inducida por TGF-β, impidiendo su unión con el DNA y bloqueando la producción de colágeno tipo I inducida por TGF-β en fibroblastos dérmicos53-55. Pines et al. demostraron incremento en la degradación del colágeno, disminución en el grosor de la dermis y disminución de la expresión del gen del colágeno tipo I en ratones tratados con halofunginona independiente de la vía de administración. En voluntarios sanos se estableció la dosis oral máxima de halofunginona 1,5 mg/día, reportándose solamente efectos adversos gastrointestinales. De trece pacientes con dcSSc en los que se utilizó halofunginona tópica al 0,01% una vez al día por seis meses, cinco disminuyeron al menos un 25% el puntaje de Rodnan, encontrando como evento adverso dermatitis56. Igualmente se ha demostrado en modelos animales que la halofunginona inhibe el desarrollo de fibrosis pulmonar inducida por bleomicina57.
- b. Relaxina
Es una hormona peptídica que usualmente se ha asociado con el embarazo y el parto pues favorece la maduración cervical al igual que relaja la musculatura uterina. Se ha encontrado que en fibroblastos renales inhibe la fosforilación de Smad2, su translocación al núcleo y la formación de heterodímeros con Smad3; además favorece la síntesis y secreción de metaloproteinasas58.
Seibold et al. realizaron un estudio fase II multicéntrico, de distribución aleatoria, doble ciego, controlado con placebo, en 68 pacientes con dcSSc, para evaluar la eficacia, la seguridad y la dosis-respuesta de la relaxina recombinante humana. Encontraron que los pacientes que recibieron 25 mcg/k/d subcutáneos de relaxina durante veinticuatro semanas, tuvieron menores puntajes de gravedad cutánea comparados con placebo, y en forma dosis dependiente. Igual tendencia fue observada en la capacidad vital forzada, la apertura oral y la clase funcional. Los eventos adversos descritos fueron menometrorragia, anemia e irritación local59. Sin embargo, en otro estudio de fase II realizado recientemente y con un mayor número de pacientes (231 pacientes con dcSSc moderada a grave) en el que compararon la administración de 10 y 25 mcg/kg/ d subcutáneos de relaxina contra placebo durante veinticuatro semanas, no se encontraron diferencias en el compromiso cutáneo y pulmonar, pero se produjeron eventos adversos renales con azoemia reversible al suspender el medicamento, hipertensión arterial grave y el desarrollo de crisis renal, por lo que no se ha recomendado su uso60.
- c. SIS3
Es un derivado indol, que actúa como ligando de receptores nucleares con alta afinidad. Un estudio realizado por Jinnin et al. demostró que reduce la actividad transcripcional del gen de la proteína procolágeno tipo I en los miofibroblastos esclerodérmicos y que estos efectos son mediados por la supresión de la fosforilación de Smad3 inducida por TGF-β61.
- d. Paclitaxel
Es un medicamento usado en quimioterapia anti-neoplásica, interfiere con el desajuste de la función normal del microtúbulo hiperesta-bilizando su estructura y alterando así la capacidad de la célula de usar su citoesqueleto de una forma flexible. En ratones con inmunodeficiencia combinada severa transplantados con injertos cutáneos de pacientes con SSc se encontró que disminuyó la fosforilación de Smad2 y Smad3 y el depósito de colágeno62. Zhang et al. demostraron que en un modelo animal de obstrucción ureteral unilateral, el uso de paclitaxel intra-peritoneal en dosis más bajas que las usadas para quimioterapia suprimió la señalización renal aumentada inducida por TGF-β a través de Smad63.
4. Inhibidores de cinasa de tirosina Imatinib
Es un medicamento usado en el tratamiento de la leucemia mieloide crónica. Se une al bolsillo de unión al ATP en c-Abl provocando su cambio conformacional y bloqueando su actividad de cinasa de tirosina. Se ha demostrado que de esta manera puede suprimir la respuesta fibrogénica de los fibroblastos al estímulo por TGF-β38,64. In vitro, imatinib bloquea la síntesis de colágeno y la proliferación de fibroblastos inducida por TGF-β. Se ha demostrado que también previene la fibrosis cutánea inducida por bleomicina en ratones65.
Van Daele et al. describieron los estudios realizados en fibroblastos pulmonares obtenidos de biopsias bronquiales de un paciente con SSc y fibrosis pulmonar cuyo compromiso pulmonar progresó a pesar del tratamiento con ciclofos-famida intravenosa bimensual y dosis bajas de esteroides. Imatinib mesilato previno in vitro la estimulación de la transcripción del gen del colágeno tipo I. El tratamiento de este paciente con imatinib mesilato produjo mejoría en el grosor de la piel, con reducción importante del puntaje de Rodnan luego de tres meses de inicio del medicamento, junto con estabilización de la función pulmonar y de los hallazgos en el TA-CAR66. En un caso publicado por Distler et al., veinte semanas de tratamiento con imatinib mesilato causaban marcada mejoría en la función pulmonar y los hallazgos en la TACAR en un paciente con enfermedad mixta del tejido conectivo asociada con fibrosis pulmonar rápidamente progresiva67. Chung et al. reportaron los resultados del tratamiento con 200 mg/día de imatinib en dos pacientes con SSc. El primero tenía tres años de evolución y a pesar del tratamiento con ciclofosfamida tenía deterioros pulmonares y cutáneos progresivos. Luego de tres meses de tratamiento con imatinib, el puntaje de Rodnan disminuyó y el compromiso pulmonar se estabilizó. El segundo paciente había sido diagnosticado recientemente y se inició imatinib debido a intolerancia a otros medicamentos. Tras seis meses de tratamiento, el puntaje de Rodnan había disminuido de forma importante. Ambos pacientes toleraron imatinib y no se reportaron eventos adversos graves68.
Estudios abiertos usando 400 mg de imatinib han reportado su eficacia en SSc. La mejoría cutánea se vuelve aparente a los seis meses de tratamiento y es sostenida hasta por un año de seguimiento. Como eventos adversos se han reportado infecciones, edema, náuseas, mialgias y fatiga. Muchos de estos son autolimitados y mejoran en la casi totalidad de los pacientes al disminuir la dosis69.
Recientemente fueron publicados los resultados del estudio Gleevec, ensayo clínico fase II, abierto, realizado en treinta pacientes con esclerodermia y compromiso cutáneo grave con un año de seguimiento. El objetivo era evaluar la seguridad y tolerancia de 400 mg/día de imatinib vía oral en el tratamiento de estos pacientes. Se encontró una tolerancia adecuada, siendo los edemas, las náuseas y mialgias los principales eventos adversos descritos. Se esperan estudios que busquen establecer su eficacia y responder lo más rápido posible a la pregunta actual de si será imatinib el primer tratamiento antifibrosis realmente eficaz para la esclerodermia70,71.
Reflexiones finales
TGF-β es la principal citoquina implicada en la patogénesis de la esclerodermia. La identificación de las moléculas implicadas en señalización a través de Smad y de otras moléculas intracelulares proporciona nuevos blancos terapéuticos pero son necesarios más estudios en modelos animales y en humanos que logren reproducir los resultados satisfactorios con la menor cantidad posible de eventos adversos.
Referencias
1. Jimenez SA, Derk CT. Following the molecular pathways toward an understanding of the pathoge-nesis of systemic sclerosis. Ann Intern Med 2004;140(1):37-50. Epub 2004/01/07. [ Links ]
2. Vuorio T, Kahari VM, Black C, Vuorio E. Expression of osteonectin, decorin, and transforming growth factor-beta 1 genes in fibroblasts cultured from patients with systemic sclerosis and morphea. J Rheumatol 1991;18(2):247-51. Epub 1991/02/01. [ Links ]
3. Rajkumar VS, Howell K, Csiszar K, Denton C P, Black CM, Abraham DJ. Shared expression of phenotypic markers in systemic sclerosis indicates a convergence of pericytes and fibroblasts to a myofibroblast lineage in fibrosis. Arthritis Res Ther 2005;7(5):R1113-23. Epub 2005/10/07. [ Links ]
4. Chizzolini C. T cells, B cells, and polarized immune response in the pathogenesis of fibrosis and systemic sclerosis. Curr Opin Rheumatol 2008;20(6):707-12. Epub 2008/10/24. [ Links ]
5. Jinnin M. Mechanisms of skin fibrosis in systemic sclerosis. J Dermatol 2010;37(1):11-25. Epub 2010/02/24. [ Links ]
6. Helmbold P, Fiedler E, Fischer M, Marsch W. Hyperplasia of dermal microvascular pericytes in scleroderma. J Cutan Pathol 2004;31(6):431-40. Epub 2004/06/10. [ Links ]
7. Peltonen J, Kahari L, Jaakkola S, Kahari VM, Varga J, Uitto J, et al. Evaluation of transforming growth factor beta and type I procollagen gene expression in fibrotic skin diseases by in situ hybridization. J Invest Dermatol 1990;94(3):365-71. Epub 1990/03/01. [ Links ]
8. Varga J. Scleroderma and Smads: dysfunctional Smad family dynamics culminating in fibrosis. Arthritis Rheum 2002;46(7):1703-13. Epub 2002/07/19. [ Links ]
9. Derynck R, Zhang Y. Intracellular signalling: the mad way to do it. Curr Biol 1996;6(10):1226-9. Epub 1996/10/01. [ Links ]
10. Mori Y, Chen SJ, Varga J. Expression and regulation of intracellular SMAD signaling in scleroderma skin fibroblasts. Arthritis Rheum 2003;48(7):1964-78. Epub 2003/07/09. [ Links ]
11. Zawel L, Dai JL, Buckhaults P, Zhou S, Kinzler KW, Vogelstein B, et al. Human Smad3 and Smad4 are sequence-specific transcription activators. Mol Cell 1998;1(4):611-7. Epub 1998/07/14. [ Links ]
12. Shi Y, Massague J. Mechanisms of TGF-beta signaling from cell membrane to the nucleus. Cell 2003;113(6): 685-700. Epub 2003/06/18. [ Links ]
13. Lutz M, Knaus P. Integration of the TGF-beta pathway into the cellular signalling network. Cell Signal 2002;14(12):977-88. Epub 2002/10/03. [ Links ]
14. Flanders KC. Smad3 as a mediator of the fibrotic response. Int J Exp Pathol 2004;85(2):47-64. Epub 2004/05/25. [ Links ]
15. The Smads. Genome Biol 2001;2(8):REVIEWS3010. Epub 2001 Aug 2. [ Links ]
16. Runyan CE, Schnaper HW, Poncelet AC. The role of internalization in transforming growth factor beta1-induced Smad2 association with Smad anchor for receptor activation (SARA) and Smad2-dependent signaling in human mesangial cells. J Biol Chem 2005;280(9):8300-8. Epub 2004/12/23. [ Links ]
17. Kawabata M, Inoue H, Hanyu A, Imamura T, Miyazono K. Smad proteins exist as monomers in vivo and undergo homo- and hetero-oligomerization upon activation by serine/threonine kinase receptors. EMBO J 1998;17(14):4056-65. Epub 1998/07/22. [ Links ]
18. Inagaki Y, Truter S, Ramirez F. Transforming growth factor-beta stimulates alpha 2(I) collagen gene expression through a cis-acting element that contains an Sp1-binding site. J Biol Chem 1994;269(20): 14828-34. Epub 1994/05/20. [ Links ]
19. Bhattacharyya S, Ghosh AK, Pannu J, Mori Y, Takagawa S, Chen G, et al. Fibroblast expression of the coactivator p300 governs the intensity of profibrotic response to transforming growth factor beta. Arthritis Rheum 2005;52(4):1248-58. Epub 2005/04/09. [ Links ]
20. Greenwel P, Inagaki Y, Hu W, Walsh M, Ramirez F. Sp1 is required for the early response of alpha2(I) collagen to transforming growth factor-beta1. J Biol Chem 1997;272(32):19738-45. Epub 1997/08/08. [ Links ]
21. Ihn H, Yamane K, Asano Y, Jinnin M, Tamaki K. Constitutively phosphorylated Smad3 interacts with Sp1 and p300 in scleroderma fibroblasts. Rheumatology (Oxford). 2006;45(2):157-65. Epub 2005/12/02. [ Links ]
22. Massague J, Seoane J, Wotton D. Smad transcription factors. Genes Dev 2005;19(23):2783-810. Epub 2005/12/03. [ Links ]
23. Asano Y, Ihn H, Yamane K, Kubo M, Tamaki K. Impaired Smad7-Smurf-mediated negative regulation of TGF-beta signaling in scleroderma fibroblasts. J Clin Invest 2004;113(2):253-64. Epub 2004/01/15. [ Links ]
24. Nakao A, Imamura T, Souchelnytskyi S, Kawabata M, Ishisaki A, Oeda E, et al. TGF-beta receptor-mediated signalling through Smad2, Smad3 and Smad4. EMBO J 1997;16(17):5353-62. Epub 1997/ 10/06. [ Links ]
25. Takagawa S, Lakos G, Mori Y, Yamamoto T, Nishioka K, Varga J. Sustained activation of fibroblast transforming growth factor-beta/Smad signaling in a murine model of scleroderma. J Invest Dermatol 2003;121(1):41-50. Epub 2003/07/04. [ Links ]
26. Kavsak P, Rasmussen RK, Causing CG, Bonni S, Zhu H, Thomsen GH, et al. Smad7 binds to Smurf2 to form an E3 ubiquitin ligase that targets the TGF beta receptor for degradation. Mol Cell 2000;6(6):1365-75. Epub 2001/02/13. [ Links ]
27. Afrakhte M, Moren A, Jossan S, Itoh S, Sampath K, Westermark B, et al. Induction of inhibitory Smad6 and Smad7 mRNA by TGF-beta family members. Biochem Biophys Res Commun 1998;249(2):505-11. Epub 1998/08/26. [ Links ]
28. Nagarajan R P, Chen F, Li W, Vig E, Harrington MA, Nakshatri H, et al. Repression of transforming-growth-factor-beta-mediated transcription by nuclear factor kappaB. Biochem J 2000;348 Pt 3:591-6. Epub 2000/ 06/07. [ Links ]
29. Ross S, Hill CS. How the Smads regulate transcription. Int J Biochem Cell Biol 2008;40(3):383-408. Epub 2007/12/07. [ Links ]
30. Itoh S, ten Dijke P. Negative regulation of TGF-beta receptor/Smad signal transduction. Curr Opin Cell Biol 2007;19(2):176-84. Epub 2007/02/24. [ Links ]
31. Zhu HJ, Burgess AW. Regulation of transforming growth factor-beta signaling. Mol Cell Biol Res Commun 2001;4(6):321-30. Epub 2001/11/13. [ Links ]
32. Tajima Y, Goto K, Yoshida M, Shinomiya K, Sekimoto T, Yoneda Y, et al. Chromosomal region maintenance 1 (CRM1)-dependent nuclear export of Smad ubiquitin regulatory factor 1 (Smurf1) is essential for negative regulation of transforming growth factor-beta signaling by Smad7. J Biol Chem 2003;278(12): 10716-21. Epub 2003/01/10. [ Links ]
33. Levy L, Howell M, Das D, Harkin S, Episkopou V, Hill CS. Arkadia activates Smad3/Smad4-dependent transcription by triggering signal-induced SnoN degradation. Mol Cell Biol 2007;27(17):6068-83. Epub 2007/06/27. [ Links ]
34. Moustakas A, Heldin CH. Non-Smad TGF-beta signals. J Cell Sci 2005;118(Pt 16):3573-84. Epub 2005/08/18. [ Links ]
35. Wilkes MC, Leof EB. Transforming growth factor beta activation of c-Abl is independent of receptor internalization and regulated by phosphatidylinositol 3-kinase and PAK2 in mesenchymal cultures. J Biol Chem 2006;281(38):27846-54. Epub 2006/07/27. [ Links ]
36. Varga J, Abraham D. Systemic sclerosis: a prototypic multisystem fibrotic disorder. J Clin Invest 2007; 117(3):557-67. Epub 2007/03/03. [ Links ]
37. Takahashi T, Abe H, Arai H, Matsubara T, Nagai K, Matsuura M, et al. Activation of STAT3/Smad1 is a key signaling pathway for progression to glomerulos-clerosis in experimental glomerulonephritis. J Biol Chem 2005;280(8):7100-6. Epub 2004/12/14. [ Links ]
38. Pannu J, Asano Y, Nakerakanti S, Smith E, Jablonska S, Blaszczyk M, et al. Smad1 pathway is activated in systemic sclerosis fibroblasts and is targeted by imatinib mesylate. Arthritis Rheum 2008;58(8):2528-37. Epub 2008/08/01. [ Links ]
39. Dong C, Zhu S, Wang T, Yoon W, Li Z, Alvarez RJ, et al. Deficient Smad7 expression: a putative molecular defect in scleroderma. Proc Natl Acad Sci U S A. 2002;99(6):3908-13. Epub 2002/03/21. [ Links ]
40. Christner PJ, Jimenez SA. Animal models of systemic sclerosis: insights into systemic sclerosis pathogenesis and potential therapeutic approaches. Curr Opin Rheumatol 2004;16(6):746-52. Epub 2004/12/04. [ Links ]
41. Callahan J F, Burgess JL, Fornwald JA, Gaster LM, Harling JD, Harrington F P, et al. Identification of novel inhibitors of the transforming growth factor beta1 (TGF-beta1) type 1 receptor (ALK5). J Med Chem 2002;45(5):999-1001. Epub 2002/02/22. [ Links ]
42. Kondo M, Cubillo E, Tobiume K, Shirakihara T, Fukuda N, Suzuki H, et al. A role for Id in the regulation of TGF-beta-induced epithelial-mesenchy-mal transdifferentiation. Cell Death Differ 2004; 11(10):1092-101. Epub 2004/06/08. [ Links ]
43. Prud'homme GJ, Piccirillo CA. The inhibitory effects of transforming growth factor-beta-1 (TGF-beta1) in autoimmune diseases. J Autoimmun 2000;14(1):23-42. Epub 2000/01/29. [ Links ]
44. Mallat Z, Gojova A, Marchiol-Fournigault C, Esposito B, Kamate C, Merval R, et al. Inhibition of transforming growth factor-beta signaling accelerates atherosclerosis and induces an unstable plaque phenotype in mice. Circ Res 2001;89(10):930-4. Epub 2001/11/10. [ Links ]
45. Yu L, Border WA, Anderson I, McCourt M, Huang Y, Noble NA. Combining TGF-beta inhibition and angiotensin II blockade results in enhanced antifibrotic effect. Kidney Int 2004;66(5):1774-84. Epub 2004/ 10/22. [ Links ]
46. Denton C P, Merkel PA, Furst DE, Khanna D, Emery P, Hsu VM, et al. Recombinant human anti-transforming growth factor beta1 antibody therapy in systemic sclerosis: a multicenter, randomized, placebo-controlled phase I/II trial of CAT-192. Arthritis Rheum 2007;56(1):323-33. Epub 2006/12/30. [ Links ]
47. Ishida W, Mori Y, Lakos G, Sun L, Shan F, Bowes S, et al. Intracellular TGF-beta receptor blockade abrogates Smad-dependent fibroblast activation in vitro and in vivo. J Invest Dermatol 2006;126(8):1733-44. Epub 2006/06/03. [ Links ]
48. Baraut J, Farge D, Jean-Louis F, Kesmandt H, Durant C, Verrecchia F, et al. [Cytokines in systemic sclerosis.]. Pathol Biol (Paris). 2010. Epub 2010/02/02. Les cytokines dans la sclerodermie systemique. [ Links ]
49. Nakao A, Fujii M, Matsumura R, Kumano K, Saito Y, Miyazono K, et al. Transient gene transfer and expression of Smad7 prevents bleomycin-induced lung fibrosis in mice. J Clin Invest 1999;104(1):5-11. Epub 1999/07/07. [ Links ]
50. Terada Y, Hanada S, Nakao A, Kuwahara M, Sasaki S, Marumo F. Gene transfer of Smad7 using electroporation of adenovirus prevents renal fibrosis in post-obstructed kidney. Kidney Int 2002;61(1 Suppl):S94-8. Epub 2002/02/14. [ Links ]
51. Nie J, Dou X, Hao W, Wang X, Peng W, Jia Z, et al. Smad7 gene transfer inhibits peritoneal fibrosis. Kidney Int 2007;72(11):1336-44. Epub 2007/09/14. [ Links ]
52. Lan HY. Smad7 as a therapeutic agent for chronic kidney diseases. Front Biosci 2008;13:4984-92. Epub 2008/05/30. [ Links ]
53. Nagler A, Miao HQ, Aingorn H, Pines M, Genina O, Vlodavsky I. Inhibition of collagen synthesis, smooth muscle cell proliferation, and injury-induced intimal hyperplasia by halofuginone. Arterioscler Thromb Vasc Biol 1997;17(1):194-202. Epub 1997/ 01/01. [ Links ]
54. Halevy O, Nagler A, Levi-Schaffer F, Genina O, Pines M. Inhibition of collagen type I synthesis by skin fibroblasts of graft versus host disease and scleroderma patients: effect of halofuginone. Biochem Pharmacol 1996;52(7):1057-63. Epub 1996/10/11. [ Links ]
55. McGaha TL, Phelps RG, Spiera H, Bona C. Halofu-ginone, an inhibitor of type-I collagen synthesis and skin sclerosis, blocks transforming-growth-factor-beta-mediated Smad3 activation in fibroblasts. J Invest Dermatol 2002;118(3):461-70. Epub 2002/ 03/05. [ Links ]
56. Pines M, Snyder D, Yarkoni S, Nagler A. Halofuginone to treat fibrosis in chronic graft-versus-host disease and scleroderma. Biol Blood Marrow Transplant 2003;9(7):417-25. Epub 2003/07/19. [ Links ]
57. Nagler A, Firman N, Feferman R, Cotev S, Pines M, Shoshan S. Reduction in pulmonary fibrosis in vivo by halofuginone. Am J Respir Crit Care Med 1996;154(4 Pt 1):1082-6. Epub 1996/10/01. [ Links ]
58. Heeg MH, Koziolek MJ, Vasko R, Schaefer L, Sharma K, Muller GA, et al. The antifibrotic effects of relaxin in human renal fibroblasts are mediated in part by inhibition of the Smad2 pathway. Kidney Int 2005;68(1):96-109. Epub 2005/06/16. [ Links ]
59. Seibold JR, Korn JH, Simms R, Clements PJ, Moreland LW, Mayes MD, et al. Recombinant human relaxin in the treatment of scleroderma. A randomized, double-blind, placebo-controlled trial. Ann Intern Med 2000;132(11):871-9. Epub 2000/06/03. [ Links ]
60. Khanna D, Clements PJ, Furst DE, Korn JH, Ellman M, Rothfield N, et al. Recombinant human relaxin in the treatment of systemic sclerosis with diffuse cutaneous involvement: a randomized, double-blind, placebo-controlled trial. Arthritis Rheum 2009;60(4): 1102-11. Epub 2009/04/01. [ Links ]
61. Jinnin M, Ihn H, Tamaki K. Characterization of SIS3, a novel specific inhibitor of Smad3, and its effect on transforming growth factor-beta1-induced extracellular matrix expression. Mol Pharmacol 2006;69(2): 597-607. Epub 2005/11/17. [ Links ]
62. Liu X, Zhu S, Wang T, Hummers L, Wigley FM, Goldschmidt-Clermont PJ, et al. Paclitaxel modulates TGFbeta signaling in scleroderma skin grafts in immunodeficient mice. PLoS Med 2005;2(12):e354. Epub 2005/10/28. [ Links ]
63. Zhang D, Sun L, Xian W, Liu F, Ling G, Xiao L, et al. Low-dose paclitaxel ameliorates renal fibrosis in rat UUO model by inhibition of TGF-beta/Smad activity. Lab Invest 2010;90(3):436-47. Epub 2010/02/10. [ Links ]
64. Daniels CE, Wilkes MC, Edens M, Kottom TJ, Murphy SJ, Limper AH, et al. Imatinib mesylate inhibits the profibrogenic activity of TGF-beta and prevents bleomycin-mediated lung fibrosis. J Clin Invest 2004;114(9):1308-16. Epub 2004/11/03. [ Links ]
65. Distler JH, Jungel A, Huber LC, Schulze-Horsel U, Zwerina J, Gay RE, et al. Imatinib mesylate reduces production of extracellular matrix and prevents development of experimental dermal fibrosis. Arthritis Rheum 2007;56(1):311-22. Epub 2006/12/30. [ Links ]
66. van Daele PL, Dik WA, Thio HB, van Hal PT, van Laar JA, Hooijkaas H, et al. Is imatinib mesylate a promising drug in systemic sclerosis? Arthritis Rheum 2008;58(8):2549-52. Epub 2008/08/01. [ Links ]
67. Distler JH, Manger B, Spriewald BM, Schett G, Distler O. Treatment of pulmonary fibrosis for twenty weeks with imatinib mesylate in a patient with mixed connective tissue disease. Arthritis Rheum 2008;58(8): 2538-42. Epub 2008/08/01. [ Links ]
68. Chung L, Fiorentino D F, Benbarak MJ, Adler AS, Mariano MM, Paniagua RT, et al. Molecular framework for response to imatinib mesylate in systemic sclerosis. Arthritis Rheum 2009;60(2):584-91. Epub 2009/01/31. [ Links ]
69. Ong VH, Denton C P. Innovative therapies for systemic sclerosis. Curr Opin Rheumatol 2010;22(3):264-72. Epub 2010/03/02. [ Links ]
70. Taieb A, Constans J, Mahon FX. [A new therapeutic avenue for severe systemic sclerosis: imatinib mesylate]. Rev Med Interne 2008;29(3):173-5. Epub 2007/06/29. Une nouvelle piste therapeutique pour les sclerodermies graves: le mesylate d'imatinib. [ Links ]
71. Spiera R F, Gordon JK, Mersten JN, Magro CM, Mehta M, Wildman H F, et al. Imatinib mesylate (Gleevec) in the treatment of diffuse cutaneous systemic sclerosis: results of a 1-year, phase IIa, single-arm, open-label clinical trial. Ann Rheum Dis England 2011. p. 1003-9. [ Links ]














