Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista Colombiana de Reumatología
versión impresa ISSN 0121-8123
Rev.Colomb.Reumatol. vol.19 no.4 Bogotá oct./dic. 2012
INVESTIGACIÓN ORIGINAL
Síndrome antifosfolípido: descripción de una cohorte de pacientes colombianos y evaluación de los factores de riesgo para trombosis
Antiphospholipid syndrome: description of a cohort from Colombia and evaluation of thrombosis risk factors
Miguel Mesa1, Carolina Saldarriaga1, Carolina Aguilar1, Carlos Builes1, Alicia Quiroga1, Natalia Aristizábal1, John Jairo Zuleta2, Francisco Vargas3, Aura Ligia Zapata3, Oscar Jaír Felipe3, Javier Darío Márquez4, Carlos Jaime Velásquez3,4, Luis Fernando Pinto4
1Departamento de Medicina Interna. Facultad de Medicina. Universidad Pontificia Bolivariana. Medellín, Colombia.
2Unidad de Investigaciones. Hospital Pablo Tobón Uribe, Universidad de Antioquia. Medellín Colombia.
3Grupo UNIR. Clínica Universitaria Bolivariana. Escuela de Ciencias de la Salud. Universidad Pontificia Bolivariana. Medellín, Colombia.
4Departamento de Medicina Interna y Reumatología. Unidad de Especialidades Médicas. Unidad de Investigaciones Hospital Pablo Tobón Uribe. Medellín, Colombia.
Correspondencia: Luis Fernando Pinto: lfpintop@hotmail.com
Los autores declaran no presentar ningún conflicto de interés al momento de la redacción del manuscrito.
Recibido: 16 de octubre de 2012 Aceptado: 29 de noviembre de 2012
Resumen
Introducción: El síndrome antifosfolípido es una enfermedad autoinmune, caracterizada por trombosis vascular y morbilidad gestacional en presencia de anticuerpos antifosfolípidos. Se han descrito varios factores de riesgo para el desarrollo de trombosis en estos pacientes, pero los estudios son heterogéneos y no discriminan entre eventos arteriales y venosos.
Objetivo: Describir las manifestaciones clínicas e inmunológicas del síndrome antifosfolípido en una cohorte de pacientes colombianos y establecer los factores de riesgo para el desarrollo de trombosis venosa y arterial.
Materiales y métodos: Se condujo un estudio analítico de corte transversal. Criterio de inclusión: Consenso de Sydney de 2006 y clasificación del síndrome antifosfolípido como secundario, según criterios del American College of Rheumatology.
Resultados: Se incluyeron 100 pacientes; 84 de ellos mujeres; edad promedio 37.6 años. El 59% de los pacientes correspondía a síndrome antifosfolípido secundario. La manifestación clínica más frecuente inicial y durante el seguimiento fue la trombosis venosa (56.52% y 47%, respectivamente), seguida por "manifestaciones no criterio" (23.91%), especialmente neurológicas. La trombosis venosa profunda fue recurrente en el 46%; 30% de los individuos presentó trombocitopenia severa. La ausencia de autoanticuerpos específicos discriminó entre formas primarias y secundarias. La diabetes mellitus fue un factor de riesgo significativo para trombosis venosa (6.4% vs. 0%; OR 2.205, IC 95%: 1.772-2.742) y el tabaquismo para enfermedad cerebrovascular (33.3% vs. 6%, OR 7.9, IC 95%: 1.5-41.324).
Conclusiones: Esta cohorte de pacientes colombianos con síndrome antifosfolípido presenta alto porcentaje de manifestaciones no incluidas en los criterios clasificatorios, con compromiso orgánico grave, atípico y recurrente.
Palabras clave: Síndrome antifosfolípido; diabetes mellitus; tabaquismo; trombosis venosa.
Summary
Introduction: Antiphospholipid syndrome is an autoimmune disease characterized by vascular thrombosis and gestational morbidity in the presence of antiphospholipid antibodies. Several risk factors for the development of thrombosis have been described in these patients, but the studies are heterogeneous and do not discriminate between arterial and venous events.
Objective: To describe the clinical and immunological manifestations of antiphospholipid syndrome in a cohort of Colombian patients and to establish risk factors for the development of arterial and venous thrombosis.
Materials and Methods: We conducted a cross-sectional analytical study. Inclusion criteria: 2006 Sydney Consensus Statement and classification in secondary antiphospholipid syndrome according to the American College of Rheumatology criteria.
Results: We included 100 patients, 84 of them women, with a mean age of 37.6 years. 59% of patients fulfilled secondary antiphospholipid syndrome criteria. The most common clinical manifestation during the initial evaluation and follow-up visit was venous thrombosis (56.52% and 47%, respectively), followed by "non-criteria" manifestations (23.91%), especially neurological. Deep venous thrombosis was recurrent in 46%, and 30% of individuals presented severe thrombocytopenia. Absence of specific autoantibodies discriminated between primary and secondary forms. Diabetes mellitus was a significant risk factor for venous thrombosis (6.4% vs. 0%, OR 2.205: 95% CI 1.772-2.742) and smoking for cerebrovascular disease (33.3% vs. 6%, OR 7.9, 95% CI 1.5- 41.324).
Conclusions: This cohort of Colombian patients with antiphospholipid syndrome had a high percentage of events not included in the classification criteria, with severe, atypical, and recurrent organic involvement.
Key words: Antiphospholipid syndrome; diabetes mellitus; smoking; venous thrombosis.
Introducción
El síndrome antifosfolípido (SAF) es una enfermedad autoinmune caracterizada por trombosis vascular y morbilidad gestacional en la presencia de anticuerpos antifosfolípidos (AAF). Es la causa más común de trombofilia adquirida. El SAF puede ser primario o secundario (asociado a otras enfermedades autoinmunes), particularmente a lupus eritematoso sistémico (LES)1. La presencia aislada de AAF en pacientes asintomáticos no es suficiente para el desarrollo de trombosis en este grupo de individuos; se ha propuesto la hipótesis del "segundo hit", como la necesidad de un disparador que conduzca al desarrollo de estos eventos clínicos2.
Se han descrito varios factores de riesgo para el desarrollo de eventos trombóticos en estos pacientes: la presencia de anticoagulante lúpico (LA), los títulos altos de anticuerpos anticardiolipina IgG (aCL IgG), la persistencia de AAF en el tiempo, la hipertensión arterial y la hipertrigliceridemia, entre otros3,4.
Los estudios que han descrito estas asociaciones son heterogéneos en la naturaleza de los eventos trombóticos (arteriales, venosos o morbilidad gestacional) y no discriminan con claridad si estos factores de riesgo están presentes en pacientes con SAF primario o secundario.
El objetivo de este trabajo es describir las manifestaciones clínicas e inmunológicas de la cohorte y establecer los factores de riesgo para el desarrollo de eventos trombóticos en pacientes colombianos con SAF.
Materiales y métodos
Se hizo un estudio analítico de corte transversal. Se incluyeron todos los pacientes mayores de 18 años, seguidos en los servicios de Reumatología del Hospital Pablo Tobón Uribe y la Clínica Universitaria Bolivariana de la ciudad de Medellín, entre enero de 2000 y diciembre de 2010, y que cumplían los criterios de Sydney de clasificación para SAF5. También se analizaron las "manifestaciones no criterio" según se definieron en esta reunión de consenso5. Los pacientes fueron clasificados como SAF secundario si cumplían los criterios del Colegio Americano de Reumatología, ACR, para otras enfermedades del tejido conectivo (LES, artritis reumatoide, esclerosis sistémica, dermatomiositis, polimiositis, síndrome de Sjögren y vasculitis sistémicas) y como "lupus-like" si cumplían dos o tres criterios para LES del ACR. Las pruebas inmunológicas fueron realizadas en laboratorios de referencia (ANAs por inmunofuorescencia indirecta con células Hep-2, anticuerpos anti-DNA por inmunofuorescencia indirecta con Crithidia Luciliae o ELISA, anticuerpos anti-ENA, anti-b2GP1 y aCL por ELISA y LA siguiendo las guías de la Sociedad Internacional de Trombosis y Hemostasis6.
Se realizó una descripción general de la cohorte, utilizando promedios para las variables cuantitativas y números absolutos y sus respectivos porcentajes para las cualitativas. Se hizo un análisis exploratorio de los factores de riesgo para trombosis arterial y venosa para lo cual se calcularon los OR con sus respectivos intervalos de confianza del 95%. No se realizaron análisis multivariados porque el objetivo era identificar la asociación entre los diferentes factores y el desenlace; no se pretendía hacer modelos predictivos. Se utilizó el programa SPSS 13.0. El estudio contó con la aprobación de los comités de investigación y de ética en investigación, de ambas instituciones.
Resultados
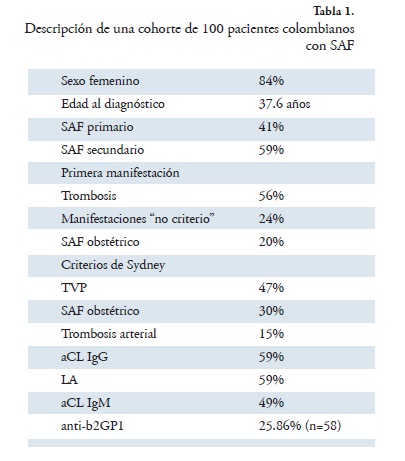
La población está constituida por 100 pacientes, 84 mujeres (84%) y 16 hombres (16%); la edad promedio al diagnóstico de SAF fue de 37.6 en la cohorte completa, de 37.4 en las mujeres, de 35.3 en los hombres y de 36.4 en el subgrupo de SAF obstétrico. El 41% de los pacientes se clasificó como SAF primario y el 59% como SAF secundario distribuido de la siguiente manera: LES (48%), "lupus-like" (7%), síndrome de Sjögren primario (2%), artritis reumatoide (1%) y poliarteritis nodosa (1%).
La manifestación clínica inicial de SAF fue la trombosis (56.52% de los casos), seguida por "manifestaciones no criterio" (23.91%) y por compromiso obstétrico (19.57%). Entre los criterios clínicos de Sydney se presentaron, en orden de frecuencia: trombosis venosa (47%), SAF obstétrico (30%), trombosis arterial (15%) y entre los criterios de laboratorio: aCL IgG (59%), LA (59%), aCL IgM (49%) y anti-β2GP1 (25.86%, n=58) (Tabla 1).
Las manifestaciones vasculares fueron las más frecuentes, tanto al debut de la enfermedad como durante el seguimiento; la más común fue la trombosis venosa profunda (TVP) que ocurrió en el 47% de los pacientes; el 62% de los episodios (n=32) se localizó en los miembros inferiores, el 5.8% (n=3) en los miembros superiores y el 3.9% (n=2) en ambos. En el 21.5% (n=11) la trombosis venosa se localizó en sitios poco usuales, tales como: senos venosos durales (n=5), suprahepáticas (n=3), cava inferior (n=1) y mesentérica (n=2). En el 46% de los casos las TVP fueron recurrentes y el 15% se complicó con tromboembolismo pulmonar (TEP). El 15% de los pacientes presentó oclusiones arteriales; úlceras en los miembros inferiores (12%), enfermedad cerebrovascular (ECV) (11%) y compromiso microvascular (4%), (enfermedad multiinfarto y corea secundaria, úlcera cutánea con evidencia de microtrombosis y neuropatía trombótica del nervio fibular). En el 3% de los casos se documentó recurrencia de la trombosis arterial.
Las obstétricas corresponden al tercer grupo más frecuente de manifestaciones clínicas; el 32%, de las mujeres, tuvo algún tipo de complicación obstétrica y fue la manifestación inicial en el 51% de ellas. Se presentaron veinte pérdidas fetales, trece pérdidas embrionarias, nueve partos prematuros, nueve casos de preeclampsia, diez cesáreas urgentes, cuatro casos de bajo peso al nacer y cuatro de síndrome HELLP.
La mayoría de las manifestaciones neurológicas fueron de origen vascular. El 11% de los pacientes tuvo ECV; uno de ellos (1%) presentó demencia multiinfarto. Otras manifestaciones fueron: epilepsia (2%), neuritis óptica (2%), mielopatía (2%, uno de ellos asociado a neuritis óptica), corea (1%), síndrome de Sneddon (1%) y pseudotumor cerebri (1%).
En el 33% de los pacientes se demostró trombocitopenia en algún momento de la evolución; el 53.3% tuvo recuentos entre 101.000 y 150.000 plaquetas/ mm3, el 16.6% entre 50.000 y 100.000/mm3 y el 30% menos de 50.000 plaquetas/mm3. Se documentó anemia hemolítica autoinmune en el 6% de los pacientes y síndrome de Evans en el 5% de ellos.
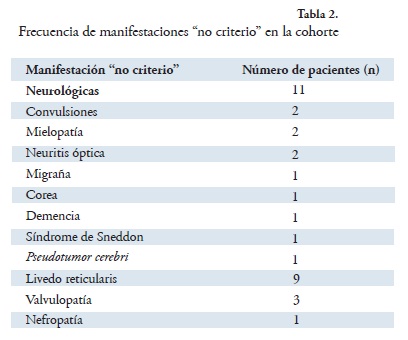
Las manifestaciones "no criterio" fueron el segundo grupo más frecuente de presentación de SAF en la cohorte. El 16% de los pacientes presentó algún tipo de nefropatía: nefritis lúpica (11%), uno de ellos con microangiopatía trombótica por SAF asociada, enfermedad renal de causa no determinada (4%) y una paciente presentó glomerulonefritis proliferativa difusa con patrón "full-house" en la inmunofuorescencia sin cumplir los criterios clasificatorios de LES y sin autoanticuerpos diferentes a los AAF, luego de 5 años de seguimiento. El 3% de los pacientes presentó valvulopatías cardíacas y el 1% hemorragia alveolar difusa. La Tabla 2 muestra la frecuencia de las manifestaciones "no criterio" presentadas en la cohorte.
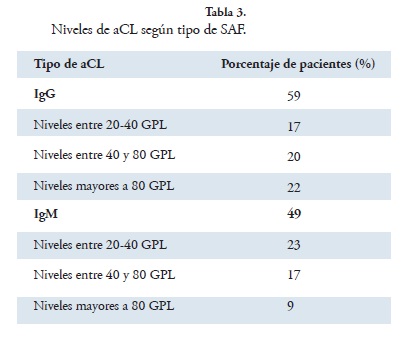
El 59% de los pacientes presentó aCL IgG y el 49% aCL IgM positivos. La frecuencia según los títulos puede verse en la Tabla 3. LA fue positivo en el 59% de los casos y anti-β2GP1 en el 25.86% de los pacientes evaluados con este estudio.
Nueve pacientes con SAF primario (21.95%) tuvieron ANAS positivos, todos con anti-DNA negativo y ocho de ellos con anti-ENAs negativos; un paciente presentó anticuerpos anti-Ro positivo sin cumplir criterios para SAF secundario.
El 37% de los pacientes fue tratado con ácido acetilsalicílico, 52% con warfarina y 6% con ambos medicamentos; el 15% utilizó heparinas de bajo peso molecular, en dos casos intercalado con warfarina. Del total de pacientes tratados con warfarina, los rangos de INR en los que se mantuvieron en promedio fueron: menor de 2 (22.4%; n=13); entre 2-2.5 (46.55%; n=27); entre 2.6-3 (15.51%; n=9) entre 3.1-3.5 (10.34%; n=6) y rangos mayores a 3.6 (5.17%; n=3).
Veintiún pacientes tuvieron episodios de retrombosis, todas venosas; al momento de la recaída trombótica el 23% tenía INR menor a 2, 33% entre 2-2.5; 4.8% entre 2.6-3; 14.3% entre 3.1-3.5 y 9.5% en rangos mayores de 3.6.
La presencia de factores de riesgo tradicionales para trombosis al momento del diagnóstico, se observó en un bajo porcentaje de los pacientes; hipertensión arterial (HTA) (17%), tabaquismo (8%), dislipidemia (7%), diabetes mellitus (3%) y uso de anticonceptivos orales (2%).
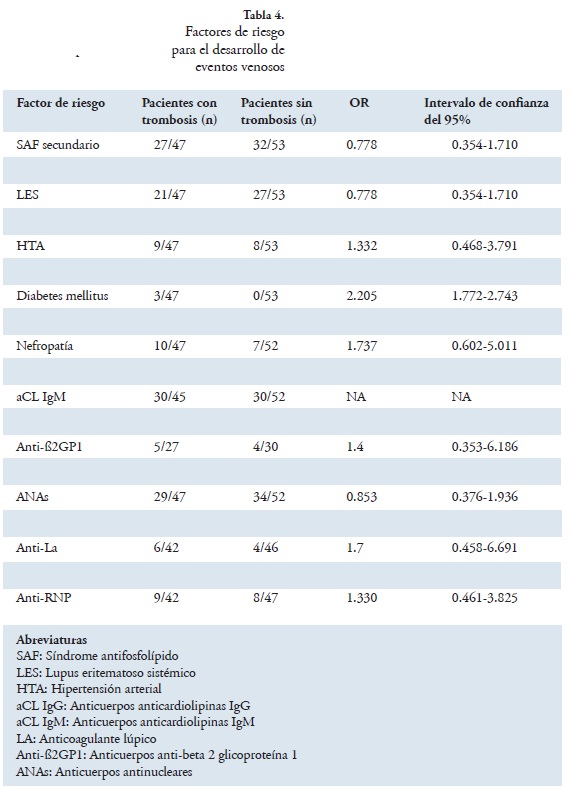
Los pacientes con trombosis venosa tuvieron mayor frecuencia de diabetes mellitus (6.4% vs. 0%), OR 2.205: IC 95%: 1.772-2.742, pero ninguno de los factores de riesgo tradicionales ni de los autoanticuerpos evaluados se asoció a recurrencia trombótica (Tabla 4).
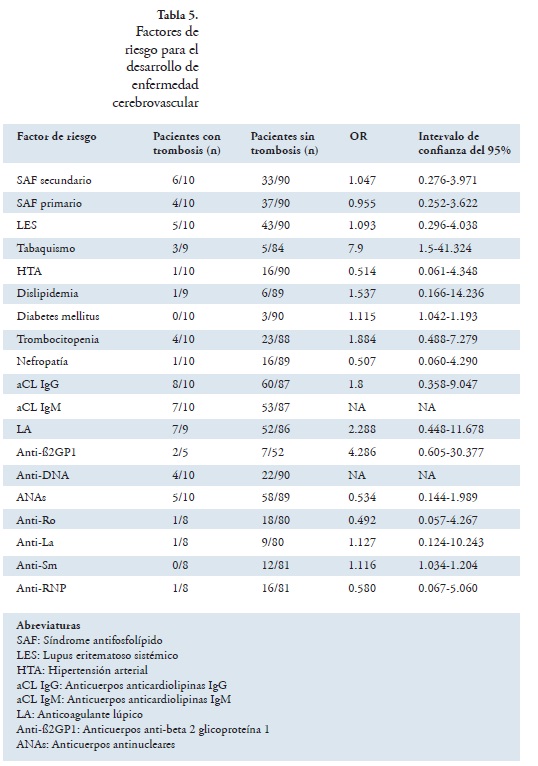
La ECV se asoció al tabaquismo (33.3% vs. 6%, OR 7.9, 95%IC 1.5-41.324) (Tabla 5) pero la trombosis arterial periférica no mostró asociaciones específicas.
Discusión
En este estudio se evaluó la frecuencia de las principales manifestaciones clínicas e inmunológicas de una cohorte de 100 pacientes adultos colombianos con SAF, con criterios clasificatorios de Sydney, seguidos en dos centros de referencia de reumatología de alto nivel de complejidad. Los grupos son homogéneos en sus características raciales y sociodemográficas.
La edad promedio de la cohorte total (37.6 años) es similar a la publicada por otros grupos (42.1±15.4 años)7,8 pero mayor a la de otra cohorte colombiana9 y a la edad de presentación de dos cohortes latinoamericanas (México y Ecuador) que incluyeron pacientes pediátricos10.
Tanto en la cohorte completa como en los subgrupos de SAF primario y secundario predominó el sexo femenino (84%, 75% y 90%, respectivamente); tal como se reportó previamente, el SAF secundario es más frecuente en las mujeres, probablemente por el alto porcentaje de pacientes con LES y "lupus-like" incluido9.
Al igual que en otros grupos7,10,11 la TVP fue la manifestación más común, tanto al inicio (56.52%) como durante la evolución (47%), pero fue más frecuente que en la cohorte latinoamericana (31% al inicio y 32% acumulado) y que en la cohorte Eurofosfolípido (31.7% al inicio y 39.1% acumulado).
Miyakis y cols.5 definieron las manifestaciones "no criterio" de SAF, sugirieron utilizar este término en lugar de manifestaciones "pre SAF" y enfatizaron en la importancia de éstas en la historia natural de la enfermedad; uno de los hallazgos más llamativos de este estudio fue que este grupo de manifestaciones ocupó el segundo lugar entre las más frecuentes con las que debutó la enfermedad (23.91%). García-Carrasco y Galarza encontraron livedo reticularis (32%), trombocitopenia (27%) y migraña (25%) al momento del diagnóstico de SAF pero no describieron su frecuencia como manifestación inicial10.
En el 19.57% de nuestra cohorte la primera manifestación de SAF fue una complicación obstétrica. Cervera y cols.7 encontraron que las complicaciones obstétricas más frecuentes fueron: preeclampsia (9.5%), eclampsia (4.4%) y abrupsio de placenta (2.0%) y, entre las fetales, pérdidas embrionarias (35.4%), pérdidas fetales (16.9%) y partos pretérmino (10.6%), hallazgos similares a los encontrados en nuestra cohorte. García-Carrasco y cols10 encontraron el más alto porcentaje de pérdidas embrionarias (49.6%) y de partos pretérmino (16.8%).
El 15% de los pacientes presentó trombosis arterial, incluyendo ECV y oclusión periférica, que es similar a lo descrito en pacientes colombianos9, ecuatorianos, mexicanos10, y europeos7, pero menor que lo descrito por Pengo y cols. en un grupo de pacientes italianos con alto riesgo para trombosis (47.1%)11. En el 3% de los casos documentamos recurrencia de la oclusión arterial. La mayoría de los episodios oclusivos arteriales de esta cohorte correspondieron a ECV (11% del total) lo que es igual a lo descrito por los autores mencionados. La diferencia en la frecuencia de recurrencia de la trombosis entre nuestra cohorte y la de Cervera y cols. (16% a 5 años, ECV 2.4%, isquemia cerebral transitoria 2.3%, TVP 2.1% y TEP 2.1%) se explica por el carácter prospectivo de esta última y porque 420 pacientes (42%) recibieron anticoagulación indefinida y 350 (35%) recibieron bajas dosis de aspirina12.
La trombocitopenia fue la manifestación hematológica más común (33%), con una frecuencia mayor a la publicada por otros grupos (21.4% en la cohorte eurofosfolípido, 23.4% en el Hospital Saint Tomas y 24% en la cohorte colombiana)7,9, y similar a la frecuencia observada en la cohorte latinoamericana (28%)10. En el 33% de los casos se presentó trombocitopenia grave en algún momento de la evolución lo cual es más frecuente en comparación con lo publicado por otros autores (17.5%) y probablemente se debe al número de pacientes con LES incluidos7,9,10,13.
Si bien la ECV es la manifestación neurológica más frecuente, otras pueden hacer parte de la amplia gama de afecciones asociadas al SAF, incluso ser la manifestación inicial de la enfermedad. En nuestra cohorte observamos casos de epilepsia, neuritis óptica, mielopatía, corea, síndrome de Sneddon y pseudotumor cerebri. Estas son complicaciones poco frecuentes pero devastadoras del SAF y su frecuencia es similar a las publicadas previamente9,14-16.
La frecuencia de los AAF fue similar a la reportada por Soltesz y cols. en una cohorte semejante a la nuestra: aCL IgM 59% y aCL IgG 49% vs. 87.9% y LA 59% vs. 50%17 y no difiere de los datos de las cohortes europea7 y latinoamericana10. El 28.3% de los pacientes con SAF tuvieron títulos de aCL menores a 40 unidades GPL y MPL, lo cual ha sido observado por otros grupos; Dunn y cols. observaron, en 103 pacientes de varias clínicas de anticoagulación, que sólo el 46% presentó niveles medios o altos de aCL18. Vanegas y cols.19 no observaron relación entre los títulos de aCL y el riesgo de trombosis en una cohorte de pacientes con SAF del Hospital Universitario San Vicente de Paúl de Medellín; el 82% de los pacientes con trombosis tuvo aCL IgG positivas pero sólo el 40% cursó con títulos de 40 unidades GPL o mayores. Vargas y cols observaron que el 30% de los pacientes presentó eventos clínicos con títulos bajos de aCL IgG. Estos hallazgos sugieren que en nuestra población de pacientes con SAF, títulos bajos de aCL se asocian a trombosis y realza la importancia de estandarizar las técnicas para detección de estos anticuerpos y de determinar cuáles son los valores de corte positivos para nuestra población.
El 21.95% de los pacientes con SAF primario tuvieron ANAs positivos en títulos bajos con autoanticuerpos específicos negativos; este hallazgo realza el valor discriminatorio que tienen éstos para el diagnóstico diferencial entre el SAF primario y secundario. Recientemente Veres y cols. demostraron que el 37% de los pacientes clasificados como SAF primario hacen transición a enfermedades del tejido conectivo luego de 5.2 años de seguimiento y tienen mayor probabilidad de viraje los que poseían autoanticuerpos diferentes a los AAF y los que debutaron con trombosis arterial20.
En esta cohorte se observó un mayor uso de anticoagulantes en comparación con la cohorte de Cervera y cols.12 (52 vs. 42%), pese a esto se presentó una importante frecuencia de retrombosis, ligeramente superior a la reportada en esta misma serie (21 vs. 16.4%)12 y similar a la informada por Vargas y cols.9, en pacientes colombianos (22.6%). El 68.5% de los pacientes que sufrieron un segundo episodio de trombosis venosa lo presentaron mientras tenían INR mayor o iguales a 2 y el 26% mayor o iguales a 3. Estos hallazgos son similares a los de la cohorte europea12 en la que el 54%, de los pacientes con recidivas, estaba recibiendo warfarina al momento del nuevo episodio de trombosis, 76% de ellos con INR entre 2-3, y 21% con INR mayor a 3.
La TVP se asoció a diabetes mellitus y la ECV al consumo de tabaco en el análisis univariado, pero no demostramos asociación con los títulos de aCL, presencia de LA, triple positividad y otros factores tradicionales, como la dislipidemia y la HTA. El número de eventos de trombosis y de recurrencia trombótica no fueron suficientes para hacer un análisis multivariado para detectar los factores de riesgo predictores independientes de estos desenlaces. Vargas y cols.9 encontraron que la diabetes mellitus se asoció a trombosis arterial en el análisis univariado. Cervera y cols12 no encontraron que la edad, el sexo, la historia de diabetes, HTA, tabaquismo y dislipidemia, LA y aCL IgG o IgM, se asociaran al aumento de la incidencia de ninguna manifestación clínica específica de SAF.
Son varias las hipótesis que involucran a la diabetes mellitus y al SAF. Ambas entidades se consideran anexinopatías, donde mutaciones en estas proteínas dan lugar a diversas manifestaciones clínicas21, también se han encontrado, con frecuencia en pacientes diabéticos, títulos bajos de aCL y de AAF, como los anti fosfatidilinositol y fosfatidilcolina, probablemente, relacionados con enfermedad macrovascular y mayor presencia de aCL IgG en familares de primer grado asintomáticos22; también hay estudios que demuestran disminución de la elasticidad arterial23 y alteración en la función endotelial24 en pacientes con SAF primario en igual magnitud que en pacientes diabéticos.
Pengo y cols demuestran factores de riesgo tradicionales en el 40.3% de sus pacientes con TVP y en el 49.4% de aquellos con trombosis arterial; además demuestran que la triple positividad predispone a recurrencia11.
Según Rufati y cols., la HTA y el LA son los principales determinantes del primer evento trombótico en los pacientes con AAF25; mientras que Danowski y cols encuentran que la TVP se asocia a títulos de aCL mayores a 40 unidades, hipertrigliceridemia y a la presencia de trombofilias hereditarias, y la trombosis arterial se asocia a HTA4.
Turiel y cols.3 demostraron que los niveles de aCL IgG mayores a 40 GPL son un factor de riesgo independiente para el desarrollo de trombosis en pacientes con SAF primario (OR 9.17; 95% CI 1.83-46.05).
Quintana y cols. demostraron que los pacientes con aCL persistentemente positivos tenían mayor riesgo de recurrencias trombóticas y caracterizaron tres perfles de AAF que predisponen a eventos recurrentes: LA, aCL IgG y la combinación de estos26. Vanegas y cols.19 también observaron que los títulos de aCL persistentemente positivos predisponen a trombosis.
Las diferencias de nuestros resultados con relación a las otras series, en lo que respecta a factores de riesgo asociados a desenlaces vasculares, puede explicarse por diferencias raciales, por el limitado tamaño de la muestra y por el pequeño número de eventos clínicos.
Nuestro estudio tiene varias debilidades, como el carácter retrospectivo y de corte transversal y la inclusión de un número pequeño de pacientes, todos mestizos, por lo cual no es representativo del total de la población con SAF; lo anterior no permite extrapolar los resultados a pacientes de otras etnias y países.
Las fortalezas del estudio consisten en que la cohorte tiene un seguimiento adecuado por reumatólogos con experiencia en el diagnóstico y manejo del SAF y que se incluye, hasta donde se sabe, el número más grande de pacientes colombianos con la enfermedad.
En conclusión en esta población seleccionada de pacientes colombianos con SAF, las complicaciones trombóticas fueron las más frecuentes, tanto al inicio de la enfermedad como durante su evolución. La trombosis venosa fue más frecuente y tuvo mayor tasa de recurrencia que la trombosis arterial. La trombosis venosa se asoció a la presencia de diabetes mellitus y la arterial (ECV) al tabaquismo.
Nuestros pacientes mostraron una alta frecuencia de manifestaciones "pre-SAF", trombocitopenia grave y bajos títulos de anticardiolipinas y se caracterizaron por un comportamiento agresivo con trombosis venosa recurrente, TEP, manifestaciones neurológicas graves y trombocitopenia severa.
Fuente de financiación: Recursos propios.
Referencias
1. Levine JS, Branch W, Rauch J. Te antiphospholipid syndrome. N Engl J Med 2002; 346:752-763. [ Links ]
2. Ekran D, Lockshin MD. What is antiphospholipid syndrome? Curr Rheumatol Rep 2004; 6:451.457. [ Links ]
3. Turiel M, Sarzi-Puttini P, Peretti R, Rossi E, Atzeni F, Parsons W, et al. Trombotic Risk Factors in Primary Antiphospholipid Syndrome: A 5-Year Prospective Study. Stroke 2005; 36:1490-1494. [ Links ]
4. Danowski A, Leitao de Azevedo MJ, De Souza Papi JA, Petri M. Determinants of Risk for Venous and Arterial Trombosis in Primary Antiphospholipid Syndrome and in Antiphospholipid Syndrome with Systemic Lupus Erythematosus. J Rheumatol 2009; 36:1195-1199. [ Links ]
5. Miyakis S, Lockshin MD, Atsumi D, Branco DC, Brey RL, Cervera R, et al. International Consensus Statement on an update of the classification criteria for definite Antiphospholipid Syndrome (APS). J Tromb Haemost 2006; 4:295-306. [ Links ]
6. Brandt J T, Triplett DA, Alving B, Scharrer I. Criteria for the diagnosis of lupus anticoagulants: an update. On behalf of the Subcommittee on Lupus Anticoagulant/Antiphospholipid Antibody of the Scientific and Standardisation Committee of the ISTH. Tromb Haemost 1995; 74:1185-1190. [ Links ]
7. Cervera R, Piette JC, Font J, Khamastha M, Shoendfeld Y, Camps M, et al. Antiphospholipid Syndrome. Clinical and immunological manifestations and pattern of disease expression in a cohort of 1000 patients. Arthritis Rheum 2002; 4:1019-1027. [ Links ]
8. Babikian VL, Brey RL, Coull BM, Dewitt LD, Feinberg WM, Feldmann E, et al. Te Antiphospholipid antibodies in the stroke study group: Clinical ad laboratory findings in patients with antiphospholipid antibodies and cerebral ischemia. Stroke 1990; 21:1268-1273. [ Links ]
9. Vargas F, Pinto LF, Molina J F, Donado JH, Eraso R, Tobón JA, et al. Síndrome Antifosfolípido: morbilidad y evolución de una cohorte de pacientes del Hospital Pablo Tobón Uribe de Medellín - Colombia. Rev Colomb Reumatol 2006; 13:109-119. [ Links ]
10. García-Carrasco M, Galarza C, Gómez-Ponce M, Cervera R, Rojas-Rodríguez J, Espinosa G, et al. Antiphospholipid syndrome in Latin American patients: Clinical and immunological characteristics and comparison with European patients. Lupus 2007; 16:366-373. [ Links ]
11. Pengo V, Rufatti A, Legnani G, Gresele P, Barcellona D, Erba N, et al. Clinical course of high-risk patients diagnoses with antiphopholipid syndrome J Tromb Haemost 2009; 8:237-242. [ Links ]
12. Cervera R, Khamasta MA, Schoenfeld Y, Camps MT, Jacobsen S, Kiss E. Morbidity and mortality in the antiphospholipid syndrome during a 5-year period: a multicentre prospective study on 1000 patients. Ann Rheum Dis 2009; 68:1428-1432. [ Links ]
13. Cuadrado M, Mujic F, Muñoz E, Khamastha M, Hughes GRV. Trombocytopenia in the Antiphospholipid Syndrome. Ann Rheum Dis 1997; 56:194-196. [ Links ]
14. Tanne D, Hassin-Baer S. Neurological manifestations of the antiphospholipid Syndrome. Curr Rheumatol Rep 2001; 3:286-292. [ Links ]
15. Cervera R, Asherson RA, Font J, Tikly M, Pallarés M, Chamorro A, et al. Chorea in the Antiphospholipid Syndrome: Clinical, Radiologic and immunologic characteristics of 50 patients from our clinics and the recent literature. Medicine 1997; 76:203-212. [ Links ]
16. Kovacs B, Laferty TL, Brent LH, DeHoratius RJ. Transverse myelopathy in Systemic Lupus Erythematosus: Analysis of 14 cases and review of the literature. Ann Rheum Dis 2000; 59:120-124. [ Links ]
17. Soltesz P, Veres K, Lakos G, Muszbeck L, Szegedi G. Evaluation of clinical and laboratory features of antiphospholipid syndrome: A retrospective study of 637 patients. Lupus 2003; 12:302-307. [ Links ]
18. Dunn AS, Kaboli P, Halfdanarson T, Chan H, Hubert R, Rosen S, et al. Do patients followed in anticoagulation clinics for antiphospholipid syndrome meet criteria for the disorder? Tromb Haemost 2005; 94:548-554. [ Links ]
19. Vanegas AL, Díaz J, Arango M, Velásquez GA, Toro JM, Vásquez GM. Asociación entre títulos e anticuerpos anticardiolipinas y eventos trombóticos. Revista Colombiana de Reumatología 2011; 18:88-95. [ Links ]
20. Veres K, Szodoray P, Szekanecz Z, Lakos G, Kiss E, Laczik R, et al. Clinical and immunoserological characteristics of the transition from primary to overlap antiphospholipíd syndrome. Lupus 2010; 19:1520-1526. [ Links ]
21. Hayes MJ, Longbottom RE, Evans MA, Moss SE. Annexinopahies. Subcell Biochem 2007; 45:1-28. [ Links ]
22. Uthman I, Salti I, Khamashta M. Endocrinologic manifestations of the antiphospholipid syndrome. Lupus 2006; 15:485-489. [ Links ]
23. Reitblat T, Polishchuk I, Zamir D, Isakov I, Oren S. Arterial compliance: Is it reduced in antiphospholipid syndrome? J Hum Hypertens 2006; 20:504-509. [ Links ]
24. Blum A, Simsolo C. Te antiphospholipid syndrome and endothelial function. Is Med Assoc J. 2004 Sep; 6(9):556-8. [ Links ]
25. Rufati A, Del Ross T, Ciprian M, Bertero M, Sciascia S, Scarpato S, et al. Risk factors for a first thrombotic event in antiphospholipid antibody carriers: A prospective multicentre follow-up study. Ann Rheum Dis 2011; 70:1083-1108. [ Links ]
26. Quintana G, Espinosa G, Bucciarelli S, Tássies D, Bové A, Plaza J, et al. Los valores persistentemente positivos de anticuerpos antifosfolipídicos están relacionados con la aparición de trombosis durante el seguimiento en pacientes con síndrome antifosfolipídico. Rev Colom Reumatol 2007; 14:253-259. [ Links ]