Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Reumatología
Print version ISSN 0121-8123
Rev.Colomb.Reumatol. vol.22 no.1 Bogotá Jan./June 2015
https://doi.org/10.10167j.rcreu.2015.01.003
Informe de caso
http://dx.doi.org/10.10167j.rcreu.2015.01.003
Taponamiento cardiaco por pericarditis lúpica: reporte de dos casos
Cardiac tamponade due to lupic pericarditis: report of two cases
Diana María Ronderos Boteroa,b, Daniel Gerardo Fernández-Ávilaa,b,*, María Claudia Díaz Jiméneza,b y Juan Martín Gutiérrez Dávilaa,b
a Unidad de Reumatología, Hospital Universitario San Ignacio, Pontificia Universidad Javeriana, Bogotá, Colombia
b Grupo Javeriano de Investigación en Enfermedades Reumáticas, Bogotá, Colombia
* Autor para correspondencia. Correo electrónico: danielfernandezmd@gmail.com (D.G. Fernández-Ávila).
Historia del artículo: Recibido el 4 de abril de 2014 Aceptado el 27 de enero de 2015 On-line el 5 de marzo de 2015
Resumen
La serositis es uno de los hallazgos clínicos en pacientes con lupus eritematoso sistémico. Cuando se presenta a nivel de pericardio, generalmente causa derrames pericárdicos crónicos que no generan inestabilidad hemodiná mica en el paciente. Presentamos 2 casos clínicos de mujeres con lupus con derrame pericárdico que lleva a taponamiento cardiaco, presentación inusual de esta manifestación clínica del lupus eritematoso sistémico.
Palabras clave: Lupus, Serositis, Taponamiento cardiaco.
Abstract
Serositis is one of the clinical findings in patients with systemic lupus erythematosus. When is present generally causes chronic pericardial effusions and not generate hemodynamic instability in the patient. We present two cases of women with lupus with pericardial effusion leading to cardiac tamponade, unusual presentation of this clinical manifestation in systemic lupus erythematosus
Keywords: Systemic lupus erythematosus, Serositis, Cardiac tamponade.
El compromiso cardiaco por lupus eritematoso sistémico (LES) oscila entre 15 y 50% de los pacientes con esta enfermedad1-3, sin embargo, en estudios anatomopatológicos el compromiso llega hasta el 80%4. El compromiso en pericardio comprende de 26 a 54%5-7, aunque datos derivados de la revisión estructurada de la literatura de Zapata et al., documentan que el compromiso oscila entre 40 y 80%4, de los cuales, solo el 25% son sintomáticos3,4, por lo que durante el transcurso de la enfermedad los pacientes pueden cursar con pericarditis crónicas y efusiones pericárdicas sin tener manifestaciones clínicas6. Las complicaciones de la pericarditis como el taponamiento cardiaco son infrecuentes4, con una prevalencia reportada entre 1 y 2,5%8.
En el sistema cardiovascular el pericardio es el tejido más comúnmente afectado, produciendo pericarditis crónica, aguda y taponamiento cardiaco, seguido del miocardio, endocardio, sistema de conducción y vasculatura9. Dado que el taponamiento cardiaco, como manifestación del lupus, es una entidad fatal si pasa inadvertida10, debe sospecharse y realizar estudios minuciosos para hacer un diagnóstico temprano y brindar un tratamiento oportuno11,12. Se presentan los casos de 2 pacientes con derrame pericárdico en el contexto de lupus activo.
Presentación de casos
Caso 1
Mujer de 36 años de edad, con antecedente de LES diagnosticado hace 3 años, sin manejo previo, quien consultó, por primera vez a nuestra institución, por cuadro de dolor abdominal epigástrico irradiado a región dorsal alta, diarrea acuosa, edema en miembros inferiores, ictericia y disnea. Al examen físico se encontró con tensión arterial de 100/60 mmHg, frecuencia cardiaca: 120 por minuto, frecuencia respiratoria: 23 por minuto, afebril deshidratada; ruidos cardiacos rítmicos velados, ruidos respiratorios con hipoventilación bibasal, abdomen ligeramente distendido sin irritación peritoneal y el resto del examen físico sin alteraciones.
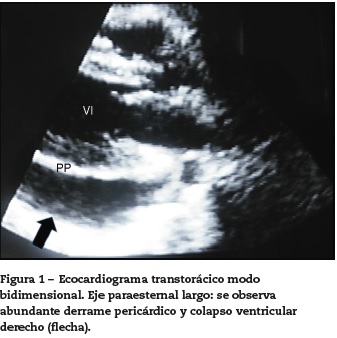
Se sospecha pancreatitis aguda, se solicitan paraclínicos con lipasa de 33.333 ul/L, se confirma diagnóstico de pancreatitis severa APACHE 8. Se inician estudios para determinar etiología, sin embargo, al día siguiente del ingreso la paciente presenta deterioro hemodinámico con disnea y dolor torácico pleurítico. El EKG con bajo voltaje y taquicardia sinusal, documentándose en radiografía de tórax cardiomegalia severa que sugería derrame pericárdico y derrames pleurales bilaterales. Se solicita ecocardiograma el cual documenta signos de taponamiento cardiaco dado por disminución del llenado ventricular derecho (fig. 1).
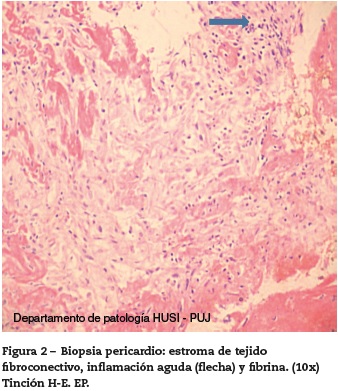
Se lleva a la paciente a ventana pericárdica dado el compromiso hemodinámico y se inicia metilprednisolona a dosis de 1 g/día, por 3 dosis. En cirugía se evidencia pericardio de características normales, se obtienen 600 cc de líquido seroso, Gram sin gérmenes, ZN negativo y cultivos negativos. El citoquímico evidenció polimorfonucleares sin tener diferencial y reporte de biopsia de pericardio con inflamación aguda y fibrina (fig. 2).
La paciente ingresa en UCI y durante la evolución cursa con actividad lúpica severa dada por ascitis, derrame pleural bilateral, falla renal con requerimiento de terapia de remplazo renal, documentándose, además, anemia hemolítica, trombocitopenia, leucopenia, piuria, hematuria, hipocomplementemia y anti-DNA 1/320 diluciones, con una puntuación en la escala SLEDAI de 24 (tabla 1).
Presenta, además, coagulopatía, hiperbilirrubinemia a expensas de la indirecta configurando cuadro de disfunción orgánica múltiple. Su evolución es tórpida, cursando con hipocalcemia severa, requerimiento de soporte ventilatorio, hemodinámico, finalmente, choque refractario al manejo médico y muerte a las 72 horas del ingreso.
Caso 2
Mujer de 24 años de edad, con antecedente de LES diagnosticado hace 7 años, manejada con cloroquina 150mg/día, azatioprina 50 mg/día y prednisolona 5 mg/día, con antecedente de hospitalización reciente por TEP de probabilidad intermedia, diagnosticado con gamagrafía ventilación perfusión, razón por la cual se anticoaguló.
Consulta por cuadro de 3 días de disnea de inicio súbito, asociado a dolor torácico pleurítico de intensidad 10/10 en hemitórax izquierdo. Al examen físico presenta tensión arterial: 110/80 mmHg, frecuencia cardiaca: 120 por minuto, frecuencia respiratoria: 28 por minuto, temperatura: 37 °C, SaO2 90% con oxígeno por cánula nasal a 2 L/min. A la auscultación se aprecian ruidos cardiacos rítmicos sin soplos, no velados, con hipoventilación bibasal, sin otros hallazgos relevantes.
Se sospecha TEP por lo que continuó anticoagulación plena. Ante esta sospecha se realiza electrocardiograma con taquicardia sinusal, bajo voltaje y eje derecho. La radiografía de tórax evidenció derrame pleural bilateral sin poder identificar parénquima de manera adecuada, sin otras alteraciones. Para visualizar parénquima se realizó TAC de tórax la cual no mostró alteraciones en parénquima pulmonar pero sí derrame pleural derecho, el cual no pudo ser drenado por radiología por su escaso volumen; se evidenció, además, gran efusión pericárdica.
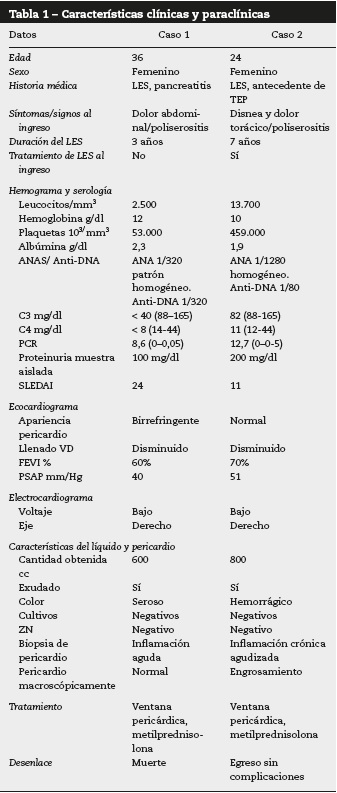
La paciente permaneció estable, se realizó ecocardiograma (fig. 3), el cual mostró abundante derrame pericárdico asociado a inadecuado llenado ventricular derecho. Dado el hallazgo de poliserositis, se solicitan paraclínicos para descartar actividad de la enfermedad, encontrando hipocomplementemia, proteinuria en rango no nefrótico, lo cual puntuaba para actividad severa SLEDAI de 11 a pesar del manejo médico previo (tabla 1).
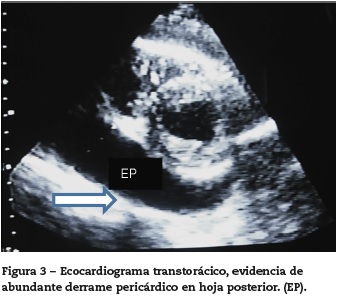
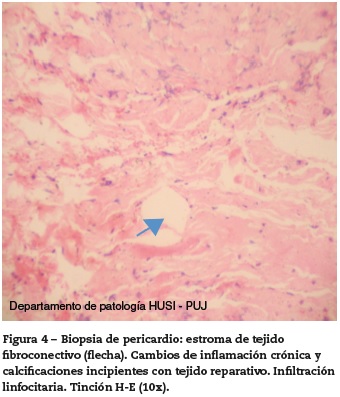
Es valorada por Reumatología y se inician bolos de metil-prednisolona durante 3 días. Por parte del servicio de cirugía de tórax se consideró alto riesgo de inestabilidad hemodinámica por lo que se programó para ventana pericárdica a la cual es llevada a los 5 días de su estancia hospitalaria. Se evidenció pericardio engrosado con paredes irregulares, se obtuvo 800 cc de líquido hemorrágico, celularidad de predominio linfocitario y Gram sin gérmenes. Las tinciones para gérmenes comunes, atípicos, hongos y micobacterias fueron negativas. La biopsia evidenció inflamación crónica activa con abundante fibrina (fig. 4). Se ajusta el manejo con azatioprina 50mg cada 12 horas y continuó con cloroquina 150 mg/día y prednisolona 1 mg/Kg/ día. Adecuada evolución dada por resolución de la disnea y estabilidad hemodinámica por lo que se da egreso a los 15 días sin complicaciones.
Discusión
Presentamos dos casos de derrame pericárdico en el contexto de pacientes con lupus activo, uno de los cuales presenta desenlace fatal, probablemente por su asociación con pancreatitis aguda.
Comparando nuestros casos con los reportados en la literatura, la edad de presentación fue de 36 y 24 años, respectivamente, similares a la edad de presentación encontrada en la literatura. El tiempo de evolución de la enfermedad en nuestras pacientes fue de 3 y 7 años y en la literatura varía entre 4,1 y 6,2 años13,14.
Es llamativa la variabilidad clínica en cada una de las pacientes de nuestros casos. En el caso número uno la paciente cursaba con 3 años de evolución, no venía con tratamiento previo, la instauración fue aguda y severa, llevando a la paciente a disfunción orgánica múltiple y deceso en los primeros 3 días. En nuestra búsqueda encontramos solamente un caso similar15, donde una mujer de 14 años cursó con taponamiento cardiaco como primera manifestación del LES, asociado a disfunción orgánica múltiple y muerte después de 3 días. A diferencia de este caso nuestras pacientes no cursaron con taponamiento cardiaco como primera manifestación de la enfermedad y en el caso de la paciente que fallece, esta presentaba una comorbilidad grave (pancreatitis aguda).
El taponamiento cardiaco secundario a pericarditis lúpica se desarrolla cuando la presión dentro del pericardio supera la presión en las cavidades cardiacas con subsiguiente reducción del llenado diastólico, caí da en el gasto cardiaco y presión arterial13. El volumen requerido para la aparición de taponamiento y su manifestación clínica es variable, depende de la tasa de acumulación del mismo y de la distensibilidad pericárdica, lo cual confiere un riesgo independiente a cada paciente13. Amir Gómez et al., en una revisión sobre manifestaciones cardiovasculares en LES, describen que si el taponamiento cardiaco es de instauración aguda el derrame puede ser de escaso a moderado6. Esto podría explicar por qué en el caso número 1 se presentó taponamiento cardiaco con menor volumen de líquido en el contexto de una pericarditis aguda.
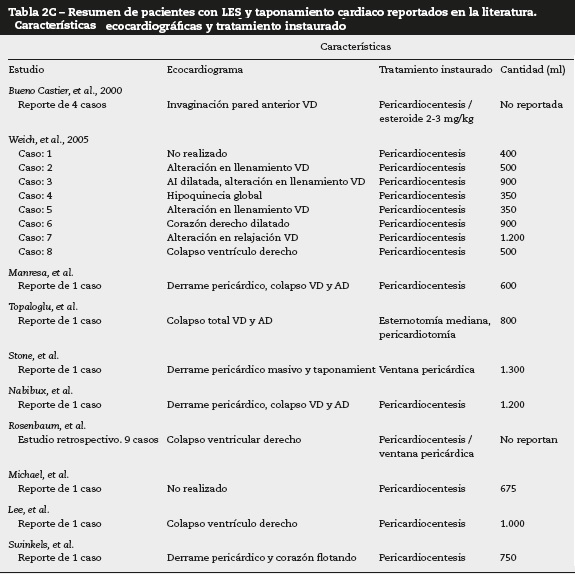
La manifestación clínica de nuestros casos es clásica al igual que se reporta en la literatura8,9,11.Enlatabla2se comparan las características clínicas y demográficas de algunas pacientes reportadas1,5,8-11,13,15,16. El ecocardiograma es el examen de elección para realizar el diagnóstico y para identificar hallazgos como colapso ventricular o auricular derecho, los cuales reflejan disfunción ventricular e inestabilidad hemodinámica. Dichos hallazgos obligaron a llevar a nuestras pacientes a derivación por medio de ventana pericárdica, como parte del manejo las pacientes recibieron esteroides a dosis altas que no fueron suficientes para controlar la actividad de la enfermedad. José María Manresa et al., reportan en su estudio que hasta el 20% de los pacientes pueden no responder adecuadamente al tratamiento con esteroide5.
En la mayoría de los casos reportados al igual que en nuestras pacientes se describe taponamiento cardiaco asociado a actividad lúpica. Es raro y no hay muchos reportes de casos en que se presente instauración de taponamiento cardiaco en una segunda ocasión, después de haber superado una crisis lúpica y de tener un tratamiento adecuado como fue el caso número 2. Hay solo un caso reportado en la literatura con estas mismas características10, el cual describe una mujer de 32 años que cursó con taponamiento cardiaco después de haber remitido una crisis lúpica. Se resalta así la variabilidad que esta entidad puede tener.
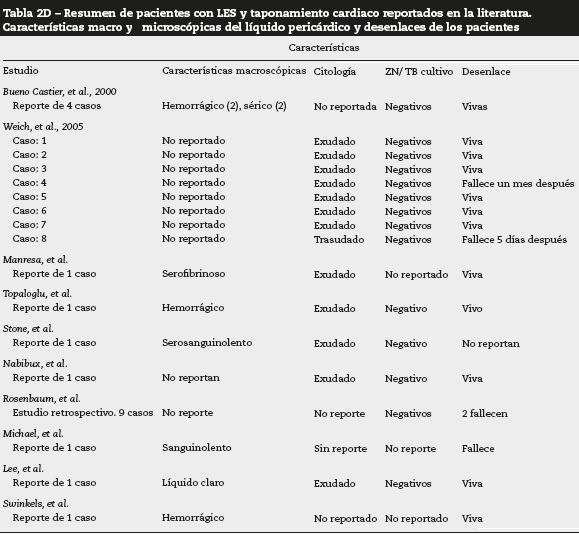
Teniendo en cuenta que los factores desencadenantes del taponamiento cardiaco no están claramente establecidos, se realizó una búsqueda en la literatura, encontrando solamente algunos estudios retrospectivos que describen factores de riesgo asociados al desarrollo de taponamiento como derrame pleural, anemia hemolítica, falla renal y bajos niveles de C4 séricos13. Nuestras 2 pacientes presentaban derrame pleural, consumo de C4, y en el caso número 1 anemia hemolítica. En las tablas 2A-2D se resumen las principales características clínicas de los casos reportados en la literatura de taponamiento cardiaco por derrame pericárdico en el contexto de LES.
Debido a la baja frecuencia del taponamiento cardíaco y LES, existen pocos trabajos que analicen las características del líquido pericárdico, la mayoría son exudados serohemáticos o hemorrágicos al igual que nuestros casos. Lo importante en todos los pacientes es descartar compromiso infeccioso asociado, más aún, teniendo en cuenta que se trata de casos de pacientes que reciben tratamiento inmunomodulador.
Se espera que este reporte de casos alerte al clínico sobre el impacto que tiene el taponamiento cardiaco, el amplio espectro y los escenarios de presentación, teniendo en cuenta que este puede darse en cualquier momento de la enfermedad10 e incluso ser la primera manifestación del lupus8,9,11,15.
Conclusión
Presentamos 2 casos de taponamiento cardiaco asociado a LES, sin bien la frecuencia de presentación sintomática clínica de este hallazgo es baja, es un aspecto para tener en cuenta dentro del enfoque diagnóstico y el seguimiento de pacientes con lupus. Las características clínicas de los 2 casos presentados son similares a las reportadas en la literatura médica disponible.
Responsabilidades éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Financiación
Esta investigación no recibióninguna contribución financiera de agencias de anuncio público o de entidades con fines lucrativos.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Bibliografía
1. Weich HS, Burgess LJ, Reuter H, Brice EA, Doubell AF. Large pericardial effusions due to systemic lupus erythematosus: a report of eight cases. Lupus. 2005;14:450-7. [ Links ]
2. Doria A, Iaccarino L, Sarzi-Puttini P, Atzeni F, Turriel M, Petri M. Cardiac involvement in systemic lupus erythematosus. Lupus. 2005;14(9):683-6. [ Links ]
3. Moder KG, Miller TD, Tazelaar HD. Cardiac involvement in systemic lupus erythematosus. Mayo Clin Proc. 1999;74:275-84. [ Links ]
4. Zapata-Cárdenas A, Pinto LF, Saldarriaga C, Velásquez CJ, Márquez JD. El corazón en lupus eritematoso sistémico: revisión estructurada de la literatura. Rev Col Reumatol. 2013;20:148-54. [ Links ]
5. Manresa JM, Gutiérrez L, Viedma P, Alfani O. Cardiac tamponade as a clinical symptom of systemic lupus erythematosus. Rev Esp Cardiol. 1997;50:600-2. [ Links ]
6. Gómez-León M, Amezcua-Guerra LM. Manifestaciones cardiovasculares en el lupus eritematoso generalizado. Arch Cardiol Mex. 2008;78:421-30. [ Links ]
7. Man BL, Mok CC. Serositis related to systemic lupus erythematosus: prevalence and outcome. Lupus. 2005;14:822. [ Links ]
8. Swinkels BM, Scheffer RC, Tahapary GJ, Jaarsma W, Plokker HW, Mast EG, et al. Cardiac tamponade as the initial manifestation of systemic lupus erythematosus in a young female patient. Neth Heart J. 2007;15:71. [ Links ]
9. Topaloglu S, Aras D, Ergun K, Altay H, Alyan O, Akgul A. Systemic lupus erythematosus: an unusual cause of cardiac tamponade in a young man. Eur J Echocardiogr. 2006;7:460-2. [ Links ]
10. Stone D, Moberg P, Respicio G, Levin S, Rooney T. Pericarditis with cardiac tamponade in systemic lupus erythematosus. Development immediately following successful control of lupus flare. Lupus. 2010;19:890-1. [ Links ]
11. Lee IH, Yang SC, Kim TH, Jun JB, Jung SS, Bae SC, et al. Cardiac tamponade as an initial manifestation of systemic lupus erythematosus-single case report. J Korean Med Sci. 1997;12:75-7. [ Links ]
12. Nabibux MN, Dijkmans PA, Dijkmans BA. A swinging heart as complication of systemic lupus erythematosus. Clin Rheumatol. 2007;26:825-6. [ Links ]
13. Rosenbaum E, Krebs E, Cohen M, Tiliakos A, Derk CT. The spectrum of clinical manifestations, outcome and treatment of pericardial tamponade in patients with systemic lupus erythematosus: a retrospective study and literature review. Lupus. 2009;18:608-12. [ Links ]
14. Kahl LE. The spectrum of pericardial tamponade in systemic lupus erythematosus. Report of ten patients. Arthritis Rheum. 1992;35:1343-9. [ Links ]
15. Mohseni MM, Rogers ER. Cardiac tamponade as the initial manifestation of systemic lupus erythematosus. J Emer Med. 2012;42:692-4. [ Links ]
16. Bueno-Castier M, Neves EM, Albuquerque MF, Costa M, Klumb E, Manes F, et al. Cardiac tamponade in systemic lupus erythematosus. Report of four cases. Arq Bras Cardiology. 2000;75:446-8. [ Links ]