Introducción
Los seres humanos presentan variación genética asociada a diferencias en su secuencia de ADN, lo que conlleva que la capacidad de respuesta a los efectos terapéuticos y tóxicos a los fármacos pueda ser diferente en cada individuo1,2.La disciplina que estudia dicha variabilidad genética, a nivel individual, en respuesta a un fármaco es la farmacogenética; por su parte, la que, además, incluye las variables ambientales en la misma es la farmacogenómica3-5. Estas disciplinas tienen utilidad en la práctica clínica para predecir la respuesta individual de los pacientes a los diferentes fármacos, en especial para el tratamiento de las enfermedades autoinmunes6.La artritis reumatoide (AR) es una enfermedad autoinmune, heterogénea, crónica, que produce la inflamación en la membrana sinovial, el cartílago y el hueso; con el tiempo genera deformidad, discapacidad y deterioro de la calidad de vida7,8. Entre los medicamentos utilizados en su tratamiento se encuentran los inhibidores del factor de necrosis tumoral alfa (TNF-α) etanercept, infliximab, adalimumab, los cuales reportan un índice de respuesta del 40%, y el metotrexato (MTX), del 50%8. Esta variabilidad puede presentarse por polimorfismos genéticos de un solo nucleótido que afectan la farmacocinética y la farmacodinámica de estos medicamentos.
Una revisión sistemática del International Journal of Rheumatology en 2013 reporta que aproximadamente el 50% de los pacientes con AR en Europa interrumpen su inhibidor de TNF-α durante los primeros 5 años debido a problemas de efectividad o de seguridad del respectivo medicamento9.De forma similar, un estudio en Boston, el Brigham and Women's Hospital Rheumatoid Arthritis Sequential Study (BRASS), reporta que el 42% de los pacientes con AR informaron del abandono de su tratamiento anti-TNF-α10. En este contexto de un elevado número de pacientes que suspenden el tratamiento con anti-TNF-α, la generación de información que mejore la capacidad de predecir los pacientes que responderán a las terapias específicas sería una contribución significativa en el manejo adecuado de la AR.
Los problemas de efectividad y seguridad mencionados podrían estar asociados a la variabilidad genética de cada paciente, incluyendo las variables ambientales, las cuales se expresan por polimorfismos genéticos. De forma general, un polimorfismo genético es una variación en una secuencia determinada de ADN presente en más del 1% de los individuos de una población11. Según el Instituto Canario de Investigación del Cáncer «se clasifican en: polimorfismos en el número de repeticiones en tándem (VNTR), polimorfismos de longitud de fragmentos de restricción (RFLP) y polimorfismos de nucleótido simple (SNP, por sus iniciales en inglés)»12. En este contexto, la variabilidad genética se asocia en un 90% a los SNP, debido a la actividad de los genes dependientes de enzimas implicadas en la farmacocinética o la farmacodinámica de los fármacos utilizados en el tratamiento de la AR, afectando así su eficacia y su seguridad13.
La AR constituye un importante problema de salud pública; en los últimos años se han logrado mejores resultados de salud con la incorporación de medicamentos modificadores de la enfermedad sintéticos y biológicos. Sin embargo, se reportan problemas de variabilidad en la respuesta, lo que conlleva inefectividad y reacciones adversas en el 30-40% de los pacientes14. En este sentido, la farmacogenómica, a través del estudio de variantes genéticas de proteínas involucradas en la farmacocinética y la farmacodinamia de los medicamentos, se convierte en una forma de maximizar la eficacia y la seguridad de la farmacoterapia. En este aspecto, la farmacogenómica favorece una comprensión mejor de los mecanismos biológicos y, con ello, el desarrollo de modelos clínicos que predigan el fármaco antirreumático con mayor beneficio en cada paciente.
Se estima que, a los 10 años de evolución de la AR, casi el 80% de los pacientes presentan algún grado de limitación. El pronóstico es incierto y las lesiones, que se producen en los primeros años de enfermedad, pueden continuar a pesar de la mejoría clínica, ya que la patogénesis de estas lesiones puede diferir de la simple inflamación aguda articular15.
En Colombia se han encontrado factores de riesgo comunes con respecto al desarrollo de la AR, tales como el tabaquismo, el sexo femenino, la presencia del HLA DRB1 y el nivel educativo16.
Datos epidemiológicos
En Canadá y Estados Unidos la prevalencia oscila entre el 0,8 y el 1,1%17,18. De forma similar, en Europa los datos de pre-valencia varían entre el 0,5 y el 1%19,20. En Latinoamérica se ha reportado en el 0,45 y el 0,9%21-23. Por su parte, diversos estudios muestran que la incidencia de la AR tiende a disminuir; así, entre 1955 y 1994 la incidencia se habría reducido en un 50%24. En Europa, las tasas de incidencia informadas de AR varían entre 0,009-0,045%; en Norteamérica varían entre 0,024-0,075% en población caucásica y entre 0,09-0,89% en población india americana. Aunque no está claro, se han propuesto varios factores que permitan explicar las diferencias en la incidencia, entre los cuales se encuentran factores genéticos, ambientales y culturales25.
Etiología y patogenia de la artritis reumatoide
La AR se caracteriza por la presencia de factor reumatoide y los anticuerpos anti-péptidos citrulinados. Esto se observa en la fase inicial de la AR e implica la activación de ambas células T y B. Las citoquinas proinflamatorias, tales como TNF, IL-1 e IL-17, estimulan la inflamación y la degradación de hueso y cartílago. Sin embargo, no se produce una disminución en el número de células Treg, lo que podría contribuir a la fisiopatología de la enfermedad26.
Susceptibilidad genética
Se estima que hasta un 66% de los pacientes con AR presentan riesgo genético, el cual se ha asociado con la presencia de ciertos alelos del complejo mayor de histocompatibilidad, especialmente con el tipo HLA-DR4. En este sentido, se acepta que la enfermedad se asocia a una carga genética determinada que genera una mayor susceptibilidad a la respuesta inmune frente a un antígeno (Ag) y, con ello, se genera la inflamación de la membrana sinovial y la destrucción osteoarticular27.
De forma global, los individuos responden diferente a la farmacoterapia y ningún medicamento es 100% eficaz en todos los pacientes28, lo cual puede presentarse por una alteración en la farmacocinética y farmacodinámica de los medicamentos asociada a condiciones genético-ambientales29. En este contexto, el estudio de genes candidatos farmacogenómicos, comparado con el de genes candidatos de la enfermedad, ha sido más exitoso en la identificación y explicación de la variación de la respuesta farmacológica30, lo que ha favorecido la prescripción personalizada31. En este marco, es necesario disponer de información sistemática de la farmacogenómica de la AR, identificando polimorfismos de relevancia clínica en la respuesta y la toxicidad de inhibidores del TNF-α y metotrexato. Este tipo de información podía contribuir al desarrollo de herramientas genéticas para apoyar la decisión farmacoterapéutica y mejorar la respuesta al tratamiento de esta enfermedad. Por ello, el objetivo de este trabajo fue identificar los polimorfismos para ser utilizados en el diseño del test de secuenciación específica en pacientes con AR antes de la prescripción de infliximab, adalimumab, etanercept y metotrexato.
Métodos
Revisión sistemática en PubMed/Medline. Para identificar los estudios se realizó una búsqueda en PubMed/Medline de septiembre de 2011 a septiembre de 2016, sin límite de idioma y tipo de estudio, utilizando los términos: «rheumatoid arthritis» and «pharmacogenomic» and «polymorphisms» and «metotrexato» and «infliximab» and «adalimumab» and «etanercept». De forma específica, se contempló la combinación de palabras clave y filtros: «rheumatoid arthritis» [MeSH Terms] AND «pharmacogenomic» [MeSH Terms] AND «polymorphisms» [MeSH Terms] AND «metotrexate» [MeSH Terms] AND «infliximab» [MeSH Terms] AND «adalimumab» [MeSH Terms] and «etanercept» [MeSH Terms]. Como criterios de inclusión se definieron estudios que reportaran polimorfismos de un solo nucleótido y que afectaran la eficacia y la seguridad de infliximab, adalimumab, etanercept y metotrexato.
Extracción de datos
Los artículos que cumplieron los criterios de inclusión fueron analizados para la extracción de datos. Se creó un formato de recolección de datos que incluyó: el autor y referencia del artículo que reportaba el polimorfismo, el o los medicamentos estudiados, el tipo de estudio, el año de publicación, la población, el polimorfismo de interés, su manifestación y el reporte o no de variabilidad farmacodinámica o farmacocinética. Finalmente, cada polimorfismo identificado se buscó en Hap Map, con el fin de identificar el gen al que pertenece, junto con sus alias, el organismo, linaje, localización y exón.
Resultados
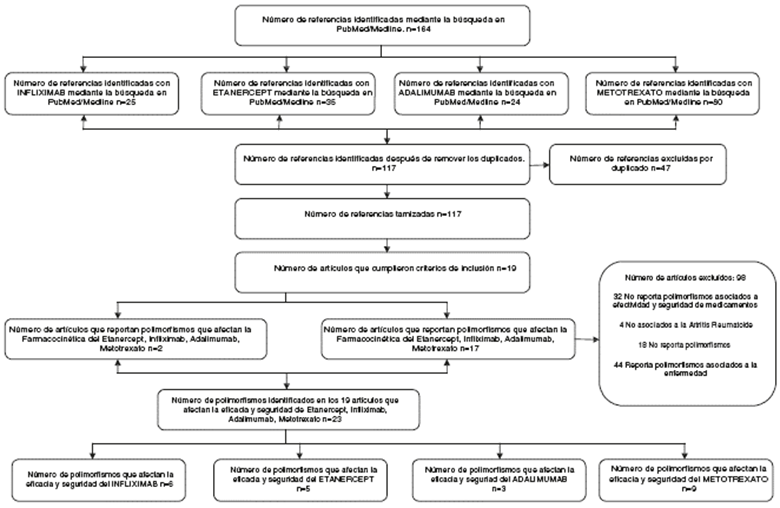
Aplicando los criterios de búsqueda definidos se encontraron 164 artículos (25 relacionados con infliximab, 24 con adalimumab, 35 con etanercept y 80 con metotrexato), de los que 47 eran repetidos, quedando 117. De este grupo de 117 artículos, 19 cumplieron con los criterios de inclusión (fig. 1). De los 19 artículos, dos reportaron polimorfismos que afectan la farmacocinética de los medicamentos infliximab, adalimumab, etanercept y metotrexato, los cuales están asociados al aumento de las concentraciones plasmáticas, mientras que 17 artículos identificaron polimorfismos que afectan la farmacodinámica de los mismos, lo que se asocia a bloqueo de receptores y se manifiesta por inefectividad de los medicamentos (tabla 1).
Tabla 1 Polimorfismos de un solo nucleótido asociados a variabilidad en la farmacocinética y farmacodinamia de metotrexato e inhibidores del factor de necrosis tumoral: infliximab, etanercept, adalimumab
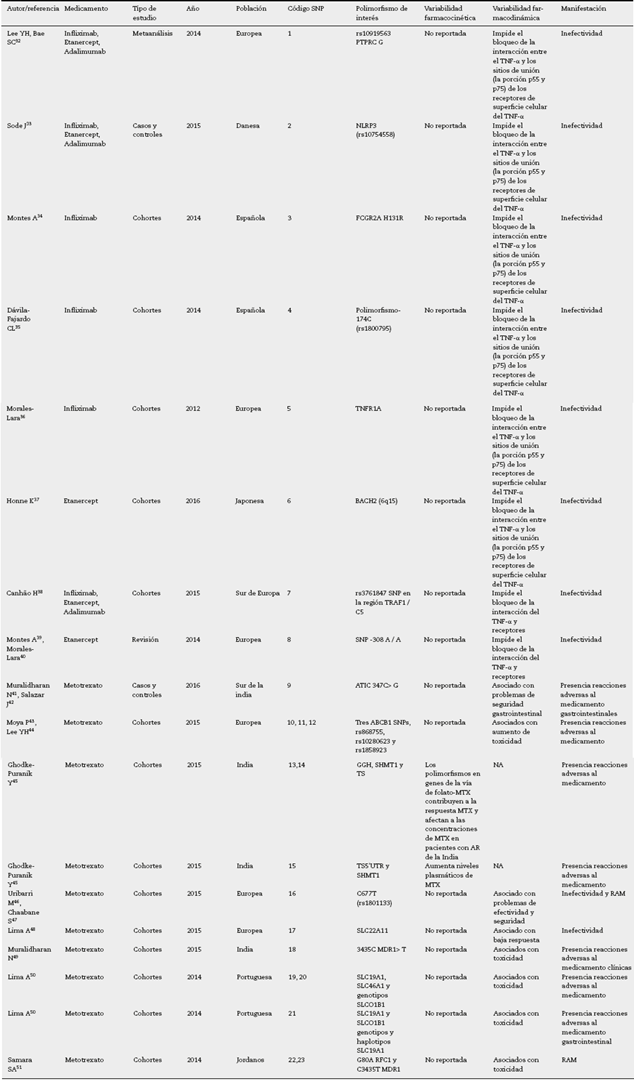
Los 19 artículos seleccionados corresponden a población europea, japonesa, jordana e india y reportan los siguientes 23 polimorfismos de un solo nucleótido: rs10919563 PTPRC G, NLRP3 (rs10754558), FCGR2A H131R, 174 C (rs1800795), TNFR1A, BACH2 (6q15), rs3761847 SNP en la región TRAF1 / C5, SNP -308 A / A, ATIC 347C> G, ABCB1 rs868755, rs10280623, rs1858923, GGH, SHMT1 y TS, TS5'UTR, C677T (rs1801133), SLC22A11, 3435C MDR1> T, SLC19A1, SLC46A1 y genotipos SLCO1B1, G80A RFC1 y C3435T MDR1 (tabla 1). De forma específica, de estos 23 polimorfismos se encontraron 6 asociados a infliximab, 5 a etanercept, 3 a adalimumaby9a metotrexato (fig. 1).
La búsqueda en la base de datos HapMap de los 23 polimorfismos identificados permitió registrar, para cada uno de ellos, el gen que lo codifica, el organismo en el que se manifiesta, su linaje, su localización o locus y el exón. En este sentido, de los 23 polimorfismos identificados se destacó (tabla 2):
Tabla 2 Localización y exones de genes identificados con polimorfismo de un solo nucleótido que afectan la efectividad y la seguridad de infliximab, etanercept, adalimumab y metotrexato
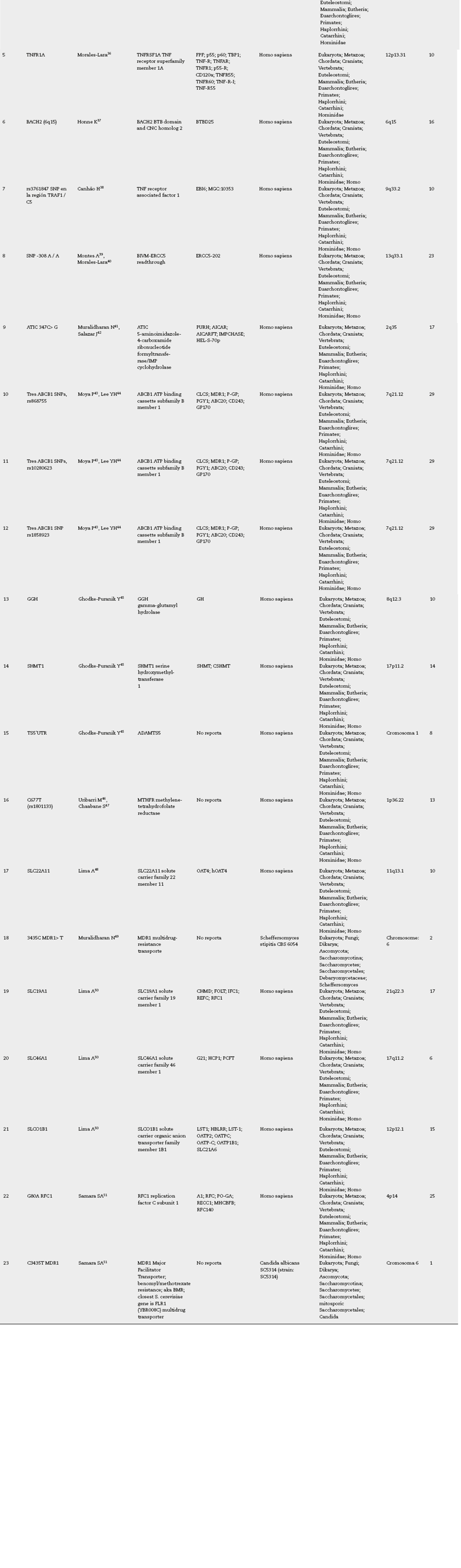
Diecinueve (82,6%) corresponden a la especie Homo sapiens.
En la secuencia del polipéptido, las regiones que se traducen a aminoácidos provienen principalmente del exón 10 (5 polimorfismos), del exón 29 (3 polimorfismos) y del exón 17 (2 polimorfismos).
El gen SLC (de diferentes familias genéticas) se encontró asociado a 4 polimorfismos, mientras que el ABCB1 (ATP binding cassette subfamily B member 1) se encontró asociado a 3 de los 23 polimorfismos y el gen MDR1 a 2 polimorfismos.
Discusión y conclusiones
En la AR, medicamentos como el metotrexato y los inhibidores del TNF-α como infliximab, adalimumab, etanercept son muy importantes para lograr la remisión de los pacientes; sin embargo, la variabilidad genética de los individuos conlleva que la capacidad de respuesta y toxicidad a estos medicamentos sea diferente y que se reporten índices inferiores al 60%8. La farmacogenómica trata las posibles asociaciones de polimorfismos genéticos con respuestas a los fármacos, es una rama de la ciencia médica que está aún en su fase inicial y requiere más tiempo para demostrar resultados positivos, así que depende de una buena articulación entre el sector investigativo, la legislación, las farmacéuticas y las instituciones de salud para que en un futuro las medicinas se desarrollen en beneficio de mejorar las condiciones de salud y los costes de tratamientos en pequeños grupos objetivo; de igual manera, no se debe dejar de lado el valor de las variables no-genéticas en el progreso de una enfermedad, como la edad, el género, la dieta y el estilo de vida, que también son claves en la respuesta a una terapia.
La relevancia de este estudio consiste en brindar la posibilidad de aplicar la investigación de genes candidatos seleccionados por su importancia biológica, ya sea en la cinética o por su relación en la acción farmacológica, en la identificación de individuos con riesgo de experimentar efectos adversos o con probabilidad de ser resistentes al tratamiento. Por ello, se espera que la información generada sea susceptible de ser utilizada en el diseño de test de secuenciación específica, contribuyendo a identificar la mejor opción terapéutica (mayor efectividad y seguridad) en pacientes con AR18.
En el tratamiento de la AR, la posibilidad de asociar ciertos polimorfismos con la eficiencia del tratamiento, reduciendo los efectos adversos del uso de un medicamento, puede ser de gran valor tanto para el paciente como para la práctica médica y para el aspecto económico de esta1. Los resultados obtenidos con la presente revisión sistemática son una base para el diseño del test de secuenciación específica en pacientes con AR antes de la prescripción de infliximab, adalimumab, etanercept y metotrexato; de aquí la importancia de diseñar y validar con estudios multicéntricos test genómicos específicos que contribuyan a una prescripción personalizada para mejorar la efectividad y la seguridad de los tratamientos con estos medicamentos y lograr disminuir costos en la atención en salud. La identificación de los 23 polimorfismos de relevancia clínica obtenidos con la revisión son muy importantes para el diseño de test genómicos; sin embargo, es necesario incluir en los estudios multicéntricos, durante la secuenciación exómica, otros genes antes de validar y estandarizar un test de uso en la práctica clínica.











 text in
text in