Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista MVZ Córdoba
versión impresa ISSN 0122-0268versión On-line ISSN 1909-0544
Rev.MVZ Cordoba v.11 n.1 Córdoba ene./jun. 2006
REVISION DE LITERATURA
DIARREA VIRAL BOVINA: PATOGÉNESIS E INMUNOPATOLOGÍA
BOVINE VIRAL DIARRHEA: PATHOGENESIS AND INMUNOPATHOLOGY
Iang Rondón
Universidad de Los Llanos. Facultad de Medicina Veterinaria y Zootecnia. Instituto de Investigaciones de La Orinoquía Colombiana. Villavicencio, Colombia. Correspondencia: iangrondon@yahoo.com.mx
RESUMEN
La diarrea viral bovina (DVB) representa un problema de ámbito mundial que causa considerables pérdidas tanto en ganado de carne como lechero, afectándolo de diversas formas las cuales están supeditadas a la edad del animal, estado inmunológico y momento de la gestación en el que se produce la infección. La DVB es causada por un virus ARN, género Pestivirus, familia Flaviviridae, el cual ha sido clasificado en 2 biotipos (citopático y no citopático) según su comportamiento en células de cultivo y en 2 genotipos (I y II) basados en su secuencia genética. Dependiendo de las cepas infectantes se presenta un cuadro clínico particular variando en severidad desde una forma subclínica, pasando por la forma clínica e incluso produciendo la fatal enfermedad de las mucosas o causando efectos deletéreos sobre el feto. A pesar de que en nuestro medio ya existen estudios sobre esta entidad, la implementación de metodologías diagnósticas constituye una limitante para el manejo de la misma. La presente revisión se enfoca en la patogenia e inmunopatología de la DVB.
Palabras clave: Pestivirus, biotipos citopático y no citopático, enfermedad de las mucosas.
ABSTRACT
Bovine viral diarrhea (BVD) represents a problem of worldwide causing considerable losses so much in meat livestock as in dairy herds, affecting it in diverse ways, which are subordinated to the age of the animal, immunologic state and moment of gestation, in which the infection takes place. BVD is caused by RNA virus, gender Pestivirus, family Flaviviridae, which has been classified in 2 biotypes (cytopathic and non cytopathic) according to its behavior in cultivation cells and in 2 genotypes (I and II) based on its genetic sequence. Depending on the infectious strains a square clinical matter is presented, varying in severity from a subclinic form, going by the clinical form and even producing the fatal disease of the mucous ones (MD) or causing deleterious effects on the fetus. Although studies already exist in our environment on this entity, the implementation of diagnostic methodologies constitutes an obstacle for the handling of the same one. This review is focused on pathogenyty and inmunopathology of the BVD.
Key words: Pestivirus, cytopathic and non cytopathic biotypes, mucosal disease.
INTRODUCCIÓN
La presencia del virus de la diarrea viral bovina (VDVB) en Colombia data de 1975, año en el cual un lote de novillas holstein, importadas de Holanda, desarrolló el cuadro clínico de enfermedad de las mucosas (EM), diagnóstico que fue confirmado por el gobierno Holandés (1). En 1996 se demostró en Colombia por primera vez la presencia de animales inmunotolerantes, persistentemente infectados (PI) por VDVB (2). El VDVB es reconocido como un agente etiológico de importancia en problemas de índole abortivo de ganado bovino en Colombia (3).
El VDVB es un miembro del género Pestivirus, familia Flaviviridae (4,5). Dentro de este mismo género se encuentra el virus de la enfermedad de las fronteras de ovinos y la peste porcina clásica (PPC) (6) con los cuales se encuentra antigénica (7) y genéticamente relacionados (8). Los Pestivirus pueden cruzar barreras de hospederos de diferente especie e infectar otras especies del orden Artiodactyla (9,10). El VDVB también infecta ganado de pezuña hendida como cerdos y ovejas (11,12). El VDVB puede infectar el cerdo y los anticuerpos contra este pueden interferir el diagnóstico de la PPC (11). Hay limitada evidencia de infecciones humanas de carácter diarréico con un pestivirus que esté serológicamente relacionado con el VDVB (11).
Existen 2 biotipos del virus: el citopático (cp) y el no citopático (ncp) (13,14) según su comportamiento en cultivos celulares (15), y por el reordenamiento genómico del gen no estructural p125/p80 (7), donde en unos no se obtiene el efecto visible (citopático) en células (ncp) (Fig. 1) y en otros se producen efectos visibles (cp) en forma de vacuolización citoplasmática mediante un mecanismo apoptótico (16, 17, Figura 2). Los virus ncp presentan afinidad por células linfocitarias mientras que los virus cp infectan de manera predominante células epiteliales (2,18).
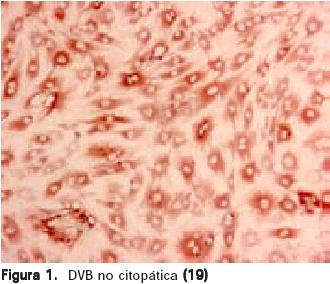
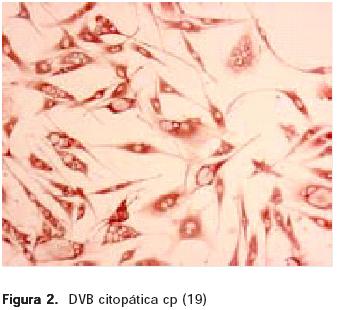
El VDVB puede ser segregado en 2 genotipos: tipo I (DVB - I) y tipo II (DVB - II) (20-22) [pestivirus tipo 1 y tipo 4 respectivamente, según la nueva división propuesta de los pestivirus] (20, 22, 23).
PATOGÉNESIS
Después del contacto con membranas mucosas de la boca o nariz, la replicación ocurre en células epiteliales con una predilección por las tonsilas palatinas, especialmente células epiteliales de la cripta (11). El virus presenta tropismo por células mitóticamente activas como: linfocitos, fagocitos mononucleares y células epiteliales (24). Se ha especulado que el biotipo cp se replica en la mucosa nasal en títulos más altos que el biotipo ncp, resultando en una eficiente diseminación en animales susceptibles (20). La replicación comienza con la adhesión a la membrana plasmática y penetración en la célula, parece ser que el receptor específico es una proteína de superficie de 50kD de las células, por mediación de la proteína de envoltura E2 (24). Además, ocurre fusión de la envoltura con la membrana endosomal - dependiente de pH -, y el virus ingresa al citoplasma mediante endocitosis mediada por receptor y libera su genoma en el citosol (25,26). La diseminación ocurre a través del virus libre en el suero o leucocitos infectados con el virus, particularmente linfocitos, monocitos, linfoblastos circulantes y células precursoras de macrófagos (20). Por otra parte, se ha determinado un bajo nivel de expresión de moléculas de alfa y beta tubulina, indicando aberraciones potenciales en la división celular, al igual que bajos niveles de expresión de los genes que codifican proteínas involucradas en la producción de energía y en la iniciación de la transducción de proteínas dependientes de cap. (27).
PATOGÉNESIS DE LA INFECCIÓN AGUDA
La forma aguda se presenta en animales seronegativos, en especial animales entre 6 y 24 mese de edad (1) y es causada, en su mayoría, por virus DVBncp (28). Puede afectar el sistema respiratorio y digestivo, resultado de la difusión activa del virus (29). La infección secundaria o mixta con otros patógenos es de presentación común (29,30). Se ha demostrado que el subtipo Id (VDVB genotipo I subtipo d) induce enfermedad respiratoria primaria (20). Se le ha atribuido un efecto sinérgico con el virus sincitial respiratorio bovino (31).
INFECCIÓN INTRAUTERINA - Efecto del virus sobre la fertilidad
Las vacas seronegativas que reciben semen de toros PI seroconvierten 2 semanas después de la inseminación o monta (1). Los toros PI son generalmente infértiles (1) o producen semen de calidad reducida (1, 32). La eliminación del virus en el semen de toros con infección aguda se extiende más allá del periodo de viremia, como consecuencia de la replicación local en vesículas seminales y próstata (1).
La infección experimental de novillas produce ovaritis prolongada (33), lo que conlleva a una disfunción ovárica (1). La alteración del medio ambiente uterino durante la fecundación o un efecto directo sobre los gametos se proponen como respuestas (1, 34). Por otra parte, también se ha comunicado que la infección con VDVB incrementa significativamente el intervalo entre ciclos ovulatorios y la progesterona postovulatoria (35). También se ha indicado que el elevado nivel de cortisol puede suprimir la liberación de hormona luteinizante y, alternativamente, la afección de los folículos preovulatorios puede resultar en reducida esteroidogénesis (1).
El embrión bovino es susceptible a infección con VDVB dentro de las 2 semanas de incubación (emergencia desde la zona pelúcida) (36). La ausencia de infección viral del oocito bovino ha sido atribuida a una barrera física a la entrada viral presentada por la zona pelúcida (37). La zona pelúcida no garantiza que los oocitos se encuentren libres de VDVB (38) y se han propuesto a su vez dos rutas de acceso al oocito: el VDVB puede ganar acceso directo dentro de la piscina primordial, pues allí el oocito es metabólicamente activo y no ha completado la deposición glicoproteica requerida para formar la zona pelúcida. La segunda ruta es a través de las células del cumulus, susceptibles a infección (38, 39). En ese mismo sentido se destaca la presencia de poros en la zona pelúcida de tamaño suficiente para permitir el paso de virus tales como el VDVB (45-55nm) y el herpesvirus bovino tipo-1 (180-200nm), demostrándose que en todos los estados de desarrollo embrionario más del 96% de los poros poseen el tamaño necesario para la entrada viral (40). Probablemente comienza a ser susceptible a la infección después de la implantación a los días 19-20 post-concepción y/o al desarrollo de cotiledones fetales alrededor del día 30 post-concepción (32).
Malformaciones
El VDVB es capaz de cruzar la placenta así como la barrera hematoencefálica fetal, produciendo diversas lesiones en el sistema nervioso central (principalmente cerebelo); la severidad en las lesiones se incrementa con la edad del feto al momento de la infección (41) (Figura 3). También se ha reportado deformación esquelética (miembros posteriores, frontales doblados, braquignatismo mandibular, alopecia y anormalidades en cabeza y mandíbula) (32, 42) (Figura 4).
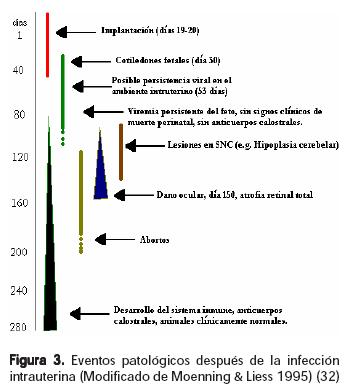
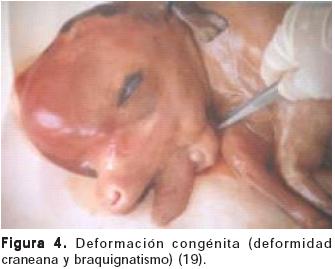
Mecanismo patogénico
Gran parte de la patogenicidad del VDVB, puede corresponder al proceso descrito en el año de 1991 para la enfermedad de las fronteras en ovinos (43). Este describe una afección en la glándula tiroidea fetal que resulta en niveles hormonales bajos de T3 (triyodotironina) y T4 (tiroxina); dicha deficiencia afecta, adversamente, la concentración de 2’, 3’- nucleótido cíclico -3’- fosfodiesterasa, una enzima esencial para la mielinización normal (afectando procesos en los oligodendrocitos). Igualmente, la hipotética alteración tiroidea afectaría el desarrollo esquelético.
PATOGÉNESIS DE LA ENFERMEDAD DE LAS MUCOSAS (EM)
La EM requiere una infección persistente congénita con virus biotipo ncp y una subsecuente superinfección con virus biotipo cp (44 – 46, 15). En bovinos la EM se genera cuando animales PI con una cepa ncp son superinfectados con una cepa cp de origen exógeno o generada de cambios genéticos o recombinación del ARN de las cepas ncp residentes (47, 20) principalmente por inserción de secuencias celulares o rearreglos genómicos (48), esto suele ocurrir entre los 6 a 24meses de edad (42) (Figura 5).

Animales persistentemente infectados (PI)
La infección fetal con VDVB puede resultar en el nacimiento de ganado inmunotolerante a DVB con una infección persistente inaparente (49). Los animales PI resultan por la infección fetal con DVBncp durante el primer trimestre de gestación (38, 50) dado que el sistema inmune fetal infectado con virus de la DVBncp antes del día 125 de preñez, no reconoce el VDVB como agente infeccioso o foráneo (29), además la mayor expansión de órganos linfoides fetales y sus poblaciones leucocitarias ocurre en el tercer trimestre de gestación (51).
Solo el biotipo ncp del VDVB ha sido reportado capaz de establecer una infección persistente en el feto (44, 51).También se propuso propusieron que la capacidad del virus de la DVBncp y DVBcp para establecer la infección persistente está relacionada con diferencias en la habilidad de inducir interferón (IFN) (32). Aunque se cree que la multiplicación considerable del virus genera diversidad, no se han detectado cambios genéticos en virus aislados en diferentes momentos del mismo animal (6). Algunos investigadores han demostrado que los animales PI estabilizan las cepas del VDVB guiando a cepas especificas del rebaño, lo cual es contrario al dogma que las infecciones agudas favorecerían variantes del virus que pueden escapar a la respuesta inmune (6).
INMUNOPATOLOGÍA
Un aspecto importante de la infección con VDVB es la aparente afinidad del virus por el sistema inmune (53) y la inmunosupresión es una de sus principales características (29, 12, 54). El VDVB parece inducir respuestas mediadas por células T y B (55); existiendo una distinción entre respuestas humorales y mediadas por células, lo que sugiere la existencia de subpoblaciones de linfocitos T ayudadores 1 (Th1) y Th2 en la regulación de las respuestas inmunes especificas dirigidas contra el VDVB (7). Esto puede deberse a la afección de la función de células presentadoras de antígeno (APC: antigen presenting cells), llevando a una reducción en la habilidad para estimular respuestas de las células T (50).
Estudios in vitro con VDVB, han demostrado que la infección de monocitos o macrófagos causa la síntesis de citoquinas que pueden ser responsables de la reducida habilidad para estimular respuestas de células T a antígenos específicos y mitógenos; por tanto es posible que la inmunotolerancia al VDVB sea una consecuencia de la infección de las células APC (50).
Se ha demostrado que el biotipo DVBncp induce en animales, experimentalmente, una respuesta primaria de anticuerpos significativamente más rápida y superior que su biotipo homólogo DVBcp, indicando que esta es dependiente del biotipo de la cepa envuelta (7).
Algunos investigadores especulan que el biotipo puede jugar un papel importante en la distribución del virus en los tejidos durante el curso de la infección y su tropismo es dependiente del biotipo, sugiriendo que el biotipo cp esta restringido al tejido linfoide asociado al intestino, mientras el ncp se distribuye en el tracto respiratorio, células sanguíneas y órganos asociados con el tejido hematopoyético y que tales diferencias se limitan a mecanismos regulatorios similares a los ejercidos por las células Th1 y Th2 (56).
En estudios acerca de la depleción linfocítica especifica causada por VDVB, se pudo indicar un papel importante de las células T CD4+ pero no de células T CD8+, lo cual indica una actividad citotóxica restringida del complejo mayor de histocompatibilidad (MHC: Major Histocompatibility Complex) clase II de las células T (57). Se ha sugerido que las células T CD4+ juegan un papel decisivo en el establecimiento de la memoria inmune al VDVB (7).
En algunos trabajos se ha podido establecer que monocitos ex vivo de animales PI fueron capaces de estimular las células T CD4+ de memoria permanentes, esto implica que las APC pueden tomar antígeno del VDVB exógeno, procesarlo vía endosomal y presentar los péptidos resultantes en asociación con moléculas MHC clase II. Los monocitos de animales PI fueron capaces de estimular respuestas de las células T CD8+ restringida a MHC clase I en células T CD8+ aisladas de ganado inmune a DVB, lo que sugiere que las células APC de animales PI, no están comprometidas en la habilidad para estimular una respuesta inmunitaria de células T restringida a MHC clase I y que el VDVB no ejerce un efecto supresor sobre la vía endógena de procesamiento del antígeno (50).
Igualmente, se ha destacado la depleción de células T CD4+ y CD8+ in vivo (57). De manera similar, se ha observado que anticuerpos pasivos pueden proteger contra infección transitoria y aguda con VDVB (58), indicando que las células T CD4+, son el principal componente de la recuperación e inmunidad de animales al VDVB.
El componente CD4+ de la respuesta celular al virus se caracteriza por altos niveles de IL-4 (IL: interleuquina) y factor de crecimiento de células B, y niveles relativamente bajos de IL-2 e interferón gamma (IFN-g); mientras el componente CD8+ es más variable y posee niveles más altos de IL-2 e IFN-g pero no de IL-4; soportando que las células CD8+ son capaces de actuar como efectores contra células infectadas con el virus mientras las células CD4+ pueden proveer ayuda para la producción de anticuerpos neutralizantes capaces de limitar la diseminación del virus (59).
El potencial inmunogénico de las proteínas vírales (glicoproteínas) aún no ha sido dilucidado. La inmunización con virus vivos o inactivados desencadena la producción de anticuerpos contra numerosas proteínas vírales (60, 61) y se han relacionado algunas proteínas, E2 y NS3, como inmunodominantes (62).
Se podría hipotetizar que las diferencias en el modo de interacción de los biotipos del VDVB con las células del hospedero, independiente del tropismo tisular, son el origen de la variación en la frecuencia de células que respondan específicamente a la proteína NS3 (7, 48), esto aunado a que los mecanismos de defensa son efectivos contra el biotipo DVBcp y no contra DVBncp (44). Las otras glicoproteínas, E1 y ERNS, no desencadenan la producción de anticuerpos que neutralicen eficientemente el virus (63).
La apoptosis, el IFN y las citoquinas son importantes mecanismos de defensa que actúan a nivel de células hospederas como mecanismos antivirales humorales (48). Por lo tanto es predecible que el virus desarrolle mecanismos de evasión o inhibición de los procesos desencadenados a nivel celular previniendo la apoptosis ó subvirtiendo las respuestas al IFN. Estas estrategias incluyen modulación de las vías de Bcl-2/Bax, interferencia de caspasas, o inhibición de la vía PKR/ARNasa L (48).
Existe una relación entre el IFN y la apoptosis, pues se ha documentado que el IFNa/b (IFN tipo I), específicamente, ha mostrado ser mediador esencial o un potenciador de la muerte celular apoptótica en células infectadas por virus (64). La secreción de IFNa/b en estudios in vitro (52) fue inducida por virus de la DVBcp (52) pero no por el DVBncp (44) y en este último inhibió la inducción endógena de IFN tipo I por otros virus (65).
En células cultivadas e infectadas con virus de la DVBncp, se incrementó la replicación de otros virus (66). En el caso de la enfermedad de Newcastle, un paramixovirus el cual induce IFN y es sensible a este, el incremento ha sido asociado con una reducción en los títulos de IFN inducidos en cultivos co-infectados con VDVBncp; un resultado similar fue descrito para el virus de la PPC (45).
El VDVB ha sido reportado como modulador de las funciones celulares del sistema inmune in vitro, con un incremento en la producción de óxido nítrico de macrófagos infectados (67), disminuyendo la producción del factor de necrosis tumoral alfa (TNFa) en macrófagos estimulados con lipopolisacárido (LPS) (14), reducción en la expresión de Fc (fracción cristalizable) y receptor C3 del complemento, y la actividad fagocítica de macrófagos alveolares (68).
Otros factores inmunosupresores incluyen quimiotaxis reducida, liberación de un inhibidor de la actividad de la IL-1, disminución de la secreción de inmunoglobulinas (42, 69), supresión de las respuestas proliferativas de células mononucleares bovinas frente a sustancias blastogénicas y alteración de la función neutrofílica (54, 69) disminuyendo su capacidad de degranulación y citotoxicidad celular dependiente de anticuerpos (54), además de disminución de la iodinación en polimorfonucleares y disminución en el nivel de proteínas séricas (69). Infecta preferentemente linfocitos T CD8+ e interfiere en sus funciones citotóxicas e inmunoreguladoras (54). La subregulación de la producción de TNFa podría ser causada por diversos mecanismos incluyendo una alteración en la cinética de producción de ARNm y su estabilidad (14).
El virus de la DVBncp induce estrés oxidativo en los estados tempranos de infección celular (16). El estrés oxidativo ha sido sugerido como un mediador de la apoptosis (70). Tal proceso de estrés puede estar ayudado por la inhibición de la síntesis protéica, observada durante infecciones con virus de la DVBncp.
También se ha demostrado los efectos in vitro del VDVB en células bovinas (aumento en la síntesis óxido nítrico, con el biotipo ncp, más no con el cp, después del tratamiento con lipopolisacárido o Salmonella Dublín). La actividad inhibidora de IL-1 inducida por lipopolisacárido fue incrementada para ambos biotipos. Contrario a esto, la síntesis de TNFá, quimiotaxis inducida por citoquinas así como la actividad procoagulante inducida por Salmonella dublin fue disminuida para ambos biotipos. La síntesis de IFN tipo I y de prostaglandina E2 solo estuvo presente en células infectadas con biotipo cp (71).
CONCLUSIONES Y PERSPECTIVAS
La DVB es producida por un virus del genero Pestivirus, familia Flaviviridae, que comprende un complejo de presentaciones clínicas pasando desde una presentación subclínica hasta la fatal EM, dadas principalmente por la capacidad inmunosupresora del virus y, en algunos casos, por acción directa del mismo - efecto citopático o no citopático-. Los animales PI juegan un papel importante en la transmisión y diseminación del virus, dado que son portadores asintomáticos, caracterizados principalmente por retraso en el crecimiento y susceptibilidad a infecciones secundarias. La DVB además es causante de problemas reproductivos asociados a disminución de la fertilidad en hembras y machos - evidenciando una disminución de la calidad seminal, reabsorción embrionaria, muerte fetal, momificación fetal, pudiendo producir muerte temprana en neonatos y defectos congénitos.
El control de la DVB requiere la identificación de los animales PI dentro de la producción así como la implementación de planes vacunales (en zonas de reactividad positiva), con la premisa de la determinación y análisis de los blancos moleculares -glicoproteínas (e.g. E2)- que permitan la generación de una respuesta inmune eficaz, aunado al uso de adyuvantes (incluyendo citoquinas, CpG, etc.) y/o utilización de vectores vacunales tales como el herpesvirus bovino tipo 1 o poxvirus. De la misma forma deben ser consideradas las vacunas de ADN en las cuales se insertan genes (e.g. E2) dentro del plásmido.
AGRADECIMIENTOS
Al profesor Pedro Eslava, Alejandra Bohórquez y Wilson Ramírez; por sus aportes críticos para la elaboración de esta revisión.
BIBLIOGRAFÍA
1. Ramírez G, Vera V, Villamil L. Diarrea viral bovina – DVB: Inmunosupresión y efectos en la reproducción bovina. El Cebú 1999. 32-40. [ Links ]
2. Jaime J, Villamil L, Vera V, Ramírez G. Infección persistente con el virus de la diarrea viral bovina (VDVB) en hatos lecheros de la sabana de Bogotá. Rev Med Vet Zoo 1996; 49:46-53. [ Links ]
3. Benavides E, Ortiz D. Epidemiología del Aborto bovino en Colombia: Una aproximación Conceptual. 2003. Red de Epidemiología Veterinaria (Notiepivet). [ Links ]
4. Saliki J, Fulton R, Hull S, Dubovi E. Microtiter virus isolation and enzyme immunoassays for detection of bovine viral diarrhea virus in cattle serum. J Clin Microb 1997; 35:803-807. [ Links ]
5. Wengler G, Bradley M, Collet F, Heinz R, Schlesinger W, Strauss J. 1995. Flaviviridae. Virus Taxonomy. In: Baule C, Kulcsar G, Belak K, Albert M, Mittelholzer C, Soos T, et al. Pathogenesis of primary respiratory disease induced by isolates from a new genetic cluster of bovine viral diarrhea virus type I. J Clin Microbiol 2001; 39:146-153. [ Links ]
6. Toplak I, Barlic-Maganja D, Hostnik P, Grom J. Genetic heterogeneity of bovine viral diarrhoea virus (BVDV) strains isolated in Slovenia. Slov Vet Res 2002; 39:113-123. [ Links ]
7. Lambot M, Douart A, Joris E, Letesson J, Pastoret P. Characterization of immune response of cattle against non-cytopathic and cytopathic biotypes of bovine viral diarrhoea virus. J Gen Virol 1997; 78:1041-1047. [ Links ]
8. Katz J, Ridpath J, Bolin S. Presumptive diagnostic differentiation of hog cholera virus from bovine viral diarrhea and border disease viruses by using cDNA nested-amplification approach. J Clin Microbiol 1993; 31:565-568. [ Links ]
9. Liang D, Sainz F, Ansari I, Gil L, Vassilev V, Donis R. The envelope glycoprotein E2 is a determinant of cell culture tropism in ruminant pestiviruses. J Gen Virol 2003; 84:1269-1274. [ Links ]
10. Becher P, Orlich M, Shannon A, Horner G, Konig M, Thiel H. Phylogenetic analysis of pestivirus from domestic and wild ruminants. J Gen Virol 1997; 78:1357-1366. [ Links ]
11. Jubb K, Kennedy P, Palmer N. Pathology of domestic animals. Fourth edition. London. Academic Press Inc. 1993; 2:149-158. [ Links ]
12. Laven R. Bovine Viral Diarrhoea Virus (BVDV). 2001. NADIS. Disponible en: www.mdc.org.uk/mdc-technichal/documents/BVD.pdf. [ Links ]
13. Uruno K, Shibata I, Nakane T. Detection of Bovine Viral Diarrhea Virus (BVDV) Using Reverse Transcription Polymerase Chain Reaction Assay. J Vet Med Sci 1998; 60:867-870. [ Links ]
14. Adler H, Jungi W, Pfister H, Strasser M, Sileghem M, Peterhans E. Cytokine regulation by virus infection: bovine viral diarrhea virus, flavivirus, downregulates production of tumor necrosis factor alpha in macrophages in vitro. J Virol 1996; 70:2650-2653. [ Links ]
15. Becher P, Orlich M, König M, Thiel J. Nonhomologous RNA Recombination in Bovine Viral Diarrhea Virus: Molecular Characterization of a Variety of Subgenomic RNAs Isolated during an Outbreak of Fatal Mucosal Disease. J Virol 1999; 73:5646–5653. [ Links ]
16. Schweizer M, Peterhans E. Oxidative stress in cells infected with bovine viral diarrhoea virus: a crucial step in the induction of apoptosis. J Gen Virol 1999; 80:1147-1155. [ Links ]
17. Zhang G, Aldridge M, McCauley J. Cell death induced by cytopathic bovine viral diarrhea virus is mediated by apoptosis. J Gen Virol 1996; 77:1677-1681. [ Links ]
18. Dubovi E. Fatal BVD virus-induced disease: role of persistently infected animals. The Bov Proc 1986; (18). [ Links ]
19. Peterhans E. 2002b. www.vetmed.unibe.ch/.../Mikrobio-popmed/Peterhans/BVD_Student_Bern_2002_05_21_handout_6_short.pdf. [ Links ]
20. Baule C, Kulcsar G, Belak K, Albert M, Mittelholzer C, Soos T, Kucsera L, Belak S. Pathogenesis of primary respiratory disease induced by isolates from a new genetic cluster of bovine viral diarrhea virus type I. J Clin Microbiol 2001; 39:146-153. [ Links ]
21. Stokka G, Falkner R, Bierman P, Van Boening J. Bovine Virus Diarrhea. Kansas State University. Agricultural Experiment Station and Cooperative Extension Service. 2000. [ Links ]
22. Pellerin C, Den Hurk V, Lecomte J, Tijssen P. Identification of a new group of bovine viral diarrhea virus strains associated with severe outbreaks and high mortalities. Virology 1994; 203:260-268. [ Links ]
23. Paton D, Sands J, Lowings J, Smith E, Ibata G, Edwards S. A proposed division of the pestivirus genus using monoclonal antibodies, supported by cross-neutralisation assays and genetic sequencing. Vet Res 1995; 26: 92-109. [ Links ]
24. Morales S. Detección de terneros con infección congénita con el virus de la diarrea viral bovina en dos hatos lecheros de la provincia de Arequipa. 2001. (http://sisbib.unmsm.edu.pe/bibvirtual/tesis/Salud/Morales_C_S/Rev_Bibli.htm). [ Links ]
25. Johnson C, Perez D, French R, Merrick W, Donis R. The NS5A protein of bovine viral diarrhoea virus interacts with the a subunit of translation elongation factor-1. J Gen Virol 2001; 82:2935–2943. [ Links ]
26. Donis R. Molecular biology of bovine viral diarrhea virus and its interactions with the host. Vet Clin North Amer 1995; 11:393-423. [ Links ]
27. Nelly J. Use serial analysis of gene expression to measure changes in gene expression in BVDV2 - infected MDBK cells. National Animal Disease Center (NADC). 2002. Disponible en: www.vetmed.iastate.edu/services/institutes/iicab/speaker%20abstracts.doc. [ Links ]
28. Baker J. The clinical manifestations of bovine viral diarrhea infection. Vet Clin North Amer 1995; 11:425-445. [ Links ]
29. Raymond G. BVDV – Bovine Virus Diarrhea Virus. Veterinarian’s Corner 2002; 2(9). [ Links ]
30. Heuschele W. Bovine viral diarrhea – Mucosal disease. Pennsylvania. Current Veterinary Therapy 3 Food Animal Practice. W.B. Saunders Company. 1993. 432-434. [ Links ]
31. Brodersen B, Kelling C. Effect of concurrent experimentally induced bovine respiratory syncytial virus and bovine viral diarrhea virus infection on respiratory tract and enteric diseases in calves. Amer J Vet Res 1998; 59:1423-1430. [ Links ]
32. Moennig V, Liess B. Pathogenesis of intrauterine infections with bovine viral diarrhea virus. Vet Clin North Amer 1995; 11:477-487. [ Links ]
33. Ssetongo Y, Johnson R, Smith J. 1980. In: Moennig V, Liess B. Pathogenesis of intrauterine infections with bovine viral diarrhea virus. Vet Clin North Amer 1995; 11:477-487. [ Links ]
34. Brock K, Lapin D, Skrade D. Embryo transfer from donnor cattle persistently infected with bovine viral diarrhea virus. Theriogenology 1997; 47:837-844. [ Links ]
35. Fray M, Mann G, Bleach E, Knight P, Clarke M, Charleston B. Modulation of sex hormone secretion in cows by acute infection with bovine viral diarrhoea virus. Reproduction 2002; 123:281-289. [ Links ]
36. Brock K, Stringfellow D. 1993. In: Fray M, Prentice M, Clarke C, Charleston B. Immunohistochemical evidence for the localization of bovine viral diarrhea virus, a single-stranded RNA virus, in ovarian oocytes in the cow. Vet Pathol 1998; 35:253-259. [ Links ]
37. Gillespie J, Schlafer D, Foote R, et al. 1990. In: Fray M, Prentice M, Clarke C, Charleston B. Immunohistochemical evidence for the localization of bovine viral diarrhea virus, a single-stranded RNA virus, in ovarian oocytes in the cow. Vet Pathol 1998; 35:253-259. [ Links ]
38. Fray M, Prentice M, Clarke C, Charleston B. Immunohistochemical evidence for the localization of bovine viral diarrhea virus, a single-stranded RNA virus, in ovarian oocytes in the cow. Vet Pathol 1998; 35:253-259. [ Links ]
39. Booth P, Stevens D, Collins M, Brownlie J, 1995. In: Fray M, Prentice M, Clarke C, Charleston B. Immunohistochemical evidence for the localization of bovine viral diarrhea virus, a single-stranded RNA virus, in ovarian oocytes in the cow. Vet Pathol 1998; 35:253-259. [ Links ]
40. Vanroose G, Nauwynck H, Van Soom A, Ysebaert M, Charlier G, Van Oostveldt P, et al. Structural Aspects of the Zona Pellucida of In Vitro-Produced Bovine Embryos: A Scanning Electron and Confocal Laser Scanning Microscopic Study Biol Reprod 2000; 62:463–469. [ Links ]
41. Brown T, De La Hunta A, Scott F, et al. 1975. In: Moennig V. Liess B. Pathogenesis of intrauterine infections with bovine viral diarrhea virus. Vet Clin North Amer 1995; 11:477-487. [ Links ]
42. Blood D, Henderson J, Radostis D. Medicina veterinaria. España. Editorial Interamericana de España Mc Graw Hill. 1992. 2:909-922. [ Links ]
43. Sawyer et al., 1991. In: Bolin S. The pathogenesis of the mucosal disease. Vet Clin North Amer 1995; 11:489-500 [ Links ]
44. Charleston B, Fray M, Baigent S, Carr B, Morrison I. Establishment of persistent infection with non-cytopathic bovine viral diarrhoea virus in cattle is associated with failure to induce type I interferon. J Gen Virol 2001; 82:1893-1897. [ Links ]
45. Baigent S, Zhang G, Fray M, Flick-Smith, H, Goodbourn S, Mccauley J. Inhibition of beta interferon transcription by noncytopathogenic bovine viral diarrhea virus is through an interferon regulatory factor 3-dependent mechanism. J Virol 2002; 76:8979-8988. [ Links ]
46. Loehr B, Frey H, Moenning V, Greiser-Wilke I. Clinical-virological course after superinfection of persistently infected cattle with strains of cytpathogenic bovine viral diarrhoea virus. Deutsche Tieraerztliche Wochenschrift 1998; 105:201-205. [ Links ]
47. Vera V. Genética molecular del virus de la diarrea viral bovina. Memorias: Aspectos básicos de la fisiología reproductiva y perspectivas de la biotecnología en Colombia. 1999. Oct. 24. Villavicencio, Meta. [ Links ]
48. Schweizer M, Peterhans E. Noncytopathic bovine viral diarrhea virus inhibits double-stranded RNA-induced apoptosis and interferon synthesis. J Virol 2001; 75:4692-4698. [ Links ]
49. Weinstock D, Bhudevi B, Castro A. Single-tube single-enzyme reverse transcriptase PCR assay for detection of bovine viral diarrhea virus in pooled bovine serum. J Clin Microbiol 2001; 39:343-346. [ Links ]
50. Glew E, Howard C. Antigen-presenting cells from calves persistently infected with bovine viral diarrhoea virus, a member of the Flaviviridae, are not compromised in their ability to present viral antigen. J Gen Virol 2001; 82:1677-1685. [ Links ]
51. Frederiksen B, Press C, Loken T, Odegaard SA Distribution of viral antigen in uterus, placenta and foetus of cattle persistently infected with bovine virus diarrhoea. Vet Microbiol 1999; 64:109-122. [ Links ]
52. Adler B, Adler H, Jungi T, Peterhans F. Macrophages infected with cytopathic bovine viral diarrhoea virus release a factor (s) capable of priming uninfected macrophages for activation-induced apoptosis. J Gen Virol 1997; 71:3255-3258. [ Links ]
53. Lambot M, Hanon E, Lecomte C, Hamers C, Letesson J, Pastoret P. 1998a. Bovine viral diarrhoea virus induces apoptosis in blood mononuclear cells by a mechanism largely dependent on monocytes. J Gen Virol 1998; 79:1745-1749. [ Links ]
54. Tizard I. Inmunología veterinaria. Sexta edición. Mc Graw Hill Interamericana. 2002; 229, 449. [ Links ]
55. Larsson B, Fossum C. Bovine virus diarrhoea virus induces in vitro a proliferative response of peripheral blood mononuclear cells from cattle immunized by infection. Vet Microbiol 1992; 31:317-325. [ Links ]
56. Lambot M, Joris E, Douart A, Lyaku J, Letesson J, Pastoret P. 1998b. Evidence for biotype-specific effects of bovine viral diarrhoea virus on biological responses in acutely infected calves. J Gen Virol 1998; 79:27–30. [ Links ]
57. Howard C, Clarke M, Sopp P, et al. 1992. In: Potgieter L. Immunology of bovine viral diarrhea virus. Vet Clin North Amer 1995; 11:501-520. [ Links ]
58. Howard C, Clarke M, Brownlie J. Protection against respiratory infection with bovine virus diarrhoea virus by passively acquired antibody. Vet Microbiol 1989; 19:195-203. [ Links ]
59. Rhodes S, Cocksedge J, Collins R, Morrison W. Differential cytokine responses of CD4+ and CD8+ T cells in response to bovine viral diarrhoea virus in cattle. J Gen Virol 1999; 80:1673–1679. [ Links ]
60. Bolin S, Ridpath J. In: Potgieter L. Immunology of bovine viral diarrhea virus. Vet Clin North Amer 1995; 11:501-520. [ Links ]
61. Donis R, Dubovi E. Molecular specificity of the antibody responses of cattle naturally infected with cytopathic and noncytopathic of bovine biotypes of bovine virus diarrhea-mucosal disease virus. Virology 1987; 158:168-173. [ Links ]
62. Bolin S. The pathogenesis of the mucosal disease. Vet Clin North Amer 1995; 11:489-500. [ Links ]
63. Bolin S. Immunogens of bovine viral diarrhea virus. Vet Microbiol 1993; 37:263-271. [ Links ]
64. Balachandran S, Roberts C, Kipperman T, Bhalla N, Compans R, Archer D, Barber G. Alpha/beta interferons potentiate virus induce apoptosis through activation of the FADD/caspase-8-death signaling pathway. J Virol 2000; 74:1513-1523. [ Links ]
65. Nakamura S, Shimazaki T, Sakamoto K, Fukusho A, Inoue Y, Ogawa N. 1995. In: Charleston B, Fray M, Baigent S, Carr B, Morrison I. Establishment of persistent infection with non-cytopathic bovine viral diarrhoea virus in cattle is associated with failure to induce type I interferon. J Gen Virol 2001; 82:1893-1897. [ Links ]
66. Diderholm H, Dinter Z. 1966. In: Baigent S, Zhang G, Fray M, Flick-Smith H, Goodbourn, S, McCauley J. Inhibition of beta interferon transcription by noncytopathogenic bovine viral diarrhea virus is through an interferon regulatory factor 3-dependent mechanism. J Virol 2002; 76:8979-8988. [ Links ]
67. Adler H, French B, Jungi T, Peterhans E. 1994. In: Glew, E.; Howard C. Antigen-presenting cells from calves persistently infected with bovine viral diarrhoea virus, a member of the Flaviviridae, are not compromised in their ability to present viral antigen. J Gen Virol 2001; 82:1677-1685. [ Links ]
68. Welsh et al. 1995. In: Glew E, Howard C. Antigen-presenting cells from calves persistently infected with bovine viral diarrhoea virus, a member of the Flaviviridae, are not compromised in their ability to present viral antigen. J Gen Virol 2001; 82:1677-1685. [ Links ]
69. Jaime J, Ramírez G. Inmunosupresión e inmunotolerancia asociados a infección por virus de la diarrea viral bovina (VDVB). Rev Med Vet Zoo 1996; 49:54-58. [ Links ]
70. Buttke T, Sandstorm P. 1994. In: Schweizer M, Peterhans E. Oxidative stress in cells infected with bovine viral diarrhoea virus: a crucial step in the induction of apoptosis. J Gen Virol 1999; 80:1147-1155. [ Links ]
71. Peterhans E. Instituto de Virología Veterinaria. Universidad de Bern. Suiza. 2002a (www.vetmed.iastate.edu/services/institutes/iicab/speaker%20abstracts.doc) [ Links ]














