Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Ciencia y Tecnología Agropecuaria
Print version ISSN 0122-8706
Corpoica cienc. tecnol. agropecu. vol.18 no.1 Mosquera Jan./Apr. 2017
https://doi.org/10.21930/rcta.vol18_num1_art:563
Artículo de investigación científica y tecnológica
DOI: http://dx.doi.org/10.21930/rcta.vol18_num1_art:563
Degradación de la vitamina C en un producto de mango (Mangifera indica L.) y lactosuero
Degradation of vitamin C in a product made from mango (Mangifera indica L.) and whey protein
Degradação da vitamina C em um produto de manga (Mangifera indica L.) e lactisoro
Fernando Alonso Mendoza-Corvis,1 Margarita Rosa Arteaga-Márquez,2 Omar Andrés Pérez-Sierra3
1 MSc, Universidad Internacional de la Rioja. Docente, Programa de Ingeniería de Alimentos, Facultad de Ingeniería, Universidad de Córdoba. Montería, Colombia. Docente, Programa de Ingeniería Agroindustrial, Facultad de Ingeniería, Universidad de Sucre. Sincelejo, Colombia. fmendoza@correo.unicordoba.edu.co
2 MSc, Universidad Austral de Chile. Docente, Programa de Ingeniería de Alimentos, Facultad de Ingeniería, Universidad de Córdoba. Montería, Colombia. mrarteaga@correo.unicordoba.edu.co
3 PhD, Universidade Federal de Viçosa. Docente, Programa de Ingeniería de Alimentos. Facultad de Ingeniería. Universidad de Córdoba. Montería, Colombia. oaperez@correo.unicordoba.edu.co
Fecha de recepción: 08/10/2015 Fecha de aceptación: 06/06/2016
Para citar este artículo: Mendoza-Corvis FA, Arteaga-Márquez MR, Pérez-Sierra OA. 2017. Degradación de la vitamina C en un producto de mango (Mangifera indica L.) y lactosuero. CORPOICA Cienc Tecnol Agropecuria. 18(1):125-137
Resumen
Esta investigación buscó determinar la cinética de degradación de la vitamina C en un producto en polvo elaborado a base de pulpa de mango (Mangifera indica L. var. Hilacha) y lactosuero, con el fin de conocer el efecto de la temperatura en su conservación y además evaluar el comportamiento de los parámetros L*, a*, b* y la diferencia total del color (ΔE) en el producto. La vitamina C se determinó mediante el método AOAC 967.21/90, con 2,6-diclorofenol indofenol; mientras que el color se cuantificó con un colorímetro Color Flex EZ marca HunterLab. La vitamina C exhibió mayor estabilidad en el producto en polvo almacenado a una temperatura de 4 °C, con una concentración (al término de la octava semana de muestreo) de 13,94 ± 1,2 mg/100 g por muestra, presentando una cinética de degradación de primer orden con valores de k1 de 0,014 y 0,041 mg/100 g/por semana para las temperaturas de 4 °C y 28 °C, respectivamente. Las mayores variaciones en el color se dieron en las muestras almacenadas a 28 °C, lo cual indica la influencia de la temperatura en el cambio de los componentes del producto. Los parámetros L*, a* y b* se vieron menos afectados a la temperatura de conservación de 4 °C y sus valores se ajustaron a un polinomio de segundo orden.
Palabras clave: Mangifera indica, secado por aspersión, cinética de degradación, calidad de los alimentos.
Abstract
This study aimed to determine the kinetics of vitamin C degradation in a product made from mango pulp (Mangifera indica L.) and whey protein powder, in order to determine the effect of temperature on its conservation and further evaluate the behavior of the L*, a*, b* and the total color difference (ΔE) in the powder product. Vitamin C was determined by the AOAC 967.21/90 method using 2,6-dichlorophenol indophenol, and the color was quantified with a HunterLab Color Flex EZ colorimeter. Vitamin C showed greater stability in the powder product stored at 4 °C with a concentration at the end of the eighth sampling week of 13.94 ± 1.2 mg/100 g-1 sample and showing a first order degradation kinetics with k1 values of 0.014 and 0.041 mg/100 g/week at temperatures of 4 °C and 28 °C, respectively. The greatest variations in color occurred in samples stored at 28 °C, indicating the influence of the temperature change on the product components. In addition, L*, a* and b* parameters were less affected under storage temperature of 4 °C, and their values correspond to a second degree polynomial.
Keywords: Mangifera indica, spray drying, degradation kinetics, food quality.
Resumo
Esta pesquisa procurou determinar a cinética de degradação da vitamina C em um produto em pó elaborado a base de polpa de manga (Mangifera indica L. var. Hilacha) e lactisoro, com o fim de conhecer o efeito da temperatura na sua conservação e ademais avaliar o comportamento dos parâmetros L*, a*, b* e a diferença total da cor (ΔE) no produto. A vitamina C determinou-se mediante o método AOAC 967.21/90, com 2,6-diclorofenol indofenol; enquanto que a cor se quantificou com um colorímetro cor Flex EZ marca HunterLab. A vitamina C exibiu maior estabilidade no produto em pó armazenado a uma temperatura de 4 °C, com uma concentração (ao término da oitava semana de amostragem) de 13,94 ± 1,2 mg/100 g por amostra, presentando uma cinética de degradação de primeira ordem com valores de k1 de 0,014 e 0,041 mg/100 g/por semana para as temperaturas de 4 °C e 28 °C, respectivamente. As maiores variações na cor deram-se nas amostras armazenadas a 28 °C, o qual indica a influência da temperatura na mudança dos componentes do produto. Os parâmetros L*, a* e b* viram-se menos afetados à temperatura de conservação de 4 °C e os seus valores se ajustaram a um polinômio de segunda ordem.
Palavras chave: Mangifera indica, secado por aspersão, cinética de degradação, qualidade dos alimentos.
Introducción
El mango (Mangifera indica L.) es uno de los frutos tropicales más importantes producidos en el mundo según la Organización para la Agricultura y la Alimentación (FAO 2015; Wibowo et al. 2015a; 2015b). En Colombia se producen actualmente más de 270 mil toneladas de mango al año (FAO 2015), lo que representa aproximadamente cerca del 0,8% de la producción agrícola del país (Agronet 2015). Esta fruta se comercializa, en su mayoría, como producto fresco —sin aportar ningún valor agregado al consumidor primario— y, en menor proporción, para la agroindustria. Además de ser un alimento, es una buena fuente de compuestos bioactivos con beneficios potenciales para la salud, como el ácido ascórbico, el ácido dehidroascórbico, β-carotenos, polifenoles, fibra, terpenoides y antioxidantes minerales (Ribeiro y Schieber 2010).
La vitamina C funciona como un antioxidante natural que previene los daños en las macromoléculas del cuerpo humano a causa de los radicales libres (De Lorgeril y Salen 2006; Sikorska-Wisniewska y Szumera 2007; Gabriel et al. 2015), además, está relacionada con la síntesis de aminoácidos y de adrenalina, con la producción de colágeno, la desintoxicación del hígado y la prevención de enfermedades cardiovasculares (Yahia et al. 2001; García-Alonso et al. 2004; Ordoñez-Santos y Yoshioka-Tamayo 2012). No obstante, el ácido dehidroascórbico se caracteriza por ser uno de los constituyentes más termosensibles en los alimentos, y su disminución durante el almacenamiento de los productos es ocasionada por la exposición de los constituyentes de estos a condiciones adversas de conservación.
Generalmente, los cambios en la calidad de los alimentos son reportados en la literatura mediante modelos cinéticos de degradación de orden cero y de primer orden (Wang et al. 2006; Torres et al. 2011; Liu et al. 2014a). El estudio de la cinética de degradación de la vitamina C ayuda a entender el comportamiento de un determinado producto y sus componentes, lo cual permite predecir las mejores condiciones de almacenamiento, el tiempo de vida media y la vida útil de dicho producto.
Ordóñez-Santos y Yoshioka-Tamayo (2012), por ejemplo, estudiaron la degradación térmica de la vitamina C en la pulpa de mango (M. indica) y encontraron que esta sigue una cinética de primer orden con constante de velocidad de degradación de 0,028-0,056 min-1 a temperaturas entre 60 °C y 80 °C. Por su parte, Liu et al. (2014b), en el estudio de la cinética de degradación de la vitamina C en néctar de mango, reportaron que esta presenta una degradación de orden combinado. Sin embargo, otros investigadores encontraron que la cinética de degradación era de primer orden en el zumo de fresa (Cao et al. 2012) y en el zumo de naranja (Torres et al. 2011) durante el almacenamiento a diferentes temperaturas.
Color, aroma, sabor y apariencia son los cuatro factores más importantes que influyen en la elección de los alimentos por parte de las personas (Chen 2008). Si bien el color es un atributo de calidad muy importante durante el procesamiento de los alimentos, la determinación del tiempo de vida útil de un producto también es muy apreciado por los consumidores (Cortés y Chiralt 2008). Este tiempo actualmente se mide con el sistema Cielab o sistema L* (luminosidad), a* (cromaticidad verde-roja) y b* (cromaticidad amarilla-azul) (Chen 2008). Recientemente se han realizado muchos estudios que han demostrado que el encapsulamiento de materias primas y de pigmentos mediante secado por aspersión es una excelente alternativa para el procesamiento y la conservación durante el almacenamiento de algunos productos, entre los cuales encontramos el polvo de zumaque (Caliskan y Nur Dirim 2013), el polvo de batata (Peng et al. 2013) y el polvo de amla (Mishra et al. 2014). Por ejemplo, Jiménez-Aguilar et al. (2011), en un estudio sobre la estabilidad química del extracto de arándano secado por aspersión, almacenado a 4 °C y 25 °C, encontraron que los parámetros L*, a* y b* seguían una cinética de degradación de primer orden, y relacionaron el color rojo de las muestras con el contenido en antocianinas.
Con esta investigación, se buscó determinar la cinética de degradación de la vitamina C en un producto en polvo elaborado a base de pulpa de mango de hilacha (M. indica) y lactosuero, con el fin de conocer el efecto de las condiciones de conservación de la vitamina C y los parámetros L*, a* y b* del producto.
Materiales y métodos
Obtención y almacenamiento de la muestra
Se elaboró un producto a base de pulpa de mango de hilacha Mangifera indica L. (Anacardiaceae), lactosuero y azúcar en concentraciones de 24%, 69% y 7%, respectivamente. El mango fue seleccionado, lavado, desinfectado y despulpado, para posteriormente ser mezclado con los demás ingredientes y ser sometido a un proceso de pasteurización a 72 °C por 15 segundos (Jiménez-Guzmán et al. 2003). Una vez frío, el producto se procesó en un secador por aspersión modelo Pasalb 1.5 marca Vibrasec, con una temperatura de entrada de aire caliente de 138 °C, una temperatura de salida de 70 °C y una velocidad de aspersión de 24.908 rpm. Se utilizó maltodextrina en una concentración de 27,5% como agente encapsulante (Mendoza-Corvis 2015).
Las muestras fueron empacadas en bolsas de lámina metalizada de polipropileno orientado flexible (espesor de 10 micras, permeabilidad al oxígeno de 0,5-0,8 cc/m2 en 24 horas, permeabilidad al CO2 0,4-6,0 cc/m2 en 24 horas y permeabilidad al vapor de agua 2x10-13-7x10-13 g/m*s*Pa). Estas bolsas fueron almacenadas a temperaturas de 4 °C y 28 °C, durante ocho semanas, tiempo en el cual se realizó el seguimiento de la concentración de vitamina C y del color del producto en polvo cada ocho días.
Evaluación de la cinética de degradación de la vitamina C
La determinación de la concentración de vitamina C en las muestras se llevó a cabo mediante el método AOAC 967.21/90 (AOAC 1990) para concentraciones máximas de hasta 50 ppm de ácido ascórbico. Se empleó una solución de 2,6-diclorofenolindofenol a 400 ppm para titular las muestras (5 g de cada tratamiento) diluidas en 20 ml de una solución de ácido oxálico 2%. Se usó como patrón una solución de ácido ascórbico 0,2% y un blanco correspondiente a 0,2 ml de agua destilada. Los resultados se expresaron en mg de vitamina C por 100 g de muestra.
Para determinar la cinética de degradación de la vitamina C, los datos obtenidos se sometieron a un análisis de regresión con los modelos de cinética de orden cero (Ecuación 1) y de primer orden (Ecuación 2) (Liu et al. 2014b).
Cinética de orden cero:

Cinética de primer orden:

Donde C es la concentración de ácido ascórbico (mg/100 g) en el tiempo t; Co es la concentración de ácido ascórbico en el tiempo cero; Ko y K1 son las constantes de velocidad de la degradación del ácido ascórbico (mg/100 g/semana); y t es el tiempo de almacenamiento (semanas). Además, a partir del resultado de la cinética de degradación de la vitamina C, se calculó el tiempo de vida media de esta (t ½, en semanas) —de acuerdo con las ecuaciones 3 y 4 (Pulido y Beristain 2010)— y el tiempo de reducción decimal "D" (ecuación 5) (Ordóñez-Santos et al. 2013).
Cinética de orden cero:

Cinética de primer orden:

Tiempo de reducción decimal:

Evaluación de la cinética de degradación del color
El color se determinó empleando un colorímetro Color Flex EZ marca HunterLab, con un ángulo de observación de 10° e iluminante estándar D65. Se realizó la calibración del equipo con un plato de cerámica de color verde estándar y un plato blanco estándar (X: 80,09; Y: 84,99; Z: 87,67), antes de la medición del color. Para determinar la diferencia total en el color (ΔE) se utilizó la ecuación de Hunter-Scofield (Ecuación 6) (Liu et al. 2014b).
Diferencia total de color (ΔE):
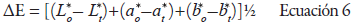
Donde L*0 y L* corresponden a la luminosidad de las muestras; los subíndices "0" y "t" son, para todas las variables, el tiempo cero y el tiempo durante el seguimiento de las muestras; a*0 y a* son la cromaticidad verde (-) roja (+); y b*0- b* la cromaticidad amarilla (+) azul (-) para los tiempos "0" y "t". Además, se evaluaron los parámetros cinéticos de estas tres variables con las Ecuación 1, 2 y 7 (Cortés y Chiralt 2008) .
Polinomio de segundo grado:

Análisis estadístico
Los tratamientos fueron realizados con un diseño completamente al azar. Se estudió el comportamiento de las variables mediante análisis de varianza y test de Tukey, a un nivel de significancia del 5%, con el software SAS 9.2. Los análisis se hicieron por triplicado. Las órdenes de reacción, las constantes de velocidad de degradación de la vitamina C y el color se determinaron mediante análisis de regresión lineal simple, empleando el coeficiente de determinación (R2) y el error cuadrático medio (ECM) como criterios para escoger el modelo de mejor ajuste.
Resultados y discusión
Cinética de degradación de la vitamina C
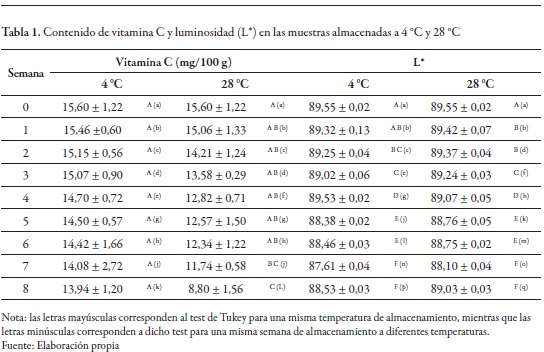
El resultado de la variación en la concentración de la vitamina C en las muestras almacenadas a 4°C y 28°C se presenta en la tabla 1. El análisis de varianza exhibió diferencia significativa (p<0,05) de esta, con relación a los factores tiempo y temperatura de conservación, mas no con respecto a la interacción de estos. El contenido de vitamina C en las muestras en polvo almacenadas a las diferentes temperaturas de conservación presentó un decrecimiento con el tiempo de almacenamiento. En la tabla 1 se muestran los resultados del test de separación de medias tanto para las distintas semanas de almacenamiento como entre las temperaturas empleadas.
Para el tratamiento a 28 °C, se evidencia que no existió diferencia significativa en la concentración de vitamina C entre el tiempo 0 y la sexta semana de almacenamiento del producto. Se presentó una variación en la concentración de 15,60 mg/100 g a 12,34 mg/100 g de producto en dicho lapso, con una diferencia entre la sexta y la octava semana. Los tratamientos a 4 °C no presentaron diferencia significativa a lo largo de las ocho semanas, con una variación de la concentración de vitamina C de 15,60 mg/100 g a 13,94 mg/100g, lo que evidencia una mayor estabilidad de esta a una temperatura de conservación del producto de 4 °C.
Al comparar las medias en la concentración de vitamina C para una misma semana, a diferentes temperaturas de almacenamiento, se observó que no existió diferencia significativa en la concentración de vitamina C entre las semanas 0-3 y 5-7; solo se presentó en las semanas 4 y 8. La menor concentración fue la del tratamiento a 28 °C. Estos resultados nos muestran cierta estabilidad de la vitamina C en ambas condiciones de almacenamiento. La mayor concentración se presentó en el producto conservado a 4 °C. Resultados similares fueron reportados por Borrmann et al. (2013).
Al aplicar las ecuaciones 1 y 2 de reacción de cero y primer orden para tratar de conocer la cinética de degradación de la vitamina C, se obtuvieron los parámetros cinéticos y los coeficientes de determinación para esta en el producto almacenado durante ocho semanas (tabla 2).
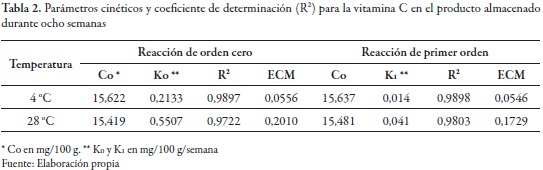
Los modelos de reacción de orden cero y de primer orden describieron satisfactoriamente la cinética de degradación de la vitamina C, ya que presentaron coeficientes de determinación (R2) superiores a 90% y errores cuadráticos medios inferiores al 10%. Sin embargo, el que mejor describe su comportamiento es el modelo de cinética de primer orden, pues presenta los valores más bajos en el error cuadrático medio (ECM). Las constantes de velocidad cinética dependen estrechamente de la temperatura de estudio: un aumento en la temperatura de conservación implicó un valor mayor en las constantes de velocidad de degradación para cada uno de los modelos cinéticos estudiados. En efecto, casi se triplicó el valor de K1, al pasar de 0,014 mg/100 g* semana (en el tratamiento con una temperatura de 4 °C) a 0,041 mg/100 g/semana (en el tratamiento a 28 °C). Lo anterior evidencia el aumento de la velocidad de degradación de la vitamina C con el incremento de la temperatura de conservación.
Similarmente, Bosch et al. (2013) reportaron que la degradación de la vitamina C en un puré de frutas seguía una cinética de primer orden, con el aumento de la constante de degradación (K1) de 0,0135 a 0,0550 al incrementar la temperatura de almacenamiento de 25 °C a 37 °C. Remini et al. (2015) también analizaron que la vitamina C en el jugo de naranja pasteurizado seguía una cinética de primer orden, con el incremento de la constante de degradación (k1) de 0,049 dia-1 a 0,122 dia-1 a 4 °C y 20 °C, respectivamente. Resultados afines fueron reportados por Wibowo et al. (2015a, 2015b) en jugo de mango, por Ordóñez-Santos et al. (2013) en guayaba y por Dermesonluoglu et al. (2015) en espinacas.
La vitamina C es una de las más termosensibles y su degradación térmica está asociada con la isomerización (apertura o cierre del anillo de lactona) de L-isómeros a D-isómeros y/o la formación de compuestos aquirales (Dabbagh y Azami 2014). Según Jesse (2000), hay tres rutas de degradación del ácido ascórbico (AA): la vía oxidativa catalizada, la vía oxidativa no catalizada y la vía bajo condiciones anaeróbicas. La primera se lleva a cabo mediante procesos oxidativos que implican la transferencia de dos electrones: inicialmente se forma el monoanión ascorbato (AH-), el cual, con la pérdida adicional de un segundo electrón, forma ácido dehidroascórbico (ADA), altamente inestable y susceptible a la hidrólisis del anillo de lactona. Este último se hidroliza fácilmente para producir ácido 2,3-dicetogulónico (DCG), que, a continuación, se degrada por decarboxilación, con la consiguiente pérdida del valor nutricional del AA.
En la vía oxidativa no catalizada, el AH- es atacado directamente por el oxígeno molecular, lo cual genera primero los radicales aniónicos AH• y H2O2•, que se transforman en ADA y H2O2. Estos dan lugar, posteriormente, a la apertura del anillo de lactona, para originar el DCG.
Estudios llevados a cabo sobre la cinética de degradación de la vitamina C en diversos alimentos coinciden en que esta corresponde a una cinética de primer orden (Pulido y Beristain 2010). Nisha et al. (2004) estudiaron la cinética de degradación del ácido ascórbico en amla durante su cocción y demostraron que correspondía a reacciones de primer orden. Así mismo, Uddin et al. (2001) estudiaron la cinética de reacción de la vitamina C durante el almacenamiento del kiwi deshidratado, y evidenciaron cinéticas de degradación de primer orden: la degradación de la vitamina C depende de la concentración de esta. Por su parte, Ordóñez-Santos y Yoshioka-Tamayo (2012), al realizar la cinética de degradación térmica de la vitamina C en pulpa de mango, reportaron que esta siguió una cinética de orden cero.
Al aplicar las ecuaciones 4 y 5, se encontró que el tiempo de vida media (t ½) del producto y el tiempo de reducción decimal (D) (tabla 3) se mostraron acordes con el orden de reacción reportado en la tabla 2.

La vida media de una reacción (t ½) es el tiempo necesario para que la concentración de un reactivo descienda a la mitad de su valor original (Brown et al. 2009). Esta es una forma conveniente de describir la rapidez con la que una reacción ocurre; una reacción rápida tiene una vida media breve (Brown et al. 2009). En esta investigación se determinaron tiempos de vida media para la vitamina C de 47,99 y 16,91 semanas para los productos almacenados a 4 °C y 28 °C, respectivamente. Esto corroboró que la temperatura de 4 °C es la que ofrece mayor estabilidad en la preservación de este parámetro en el producto, lo cual concuerda con el valor de D obtenido (164,47 semanas). Sin embargo, se puede decir que esto solo se cumple si no existen otros factores que puedan influenciar dicho parámetro durante el tiempo de almacenamiento.
Color
El comportamiento de los parámetros L*, a* y b* de las muestras almacenadas a 4 °C y 28 °C durante 8 semanas se observa en las tablas 1 y 4. Se evidenciaron diferencias significativas en L*, a* y b*, con respecto a los factores tiempo y temperatura, al igual que en la interacción de estos. Pese a existir tales diferencias, el cambio en la media es mínimo para los parámetros L* y a* en ambas condiciones de almacenamiento, y para b* a 4 °C, lo cual indica que estas variaciones no son críticas para el producto. La cromaticidad amarilla (+) azul (-) a 28 °C presenta la mayor variación en su media, lo que podría deberse a la degradación de los pigmentos presentes en el producto aportados por la pulpa de mango, específicamente, los carotenoides. Estos últimos son los principales pigmentos que le confieren el color amarillo al mango y contienen enlaces insaturados que pueden ser oxidados por el mismo mecanismo de oxidación de los lípidos, lo que resulta en una reducción de la coloración amarilla (Du y Ahn 2000).
Estos procesos oxidativos involucran reacciones de epoxidación, formación de apocarotenoides (carotenoides de menos de 40 átomos de carbono) e hidroxilación, lo cual genera compuestos de bajo peso molecular similares a los que aparecen como consecuencia de la oxidación de ácidos grasos. Debido a estas reacciones, los carotenoides, tras perder su color y sus propiedades favorables para la salud, dan lugar a compuestos aromáticos que en algunos casos son agradables (té, vino) y en otros no (zanahoria deshidratada) (Meléndez-Martínez et al. 2004).
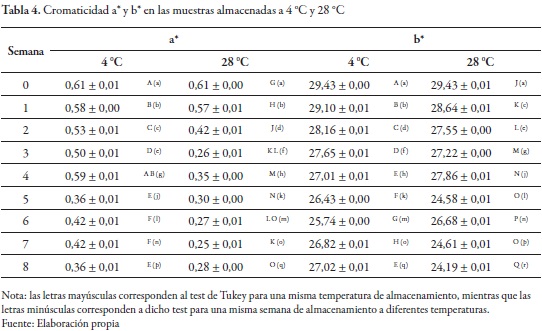
El valor de L*, a* y b* fue disminuyendo en las muestras en ambas temperaturas de conservación a medida que transcurría el tiempo de almacenamiento; el valor de estos parámetros fue siempre mayor en las muestras que se mantuvieron a 4 °C. Todos los tratamientos presentaron diferencia significativa para los factores L*, a* y b* desde la primera semana de almacenamiento, con excepción del valor de L* durante la primera semana para las muestras mantenidas a 4 °C. De modo similar, en su estudio sobre la estabilidad del color de la yema de huevo secada por aspersión, Gonçalves et al. (2014) reportaron la disminución de los valores de L*, a* y b* durante el almacenamiento. Efectos semejantes fueron reportados por Hernández (2010), quien evidenció cambios significativos en estos parámetros en un producto en polvo a base de uchuva almacenado a 4 ºC y 20 °C.
La reducción de la cromaticidad a* y b* en el tiempo y según la temperatura manifiesta la degradación de los pigmentos carotenoides. Esta degradación hace que, en el plano cromático a*b*, las muestras tengan un desplazamiento hacia el interior del área de los grises, con disminución en la saturación o croma (C*) y en la coordenada polar, tono o matiz (H*) (Ruiz et al. 2005; Hernández 2010).
Al comparar las medias de estos factores para una misma semana de almacenamiento a distintas temperaturas, se observó que no hubo diferencia significativa dentro de las primeras dos semanas de conservación, con excepción del valor de b* durante la segunda semana.
Al aplicar la ecuación 6, encontramos que la diferencia total en el color (ΔE) al término de las ocho semanas de almacenamiento fue de 2,860 para las muestras mantenidas a 4 °C y de 5,625 para las muestras almacenadas a 28 °C (tabla 5).
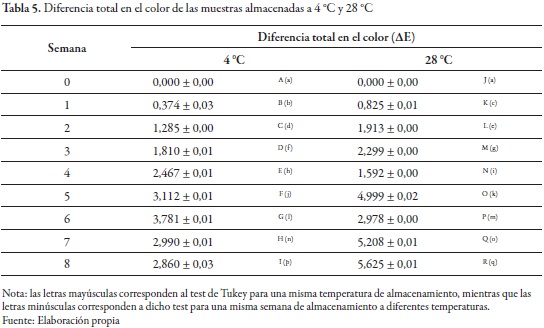
Las mayores variaciones en el color se dieron en las muestras almacenadas a 28 °C, lo cual indica la influencia de la temperatura en el cambio de los componentes del producto, específicamente, en los pigmentos, lo que sugiere una mayor estabilidad en el color del producto conservado a 4 °C. El aumento en la diferencia total en el color (ΔE) se puede deber a procesos de oxidación de los pigmentos, lo cual está directamente relacionado con la permeabilidad del empaque (por la influencia del oxígeno, el vapor de agua y otros gases), el tiempo de almacenamiento y el aumento de la velocidad de reacción de las moléculas por la temperatura.
Según las condiciones del almacenamiento podrán afectarse los carotenoides. La variación que se da en los a-carotenos, los ß-carotenos y la luteína obtenidos a partir de un polvo de zanahoria, cuando el producto se conserva en la oscuridad a diferentes temperaturas (4 °C, 25 °C y 45 °C), reveló que los niveles de dichos componentes disminuyen con el aumento de la temperatura de almacenamiento (Meléndez-Martínez et al. 2004). Una diferencia total en el color (?E) con un máximo de 5,625 para el tratamiento conservado a 28 °C durante ocho semanas se puede considerar como satisfactoria, en comparación con los resultados obtenidos por Jiménez-Aguilar et al. (2011). Estos últimos reportaron un ?E máximo de 5, que interpretaron como apropiado, pues se demostró que el secado por aspersión del arándano proporciona una ventaja en la conservación del color del producto.
La cinética del color durante el almacenamiento de las muestras conservadas a 4 °C y 28 °C se detalla en la tabla 6. Como se observa en esta, la luminosidad a 4 °C presentó un orden de reacción cero, ya que contó con el coeficiente de determinación más elevado y el ECM más bajo; asimismo presentó un valor en la constante de velocidad de reacción (k) inferior, en comparación con el obtenido para las muestras almacenadas a 28 °C. Lo anterior indica una menor velocidad de reducción de L* a dicha temperatura; mientras que para la muestra almacenada a 28 °C el valor de L* se ajustó a un orden de reacción cero durante las tres primeras semanas de almacenamiento. Esto es así probablemente debido a la influencia de otros parámetros relacionados con el empaque y las condiciones de almacenamiento. El parámetro a* se ajustó de modo semejante a un orden de reacción cero a 4 °C durante todo el almacenamiento, mientras que a 28 °C se ajustó al mismo orden de reacción, con un buen coeficiente de determinación solo hasta la tercera semana de evaluación.
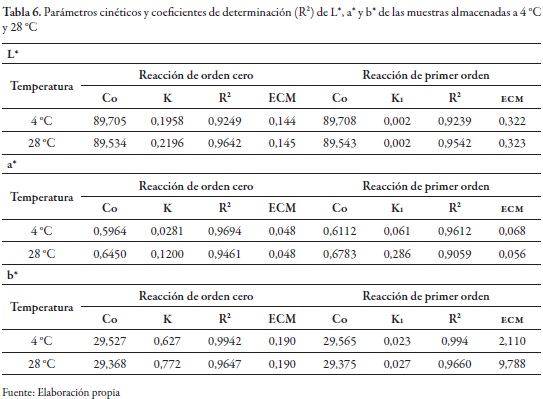
El parámetro b* a 28 °C describe una cinética de primer orden dentro de las primeras tres semanas de conservación, mientras que para las muestras almacenadas a 4 °C se obtuvo un ajuste aceptable en el coeficiente de determinación para las primeras seis semanas de almacenamiento. Estas últimas muestras exhibieron un orden de reacción cero, por lo que se decidió revisar el ajuste de los parámetros L*, a* y b* con un polinomio de segundo grado (ecuación 7). Se observó que los coeficientes de determinación mejoraron al evaluar las muestras con las temperaturas de trabajo durante las ocho semanas de almacenamiento (tabla 7).
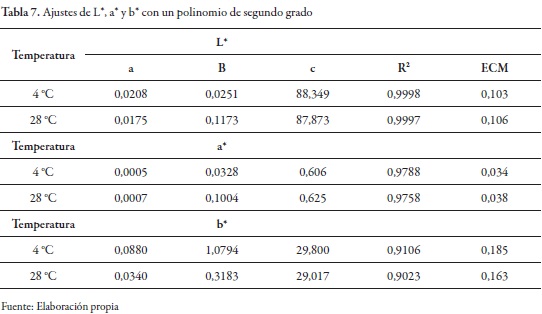
Cortés y Chiralt (2008), al evaluar la cinética del cambio de color en manzanas deshidratadas, encontraron que los modelos de orden 0 y 1 presentaron ajustes de regresión aceptables para L* en ciertos tratamientos. Sin embargo, en general, para la mayoría de los parámetros de color, el modelo cinético de segundo orden presentó los mejores coeficientes de regresión, con algunas excepciones.
Conclusiones
La vitamina C presentó mayor estabilidad en el producto en polvo almacenado a una temperatura de 4 °C y exhibió una diferencia no significativa al término de la octava semana de muestreo: la concentración fue de 13,94 ± 1,2 mg/100 g muestra, con una cinética de degradación de primer orden en todos los tratamientos y valores de k1 de 0,014 y 0,041 mg/100 g/semana para las temperaturas de 4 °C y 28 °C, respectivamente. Los parámetros L*, a* y b* se vieron menos afectados con la temperatura de conservación de 4 °C, con un ajuste de sus valores con un polinomio de segundo orden.
Descargos de responsabilidad
Los autores están de acuerdo con la publicación del presente artículo y declaran que no existe ningún conflicto de interés que afecte los resultados.
Referencias
Agronet. 2015. Sistema de estadísticas agropecuarias. Bogotá (Colombia): Ministerio de Agricultura y Desarrollo Rural; [2015 oct 7] http://agronet.gov.co/agronetweb1/Estad %C3%ADsticas.aspx. [ Links ]
[AOAC] Association of Official Analytical Chemists. 1990. Official Methods of Analysis. 15a ed. Arlington, EE. UU.: AOAC. [ Links ]
Borrmann D, Pierucci APTR, Leite SGF, Leão MHMR. 2013. Microencapsulation of passion fruit (Passiflora) juice with n-octenylsuccinate-derivatised starch using spray-drying. Food Bioprod Process. [consultado 2015 jul 15];91(1):23-27. http://www.fbp.ichemejournals.com/article/S0960-3085(12)00061-2/abstract. doi: http://doi.org/10.1016/j.fbp.2012.08.001. [ Links ]
Bosch V, Cilla A, García-Llatas G, Gilabert V, Boix R, Alegría A. 2013. Kinetics of ascorbic acid degradation in fruit-based infant foods during storage. J Food Eng. [consultado 2015 may 18];116(2):298-303. http://www.sciencedirect.com/science/article/pii/S0260877412005870. doi: http://doi.org/10.1016/j.jfoodeng.2012.12.003. [ Links ]
Brown TL, LeMay HE, Bursten BC, Burdge JR. 2009. Química: la ciencia central. México: Pearson. [ Links ]
Caliskan G, Nur Dirim S. 2013. The effects of the different drying conditions and the amounts of maltodextrin addition during spray drying of sumac extract. Food Bioprod Process. [consultado 2015 jun 9];91(4):539-548. http://www.fbp.ichemejournals.com/article/S0960-3085(13)00063-1/abstract. doi: http://doi.org/10.1016/j.fbp.2013.06.004. [ Links ]
Cao X, Bi X, Huang W, Wu J, Hu X, Liao X. 2012. Changes of quality of high hydrostatic pressure processed cloudy and clear strawberry juices during storage. Innov Food Sci Emerg. [consultado 2015 may 8];16:181-190. http://www.sciencedirect.com/science/article/pii/S146685641200077X. doi: http://doi.org/10.1016/j.ifset.2012.05.008. [ Links ]
Chen XD. 2008. Food drying fundamentals. En: Chen XD, Mujumdar AS, editores. Drying technologies in food processing. New Jersey, EE. UU.: Wiley. [ Links ]
Cortés M, Chiralt BA. 2008. Cinética de los cambios de color en manzana deshidratada por aire fortificada con vitamina E. Vitae. 15(1):8-16. [ Links ]
Dabbagh HA, Azami F. 2014. Experimental and theoretical study of racemization, stability and tautomerism of vitamin C stereoisomers. Food Chem. [consultado 2015 julio 12];164:355-362. http://www.sciencedirect.com/science/ article/pii/S0308814614007596. doi: http://doi.org/10.1016/j.foodchem.2014.04.121. [ Links ]
De Lorgeril M, Salen P. 2006. Antioxidant nutrients and antioxidant nutrient-rich foods against coronary heart disease. En: Bourassa MG, Tardif JC, editores. Antioxidants and cardiovascular disease. New York, EE. UU.: Springer Science+Business Media, Inc. [ Links ]
Dermesonluoglu E, Katsaros G, Tsevdou M, Giannakourou M, Taoukis P. 2015. Kinetic study of quality indices and shelf life modelling of frozen spinach under dynamic conditions of the cold chain. J Food Eng. [consultado 2015 may 18];148:13-23. http://www.sciencedirect.com/science/article/pii/S0260877414003070. doi: http://doi.org/10.1016/j.jfoodeng.2014.07.007. [ Links ]
Du M, Ahn DU. 2000. Effects of antioxidants and packaging on lipid and cholesterol oxidation and color changes of irradiated egg yolk powder. J Food Sci. [consultado 2015 may 16];65(4):625-629. http://onlinelibrary.wiley.com/doi/10.1111/j.1365-2621.2000.tb16062.x/abstract;jsessionid=B99C2C31A2D62E301BD93239434A0C9A.f01t01. doi: http://doi.org/10.1111/j.1365-2621.2000.tb16062.x. [ Links ]
[FAO] Organización de las Naciones Unidas para la Alimentación y la Agricultura. 2015. Bases de datos. Roma (Italia): fao; [consultado 2015 oct 7]. http://www.fao.org/statistics/databases/es/. [ Links ]
Gabriel AA, Usero JMCL, Rodriguez KJ, Diaz AR, Tiangson- Bayaga CLP. 2015. Estimation of ascorbic acid reduction in heated simulated fruit juice systems using predictive model equations. lwt Food Sci Technol. [consultado 2015 sep 8];64(2):1163-1170. http://www.sciencedirect.com/science/article/pii/S002364381530058X. doi: http://doi.org/10.1016/j.lwt.2015.07.041. [ Links ]
García-Alonso M, Pascual-Teresa S, Santos-Buelga C, Rivas- Gonzalo JC. 2004. Evaluation of the antioxidant properties of fruits. Food Chem. [consultado 2015 sep 16];84(1):13-18. http://www.sciencedirect.com/science/article/pii/S0308814603001602. doi: http://doi.org/10.1016/S0308-8146(03)00160-2. [ Links ]
Gonçalves VK, Fernandes Pereira AL, Rodrigues de Freitas E, Sales Trevisan MT, Correia da Costa JM. 2014. Effect of anacardic acid on oxidative and color stability of spray dried egg yolk. lwt Food Sci Technol. [consultado 2015 oct 2];55(2):466-471. http://www.sciencedirect.com/science/article/pii/S0023643813003496. doi: http://doi.org/10.1016/j.lwt.2013.10.006. [ Links ]
Hernández G. 2010. Desarrollo de un producto de uchuva (Physalis peruviana L.) en polvo secado por atomización adicionado con vitamina C, ácido fólico, hierro y fibra soluble [tesis de maestría]. [Medellín]: Universidad Nacional de Colombia. [ Links ]
Jesse FC. 2000. Vitaminas. En: Fennema OR, director. Química de los alimentos. 2.ª ed. Zaragosa (España): Acribia. [ Links ]
Jiménez-Aguilar DM, Ortega-Regules AE, Lozada-Ramírez JD, Pérez-Pérez MCI, Vernon-Carter EJ, Welti-Chanes J. 2011. Color and chemical stability of spray-dried blueberry extract using mesquite gum as wall material. J Food Comp Anal. [consultado 2015 sep 22];24(6):889-894. http://www.sciencedirect.com/science/article/pii/S0889157511001189. doi: http://doi.org/10.1016/j.jfca.2011.04.012. [ Links ]
Jiménez-Guzmán J, Gómez-Ruiz L, García-Garibay M. 2003. Efecto del tratamiento térmico de la leche sobre la actividad y aplicaciones tecnológicas de diversas enzimas. Inf Tecnol. 14(3):7-12. [ Links ]
Liu F, Li R, Wang Y, Bi X, Liao X. 2014a. Effects of high hydrostatic pressure and high-temperature short-time on mango nectars: changes in microorganisms, acid invertase, 5- hydroxymethylfurfural, sugars, viscosity, and cloud. Innov Food Sci Emerg Technol. [consultado 2015 jun 30];22:22-30. http://www.sciencedirect.com/science/article/pii/S1466856413001975. doi: http://doi.org/10.1016/j.ifset.2013.11.014. [ Links ]
Liu F, Wang Y, Li R, Bi X, Liao X. 2014b. Effects of high hydrostatic pressure and high temperature short time on antioxidant activity, antioxidant compounds and color of mango nectars. Innov Food Sci Emerg Technol. [consultado 2015 may 25];21:35-43. http://www.sciencedirect.com/science/article/pii/S1466856413001537. doi: http://doi.org/10.1016/j.ifset.2013.09.015. [ Links ]
Meléndez-Martínez AJ, Vicario IM, Heredia FJ. 2004. Estabilidad de los pigmentos carotenoides en los alimentos. Arch Latinoam Nutr. 54(2):209-215. [ Links ]
Mendoza-Corvis FA. 2015. Evaluación de las condiciones de secado por aspersión de un producto a base de lactosuero y pulpa de mango variedad Magdalena River (Mangifera indica) adicionado con Bifidobacterium bifidum [tesis de maestría]. [Montería, Colombia]: Universidad de Córdoba. [ Links ]
Mishra P, Mishra S, Mahanta CL. 2014. Effect of maltodextrin concentration and inlet temperature during spray drying on physicochemical and antioxidant properties of amla (Emblica officinalis) juice powder. Food Bioprod Process. [consultado 2015 sep 14];92(3):252-258. http://www.fbp.ichemejournals.com/article/S0960-3085(13)00080-1/abstract. doi: http://doi.org/10.1016/j.fbp.2013.08.003. [ Links ]
Nisha P, Singhal RS, Pandit AB. 2004. A study on degradation kinetics of ascorbic acid in amla (Phyllanthus emblica L.) during cooking. Int J Food Sci Nutr. [consultado 2015 oct 02];55(5):415-422. http://www.tandfonline.com/doi/abs/10.1080/09637480412331321823. doi: http://doi.org/10.1080/09637480412331321823. [ Links ]
Ordóñez-Santos LE, Ospina Portilla MA, Rodríguez Rodríguez DX. 2013. Cinética de degradación térmica de vitamina C en frutos de guayaba (Psidium guajava L.). Rev Lasallista Investig. 10(2):44-51. [ Links ]
Ordóñez-Santos LE, Yoshioka-Tamayo LS. 2012. Cinética de degradación térmica de vitamina C en pulpa de mango (Mangifera indica L.). Vitae. 19(1):81-83. [ Links ]
Peng Z, Li J, Guan Y, Zhao G. 2013. Effect of carriers on physicochemical properties, antioxidant activities and biological components of spray-dried purple sweet potato flours. lwt - Food Sci Technol. [consultado 2015 jun 18];51(1):348-355. http://www.sciencedirect.com/science/article/pii/S0023643812004021. doi: http://doi.org/10.1016/j.lwt.2012.09.022. [ Links ]
Pulido A, Beristain CI. 2010. Encapsulación de ácido ascórbico mediante secado por aspersión, utilizando quitosano como material de pared. Rev Mex Ing Quim. 9(2):189-195. [ Links ]
Remini H, Mertz C, Belbahi A, Achir N, Dornier M, Madani K. 2015. Degradation kinetic modelling of ascorbic acid and colour intensity in pasteurised blood orange juice during storage. Food Chem. [consultado 2015 may 18];173:665-673. http://www.sciencedirect.com/science/article/pii/S0308814614016318. doi: http://doi.org/10.1016/j.foodchem.2014.10.069. [ Links ]
Ribeiro SMR, Schieber A. 2010. Bioactive compounds in mango (Mangifera indica L.). En: Ross R, Preedy V, editores. Bioactive foods in promoting health. London: Elsevier. [ Links ]
Ruiz D, Egea J, Tomás-Barberán FA, Gil MI. 2005. Carotenoids from new apricot (Prunus armeniaca L.) varieties and their relationship with flesh and skin color. J Agric Food Chem. [consultado 2015 jun 2];53(16):6368-6374. http://pubs.acs.org/doi/abs/10.1021/jf0480703. doi: http://doi.org/10.1021/jf0480703. [ Links ]
Sikorska-Wisniewska G, Szumera M. 2007. The role of food components in children's nutrition. En: Sikorski ZE, editores. Chemical and functional properties of food components. 3.ª ed. Florida, EE. UU.: Taylor y Francis Group. [ Links ]
Torres B, Tiwari BK, Patras A, Cullen PJ, Brunton N, O'Donnell CP. 2011. Stability of anthocyanins and ascorbic acid of high pressure processed blood orange juice during storage. Innov Food Sci Emerg. [consultado 2015 may 24];12(2):93-97. http://www.sciencedirect.com/science/article/pii/S1466856411000087. doi: http://doi.org/10.1016/j.ifset.2011.01.005. [ Links ]
Uddin MS, Hawlader MN, Zhu HJ. 2001. Microencapsulation of ascorbic acid: effect of process variables on product characteristics. J Microencapsul. [consultado 2015 sep 20];18(2):199-209. http://www.tandfonline.com/doi/abs/10.1080/02652040010000352. doi: http://doi.org/10.1080/02652040010000352. [ Links ]
Wang H, Hu X, Chen F, Wu J, Zhang Z, Liao X, Wang Z. 2006. Kinetic analysis of non-enzymatic browning in carrot juice concentrate during storage. Eur Food Res Technol. [consultado 2015 jun 2];223(2):282-289. http://link.springer.com/article/10.1007%2Fs00217-005-0202-z. doi: http://doi.org/10.1007/s00217-005-0202-z. [ Links ]
Wibowo S, Grauwet T, Gedefa GB, Hendrickx M, Van Loey A. 2015a. Quality changes of pasteurised mango juice during storage. Part I: Selecting shelf-life markers by integration of a targeted and untargeted multivariate approach. Food Res Int. [consultado 2015 may 15];78: 396-409. http://www.sciencedirect.com/science/article/pii/S0963996915301769. doi: http://doi.org/10.1016/j.foodres.2015.09.002. [ Links ]
Wibowo S, Grauwet T, Gedefa GB, Hendrickx M, Van Loey A. 2015b. Quality changes of pasteurised mango juice during storage. Part II: Kinetic modelling of the shelf-life markers. Food Res Int. [consultado 2015 jun 25];78:410-423. http://www.sciencedirect.com/science/article/pii/S0963996915301757. doi: http://doi.org/10.1016/j/foodres.2015.09.001. [ Links ]
Yahia EM, Contreras-Padilla M, Gonzalez-Aguilar G. 2001. Ascorbic acid content in relation to ascorbic acid oxidase activity and polyamine content in tomato and bell pepper fruits during development, maturation and senescence. LWT - Food Sci Technol. [consultado 2015 jun 10];34(7):452-457. http://www.sciencedirect.com/science/article/pii/S002364380190790X. doi: http://doi.org/10.1006/fstl.2001.0790. [ Links ]














