Introducción
Los preparados cárnicos son definidos por la legislación europea (European Commission, 2004) como aquellos productos provenientes de carne fresca reducida a fragmentos a los que se les pueden añadir condimentos o aditivos, pero que no han sufrido procesos que modifiquen la estructura de su fibra muscular interna o eliminen su característica de carne fresca.
Respecto al uso de aditivos, hay una tendencia en la industria alimentaria a la utilización de sustancias naturales, sintetizadas por las plantas, que se ha reconocido como antimicrobiana efectiva en un amplio espectro microbiano (Recio et al., 1989). Tal es el caso del romero (Rosmarinus officinalis), de interés por su actividad antioxidante (López-Luengo, 2012; Vergara-Vélez et al., 2016), y la colza (Brassica napus), por su contenido de ácidos grasos benéficos para la salud humana, además de sus compuestos volátiles y aromas provenientes de su flor (Machado et al., 2021; Ruisinger & Schieberle, 2012). La miel, al provenir de los néctares de las plantas, cuenta entre sus componentes minoritarios con flavonoles, fenoles, flavonoides, ácidos fenólicos, ácido ascórbico, ácidos grasos y otros, lo cual le confiere muchas de las propiedades antioxidantes y antimicrobianas que le otorgan las plantas, pero también que le aportan las abejas.
Las mieles que proceden del romero destacan especialmente por su buena actividad antioxidante, posiblemente porque gran parte de sus compuestos fenólicos se corresponden con ácidos del tipo rosmarínico (Jovanović et al., 2021), los cuales contribuyen junto con los demás compuestos al efecto sobre el crecimiento microbiano (Estevinho et al., 2008). Estudios hechos por Rojo (2013), Istrati et al. (2011), Alabdulkarim et al. (2012), Naveena et al. (2007) y Tänavots et al. (2018) han incorporado miel y mielato en preparaciones cárnicas de pollo y ternera, con resultados positivos en reducción de reacciones oxidativas y ralentización de crecimiento microbiano, lo cual demuestra su efecto conservante, sin embargo, su viscosidad por el alto contenido de azúcares dificulta su manejo como aditivo (Machado De-Melo et al., 2018; Samborska, 2019), lo cual ha potenciado la investigación en pulverización de miel, con el uso de vehículos de mezcla que faciliten su pulverización para posteriormente ser incorporada en cualquier matriz alimentaria sin los problemas de manejo de miel la líquida o cristalizada.
Algunos estudios (Samborska, 2019; Samborska et al., 2017, 2019; Samborska & Czelejewska, 2014) han evaluado la obtención de miel en polvo con diferentes aditivos (goma arábiga, caseinato de sodio) y métodos (spray drying, diafiltración y aglomeración), con aceptables resultados en cuanto a la estabilidad de la miel. Nurhadi et al. (2012) obtuvieron miel en polvo usando goma arábiga con secado al vacío y Samborska & Czelejwska (2014) también reportaron características aceptables de miel en polvo a partir de miel de colza, sin embargo, además del desarrollo de los métodos de obtención de miel en polvo natural que permita la eficiencia en su manejo como aditivo en aplicaciones alimentarias, es importante evaluar su efecto sobre la calidad microbiológica del alimento objeto de estudio. Así, algunos estudios ya dan cuenta del uso de miel en polvo: Tong et al. (2010) y Sathivel et al. (2013), quienes utilizaron miel en polvo en panificación, encontrando potencialidad de uso en esta industria; también Kılınç & Demir (2017), quienes hallaron la posibilidad de sustituir el azúcar por miel en polvo, mejorando las características nutricionales y sensoriales de galletas y Antony et al. (2006), quienes emplearon miel en polvo (5 % y 15 %) sobre carne de pavo, obteniendo aceptables resultados en cuanto su efecto antioxidante.
El empleo en carne molida puede ser interesante por la posibilidad de conseguir la adición de miel de forma homogénea al producto. En estudios previos, Rojo (2013) añadió miel de romero y mielatos en polvo (mezcla harina miel en proporciones entre 50:50 y 70:30), obtenida por deshidratación a vacío a carne molida de ternera (19 % p/p de miel), y observó una reducción de la oxidación de los lípidos y el crecimiento de aerobios mesófilos y bacterias ácido-lácticas. De modo que, como se observa, la miel tiene variadas posibilidades e interesantes perspectivas de uso en la industria alimentaria, sola o como componente de diferentes matrices, en búsqueda de mejoramiento de características sensoriales, fisicoquímicas o microbiológicas en diferentes productos. En este sentido, planteamos la hipótesis de que es posible el uso de miel liofilizada en mezcla con harina de trigo como conservante de carne molida, manteniendo sus características fisicoquímicas. En consecuencia, este trabajo tiene como objetivo evaluar el efecto de la adición de la miel multifloral de romero y colza pulverizada, mediante liofilización (para mantener en mayor medida las características de la miel) en dos concentraciones diferentes y empleando harina de trigo como agente transportador y ligante, sobre las características fisicoquímicas y microbiológicas de la carne molida de ternera almacenada en refrigeración.
Materiales y métodos
Materias primas
Se emplearon 1,4 kg de carne (contratapa de ternera) comprada ya molida en un local comercial 10 días post mortem, almacenada en su empaque original al vacío a 4 ºC ± 1 ºC y usada un día después de su compra. Miel multifloral de romero (Rosmarinus officinalis) y colza (Brassica napus) fue donada por la Asociación de Apicultores de Navarra (España) y almacenada en oscuridad a 20 ºC ± 2 ºC hasta su uso. Esta miel fue usada por su procedencia botánica, dada la referida capacidad antioxidante de este tipo de miel y además por tener un color claro. Además, se utilizó harina de trigo comercial (Granollers, Barcelona, España).
Obtención de miel en polvo
Se prepararon 10 muestras de 20 g de miel y harina al 50 % (p/p) mediante agitación (Rojo, 2013; Suberviola, 2020), las cuales fueron liofilizadas a presión de vacío de 0,100 mbar con un secado primario durante 6 h a 15 ºC y un secado secundario de 9 h a 25 ºC, en un liofilizador Lyobeta25 (Telstar Industrial, S. L., Barcelona, España). Por último, se trituró la mezcla liofilizada en un molino (Moulinex, Mayenne, Francia) con una potencia de 180 W durante 5 s aproximadamente, hasta obtener la pulverización total del producto buscando que sea homogéneo y no requiera de tamizaje para evitar que quede miel en el residuo. El resultado se empacó en bolsas plásticas de autocierre de polietileno, las cuales se almacenaron en un desecador para evitar la rehidratación.
Aplicación de los tratamientos
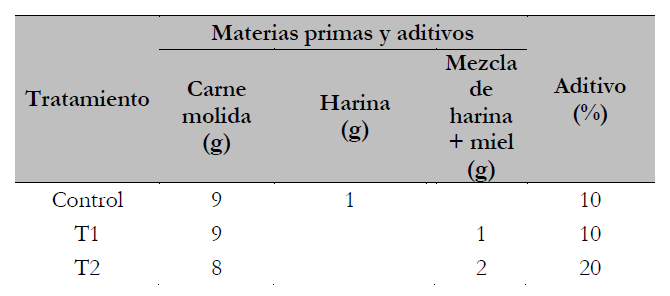
Se usaron muestras de 10 g de carne molida en forma de hamburguesa. Se elaboraron 48 muestras por cada tratamiento con la formulación y las cantidades indicadas en la tabla 1, incorporando manualmente la harina y la mezcla de harina más miel liofilizada a la carne (aditivo).
Empaque y almacenamiento
Las muestras se empacaron sin aplicación de ningún tipo de tecnología de atmósfera modificada, en bolsas de poliamida/polietileno (PA20/PE70 TR 300,0, España) que se sellaron térmicamente (Sacopisa SB-400-ECO, Barcelona, España) y se almacenaron a 4 ºC ± 1 ºC hasta su evaluación. Se prepararon 12 bolsas de cuatro muestras por tratamiento (3 bolsas para cada día de análisis).
Para los análisis de pH y color se tomaron tres muestras por cada bolsa por tratamiento y por día de seguimiento. Adicionalmente, se usó una muestra por bolsa por tratamiento y por día de seguimiento para el análisis microbiológico.
Parámetros fisicoquímicos de la miel
Para la miel, se midió contenido de agua, actividad del agua, sólidos solubles, acidez libre, conductividad eléctrica y pH, de acuerdo con la metodología oficial del análisis de la miel en España (Codex Committee on Sugars, 1981). Para la determinación de color, se midieron las coordenadas L*, a* y b* del espacio CIELab usando un equipo DigiEye (VeriVide, Leicester, Reino Unido), de acuerdo con el procedimiento descrito por Matusiak (2015). De esta manera se analizaron cinco áreas de la imagen para cada repetición (n = 3).
Contenido de fenoles totales
El contenido de los fenoles totales de la miel se determinó siguiendo el método Folin-Ciocalteu (Bobo-García et al., 2015) y los resultados se expresaron como mg de ácido gálico equivalente por 100 g de miel.
Contenido de flavonoides
El contenido de flavonoides de la miel se determinó usando el método de cloruro de aluminio descrito por Meda et al. (2005) y los resultados se expresaron como mg de quercetina por 100 g de miel.
Actividad antioxidante
La actividad antioxidante se evaluó mediante el ensayo 2,2-diphenyl-1-picrylhydrazyl (DPPH), siguiendo el método descrito por Bobo-García et al. (2015), y los resultados se expresaron como µmol Trolox (6-hydroxy-2,5,7,8-tetramethylchroman-2-carboxylic acid) equivalente por 100 g de miel.
Análisis microbiológico de las muestras tratadas
Se analizaron aerobios mesófilos totales, enterobacterias y psicrótrofos en el día 0 de tratamiento y a los 3, 7 y 10 días de almacenamiento en refrigeración, siguiendo los métodos oficiales de análisis microbiológico descritos en el manual de análisis bacteriológico para alimentos (U.S. Food & Drug Administration, 1995).
Parámetros fisicoquímicos de las muestras tratadas
Todos los parámetros fisicoquímicos se determinaron por triplicado en el día 0 de tratamiento y a los 3, 7 y 10 días de almacenamiento en refrigeración.
El pH se midió en diferentes sitios de cada muestra con un pH-metro (Sentron Europe B. V., Países Bajos) equipado con un punzón metálico. Las coordenadas de color L*, a* y b* se determinaron con un espectrofotómetro (Minolta CM-2500d, Minolta Co., Japón), el espacio de color CIELab con iluminante D65 y un observador de 10 º.
Análisis estadístico
Los datos se trataron con un análisis de varianza unidireccional (α = 0,05) y cuando se encontraron diferencias significativas entre las medias, se compararon mediante prueba Tukey. El análisis estadístico se realizó con el programa estadístico IBM SPSS 25 de Windows (IBM Corp., Nueva York, Estados Unidos).
Resultados y discusión
Caracterización de la miel
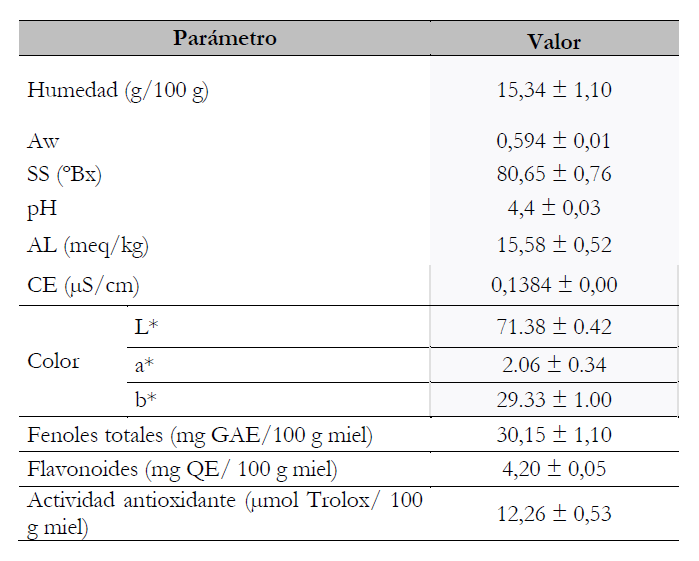
La tabla 2 muestra los resultados de la caracterización de la miel. El valor de pH obtenido en la muestra usada en este estudio es algo superior al observado por Oroian et al. (2013) en mieles multiflorales y de romero (entre 3,78 ± 0,03 y 3,86 ± 0,03). Respecto al color, los datos de este estudio (tabla 2) coinciden con lo enunciado por Gómez-Pajuelo (2004), quien afirma que la miel de romero se caracteriza por ser una miel clara (alto valor en L* y bajos valores en a* y b*). Los valores de los fenoles encontrados se sitúan entre los reportados por otros autores para mieles de romero (Alves et al., 2013; Anjos et al., 2015; Boussaid et al., 2018), encontrándose entre las mieles con valores medio-bajos de estos compuestos (15-78 mg GAE/100 g). De la misma manera, se observó en los estudios de Boussaid et al. (2018) que el contenido de flavonoides es bajo (1,62 mg QE/100 g), pero a pesar de este bajo contenido en fenoles y flavonoides, la actividad antioxidante de esta miel es elevada, lo que puede deberse a la presencia de ácidos orgánicos del tipo rosmarínico, entre otros (Fernández-López et al., 2005; Jovanović et al., 2021).
Caracterización de la carne molida
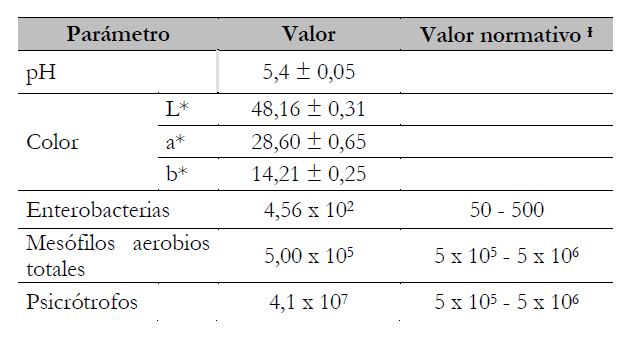
La tabla 3 muestra la medición de parámetros para la carne molida antes de la aplicación de los tratamientos. La carga inicial de enterobacterias y mesófilos aerobios totales se encontró dentro de los límites normativos (European Commission, 2005). Cabe destacar que en el caso de las enterobacterias, hubo un recuento prácticamente en los límites, sin embargo, en el caso de los psicrótrofos los recuentos se superan, posiblemente a causa de la manipulación y el almacenamiento posteriores a su adquisición.
Evaluación de la calidad de la carne durante su almacenamiento
Análisis microbiológico
Enterobacterias
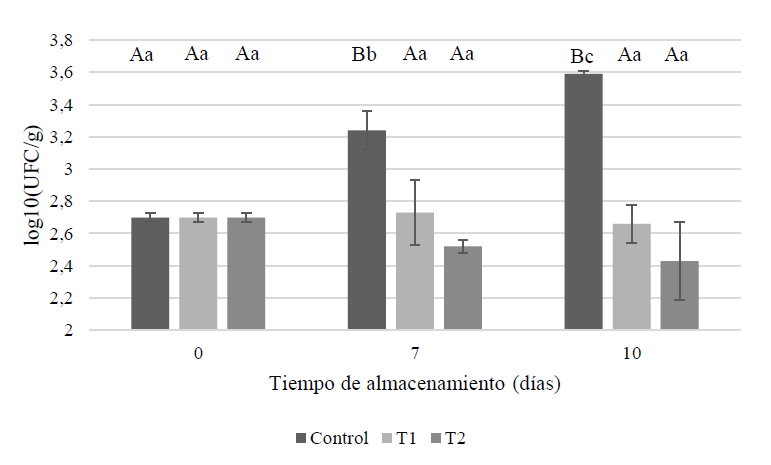
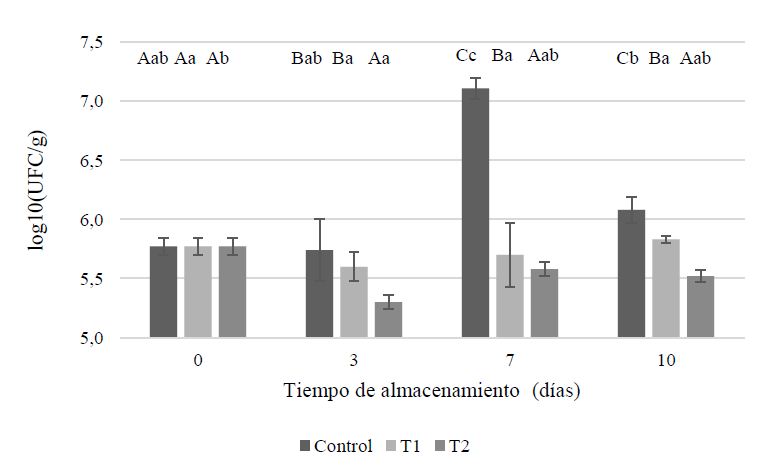
En la figura 1 se muestran los datos obtenidos del recuento de enterobacterias de todas las muestras a lo largo del tiempo de almacenamiento. Para el día 3 se obtuvieron resultados anormales, por lo cual no se consideraron válidos. La figura 1 muestra claramente el incremento del recuento de enterobacterias con el tiempo en la muestra control y en las muestras tratadas, sin embargo, se observa que la aplicación de la miel frena el crecimiento microbiano, puesto que, pese a no encontrarse diferencias significativas entre T1 y T2 en el tiempo, sí disminuye el recuento para enterobacterias en los días 7 y 10 frente a la muestra control y se nota una mayor disminución con el T2. La ralentización del crecimiento microbiano en carne molida, por el efecto de la adición de miel deshidratada, fue también observado por Rojo (2013).
Mesófilos aerobios totales
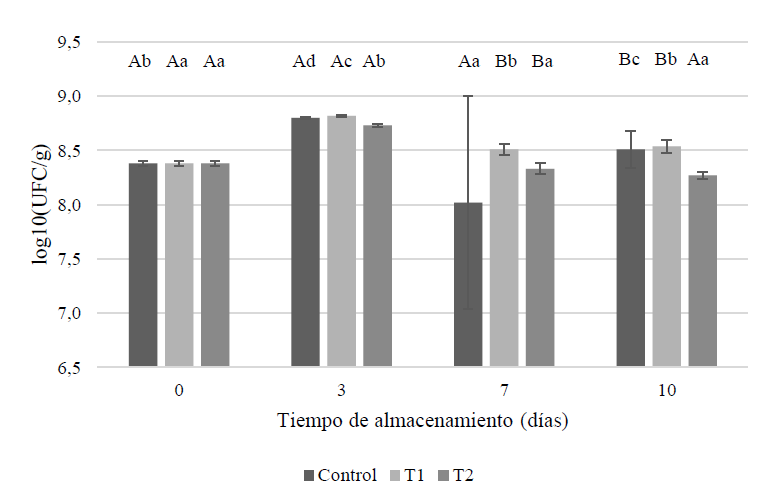
La figura 2 muestra el comportamiento de la población en mesófilos aerobios totales. Se puede observar el efecto de los tratamientos con miel sobre las muestras a lo largo del tiempo, con una significativa reducción del recuento microbiano, sobre todo con el uso del 20 % de miel (T2) a partir del día 3, aunque pequeña (< 1 log), sin embargo, el mayor efecto sobre estos microorganismos se logra evidenciar entre los tratamientos que incluyen miel y el tratamiento control. Esta reducción del crecimiento de mesófilos aerobios totales fue observada también por Istrati et al. (2011), quienes ensayaron aplicaciones que incluían miel sobre carne marinada empacada al vacío, López-Patiño et al. (2021), quienes emplearon miel con propóleo en filetes de carne de ternera y Rojo (2013), quien reportó una reducción del crecimiento de aerobios mesófilos totales entre 0,5 y 1 unidades logarítmicas de unidades formadoras de colonias, tras la aplicación antimicrobiano de miel y mielato en carne molida durante seis días a 4 ºC.
Fuente: Elaboración propia
Figura 1. Crecimiento de enterobacterias en muestras tratadas durante el almacenamiento refrigeradoNota: Los valores representan la media de tres mediciones para cada tratamiento y el día de evaluación. Las letras mayúsculas significan diferencias significativas (p < 0,05) entre tratamientos por cada día de evaluación y las letras minúsculas indican diferencias significativas (p < 0,05) entre los días de evaluación para cada tratamiento.
Fuente: Elaboración propia
Figura 2. Crecimiento de mesófilos aerobios totales en muestras tratadas durante el tiempo de almacenamientoNota: Las letras mayúsculas significan diferencias significativas (p < 0,05) entre tratamientos por cada día de evaluación y las letras minúsculas indican diferencias significativas (p < 0,05) entre los días de evaluación para cada tratamiento.
Psicrótrofos
La figura 3 muestra el recuento para psicrótrofos, donde no se encontró efecto de la adición de la miel en el control de este grupo específico de microorganismos.
Ph
La tabla 4 muestra la evolución del pH en las muestras tratadas durante los 10 días del almacenamiento refrigerado. El pH desciende ligeramente durante el almacenamiento en todos los casos, sin embargo, solo existe una diferencia significativa en el día 10 entre la muestra control y los tratamientos T1 y T2, siendo el pH del T2 (20 %) el más bajo. A pesar de ello, los tratamientos T1 y T2 registraron valores menores frente a la muestra control en el día 0 de la aplicación, esto puede deberse a que el pH de la miel (alrededor de 4,4) es más bajo que el de la carne (alrededor de 5,4).
Estos resultados concuerdan con los de Rojo (2013), quien encontró un descenso en el pH para la carne tratada con miel y mielato, atribuido a los carbohidratos de la miel que pueden servir como sustratos de bacterias ácido-lácticas, con la consecuente producción de ácidos orgánicos. Así, resultados similares se encontraron en las muestras de carne de pollo con miel (Naveena et al., 2007), empanadas de pollo tratadas con miel y una mezcla de especias (Alabdulkarim et al., 2012) y carne tratada con una mezcla de miel y propóleo (López-Patiño et al., 2021), quienes atribuyeron la disminución del pH en general al crecimiento de enterobacterias durante el tiempo de almacenamiento. Por último, cabe destacar el aumento de pH en la muestra control y en el T1 en el día 10 frente al día 7, mientras que en el T2 continuó su descenso hasta este último día de almacenamiento evaluado, posiblemente por la presencia de los ácidos orgánicos mencionados; en tanto que para los tratamientos donde hay menores de cantidades de miel, el incremento podría deberse al envejecimiento de la muestra (Jin et al., 2007) al final del periodo de almacenamiento, por la carencia del efecto conservante que pudiera generar la miel.
Tabla 4. pH de las muestras tratadas durante el almacenamiento
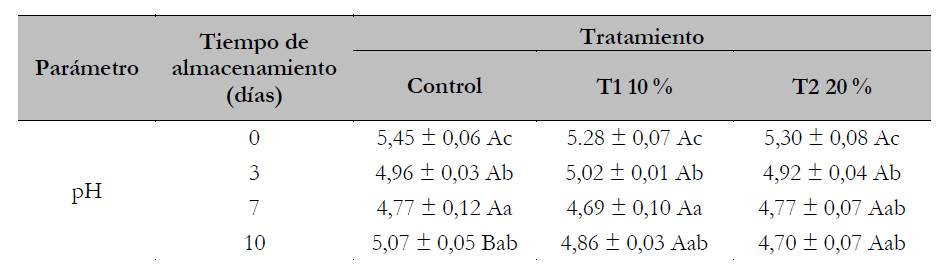
Nota:Los valores representan la media de tres mediciones para cada tratamiento y el día de evaluación. Intervalo de confianza (p < 0,05) para la media, las letras mayúsculas significan diferencias significativas (p < 0,05) entre tratamientos por cada día de evaluación y las letras minúsculas indican diferencias significativas (p < 0,05) entre los días de evaluación para cada tratamiento.
Fuente: Elaboración propia
Fuente: Elaboración propia
Figura 3. Crecimiento de psicrótrofos en las muestras tratadas durante el tiempo de almacenamientoNota: Las letras mayúsculas significan diferencias significativas (p < 0,05) entre tratamientos por cada día de evaluación y las letras minúsculas indican diferencias significativas (p < 0,05) entre los días de evaluación para cada tratamiento.
Color
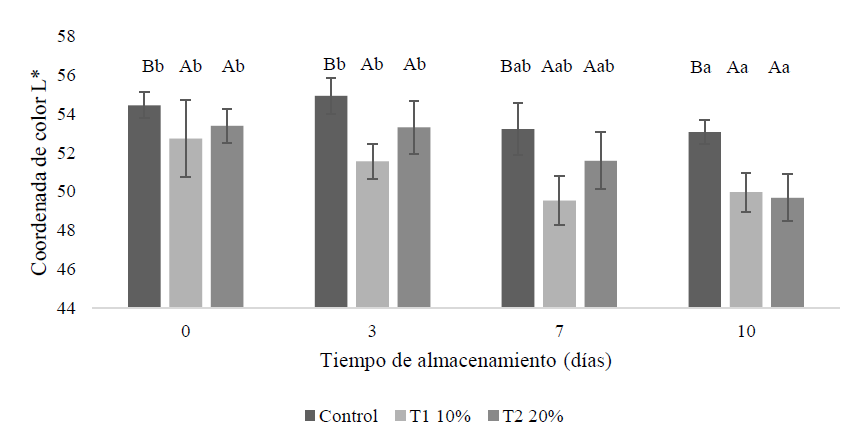
Las figuras 4 y 5 muestran los resultados para las coordenadas de color en el espacio CIELab: L* (luminosidad) y a* (rojo-verde), respectivamente. La luminosidad se incrementa significativamente en la muestra control y en los tratamientos frente al dato en la carne molida sin ninguna adición, lo que se reporta en la tabla 3 y con lo cual se puede deducir el efecto de la adición de harina y harina-miel que le agrega un tono más claro a las muestras, posiblemente por los mayores valores de L* de la miel, sumado al color blanco propio de la harina.
Por otra parte, como se puede observar en la figura 4, la luminosidad disminuye ligeramente con la aplicación de los tratamientos en el día 0. Desde este día y durante todo el almacenamiento también se registraron valores significativamente menores en este parámetro en las muestras tratadas con respecto a la muestra control para cada día de evaluación. Resultados similares obtuvo Rojo (2013) en su estudio usando miel de romero en concentraciones de 5 %, 10 % y 15 % como conservante en falda de ternera, donde encontró que la luminosidad de las muestras disminuyó con las adiciones mencionadas. Pese al incremento inicial del valor L* por efecto de los tratamientos (control, T1 y T2 respecto a carne sin ninguna adición), es posible que la miel pueda impartir una tonalidad más oscura a la carne inicialmente, produciéndose además una reducción de la luminosidad con el tiempo como resultado de los procesos oxidativos de la carne, ya que los cambios en el color de esta son causados por las modificaciones en los estados de la mioglobina (pigmento responsable del color), dependiendo de su exposición al oxígeno, porque en presencia de oxígeno y al cabo de un tiempo, la mioglobina pasa a estado de metamioglobina (MMb), la cual le da una tonalidad oscura a la carne (Hernández-Salueña et al., 2019).
Fuente: Elaboración propia
Figura 4. Coordenada L* de color del espacio CIELab de las muestras tratadas durante el almacenamientoNota: Las letras mayúsculas indican diferencias significativas (p < 0,05) entre tratamientos y para cada tratamiento las letras minúsculas indican diferencias significativas (p < 0,05) entre los días de evaluación.
La figura 5 muestra el comportamiento de las muestras tratadas frente a la coordenada de color a*. En todos los casos hubo una disminución de los valores para esta coordenada durante el almacenamiento, lo cual puede ser un indicio de la oxidación de la carne con el paso del tiempo.
Disminuciones similares para el valor de a* se encontraron en estudios hechos por Rojo (2013), López-Gajardo (2018), Li et al. (2020) y Hernández-Salueña et al. (2019), quienes relacionaron estos cambios de color con la función redox de la mioglobina como responsable del color de la carne. En cuanto al efecto de los tratamientos con miel sobre el parámetro a*, en el día 0 se observó en la muestra control un valor significativamente mayor que en las muestras T1 y T2, esto puede justificarse, además, por el bajo valor para a* de la miel, es decir, un color claro nada rojizo que, sumado al color blanco de la harina, también puede contrarrestar el color rojo natural de la carne. Esta diferencia entre tratamientos desaparece durante el almacenamiento, pero al final (día 10) se encuentra al contrario un valor de a* ligeramente menor en la muestra control con respecto a las muestras tratadas, aunque no significativamente diferente. Estos resultados pueden indicar que la miel finalmente logra un efecto antioxidante, dado el leve incremento en color rojo para las muestras con contenido de miel. Lo anterior, en razón, como se ha comentado, a la capacidad antioxidante de la miel por su contenido de compuestos bioactivos, tipo fenoles y flavonoides, cuyas moléculas retardan o previenen la oxidación de otras moléculas actuando como agentes reductores.
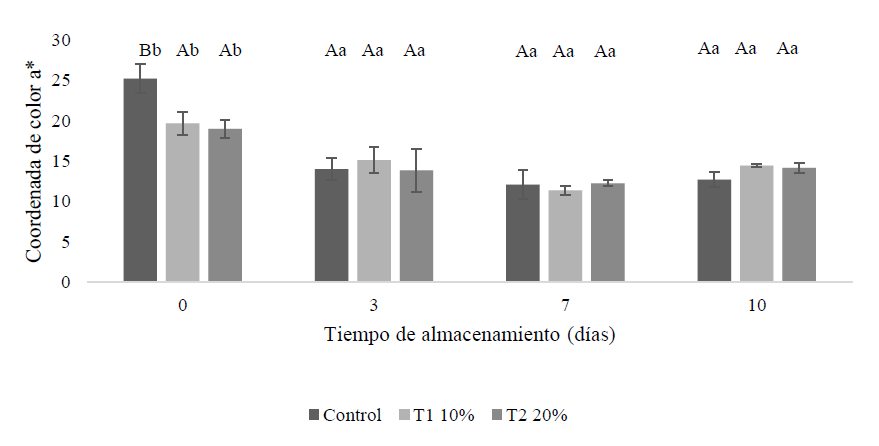
Fuente: Elaboración propia
Figura 5. Coordenada a* de color del espacio CIELab de las muestras tratadas durante el almacenamientoNota: Las letras mayúsculas indican diferencias significativas (p < 0,05) entre tratamientos y para cada tratamiento las letras minúsculas indican diferencias significativas (p < 0,05) entre los días de evaluación.
Respecto a la coordenada de color b*, no se encontraron diferencias significativas ni en tratamientos ni a lo largo del tiempo de almacenamiento. El valor más bajo se registró para el T2 en el día 10 (11,49 ± 0,78) y el más alto para la muestra control en el día 0 (13,93 ± 1,20). Lo anterior permite inferir que la adición de miel a la carne molida no tuvo efecto sobre esta coordenada de color y que su tonalidad amarilla se mantuvo a lo largo del tiempo, pese a la aplicación de los tratamientos.
Conclusiones
La incorporación de la miel multifloral de romero y colza y harina liofilizada en carne molida puede ralentizar el crecimiento microbiano de enterobacterias y aerobios mesófilos totales, incrementándose ligeramente el efecto al pasar de 10 % a 20 % de concentración de miel en la carne molida. Este efecto no se observó en cambio para los psicrótrofos, sin embargo, la aplicación de la mezcla harina y miel (liofilizada) afecta el color de las muestras, reduciendo los valores de L*(luminosidad) y a* (verde-rojo), aunque este efecto desaparece a lo largo del almacenamiento en este último parámetro.
Con los resultados de este estudio se concluye que la utilización de miel en los productos cárnicos es una buena alternativa para su conservación, junto con la adición de harina, para facilitar su manejo como miel en polvo y es una alternativa viable. A partir de estos resultados, se sugieren nuevos estudios que incluyan el seguimiento de más parámetros para la calidad de la carne, como, por ejemplo, un seguimiento a la oxidación y un análisis sensorial que permitan evaluar el uso de la miel en polvo liofilizada como conservante en la industria cárnica, así como la utilización de la miel de otros orígenes botánicos.
Contribución de los autores
Carmenza López-Patiño: diseño de metodologías, construcción de bases de datos, registro y análisis de información y elaboración de manuscrito; Cristina Arroqui: diseño de metodologías, análisis de información y revisión; Sandra Horvitz: construcción de bases de datos, análisis de información y revisión; Paloma Virseda: elaboración de proyecto para acceso a recursos económicos, diseño de metodologías, análisis de información y revisión.