Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de Medicina Veterinaria
Print version ISSN 0122-9354
Rev. Med. Vet. no.28 Bogotá July/Dec. 2014
Aspergilosis nasal en un perro:
reporte de un caso
Camilo Padilla Peñuela1 / Vladimir Galindo Z.2
1 MSc. Corporación Universitaria Lasallista, Facultad de Ciencias Administrativas y Agropecuarias, Caldas, Antioquia.
japadilla@lasallistadocentes.edu.co
2 PhD. Universidad Nacional, Facultad de Medicina Veterinaria y de Zootecnia, Bogotá, Colombia.
Recibido: 18 de marzo del 2013. Aceptado: 26 de abril del 2014
Cómo citar este artículo: Padilla Peñuela C, Galindo V. Aspergilosis nasal en un perro: reporte de un caso. Rev Med Vet. 2014;(28): 81-9.
Resumen
La aspergilosis nasal es una de las principales causas de afección crónica de las fosas nasales en el canino. La sinología clínica es típica en toda enfermedad nasal crónica. Se presenta sobre todo epistaxis y ocasionalmente dolor. La evaluación rinoscópica de la zona permite encontrar hallazgos asociados con la patología y tomar muestras para citología y cultivo. La terapéutica sistémica con antifúngicos orales ha sido de utilidad variable, pero actualmente se ha remplazado con la medicación tópica directa en el área afectada. Este artículo describe el caso clínico de un canino, macho de cuatro años de edad, que fue presentado a consulta por secreción nasal mucosanguinolenta unilateral con una semana de evolución. El paciente se venía tratando en otro centro veterinario con ciclonamina y vitamina K por un posible trastorno en la coagulación. Después de una serie de exámenes que incluyeron rinoscopia y cultivo para hongos, se diagnosticó aspergilosis nasal. Se realizaron dos aplicaciones de clotrimazol intranasal que permitieron la resolución de los signos clínicos.
Palabras clave: aspergilosis nasal, canino, rinoscopia, clotrimazol.
Nasal Aspergillosis in a Dog:
A Case Report
Abstract
Nasal aspergillosis is a major chronic disease affecting the nostrils in dogs. Clinical sinology is typical in every chronic nasal disease. Epistaxis and occasional pain occurs. Rhinoscopic assessment of the area evidences findings associated with the pathology and allows collecting samples for cytology and culture. Systemic therapy with oral antifungals has had variable utility, but now it has been replaced by direct topical medication to the affected area. This article describes the case of a 4-years-old male dog, submitted to consultation by unilateral muco-bloody nasal discharge with a week of evolution. The patient was treated by another vet center with cyclonamine and vitamin K for a possible clotting disorder. After a series of tests that included rhinoscopy and fungal culture, nasal aspergillosis was diagnosed. Intranasal clotrimazole was applied twice and it allowed the resolution of the clinical signs.
Keywords: nasal aspergillosis, canine, rhinoscopy, clotrimazole.
Aspergilose nasal em um cachorro:
reporte de um caso
Resumo
A aspergilose nasal é uma das principais causas de afecção crônica das fossas nasais no canino. A sinologia clínica é típica em toda doença nasal crônica. Apresenta-se sobre tudo epistaxe e ocasionalmente dor. O exame rinoscópico da zona permite encontrar achados associados com a patologia e tomar amostras para citologia e cultivo. A terapêutica sistêmica com antifúngicos orais tem sido de utilidade variável, mas atualmente substituiu-se com a medicação tópica direta na área afetada. Este artigo descreve o caso clínico de um canino, macho de 4 anos de idade, que foi apresentado à consulta por secreção nasal muco sanguinolento unilateral com uma semana de evolução. O paciente estava sendo tratado em outro centro veterinário com ciclonamina e vitamina K por um possível transtorno na coagulação. Depois de uma série de exames que incluíram rinoscopia e cultivo para fungos, se diagnosticou aspergilose nasal. Realizaram-se duas aplicações de clotrimazol intranasal que permitiram a resolução dos sinais clínicos.
Palavras chave: aspergilose nasal, canino, rinoscopia, clotrimazol.
INTRODUCCIÓN
La aspergilosis sinonasal es la segunda causa en importancia de secreción nasal, después de la neoplasia de esta misma ubicación (1). Está entre el 7 y el 34% de las patologías generadoras de enfermedad nasal crónica (2,3). El Aspergillus es un hongo saprófito de ubicación ambiental, que suele causar infecciones nasales o pulmonares en perros y gatos. En un día normal, un perro puede inhalar entre 10 y 15 esporas del hongo (3-5). El término aspergilosis se aplica generalmente a infecciones ocasionadas por hongos de los géneros Aspergillus y Penicillium, ya que son indistinguibles morfológicamente cuando se examinan por citología o histología (6,7).
DESCRIPCIÓN DEL CASO
Se presentó a consulta un canino beagle, macho de cuatro años de edad por estornudo y sangrado nasal durante una semana. Para ese momento el paciente presentó actitud y apetito normal; previamente, en otro servicio veterinario, se administró ciclonamina y vitamina K a dosis y vías desconocidas. Como historia adicional, el paciente asistía a un colegio canino diariamente en una finca en la sabana de Bogotá, en la cual interactuaba con otros perros y llevaba varios meses de tratamiento por una pododermatitis micótica de los miembros anteriores con medicamentos y dosis desconocidas.
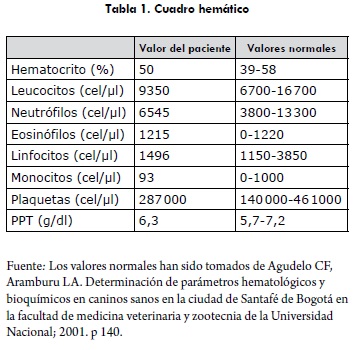
En el examen clínico, el paciente se encontró alerta, con temperamento nervioso, peso de 16 kg, tiempo de llenado capilar de 2 s, membranas mucosas rosadas, frecuencia cardiaca de 120 ppm, frecuencia respiratoria de 38 rpm y temperatura de 38,7°C. Como hallazgos anormales se encontraron: aumento en la condición corporal (3,5/5); lesiones alopécicas y eritematosas entre los dedos de los miembros anteriores (la propietaria comentó que se rascaba y lamía las patas desde hace más de dos meses); aumento de reflejo tusígeno y secreción mucosanguinolenta de leve a moderada por la fosa nasal izquierda. Como diagnósticos diferenciales para ese momento se plantearon: a) traqueobronquitis infecciosa (para la tos y el aumento del reflejo tusígeno); b) lesión vascular local (vaso nasal sangrante), trauma, cuerpo extraño, aspergilosis nasal, neoplasia nasal, rinitis alérgica (para la secreción nasal), y c) dermatofitósis podal (para los signos dermatológicos). Como planes diagnósticos se realizó un cuadro hemático que se encontró dentro de los valores normales (tabla 1).
Como plan terapéutico para este momento se instauró meloxicam (O,1 mg/kg PO SID) durante 6 días, clorfeniramina (4 mg DT PO BID) durante 8 días y pediluvios con una solución de acetato de aluminio en agua TID por 8 días. Después de 10 días de tratamiento, el paciente continuaba con sangrado nasal y tos, por lo cual se realizó la toma de placas radiográficas de tórax, tráquea extratorácica y cráneo, en las que no se observaron alteraciones. Para este momento se mantenía como principal diagnóstico diferencial la traqueobronquitis infecciosa y se instauró como plan terapéutico amoxicilina + ácido clavulánico (12,5 mg/kg PO BID) durante 7 días y bromhexina (1,5 mg PO TID) durante 7 días.
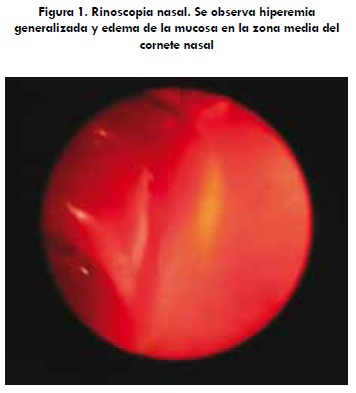
Luego de 10 días de tratamiento, el paciente volvió a control; continuaba con sagrado nasal pero ya no presentaba tos. Para este día se realizó rinoscopia, citología y toma de muestras para cultivo de hongos. En la rinoscopia se encontró la mucosa nasal con hiperemia generalizada, edema de la mucosa de la zona media del cornete nasal, leve exudación serosanguinolenta, y no se encontraron masas o estructuras ajenas al ambiente nasal (figura 1). También se observó una leve elongación del paladar blando; los cartílagos aritenoideos se encontraron de coloración normal con leve presencia de moco originado desde las coanas. En la citología, se observaron incontables neutrófilos y gran cantidad de eritrocitos intactos junto con unas pocas células epiteliales con leves anormalidades morfológicas. No se encontraron microorganismos. En el cultivo de hongos se aisló: Penicillum spp., Aspergilus spp. y Chaelomun spp. Por lo anterior, el diagnóstico de trabajo fue Aspergilosis nasal y se instauró como nuevo plan terapéutico Itraconazol (5 mg/kg PO BID) durante 90 días.
Posterior a 30 días de tratamiento, el paciente continuaba presentando secreción nasal muco-sanguinolenta y leve secreción seromucosa proveniente del ojo izquierdo, por lo cual se le adicionó al tratamiento clotrimazol tópico en el ojo afectado. Debido a la evolución negativa del paciente, se planteó la aplicación tópica de clotrimazol por instilación nasal durante una hora bajo anestesia general, y se suspendió el tratamiento con Itraconazol.
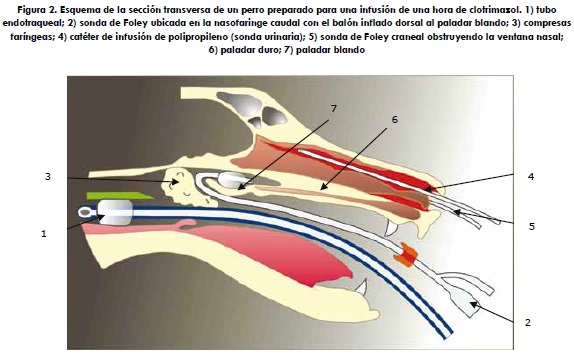
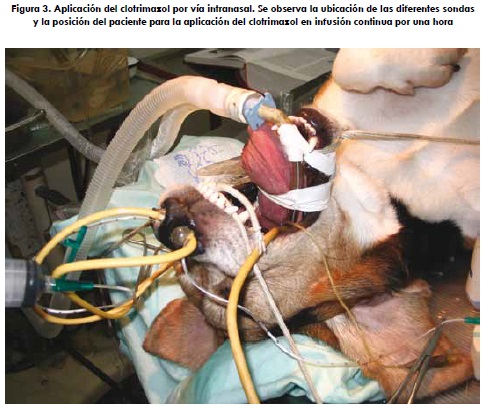
El paciente se sometió a anestesia general con el siguiente protocolo: premedicación, xilacina 0,25 mg/kg, más morfina 0,5 mg/kg, más atropina 0,022 mg/kg por vía subcutánea; inducción, tiopental sódico 5 mg/kg por vía intravenosa; mantenimiento, enfluorano 2%; y oxigenación mediante un tubo endotraqueal con neumotapón. El canino se ubicó en decúbito dorsal con la nariz en paralelo a la mesa. Se introdujo a través de la cavidad oral una sonda Foley 24 Fr (french), la cual se posicionó dentro de la nasofaringe caudal de manera que el balón quedara en la unión de los paladares blando y duro. El balón se infló con cerca de 10 mL de aire para asegurar una fijación hermética. Se insertó una compresa quirúrgica por encima del paladar blando para ayudar a mantener la sonda en posición y obstruir mejor la nasofaringe. Se ubicaron compresas adicionales en la parte posterior de la boca alrededor del tubo traqueal para evitar que el medicamento que se filtrara de la obturación nasofaríngea pueda alcanzar el esófago, la laringe o la tráquea. Una sonda urinaria de polipropileno 8 Fr se introdujo dentro del meato dorsal de cada cavidad nasal hasta una distancia aproximada a la mitad de camino entre la ventana externa y el canto media del ojo. Una sonda Foley 12 Fr se pasó en adyacencia de la sonda urinaria dentro de cada fosa nasal. El balón se infló y traccionó contra el lado interno de la nariz (figuras 2 y 3).
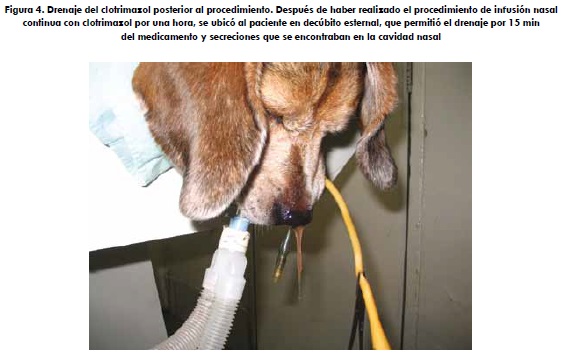
Por cada sonda urinaria se aplicaron 20 mL de una solución de clotrimazol al 1%. Cada sonda se obturó utilizando pinzas hemostáticas cuando el medicamente comenzó a gotear por rebosamiento. Después de los 30 min iniciales, la cabeza del paciente se inclinó ligeramente hacia un lado y luego hacia el otro permaneciendo en cada lado durante 15 min. Luego de la hora de contacto, el perro se giró sobre el decúbito esternal con la cabeza colgando sobre el extremo de la mesa y la nariz dirigida hacia el suelo. Las sondas se extrajeron desde las ventanas externas y se dejó drenar el clotrimazol y el moco resultante (figura 4). Las compresas se retiraron desde la nasofaringe y la cavidad bucal. Se extrajo la sonda de la nasofaringe (8).
Un mes después se realizó una nueva aplicación de clotrimazol intranasal, ya que había reincidido el sangrado después de un periodo de mejoría de aproximadamente 20 días. Posterior a un mes, los propietarios reportaron normalidad en cuanto a la condición del paciente sin recidiva de los signos respiratorios y no permitieron el desarrollo de pruebas adicionales.
DISCUSIÓN
La aspergilosis nasal afecta a caninos de cualquier edad, pero aproximadamente el 40% de los pacientes afectados tienen menos de tres años y el 80% menos de siete años. Los machos parecen tener un mayor riesgo de presentación que las hembras. La enfermedad suele observarse en perros dolicocéfalos y es muy poco frecuente en braquicéfalos (3,5).
Los primeros síntomas que sugieren micosis nasal son dolor a la palpación nasal, presencia de estornudos con descarga muco-sanguino o purulenta uni- o bilateral, y dependiendo de la severidad del problema, mal olor, epistaxis y erosión con despigmentación de la narina (5,6,9,10). El paciente presentado aquí llevaba por lo menos una semana con secreción nasal mucosanguinolenta unilateral y estornudo episódico, no complicados con otros síntomas, posiblemente por ser una enfermedad de curso temprano.
El seno frontal es el sitio predilecto para el establecimiento del microorganismo antes de que sus metabolitos comiencen la rápida destrucción de las turbinas y tejido óseo aledaño (4). La enfermedad canina suele permanecer limitada a la cavidad nasal o los senos paranasales, pero casi siempre se observa una notable destrucción de la mucosa y del hueso de los cornetes, tal vez como resultado de vasculitis de los vasos submucosos (5). Estas alteraciones generan cambios radiográficos semanas después del comienzo del desarrollo de la patología.
No se conoce a ciencia cierta la patogénesis de la aspergilosis nasal en el canino. Sin embargo, es posible que se encuentre asociada con una alteración en la inmunidad de mucosas (susceptibilidad propia o individual de ciertos animales) que podría predisponer al paciente a desarrollar la infección (1). Se ha reportado una alteración en la proliferación de linfocitos en estos perros, pero no está claro si esto es la causa primaria o una consecuencia de la infección (11). También cabe anotar que en el desarrollo de esta infección nasal es de importancia la preexistencia de otra enfermedad nasal, la terapéutica antimicrobiana prolongada o la presencia de cuerpos extraños (4,5). Los productos de A. fumigatus inhiben la transformación de linfocitos tanto de las células B como T in vitro; A. fumigatus produce una endotoxina hemolítica y dermonecrótica que posiblemente ocasiona la necrosis de los cornetes y la erosión del rinario que ocurre en la aspergilosis nasal canina (5).
El diagnóstico de la aspergilosis nasal en perros se hace teniendo en cuenta la historia, los signos clínicos, el examen clínico, la rinoscopia y el cultivo para hongos junto con los resultados de serología, citología, histología y estudios imagenológicos (radiografía, tomografía, resonancia magnética); para considerarse positivo a la patología, el paciente sospechoso debe ser positivo por lo menos a dos pruebas (preferiblemente tres) (3,10).
En este caso, se llegó al diagnóstico con base en la historia, el examen clínico, la rinoscopia y los resultados de la citología y del cultivo para hongos. Los hallazgos citológicos más frecuentes son la inflamación neutrofílica con fagocitosis de bacterias (cocos y bacilos) sin importar la técnica utilizada para la toma de muestra, lo que puede confundir el diagnóstico inicial con la rinitis de tipo bacteriano; sin embargo, el diferencial más importante para la aspergilosis nasal es la neoplasia nasal (6).
La toma de muestras para cultivo y citología con ayuda de endoscopia permite identificar hifas de hongos en el 93% de los casos por cepillado y 100% por toma de biopsia, y los frotis de exudado nasal a ciegas son menos útiles (4,6). También se ha reportado la utilización de pruebas en sangre (inmunodifusión en agar-gel o Elisa para IgG) con buena sensibilidad y excelente especificidad (12). En este caso, la rinoscopia permitió encontrar la zona más afectada de la mucosa nasal de la cual se realizó la toma de muestras para citología y cultivo por uso de hisopado directo.
Los estudios imagenológicos deben desarrollarse antes de la rinoscopia y la biopsia debido a que estos procedimientos generan hemorragia y pueden opacar pequeñas lesiones induciendo la formación de artefactos (3,12). La radiografía convencional permite diferenciar entre neoplasia nasal y aspergilosis nasal en la mayoría de los perros. Las características radiológicas principales de la aspergilosis nasal son pérdida de las turbinas con puntos de radiolucidez de los huesos de soporte, incremento en la radiolucidez rostralmente e incremento en la opacidad caudalmente en la cavidad nasal y un incremento en la opacidad en el seno frontal con engrosamiento del hueso frontal (6,11,13). En el caso presentado aquí no se observaron anormalidades radiográficas en la placa de cráneo, posiblemente por el curso temprano de la enfermedad.
Las imágenes de tomografía son superiores a la radiografía convencional, ya que permiten detallar la extensión de las lesiones y mejora la diferenciación entre la rinitis infecciosa y la neoplasia en perros y gatos (2). Con la resonancia magnética es posible mejorar la evaluación de los tejidos blandos, lo cual ha hecho que se use ampliamente en humanos para el examen de las cavidades nasales, senos paranasales y estructuras asociadas (3,10,13,14).
Es difícil lograr el control efectivo de la enfermedad; por lo tanto, se ha investigado una gran variedad de modalidades terapéuticas, incluyendo la administración tópica y sistémica de agentes antifúngicos o la combinación de dos rutas de administración (10). Varios antimicóticos se utilizan para tratar la aspergilosis nasal; de ellos, los derivados del azol más recientes (fluconazol e itraconazol) evidencian los mejores resultados (5); sin embargo, la administración oral de estos medicamentos se considera poco óptima y se asocia con tratamientos muy prolongados, alto costo de los medicamentos y pobres resultados debido sobre todo a que histopatológicamente se ha determinado que la enfermedad no es invasiva, lo que hace que la penetración del medicamento a la placa fúngica sea limitada (15). Se ha obtenido mejoría clínica en únicamente el 50% de pacientes tratados con tiabendazol y ketoconazol y cerca al 70% en pacientes tratados con itraconazol o fluconazol.
El tratamiento tópico con enilconazol o clotrimazol se asocia con mayores tasas de éxito (7,9,10). La hepatotoxicidad, anorexia y erupciones cutáneas son algunas de las complicaciones observadas con el tratamiento antifúngicos sistémicos (10). En el paciente reportado aquí se utilizó itraconazol a dosis de 5 mg/kg BID por 30 días, con el que no se observó ningún tipo de mejoría, por lo tanto se suspendió. No obstante, cabe anotar que la duración del tratamiento solo con itraconazol debe ser de por lo menos 10 semanas (5).
En cuanto al tratamiento tópico, por muchos años consistió en la implantación quirúrgica de tubos en la cavidad nasal y senos frontales y la irrigación con enilconazol dos veces al día entre siete y catorce días (3,15). También se ha utilizado la combinación de rinotomía con infusión de enilconazol al 2% por una hora y posterior administración de itraconazol con resultados prometedores en casos severos o recurrentes (9). En la actualidad, se utiliza una técnica menos invasiva en la cual se ubican catéteres en el meato nasal dorsal que permite una mejoría en la distribución de medicamentos dentro de los senos, con mejores resultados y menores complicaciones posterapéuticas (8,9). En la literatura también se han descrito técnicas mixtas en la cuales se hace un abordaje no invasivo a la cavidad nasal similar a la realizada en el paciente descrito en este reporte, combinado con un componente invasivo al hacer la trepanación de los senos frontales con el fin de mejorar la penetración de los medicamentos (15).
También se ha propuesto otro protocolo mixto en el que aparte de la instilación de clotrimazol en solución, se aprovecha la trepanación de los senos frontales para por esa vía aplicar clotrimazol en crema. Este protocolo ha demostrado mejores resultados al incrementar la distribución de los medicamentos en este compartimento y su mayor persistencia en contacto con las placas fúngicas (16).
Greci y colaboradores (17) reportaron el desarrollo de tumores sinunasales en tres pacientes que se trataron exitosamente contra aspergilosis nasal por medio de la infiltración local con clotrimazol. No es claro si realmente el tratamiento estuvo asociado con el desarrollo de las neoplasias y se sabe que el clotrimazol carece de efectos carcinogénicos y mutagénicos, y que la inflamación crónica o algunas toxinas fúngicas podrían estar asociadas con el desarrollo potencial de tumores. Por lo tanto, y teniendo en cuenta esta asociación, es importante incrementar la observación y la investigación en la identificación de tumores nasales asociados de alguna manera con la presencia de una infección fúngica en esta zona.
La persistencia de la infección a pesar de la terapia adecuada en algunos pacientes caninos puede ser el resultado de defectos en los mecanismos de defensa local (limpieza mucociliar) o disfunción del sistema inmune local (11).
En conclusión, existen pocos reportes de la presentación de aspergilosis nasal en la literatura nacional indexada. Esto no necesariamente indica que exista una baja presentación de la patología; es más posible que se esté subdiagnosticando, ya que es muy frecuente enfrentarse en la práctica clínica a casos asociados con descarga nasal crónica, que tienden a ser tratados solo sintomáticamente, pero en los que no se ahonda en el diagnóstico final, sin tener en cuenta que esto redundaría en mejores tasas de efectividad terapéutica al orientar específicamente el tratamiento.
Se debe seguir un protocolo ordenado de planes diagnósticos que permitan descartar paulatinamente las enfermedades más comunes causantes de secreción nasal. En la medida que la enfermedad no evoluciona positivamente, es necesario incorporar pruebas diagnosticas más avanzadas (cultivo, rinoscopia o tomografía) con el fin de determinar y aislar el patógeno involucrado. Sin embargo, se debe tener en cuenta que no es posible tener certeza del diagnóstico con los resultados de una sola prueba.
En cuanto al manejo médico, se pudo confirmar con la evolución clínica del paciente que el tratamiento actual más efectivo es la aplicación tópica de un antifúngico como el clotrimazol, bajo anestesia general, siendo superior al uso de antimicóticos sistémicos.
REFERENCIAS
1. Rodrigues R, Ferreiro L, Spanamberg A, Driemeier D, Da Silva ML, Passos S, et al. Canine sino-nasal aspergillosis. Acta Sci Vet. 2011;39(4):1-6. [ Links ]
2. Saunders JH, Zonderland JL, Clercx C, Gielen I, Snaps FR, Sullivan M, et al. Computed tomographic findings in 35 dogs with nasal aspergillosis. Vet Radiol Ultrasound. 2002;43(1):5-9. [ Links ]
3. Saunders JH, Clercx C, Snaps FR, Sullivan M, Duchateau L, van Bree HJ, et al. Radiographic, magnetic resonance imaging, computed tomographic, and rhinoscopic features of nasal aspergillosis in dogs. J Am Vet Med Assoc 2004; 225(11):1703-12. [ Links ]
4. Dick W. Canine nasal mycosis--light at the end of a long diagnostic and therapeutic tunnel. J Small Anim Pract. 2006;47(6):307. [ Links ]
5. Greene CE. Enfermedades infecciosas en perros y gatos. 2a. ed: Mexico: McGraw-Hill Interamericana; 2000. p. 445-451. [ Links ]
6. De Lorenzi D, Bonfanti U, Masserdotti C, Caldin M, Furlanello T. Diagnosis of canine nasas aspergillosis by comparison of four different collection techniques. J Small Anim Pract. 2006;47(6):316-9. [ Links ]
7. Rochette R, Engelen M, Vanden Bossche H. Antigungal agents of use in animal health -practical applications. J Vet Pharmacol Ther. 2003;26(1):31-53. [ Links ]
8. Nelson RW, Couto CG. Medicina interna de animales pequeños. 2a. ed: Buenos Aires: Intermédica; 2000. p. 253-6. [ Links ]
9. Claeys S, Lefebvre JB, Schuller S, Hamaide A, Clercx C. Surgical treatment of canine nasal aspergillosis by rhinotomy combined with enilconazole infusion and oral itraconazole. J Small Anim Pract 2006;47(6):320-4. [ Links ]
10. Sissener TR, Bacon NJ, Friend E, Anderson DM, White RAS. Combined clotrimazole irrigation and depot therapy for canine nasal aspergillosis. J Small Anim Pract. 2006;47(6):312-5. [ Links ]
11. Peeter D, Day MJ, Clerex C. An immunohistochemical study of canine nasal aspergillosis. J Comp Pathol. 2005;132(4):283-8. [ Links ]
12. Cohn L. Canine nasal disease. Vet Clin North Am Small Anim. 2014;44(1):75-89. [ Links ]
13. Saunder JH, Duchateau L, Stork C, VanBree H. Use of computed tomography to predict the outcome of a noninvasive intranasal infusion in dogs with nasal aspergillosis. Can Vet J. 2003;44(4):305-11. [ Links ]
14. Saunders JH, Van Bree H. Comparison of radiography and computed tomography for the diagnosis of canine nasal aspergillosis. Vet Radiol Ultrasound. 2003;44(4):414-19. [ Links ]
15. Sharman M, Lenard Z, Hosgood G, Mansfiled C. Clotrimazole and enilconazole distribution within the frontal sinuses and nasal cavity of nine dogs with sinonasal aspergillosis. J Small Anim Pract. 2012;53(3):161-7. [ Links ]
16. Hayes GM, Demetrium JL. Distribution and persistence of topical clotrimazole after sinus infusión in normal canine cadavers. J Small Anim Pract. 2012;53(2):95-100. [ Links ]
17. Greci V, Stefanello D, Di Giancamillo M, Mortellaro C. Sinonasal tumor in 3 dogs after succesful topical treatment for frontal sinus aspergillosis. Can Vet J. 2009;50(11):1191-95. [ Links ]