Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de Medicina Veterinaria
Print version ISSN 0122-9354
Rev. Med. Vet. no.31 Bogotá Jan./June 2016
Efectos de la inclusión de dietas ricas en flavonoides en la calidad de la leche bovina
Effects of Diets Rich in Flavonoids on the Quality of Bovine Milk
Efeitos da inclusão de dietas ricas em flavonoides sobre a qualidade do leite bovino
Anastasia Cruz Carrillo1 / Carlos Sebastián Lizarazo Cely2
1 Médico veterinario. MSc., Esp. Integrante del grupo GIBNA. Línea Farmacología y Fitofarmacología. Medicina Veterinaria y Zootecnia, Universidad Pedagógica y Tecnológica de Colombia, Tunja, Colombia.
anastasia.cruz@uptc.edu.co.
2 Estudiante de último año de Medicina Veterinaria y Zootecnia, Universidad Pedagógica y Tecnológica de Colombia, Tunja, Colombia. Integrante del grupo GIBNA.
equimvz@gmail.com
Recibido: 2 de abril de 2015 / Aceptado: 30 de abril de 2015
Cómo citar este artículo: Cruz Carrillo A, Lizarazo Cely CS. Efectos de la inclusión de dietas ricas en flavonoides en la calidad de la leche bovina. Rev Med Vet. 2015;(31):137-150.
Resumen
La leche bovina constituye uno de los principales alimentos para los mamíferos y, específicamente, para el ser humano; por ello su calidad debe ser óptima y cumplir con todos los aspectos nutricionales y de inocuidad. El objetivo de esta revisión fue recopilar información científica actualizada sobre la importancia de la presencia de flavonoides en la leche bovina, respecto a su valor nutricional y los beneficios que estos metabolitos traen para la leche y el consumidor. La descomposición de la leche está dada por el efecto de la luz, la temperatura y el tiempo sobre la grasa y las proteínas presentes en esta, así como por la fermentación láctica realizada por las bacterias. De esa manera, el control de los tres factores o de uno de ellos contribuye a prolongar la vida útil de la leche y demás productos lácteos. Así, se pudo determinar que buscando retardar el enranciamiento de la leche y de sus subproductos, se ha propuesto incluir forrajes que contengan sustancias antioxidantes como los flavonoides en la ración de las hembras bovinas en producción, que siendo biodisponibles en la especie, también salen en la leche en forma activa y en concentraciones equivalentes a las plasmáticas. Adicionalmente, la presencia de flavonoides en la leche bovina puede aportar una fuente de antioxidantes naturales para el consumidor, lo cual constituye un efecto benéfico para la prevención de algunos procesos patológicos mediados por radicales libres.
Palabras clave: enranciamiento, flavonoides, grasa, metabolitos secundarios, oxidación.
Abstract
Bovine milk is one of the main foods for mammals and, specifically, for humans; therefore, its quality should be optimal and should comply with all safety and nutritional aspects. The objective of this review was to collect updated scientific information on the importance of the presence of flavonoids in bovine milk, regarding their nutritional value and the benefits of these metabolites for the milk and its consumers. Milk decomposition is due to the effect of light, temperature and time on the fat and protein present in it, as well as to lactic fermentation by bacteria. Thus, the control of these three factors or one of them contributes to extend the useful life of milk and other dairy products. Thus, by seeking to delay the rancidification of milk and its by-products, it has been proposed that forage containing antioxidants such as flavonoids should be included in the diet of female cattle, as these, being bioavailable in cattle, also actively appear in the milk in concentrations equivalent to plasma. Additionally, the presence of flavonoids in bovine milk can provide a source of natural antioxidants for the consumer, which is beneficial for the prevention of some pathological processes mediated by free radicals.
Keywords: rancidification, flavonoids, fat, secondary metabolites, oxidation.
Resumo
O leite bovino constitui um dos principais alimentos para os mamíferos e, especificamente, para o ser humano; por isso sua qualidade deve ser ótima e também cumprir com todos os aspectos nutricionais e de inocuidade. O objetivo desta revisão foi recopilar informação científica atualizada sobre a importância da presença de flavonoides no leite bovino, com respeito ao seu valor nutricional e os benefícios que estes metabolitos trazem para o leite e para o consumidor. A decomposição do leite é causada pelo efeito da luz, a temperatura e o tempo sobre a gordura e as proteínas presentes nesta, assim\ como pela fermentação láctica realizada pelas bactérias. Dessa maneira, o controle dos três fatores ou de um deles contribui a prolongar a vida útil do leite e dos outros produtos lácteos. Assim, foi possível determinar que buscando retardar a rançagem do leite e de seus subprodutos, propuseram incluir forragens que contenham substâncias antioxidantes como os flavonoides na ração das fêmeas bovinas em produção, que sendo bio disponíveis na espécie, também saem no leite em forma ativa e em concentrações equivalentes às plasmáticas. Adicionalmente, a presença de flavonoides no leite bovino pode fornecer uma fonte de antioxidantes naturais para o consumidor, o que constitui um efeito benéfico para a prevenção de alguns processos patológicos mediados por radicais livres.
Palavras chave: rançagem, flavonoides, gordura, metabolitos secundários, oxidação.
INTRODUCCIÓN
En Colombia, por lo general, se reconocen dos sistemas de producción de leche: la producción especializada, que se encuentra en el trópico alto (altiplanos cundiboyacense, nariñense y norte y nordeste antioqueño), y se caracteriza por el uso intensivo de los recursos y la realización de dos ordeños al día o, en algunos casos, tres; y el sistema del doble propósito, que predomina en el trópico bajo (costa atlántica, valle de los ríos, Magdalena, Cauca y el piedemonte llanero), en el cual se manejan sistemas extensivos (1). En uno y otro caso, la calidad de la leche constituye uno de los aspectos más importantes para tener en cuenta por parte del productor, toda vez que las tendencias mundiales de los mercados conducen a exigir productos de alta calidad que además cumplan todos los aspectos de la inocuidad alimentaria (2). En tal sentido, el productor no solo se debe preocupar por obtener volúmenes altos de leche, sino principalmente que esta cumpla con los estándares de calidad composicional, higiénica y sanitaria requeridos.
Uno de los aspectos que influye de manera determinante en la calidad de la leche, sea cruda, pasteurizada o ultrapasteurizada, es la oxidación que sufre la grasa de esta, proceso conocido como "enranciamiento", el cual conduce a un descenso del pH y a alteraciones organolépticas, principalmente del sabor y olor, que son indicativos del proceso de descomposición química. Dicho problema es más importante en la leche cruda y en aquellas zonas del país donde los productores no cuentan con un correcto manejo del producto en cuanto a transporte y de la cadena de frío (figura 1). Tales condiciones aceleran los procesos enzimáticos lipolíticos y proteolíticos que conducen a alteraciones del sabor y del pH, como ya se mencionó, pero también a alteraciones en la composición de la caseína, lo que impacta negativamente en la elaboración de alimentos de origen lácteo (3).
Por lo anterior, se ha buscado la posibilidad de utilizar forrajes que contengan metabolitos con acción antioxidante que se eliminen en la leche en forma activa y puedan retardar el proceso de oxidación de la grasa y con ello se prolongue la vida medía, principalmente en sistemas de pequeños productores. Adicional a esto, la salida de metabolitos en la leche puede constituir una forma de ofrecer un alimento no solo de buena calidad, sino también que contenga sustancias benéficas para la salud humana. Por tal razón, el objetivo de esta revisión fue recopilar información actualizada sobre la presencia de metabolitos con actividad antioxidante en la leche de vacas suplementadas con leguminosas que contienen flavonoides, como propuesta para la producción de leche bovina mejorada con la presencia de metabolitos de acción antioxidante.
CALIDAD DE LA LECHE
La leche es uno de los principales alimentos de la dieta humana y de los mamíferos en general; aporta proteínas, carbohidratos, vitaminas, minerales y grasa, lo cual constituye cerca del 15 al 25 % del total de grasa consumida y cerca del 25 al 35 % de los ácidos grasos de la ración. La leche de vaca contiene del 70 al 75 % de ácidos grasos (AG) saturados, 20 al 25 % de monoinsaturados y 5 % de poliinsaturados del total de los compuestos grasos o li-pídicos. La concentración exacta de dichos AG y la cantidad general de grasa presente en la leche depende del animal, específicamente de la raza (4), y de la dieta que recibe (figura 2) (4-6), esta situación permite incluir suplementos en la ración de los animales para obtener leche mejorada con compuestos benéficos para la salud humana.
Cuando se hace referencia a la calidad de la leche, frecuentemente se abordan tres aspectos: la composición (calidad composicional), la presencia de microorganismos (calidad microbiológica o higiénica) y el recuento de células somáticas (RCS) (calidad sanitaria). En el primer caso, se determina la presencia y cantidad de los principales constituyentes nutricionales de la leche como proteínas, grasa, lactosa, minerales, vitaminas, sólidos no grasos y sólidos totales, así como su pH. El segundo aspecto se relaciona con la presencia de microorganismos patógenos que constituyen un problema para la salud pública y que pueden provenir de la glándula mamaria o de una mala manipulación de la leche, una vez obtenida (1); esta depende del estado sanitario de los animales, de la rutina de ordeño y del manejo de la leche (7). Adicionalmente, la presencia de células somáticas en alta cantidad es indicativo de procesos inflamatorios, que si bien no se manifiestan clínicamente en el animal, alteran la calidad de la leche.
De acuerdo con lo indicado por el Ministerio de Agricultura en 2012, los estándares de calidad higiénica de la leche en Colombia corresponden a un recuento de unidades formadoras de colonia (UFC), entre 175.000 y 200.000 UFC/ml, aunque según la región pueden exigirse desde 100.000 UFC/ml. Por su parte, la Unión Europea considera que una leche con adecuada calidad higiénica puede tener un RCS hasta de 400.000 células/ ml, mientras que en Estados Unidos se considera un RCS máximo de 750.000 células/ml (2). Respecto a la calidad composicional, esta varía con la raza del animal y su alimentación, principalmente; sin embargo, se puede determinar que el porcentaje de proteína puede estar entre 2,6 y 3,2 % en leches entre "regulares" y "excelentes", aunque la concentración puede ser mayor. Así mismo, la grasa puede encontrarse en promedio entre 3 y 3,5 %, aunque dichos valores pueden estar por encima o por debajo de lo indicado. La lactosa en leches excelentes se encuentra sobre 5,3 % y en leches "buenas" y "regulares" entre 4,6 y 5,3 % (1).
OXIDACIÓN DE LA GRASA DE LA LECHE
La oxidación de la grasa de la leche constituye uno de los principales problemas de esta industria. El proceso es un reacción en cadena, que inicia con la producción de radicales libres, producto de la liberación de los ácidos grasos (8) y que se ve favorecido por tres factores principales: temperatura, contacto con el aire y la luz, acompañados del tiempo de permanencia de la leche frente a estos (9).
En muchos países del mundo, la obtención, manipulación, almacenamiento y transporte de la leche se hacen a temperaturas cercanas a 40 oC, lo cual favorece la hidrólisis no enzimática de la grasa. De esta forma, se aumenta la concentración de ácidos grasos libres que conducen al proceso de rancidez de la leche y por ello a cambios en su sabor y olor. Adicionalmente, los ácidos grasos libres son precursores de acetonas y aldehídos, compuestos que dan a la leche sabores metálico, oxidado y a cebo (10). En consecuencia, la variación de los ácidos grasos en la leche líquida o en polvo es indicativo de un proceso de peroxidación, bien sea por tiempo o bien por temperatura. Se ha registrado que los ácidos grasos de cadena corta disminuyen de manera proporcional al proceso de rancidez (11), porque, como ya se dijo, una vez libres, producto de la oxidación de la grasa, se degradan formando nuevas moléculas. Otra de las sustancias que se modifica cuando se pierde la estabilidad oxidativa de la leche es la vitamina B2, la cual sufre fotodegradación y participa en la alteración del sabor de la leche rancia (12).
Se ha propuesto el uso de antioxidantes en la ración de las hembras bovinas en producción, con el fin de que dichas sustancias retarden o interrumpan la oxidación de la grasa de la leche, y de esta forma se puedan proteger los ácidos grasos poliinsaturados que mantienen la integridad del glóbulo graso y con ello evitar las alteraciones del sabor y calidad del producto (8). Dentro de dichos antioxidantes, los carotenoides presentes en vegetales como la zanahoria pueden favorecer la estabilidad oxidativa de la grasa, lo cual prolonga la vida útil de la leche, cuando las vacas en producción reciben este tipo de suplementos (12). De igual forma, los flavonoides presentes en el forraje, como compuestos antioxidantes, ejercen el mismo efecto (13,14), así como lo ejercen otros compuestos que se mencionarán más adelante.
METABOLITOS SECUNDARIOS DE LAS PLANTAS
Dentro del mecanismo de defensa que tienen las plantas contra las agresiones biótica y abiótica, se destaca su capacidad de sintetizar metabolitos secundarios, los cuales son compuestos de bajo peso molecular que participan en procesos de adaptación de la plantas a su ambiente, como el establecimiento de la simbiosis con otros organismos. Se producen en condiciones adversas como ataque por herbívoros, ataque por microorganismos, competencia por espacio, luz o nutrientes y cualquier otro tipo de estrés abiótico (15). Dichos compuestos difieren de los metabolitos primarios en que no participan en procesos fotosintéticos, respiratorios, de asimilación de nutrientes o síntesis de proteínas, carbohidratos y lípidos. Tampoco son producidos por todas las plantas, y son específicos de ciertos géneros y familias (16). Los precursores de la síntesis de metabolitos secundarios se derivan del metabolismo primario como la glicólisis, el ciclo de Kreps o la vía del Shikimato (17). En términos generales, se agrupan en cuatro clases: terpenos, fenólicos, glucósidos y alcaloides (18), pero para los intereses de esta revisión, se hará referencia a solo un tipo de compuestos fenólicos: las flavonas.
CARACTERÍSTICAS GENERALES DE LOS FLAVONOIDES
Los flavonoides son sólidos amorfos que forman parte de los compuestos fenólicos policíclicos, los cuales derivan del fenol, que es un compuesto aromático con un grupo hidroxilo; así mismo, se definen como pigmentos aromáticos heterocíclicos que contienen oxígeno y que dan color amarillo, rojo y azul a las plantas y frutas (16,19,20). Por lo general, los flavonoides se encuentran principalmente en plantas y muy poco en hongos y algas, en sus partes aéreas en diferentes concentraciones, aunque en algunos casos también en la raíz (21).
Químicamente, los flavonoides poseen dos anillos ben-cénicos unidos por una cadena corta de tres carbonos (C6C3C6 o difenilpropano), por lo que contienen 15 carbonos y gran cantidad de grupos hidroxilo. Se clasifican según el grado de oxidación en antocianinas, flavonas, flavonoles e isoflavonas. Adicional a esto, se mencionan otras formas de clasificarlos de acuerdo con las características de la cadena de tres carbonos en chalconas, flavonas, flavonoles, flavononas, flavononoles, antocianidinas, catequinas, epicatequinas, auronas, isoflavonoides, pterocarpanos y rotenoides, entre otros (16,21,22). Dentro de las plantas, los flavonoides se pueden encontrar libres, en cuyo caso se denomina flavonoides aglicona, unidos a carbohidratos conocidos como glicósidos flavonoides y también en forma de sulfatos, como dímeros o polímeros.
Esta composición influye en la solubilidad de los compuestos, de manera que los glicósidos y los sulfatos son solubles en agua y en alcohol, mientras que las agliconas flavonoides muy hidroxiladas son solubles en etanol, metanol y n-butanol, y las poco hidroxiladas, en acetona y en éter y acetato etílicos. Finalmente, las agliconas metoxiladas se disuelven solo en éter de petróleo y cloroformo (21). Otra clasificación basada en el tipo de enlace de la cadena corta con los bencenos, los divide en tres grupos: los 2-fenilbenzopiranos o flavonoides propiamente dichos, los 3-fenilbenzopiranos o isoflavonoides y los 4-fenilbenzopiranos o neoflavonoides (23).
La presencia de los grupos hidroxilo le confieren acción antioxidante, es decir, impiden la oxidación de los lípidos presentes en diferentes partes, lo cual logran neutralizando el oxígeno reactivo de radicales hidroxilo, de los peróxidos lipídicos y de los aniones superóxido (20). El efecto antioxidante se ha explicado por la presencia del grupo O-dihidroxi en el anillo B, el cual le da mayor estabilidad, y de esta forma permite captar el electrón radicalario. Igualmente, el doble enlace en la unión con la función 4-oxo del anillo, es capaz de captar dichos electrones y los grupos 3-OH y 5-OH, con la función 4-0x0 de los anillos A y C que tienen la mayor capacidad antioxidante (20). Sumado a lo anterior, el efecto antioxidante también es debido a su capacidad de quelar el hierro y de inhibir enzimas como lipo-oxigenasa, ciclooxigenasa, mieloperoxidasa, NAPH oxidasa y xantina oxidasa, enzimas relacionadas con procesos oxidativos, y al mismo tiempo por estimular enzimas que participan en eventos antioxidantes como la catalasa y la superóxido dismutasa, las cuales forman parte de los sistemas endógenos, captadores de radicales libres (24).
Las características químicas mencionadas han permitido explicar la acción protectora de los flavonoides en animales y humanos frente a ciertas enfermedades, en las cuales hay una excesiva producción de radicales libres por peroxidación lipídica, dentro de las que se incluyen aterosclerosis, cáncer, trombopatías, procesos inflamatorios diversos, alergias, lipidemias y colesterolemias (22,24,25).
FLAVONOIDES EN LA RACIÓN DE LOS RUMIANTES
Como se ha mencionado, los diferentes tipos de flavonoides se encuentran en gran cantidad de vegetales; sin embargo, en las leguminosas usadas para la alimentación de los bovinos, como soya (Glicine max), alfalfa (Medica-go sativa) y trébol rojo (Trifolium pratense), se destaca la presencia de estos (26), algunos de los cuales también se encuentran en la leche de animales alimentados con leguminosas (18,27,28).
El tipo de flavonoide presente en los vegetales depende del tipo de leguminosa. De esta manera, en la alfalfa se encuentran isoflavonas y cumestanos; en el trébol rojo predomina la presencia de formononetina, daid-zeína, buicanina A y genisteína, y también se encuentra el cumestrol cumetano, que se considera propio de este género de leguminosa; en el trébol blanco, aunque se encuentran flavonoides, estos están en menor concentración que en el rojo (29,30,31); en la soya se hay mayor concentración de daidzeína, también genisteína, genistina y otro flavonoide exclusivo de esta que es la prunetina (30,32,33).
Los flavonoides presentes en los alimentos son hidrolizados en el rumen e intestino por las glucosidasas bacterianas, lo cual hace que se separen la forma glicolisada y la aglicona (efecto de primer paso), de manera que esta última y los metabolitos producidos se absorben en el íleon e intestino grueso, en rumiantes y monogástricos (18,30,34). Las isoflavonas como la biocanina A y la genisteína son parcialmente metabolizadas por la microflora a p-etilfenol, metabolito inactivo. Por su parte, la formononetina se convierte en daidzeína y esta en equol. Los ligananos son metabolizados a secoisolaricirestinol y a matairestinol, que son convertidos a lignano esterodiol y enterolactona (14,27,29,35,36).
A pesar de que algunos autores indican que la absorción de flavonoides provenientes de la dieta, en el tracto gastrointestinal de los bovinos, es limitada y por ello cuestionan su eficacia como suplemento nutricional en estos animales, actualmente se sabe que existe absorción intestinal, aunque la biodisponibilidad es menor que en monogástricos; por ello se propone el uso de isoflavonas protegidas o sobrepasantes que no sufren metabolismo ruminal (34). Una vez absorbidos, pasan por el hígado donde son metabolizados por glucuronidación y sulfatia-ción. Aunque una fracción de los metabolitos hace ciclo enterohepático, la mayoría pasan a circulación general (37,38).
Posteriormente, se distribuyen en los tejidos incluyendo sistema nervioso central por pasar la barrera hematoen-cefálica y también en el líquido amniótico y tejidos fetales porque pasan placenta; se eliminan por la orina, la materia fecal, a través de la bilis y por la leche (18,36,39,40). La concentración de flavonoides presentes en la leche de bovinos suplementados con fuentes de flavonoides varía de un individuo a otro constituyendo así una fuente de estos metabolitos (28,35,40).
Se considera que el paso de los metabolitos de flavonoi-des de la ración a la leche es fácil, porque las concentraciones de isoflavonas en la leche bovina son similares a las concentraciones plasmáticas (41) y directamente proporcionales a la cantidad ingerida en la dieta. Adicional a esto, hay coincidencia en afirmar que la formononeti-na es la que se encuentra en mayor concentración en la leche, seguida por la daidzeína (29), aunque también se registra la presencia de cumestanos cuando las hembras son suplementadas con trébol rojo (30).
Las concentraciones de los metabolitos derivados de las isoflavonas en la leche de bovinos alimentados con leguminosas varían de un caso a otro. Así es como los resultados obtenidos en un estudio indican que en vacas suplementadas con trébol blanco se logra una mayor concentración de enterodiol que de equol, enterolactona y formononetina en la leche (29). Sin embargo, en otro estudio encontraron mayores concentraciones en leche de equol, enterolactona y formononetina bajo las mismas condiciones (42). A pesar de que la soya contiene altas cantidades de isoflavonas (0,2-6,5 mg/ml), las concentraciones de sus metabolitos alcanzadas en la leche son bajas (56-91 ng/ml) (29). No obstante, también se registran altos niveles de equol en la leche producida por vacas alimentadas con soya (1128-1557 ng/ml) (41).
EFECTOS Y UTILIDAD DE LOS FLAVONOIDES EN LA LECHE BOVINA
A las isoflavonas se les atribuye efectos medicinales dentro de los que se destacan la prevención del cáncer de la glándula mamaria y próstata, así como de algunas enfermedades cardiovasculares, de osteoporosis y de los síntomas de la menopausia. Dichos efectos se explican por la estructura química de las isoflavonas, que es similar al 17 (β-estradiol, lo cual permite que se unan a sus receptores, y genera un efecto estrogénico moderado del tipo concentración dependiente (41). Así mismo, poseen efectos antiinfamatorios, antimicrobianos, antitrombóticos, antialérgicos, antitumorales y antioxidantes (14,18,34,26,43).
Los fitoestrogenos (cumarinas e isoflavonas) presentes en las leguminosas usadas para suplementar a los bovinos tienen la capacidad de unirse a los receptores estrogénicos, lo que produce efectos agonistas o antagonistas (36). Es de notar que existen dos tipos de receptores es-trogénicos, los alfa (ER-α) y los beta (ER-β), que se encuentran, respectivamente, en útero, glándula mamaria, placenta, hígado, sistema nerioso central, sistema cardiovascular, huesos, próstata, ovarios, testículos, glándula pineal, tiroides, paratiroides, adrenal, páncreas, hipotálamo y cerebelo.
Considerando que los estrógenos endógenos poseen acción agonista sobre los receptores alfa y antagonista sobre los receptores beta, generan efectos opuestos según el receptor al cual se unan. Se sabe que el cumestrol se une al receptor ER-β con mayor afinidad y menos al ER-α; en consecuencia, puede actuar en las células secretoras de gonadotropinas inhibiendo los picos de LH como se demuestra en ratones y ovejas (44), y en altas concentraciones produce un cuadro pseudoestrogénico caracterizado por irregularidades de ciclo estral, disminución de la tasa de concepción, ninfomanía, hiperemia vulvar, quistes ováricos, hiperplasia de glándula mamaria y útero, prolapso vaginal, aumento de moco cervical, aborto en el primer tercio de la gestación y metritis.
Algunos autores registran que a partir de 33 mg de cumestrol/kg de materia seca se pueden presentar las alteraciones reproductivas anteriormente mencionadas (45). Otros describen dichos efectos pero con dosis de 22-33 mg de cumestro/kg de materia seca, y también se indican dosis entre 20-50 mg de cumestrol/kg de materia seca (46). Se reitera que el tipo de efecto producido por los flavonoides es concentración dependiente y varía de acuerdo con el receptor sobre el que actúe, de manera que dicho efecto no se puede considerar completamente adverso o benéfico. Entonces, el efecto puede ser estrogénico, y por ello la presencia de flavonoides en los alimentos ayuda a disminuir las alteraciones propias de la menopausia y aquellas relacionadas con la falta de estrógenos (acción estrogénica moderada), o bien disminuir los tumores mediados por estrógenos (acción antiestrogénica) y solo en casos de sobredosis produce alteraciones reproductivas consideradas como indeseables (47,48).
El otro efecto destacable de los flavonoides es el antioxidante debido a su capacidad de neutralizar los radicales libres (47,49). Los sistemas o sustancias capaces de neutralizar las especies reactivas de oxígeno se dividen en dos: los endógenos o enzimáticos y los no enzimáticos. Los primeros corresponden a enzimas producidas por el organismo, dentro de las que se incluye: superóxido dismutasa, glutatión peroxidasa, catalasa, tiorredoxina reductasa y glutatión reductasa. Estos sistemas requieren de cofactores como el selenio para el caso de la glutatión peroxidasa y la tiorredoxin; el cobre y el zinc para la superóxido dismutasa y la glutatión reductasa necesitan de la riboflavina. Por su parte, en el sistema no enzimático están el ácido lipoico, la bilirrubina, la ubiquinosa, los bioflavonoides, los carotenoides, las vitaminas E, A y C, el selenio, el cobre, el zinc y el magnesio. De esa manera los antioxidantes exógenos participan como sustancias protectoras de algunas enfermedades como aterosclerosis, enfermedades cardiovasculares, cáncer y enfermedad de Hansen (lepra), entre otras (50).
Respecto a la relación estructura actividad, la acción antioxidante de los flavonoides se debe a la presencia de los grupos OH en los C3 y C4, el doble enlace en los C2 y C3 conjugados con el carbonil C4 y a los grupos OH de los C3 y C5, a través de los grupos OH; reacciona con las SRO (especies reactivas de oxígeno), por lo que con mayor presencia de estos grupos se mejora la acción antioxidante. Adicionalmente, el efecto lo ejercen en tres momentos en la iniciación, uniéndose al O2, en la peroxidación de los lípidos y durante la formación de la especie radicalaria, al unirse al hierro (51-53).
Es sabido que las especies reactivas de oxígeno como anión superóxido (O2'), radical hidroxilo, óxido nítrico y peróxido de hidrógeno están relacionadas con procesos del estrés oxidativo, ocurridos en algunas patologías (ateroesclerosis, enfermedad de Alzheimer y cáncer). Por tal razón, las sustancias antioxidantes protegen al organismo del daño producido por los radicales libres y esto ha llevado a proponer la suplementación con alimentos que contienen sustancias captadoras de radicales libres. Los flavonoides presentes en la alfalfa neutralizan el H2O2, lo cual impide que este se haga radicalario. Igualmente, captan el anión superóxido y quelan el ion ferroso. Se afirma que esta es una planta con acción antioxidante debido a su habilidad para donar hidrogeniones, lo cual también le permite quelar metales como el hierro (54).
Si bien el efecto antioxidante de los flavonoides se ha destacado con fines medicinales para controlar o evitar enfermedades mediadas por estos, es de anotar que en la industria láctea la acción antioxidante sobre la grasa de la leche constituye un factor importante para prolongar el tiempo de vida útil de estos alimentos. Por ello la presencia de flavonoides en la leche o en cualquier alimento que contenga grasa favorece la estabilidad lipídica y protege del efecto oxidativo. Esta premisa ha permitido proponer que el uso de antioxidantes de síntesis como aditivos en los alimentos sea remplazado por antioxidantes de origen natural como las vitaminas o los flavonoides (55), o bien que los bovinos sean suplementados con raciones ricas en antioxidantes como los flavonoides, para lograr la estabilidad de la grasa de la leche y protegerla del estrés oxidativo, aprovechando que los metabolitos se eliminan por esta, en cantidades suficientes como para lograr acciones benéficas (13,56). Iguales resultados se han logrado suplementando vacas en producción con carotenoides, tocoferoles o con algas marinas sobrepasantes, ricas en docosahexaenoico, el cual sale en la leche y logra un efecto antioxidante de la grasa de la mantequilla preparada con esa leche, lo que alarga su vida útil (57). La adición de tetrahalosa (disacárido natural con acción antioxidante) en la ración de vacas en producción disminuye la oxidación de los ácidos grasos insaturados, lo cual aumenta la presencia del antioxidante en la leche y disminuye la peroxidación lipídica de esta (58).
Complementando el efecto captador de radicales libres, los flavonoides también poseen acción antiinflamatoria, como lo demuestra un estudio en el que la apigenina, flavonoide presente en frutas cítricas, cebolla, manzanilla, perejil y trigo, inhibe la expresión de los genes que codifican la síntesis de citocinas proinflamatorias producidas por los macrófagos frente a la activación inducida por lipopolisacáridos (59). En los cítricos, además de las vitaminas, también se encuentran flavonoides, y por ello se reconocen como alimentos altamente antioxidantes (55).
Finalmente, se describe el efecto antineoplásico de la genisteína, la cual inhibe la tirosina-proteína-cinasa y la ADN topoisomerasa en células cancerosas, al inducir apoptosis e interrumpir el ciclo mitótico (26,43). Utilizando un biomodelo de lechones, se pudo determinar que la genisteína presente en la leche de soya administrada a los lechones disminuye la proliferación y migración de los enterocitos sin afectar el tamaño ni la superficie de la vellosidad (60,61).
Con base en lo anterior, a las plantas que contienen altos niveles de flavonoides se les describen varios efectos medicinales, muchos de ellos explicados por la presencia de dichos metabolitos. Es así como Medicago sativa se ha utilizado para tratamientos de diátesis reumática, diabetes, hipercolesterolemia y ateroesclerosis, así como ansiedad y algunas alteraciones hepáticas (54). También se le describe el efecto antihemorrágico, antianémico, estrogénico, remineralizante, proteinizante, antiartrítico, estimulante del apetito y antiulceroso. Experimentalmente, se ha demostrado que los extractos de alfalfa evitan el aumento de las transaminasas hepáticas, el glutamato oxalacetato transaminasa (SGOT), el glutamato piruvato transaminasa (SGPT), la gama glutamil transferasa (GGT) y la fosfatasa alcalina (ALP), enzimas que aumentan cuando hay daño hepatocelular causado por sustancias hepatotóxicas. Además de lo anterior, disminuye el colesterol (efecto hipolipemiante), los triglicéridos séricos y las concentraciones de lipoproteínas de baja densidad (LDL) y de lipoproteínas de muy baja densidad (VLDL), con aumento de las lipoproteínas de alta densidad (HDL) (62).
Estudios epidemiológicos indican que en personas originarias de Occidente, el consumo de alimentos ricos en flavonoides disminuye el riesgo de presentación de algunas enfermedades, como cáncer de próstata y mamas, osteoporosis y enfermedades cardiovasculares. En el continente asiático, por el tipo de dieta, se estima que se consume entre 25-100 mg al día, mientras que en Occidente el consumo aproximado es 3 mg al día, aunque en varios países el consumo es inferior, puesto que llega a 1 mg al día. Igualmente, la población de origen oriental que vive en Occidente también muestra un consumo más alto de isoflavonas, así como las personas de hábitos vegetarianos (30).
Si se parte del hecho de que estos hallazgos no se deben a razones genéticas o raciales sino a los hábitos alimenticios, la ingestión de alimentos con flavonoides puede propiciar sus efectos benéficos, lo cual se considera necesario en la población, ya que muchas de las enfermedades que afectan a los humanos pueden tener su origen en una mala alimentación y muchas de las enfermedades crónicas se deben a deficiencias nutricionales o se ha determinado que estas son factores de riesgo para su presentación. Por lo anterior, una buena dieta y la presencia de compuestos antioxidantes en esta pueden constituir un mecanismo preventivo para la presencia de las enfermedades relacionadas con la peroxidación lipídica (50,63,64). El aporte de isoflavonas en la dieta de los humanos está representado en vegetales, pescado y leche.
De acuerdo con lo anterior, los flavonoides presentes en la dieta de los rumiantes, que son biodisponibles, finalmente pasan a la leche de los bovinos, y se encuentran, en términos generales, en rangos entre 0,1 a 7,7 µg/L, en los que el equol se encuentra en mayores concentraciones, entre 45 a 164 µg/L (29,65). En tal sentido, con la presencia de isoflavonas en la leche de vacas suplementadas con alfalfa fresca se logra aumentar la proporción de ácidos grasos insaturados y disminuir los saturados (42,66). Se registra aumento de ácido linoléico y a-linoléico y en general de los poliinsatuados n-3 y n-6 (57), lo que le da un valor agregado al aporte nutricional de la leche, ya que a través de ella se podría aportar este tipo de ácidos grasos benéficos para la salud con la sola suplementación de los bovinos con raciones ricas en isoflavonas. Es de anotar, según se afirma en los estudios, que la administración de alfalfa en bovinos puede producir acidosis ruminal leve, porque al tener baja fibra y alta digestibilidad disminuye la salivación, la masticación y la rumia; sin embargo, tal situación no disminuye la producción de leche y en cambio aumenta la proteína de esta (67).
De la misma manera, en vacas en producción suplementadas con trébol rojo rico en flavonoides, se encuentra un aumento en la concentración de equol, formononetina y daidzeína en la leche, que supera diez, dos y tres veces, respectivamente, la de hembras no suplementadas. Igualmente, se encuentra biocanina A y genisteína en los animales suplementados con trébol y mayor concentración de prunetina en hembras suplementadas con soya (36). La concentración de equol en la leche de vacas alimentadas con trébol rojo varía ampliamente de una animal a otro. Estas variaciones dependen de la concentración de flavonoides en el trébol, de la cantidad de trébol consumido por el animal, pero principalmente de la flora ruminal (31,36); aunque también se considera que otros componentes del forraje como los taninos pueden afectar el paso de las isoflavonas por el rumen, y por ello ocurre su bio-disponibilidad y posterior eliminación por la leche (68).
Así mismo, la inclusión de soya en la ración de los rumiantes aumenta la concentración de flavonoides en la leche, principalmente genisteína, daidzeína y equol; este último es el de mayor concentración (69). Si bien la soya es uno de los alimentos con mayores cantidades de flavonoides, así como el trébol y la alfalfa, los bovinos que no son suplementados con estos poseen metabolitos de isoflavonas en la leche, solo que en menor cantidad, a excepción de la genisteína, la cual se encuentra únicamente cuando hay suplementación (70,71).
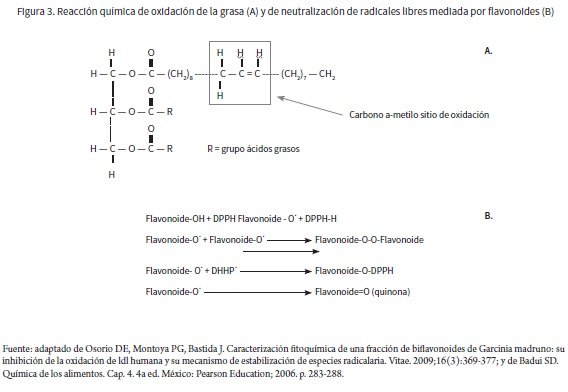
Con lo anterior, y partiendo de los estudios de cinética que se han desarrollado con estos flavonoides (41,66,69), se demuestra que la administración de forrajes o suplementos nutricionales ricos en flavonoides en vacas, cabras y ovejas en producción, aparte de hacer su aporte nutricional, también propicia la presencia de dichos metabolitos en la leche (37,69), lo que permite que estos ejerzan sus efectos antioxidantes en la leche y en el humano que la consume. Los radicales libres producidos en el proceso de oxidación de la leche pueden ser neutralizados por los flavonoides, mediante reacciones de intercambio de electrones, tal como lo demuestran los estudios realizados con el compuesto 2,2 difenil-1-picrilhidrazil (DHHP), el cual es un reconocido radical libre que es neutralizado a un compuesto quinona no radicalario, cuando se pone en contacto con los flavonoides (72,73) (figura 3).
CONCLUSIONES
La utilización de suplementos alimenticios en las vacas en lactancia que contengan metabolitos antioxidantes como los flavonoides, los cuales, se sabe, salen en la leche en forma activa, podría significar dos ventajas simultáneas. La primera se refleja en la hembra suplementada, ya que dichos metabolitos podrían actuar benéficamente en algunos procesos de enfermedad sufridos por esta, como aquellos de tipo inflamatorio. El segundo beneficio se relaciona con lograr producir leche para consumo humano con la presencia de estos metabolitos como un valor agregado al aporte nutricional, lo que ofrece al consumidor un alimento mejorado que mantiene su calidad composicional. De manera complementaria, la acción antioxidante sobre la grasa de la leche puede contribuir a mejorar el tiempo de vida media de esta, lo cual beneficia directamente a los pequeños y medianos productores, quienes por razones de ubicación y tecnología tienen dificultades en la entrega de la leche a las pasteurizadoras.
No obstante, es de anotar que la durabilidad de la leche depende de varios factores, aparte del ya mencionado, como son la calidad higiénica y la estabilidad proteica; por eso el descenso del pH causante del cambio del sabor y olor de la leche está dado por su fermentación causada por bacterias y por la descomposición de grasas y proteínas propias del producto. En consecuencia, el mantenimiento de la calidad de la leche y la prolongación de su durabilidad deberían ser considerados desde estos tres factores de forma simultánea.
REFERENCIAS
1. Calderón A, García F, Martínez G. Indicadores de calidad de leches crudas en diferentes regiones de Colombia. Rev MVZ Córdoba. 2006;11(1):725-37. [ Links ]
2. Vásquez JF, Loaiza ET, Olivera M. Calidad higiénica y sanitaria de leche cruda acopiada en diferentes regiones colombianas. Orinoquía. 2012;16(2):13-23. [ Links ]
3. Ma Y, Ryan C, Barbano DM, Galton DM, Rudan MA, Boor KJ. Effects of somatic cell count on quality and shelflife of pasteurized fluid milk. J Dairy Scie. 2000;83(2):264-74. [ Links ]
4. Samkova E, Pesek M, Spicka J, Pelikanova T, Hanus O. The effect of feeding diets markedly differing in the proportion of grass and maize silages on bovine milk fat composition. Czech J Anim Sci. 2009;54(3):93-100. [ Links ]
5. Kalac P, Samkova E. The effects of feeding various forages on fatty acid composition of bovine milk fat: A review. Czech J Anim Sci. 2010;55(12):521-37. [ Links ]
6. Sterk A, Johansson BEO, Taweel HZH, Murphy M, Van Vuuren AM, Hendriks WH, Dijkstra J. Effects of forage type, forage to concentrate ratio, and crushed linseed supplementation on milk fatty acid profile in lactating dairy cows. J Dairy Sci. 2011;94(12):6078-91. [ Links ]
7. Méndez M, Osuna A. Caracterización de la calidad higiénica y sanitaria de la leche cruda en algunos sistemas productivos de la región del Alto del Chicamocha (Departamento de Boyacá) [tesis de pregrado]. Bogotá: Universidad de La Salle. Bogotá; 2007. [ Links ]
8. Panda N, Kaur H. Influence of vitamin E supplementation on spontaneous oxidized flavour of milk in dairy buffaloes. Int J Dairy Technol. 2007;60(3):198-204. [ Links ]
9. Van Aardt M, Duncan SE, Marcy JE, Long TE, O'Keefe SF, Nielsen-Sims SR. Effect of antioxidant (a-tocopherol and ascorbic acid) fortification on light-induced flavor of milk. J Dairy Sci. 2005;(88):872-80. [ Links ]
10. Chen L, Daniel RM, Coolbear T. Detection and impact of protease and lipase activities in milk and milk powders. Int Dairy J. 2013;13(4):255-75. [ Links ]
11. Páez R, Pensel N, Sabbag N, Taverna M, Cuatrin A, Zalaza C. Changes in free fatty acid composition during storage of whole milk powder. Int J Dairy Technol. 2006;59(4):236-42. [ Links ]
12. Unigunde A, Vita S, Jelena Z. Investigations into the enhancemen of cow's milk oxidative stability. Documento procedente del Annual 18th International Scientific Conference "Research for Rural Development", 2012 may 16-18; Jelgava, Latvia. p. 164-70. [ Links ]
13. De Feo V, Quaranta V, Fedele S, Claps R, Rubino C. Flavonoids and terpenoids in goat milk in relation to forage intake. Ital J Food Sci. 2006;18(1):85-92. [ Links ]
14. Sakakibara H, Viala D, Ollier A, Combeau A, Besle JM. Isoflavones in several clover species and in milk from goats fed clovers. BioFactors. 2004;22(1-4):237-9. [ Links ]
15. Sepúlveda FG, Porta DH, Rocha SM. La participación de los metabolitos secundarios en la defensa de las plantas. Rev Mex Fitopatol. 2003;21(3):355-63. [ Links ]
16. Ávalos GA, Pérez UCE. Metabolismo secundario de las plantas. Reduca (Biología). Serie Fisiología Vegetal. 2009;2(3):119-4. [ Links ]
17. Samková E, Certiková J, Spicka J, Hanus O, Pelikánová, Kvác M. Eighteen-carbon fatty acids in milk fat of Czech Fleckvieh and Holstein cows following feeding with fresh lucerne (Medicago sativa L.). Anim Sci Pap Rep. 2014;32(3):209-18. [ Links ]
18. Escamilla JCI, Cuevas MEY, Guevara FG. Flavonoides y sus acciones antioxidantes. Rev Fac Med UNAM. 2009;52(2):73-5. [ Links ]
19. Piskula MK. Factors affecting flavonoids absorption. BioFactors. 2000;12(1-4):175-80. [ Links ]
20. Russo RO, Speranza SM. Los flavonoides en la terapia cardiovascular. Rev Costarric Cardiol. 2006;8(1):13-8. [ Links ]
21. Martínez MA. Flavonoides. Medellín: Universidad de Antioquia; 2005. [ Links ]
22. Luis DA, Aller R. Papel de los flavonoides del té en la protección cardiovascular. An Med Interna. 2008;25(3):105-7. [ Links ]
23. Osorio DEJ. Búsquedas de sustancias bioactivas a partir de dos especies de la flora colombiana: alcaloides de Phaedranassa dubia (Amarylludaceae) y biflavonoides de Garcinia madruno (Clusiaceae) [tesis doctoral]. Universidad de Barcelona; 2008. [ Links ]
24. Pérez TG. Los flavonoides antioxidantes o prooxidantes. Rev Cubana Invet Biomed. 2003;22(1):48-57. [ Links ]
25. Barros YRM, García MMR, Soto HRM, Colinas LT, Kite G. Flavonoides y actividad antioxidante de Calia secundiflora (Ort.) Yacovlev. Rev Fitotec Mex. 2011:34(3):151-7. [ Links ]
26. Mizunuma H, Kanazawa K, Ogura S, Otsuka S, Nagai H. Anticarcinogenic effects of isoflavones may be mediated by genistein in mouse mammary tumor virus-induced breast cancer. Oncology. 2002;62(1):78-84. [ Links ]
27. Hoikkala A, Mustonen E, Saastamoinen I, Jokela T, Taponen J, Saloniemi H, Wãhãlá K. High levels of equol inorganic skimmed finish cow milk. Mol Nutr Food Res. 2007;51(7):782-6. [ Links ]
28. Nielsen TS, Norgaard JV, Purup S, Frette XC, Bonefeld EC. Estrogenic activity of bovine milk high or low in equol using immature mouse uterotropic responses and an estrogen receptor transactivation assay. Cancer Epidemiol. 2009;33(1):61-8. [ Links ]
29. Andersen C, Nielsen TS, Purup S, Kristensen T, Eriksen J, Soegaard K. et al. Phyto-oestrogens in herbage and milk from cows grazing white clover, red clover, lucerne or chicory-rich pastures. Animal. 2009;3(8):1189-95. [ Links ]
30. Mullingan AA, Welch AA, McTaggart A, Bhaniani A, Bingham SA. Intakes and sources of soya foods and isoflavones in a UK population cohort study (EPIC-Norfolk). Eur J C Nutr. 2007;61(2):248-54. [ Links ]
31. Mustonen EA, Tuori M, Saastamoinen MI, Taponen J, Wähälä K, Saloniemi H, Vanhatalo A. Equol in milk of dairy cows is derived from forage legumes such as red clover. Br J Nutr. 2009;102(11):1552-6. [ Links ]
32. Donovan SM, Andres A, Mathai RA, Kuhlenschmidt TB, Kuhlenschmidt MS. Soy formula and isoflavones and the developing intestine. Nutr Rev. 2009;67(Suppl 2):S192-200. [ Links ]
33. Fujioka M, Uehara M, Wu J, Adlercreutz H, Suzuki K, Kanazawa K, et al. Equol, a metabolite of daidzein, inhibits bone loss in ovariectomized mice. J Nutr. 2004;134(10):2623-7. [ Links ]
34. Gohlke A, Ingelmann CJ, Nümberg G, Starje A, Wolffram S, Metges CC. Bioavailability of quercetin from its aglycone and its glucorhamnoside rutin in lactating dairy cows after intraduodenal administration. J Dairy Sci. 2013;96(4):2303-13. [ Links ]
35. Cederroth CR, Nef S. Soy phytoestrogens and metabolism: review. Mol Cell Endocrinol. 2009;304 (1-2):30-42. [ Links ]
36. Höjer A, Adler S, Purup S, Hansen-Moller J, Martinsson K, Steinshamn H, Gustavsson AM. Effects of feeding dairy cows different legume-grass silages on milk phytoestrogen concentration. J Dairy Sci. 2012;95(8):4526-40. [ Links ]
37. Adlercreutz H, Fotsis T, Bannwart C, Ma' kela' T, Wa" ha' la" K, Brunow G, Hase T. Assay of lignans and pha-toestrogens in urine of women and in cow's milk by GC/ MS (SIM). Todd JFJ, editor. Advances in mass spectrometry. Precedente del 10th International Mass Spectrometry Conference. Chichester (UK): John Wiley; 1985. [ Links ]
38. Setchell KDR, Faughnan MS, Avades T, Zimmer-Nechemias L, Brown NM, Wolfe BE, et al. A comparison of the pharmacokinetics of[13C] labeled daidzein and genistein in premenopausal women. Am J Clin Nutr. 2003;77(2):411-9. [ Links ]
39. Campos RG, Hernández EA. Relación nutrición fertilidad en bovinos. Un enfoque bioquímico y fisiológico. Palmira: Universidad Nacional de Colombia; 2008. [ Links ]
40. Jarrell J, Foster WG, Kinniburgh DW. Phytoestrogens in human pregnancy. Obstet Gynecol Int [internet]. 2012 [citado 2014 dic 20]. Disponible en http://www.hindawi.com/journals/ogi/2012/850313/ [ Links ]
41. Krajcova A, Schulzova, Lojza J, Krizova L, Hajslova J. Phyto-oestrogens in bovine plasma and milk-LC-MS/ MS Analysis. Czech J Food Sci. 2010;28(4):264-74. [ Links ]
42. Steinshamn H. Effect of forage legumes on feed intake, milk production and milk quality - a review. Anim Sci Pap Rep. 2010;28(3):195-206. [ Links ]
43. Matukawa Y, Marui N, Sakai T, Satomi Y, Yoshida M, Matumoto K, et al. Genistein arrests cell cycle progression at G2-M. Cancer Res. 1993;53(6):1328-31. [ Links ]
44. Jacob DA, Temple JL, Patisaul HB, Young LJ, Rissman EF. Coumestrol antagonizes neuroendocrine action of estrogen via the estrogen receptor alfa. Exp Biol Med (Maywood). 2001;22(4):301-6. [ Links ]
45. Le Bars J, LE Bars ET, Brice G. Presence, accumulation et devenir du cumestrol dans laluzerne et ses derivés. Rec Med Vet. 1990;166(5):463-9. [ Links ]
46. Valderrabano J. Alteraciones reproductivas asociadas al consumo de fitoestrógenos. Invest Agric Producc Sanidad Animal. 1992;7(2):120-24. [ Links ]
47. Boots AW, Haenen GR, Bast A. Health effects of quercetin: From antioxidant to nutraceutical. Eur J Pharmacol. 2008;585(2-3):325-37. [ Links ]
48. Haron H, Ismail A, Shahar S, Azlan A, Pen LS. Apparent bioavailability of isoflavones in urinary excretions of postmenopausal Malay women consuming tempeh compared with milk. Int J Food Sci Nutr. 2011;62(6):642-65. [ Links ]
49. Herrera E, Jiménez R, Aruoma OI, Hercberg S, Sánchez-García I, Fraga C. Aspects of antioxidant foods and supplements in health and disease. Nutr Rev. 2009;67:S140-4. [ Links ]
50. Zamora SJD. Antioxidantes: micronutrientes en la lucha por la salud. Rev Chil Nutr. 2007;34(1):17-26. [ Links ]
51. Kurkin VA, Ryzhov VM, Biryukova OV, Mel'nikova NB, Selekho VV. Interaction of milk-thistle-fruit flavanonols with langmuir monolayers of lecithin and bilayers of liposomes. Pharm Chem J. 2009;43(2):33-42. [ Links ]
52. Sakakibara H, Honda Y, Nakagawa S, Ashida H, Kanazawa K. Simultaneous determination of all polyphenols in vegetables, fruits, and teas. J Agric Food Chem. 2003;51(3):571-81. [ Links ]
53. Martínez-Valverde I, Periago MJ, Ros G. Significado nutricional de los compuestos fenólicos de la dieta. Arch Latin Nutric.2000;50(1):5-18. [ Links ]
54. Singh BK, Sharmab A. In vitro antioxidant and free radical scavenging potential of Medicago sativa Linn. J Pharm Res. 2010;3(6):1206-10. [ Links ]
55. Moreno MJ, Guaran CY, Belén DR, García PD, Medina CA. Efecto de los extractos de flavonoides de harinas de cascaras y semillas de pomelos sobre la estabilidad de aceite de soja. Grasas y Aceites. 2007;58(4):351-8. [ Links ]
56. Lindmark-Mânsson H, Akesson B. Antioxidative factors in milk. Br J Nutr. 2000;84(Suppl 1):S103-10. [ Links ]
57. Glover KE, Budge S, Rose M, Rupasinghe HPV MacLaren L, Green-Jhonson J, Fredee AH. Effect of feeding fresh forage and marine algae on the fatty acid composition and oxidation of milk and butter. J Dairy Sci. 2012;95(6):2797-809. [ Links ]
58. Aoki N, Furukawa S, Sato K, Kurokawa Y, Kanda S, Takahashi T, et al. Supplementation of the diet of dairy cows with trehalose results in milk with low lipid peroxide and high antioxidant content. J Dairy Sci. 2010;93(9):4189-95. [ Links ]
59. Xiaoxouan Z, Wang G, Guerley EC, Zhou H. Flavonoid apigenin inhibits lipopolysaccharide-induced inflammatory response through multiple mechanisms in macrophages. PloS One. 2014;9(9):1-18. [ Links ]
60. Chen AC, Berhow MA, Tappenden KA, Donovan SM. Genistein inhibits intestinal cell proliferation in piglets. Pediatr Res. 2005;57(2):192-200. [ Links ]
61. Migliaccio A, Castoria G, Di Domenico M, de Falco A, Bilancio A, Lombardi M, et al. Steroid-induced androgen receptor-oestradiol receptor (3-Src complex triggers prostate cancer cell proliferation. EMBO J. 2000;19(20):5406-17. [ Links ]
62. Al-Dosari MS. In vitro and in vivo antioxidant activity of alfalfa ( Medicago sativa L.) on carbon tetrachloride intoxicated rat. Am J Chin Med. 2012;40(4):779-93. [ Links ]
63. Barnes S. Effect of genistein on in vitro and in vivo models of cancer. J Nutr. 1995;125(3 suppl):777S-783S. [ Links ]
64. Gotoh T, Yamada K, Yin H, Ito A, Kataoka T, Dohi K. Chemoprevention of N-nitroso-Nmethylurea-induced rat mammary carcinogenesis by soy foods or biochanin A. Jpn J Cancer Res. 1998;89(2):137-42. [ Links ]
65. Nielsen TS, Purup S, Warri A, Godschalk RW, Hilakivi-Clarke L. Effects of maternales exposure to cows milk higo or low in isoflavones on carcinogen-induced mammary tumorigenesis among rat offspring. Cancer Prev Res (Phila). 2011;4(5):694-701. [ Links ]
66. Van Dorland HA, Kreuzer M, Leuenberger H, Wettstein HR. Comparative potential of white and red clover to modify the milk fatty acid profile of cows fed ryegrass-based diets from zero-grazing and silage systems. J Sci Food Agric. 2008;88(1):77-85. [ Links ]
67. Van Zyl M, Meeske R, Scholtz GDJ, Einkamere OB. The effect of lucerne (Medicago sativa) hay quality on milk production and composition ofJersey cows. S Afr J Anim Sci. 2014;44(5 suppl 1):25-30. [ Links ]
68. Hedqvist H, Mueller-Harvey I, Reed JD, Krueger CG, Murphy M. Characterisation of tannins and in vitro protein digestibility of several Lotus corniculatus varieties. Anim Feed Sci Technol. 2000;87(1-2):41-56. [ Links ]
69. Trinacty J, Krizova L, Schulzova V, Hajslova J, Hanus O. The effect of feeding soybean-derived phytoestogens on their concentration in plasma and milk of lactating dairy cows. Arch Anim Nutr. 2009;63(3):219-29. [ Links ]
70. Piotrowska KK, Woclawek-Potocka I, Bah MM, Piskula MK, Pilawski W, Bober A, Skarzynski DJ. Phytoestrogens and their metabolites inhibit the sensitivity of the bovine corpus luteum to luteotropic factors. J Reprod Dev. 2006;52(1):33-41. [ Links ]
71. Woclawek-Potocka I, Bah MM, Korzekwa A, Piskula MK, Wiczkowski W, Depta A, Skarzynski DJ. Soybean-derived phytoestrogens regulate prostaglandin secretion in endometrium during cattle estrous cycle and early pregnancy. Exp Biol Med (Maywood). 2005;230(3):189-99. [ Links ]
72. Osorio DE, Montoya PG, Bastida J. Caracterización fitoquímica de una fracción de biflavonoides de Garcinia madruno: su inhibición de la oxidación de ldl humana y su mecanismo de estabilización de especies radicalaria. Vitae. 2009;16(3):369-377 [ Links ]
73. Badui SD. Química de los alimentos. Cap. 4. 4a ed. México: Pearson Education; 2006. p. 283-288. [ Links ]