Introducción
La tripanosomiasis bovina es una enfermedad hemoparasitaria de distribución mundial 1, ocasionada en países de América Latina por protozoos flagelados de las especies Trypanosoma vivax y Trypanosoma evansi, mediante transmisión mecánica por moscas hematófagas de la familia Tabanidae y la mosca Stomoxys calcitrans2. En áreas donde la transmisión es estrictamente mecánica, la tripanosomiasis bovina ocurre en forma de brotes epizoóticos múltiples periódicos, en un contexto enzoótico subclínico 2. Esta condición epidemiológica hace que sea difícil la detección en el torrente sanguíneo, debido a las bajas parasitemias, producto del control inmunitario y los tratamientos suministrados (2. No obstante, en periodos enzoóticos clínicos los bovinos evidencian fiebre y anemia severa con ictericia al momento del examen clínico; las complicaciones que llevan a la muerte de bovinos infectados con Trypanosoma sp. están explicadas por combinaciones de alteraciones microcirculatorias, como la trombocitopenia y la anemia persistente, que lleva a insuficiencia cardiaca congestiva 2 y cuadro nervioso, caracterizado por cojera, tremores, parestesias y convulsiones 3. Estas alteraciones en el estado de salud generan un impacto económico en el sistema productivo, como resultado principalmente de abortos, descenso en la producción láctea, pérdida de peso y mala calidad del semen3,4.
Según la Encuesta Nacional Agropecuaria para 2010, la ganadería bovina en Colombia estaba conformada por 27.753.990 bovinos, de los cuales el 74 % se dedica a la producción de carne; el 21 %, al doble propósito, y el 5 % está constituido por bovinos de sistemas especializados en producción de leche 5. La enfermedad causada por Trypanosoma sp. ha sido registrada en búfalos y bovinos de diferentes zonas del territorio colombiano 6,7, donde regiones tropicales y subtropicales establecen los ecosistemas con las características óptimas para que cohabiten reservorios, el hemoparásito y los vectores 8. T vivax es enzoótico en todo el país en zonas por debajo de los 1000 m s. n. m. 1, con condiciones ecológicas que difieren de las zonas donde se desarrollan los sistemas especializados en producción de leche en el país. En Colombia no se ha realizado ningún estudio sobre la prevalencia o el impacto económico de T. evansi en rumiantes domésticos 1.
En Entrerríos, zona de ganadería especializada en producción de leche y que se encuentra ubicada a 2486 m s. n. m., no se han realizado estudios sobre la epizootiología de la tripanosomiasis bovina. Sin embargo, en agosto de 2010 se evaluó un caso clínico compatible con una hemoparasitosis, confirmado por las técnicas de microscopia: extendido de sangre periférica (ESP) y método Buffy coat como infección por Trypanosoma sp., en una vaca productora de leche nacida en una hacienda de la zona. A partir de este caso se propuso evaluar la infección por Trypanosoma vivax y Trypanosoma evansi en ganadería bovina especializada en producción de leche en una hacienda y sus potenciales vectores.
Materiales y métodos
Zona de estudio
Enterríos es un municipio ubicado en la subregión norte del departamento de Antioquia, Colombia; presenta una extensión de 219 km2, y tiene como principal actividad económica la producción y reproducción de ganado especializado en producción de leche. Se encuentra ubicado en las coordenadas geográficas: 6° 37' 03,67" N 75° 30' 58,12" O a 2486 m s. n. m.; está clasificado como zona de vida bosque muy húmedo montano bajo (bmh-MB), y se caracteriza por su clima frío con una temperatura promedio de 16 °C (mínima: 9 °C; máxima: 24 °C) 9. Estas condiciones no son habituales para la presentación de esta entidad parasitaria.
Diseño del estudio y descripción de la población
Las muestras se tomaron entre noviembre de 2010 y febrero de 2011, en una hacienda ganadera de producción láctea ubicada en Entrerríos, Antioquia. Se diseñó un estudio de tipo descriptivo transversal. El universo muestral fue de 1296 bovinos entre 1 y 169 meses de edad pertenecientes a una hacienda dedicada a la producción láctea, con un promedio en producción de 16.000 l/d. La hacienda está conformada por siete salas de ordeño con 420 potreros en un área de 768 hectáreas -cada sala contiene hembras distribuidas en lotes de alta, media y baja producción, horro y paridero-; lotes de novillas de vientre, novillas de levante, novillas preñadas y balde estaca (cría). Se realizó un muestreo no probabilístico. Se utilizó el programa Epi-info versión 6 para calcular el tamaño muestral; para ello se tomó un nivel de confianza (z = 95 %), un error de muestreo (e = 3 %) y una probabilidad de ocurrencia del fenómeno (p = 0,07), acordes con los resultados de serorreactividad obtenidos en un estudio sobre Trypanosoma vivax en ganado bovino productor de leche en el estado de Minas Gerais, Brasil, que presenta condiciones climáticas similares 9. Se definió un tamaño muestral de 229, y se llevó a 338 bovinos para prever pérdidas en la muestra y para aumentar el poder estadístico.
Se evaluó el 50 % de los caballos de la hacienda (n = 17) y el 10 % de bovinos de producción de carne (n = 11), de una hacienda aledaña (hacienda 2), que tienen como característica ser provenientes de diferentes regiones del país, sin ningún control o evaluación para la infección por Trypanosoma sp. previo a su introducción a la zona lechera del norte de Antioquia. Estos animales se valoraron por las mismas técnicas implementadas para la ganadería de producción lechera.
Colección y conservación de muestras sanguíneas
Se obtuvo una muestra de sangre de cada bovino tomada de vena coccígea o vena yugular, recolectada en tubos Vacutainer(r) con anticoagulante ácido etilendiaminotetraacético (EDTA). Las muestras fueron conservadas en refrigeración a 4 °C. Para la identificación de especie a través de la técnica de reacción en cadena de la polimerasa (PCR) se tomaron 200 de sangre que fueron conservados en alícuotas a -20 °C.
Evaluación parasitológica, entomológica y clínico-epidemiológica
Se realizaron ESP utilizando la coloración Hemacolor (Merck(c)). Como técnica de concentración por microscopia se realizó el método Buffy coat con fijación y coloración en portaobjetos, descrito por Desquesnes 1, posterior a la lectura del hematocrito. Además, se realizó la estimación de la parasitemia con base en la fórmula:
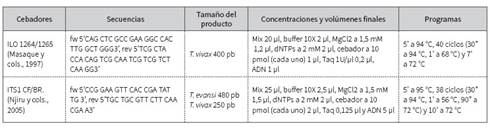
El diagnóstico molecular consistió en realizar pruebas de PCR para la identificación de las especies de Trypanosoma sp. Para obtener el ADN de las muestras de sangre bovina, se utilizó la técnica Salting out10. Para la identificación de T. vivax se empleó la pareja de cebadores ILO 1264/1265 11. Para la caracterización de T. vivax, T. evansi y otras especies patógenas aún no registradas en bovinos en Colombia, como son T. brucei y T. congolense en una sola reacción, se utilizaron cebadores que permiten amplificar una región del espacio interno transcrito (ITS): ITS1 CF/BR 12-14. Los productos de amplificación para ambas PCR fueron analizados por electroforesis en gel de agarosa al 1 % (45 min a 100 V). Para visualizar las bandas se usó bromuro de etidio al 5 % y un transiluminador BIO-RAD, modelo XRS. Los controles positivos de ADN de T. vivax, T. evansi y T. theileri fueron donados por la Corporación Colombiana de Investigación Agropecuaria (Corpoica). El control de T. cruzi fue cedido por el grupo de investigación Biología y Control de Enfermedades Infecciosas de la Universidad de Antioquia. Como control negativo se utilizó la mezcla para la PCR sin ADN (tabla 1).
Se capturaron 4251 moscas distribuidas en 16 lotes de vacas de las diferentes salas de ordeño. Utilizando una jama se capturaron moscas posadas sobre las zonas dorsal, ventral, en las patas de los bovinos y en las salas de ordeño, por un periodo aproximado de una hora en cada lote. Fueron conservadas en alcohol al 70 % para su posterior identificación taxonómica e identificación de especies de parásitos del género Trypanosoma a través de pruebas moleculares. La identificación de las moscas se efectuó con base en las claves taxonómicas descritas por Wall y Shearer 15.
La extracción de ADN se realizó para 56 muestras compuestas, conformadas a partir de los lotes evaluados y separadas según la especie de mosca. Se realizó una disección de la cabeza de las moscas con el fin de obtener el ADN del parásito que se encontrara en la probóscide. Se conformaron muestras compuestas de cabezas de Haematobia irritans (100 unidades por muestra). Las muestras compuestas de cabezas de Stomoxys calcitrans se conformaron con el total de moscas encontradas en cada lote de bovinos donde fueron capturadas (número no mayor a 100 unidades). Con el fin de encontrar el parásito en intestinos de los potenciales vectores, se hicieron muestras compuestas de tórax-abdomen de las moscas evaluadas. La extracción de ADN desde la Musca domestica se realizó con el ejemplar completo. El ADN a partir de moscas se obtuvo con la técnica de extracción de DNA Grind buffer propuesta por Collins y colaboradores 16, adaptada en el presente estudio para la extracción de ADN a partir de moscas.
Se diseñó una encuesta como instrumento para evaluar variables de tipo clínico, fisiológico, de producción y de manejo animal, como la raza, la edad, el sexo, la proveniencia del bovino, la ubicación, el estado fisiológico, la producción de leche, los días de producción de leche y el estado de salud detectado por evaluación médico-veterinaria.
Aspectos éticos
Se obtuvo la aprobación para la ejecución de la investigación a través de un consentimiento informado leído y firmado por los representantes legales de la hacienda. Así mismo, en cumplimiento de las disposiciones expuestas en la Resolución 008430 de 1993, el estudio fue evaluado y aprobado por el comité de ética en investigación animal en el Acta 65 del 29 de septiembre de 2010. También se consideraron las indicaciones expresas en la Ley 84 del 27 de diciembre de 1989, para garantizar las buenas prácticas en los procedimientos que se van a realizar en los bovinos objeto de estudio y para garantizar su bienestar en todo el proceso.
Análisis estadístico
Se realizó el análisis univariado de cada una de las variables cuantitativas y cualitativas, en las que se calculó la frecuencia absoluta y relativa para las variables cualitativas y los estadísticos descriptivos por cada variable cuantitativa. Se exploró la asociación entre las variables clínicas y de producción con la positividad, y se ajustó la positividad según la ubicación en los compartimentos de la hacienda, usando el x2 de independencia y el cálculo del odds ratio (OR) con su respectivo intervalo de confianza. Por otro lado, se recodificaron las variables susceptibles para ser analizadas en dos estratos y se usaron en tablas de 2 x 2 para explorar su asociación epidemiológica. Se realizó un análisis de normalidad mediante la prueba de Kolmogorov-Smirnov para las variables de producción, clínicas y entomológicas. Además, se exploró la aleatoriedad de las variables entomológicas y se validó el supuesto mediante la prueba de las rachas. Se efectuó un análisis de diferencia entre las variables de producción y clínicas individuales y el estado de positividad en los bovinos positivos, usando la U de Mann-Whitney. La relación entre la positividad para Trypanosoma vivax en bovinos y el número de moscas capturadas según su clasificación taxonómica se analizó mediante un modelo de regresión lineal múltiple. Dicho análisis se realizó con una agrupación resumen a nueve compartimentos (salas donde se capturaron moscas). Se validaron los supuestos del modelo de regresión, los cuales se encontraron satisfactorios. Un nivel de significancia de 0,05 fue utilizado en todas las pruebas. Los datos fueron analizados en el paquete estadístico SPSS versión 19.
Resultados
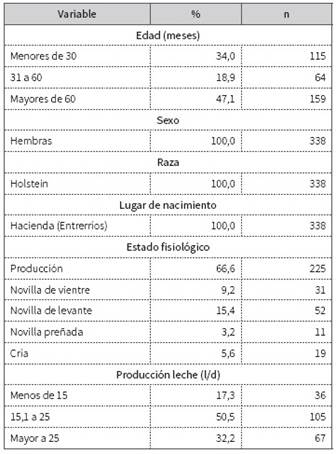
La población estudiada correspondió a bovinos de raza holstein, hembras, para las cuales se obtuvo un promedio de edad de 4,4 años (desviación 3,0), con uno de producción de 22 l/d y de 242 días en producción de leche. La población estudiada se describe en la tabla 2.
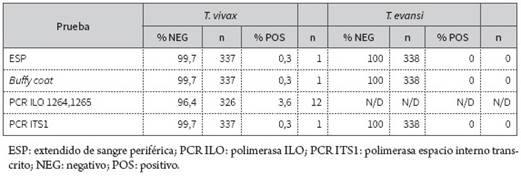
La frecuencia de infección hallada usando pruebas parasitológicas directas por microscopia (figura 1) y PCR (figuras 2a, 2b, 2c) no evidenció animales positivos para T. evansi. Los porcentajes de infección para T. vivax obtenidos por prueba se describen en la tabla 3. Para el único bovino positivo por técnicas de microscopia, la parasitemia fue de 2888 parásitos/μl.
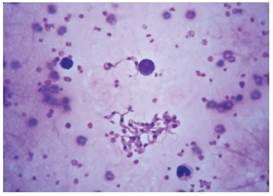
Figura 1 Agregación de tripomastigotes de Trypanosoma vivax identificados en bovino raza holstein por el método Buffy coat coloreado con Hemacolor (Merck), aumento de 400X
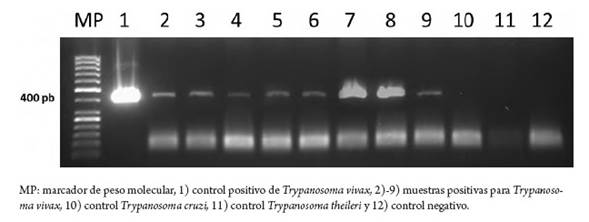
Figura 2a : Productos de amplificación de la PCR-ILO 1264, 1265 generados a partir de muestras de sangre de bovinos infectados con Trypanosoma vivax (banda de 400 pb)
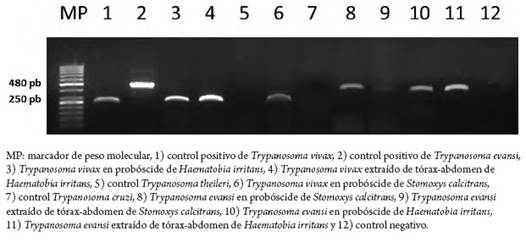
Figura 2b : Productos de amplificación de la PCR-ITS1 CF BR a partir de muestras de moscas Haematobia irritans y Stomoxys calcitrans infectadas con Trypanosoma vivax (banda de 250 pb) y Trypanosoma evansi (banda de 480 pb)
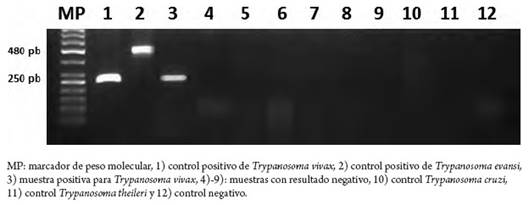
Figura 2c : Productos de amplificación de la PCR-ITS1 CF BR generados a partir de muestras de bovino
De los 17 equinos de la hacienda y 10 bovinos de la hacienda 2 no se obtuvieron resultados positivos por ninguna de las técnicas. Todos los bovinos y équidos, independientemente de ser positivos o negativos, presentaron un hematocrito dentro de los valores normales. Se obtuvo un promedio de hematocrito para los bovinos de 35 %, y en los équidos, un promedio de 38 %.
De acuerdo con el análisis bivariado con prueba χ2, no se obtuvo asociación estadísticamente significativa entre la infección por Trypanosoma vivax y las variables hematocrito (p = 0,556; OR = 0,706), edad (p = 0,997; OR =1,002), días en producción de leche (p = 0,751; OR =0,828) y el promedio de producción de leche diario (p = 0,965; OR = 1,223). Resultados similares se encontraron en el análisis bivariado con la prueba U de Mann-Withney: hematocrito (p = 0,663), edad (p = 0,547), días en producción de leche (p = 0,977) y el promedio de producción de leche diario (p = 0,889).
Mediante un análisis de la proporción de positividad de los bovinos a T. vivax (n = 12) por cada compartimento del sistema de producción, se halló un mayor número de individuos positivos en la sala de ordeño 2 (25 %).
Hallazgos entomológicos
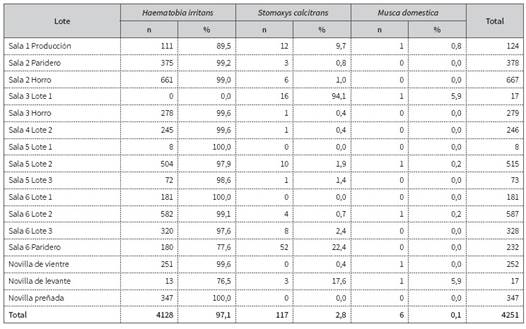
Se capturaron un total de 4251 moscas distribuidas en 16 lotes del sistema productivo. Las moscas capturadas corresponden a las especies Haematobia irritans, Stomoxys calcitrans y Musca domestica con un 97,1; 2,8 y 0,1 %, respectivamente, del total evaluado. No se encontraron especies de moscas de la familia Tabanidae. La distribución de las moscas por especie según lote se describe en la tabla 4.
De los lotes evaluados por entomología, el 6,25 % presentan moscas infectadas con T. vivax (sala 2 paridero) y el 6,25 %, con T. evansi (sala 3 horro). T. vivax fue identificado en probóscide de la mosca del establo (Stomoxys calcitrans) y en probóscide y tórax-abdomen de la mosca de los cuernos (Haematobia irritans) (figura 2b). T. evansi se encontró tanto en probóscide como en tórax-abdomen de ambas especies de moscas picadoras (figura 2b). En el caso de la mosca común (Musca domestica) no se encontraron especímenes infectados. Todos los resultados logrados en la caracterización de especies del parásito en moscas se obtuvieron con el marcador ITS1; las muestras positivas para T. vivax fueron negativas con el marcador ILO 1264, 1265.
Por análisis de regresión lineal múltiple se encontró una relación estadísticamente significativa (Anova con p =0,034) para las variables del modelo, es decir, entre el número de vacas infectadas con Trypanosoma vivax por cada compartimento de la hacienda y el número de moscas capturadas. Se validaron los supuestos del modelo de regresión, los cuales fueron satisfactorios. Las variables dentro del modelo que tuvieron significancia estadística fueron las moscas Haematobia irritans (p = 0,032) y Stomoxys calcitrans (p = 0,013) (tabla 5).
Tabla 5 Modelo de regresión lineal múltiple de las variables entomológicas relacionadas con la positividad en bovinos para Trypanosoma vivax
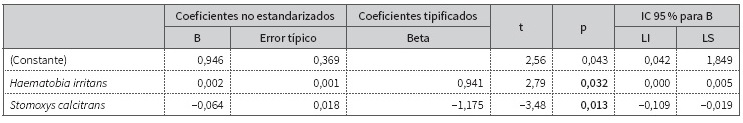
Modelo obtenido:
Bovinos positivos (T. vivax) = 0,946 + 0,002 H. irritans + (-0,064) S. calcitrans
De acuerdo con las condiciones evaluadas, el modelo indica que por cada mosca de la especie Haematobia irritans más en la hacienda habrá un incremento de 0,002 animales positivos para T. vivax, es decir, por cada incremento de 500 moscas Haematobia irritans en la zona de estudio se infectará un bovino más con T. vivax. Por otro lado, se observó una relación inversa entre el número de moscas Stomoxys calcitrans y el de animales positivos, posiblemente asociada al bajo número de individuos capturados de esta especie.
Discusión
En Colombia no se encuentran informes de Trypanosoma evansi en ganado bovino; la serorreactividad e infección por Trypanosoma vivax se ha registrado desde 1931 17, en diferentes zonas del país. Wells, Betancour y Ramírez registran seroprevalencias para T. vivax entre 1,4 y 48 % (inmunofluorescencia indirecta [IFI]) encontradas entre 1968 y 1970 en los departamentos de Córdoba, Sucre, Valle del Cauca, Boyacá y Meta; se hallaron infecciones activas por ESP en Córdoba (0,5 %), Boyacá (5,3 %) y Meta (14,9 %); y entre 1972 y 1977 se encontró serorreactividad (IFI) que osciló entre 13,5 y 62,5 % en los departamentos de Atlántico, Antioquia, Bolívar, Córdoba, Magdalena, Cauca, Valle, Caldas, Cundinamarca, Caquetá, Meta y Vichada, con infecciones activas (ESP) solo en Valle (1,3%-11,1%) y Cauca (8,3 %) 7.
En este estudio se encontró una frecuencia de infección por T. vivax en bovinos del 3,6 % (PCR con marcador ILO 1264/1265). T. vivax es un hemoprotozoario enzoótico en Colombia en alturas por debajo de los 1000 m s. n. m. 18; en pisos térmicos superiores, el parásito se ha encontrado de forma esporádica, como brotes que se han relacionado con movimientos de ganadería desde zonas enzoóticas con poblaciones de insectos hematófagos, principalmente tábanos 19. Según la literatura, a causa de la temperatura las larvas de tabánidos se desarrollan rápidamente en clima cálido y son inactivas en clima frío 20, lo que representa la interrupción en el ciclo de vida del vector. En los últimos años han comenzado a hallarse los primeros brotes por T. vivax en ganadería de leche. En Brasil, Cadioli y colaboradores 21 registraron el primer brote ocasionado por T. vivax en ganado de raza girolando y holstein de un sistema de producción semintensivo; a pesar de no haber realizado captura e identificación de vectores, los autores describen no haber observado grandes poblaciones de tabánidos, y, en contraste, abundantes cantidades de Haematobia irritans y Stomoxys calcirans. En este estudio, todos los bovinos evaluados han nacido en la hacienda; por tanto, se presenta este como un caso epidemiológico atípico de infección por Trypanosoma vivax con la posible adaptación del parásito para ser transmitido a través de potenciales vectores de la zona.
En el estudio no se identificaron episodios clínicos, no fueron evidenciados procesos de anemia ni se encontraron diferencias estadísticamente significativas (p = 0,663) entre los valores del hematocrito al comparar bovinos infectados y no infectados. Estos hallazgos difieren de los resultados obtenidos por Cuglovici y colaboradores 9 en bovinos de producción de leche con infección activa diagnosticada por la técnica de microcentrifugación del hematocrito (MHCT, por su sigla en inglés) y PCR, donde la anemia fue el signo clínico corroborado con las diferencias entre los valores del hematocrito, los cuales son menores para los bovinos infectados. Este evento puede estar relacionado con las bajas parasitemias, que son comunes en estados crónicos de la infección o también llamados periodos interepizoóticos subclínicos, los cuales se caracterizan por una relación inversamente proporcional entre la prevalencia serológica y la parasitológica, con valores de parasitemia que en ocasiones son indetectables 2,9.
Aunque no se encontró una relación estadísticamente significativa (p = 0,977) entre la producción de leche y la infección por T. vivax, es necesario considerar que bovinos en 60 meses postinfección salen de un periodo interepizoótico y comienzan nuevamente uno epizoótico, el cual constituye una etapa con un potencial riesgo para la economía del sistema productivo, debido a alteraciones en la producción y reproducción 2. Estos resultados contrastan con los obtenidos en un brote de tripanosomiasis por T. vivax en ganado de producción de leche en Colombia, donde el promedio de pérdidas económicas fue de 56,50 dólares por animal, a razón principalmente de muertes y descarte forzoso de animales adultos, reducción en la producción de leche, abortos, nacimientos de animales débiles, y el incremento en gastos por drogas y servicios veterinarios (22. En la hacienda se encontró en bovinos holstein una frecuencia de infección por Anaplasma marginale del 29,6 %; presentó coinfección el 25 % de los bovinos positivos para Trypanosoma vivax. A pesar de no haber encontrado signos clínicos en los bovinos, según la literatura, la coinfección con Anaplasma marginale y Trypanosoma vivax en bovinos limita la producción; en zonas enzoóticas la parasitemia de Anaplasma marginale puede ser baja; la inmunosupresión originada por T. vivax propicia el desarrollo de anaplasmosis, que a su vez agrava los síntomas generados por la tripanosomiasis 1.
Varios estudios en Suramérica han presentado como principales vectores de la tripanosomiasis en bovinos a moscas picadoras pertenecientes a la familia Tabanidae y a la mosca de los cuernos Stomoxys calcitrans1,23,24,25. A pesar de no haber estudios sobre capacidad vectorial en los dípteros relacionados con la transmisión de la tripanosomiasis en bovinos, la mosca Haematobia irritans no posee características anatómicas, biológicas y comportamentales para ser un buen vector. Esta mosca tiene la probóscide más pequeña de las moscas picadoras del ganado bovino, con una probóscide de 92 μm de diámetro que difiere de las 230 μm de diámetro de la probóscide de la mosca del establo 26, un ciclo de vida con una duración de dos a tres semanas; la hembra produce poca cantidad de huevos (100 a 200) al compararla con la postura de Stomoxys calcitrans (60 a 800) y aunque se alimenta de 20 a 30 veces al día, lo cual favorecería una eficiente transmisión mecánica, no es habitual que cambie de hospedero 1,20. La frecuencia de moscas encontrada y la identificación de los parásitos en moscas picadoras son indicadores de un modelo epizoótico que difiere del modelo epizoótico típico de América Latina. Los resultados nos muestran que en esta región, dedicada a la ganadería especializada en producción de leche, la mosca Haematobia irritans, con una mediana de 99,05 % (0,0-100 %) por lote, se establece probablemente como el principal potencial vector de T. vivax y T. evansi, seguida de la mosca Stomoxys calcitrans, con una mediana de 0,9 % (0,094,1 %); sin embargo, es necesario realizar estudios sobre la bionomía de las moscas y su capacidad vectorial.
Con relación a la identificación molecular de los parásitos en los vectores, se obtuvo para el marcador ITS1 CF/ BR siete muestras positivas (tres positivas para T. vivax y cuatro positivas para T. evansi); de 56 muestras evaluadas y con el marcador ILO 1264/1265 no hubo ninguna muestra positiva para T. vivax. Esta discrepancia podría estar asociada al tipo de muestra, al método de extracción del ADN y a la cantidad de parásitos en el vector mecánico. Para el marcador ILO 1264/1265 se ha registrado una buena sensibilidad (92 %) al usar ADN extraído de sangre completa o tarjetas FTA, pero su sensibilidad es muy baja cuando se utiliza papel filtro; se ha encontrado que la técnica de extracción de ADN influye sobre la sensibilidad de diferentes marcadores 27. El estudio de Gonzales y colaboradores presenta resultados de sensibilidad de tres marcadores para T. vivax incluidos los marcadores ITS1 e ILO 1264/1265 en muestras de sangre y por diferentes técnicas de extracción de ADN (27. No obstante, aún no hay estudios sobre la sensibilidad que utilicen estos marcadores con muestras de artrópodos vectores y los métodos de extracción de ADN para este tipo de muestras.
A pesar de que la captura de vectores en esta investigación se realizó entre noviembre y febrero, tiempo que correspondió en gran parte a temporada de lluvias, no se encontraron tabánidos. No hay estudios sobre tripanosomiasis y sus vectores en zonas de vida similares a Entrerríos. Sin embargo, en zonas más cálidas de Colombia y Brasil se presenta una relación entre las temporadas de lluvias de diferentes épocas del año y los picos de infestación por tabánidos 25; septiembre-octubre a diciembre-enero son los periodos con picos poblacionales de tabánidos más altos, y por tanto es considerado el periodo de mayor riesgo para la transmisión de tripanosomas en bovinos 23.
A diferencia de los resultados de este estudio, en los que Haematobia irritans se establece como el probable vector más prevalente y en los cuales estuvieron ausentes los tabánidos, un estudio sobre identificación de posibles vectores de la tripanosomiasis bovina llevado a cabo en Caucasia, norte de Antioquia, que implementó la misma técnica de captura de este estudio, encontró en un periodo entre junio y septiembre un total de 140 tabánidos de nueve especies distribuidas en los géneros Tabanus, Lepiselaga, Chrysops y Cryptotylus. En el estudio se halló en intestino medio de una mosca de la especie T. nebulosus y en intestino medio y glándulas salivales de dos moscas T. occidentalis flagelados compatibles con T. vivax25, lo cual muestra que en esta región enzoótica para la tripanosomiasis la transmisión es realizada por los típicos vectores de zonas donde la transmisión es mecánica.
Zapata y Reyes encontraron el primer caso sintomático de tripanosomiasis diagnosticado por ESP (parasitemia = 1575 tripanosomas/ul) y el método Buffy coat en un lote de producción de la hacienda. Luego, en un período de dos semanas aparecieron otros dos casos sintomáticos y diagnosticados por técnicas de microscopia. Unas semanas después, al incluirlos en el estudio, tan solo uno fue positivo por técnicas moleculares, lo que muestra periodos de parasitemia intermitentes con manifestaciones clínicas en el animal 28. Estos bovinos presentaron en común una edad superior a los 60 meses, evento epizootiológico relacionado con las prevalencias serológicas y parasitológicas de T. vivax dadas en bovinos de zonas donde la transmisión es mecánica 2. De los bovinos positivos en la investigación, el 50 % se encuentra por encima de los 60 meses (rango = 60-110,4 meses), el 41,7 % corresponde a bovinos menores de 30 meses (rango =14,4-25,2 meses) y tan solo el 8,3 % está representado por un bovino que estaba entre los 31 y 60 meses de edad (49,2 meses).
Estos hallazgos son concordantes con el modelo de tendencia de prevalencia parasitológica de T. vivax y prevalencia serológica en poblaciones expuestas a vectores mecánicos, en los cuales los 30 primeros meses posinfección corresponden a un periodo epizoótico con parasitemias detectables e intermitentes con un pico de prevalencia serológica cerca del mes 10 posinfección, período en el cual se evidencian fases clínicas de la infección; luego, entre los meses 30 y 63 hay un período interepizoótico subclínico caracterizado por parasitemias indetectables y un descenso gradual en la inmunidad; aproximadamente, de los 63 meses posinfección en adelante empieza un período epizoótico en el que la prevalencia parasitológica puede incrementarse de forma impredecible con presentación de casos clínicos 2.
El modelo de regresión lineal múltiple muestra la relación que tiene la densidad poblacional de la mosca Haematobia irritans con la infección por T. vivax en bovinos de la zona de estudio. El modelo señala que en un incremento poblacional de vectores por cada 500 moscas Haematobia irritans más en la zona de estudio puede aparecer un nuevo bovino infectado, lo que hace apremiante conocer la dinámica poblacional de Haematobia irritans a través del tiempo, y así poder implementar un manejo integral coherente con la situación epizoótica según la época del año, la cual está directamente relacionada con la variación del clima y la zona de vida. De acuerdo con los estudios en diferentes países de América Latina, son notables las variaciones poblacionales según la época del año; sin embargo, es consistente encontrar en países tropicales y subtropicales los picos de infestación más altos por Haematobia irritans al inicio y final de las temporadas de lluvias, y en primavera para países con estaciones climáticas 29,30,31.
Conclusiones
Los resultados obtenidos en este estudio nos permiten concluir que T. vivax y T. evansi están presentes en las moscas Haematobia irritans y Stomoxys calcitrans, y a pesar de haber encontrado bovinos positivos únicamente para T. vivax, ambos hemoparásitos pueden estar realizando ciclos de transmisión en bovinos raza holstein de Entrerríos, Antioquia. Por las características de la epizootiología de la tripanosomiasis en la hacienda estudiada, este se concibe como un caso atípico al ocurrido en zonas enzoóticas del país y de otros países suramericanos, donde las condiciones ecológicas y climáticas permiten la coexistencia de tabánidos como principal vector. Los análisis entomológicos y parasitológicos permiten concluir que la mosca picadora Haematobia irritans es el principal vector de T. vivax y T. evansi en la zona de estudio.