Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Boletín de Investigaciones Marinas y Costeras - INVEMAR
Print version ISSN 0122-9761
Bol. Invest. Mar. Cost. vol.34 no.1 Santa Marta Dec. 2005
Andrés M. Vidal1, Claudia M. Villamil2 y Alberto Acosta3
1Pontifica Universidad Javeriana, Carrera 7 # 43 – 82, Edificio 53 Oficina 106 B. Departamento de Biología, Bogotá, Colombia. E-mail: amvidal@javeriana.edu.co
2Pontifica Universidad Javeriana, Carrera 7 # 43 – 82, Edificio 53 Oficina 106 B. Departamento de Biología, Bogotá, Colombia. E-mail: c.villamil@javeriana.edu.co
3Pontifica Universidad Javeriana, Carrera 7 # 43 – 82, Edificio 53 Oficina 106 B. Departamento de Biología, Bogotá, Colombia. E-mail: laacosta@javeriana.edu.co
RESUMEN
El reclutamiento de corales en un arrecife determina el mantenimiento, la renovación y la estructura futura de las comunidades coralinas. Con el objeto de conocer la composición, densidad y el valor de importancia de corales juveniles escleractínios (< 2 o < 4 cm de diámetro; según la especie) se muestrearon dos localidades (Reggae Nest y El Faro) en la terraza profunda de sotavento, a 20 m de profundidad, en la isla de San Andrés. Así mismo, se cuantificó la frecuencia de mortalidad parcial, total, enfermedades y signos de depredación en los juveniles, en 47 cuadrantes de 1m², distribuidos a lo largo de una cuerda guía. Se registró un total de 397 juveniles coralinos pertenecientes a 16 especies. La densidad promedio y riqueza de juveniles no mostraron diferencias significativas entre Reggae Nest y El Faro. La densidad promedio de las localidades fue alta respecto a lo registrado en arrecifes colombianos y baja en relación a otros arrecifes del Caribe. Las especies con valores de importancia mayores, Agaricia agaricites, Scolymia sp. y Porites astreoides, aportaron el 54.9 % de todos los juveniles, lo que concuerda con lo hallado en otros arrecifes del Caribe. Los géneros de juveniles con mayor densidad, cobertura y frecuencia no concordaron con los adultos dominantes (ej. Montastraea, Colpophyllia, Diploria y Siderastrea); ya que M. annularis y Diploria sp. exhibieron los valores más bajos de importancia como juveniles. Las comunidades coralinas de Reggae Nest y El Faro, deterioradas en las últimas décadas, podría recuperarse naturalmente, teniendo en cuenta la siguiente evidencia: 1) alta densidad de corales juveniles respecto al Caribe colombiano; 2) alta riqueza de juveniles, representados en 16 de las 23 especies de corales adultos registrados para la isla; 3) alto porcentaje de especies comunes entre juveniles y adultos (mantenimiento de cada población); 4) bajos porcentajes de mortalidad parcial (0.7 %; 3 juveniles de 397) y de blanqueamiento encontrados en los juveniles (0.5 %; 2 juveniles de 397). Queda aún por comprobar, la sobrevivencia a largo plazo, si estos juveniles son de especies fugitivas o si la comunidad de constructores está siendo reemplazada.
PALABRAS CLAVE: Corales escleractínios, Juveniles, Composición, Densidad, San Andrés.
ABSTRACT
Coral reef recruitment is a fundamental process because it determines the maintenance, renovation and future reef structure. In order to determine the composition, density and importance value of scleractinian juvenile corals (<2 or < 4 cm of diameter; depending of the species) two localities were sampled (Reggae Nest and El Faro) at the deep leeward terrace site of San Andres Island. In adittion, in 47 quadrants of 1m² distributed throughout a guide line, frequency of partial mortality, total diseases and depredation signs in juvenile corals were quantified. A total of 397 juveniles of 16 species were registered. The average density and richness of juveniles were not significantly different between Reggae Nest and El Faro. The average density of both localities was high compared to other colombian reefs and lower compared to other reefs in the Caribbean. The species with higher importance value, Agaricia agaricites, Scolymia sp. and Porites astreoides, represented 54.9% of all juveniles, similar to other Caribbean reefs. The genera of juveniles with higher importance value were not the same as the dominant adults (ej. Montastraea, Colpophyllia, Diploria and Siderastrea); which showed the lowest importance value as juveniles (Montastraea annularis and Diploria sp.). The coral communities of Reggae Nest and El Faro, deteriorated in the last decades, could recover naturally, considering the following evidence: 1) high juvenile coral density compared to the Colombian Caribbean; 2) high richness of juveniles, 16 from the 23 coral adults species reported for the island; 3) high percentage of common species between juveniles and adults (maintenance of each population); 4) low partial mortality (0.7%; 3 of 397 juveniles) and bleaching found in juvenile corals (0.5%; 2 juveniles of 397). It is still to verify if these juveniles are fugitive species or if the community of builder species may be replaced.
KEY WORDS: Sleractinian corals, Juveniles, Composition, Density, San Andres Island.
INTRODUCCIÓN
El reclutamiento de corales dentro de un arrecife es un proceso fundamental ya que determina el mantenimiento, la renovación y la estructura futura de las comunidades coralinas (Bak y Engel, 1979). Los patrones de asentamiento, supervivencia y crecimiento de juveniles de coral pueden llegar a influenciar directamente la estructura y función de las comunidades coralinas y la permanencia de las especies mediante el reemplazamiento de individuos que mueren. Además, aportan nuevos genotipos al sistema, manteniendo la variabilidad genética y minimizando la posibilidad de extinciones locales (Wittenberg y Hunte, 1991; Caley et al., 1996; Porter y Tougas, 2001).
La permanencia de los corales está asociada con su reproducción sexual, mecanismo que además les permite la dispersión y colonización de nuevos ambientes (Harrison y Wallace, 1990). Dentro de la reproducción sexual se pueden encontrar especies gonocóricas o hermafroditas (Richmond y Hunter, 1990). Así mismo, se pueden distinguir especies de desove masivo (fecundación externa) o especies que incuban plánulas (fecundación interna; Birkeland, 1997).
Las plánulas de coral pueden sobrevivir en la columna de agua entre unos pocos días y hasta tres semanas, tiempo durante el cual se dispersan con la ayuda de corrientes locales (Harrison y Wallace, 1990; Richmond y Hunter, 1990; Chiappone y Sullivan, 1996). La dispersión larval ayuda a mantener el flujo genético de las poblaciones coralinas entre arrecifes (Porter y Tougas, 2001). Las larvas buscan superficies duras y finalmente logran asentarse (colonizar) para sufrir metamorfosis y transformarse en pólipos. Mediante reproducción asexual los pólipos incrementan su número, la colonia crece, se convierte en juvenil y posteriormente en colonia adulta (Richmond y Hunter, 1990; Porter y Tougas, 2001).
Como sinónimo parcial de juvenil existe el término de recluta. Los juveniles involucran corales recién reclutados (Richmond y Hunter, 1990) y otros que reclutaron un tiempo atrás, pertenecientes a otras cohortes, y que adicionalmente han logrado crecer. El recluta es un individuo nuevo, que arriba a una población dada, o pólipo solitario más pequeño que ha logrado sobrevivir desde la fijación y metamorfosis (asentamiento) hasta ser observado por un investigador. Dado que el límite superior de talla o edad de un juvenil es arbitrario; en este estudio los juveniles se definieron como el pólipo o las colonias visibles al ojo humano (> 3 mm de diámetro) con diámetro inferior a 2 cm o 4 cm según la especie, que por su tamaño no han logrado la madurez sexual (Bak y Engel, 1979; Caley et al., 1996). Por lo tanto, en esta investigación la cantidad de juveniles se tomó como variable para estimar el reclutamiento, y sirve como medida indirecta de la tasa de recambio de cada población.
El reclutamiento, definido como el proceso en donde nuevos miembros que entran a una población por reproducción sexual, se hacen visibles y pueden ser registrados en campo (Connell, 1985), es un componente importante de la historia de vida de los corales y claramente depende de un gran número de factores tales como: 1) profundidad, debido más a la falta de luz que al gradiente de presión física (Birkeland et al., 1981; Huston, 1985); 2) tipo de sustrato (rocoso, coral muerto, artificial), disponibilidad (libre de competidores; Chiappone y Sullivan, 1996) y topografía: la complejidad del sustrato favorece la formación de microhábitats óptimos para el asentamiento larval (Carleton y Sammarco, 1987; Banks y Harriot, 1996); 3) oceanografía local: la dispersión y asentamiento de larvas depende de las corrientes predominantes, 4) sedimentación: los altos niveles de sedimentación causan muerte por ahogamiento de los juveniles, además de originar un sustrato poco favorable para el asentamiento o desarrollo de algas rojas incrustantes, organismos importantes en la detección química del sustrato por parte de las plánulas coralinas (Wittemberg y Hunte, 1991; Torres y Morelock, 2002); 5) perturbaciones, como nutrificación, que favorece las macroalgas, altamente competitivas por el sustrato (Sammarco, 1991; Torres y Morelock, 2002); 6) pastoreo inadvertido sobre reclutas por parte de herbívoros (Sammarco, 1991).
Varios estudios han tratado de explicar la estructura de la comunidad coralina de adultos en términos de la composición y abundancia de juveniles. Algunos autores, sugieren que la composición de juveniles no está relacionada con la composición de adultos (Bak y Engel, 1979; Rylaarsdam, 1983), sin embargo, otros autores han demostrado que la densidad de adultos y juveniles está correlacionada positivamente (Grigg y Maragos, 1974; Chiappone y Sullivan, 1996). Para los arrecifes colombianos, la relación entre la comunidad de corales adultos y la de corales juveniles aún no es clara.
En Colombia, la mayoría de los trabajos realizados sobre corales se han restringido a describir la estructura de la comunidad de las especies coralinas adultas formadoras de arrecifes (Díaz et al., 2000; Reyes, 2000). Según Cendales et al., (2002) en el Caribe colombiano, las especies dominantes del pasado (ej. Acropora), están siendo reemplazadas por especies generalistas (de alto reclutamiento) que se adaptan rápidamente a ambientes perturbados (ej. Agaricia agaricites y Porites astreoides). Sólo el estudio de Pizarro (2002), involucra aspectos poblacionales tanto a nivel espacial como temporal de los juveniles de Diploria labyrinthiformis, D. strigosa y Colpophyllia natans en la isla de San Andrés. Pizarro (2002) sugiere que si el deterioro en los arrecifes de la isla continua, es posible que las poblaciones de estos corales pétreos disminuyan o desaparezcan. En general, se desconoce para los arrecifes colombianos, cuales especies reclutan, cuando, cuanto y donde lo están haciendo, tanto a nivel horizontal como vertical, así como en arrecifes considerados deteriorados o en mejor estado de conservación. Debido a la importancia del reclutamiento como proceso, el objetivo de este estudio fue determinar la composición y densidad de corales juveniles, tomando como modelo inicial dos localidades de la terraza profunda de sotavento de la isla de San Andrés, en uno de los arrecifes con mayor cobertura y riqueza coralina del Caribe colombiano.
ÁREA DE ESTUDIO
La isla de San Andrés está localizada en el Caribe Occidental a 800 km de Colombia (12º 32’ N, 81º 43’ W; Figura. 1). Es una isla oceánica, separada de la plataforma más cercana por profundidades superiores a los 1000 m (Díaz et al., 1995). Tanto la isla (13 km de largo y 3 km de ancho) como la plataforma circundante son de origen fundamentalmente coralino (Díaz et al., 1995).
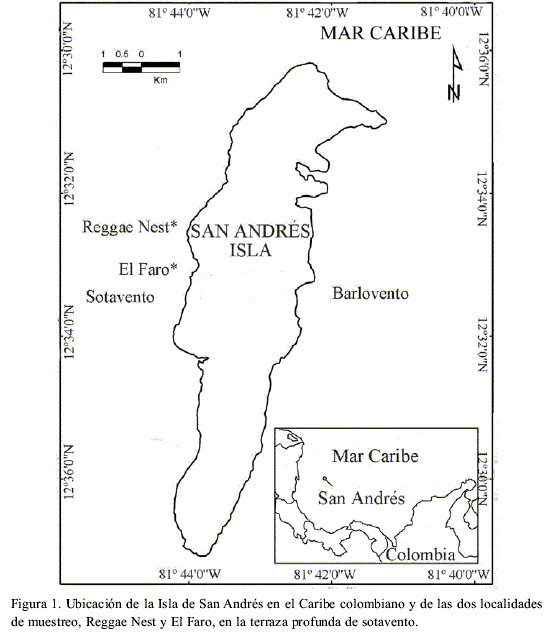
La Corriente superficial del Caribe fluye de oriente a occidente y sufre un desvío hacia el suroccidente cuando llega a la elevación de Nicaragua para formar un remolino en sentido contrario a las manecillas del reloj en el Caribe suroccidental (Geister y Díaz, 1997). La corriente enfrenta al archipiélago de San Andrés por el oriente en el lado norte y por el nororiente en el lado sur, con velocidades entre 0.5 y 1 m/s (Díaz et al., 1996). Las aguas pluviales cargadas de sedimentos provenientes del continente centroamericano no alcanzan a afectar la salinidad ni la transparencia de las aguas oceánicas del archipiélago.
La plataforma submarina occidental de la isla se encuentra dividida en tres terrazas, una emergida y dos sumergidas. La tercera terraza arrecifal, la más profunda, que fue escogida como sitio de muestreo, comienza a los 10-11 m de profundidad y termina súbitamente entre 20 y 25 m de profundidad, donde el talud se precipita en forma casi vertical hasta profundidades de más de 500 m (Díaz et al., 1995; 1996). Según Díaz et al., (1996), en la isla de San Andrés se conocen 51 especies de corales escleractínios, 24 de las cuales se encuentran en la terraza profunda de sotavento entre 18 – 20 m de profundidad, lo cual corresponde a una diversidad bastante alta en esta zona arrecifal considerada en relativo buen estado de conservación (Díaz et al., 1995; Acosta obs. pers.). Las especies dominantes (corales adultos) en dicha terraza son Montastraea annularis (sensu lato), M. cavernosa y Colpophyllia natans (Díaz et al., 1996). Se compararon dos terrazas profundas, Reggae Nest (12°31’63”N; 81°43’56”W) y El Faro (12°32’71”N; 81°44’23”W), las cuales presentan similar cobertura de coral vivo (40% y 35% respectivamente), de macroalgas como Lobophora sp. y Halimeda spp., al igual que similar composición de especies y alta diversidad de corales, esponjas y octocorales.
METODOLOGÍA
Fase de Campo y Colección de Datos
Se cuantificaron los juveniles de coral en 47 cuadrantes de 1 m2 en la terraza profunda de sotavento en abril de 2003, en las localidades conocidas como Reggae Nest y El Faro (Figura 1). Tanto las localidades como la profundidad de muestreo (20 m) fueron escogidos a partir de bibliografía, así como después de un reconocimiento en campo de las localidades con mejor desarrollo arrecifal en términos de cobertura y riqueza. Los cuadrantes, separados entre sí por 4 m, fueron colocados a lado y lado de una cuerda guía paralela a la costa.
Dentro de cada cuadrante se identificaron in situ todos los juveniles de coral, buscando en lugares crípticos y limpiando el sedimento del fondo cuando fue necesario. Los juveniles fueron definidos como las colonias menores a 4 cm de diámetro según Bak y Egenl (1979), Richmond y Hunter (1990) y Harrison y Wallace (1990) para especies de gran talla como los géneros Montastraea, Diploria y Siderastrea, entre otras. Para especies pequeñas como Porites astreoides y Favia fragum, los corales juveniles fueron definidos como aquellas colonias menores de 2 cm de diámetro. Se midió el diámetro de los juveniles para posteriormente calcular el área de cobertura por especies y para la comunidad. De igual forma, se determinó para los juveniles si estos presentaban mortalidad tanto parcial como total (evidenciada por los esqueletos), signos de depredación o algún tipo de enfermedad (ej. blanqueamiento).
Fase Analítica de Datos
Se organizaron matrices con el número de juveniles por especie en cada cuadrante y en la totalidad de cuadrantes por sitio y para las 2 localidades combinadas. Con los datos se calculó: la densidad absoluta (∑juveniles por especie / área total muestreada), la densidad relativa (∑ juveniles por especie /∑ total de juveniles de todas las especies x 100 %), la frecuencia absoluta (∑ cuadrantes donde aparece la especie), la frecuencia relativa (Frecuencia absoluta por especie / ∑ total de frecuencias absolutas de las especies x 100%), la cobertura total ocupada por especie (área total de los juveniles), la dominancia relativa (área total de juveniles por especie / ∑ área total ocupada por todas las especies x 100 %) y finalmente se calculó el índice de valor de importancia (IVI; en porcentaje) para las especies de la comunidad sugerido por Lamprecht (1990). La fórmula del IVI es densidad relativa + frecuencia relativa + dominancia relativa o cobertura / 3. El número de especies y la densidad se compararon entre Reggae Nest y El Faro con la prueba no paramétrica de Kruskal-Wallis.
RESULTADOS
Se encontraron juveniles de 16 especies de corales escleractínios en las dos localidades de muestreo. De 397 juveniles, 195 correspondieron a Reggae Nest y 202 a El Faro. La densidad promedio para las dos localidades fue de 8.4 ± 1.9 juv/m2; siendo de 8.9 ± 3.5 juv/m2 para Reggae Nest y 8.0 ± 3,0 juv/m2 para El Faro (Tabla 1). La densidad de juveniles no mostró diferencias significativas entre las dos localidades muestreadas (p = 0.3; n = 47; Kruskal-Wallis). Los juveniles de Agaricia agaricites, Scolymia sp. y Porites astreoides, contribuyeron con el 54.9 % de todos los juveniles cuantificados.
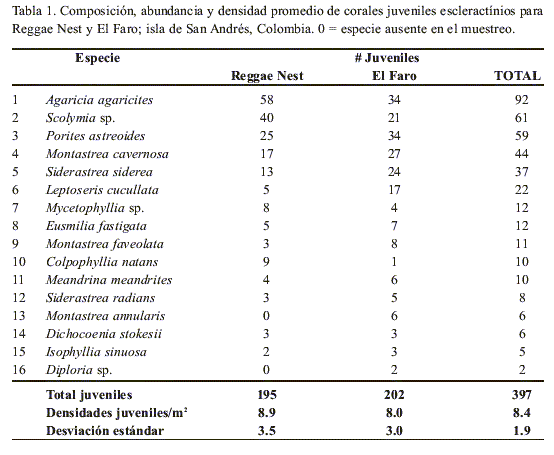
En Reggae Nest se observaron juveniles de 14 especies de corales, donde Agaricia agaricites, Scolymia sp. y Porites astreoides fueron los más abundantes, aportando el 31.8% del total de juveniles del lugar. Las especies con menor número de juveniles fueron Diploria sp., Isophyllia sinuosa, Dichocoenia stokesii, Montastraea annularis (sensu lato) y Siderastrea radians (Tabla 1). En El Faro se cuantificaron juveniles de 16 especies corales, de las cuales A. agaricites, Scolymia sp. y P. astreoides también fueron las más comunes, aportando el 23.1% del total de juveniles; la menor abundancia de juveniles fue de Diploria sp., Isophyllia sinuosa y D. stokesii (Tabla 1).
De todas las especies de juveniles, Agaricia agaricites exhibió los valores más altos de IVI (presentando mayor abundancia, densidad, frecuencia, dominancia relativa y área colonial), seguido por Scolymia sp., Porites astreoides y Montastraea cavernosa. Las especies de juveniles que presentaron los valores más bajos de importancia (menor densidad, frecuencia y dominancia) fueron Diploria sp., M. annularis, Isophyllia sinuosa y Dichocoenia stokesii (Tabla 2).
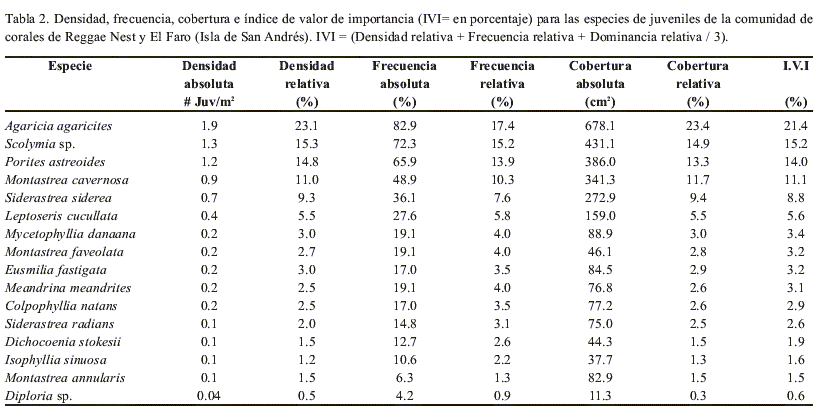
La cobertura de tejido vivo ocupado por juveniles en las dos localidades correspondió a un área total de 2894 cm2, representando el 0.6 % del área muestreada. Tan solo el 3.7 % de los juveniles muestreados presentaron signos de deterioro (Tabla 3). El porcentaje de juveniles coralinos con mortalidad total y con mortalidad parcial (depredación por mordeduras de peces) fue inferior al 1.5 % (Tabla 3), siendo Agaricia agaricites y Siderastrea siderea las más afectadas. Dos juveniles presentaron blanqueamiento. Y no fue observado contacto directo entre juveniles y macroalgas. El sustrato sobre el que se encontró la mayoría de juveniles fue de tipo coralino (esqueletos de coral). El 75 % de los juveniles cuantificados se encontraron en lugares crípticos.

DISCUSIÓN
En este estudio, Agaricia agaricites y Porites astreoides fueron las especies de juveniles dominantes, similar a lo encontrado por Chiappone y Sullivan (1996) y Edmunds (2000) en Florida y Curazao respectivamente. De igual manera, A. agaricites y P. astreoides son dominantes en otros arrecifes del Caribe colombiano (Providencia, Isla Grande e Isla Fuerte; A. Acosta, datos sin publicar). Estas especies son, de acuerdo al IVI, dos de las tres especies más importantes (primera y tercera especie respectivamente) en Reggae Nest y El Faro. No obstante, A. agaricites aportó sólo el 22.3 % del total de juveniles cuantificados a 20 m, siendo mucho menor a lo registrado en otros arrecifes del Caribe (84 %), lo cual podría explicarse por el mayor reclutamiento de esta especie en zonas someras e intermedias (< 16 m; Bak, 1979; Hughes, 1985; Vidal, 2005).
El número de especies de corales juveniles encontradas en el presente estudio a 20 m de profundidad es considerado alto comparado con la riqueza registrada en otros arrecifes del Caribe; por ejemplo, Chiappone y Sullivan (1996) también encontraron 16 especies de corales juveniles en el Florida Reef Tract, pero abarcando una mayor amplitud de profundidad (2-18 m). Adicionalmente, la riqueza de la comunidad de corales juveniles a 20 m de profundidad en San Andrés supera, en términos relativos, a la cuantificada en otros arrecifes continentales (Isla Grande, Isla Fuerte) e insulares (Providencia) de Colombia (A. Acosta, datos sin publicar). Existen 51 especies de corales escleractínios registradas para el complejo arrecifal de San Andrés (Reyes, 2000), pero tan sólo 23 de las 51 especies de coral (45 %) están presentes a 20 m (Vidal, 2005). El que la mayoría de las 23 especies de corales adultos estén reclutando a 20 m (16 especies como juveniles) sugiere que en las dos localidades de Sotavento de la isla de San Andrés podrían existir las condiciones adecuadas para procesos como asentamiento y reclutamiento coralino.
Por su parte, la densidad promedio de juveniles (8.4 juv/m²) fue mayor a lo registrado en Florida (1 a 2 juv/m²; Chiappone y Sullivan, 1996) pero menor respecto a otros arrecifes del Caribe (10 a 18 juv/m²; Edmunds y Bruno, 1996). No obstante, resultó más alta comparada con otros arrecifes colombianos (1 a 8 juv/m²; Ordóñez, 2005; J. Rodríguez, com. per.; L. Dueñas, com. per.).
Por otro lado, el hecho de que especies incubadoras de plánulas como Agaricia agaricites, Scolymia sp. y Porites astreoides aporten el mayor número de juveniles en los arrecifes estudiados, podría estar corroborando lo expuesto por Knowlton (2001) y Carlon (2002), quienes sugieren que en los últimos años las poblaciones de especies incubadoras están aumentando su número e importancia relativa, mientras que especies liberadoras de gametos y altamente constructoras como Montastraea spp., Acropora sp. y Diploria spp. están disminuyendo sus tasas de reclutamiento en todo el Caribe. Lo anterior nos plantea las siguientes preguntas: ¿será que la composición y dominancia de los arrecifes en el futuro estará a cargo de las especies incubadoras de larvas como lo han sugerido autores como Connell (1997) y Harriot (1999)?, o que ¿el alto nivel de reclutamiento de estas especies está y seguirá relacionado con su alta tasa de mortalidad (ej. 64% de los juveniles de A. agaricites no llegan a ser colonias adultas; Hughes, 1985)? Esto explicaría por qué estas especies aún no son dominantes sino fugitivas en la comunidad de corales de adultos.
Al comparar los valores de cobertura de corales juveniles de este estudio con los de corales adultos reportados por Díaz et al., (1995) a la misma profundidad y en la zona sotavento de San Andrés (ej. La Piscinita), se observó que las especies dominantes en términos de cobertura relativa para corales juveniles (Agaricia agaricites = 0.6 %, Scolymia sp. = 0.4 % y Porites astreoides = 0.3 %) no eran las mismas que para corales adultos (Montastraea annularis sensu lato)= 50 %, Colpophyllia natans = 20 % y Diploria spp. = 15 %). Wittemberg y Hunte (1991) y Edmunds (2000) demostraron similaridad en composición de corales juveniles y adultos dominantes (generalmente especies fugitivas, ej. Agaricia agaricites) en arrecifes altamente eutroficados y sedimentados; esta similaridad en composición es sugerida por los autores como un indicador del deterioro arrecifal, ya que estaría indicando fuertes presiones de selección, donde solo pocas especies con ciertas estrategias de vida lograrían colonizar, sobrevivir y reproducirse. Similar composición de especies dominantes, tanto de corales juveniles como de adultos, fue recientemente observada en Isla Fuerte, Caribe colombiano (Sepúlveda y Acosta, 2005) expuesto a alta sedimentación (descarga de ríos Sinú y Atrato); mientras que en arrecifes con menor disturbio por descargas continentales (ej. San Andrés) se ha observado diferencia entre las especies de juveniles que colonizan el sustrato en grandes números y las colonias que llegan a sobrevivir como adultos dominantes (Wittenberg y Hunte, 1991).
Dados el alto número de especies encontradas, la alta densidad de corales juveniles a 20 m en sotavento respecto al Caribe continental colombiano, el alto porcentaje de especies de adultos con éxito reproductivo (70 %, representados en 16 especies de juveniles encontrados) y la baja evidencia de deterioro de los juveniles, se puede decir que la comunidad coralina de Reggae Nest y El Faro a 20 m (sotavento en San Andrés) deteriorada en las últimas décadas (Díaz et al., 1995; Rodríguez-Ramírez, 2004), podría presentar actualmente condiciones adecuadas para que el reclutamiento coralino y la recuperación natural del arrecife se pueda llevar a cabo. No obstante, es importante corroborar esta hipótesis evaluando la sobrevivencia de juveniles de especies constructoras a lo largo de varios años y establecer el potencial que poseen los juveniles de especies fugitivas (grandes colonizadoras, competidoras interespecíficas inferiores; Lincon et al., 1998) para reemplazar a la comunidad de constructores.
AGRADECIMIENTOS
Este trabajo fue posible gracias a la colaboración de los estudiantes del curso de Ecología Marina (I semestre-2003; Katherine Bernal, Ricardo Carrera, Catalina Ramírez, Marcela Rosero, Diana Velásquez y Silvia Velásquez), Departamento de Biología, Facultad de Ciencias (PUJ), quienes participaron en los muestreos. A CORALINA por el permiso otorgado para la actividad docente, a la tienda de buceo Banda Dive Shop por los servicios prestados y a nuestros padres por su gran apoyo.
BIBLIOGRAFÍA
1. Acosta, A., P.W. Sammarco y F. Duarte. 2001. Asexual reproduction in a zoanthid by fragmentation: the role of exogenous factors. Bull. Mar. Sci., 68: 363-381. [ Links ]
2. Bak, R.P. 1979. Aspects of community organization in Caribbean stony corals (Scleractnia). Bull. Mar. Sci., 23: 51-68. [ Links ]
3. Banks, S.A. y V.J. Harriot. 1996. Patterns of recruitment at the Gneering Snoals, southeast Queensland, Australia. Coral Reefs., 5: 225-230. [ Links ]
4. Bak, R.P y M.S. Engel. 1979. Distribution, abundance and survival or juvenil hermatypic corals (Scleractinia) and the importance of life history strategies in the Parent Coral Community. Mar. Biol., 54: 341-352. [ Links ]
5. Birkeland, C. 1977. The importance of rate of biomass accumulation in early successional stages of benthic communities to the survival of coral recruits. Proc. 3th Int. Coral Reef Symp., 1:15 21. [ Links ]
6. Birkeland C., Rowley D. y R.H. Randall. 1981. Coral recruitment pattenrs at Guam. Proc. 4th Int. Coral Reef Symp., 2: 339-344. [ Links ]
7. Caley, M.J., M.H. Carr, M.A. Hixon, T.P. Hughes, G.P. Jones, y B.A. Menge. 1996. Recruitment and the local dynamics of open marine populations. An. Rev. Ecol. Syst., 27: 477-500. [ Links ]
8. Carlon, D.B. 2002. Production and supply of larvae as determinants of zonation in a brooding tropical coral. Jour. Exper. Mar. Biol. Ecol., 268: 33-46. [ Links ]
9. Carleton, J.H. y P.W. Sammarco. 1987. Effects of substratum irregularity on success of coral settlement: Quantification by comparative geomorphological techniques. Bull. Mar. Sci., 40: 85-98. [ Links ]
10. Cendales, M.H., S. Zea y J.M. Díaz. 2002. Geomorfología y unidades ecológicas del complejo arrecifal de las Islas del Rosario e Isla Barú (Mar caribe, Colombia). Rev. Acad. Colomb. Cien. Exac. Fís. Natu., 26 (101): 497-510. [ Links ]
11. Chiappone, M. y K.M. Sullivan. 1996. Distribution, abundance and species composition of juvenile scleractinian corals in the Florida reef tract. Bull. Mar. Sci., 58 (2): 555-569. [ Links ]
12. Connell, J.H. 1985. The consequences of variation in initial settlement vs. postsettlement mortality in rock intertidal communities. Jour. Exper. Mar. Biol. Ecol., 93: 11-65. [ Links ]
13. _____. 1997. Disturbance and recovery of coral assemblages. Proc. 8th Int. Coral Reef Symp., 1: 9 22. [ Links ]
14. Díaz, J.M., J. Garzón-Ferreira, y S. Zea, 1995. Los arrecifes coralinos de la isla de San Andrés: estado actual y perspectiva para su conservación. Acad. Colomb. Cien. Exac. Fís. Natu.. Colección Jorge Álvarez Lleras 7. Bogotá. Colombia 1-150. [ Links ]
15. Díaz, J.M., G. Díaz-Pulido, J. Garzón-Ferreira, J. Geister, J.A. Sánchez, y S. Zea, 1996. Atlas de los arrecifes coralinos del Caribe colombiano. Tomo I. Complejos arrecifales oceánicos. Invemar, Santa Marta. Serie Publicaciones Especiales 2: 83p. [ Links ]
16. Díaz, J.M., L.M. Barrios, M.H. Cendales, J. Garzón-Ferreira, J. Geister, M. Lopez-Victoria, H. Ospina, F. Parra-Velandia, J. Pinzon, B. Vargas-Angel, F. Zapata, y S. Zea. 2000. Areas coralinas de Colombia. Invemar, Santa Marta. Serie Publicaciones Especiales 5: 176 p. [ Links ]
17. Dustan, P. 1977. Vitality of reef coral populations off Key Largo, Florida: recruitment and mortality. Envir. Geol., 2: 51-58. [ Links ]
18. Edmunds, P.J. 2000. Patterns in the distribution of juvenile corals and coral reef community structure in St. John, US Virgin Islands. Mar. Ecol. Prog. Ser., 202: 113-124. [ Links ]
19. Edmunds, P.J. y J.F. Bruno. 1996. The importance of sampling scale in ecology kilometer-wide variation in coral reef communities. Mar. Ecol. Prog. Ser., 143: 165-171. [ Links ]
20. Geister, J. y J.M. Díaz. 1997. Field guide to the oceanic barrier reefs and atolls of the southwestern Caribbean (Archipiélago of San Andrés and Providencia, Colombia). Proc. 8th Int. Coral Reef Symp., 1: 235-262. [ Links ]
21. Grigg, R. y J.E. Maragos. 1974 Recolonization of hermatypic corals on submerged larva flows in Hawaii. Ecology, 55: 378-395. [ Links ]
22. Harriott, V.J. 1999. Coral recruitment at a high latitude pacific site: a comparison with Atlantic reefs. Bull. Mar. Sci., 65 (3): 881-891. [ Links ]
23. Harrison, P.L. y C.C. Wallace 1990. Reproduction, dispersal and recruitment of scleractinian corals: 133-207. En Z. Dubinsky, Ecosystems of the world. 25: Coral Reefs. Elsevier, Amsterdam. [ Links ]
24. Hughes, T.P. 1985. Life histories and population dynamics of early successional corals. Proc. 5th Int. Coral Reef Congress, Tahiti. 4:101 – 105. [ Links ]
25. Huston, M.A. 1985. Patterns of species diversity on coral reefs. An. Rev. Ecol. Syst., 16: 149-177. [ Links ]
26. Knowlton, N. 2001. The future of coral reefs. Proc. Nat. Acad. Sci. United States America, 98 (10) 5419-5425. [ Links ]
27. Lamprecht, H. 1990. Silvicultura en los trópicos. Deutsche Gesellschaft fuer Technische Zusammenarbeit (GTZ), GmbH, Eschborn, Alemania, 335 p. [ Links ]
28. Lincon, R., G. Boxshall y P. Clarck. 1998. A dictionary of ecology, evolution and systematics. Cambridge University Press. 361 p. [ Links ]
29. Ordoñez, M. 2005. Variación en la estructura de la comunidad de corales hermatípicos juveniles entre arrecifes continentales (Isla Grande e Isla Fuerte) y oceánicos (San Andrés y Providencia) del Caribe colombiano. Tesis Biol., Univ. Javeriana, Bogotá, Colombia, 150 p. [ Links ]
30. Pizarro, V. 2002. Dinámica poblacional de corales cerebro (Scleractinia: Faviidae) en la Isla de San Andrés, Caribe suroccidental: una aproximación. Tesis M.Sc. Biol. Mar., Univ. Nacional, Bogotá, Colombia 65 p. [ Links ]
31. Porter, J.W. y J.I. Tougas. 2001. Reef ecosystems: threats to their biodiversity. Encyclopedia of Biodiversity. 5: 73-95. [ Links ]
32. Reyes, J. 2000. Lista de los corales (Cnidaria: Anthozoa: Scleractinia) de Colombia. Biota Colombiana, 1 (2): 164-175. [ Links ]
33. Richmond, R.H. y C. Hunter, 1990. Reproduction and recruitment of corals: comparisons among the Caribbean, the tropical Pacific and the Red Sea. Mar. Ecol. Prog. Ser., 60: 185-203. [ Links ]
34. Rodríguez-Ramírez, A., C. Zambrano y J. Garzón-Ferreira. 2004. Status and recent dynamics (1998-2003) of the coral reefs of Colombia. Abstracts 10th Int. Coral Reef Symp., 410 . [ Links ]
35. Rylaarsdam, K.W. 1983. Life histories and abunfance patterns of colonial corals on Jamaican reefs. Mar. Ecol. Prog. Ser., 13: 249-260. [ Links ]
36. Sammarco, P.W. 1991. Geographically specific recruitment and postsettlement mortality as influences on coral communities: The cross-continental shelf experiment. Limnol. Oceanogr., 36: 496-514. [ Links ]
37. Sepúlveda, M. y A. Acosta. 2005. Distribución vertical, composición, riqueza y densidad de corales hermatípicos juveniles en el arrecife de Isla Fuerte, Caribe colombiano. Res. XI Congr. Latinoam. Cien. Mar. Chile. 365-366. [ Links ]
38. Torres, J.L. y J. Morelock. 2002. Effect of terrigenous sediment influx on coral cover and linear extension rates of three caribbean massive coral species. Carib. J. Sci., 38 (3,4): 222-229. [ Links ]
39. Vidal, A.M. 2005. Distribución vertical, composición, riqueza y densidad de corales hermatípicos juveniles en San Andrés Isla, Caribe colombiano. Tesis Biol., Univ. Javeriana, Bogotá, Colombia, 102 p. [ Links ]
40. Wittemberg, M. y W. Hunte. 1991. Effects of eutrophication and sedimentation on juvenile corals: abundance, mortality and community structure. Mar. Biol., 112: 131-138. [ Links ]













