Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Boletín de Investigaciones Marinas y Costeras - INVEMAR
Print version ISSN 0122-9761
Bol. Invest. Mar. Cost. vol.35 no.1 Santa Marta Jan./Dec. 2006
RACIÓN DIARIA Y CONSUMO DE ALIMENTO DE LA POBLACIÓN DE ANCHOVIA CLUPEOIDES (PISCES: ENGRAULIDAE) EN LA CIÉNAGA GRANDE DE SANTA MARTA, CARIBE COLOMBIANO
DAILY RATION AND FOOD CONSUMPTION OF THE POPULATION OF ANCHOVIA CLUPEOIDES (PISCES: ENGRAULIDAE) IN THE CIÉNAGA GRANDE DE SANTA MARTA, COLOMBIAN CARIBBEAN
Guillermo Duque1 y Arturo Acero P.2
1Universidad Nacional de Colombia, sede Palmira. Facultad de Ingeniería y Administración. Carrera 32 Chapinero, Palmira, Colombia. gduquen@palmira.unal.edu.co
2Universidad Nacional de Colombia, Departamento de Biología, CECIMAR/INVEMAR, Cerro Punta Betín, Santa Marta, Colombia. E-mail: aacero@invemar.org.co
RESUMEN
En estuarios tropicales, la mayoría de peces se alimentan a diferentes horas durante el ciclo diario. Con el objeto de determinar la ración diaria y consumo de la población de Anchovia clupeoides en la Ciénaga Grande de Santa Marta (CGSM),se realizaron muestreos mensuales en un ciclo de 24 h entre octubre de 1995 y junio de 1996. A partir de un total de 4389 individuos, se estimó que la población de A. clupeoides consume casi dos veces su biomasa al año, representando un 0.53% del peso de su cuerpo al día. Aunque la CGSM presenta una alta producción primaria (990 gC/m2/año) el porcentaje que se transfiere a la población de A. clupeoides es relativamente bajo (0.055%). Bajo este contexto, es probable que a pesar de que la CGSM presenta alta productividad, poca de esta está siendo realmente transferida a niveles tróficos superiores, debido a la calidad del fitoplancton que radica principalmente en cianobacterias.
PALABRAS CLAVE: Ecología trófica, Engráulidos, Estuarios, Caribe sur.
ABSTRACT
In tropical estuaries, most fishes feed at different hours during the day. To determine the daily ration and consumption of the Ciénaga Grande de Santa Marta (CGSM) population of Anchovia clupeoides monthly samplings of a 24 h cycle were taken at the coastal lagoon between October 1995 and June 1996. A total of 4389 specimens were examined. The population of A. clupeoides consumes almost twice its weight per year, representing a 0.53% of its body weight per day. Though the CGSM presents a high primary production (990 gC/m2/year), the percentage that is transferred to the population of A. clupeoides is relatively low (0.055%). Hence, it seems that the high productivity of the CGSM is not being transferred to upper trophic levels due to the kind of fitoplankton, mainly cianobacteria.
KEY WORDS: Trophic ecology, Engraulids, Estuaries, Southern Caribbean.
INTRODUCCIÓN
En general los estuarios son ecosistemas de alta producción primaria (200-400 gC/m2/año), pero de baja eficiencia, es decir, que no todo lo que producen es consumido por los mismos elementos estructurales del sistema (Nixon, 1982). La Ciénaga Grande de Santa Marta (CGSM), es la laguna costera con características estuarinas más grande e importante de Colombia con una alta producción primaria de 990 gC/m2/año (Hernández y Gocke, 1989) y con una producción pesquera promedio de 5623 ± 1730 ton/año, entre el 2000 y 2004 (Blanco et al., 2005). En la actualidad este ecosistema está siendo objeto de atención y existen grandes esfuerzos para su ordenamiento y manejo (Restrepo et al., 2005). En la CGSM, los peces de la familia Engraulidae son relativamente abundantes y tienen gran importancia ecológica porque sirven como alimento de varias especies de peces comerciales (Castaño, 1989; Duque et al., 1996), que en este sistema han experimentado un notable decrecimiento en el tamaño de sus poblaciones (Santos-Martínez, 1989).
Para comprender las relaciones tróficas de una especie es necesario identificar individualmente los principales componentes del sistema, así como los vínculos alimentarios efectivos y en la medida de lo posible, se debe estimar el orden de magnitud de las biomasas y transferencias de energía, con la idea de emplear una parte de la red trófica como base de hipótesis y de experimentación (Caddy y Sharp, 1988), para definir los procesos de control trófico (top-down y bottom-up) y eficiencias de transferencia de energía. Debido a esto, es importante estimar la ración diaria de consumo de alimento de la especie en estudio (Godin, 1981). Sainsbury (1986), sugirió un método para estimar la ración diaria derivada de un grupo de parámetros que incluyen las tasas de ingestión y evacuación, y el inicio y el final del período de alimentación derivado de un ciclo de alimentación de longitud arbitraria. Posteriormente, Jarre (1990) estandarizó el período de alimentación para un ciclo de 24 h. Sainsbury (1986) presentó dos modelos: el modelo I asume una tasa de ingestión constante en el tiempo y en el modelo II una tasa de ingestión inversamente proporcional al contenido estomacal. Este último modelo requiere de la estimación de un parámetro adicional, el "contenido estomacal asintótico". Ambos modelos asumen una evacuación exponencial simple. Las estimaciones de consumo del alimento (Q) basadas en la población pueden ser obtenidas de uno o varios estimados de la ración diaria y los parámetros de crecimiento y mortalidad. La aproximación usada en el programa MAXIMS (Jarre et al., 1990), se basa en la ecuación de crecimiento de von Bertalanffy y en el coeficiente de mortalidad total que son documentados en Pauly (1986) y Palomares y Pauly (1989).
En la presente investigación se cuantificó la ración diaria y el consumo de la población de A. clupeoides en la CGSM como medida del efecto entre el recurso planctónico y el siguiente nivel consumidor. Esta especie es intermediaria entre la producción en la columna de agua y los peces ictiófagos, fuente frecuente de alimento para el hombre.
ÁREA DE ESTUDIO
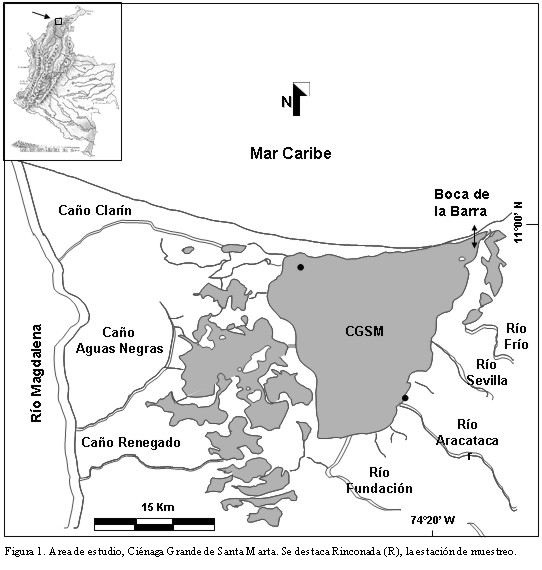
El sistema lagunar estuarino conocido como la Ciénaga Grande de Santa Marta (CGSM) es parte del delta exterior del Río Magdalena y está localizado entre los 10o 43' y 11o 00' N y entre los 74o 15' y 74o 32' O sobre la costa Caribe (Figura 1). El sistema lagunar limita al oriente y al sur-oriente con las estribaciones bajas de la Sierra Nevada de Santa Marta (SNSM) que se eleva hasta 5800 m sobre el nivel del mar y de donde provienen los tres ríos principales que desembocan en la CGSM. Por el norte está separada del Mar Caribe por una barra continental conocida como Isla de Salamanca, la cual presenta una boca artificial en la parte nororiental (Boca de la Barra) de aproximadamente 100 m de ancho, la cual es la única conexión de la Ciénaga con el mar. Finalmente, por el occidente y sur-occidente limita con el plano lodoso del Río Magdalena (Cosel, 1986; Botero, 1988; Botero y Mancera-Pineda, 1996). La CGSM tiene una extensión de 450 km² y una profundidad promedio de 1.5 m (IGAC, 1973) e históricamente ha sido la principal fuente de recursos pesqueros de la costa norte de Colombia (Santos-Martínez y Acero, 1991).
MATERIALES Y METODOS
Diseño de muestreo
Entre octubre de 1995 y junio de 1996 se efectuó un muestreo mensual en la CGSM, en puntos aleatorios del cuerpo principal de agua de la CGSM. Cada mes, se hicieron ocho faenas de pesca, una cada 3 h, en un ciclo de 24 h. Los individuos de A. clupeoides fueron capturados con una red de cerco de monofilamento de nylon de 150 m de largo por 2 m de alto, con secciones de ojos de malla de 5.40 cm (50 m), 3.81 cm (50 m) y 2.54 cm (50 m) aplicando el método de bolicheo según Rueda y Mancera-Pineda (1995). Los peces capturados a una misma hora fueron separados por clases de talla de 0.5 cm y se determinó el peso total y la frecuencia de los individuos en cada clase de
talla. Posteriormente, se extrajo el estómago de cada individuo para obtener el contenido estomacal, el cual se secó a 100 oC en una estufa y se determinó su peso (Duque y Acero 2003a). Así mismo, para establecer la biomasa de los grupos planctónicos en el área de pesca, se colectaron muestras de plancton mediante una bomba de succión Rule 1000 conectada a una batería de 12 voltios haciendo fluir 80 l de agua en tamices de 250, 125 y 63 µm. Las fracciones retenidas se secaron a 100 oC en una estufa y se determinó su peso seco (Duque y Acero 2003b).
Análisis de la información
Se utilizó el sofware MAXIMS, elaborado por Jarre et al. (1990), para estimar la ración diaria de A. clupeoides, con base en los datos de contenidos estomacales en el ciclo de 24 h. Las rutinas del MAXIMS están implementadas para uno o dos períodos de alimentación por día. Se utilizó el modelo (I) que asume una evacuación exponencial simple y una tasa de ingestión constante durante el período de alimentación. Se escogieron tasas constantes debido a que no se hicieron corroboraciones experimentales para definir la ingestión y la evacuación. De acuerdo con lo anterior, en el presente trabajo se utilizaron los modelos 1 (un período alimentario al día y tasa de ingestión constante), y 2 (dos períodos alimentarios al día y tasa de ingestión constante). A partir de los valores obtenidos de contenido estomacal a lo largo del día, se estimaron las tasas de ingestión y evacuación y el período de alimentación. Así mismo, se ajustó un algoritmo no lineal para modelar el contenido estomacal en el tiempo minimizando la suma de cuadrados residuales. Hay que tener en cuenta que la decisión de uno o dos periodos de alimentación al día se basa en el peso seco del contenido estomacal obtenido de todos los individuos capturados en cada una de las horas del mes correspondiente. El cálculo de estos parámetros se realiza de acuerdo con las ecuaciones que se explicarán a continuación:
La trayectoria del tiempo de una evacuación exponencial simple es la solución a la ecuación diferencial:
ds/dt = - E * S
Que es:
S = S0 * exp (-E * (t-t0))
Donde:
t = Tiempo
S = Contenido estomacal al tiempo t
E = Tasa de evacuación instantánea en hora-1
S0 = Contenido estomacal al comienzo del período dado
t0 = Tiempo al comienzo del período en cuestión
Como el contenido estomacal es continuamente evacuado, este proceso ha sido también tomado en consideración durante el periodo de alimentación. Por esta razón, a la cantidad del alimento ingerido se le ha restado la cantidad de alimento evacuado así:
ds/dt = J1 - E * S
Cuya solución es:
S = (Sr * exp (-E * (t-t0))) + (J1 / E * (1 - exp (-E * (t-t0)))
Donde:
J1 = Tasa de ingestión en biomasa * hora-1
Sr = Contenido estomacal al comienzo del período de alimentación
El primer sumando representa evacuación del contenido estomacal antes de un período de alimentación dado y el segundo agrega la ingestión y evacuación del nuevo alimento ingerido. Durante el período de alimentación, el contenido estomacal se incrementa de Sr hacia la asíntota J1/E. Finalmente la ración diaria es definida como la integral de la trayectoria en el tiempo del contenido estomacal sobre el período de alimentación.
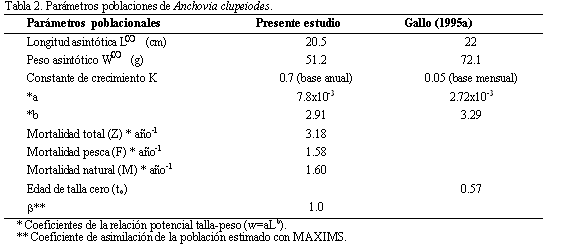
Para estimar el consumo de alimento de la población (Q/B), se utilizó el sofware MAXIMS, el cual requiere una o varias estimaciones de la ración diaria para pesos específicos y los parámetros de crecimiento y mortalidad de la población (Jarre et al., 1990). Los parámetros poblacionales se estimaron de acuerdo con la función de crecimiento de von Bertalanffy (VBGF), usando la aproximación de longitudes medias y de frecuencias de talla usando el programa FISAT (Gayanillo et al., 1993), y se ajustaron de acuerdo con los parámetros obtenidos para esta especie en la CGSM por Gallo-Nieto (1995a).
Con el MAXIMS se realizó la estimación del consumo de alimento de la población (Q/B = consumo de alimento/ biomasa de la población) así:
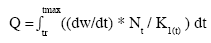 (ecuación 1)
(ecuación 1)
Donde:
tr = Edad de entrada a la población en cuestión
tmax = Edad de salida de esa población
Nt = Tamaño de la población en el tiempo t
K1(t) = Eficiencia bruta de conversión de alimento al tiempo t
Así mismo, la biomasa (B) de la población se obtuvo como la integral sobre el tiempo de las frecuencias de pesos determinados (Gayanillo et al., 1993), así:
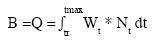 (ecuación 2)
(ecuación 2)
Donde: Wt = Peso a la edad t
Entonces, el consumo de la población (Q/B) es:
Q/B = Ecuación 1/ ecuación 2
La ración diaria (Rd) peso específica se calculó con base en valores promedios de peso para cada clase de talla, de acuerdo con la siguiente ecuación:
Rd = 3 * (K/365) * W * ((W∞ / W) 1/b - 1) / 1 - (W / W∞)ß
El coeficiente beta (ß) se calculó directamente de pares de datos de peso promedio del pez y su Rd de acuerdo con la siguiente ecuación:
dw/dt = 3 * (K/365) * W * ((W∞ / W) 1/b - 1)
donde,
K1 = (dW /dt) / Rd
ß = log (1-K1) / log (W/ W∞)
Finalmente, con los datos de ración diaria (Rdp) y los estimativos del tamaño de la población virtual por clase de tallas (estimado de las capturas por medio del análisis de poblaciones virtuales, basado en la estructura de las longitudes mediante FISAT), se calculó cuanto es el consumo diario total de la población en mg/día. Este valor se estandarizó a g/m2/año dividiendo por el área de la CGSM que es de 450 x 106 m2 según IGAC (1973) y multiplicando por 365 días. Finalmente este valor de consumo de la población en g/m2/año se transformó en g C/m2/año asumiendo que el carbono es el 35% del peso seco del zooplancton (Parsons et al., 1984) que constituye el alimento principal de la especie en estudio (Duque, 1997).
RESULTADOS
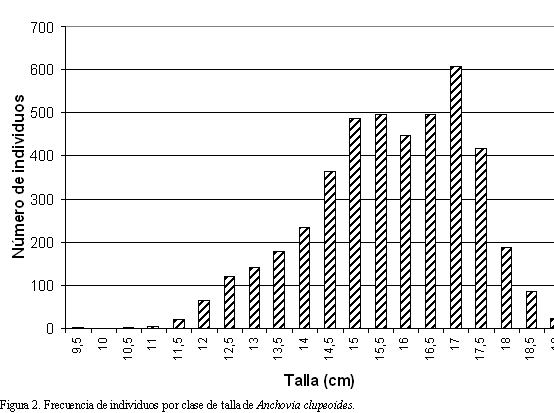
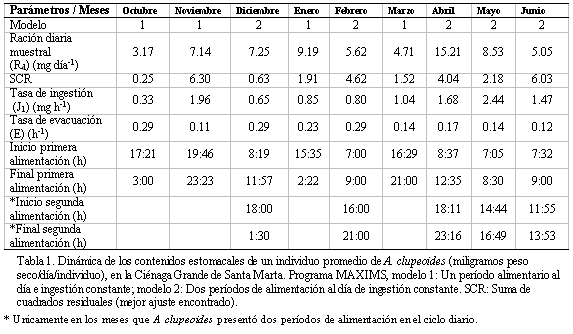
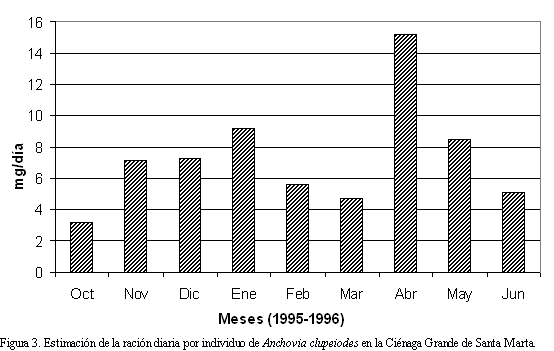
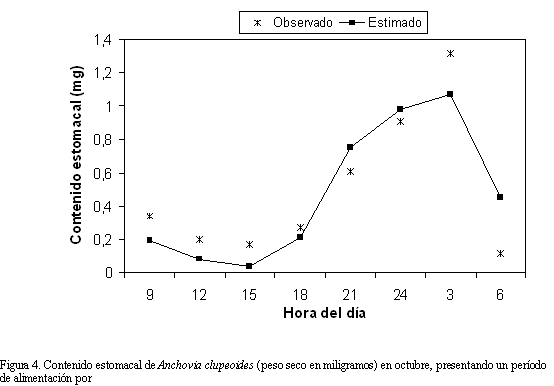
En los nueve meses de muestreo fueron colectados y analizados un total de 4389 individuos de A. clupeoides, obteniéndose las mayores capturas en diciembre y mayo y la menor en octubre. La totalidad de los individuos se encontró entre 9.5 y 19.5 cm de longitud total con una mayor frecuencia (602 individuos) en los 17 cm (Figura 2). En cinco de los nueve meses de muestreo los individuos de A. clupeoides presentaron dos períodos de alimentación en el ciclo diario (Tabla 1), entre ellos abril (alta salinidad y temperatura), mes donde se registró la mayor ración diaria por individuo (Figura 3). Sin embargo, la mayor tasa de ingestión no se presentó en abril sino en mayo (Tabla 1). Cuando se presentó un solo período de alimentación al día (Figura 4), este ocurrió entre el atardecer y la media
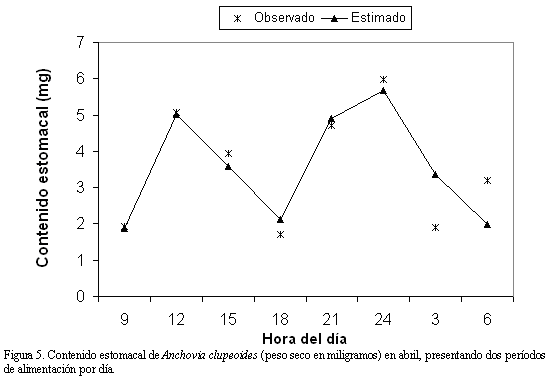
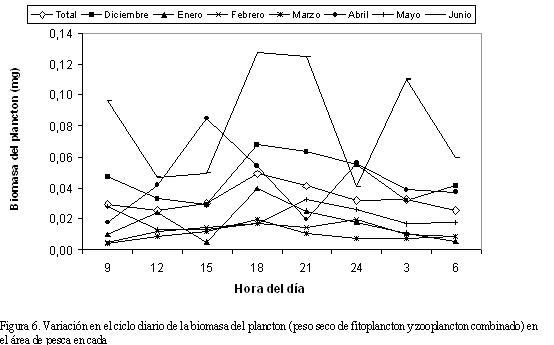
noche o la madrugada. Cuando hubo dos períodos de alimentación al día (Figura 5), existió uno corto adicional en las horas de la mañana, a veces, extendido hasta el medio día. En general no se observó ningún patrón definido entre los periodos de alimentación al día (modelos 1 y 2.1) y las tasas de consumo con el plancton disponible en el área de pesca, ya que aunque en la mayoría de meses el plancton disponible presentó un pico en biomasa alrededor de las 6 de la tarde, en algunos meses ocurrió a diferente hora (Figura 6).
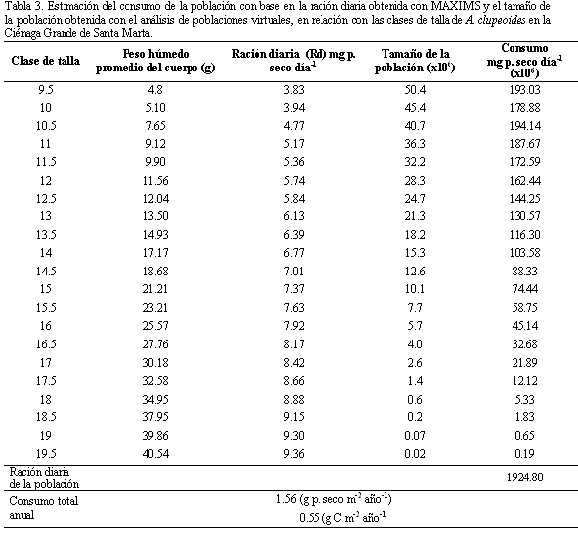
En la Tabla 2 se presentan los parámetros poblacionales calculados por medio del programa FISAT y el ß que es un parámetro que se refiere a la asimilación del alimento por la población en estudio (calculado por MAXIMS), necesarios para la obtención de la ración diaria de cada intervalo de talla de la población (Jarre et al., 1990; Pauly, 1986). Con estos parámetros por medio del MAXIMS se estimaron los valores del Q/B que indicaron que la población consumió 1.96 veces su propio peso por año y que diariamente consumió el 0.53% del peso de su cuerpo. El consumo de la población estimado a partir de la ración diaria (Rdp) multiplicado por el tamaño virtual de la población en g/m2/año y gC/m2/año se presenta en la Tabla 3. En general, a medida que A. clupeoides crece, la ración diaria de consumo de alimento aumenta. Sin embargo, el consumo de la población disminuye, ya que el tamaño de la población también disminuye a medida que crecen los individuos (Tabla 3). Aunque la CGSM presenta una alta producción primaria (990 gC/m2/año) el porcentaje que se transfiere a la población de A. clupeoides es relativamente bajo (0.055% = (0.55 g C m-2 año-1 / 990 g C m-2 año-1)*100%).
DISCUSIÓN
Una de las principales características que presentan los peces es la de aumentar el consumo de alimento en la época previa a la maduración gonadal, con el objetivo de suplir esta necesidad energética, lo cual se denomina interacción alimentación-reproducción (Luquet y Watanabe, datos sin publicar). Según Caselles y Acero (1996) y Gallo-Nieto (1995b), aunque en la CGSM A. clupeoides desova prácticamente durante todo el año, presenta un pico principal en agosto-septiembre y justo 4-5 meses antes (abril) la maduración gonadal de esta especie es la más baja. De acuerdo con lo anterior, el inicio de la madurez gonadal concuerda con la época de mayor consumo de alimento encontrado en el presente trabajo (abril). Según Pakhomov y Tseytlin (1992), las raciones diarias de los peces planctófagos de la Antártida aumentan aproximadamente un 30% en la época reproductiva. Lo anterior concuerda con lo encontrado para A. clupeoides. Sin embargo, A. clupeoides posiblemente incrementa su gasto energético debido al aumento en el tiempo diario de alimentación.
Según Leong y O'Connell (1969), para desarrollar una hipótesis concerniente a la capacidad de los peces para obtener sus requerimientos nutricionales del plancton, es necesario el conocimiento de la tasa de ingestión que presentan. En el caso de A. clupeoides de la CGSM, los meses con mayor tasa de ingestión (noviembre y mayo) no fueron los meses con mayor ración diaria (enero y abril). Debido a lo anterior, es posible que no siempre un aumento en la tasa de ingestión refleje un aumento en la ración diaria, debido a que se debe tener en cuenta también la disponibilidad del alimento y el tiempo de alimentación (p.e. dos períodos de alimentación o uno de mayor duración). Así mismo, hay que considerar la calidad del alimento, ya que una amplia oferta alimenticia, que no proporcione los requerimientos nutricionales, no genera ni una alta ración diaria, ni una tasa de ingestión alta. Este fenómeno se encuentra demostrado a nivel de zooplancton (Greame et al., 1998).
Al expresar en porcentaje la división del consumo anual de la población de A. clupeoides (0.55 gC/m2/año) por el valor de la producción primaria de la CGSM, calculada en 990 gC/m2/año según Hernández y Gocke (1989), se obtuvo que la eficiencia de transferencia de la producción primaria a la población de A. clupeoides fue de 0.055%, teniendo en cuenta que entre el fitoplancton y esta especie existen al menos dos niveles tróficos intermedios, como lo son el zooplancton herbívoro y el carnívoro. Esta baja eficiencia de transferencia estimada sugiere que posiblemente la relación entre estos dos niveles tróficos depende en gran parte de las relaciones tróficas entre el fitoplancton y el zooplancton y/o que el abundante fitoplancton no es eficientemente utilizado por los niveles tróficos superiores debido a su pequeño tamaño y a la gran proporción de cianófitas en algunas épocas, como lo registran Mancera y Vidal (1994). Esta información de baja energía de transferencia entre larváceos herbívoros, copépodos herbívoros y fitoplancton, se encuentra documentada para aguas costeras del Caribe centro, lo cual corrobora lo encontrado en el presente estudio (Rodríguez et al., 2005; Franco-Herrera, 2001). Bajo este contexto, es probable que a pesar de que la CGSM presenta alta productividad, poca de esta está siendo realmente transferida a niveles tróficos superiores, debido a la calidad del fitoplancton que radica principalmente en cianófitas.
AGRADECIMIENTOS
Se agradece el apoyo institucional y económico de la Universidad Nacional de Colombia (UNC), el Instituto de Investigaciones Marinas y Costeras (INVEMAR) y el Instituto Colombiano para el Desarrollo de la Ciencia y la Tecnología (COLCIENCIAS). Agradecimientos especiales a los profesores de la UNC, Sven Zea y Néstor Campos por su valiosa colaboración.
BIBLIOGRAFÍA
1. Blanco, J., J.C. Narváez, M. Rueda, E. Viloria, F. Newmark, M. Santos, J.A. Angulo y N. Madrid. 2005. Estado de los recursos sometidos a explotación en Colombia. Informe del estado de los ambientes marinos y costeros en Colombia: año 2004. INVEMAR, Serie de publicaciones periódicas, 8: 189-213. [ Links ]
2. Botero, L. 1988. Caracterización ecológica de la Ciénaga Grande de Santa Marta, una laguna costera tropical en la costa Caribe de Colombia: 1-47. En: L. Botero. (ed). Estudio ecológico de la Ciénaga Grande de Santa Marta. Informe final, Proyec. COLCIENCIAS-INVEMAR. CO. 215-09-029-85. Instituto Investigaciones Marinas Punta de Betín, Santa Marta. [ Links ]
3. Botero, L. y J.E. Mancera-Pineda. 1996. Síntesis de los cambios de origen antrópico ocurridos en los últimos 40 años en la Ciénaga Grande de Santa Marta (Colombia). Rev. Acad. Col. Cien., 20(78): 465-474. [ Links ]
4. Caddy J.E. y G.D. Sharp. 1988. Un marco ecológico para la investigación pesquera. FAO Documento Técnico Pesca 283., 155 p. [ Links ]
5 Caselles, A. y A. Acero P. 1996. Reproducción de Anchovia clupeiodes y Anchovia parva (Pisces: Engraulidae) en dos ciénagas del Caribe colombiano. Rev. Biol. Trop., 44(2): 781-793. [ Links ]
6. Castaño, T.L. 1989. Hábitos alimentarios de peces de la Ciénaga Grande de Santa Marta, Caribe colombiano. Tesis profesional, Biología, Pontificia Universidad Javeriana, Bogotá. 81 p. [ Links ]
7. Cosel, R.v. 1986. Moluscos de la región de la Ciénaga Grande de Santa Marta. An. Inst. Inv. Mar. Punta de Betín, 15-16: 79-370. [ Links ]
8. Duque, G. 1997. Hábitos alimentarios y relaciones tróficas de Anchovia clupeoides (Pisces: Engraulidae) en la Ciénaga Grande de Santa Marta, Caribe Colombiano. Tesis M. Sc. Universidad Nacional de Colombia, Bogotá. 89 p. [ Links ]
9. Duque, G., A. Acero P., A. Santos-Martínez y E. Rubio. 1996. Food habits of Oligoplites species in the Ciénaga Grande de Santa Marta, Colombian Caribbean. Cybium, 20(3): 251-260. [ Links ]
10. Duque, G., y A. Acero P. 2003a. Food habits of Anchovia clupeoides in the Ciénaga Grande de Santa Marta, Colombian Caribbean. Gulf of Mexico. Science, 21: 1-9. [ Links ]
11. Duque, G., y A. Acero P. 2003b. Selectivity of Anchovia clupeoides in the Ciénaga Grande de Santa Marta, Colombian Caribbean. Gulf and Caribbean Research, 15: 21:26. [ Links ]
12. Franco-Herrera, A. 2001. Estrategias de ingestión y flujo de carbono entre fitoplancton, seston total y Eucalanus spp (Copepoda: Calanoidea) en dos ambientes oceanográficos del Caribe central Colombiano. Informe final. Dirección de Investigaciones, Universidad de Bogotá Jorge Tadeo Lozano. 67 pp. [ Links ]
13. Gallo-Nieto, J. 1995a. Edad y crecimiento de la anchoveta Anchovia clupeoides (Pisces: Engraulidae) en la Ciénaga Grande de Santa Marta (Colombia). Boletín Científico INPA, 3: 135-144. [ Links ]
14. Gallo-Nieto, J. 1995b. Aspectos reproductivos y factor de condición de la anchoveta Anchovia clupeoides (Pisces: Engraulidae) en la Ciénaga Grande de Santa Marta (Colombia). Boletín Científico INPA 3: 145-154. [ Links ]
15. Gayanillo, F.C., P. Sparre y D. Pauly. 1993. The FISAT user's guide. FAO-ICLARM Stock assessment tools. FAO Comput. Inf. Ser. Fish., 99, Roma. [ Links ]
16. Godin, J.G.J. 1981. Daily patterns of feeding behavior, daily rations, and diets of juvenile pink salmon (Oncorhynchus gorbusha) in two marine bays of British Columbia. Can. J. Fish. Aquat. Sci., 38: 10-15. [ Links ]
17. Graeme, C.H., P.I. Webb y S.L. Frears. 1998. Diet changes in the carbon and nitrogen content of the copepod Metridia lucens. J. Plankton Res., 20: 727-737. [ Links ]
18. Hernández, C.A. y K. Gocke. 1989. Productividad primaria en la Ciénaga Grande de Santa Marta, Colombia. An. Inst. Inv. Mar. Punta de Betín, 19-20: 101-119. [ Links ]
19. IGAC. 1973. Monografía del departamento del Magdalena. Instituto Geográfico Agustín Codazzi, Bogotá, 163 p. [ Links ]
20. Jarre, A. 1990. Estimating the food consumption of fishes: One step in linking a species with its ecosystem. Naga, 13(2): 3-4. [ Links ]
21. Jarre, A., M.L. Palomares, M.L. Soriano, V.C. Sambilay, Jr. y D. Pauly. 1990. A user's manual for Maxims. A computer program for estimating the food comsuption of fishes from diel stomach contents data and population parameters. Software 4 ICLARM, Manila, 27 p. [ Links ]
22. Leong, R.J.H. y C.P. O'Connell. 1969. A laboratory study of particulate and filter feeding of the northern anchovy (Engraulis mordax). Journal Fisheries Research Board Canada, 26: 557-582. [ Links ]
23. Luquet, P. y T. Watanabe. Datos sin publicar. Interaction "Nutrition-Reproduction" in fish. Station d'Hydrobiol., INRA, Ascain, Francia: 22 p. [ Links ]
24. Mancera, J.E. y L.A. Vidal. 1994. Florecimiento de microalgas relacionado con mortandad masiva de peces en el complejo lagunar Ciénaga Grande de Santa Marta, Caribe colombiano. An. Inst. Inv. Mar. Punta de Betín, 23: 103-117. [ Links ]
25. Nixon, S.W. 1982. Nutrient dynamics, primary production and fisheries yields of lagoons. Acta Oceanologica Número Especial: 357-371. [ Links ]
26. Pakhomov, Y.A. y V.B. Tseytlin. 1992. Diet of seven species of Antarctic fishes and estimation of their daily rations. Vosprosy Ikhtiologii, 32(1): 138-146. [ Links ]
27. Palomares, M. L. y D. Pauly. 1989. A multiple regression model for predicting the food consumption of marine fish populations. Aust. J. Mar. Freshw. Res., 40: 259-273. [ Links ]
28. Parsons, T. R., M. Takahashi y B. Hargrave. 1984. Biological oceanographic processes. Tercera edición. Pergamon Press, Oxford. 330 p. [ Links ]
29. Pauly, D. 1986. A simple method for estimating the food consumption of fish populations from growth data and food conversion experiments. Fishery Bulletin, 84(4): 827-840. [ Links ]
30. Rodríguez, D., López, C. y A. Franco-Herrera. 2005. Impacto de pastoreo por los géneros Oikopleura spp y Eucalanus spp, en la Ensenada de Gaira, Caribe colombiano. Actualidad y Divulgación Científica, 8 (1): 57-68. [ Links ]
31. Restrepo, J., R. Espinoza, M. Copete, T.R. Ruiz, M. Arroyo, G. Calderón, G. Duque. 2005. Estado de los estuarios y manglares en Colombia: año 2004. INVEMAR, Serie de publicaciones periódicas, 8: 129-150. [ Links ]
32. Rueda, M. y J.E. Mancera-Pineda. 1995. Alteraciones fisico-químicas de la columna de agua, generadas por el uso del boliche (método de pesca artesanal) en la Ciénaga Grande de Santa Marta, Caribe colombiano. An. Inst. Inv. Mar. Punta de Betín, 24: 23-27. [ Links ]
33. Sainsbury, K. 1986. Estimation of food consumption from field observations of fish feeding cycles. J. Fish. Biol., 29: 23-36. [ Links ]
34. Santos-Martínez, A. 1989. Estudio biológico y ecológico de la ictiofauna de la Ciénaga Grande de Santa Marta, Caribe Colombiano. Tesis M. Sc. Universidad Nacional de Colombia, Bogotá. 178 p. [ Links ]
35. Santos-Martínez, A. Y A. Acero P. 1991. Fish community of the Ciénaga Grande de Santa Marta (Colombia): Composition and zoogeography. Ichthyological Exploration Freshwaters, 2(3): 247-263. [ Links ]
FECHA DE RECEPCIÓN: 31/08/05 FECHA DE ACEPTACIÓN: 25/10/06