Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Boletín de Investigaciones Marinas y Costeras - INVEMAR
Print version ISSN 0122-9761
Bol. Invest. Mar. Cost. vol.37 no.1 Santa Marta Jan./June 2008
ESTRUCTURA Y COMPOSICIÓN DE LAS COMUNIDADES DE GORGONIAS DE LOS ARRECIFES DEL ARCHIPIÉLAGO SABANA-CAMAGÜEY, CUBA: CONECTIVIDAD Y FACTORES DETERMINANTES
COMPOSITION AND STRUCTURE OF GORGONIAN COMMUNITIES OF CORAL REEFS IN THE SABANA-CAMAGÜEY ARCHIPELAGO, CUBA: CONNECTIVITY AND DETERMINANT FACTORS.
Pedro M. Alcolado1, Pedro García-Parrado2 y Darlenys Hernández-Muñoz1
1Instituto de Oceanología, Ave 1ª No. 18406, Reparto Flores, Playa, La Habana, C.P. 12100, Cuba. alcolado@ama.cu (P.M.A); biologiam@ama.cu (D.H.M).
211 Hunter Rd, Mod 1 Box 4, Pennfield, NB, E5H 1X1, Canadá. parrado@hotmail.com.
RESUMEN
Para conocer la composición y estructura de las comunidades de gorgonias de los arrecifes coralinos del Archipiélago Sabana-Camagüey (norte central de Cuba) y los factores que las gobiernan, se realizaron muestreos de estaciones en 10 transecciones de arrecife que incluyen la zona trasera (cerca de 1 m de profundidad) y la zona del arrecife frontal (entre 5 y 20 m de profundidad). La especie más predominante y frecuente fue Pseudopterogorgia americana, seguida por Eunicea flexuosa, Eunicea mammosa, Plexaurella dichotoma y Plexaura kuekenthali. La primera es típica de fondos rocosos con acumulación de sedimentos, y las demás son consideradas como resistentes a la turbulencia del agua, excepto la última. Según el análisis BIOENV la turbulencia del agua fue el único factor directo que explicó de manera significativa la composición y estructura de las comunidades de gorgonias. El ordenamiento de las estaciones revela una fuerte conectividad dentro del área de estudio. Los índices de diversidad H’ y J’ sugieren el predominio de condiciones ambientales físicas favorables y casi constantes a constantes para las comunidades de gorgonias.
PALABRAS CLAVE: Comunidades de gorgonias, Octocorales, Arrecifes coralinos, Cuba.
ABSTRACT
To know the gorgonian community composition and structure of coral reefs in the Archipelago Sabana-Camagüey (north central Cuba) and the factors governing them, sampling was carried out in 10 transects, which include the rear zone (about 1 m in depth) and the fore reef zone (between 5 m and 20 m in depth). The most dominant and frequent species was Pseudopterogorgia americana, followed by Eunicea flexuosa, Eunicea mammosa, Plexaurella dichotoma, and Plexaura kuekenthali. The first one is typical of rocky bottoms with accumulated sediments, while the others are considered resistant to water turbulence, except the last one. According the nMDS analysis, water turbulence was the only direct factor that explained in a significant way the gorgonian community composition and structure. Ordination of stations reveals a b connectivity within the study area. Diversity indices H’ and J’suggest the dominance of favorable and quasi constant to constant physical environmental conditions for gorgonian communities.
KEY WORDS: Gorgonian communities, Octocorals, Coral reefs, Cuba.
INTRODUCIÓN
Las gorgonias, por su alta conectividad sistema-ambiente físico (sensu Bradbury, 1977), son recomendables como indicadoras ambientales (Alcolado, 1984; 1992). Por tanto, sus comunidades constituyen modelos útiles para la exploración de los mecanismos abióticos que estructuran comunidades sésiles en el ambiente arrecifal y, según Preston y Preston (1975), para inferir el grado de severidad y constancia (predictibilidad) del ambiente físico.
Desde principios del presente siglo se han hecho investigaciones dirigidas a conocer la influencia de los parámetros abióticos en las especies y comunidades de octocorales (Cary, 1914; 1918). Al cabo de cerca de cinco décadas, con el desarrollo de las tecnologías de buceo, se incrementaron las investigaciones de comunidades de gorgonias en el Caribe, con los trabajos de Goldberg (1973), Kinzie (1973), Opresko (1973), Preston y Preston (1975), Jordán (1979), Alcolado (1981), Muzik (1982), Herrera- Moreno y Alcolado (1983, 1985, 1986a, 1986b), Botero (1987), Yoshioka y Yoshioka (1987, 1989a, 1989b), Jordán-Dahlgren (1989), Herrera-Moreno (1991), Márquez et al. (1997), Sánchez et al. (1997), Herrera et al. (1997) y Yoshioka (1997), entre otros. Estos autores discuten sobre los factores naturales, o conjuntos de éstos, que gobiernan las características de las comunidades de gorgonias en diferentes zonas de arrecifes y áreas geográficas del Gran Caribe (calidad y pendiente del sustrato, iluminación, turbulencia, acumulación y desplazamiento de sedimentos, relieve, entre otros) y contribuyen al conocimiento de los requerimientos ecológicos particulares de las especies.
Alcolado (1981) propone el uso del porcentaje total de colonias de especies resistentes a la agitación del agua como Índice de Tensión Hidrodinámica (ITH). Herrera- Moreno y Alcolado (1983, 1985, 1986a, 1986b) y Herrera-Moreno (1991) investigaron la influencia de la contaminación sobre las comunidades de gorgonias y las sugieren como indicadoras alternativas o complementarias de dicho tensor. Por su parte Jordán-Dahlgren (2002) aborda la conectividad de las comunidades de gorgonias en la costa oriental de México.
El Archipiélago Sabana-Camagüey (ASC), por su gran extensión geográfica a lo largo del norte central de Cuba, alto grado de conservación y diversidad de ambientes arrecifales, ofreció una oportunidad para profundizar, con una amplia red de estaciones, en los factores naturales que gobiernan la composición y estructura de las comunidades de gorgonias, y en la potencialidad de éstas como indicadoras de la severidad y predictibilidad del ambiente físico. El ASC fue declarado Zona Marítima Especialmente Sensible por la Organización Marítima Internacional (OMI) debido a los riesgos de contaminación a causa del intenso tráfico marítimo por el Canal de las Bahamas. Además, es objeto de planes de desarrollo turístico y en éste se extrae más del 20% de la pesca nacional. Por todo esto hay un gran interés conservacionista en la región, por lo que se ejecutó el Proyecto GEF/PNUD CUB/92/G31, que financió la presente investigación.
El objetivo de esta prospección fue establecer por primera vez la composición y estructura de las comunidades de gorgonias al nivel del ASC y obtener las primeras inferencias sobre los factores más importantes que las determinan en este territorio. Igualmente nos proponemos evaluar comparativamente la diversidad biológica (heterogeneidad y equitatividad de especies) de este grupo y determinar el grado de conectividad que presentan esas comunidades a escala local, entre distintas profundidades y a escala del área muestreada del archipiélago.
MATERIALES Y MÉTODOS
Zona de estudio
El ASC se extiende como una franja a lo largo de aproximadamente 465 km en el norte central de Cuba y está formado por alrededor de 2517 cayos. Los manglares están profusamente distribuidos en estos cayos y a lo largo de parte de la costa de la Isla Principal. Todo el contorno externo de la plataforma se encuentra bordeado por alrededor de 500 km de arrecifes frontales y más de 100 km de crestas arrecifales. Más de 100 km de playas se extienden en las costas septentrionales de los cayos que bordean la baja y alargada plataforma marina. Esta última posee grandes extensiones de pastos marinos (más del 50%). Los cayos adyacentes a los arrecifes están prácticamente despoblados, exceptuando algunas áreas con desarrollo turístico de sol y playa y buceo, donde se planifica y ejerce control de sus residuales e impactos costeros (Alcolado et al., 1999).
Muestreo
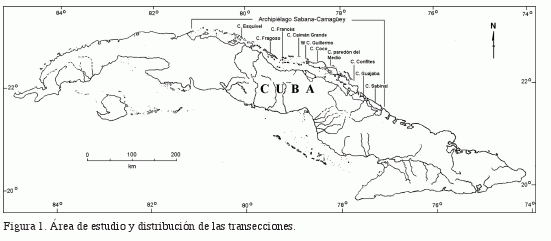
La expedición a los arrecifes del Archipiélago Sabana-Camagüey tuvo lugar del 23 de marzo al 13 de mayo de 1994, a bordo del Buque de Investigaciones Científicas “Ulises”. El muestreo se realizó mediante buceo autónomo, en estaciones distribuidas a lo largo de 10 transecciones perpendiculares al borde de la plataforma marina. Cada transección contó con dos a cuatro estaciones. En total, se muestrearon seis estaciones a 1 m de profundidad (en la zona trasera del arrecife), diez a 5 m, diez a 10 m y nueve a 15-20 m (en el arrecife frontal) (según terminología de Goreau, 1959). Cuando no existía fondo duro a 20 m se optó por muestrear en el escarpe, generalmente extendido entre 12 y 16 m de profundidad (Figura 1; Tabla 1). Las estaciones se representan abreviadamente con una letra mayúscula (desde la A hasta la J) seguida de un número equivalente a su profundidad.
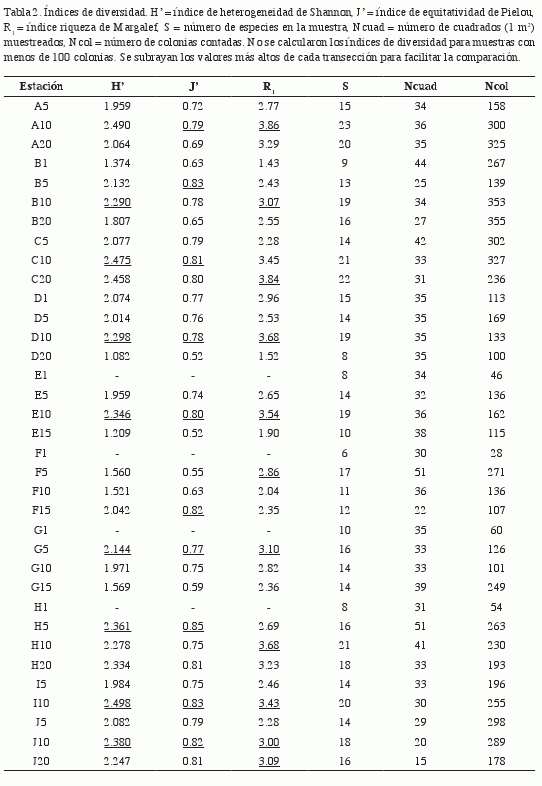
Se aplicó muestreo de tipo acumulativo (Pielou, 1975) con una unidad de muestra delimitada por cuadrado de 1 m2. En cada estación, se contaron las gorgonias dentro de este cuadrado, que se volteaba consecutivamente varias veces, tratando de mantener una variación de profundidad menor de +/- 1 m. En los escarpes se hicieron recorridos zigzagueantes para abarcar sus límites de profundidad. Se evitaron los parches y canales de arena. A juzgar por las tendencias secuenciales de estabilización del índice de heterogeneidad H’ (Shannon, 1948), calculado con respecto al número de cuadrados muestreados, las muestras fueron suficientemente representativas de la estructura de la comunidad (en densidad por especies) y de las especies dominantes y comunes. Sólo en algunos sitios (de zona trasera), que se señalan en la Tabla 2, el número de colonias no fue confiable para el cálculo de H’ pero sí da una representación suficiente de la densidad y de las especies más abundantes y comunes. En el muestreo se trató de que el número de cuadrados fuera mayor que 25, lo que no se logró en dos estaciones, donde sin embargo se obtuvieron buenas cantidades de colonias. El número de cuadrados y el número de colonias, acumulados en las muestras de cada estación, se muestran en la Tabla 2.
Las especies se identificaron y contaron in situ, y las no conocidas se recolectaron e identificaron en el laboratorio a bordo. Cuando las ramas de Briareum asbestinum (Pallas, 1766) estaban fusionadas o muy próximas entre sí formando un grupo se consideraban como de la misma colonia.
Análisis de datos
Para el análisis de la diversidad, se calcularon los índices de heterogeneidad H’ de Shannon (1948), de riqueza de especies R1 de Margalef (1951) y de equitatividad J’ de Pielou (1966), empleando logaritmos neperianos. La clasificación de las comunidades por su composición específica y densidades de las especies se realizó con un análisis de agrupamiento (PRIMER) a partir de las listas de especies con sus respectivas densidades (número total de colonias entre el número total de cuadrados) de cada estación. Se aplicó transformación cuadrática, el índice de disimilitud Bray-Curtis (Bray y Curtis, 1957) y el método de promedio no ponderado de pares de grupos (Field et al., 1982).
También se aplicó el método de ordenamiento escalado multidimensional (nMDS). Para identificar los factores o conjunto de factores que más contribuyen a las diferencias entre las comunidades, se aplicó el análisis BIOENV que da la correlación del ordenamiento de las estaciones por sus comunidades con el de los factores ambientales. La matriz de similitud de factores se obtuvo con distancia euclidiana normalizada y con estandarización. La significancia de la influencia de los factores seleccionados como parte del mejor resultado de BIOENV, fue posteriormente consolidada mediante la rutina RELATE de PRIMER (Prueba de Mantel), considerando como límite de significación 5%.
En el análisis BIOENV se incluyeron las variables: (1) longitud de coordenada geográfica; (2) porcentaje de colonias de gorgonias que son resistentes a la turbulencia del agua, según Kinzie (1973), Alcolado (1981) y Botero (1987), como indicador de esta última variable; (3) biomasa total de algas en peso seco (hasta peso constante) sin descalcificar, en espacio libre de corales, proporcionada por M.C. Beatriz Martínez- Daranas (los valores más altos corresponden a mayor cobertura del sustrato rocoso); (4) relieve, en la escala de puntuación incremental visual que se corresponde con la intensidad de la variable: 1 = pavimento rocoso casi plano, 2 = pavimento rocoso ondulado o con algunos pequeños promontorios bajos; 3 = sistemas de camellones suaves (“spurs and grooves”) con escasa altura (hasta poco más de 1 m) y poca anfractuosidad, 4 = escarpes, camellones bien desarrollados o arrecifes de parche, todos con marcada pendiente y mucha anfractuosidad, y (5) acumulación de sedimentos sobre el fondo en una escala de puntuación del mismo tipo que la anterior: 1 = no se observan sedimentos esparcidos (“rociados”) sobre el fondo, 2 = algún sedimento esparcido sin formar capas, 3 = se ven acumulaciones de sedimentos parcheadas de más de 1 cm de espesor y mucho sedimento esparcido sobre los salientes rocosos, 4 = capa delgada de arena de más de 1 cm de espesor casi continua en grandes extensiones y abundante sedimento esparcido sobre las partes sobresalientes rocosas (Tabla 1).
RESULTADOS
Composición en especies del ASC y especies dominantes y comunes según la profundidad
En el ASC se contaron 6787 colonias pertenecientes a 39 especies. Las especies que más dominaron (más de 4.5% de las colonias contadas) fueron en primer lugar y de manera muy sobresaliente Pseudopterogorgia americana (Gmelin, 1791), seguida por Eunicea flexuosa (Lamouroux, 1821), Eunicea mammosa Lamouroux, 1816, Plexaurella dichotoma (Esper, 1791), Plexaura kuekenthali Moser, 1921 y, en menor grado, Eunicea tourneforti Milne Edwards y Haime, 1857, Briareum asbestinum, Eunicea clavigera Bayer, 1961 y Eunicea calyculata f. coronata Bayer, 1961. Todas estas, excepto P. kuekenthali y E. clavigera, presentaron una alta frecuencia de aparición (> 59%). Aunque con baja dominancia (<4.5%), fueron frecuentes E. calyculata f. typica Bayer, 1961 y Gorgonia ventalina Linnaeus, 1758 (Tabla 3).
A 1 m de profundidad aparecieron con mayor porcentaje E. mammosa, G. flabellum, B. asbestinum, E. tourneforti, E. flexuosa y P. americana. Estas, excepto G. flabellum y P. americana, fueron muy frecuentes. G. ventalina y Muricea muricata (Pallas, 1766) dominaron muy poco a pesar de ser muy frecuentes (Tabla 3). A 5 m de profundidad las gorgonias que más se destacaron, tanto en dominancia como en frecuencia de aparición, fueron P. americana, P. dichotoma (16%), E. mammosa, E. flexuosa y E. tourneforti. Las especies G. ventalina, M. muricata, E. calyculata f. typica y Plexaurella grisea Künze, 1916 fueron frecuentes pero muy poco dominantes (Tabla 3). A 10 m de profundidad tuvieron mayor dominancia y frecuencia de aparición P. americana, seguida, bien por debajo, por un número notable de especies: E. flexuosa, P. dichotoma, E. mammosa, P. kuekenthali, B. asbestinum, E. calyculata f. coronata y E. tourneforti. Las gorgonias E. calyculata f. coronata, E. clavigera, G. ventalina, Muricea pinnata Bayer, 1961, Muriceopsis flavida (Lamarck, 1815), P. grisea y Pseudoplexaura flagellosa Houtuyn, 1772 fueron frecuentes pero pobremente dominantes (Tabla 3).
En los 15-20 m de profundidad aparecieron con mayor dominancia y frecuencia, casi juntas y en primer lugar P. americana y P. kuekenthali, seguidas por E. calyculata f. coronata, E. clavigera, E. flexuosa y B. asbestinum. Las especies E. calyculata f. typica, E. mammosa, M. flavida, G. ventalina y P. flagellosa fueron frecuentes pero muy poco dominantes (Tabla 3).
Diversidad de especies en el ASC y su variación con la profundidad
El número de especies por estación varió de seis a 23. Los valores más altos de H’ (2.458-2.498 natios) se registraron en tres estaciones a 10 m de profundidad frente a los cayos
Esquivel (oeste del archipiélago), Francés (centro) y Guajaba (este), y en Cayo Caimán Grande, a 20 m (Tabla 2). Los menores valores (1.082-1.374 natios) correspondieron a la estación D20 (Cayo Caimán Grande) y a la zona trasera B1 (Cayo Fragoso y Oeste de Cayo Guillermo, respectivamente). En la mayoría de las transecciones se observaron los mayores valores de H’, J’ y R1 a 10 m de profundidad (Tabla 2). Las especies con dominancia muy alta en las estaciones que presentaron baja equitatividad (< 0.69) fueron P. americana (F5, F10, E15, y B20), E. clavigera (G15), G. flabellum (B1), B. asbestinum (B1) y P. kuekenthali (D20).
Ordenamiento de las comunidades
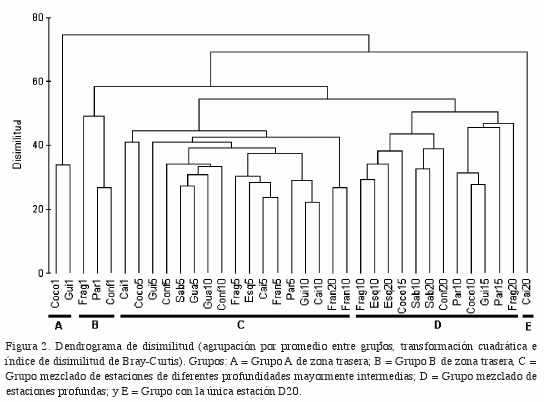
La clasificación de las estaciones mostró una cierta tendencia de separación de las estaciones en más someras, intermedias y más profundas. En los grupos centrales se observa una mezcla de estaciones de profundidades diferentes pero mayormente intermedias, como se explica a continuación. Se produjeron cuatro grupos con más de una estación y uno con una sola: el grupo A con dos estaciones de 1 m (grupo A); B, con tres estaciones 1 m (grupo B); C, con una estación de 1 m, todas las de 5 m, cinco de 10 m y una de 20 m (grupo mezclado de estaciones mayormente de profundidades intermedias); D, con estaciones de 10 m a 20 m (grupo mezclado de estaciones profundas); y E, con sólo la estación D20 (Figura 2).
En el primer eje del análisis nMDS se muestra un ordenamiento de las estaciones también con una tendencia a lo largo de un gradiente de profundidad con las más profundas hacia la derecha y las más someras a la izquierda. Igualmente se observa una tendencia opuesta con relación a la turbulencia generada por el oleaje (Figura 3).
El Análisis BIOENV de correlación entre el ordenamiento de las comunidades (nMDS) y el de los factores considerados señaló a la turbulencia como único factor que explica la composición y estructura de las comunidades (Rho = 0.581). La rutina RELATE dio un Rho = 0.595 y un nivel de significancia de 0.1% para este factor. Particularmente, el aporte del factor de la longitud de coordenadas geográficas fue extremadamente bajo y no significativo (Rho = -0.015; nivel de significancia = 56.8%) lo que coincide con la ausencia de tendencia geográfica observada en la clasificación (Figura 3).
DISCUSIÓN
Especies dominantes y comunes en el ASC
Los octocorales más dominantes fueron especies cuya abundancia está fuertemente determinada por la turbulencia (E. flexuosa, E. mammosa y P. dichotoma, que son resistentes, y P. kuekenthali, poco resistente) y por una especie tolerante a la sedimentación y no mucho a la turbulencia (P. americana), de acuerdo con Kinzie (1973) y Alcolado (1981). Las especies más comunes coinciden con las que registran como tales varios autores en sus respectivas áreas de estudio. Sin embargo, llama la atención la generalizada escasez o ausencia de Pseudopterogorgia bipinnata (Verrill, 1864) y en menor grado de Pseudoterogorgia elisabethae Bayer, 1961 en las estaciones de 15-20 m de profundidad (con excepción de Cayo Fragoso, para ambas especies). La primera especie fue registrada por varios autores (Goldberg, 1973; Kinzie, 1973; Opresko, 1973; Alcolado, 1981) en las profundidades típicas de 10-40 m, así como en áreas bajas (2-4 m) sólo bajo condiciones de efectiva protección del oleaje (zonas traseras de arrecifes y ubicación a sotavento). Por ello, Kinzie (1973) refiere que P. bipinnata está más limitada por el batimiento que por la luz. Goldberg (1973) y Sánchez et al. (1997) también la consideran una especie de aguas tranquilas. La especie P. elisabethae es informada a profundidades de 20-72 m por Kinzie (1973) y de 2.5-4 m (también en lugares muy protegidos a sotavento), así como a 10-30 m por Alcolado (1981).
El grado de exposición tendiente a barlovento de los vientos como generadores de turbulencia (línea perpendicular al borde arrecifal con un ángulo entre 6° y 68° con respecto al ENE que es el vértice del sector de los vientos dominantes) de los arrecifes estudiados explicaría la escasez de ambas especies. De manera parecida, el Este de
la costa (barlovento) de Florida pudiera ser una situación semejante más acentuada, donde Goldberg (1973) sólo encontró escasas colonias de P. elisabethae y ninguna de P. bipinnata.
La estación B20, la única donde ambas especies estaban bien representadas, fue una de las dos con mayor relieve y cubrimiento vivo de corales. P. bipinnata es capaz de tomar ventaja de los fondos de este tipo, ya que por tener plánulas sin zooxantelas son capaces de colonizar oquedades, áreas sombreadas y las partes inferiores de dichos corales, y luego crecer buscando la luz (Kinzie, 1973; Sánchez et al., 1997). Esto es aplicable a P. elisabethae, que también es aposimbiótica (Kinzie, 1974). En dicha estación se obtuvo un menor porcentaje de colonias de especies resistentes al oleaje (sensu Alcolado, 1981; Tabla 1) lo que sugiere que puede ser el lugar más tranquilo de toda el área de estudio. En la estación D20 el cubrimiento por corales también era elevado pero abundaban más las algas y había un poco más de sedimentos sobre el fondo, lo que quizás también explique la inesperada ausencia de ambas especies en la misma.
Diversidad de especies en el ASC y su tendencia de variación con la profundidad
Los valores altos de H’ (>2.29 natios) aparecieron indistintamente en estaciones con cualquier grado de relieve, por lo que el ASC no presentó una tendencia de mayor diversidad de especies en fondos con relieve bajo, a diferencia de las áreas trabajadas por Jordán (1979), Yoshioka y Yoshioka (1989b) y Sánchez et al. (1997), lo que pone de manifiesto el carácter tan variable de la distribución y abundancia de las gorgonias, según la localidad.
Siguiendo el modelo de inferencia ambiental de Preston y Preston (1975), la abundancia de valores altos y muy altos de H’ revela la existencia generalizada de condiciones favorables para el desarrollo de comunidades complejas de octocorales en el ASC. Sin embargo, el máximo de H’ del área de estudio es superado por los registrados por Herrera-Moreno y Alcolado (1986a, 1986b), Herrera-Moreno (1991) y Herrera et al. (1997) quienes obtuvieron valores superiores a 2.6 natios en el noroeste de Cuba (entre Santa Cruz del Norte y la bahía de Mariel), a profundidades de 5 a 20 m (una vez a 5 m, seis a 10 m, tres a 15 m y una a 20 m).
Por otro lado, la gran frecuencia de valores altos y muy altos de J’ (igual o mayor que 0.69) sugiere el predominio de ambientes físicos tendientes a la constancia, según el modelo de Preston y Preston (1975). El último evento meteorológico extremo acaecido en el ASC antes del muestreo tuvo lugar ocho años antes, en noviembre de 1985 (ciclón “Kate”). Este tiempo evidencia haber sido suficiente para que la equitatividad se incrementara notablemente. Según el patrón histórico de isopletas de frecuencia de tormentas tropicales y huracanes en el Gran Caribe publicado por Lewis y Hsu (1992), el ASC es un área comparativamente poco afectada (entre 29 y 36 tormentas tropicales y huracanes que pasan a menos de 75 millas náuticas de distancia cada 100 años).
La tendencia de mayores índices de diversidad (H’, R1 y J’) a profundidades intermedias (10 m y en muy pocos casos 5 m), observada en el ASC, fue encontrada también por Goldberg (1973) en el sudeste de Florida, a juzgar por un gráfico y cálculos a partir de sus datos, y por Muñoz-Chagín (1992) en su análisis conjunto de corales duros y gorgonias de Akumal, México. Esta tendencia podría explicarse por:
(1) Las condiciones moderadas de agitación del agua a esas profundidades son soportadas por la mayoría de las especies (las que prefieren aguas someras, o profundas, o de amplio espectro batimétrico). En efecto, en las seis transecciones donde se observó la mencionada tendencia, las profundidades intermedias presentaron mayor número de especies.
(2) Las especies E. clavigera, E. calyculata f. coronata, P. kuekenthali, P. elisabethae, independientemente de ser capaces de prosperar también a poca profundidad en lugares tranquilos, tienden a predominar marcadamente en las profundidades mayores lo que conduce a menores valores de equitatividad. Lo mismo sucede en las profundidades menores a través de las especies mejor adaptadas al oleaje.
Ordenamiento de las comunidades, conectividad y factores ambientales
La ausencia de grupos geográficos y la baja correlación obtenida entre el ordenamiento de las estaciones de acuerdo con sus comunidades (nMDS) y el de las longitudes de coordenada geográfica (BIOENV), sugieren una conectividad elevada entre los arrecifes del ASC, lo que era de esperar ya que no existen barreras oceanográficas aparentes, ni de tipo de fondo o de las características del agua, que limiten el intercambio de plánulas a lo largo de un arrecife continuo que se extiende abiertamente al océano. De hecho, los modelos de transporte biofísico simulado (Miami Isopycnal Coordinate Ocean Model, RSMAS) mostrados por Paris et al. (2005) reflejan un alto grado de residencia de las aguas que circulan frente al ASC y un notable potencial de auto-reclutamiento. Esto difiere de lo observado por Jordán-Dahlgren (2002) en áreas del Golfo de México y el Caribe mexicano, donde detectó algunas restricciones de la conectividad. Además se obtuvo una mezcla de estaciones de diferentes profundidades, lo que también revela una elevada conectividad entre estas. Esto sin duda se debe a la gran dominancia de especies con amplio ámbito de distribución batimétrica. Por ello, el patrón observado ha de estar dado por factores que afectan la fijación de las larvas o al desarrollo de las gorgonias y no por limitaciones de inmigración larval.
El patrón de ordenamiento mezclado que obtuvimos con la profundidad, tanto en la clasificación como en el nMDS, formando un continuo, fue observado también por Márquez et al. (1997) en Venezuela. Esto parece deberse a que en un área tan extensa y variada, estaciones con una misma profundidad pueden tener comunidades diferentes (por ejemplo, por diferencias en la intensidad de la turbulencia de acuerdo a la localidad), o estaciones con profundidades diferentes tener comunidades parecidas por condiciones ambientales semejantes.
La turbulencia generada por el oleaje, factor con significancia en nuestro análisis BIOENV, es ampliamente reconocida como uno de los factores determinantes directos o indirectos de la composición y estructura de las comunidades de octocorales (Barham y Davies, 1968; Kinzie, 1973; Alcolado, 1981; Botero, 1987; Jordán- Dahlgren, 1989; Yoshioka y Yoshioka, 1989a, 1989b; Sánchez et al., 1997, 1998; entre otros). No obstante, Yoshioka y Yoshioka (1989a) cuestionan la acción del oleaje como regulador directo de las comunidades, y se la adjudican al desplazamiento masivo de los sedimentos del fondo, pero sus conclusiones están referidas al efecto extremo de huracanes, que producen este tipo de desplazamiento súbito y no al oleaje habitual.
La iluminación es una variable dependiente de la profundidad, que no fue medida en el presente estudio, y que es mencionada como factor determinante por Kinzie (1973), Alcolado (1981), Botero (1987), Yoshioka y Yoshioka (1989a) y Sánchez et al. (1998), entre otros. En el ASC, la mayor parte de las especies fueron de amplia distribución batimétrica para el margen de profundidades estudiado, incluyendo principalmente a P. americana y P. kuekenthali. Esto imprime un alto nivel de conectividad entre las comunidades en ese margen. Sin embargo, la luz debe haber influido en la distribución y abundancia de especies aparentemente muy fotófilas como P. homomalla y G. flabellum.
Si bien la acumulación de sedimentos no tuvo significancia en explicar la estructura y composición de las comunidades del ASC (BIOENV), otros autores en sus áreas de estudio refieren la influencia de este factor. Un ejemplo es lo ya referido arriba de Yoshioka y Yoshioka (1989a) sobre el carácter determinante inmediato que puede tener el desplazamiento de sedimentos sobre las comunidades donde existen acumulaciones. Por otra parte, Opresko (1973) menciona la vulnerabilidad de las larvas plánulas a la acumulación de sedimentos finos y Jordán (1979) refiere cómo la oclusión de las hendiduras y cavidades por sedimentos en fondos continuos, limita el asentamiento de aquellas.
En coincidencia con nuestro resultado, que descartó la biomasa de algas como factor significativo en el ASC, al parecer ésta no ha sido mencionada en la literatura como determinante en la estructura y composición de las comunidades de gorgonias. No obstante, su presencia sí ha sido sugerida por Yoshioka y Yoshioka (1989a) como influyente sobre la mayor densidad de gorgonias en el noroeste de Puerto Rico, donde las abundantes algas limitan el desplazamiento de los sedimentos acumulados en el fondo y por lo tanto evitan una mayor afectación de las colonias más pequeñas.
AGRADECIMIENTOS
Esta investigación fue financiada por Proyecto GEF/PNUD CUB/92/G31 “Protección de la biodiversidad y establecimiento de un desarrollo sostenible en el Ecosistema Sabana-Camagüey”. Agradecemos a la tripulación y buzos del buque “Ulises” por su apoyo eficiente y cordial. Igualmente, deseamos expresar nuestra especial gratitud a Maickel Armenteros por las consultas sobre análisis multivariado y a José Luis Carballo por la minuciosa revisión del manuscrito y por sus útiles señalamientos críticos y sugerencias.
BIBLIOGRAFÍA
1 Alcolado, P.M. 1981. Zonación de los octocorales someros de Cuba y su posible uso como indicadores comparativos de tensión hidrodinámica sobre los organismos del Bentos. Inf. Cient. Téc. Instituto de Oceanología, 187: 1-43. [ Links ]
2 Alcolado, P.M. 1984. Utilidad de algunos índices ecológicos estructurales en el estudio de comunidades marinas de Cuba. Cien. Biol., 11: 61-77. [ Links ]
3 Alcolado, P.M. 1992. Sobre la interpretación del ambiente marino mediante el uso de los índices de diversidad y equitatividad. Cien. Biol., 24: 124- 127. [ Links ]
4 Alcolado, P.M., E.E. García y N. Espinosa (Eds.). 1999. Protecting biodiversity and establishing sustainable development in the Sabana-Camagüey Archipelago. GEF/UNDP Project Sabana-Camagüey CUB792/G31. CESYTA S.L., Madrid. 145 p. [ Links ]
5 Barham, E. y J. Davies. 1968. Gorgonians and water motion studies in Gulf of California. Underwater Naturalist, 5(3):24-28. [ Links ]
6 Botero, L. 1987. Zonación de octocorales en el área de Santa Marta y Parque Nacional Tayrona, costa Caribe colombiano. An. Inst. Inv. Mar. Punta Betín, 17: 61-80. [ Links ]
7 Bradbury, R.H. 1977. Independent lies and holistic truths: towards a theory of coral reefs communities as complex systems. Proc. 3rd Int. Coral Reef Symp., Miami, I: 2-17. [ Links ]
8 Bray, J.R. y J.T. Curtis. 1957. Ordination of the upland forest community of Southern Wisconsin. Ecol. Monogr., 27: 325-349. [ Links ]
9 Cary, L.R. 1914. Observations upon the growth-rate and ecology of gorgonians. Carnegie Inst. Washington Publ., 182: 79-90. [ Links ]
10 Cary, L.R. 1918. A study of respiration in Alcyonaria. Carnegie Inst. Washington Publ., 252: 185-191. [ Links ]
11 Field, J.G., K.R. Clarke y R.M. Warwick. 1982. A practical strategy for analyzing multispecies distribution patterns. Mar. Ecol. Prog. Ser., 8: 37-52. [ Links ]
12 Goldberg, W. 1973. The ecology of the coral-octocoral communities off the southeast Florida coast: geomorphology, species composition and zonation. Bull. Mar. Sci., 23 (3): 465-488. [ Links ]
13 Goreau, T. 1959. The ecology of Jamaican coral reefs I: Species composition and zonation. Ecology, 40 (1): 67-90. [ Links ]
14 Herrera-Moreno, A. 1991. Efectos de la contaminación sobre la estructura ecológica de los arrecifes coralinos en el litoral Habanero. La Habana. Tesis de Doctor Ciencias Biológicas, Instituto de Oceanología, Habana.110 p. [ Links ]
15 Herrera-Moreno, A. y P.M. Alcolado. 1983. Efecto de la contaminación sobre las comunidades de gorgonáceos al Oeste de la bahía de La Habana. Cien. Biol., 10: 69-86. [ Links ]
16 Herrera-Moreno, A. y P.M. Alcolado. 1985. Monitoreo de la contaminación mediante el análisis de la estructura comunitaria de los gorgonáceos. Contrib. Simp. Cien. Mar y VII Jornada Cient. Inst. Oceanol. XX Aniversario. Ciudad de la Habana, 253-257. [ Links ]
17 Herrera-Moreno, A. y P.M. Alcolado. 1986a. Estructura ecológica de las comunidades de octocorales en el litoral de Mariel y su comparación con el litoral habanero. Cien. Biol., 15: 55-75. [ Links ]
18 Herrera-Moreno, A. y P.M. Alcolado. 1986b. Estructura ecológica de las comunidades de octocorales del arrecife de Santa Cruz del Norte. Rep. Inv. Inst. Oceanol. Acad. Cienc. Cuba, 49: 1-27. [ Links ]
19 Herrera, A., P.M. Alcolado y P. García-Parrado. 1997. Estructura ecológica de las comunidades de octocorales en el arrecife de barrera del Rincón de Guanabo. Avicennia, 6 y 7: 73-85. [ Links ]
20 Jordán, E. 1979. An analysis of gorgonian community in reef calcareous platform of the Caribbean coast of Mexico. An. Cent. Cien. Mar Limnol., UNAM. 61: 87-96. [ Links ]
21 Jordán-Dahlgren, E. 1989. Gorgonian community structure and reef zonation patterns on Yucatán coral reefs. Bull. Mar. Sci., 45: 673-696. [ Links ]
22 Jordán-Dahlgren, E. 2002. Gorgonian distribution patterns in coral reef environments of the Gulf of Mexico: evidence of sporadic ecological connectivity? Coral Reefs, 21: 205-215. [ Links ]
23 Kinzie, R.A. 1973. The zonation of West Indian gorgonians. Bull. Mar. Sci., 231: 559-592. [ Links ]
24 Kinzie, R.A. 1974. Experimental infection of aposymbiotic gorgonian polyps with zooxanthellae. J. Exp. Mar. Biol. Ecol., 15: 335-345. [ Links ]
25 Lewis, J.K. y S.A. Hsu. 1992. Mesoscale air-sea interactions related to tropical and extra tropical storms in he Gulf of Mexico. J. Geophys. Res., 97 (C2): 2215-2228. [ Links ]
26 Margalef, R. 1951. Diversidad de especies en las comunidades naturales. Publ. Inst. Biol. Aplic. Barcelona, 9: 5-27. [ Links ]
27 Márquez, L.M., M. Rodríguez y F.J. Losada. 1997. Zonation and structure of a gorgonian community in Venezuela. Proc. 8th Int. Coral Reef Symp., Panamá, I: 447-450. [ Links ]
28 Muñoz-Chagín, R.F. 1992. Estructura de la comunidad bentónica del arrecife de Akumal, Quintana Roo, México. Tesis M.Sc., CINVESTAV, Instituto Politécnico Nacional, Unidad Mérida, México. 76 p. [ Links ]
29 Muzik, K. 1982. Octocorallia (Cnidaria) from Carrie Bow Cay, Belize. Smithsonian Contr. Mar. Sci., 12: 303-310. [ Links ]
30 Opresko, D. 1973. Abundance and distribution of shallow-water gorgonians in the area of Miami, Florida. Bull. Mar. Sci., 233: 535-558. [ Links ]
31 Paris, C.B., R.K. Cowen, R. Claro y K.C. Lindeman. 2005. Larval transport pathways from Cuban snapper (Lutjanidae) spawning aggregations based on biophysical modeling. Mar. Ecol. Prog. Ser., 296: 93-106. [ Links ]
32 Pielou, E.C. 1966. The measurement of diversity in different types of biological collections. J. Theoret. Biol., 13: 131-144. [ Links ]
33 Pielou, E.C. 1975. Ecological diversity. Wiley Interscience, Nueva York. 159 p. [ Links ]
34 Preston, E.M. y J.L. Preston. 1975. Ecological structure in a West Indian gorgonian fauna. Bull. Mar. Sci., 252: 248-258. [ Links ]
35 Sánchez, J.A., J.M. Díaz y S. Zea. 1997. Gorgonian communities in two contrasting environments on oceanic atolls of the south-western Caribbean. Bull. Mar. Sci., 612: 453-465. [ Links ]
36 Sánchez, J.A., S. Zea y J.M. Díaz. 1998. Pattern of octocoral and black coral distribution in the oceanic barrier reef-complex of Providencia Island, Southwestern Caribbean. Caribb. J. Sci., 34 (3-4): 250-264. [ Links ]
37 Shannon, C.E. 1948. A mathematical theory of communication. Bell Syst. Tech. J., 27: 379-423, 623-656. [ Links ]
38 Yoshioka, P. 1997. Are variations in gorgonian recruitment determined by "pre-settlement" or "post-settlement" processes? Proc. 8th Int. Coral Reef Symp., Panamá, II: 1175-1178. [ Links ]
39 Yoshioka, P. y B. Yoshioka. 1987. Variable effect of hurricane David on the shallow-water gorgonians of Puerto Rico. Bull. Mar. Sci., 40: 132-144. [ Links ]
40 Yoshioka, P. y B. Yoshioka. 1989a. Effects of wave energy, topographic relief and sediment transport on the distribution of shallow-water gorgonians of Puerto Rico. Coral Reefs, 8: 145-152. [ Links ]
41 Yoshioka, P. y B. Yoshioka. 1989b. A multispecies, multiscale analysis of spatial pattern and its application to a shallow-water gorgonian community. Mar. Ecol. Prog. Ser., 54: 257-264. [ Links ]
FECHA DE RECEPCIÓN: 16/03/06 FECHA DE ACEPTACIÓN: 21/01/08