Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Boletín de Investigaciones Marinas y Costeras - INVEMAR
Print version ISSN 0122-9761
Bol. Invest. Mar. Cost. vol.38 no.1 Santa Marta Jan./June 2009
VELOCIDAD DE DESCOMPOSICIÓN DE LA HOJARASCA EN DIFERENTES SUSTRATOS DE MANGLAR DURANTE LA ÉPOCA DE LLUVIAS EN SAN ANDRÉS ISLA, CARIBE COLOMBIANO*
VELOCITY OF LITTER DECOMPOSITION IN DIFFERENT MANGROVE SUBSTRATES DURING THE RAINY SEASON IN SAN ANDRÉS ISLAND, COLOMBIAN CARIBBEAN
Omar Sierra-Rozo1, José Ernesto Mancera Pineda1 y Adriana Santos-Martínez2
1Universidad Nacional de Colombia, Sede Caribe, Instituto de Estudios Caribeños, Departamento de Biología, San Andrés isla, San Luis Free Town No. 52-44. oasierrar@unal.edu.co (O.S.R); jemancerap@unal.edu.co (J.E.M).
2Universidad Nacional de Colombia, Sede Caribe, Instituto de Estudios Caribeños, San Andrés isla, San Luis Free Town No. 52-44. asantosma@unal.edu.co
RESUMEN
La degradación de la hojarasca de manglar fue estudiada en diferentes sustratos de tres humedales de manglar en San Andrés isla, Caribe colombiano, durante la temporada de lluvias. Las tasas de descomposición de Rhizophora mangle L. (mangle rojo), Laguncularia racemosa (L.) C. F. Gaertn. (mangle blanco) y Avicennia germinans (L.) L. (mangle negro) fueron medidas en bolsas tipo malla. Algunas bolsas fueron dispuestas bajo el suelo, otras sumergidas en el agua y otras sobre la superficie del suelo. Dos humedales del estudio fueron de borde y uno interno. Algunos factores fisicoquímicos que influyen sobre la descomposición de la materia orgánica vegetal fueron evaluados. El modelo de regresión que mejor se ajustó al comportamiento de descomposición fue el simple de raíz cuadrada. La interacción del tiempo con factores bióticos y abióticos determinó la pérdida de biomasa foliar. Las mayores tasas de degradación se obtuvieron en humedales de borde; microambientes acuáticos y edáficos húmedos, sobre la especie A. germinans y en los lugares con macrofauna consumidora asociada. En las etapas tempranas de descomposición se presentó la mayor velocidad de degradación. En general, el menor porcentaje de biomasa remanente después de 15 semanas de incubación lo presentó A. germinans (10 %), respecto a R. mangle (29 %) y L. racemosa (28 %). Con base en los resultados obtenidos y aquellos de trabajos previos relacionados con las tasas de producción de hojarasca en los mismos humedales de estudio, se propone un modelo básico conceptual-cuantitativo de la dinámica producción-descomposición de hojarasca en San Andrés isla.
PALABRAS CLAVE: Rhizophora mangle, Laguncularia racemosa, Avicennia germinans, Descomposición, Hojarasca.
ABSTRACT
Litter degradation was studied in various substrates of three mangrove wetlands in San Andrés Island, Colombian Caribbean, during the rainy season. Decomposition rates of Rhizophora mangle L. (red mangrove), Laguncularia racemosa (L.) C. F. Gaertn. (white mangrove) and Avicennia germinans (L.) L. (black mangrove) were measured in mesh bags. Some bags were placed below ground, other submerged in water, and other on the ground. Two sites in the study were fringe wetlands and the other one was an inland wetland. Some physical-chemical factors influencing the decomposition of vegetal organic matter were evaluated. The best regression model fitted to the degradation trends was the single square root. The interactions of time with biotic and abiotic factors determined the loss of weight from leaves. The faster degradation rates were obtained in fringe wetlands; aquatic and moisten edaphic environments; on A. germinans; and at the sites with associated consumer macrofauna. The fastest velocities were presented In the early stages of decomposition. In general, the smaller average percentage of remaining biomass after 15 weeks of incubation was presented by A. germinans (10 %), respect to R. mangle (29 %) and L. racemosa (28 %). By means of the results obtained and those one related with the rates of litter production in the same wetlands in study, a basic conceptual-quantitative model of litter production-decomposition dynamic in San Andrés Island is proposed.
KEY WORDS: Rhizophora mangle, Laguncularia racemosa, Avicennia germinans, Decomposition, Litter.
INTRODUCCIÓN
Los manglares son agrupaciones de árboles y arbustos que dominan las zonas intermareales a lo largo de las líneas de costa, los estuarios y las islas en regiones tropicales y subtropicales del mundo (Middleton y McKee, 2001). Los humedales de manglar son ecosistemas altamente productivos, poseen una elevada tasa de producción primaria y además exportan materia orgánica a destinos variados sirviendo de sustrato para el desarrollo de diversos microorganismos (Mancera, 2003). La necromasa de origen aéreo del manglar es el elemento más importante respecto a la relación energética del manglar con el mar y los biomas vecinos. Al caer las hojas, una porción se mezcla con el fango y otra es exportada por la acción de las corrientes superficiales que generan las mareas, al tiempo que se constituyen en restos orgánicos importantes que se integran al ciclo de materia a través del proceso de descomposición (Escallón y Rodríguez, 1986). La cantidad de energía y materia orgánica exportada depende de las tasas de degradación de la hojarasca, la cual a su vez depende del grado y frecuencia de la inundación mareal, factores climáticos y edáficos y de la presencia o ausencia de fauna consumidora de hojarasca dentro de los humedales (Boonruang, 1978). Por tanto, la dinámica de la degradación de la hojarasca puede variar geográficamente entre sitios y tipos de humedales. Además, las tasas de descomposición varían significativamente entre especies vegetales, según la anatomía y composición química foliar (particularmente, las concentraciones de lignina y nutrientes) (Tam et al., 1998). Tal variación debe considerarse al desarrollar modelos pertinentes de cadenas alimentarias para los humedales de manglar (Robertson, 1988).
La composición de la turba de manglar respecto a la proporción relativa de hojas, madera y raíces da pautas sobre la pedogénesis del humedal de manglar. Se han hallado bajas proporciones de escombros aéreos respecto a los de las raíces en algunas turbas de manglar (Spackman et al., 1966). Sin embargo, las hojas pueden ser un aporte significativo de materia orgánica al suelo (Lacerda et al., 1995). La diferencia proporcional puede deberse a la variación en las tasas de degradación relativas de los tejidos de manglar dentro y entre humedales de manglar causadas por diferencias en factores bióticos y abióticos (Middleton y McKee, 2001).
Las islas con formaciones de manglar proveen un escenario ideal para el estudio de la degradación y la importancia relativa que la acumulación de materia orgánica tiene sobre la formación del suelo (Middleton y McKee, 2001). Cuando las islas son lejanas a las costas continentales, los ingresos alóctonos de sedimentos minerales son limitados (Macintyre et al., 1995) y la autoacumulación de sustrato es lenta. Exámenes de la composición edáfica del ecosistema de manglar revelan que el sustrato es primordialmente turba y que la contribución de la materia orgánica es clave para la acreción vertical, la estabilidad de hábitats (Cahoon y Lynch, 1997) y el mantenimiento de los humedales de manglar con respecto al nivel del mar (Cameron y Palmer, 1995). Para que la acumulación de sustrato se dé, la tasa de pérdida de materia orgánica en el sistema debe ser menor que la de producción de biomasa (Glaser, 1987).
La alta producción de los manglares tradicionalmente se ha explotado con una amplia variedad de propósitos, tales como fuentes de recursos forestales y de pesca y como espacio de colonización humana (Farnsworth y Ellison, 1997). Más recientemente, estos humedales han sido extensivamente talados y reemplazados por pozos de acuacultura para el cultivo de langosta (Primavera, 2005) y de camarón. El desarrollo turístico y la apertura de vías también han afectado negativamente estos humedales. Se estima que éstos y otros usos de consumo, ocasionan la reducción anual del 1 % de los recursos mundiales de manglar tropical (Hatcher et al., 1989). Tal reducción puede alterar las tasas de producción o pérdida de materia orgánica (Middleton y McKee, 2001).
Son abundantes los estudios de descomposición de hojarasca en manglares, especialmente en las regiones tropicales de Australia (Queensland), EE. UU. (Florida), Tailandia y Malasia (Tam et al., 1998). La mayoría de la información publicada es sobre géneros como Rhizophora y Avicennia (Tam et al., 1998), mientras que otros como Laguncularia poseen escasa información. Suramérica sólo cuenta con estudios realizados en Brasil con Rhizophora mangle, Avicennia schaueriana y Laguncularia racemosa (Sessegolo y Lana, 1991) y en Ecuador con Rhizophora spp. (Twilley et al., 1997).
El diseño de experimentos sobre descomposición y la elaboración de inventarios locales que resulten en una síntesis informativa general, permitiría desarrollar modelos conceptuales y numéricos del proceso de descomposición de la hojarasca, la pedogénesis y el almacenamiento de carbono y nutrientes en los ecosistemas (Harmon et al., 1999). El presente estudio responde a la necesidad de emprender investigaciones en el neotrópico que midan y analicen el proceso de la descomposición de la hojarasca en islas carentes de ríos y cuyo único ingreso de materia es autóctono, lo cual trae serias implicaciones en la formación del suelo y la estabilidad de los hábitats insulares. El potencial de hundimiento de los manglares en las zonas costeras es primariamente determinado por factores locales relativos al nivel del mar y el nivel del suelo litoral, la geomorfología costera, el aporte de sedimentos y la frecuencia de fuertes tormentas (Gornitz, 1995). La conservación de los humedales de manglar es estratégica en los lugares que están sometidos potencialmente al embate de disturbios naturales, como las islas del Caribe, dado que estas formaciones vegetales protegen las costas contra procesos erosivos, mitigan el efecto de vientos y mareas y actúan como barrera física protectora del impacto de huracanes resguardando el interior de las islas (Alongi, 2002).
Se presentan los resultados de un experimento de campo sobre la descomposición de la hojarasca de manglar usado para obtener las tasas de degradación dadas principalmente por lixiviación y acción de microorganismos y también por el efecto fragmentador de algunos macroorganismos edáficos, en diferentes sustratos de distintos humedales de manglar. A su vez se comparan tres importantes especies de manglar en el Caribe insular colombiano, el cual carece de estudios enfocados primariamente a la dinámica de la descomposición de la hojarasca. Además, se midieron semanalmente los cambios en algunas variables fisicoquímicas en cada sitio de estudio. Los resultados dan pautas acerca del recambio de materia orgánica y sobre los patrones y procesos que controlan la pedogénesis en humedales de manglar de las islas caribeñas. Aunque esta investigación es sitio-específica, los resultados proveen conocimientos valiosos para la orientación de proyectos de restauración o rehabilitación ecológica en ecosistemas de manglar caribeños.
ÁREA DE ESTUDIO
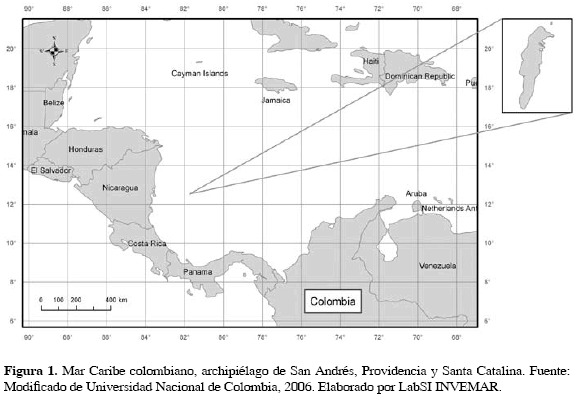
La isla de San Andrés pertenece al archipiélago colombiano San Andrés, Providencia y Santa Catalina (Reserva de la Biosfera SEAFLOWER). La isla se localiza en el mar Caribe (Fig. 1) al sur-oeste del archipiélago entre 12°28' y 12°36' N y 81°40' y 81°44' W, a unos 240 Km de la costa centroamericana (IGAC, 1986). Su área es de 27 Km2 (IGAC, 1992). La constitución geológica fundamental de la isla es de basamento volcánico del mioceno que yace bajo grandes depósitos de arena y lodo calcáreo consolidados en caliza maciza y una capa más blanda denominada caliche La plataforma marina del costado oriental es de poca profundidad y se amplía hasta los arrecifes coralinos que la rodean, conformando una barrera contra el fuerte oleaje del mar abierto. Sobre esta terraza submarina se han depositado fragmentos de corales, algas coralinas, erizos y otros animales originando arenas calcáreas (Hubach, 1956) En el costado occidental es abrupto el contacto tierra-mar formándose acantilados que reflejan la fuerte erosión marina (IGAC, 1986).
La isla se sitúa en la zona de transición entre los trópicos húmedos y secos, sin embargo, la influencia de los vientos Alisios mitiga el clima seco y cálido (Márquez et al., 2006). Según IDEAM (1995), la temperatura media anual es de 27.4 °C, con valores máximos entre 29 °C y 30 °C durante mayo y junio y mínimos entre 25.5 °C y 26.0 °C de diciembre a febrero. El régimen pluviométrico es monomodal (IDEAM, 1995). La precipitación anual promedio es de 1797 8 mm, distribuidos en un período seco (enero-abril), un período de lluvias moderadas (mayo-julio) y un período con máximos pluviométricos (octubre-diciembre) durante el cual se registra el 80 % de las lluvias anuales (IDEAM, 1995). No existen corrientes de agua permanentes, sino la formación de depósitos de agua subterráneos alimentados por las lluvias, pantanos y charcas que fluctúan su nivel de modo considerable según la época del año (Barriga et al., 1969; IGAC, 1986).
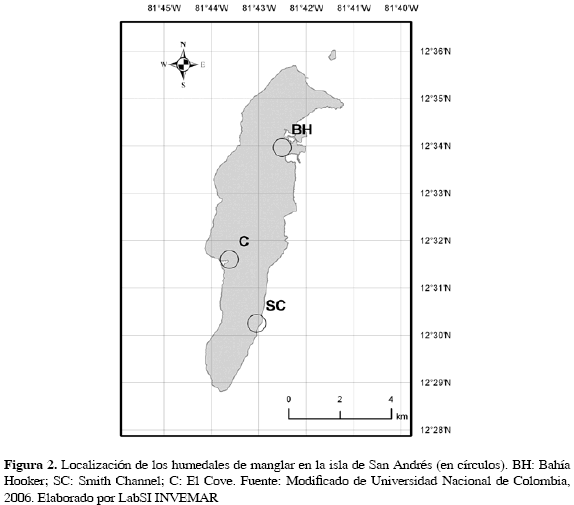
Los manglares en la isla, ocupan una extensión aproximada de 96.98 Ha (García y Gaviria, 1996). Al costado este (sotavento) se hallan seis zonas de manglar, las cuales crecen como rodales aislados y de escasa cobertura (Fig. 2) Al oeste de la isla solamente hay un parche de manglar Los humedales considerados en este estudio son:
- Bahía Hooker (N 12°33.962', W 81°42.511'; 34.4 Ha), ubicado al nororiente de la isla. Es un habitat de borde asociado al litoral arenoso, sus suelos son arenosos y fangosos; las especies de manglar presentes son Rhizophora mangle, Avicennia germinans y Laguncularia racemosa; la dominancia relativa (DR) para R. mangle y A. germinans es de 37 % y para L. racemosa de 26 %; el índice de importancia relativa (IVI) es R. mangle > A. germinans > L. racemosa; la altura promedio de los árboles del manglar es de 5.1 m; el promedio del diámetro a la altura del pecho (DAP) es de 18.7 cm; el promedio del diámetro de copa (DC) es de 2.9 m; la densidad total es de 130 individuos/0.1 Ha; y tiene un área basal total de 5.82 m2/0.1 Ha. La producción de hojarasca es: R. mangle (705.9 g/m2/año), L. racemosa (379.3 g/m2/año), y A. germinans (701.7 g/m2/año). La bahía en su mayor parte está bordeada por R. mangle; el interior consta de la mezcla de las tres especies de manglar Bahía Hooker es el humedal menos desarrollado de la isla, y presenta moderada contaminación por hidrocarburos (García y Gaviria, 1996).
- Smith Channel (N 12°30.244', W 81°43.051'; 17.8 Ha), localizado al suroriente de la isla. Este rodal de hábitat interno se halla aislado del mar por una carretera y playa arenosa, posee sedimentos oscuros y consistentes; cuenta con L. racemosa y R. mangle; la DR para las dos especies es del 50 %, pero el IVI es más alto para R. mangle; la altura promedio de los árboles del manglar es de 12.8 m, el promedio del DAP es de 46.4 cm, el DC promedio es de 5.2 m, la densidad total es de 24 individuos/0. 1 Ha; y tiene un área basal total de 4.3 m2/0. 1 Ha. La producción de hojarasca es: R. mangle (683.8 g/m2/año) y L. racemosa (746.4 g/m2/año). El humedal no presenta zonación de las especies de manglar (García y Gaviria, 1996).
- El Cove (N 12°31.597', W 81°43.625'; 1.2 Ha). Es el único parche de manglar sobre el costado occidental de la isla (García y Gaviria, 1996). Es un hábitat de borde en contacto con el litoral rocoso, sus sedimentos son lodosos y de color tabaco; R. mangle es la única especie presente; la altura promedio de los árboles del manglar es de 7.6 m; el DAP promedio es de 24.1 cm; el DC promedio es de 3.47 m; la densidad total es de 85 individuos/0. 1 Ha; y tiene un área basal total de 5.10 m2/0. 1 Ha. La producción de hojarasca es de 700.0 g/m2/año. Este humedal está alimentado por un drenaje casi permanente (Cove Gully), que contribuye al aporte hídrico de la zona (García y Gaviria, 1996).
MATERIALES Y MÉTODOS
Diseño experimental
Se estudió la descomposición de la hojarasca de manglar siguiendo la técnica de la bolsa de hojarasca (litterbag), propuesta por Harmon et al. (1999). De cada una de las especies de manglar pertenecientes a cada humedal de estudio, se colectaron hojas senescentes a finales de septiembre de 2006, procurando que estuvieran completas y que hicieran parte de la fronda. Estas hojas se secaron al aire por una semana, y muestras de 5 g (+/- 0.15 g) de cada especie fueron empacadas en bolsas de nylon tipo malla (10 x 20 cm) con un ojo de malla de 0.4 cm, el cual limita el acceso de organismos de mayor tamaño al material en descomposición. Cada bolsa representó una unidad experimental (UE) y contó con tres réplicas. Cantidades adicionales de 5 g para cada especie fueron secadas a 55 °C hasta alcanzar el peso seco constante y con él establecer la conversión inicial de masa seca al aire a masa seca en horno.
Durante la primera semana de octubre de 2006, en cada uno de los humedales de colecta, se dispusieron las UE de forma equidistante y aleatoria en tres sustratos de descomposición diferentes: suspendidas en el agua (sustrato agua), enterradas diagonalmente en el suelo (sustrato suelo) y sobre el suelo del humedal (sustrato superficie). Constituyéndose así cada tratamiento por humedal, especie, y sustrato de descomposición. 324 UE se ubicaron en Bahía Hooker, 216 en Smith Channel y 108 en El Cove. En B. Hooker y en S. Channel las muestras del sustrato agua se colocaron en lagunas internas del humedal, mientras que en El Cove las muestras se dejaron sumergidas en el mar. Semanalmente y durante las primeras seis semanas (octubre-noviembre) se recogieron al azar, tres UE de cada tratamiento, posteriormente tal colecta se realizó cada dos semanas hasta completar 15 semanas de incubación de las muestras en campo (noviembre-febrero), colectándose así el material biológico predominantemente en la temporada lluviosa de la isla.
Después de cada colecta, el material fue transportado al laboratorio de biología y química de las instalaciones de la Universidad Nacional de Colombia sede Caribe. Allí se lavó cuidadosamente con agua para retirar los sedimentos y los animales visibles. Posteriormente, el material limpio se secó a 55 °C hasta obtener peso constante (cinco días) y se pesó, actividad realizada con equipos pertenecientes al Laboratorio del Herbario del Jardín Botánico de la Universidad Nacional de Colombia sede Caribe. Una vez obtenidos los datos de peso seco, el material biológico se pulverizó y envasó, con el fin de desarrollar análisis químicos posteriormente. Los valores de peso seco registrados son porcentajes remanentes del peso seco original en cada intervalo temporal de colecta.
Simultáneamente a cada colecta, se midieron in situ (excavando hoyos adyacentes a las muestras) en el agua asociada a cada sustrato las variables fisicoquímicas pH (electrodo de vidrio de pHmetro Schott handylab 1), salinidad (refractómetro Vista A366ATC), temperatura y oxígeno disuelto (Oxímetro YSI 550 DO). Los valores de salinidad se expresan en la escala práctica de salinidad, la cual es adimensional (UNESCO, 1985). Además, el estado de humedad de las muestras se revisó cualitativamente considerando si las muestras se hallaban sumergidas (muestras acuáticas) o saturadas de agua (muestras superficiales y edáficas). Para cada humedal, en cada una de las 15 visitas de recolección de muestras, se registró la temperatura instantánea (la presente en el momento de llegada al humedal), máxima y mínima (presentadas en el transcurso de la semana previa a la recolección), mediante un termómetro de máximos y mínimos fijado a 50 cm del suelo.
Análisis de los datos
Mediante ANOVAS de medidas repetidas empleando el paquete estadístico STATISTICA 6 0, se compararon dentro y entre tratamientos las tasas medias de degradación y los cambios en los promedios de biomasa foliar remanente. Se tuvieron en cuenta niveles de significancia en p< 0.05 (Sokal y Rohlf, 1981). Se hicieron comparaciones de diversos modelos de regresión con el paquete STATGRAPHICS Plus para determinar el modelo que mejor describiera el patrón de pérdida de biomasa en el tiempo para cada tratamiento. Los datos fisicoquímicos se trataron mediante estadística descriptiva y se realizaron comparaciones entre sitios por sustrato y sustratos por sitio empleando el test de Kruskal-Wallis. Se consideró significancia en p< 0.05.
RESULTADOS
Variables fisicoquímicas
Condiciones edafológicas
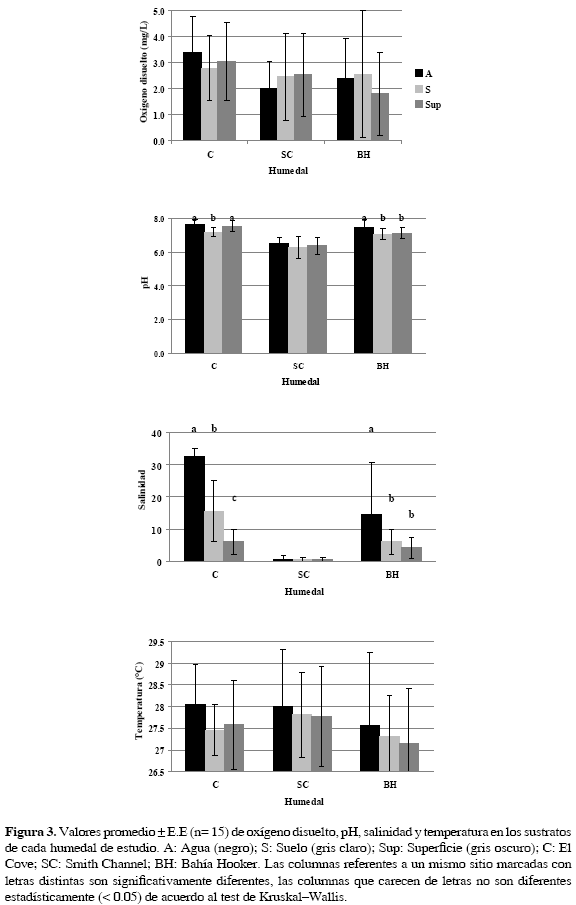
En general, para el área total de estudio, los valores promedio registrados de pH estuvieron cercanos al neutro (6.3-7.6), de oxígeno disuelto fueron bajos (1.83.4 mg/L) y de temperatura próximos a 28 °C. La salinidad varió desde valores promedio cercanos a 0 hasta próximos al valor del agua de mar (35) (Fig. 3).
- Comparación de las variables fisicoquímicas entre los humedales (Fig. 3): Para el sustrato agua, El Cove presentó significativamente el mayor valor promedio para el oxígeno disuelto (3.39±1.38). Los máximos valores promedios de pH se presentaron en El Cove (7.64±0.34) y B. Hooker (7.44±0.49). La mayor salinidad se presentó en El Cove (32.44±2.53), fue intermedia en B. Hooker (14.45±16.14) y muy baja en S. Channel (0.60±1.07).
En el sustrato superficie, el oxígeno disuelto no presentó diferencias significativas entre los humedales. El pH y la salinidad fueron mayores en El Cove (7. 34±0. 33; 5. 90±3. 93 respectivamente) y B. Hooker (7.13±0. 35; 4.13±3. 21 respectivamente).
En el sustrato suelo, el oxígeno disuelto fue homogéneo para los tres humedales. El pH fue mayor en El Cove (7. 17±0. 25) y en B. Hooker (7. 07±0. 33). La salinidad fue mayor en El Cove (15. 46±9. 41) y menor en S. Channel (0. 41±0. 55). La temperatura registrada en los tres humedales no fue significativamente diferente.
- Comparación de las variables fisicoquímicas de los sustratos en cada humedal (Fig. 3): En S. Channel las variables fisicoquímicas fueron homogéneas para los sustratos. Las lecturas medias de oxígeno disuelto y salinidad fueron bajas, el pH fue próximo a 6 y la temperatura cercana a 28 °C.
En el humedal El Cove las medidas tanto de pH y de temperatura fueron similares en los sustratos, pero el sustrato agua presentó significativamente el mayor pH (7.64±0.34) y la mayor temperatura (28.04±0.93 °C). La mayor salinidad se registró en el sustrato agua (32.44±2.53) y la menor en el sustrato superficie (5.90±3.93). Las lecturas de oxígeno disuelto no fueron significativamente diferentes.
En B. Hooker el mayor pH se registró en el sustrato agua (7.44±0.49), la mayor y menor salinidad se obtuvo en el sustrato agua (14.45±16.14) y superficie (4.13±3.21) respectivamente. El oxígeno disuelto no presentó diferencias significativas entre los sustratos.
Temperatura ambiental y estado de humedad de las muestras
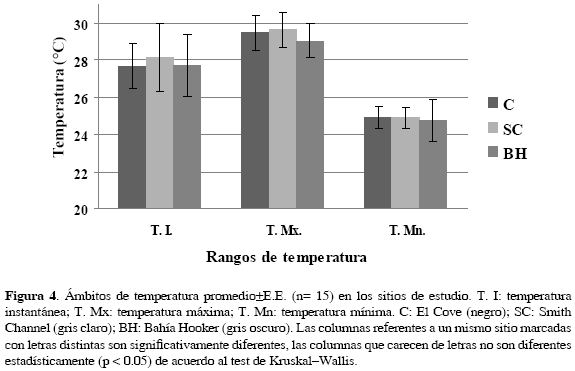
En general, la temperatura en los tres humedales osciló entre 25 y 30 °C (Fig. 4). Las temperaturas instantáneas, máximas y mínimas no fueron significativamente diferentes entre los humedales.
Con relación a la humedad de las muestras, las observaciones pueden generalizarse para los tres humedales. Las muestras acuáticas permanecieron durante el experimento en condición de permanente anegamiento; las edáficas, la mayor parte del tiempo estuvieron en contacto con agua intersticial, el nivel freático se encontró por lo general entre 5 y 10 cm de profundidad; y las supericiales, tuvieron oscilaciones respecto a la cantidad de agua circundante, aunque casi siempre permanecieron en contacto con agua por su base, pues la altura de la columna de agua desde el nivel del suelo fue generalmente de 1.2 cm.
Degradación de la hojarasca
Consideraciones generales
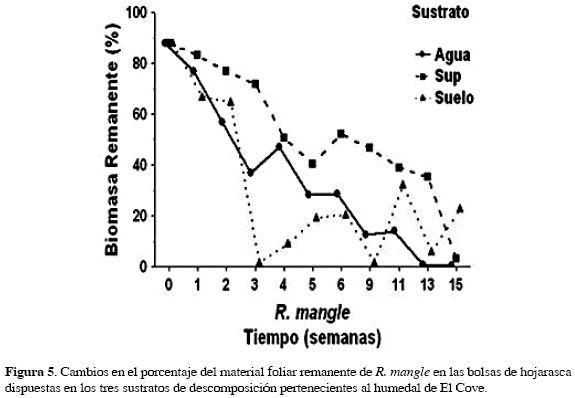
Las tendencias de pérdida de biomasa en el tiempo, se muestran en las figuras 5, 6 y 7. Durante las tres primeras semanas de incubación se presentó en general la mayor pérdida de biomasa: A. germinans perdió alrededor del 54 % de su biomasa inicial, R. mangle el 40 % y L. racemosa el 36 %. Al finalizar el experimento, la biomasa promedio remanente en los humedales fue de 29, 28 y 10 % para R. mangle, L. racemosa y A. germinans respectivamente.
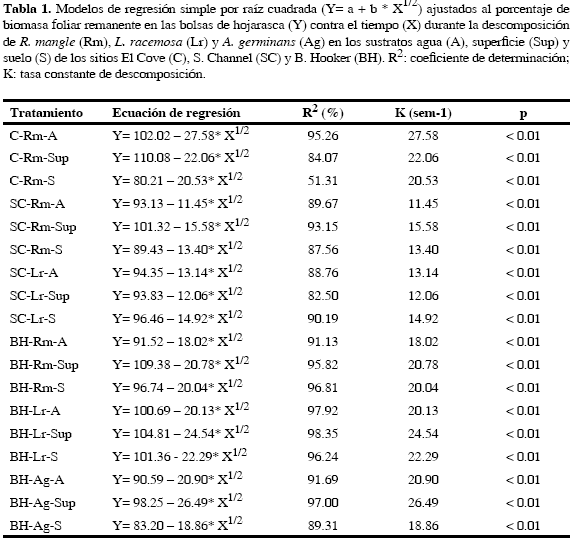
En general, las curvas de pérdida de biomasa se caracterizan por tener una pendiente más pronunciada en la fase inicial de descomposición (Figs. 5, 6 y 7) y por ajustarse al modelo de regresión simple por raíz cuadrada (Tabla 1). Todos los modelos muestran una relación significativa (p< 0.01) (Tabla 1) entre la biomasa y el tiempo. Desde la semana seis de experimentación, cada especie en todos los tratamientos tiende a disminuir la velocidad de degradación y a nivelar el porcentaje de biomasa remanente entre los sustratos (Figs. 5, 6 y 7).
Los coeficientes de determinación R2 (Tabla 1) oscilaron, en su mayoría, entre valores del 80 y 90 %, indicando que en buena proporción la variación de los datos es explicada por el tiempo. Sólo el caso correspondiente al sustrato suelo en El Cove mostró un R2 inferior (51 %).
Descomposición de la hojarasca en El Cove
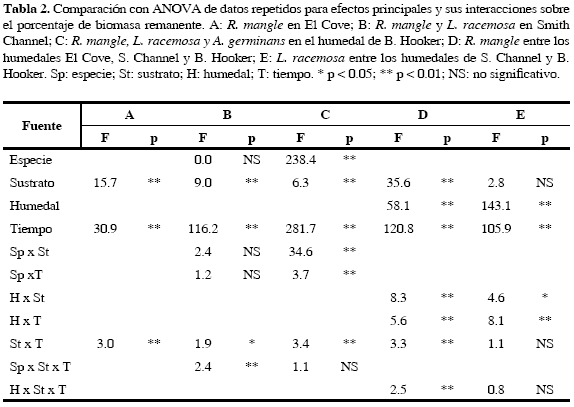
Para el humedal El Cove, el ANOVA de medidas repetidas determina diferencias significativas en los factores sustrato, tiempo y para la interacción sustrato x tiempo (Tabla 2A). La interacción sugiere que la dinámica de la pérdida de biomasa cambia significativamente a través del período de incubación según el sustrato. El tratamiento en el sustrato suelo se vio afectado notablemente por la influencia de cangrejos (Armases ricordi H. Milne Edwards), los cuales rompieron las bolsas de nylon y facilitaron la dispersión y degradación del material foliar. Lo anterior se vio reflejado en el comportamiento de la pérdida de biomasa en este sustrato, el cual exhibió fuertes cambios y no siguió un patrón claro durante el período de incubación, también se refleja en el bajo valor de R2; lo anterior hace diferir marcadamente este tratamiento de los otros dos.
Se presenta una descomposición más rápida en el sustrato agua (Fig. 5), soportada con los valores de los coeficientes de degradación por semana (Tabla 1). En la semana 15 cerca del 26,4 y 0 % de biomasa de R. mangle permanece en las bolsas de descomposición, para los sustratos suelo, superficie y agua, respectivamente (Fig. 5).
Descomposición de la hojarasca en S. Channel
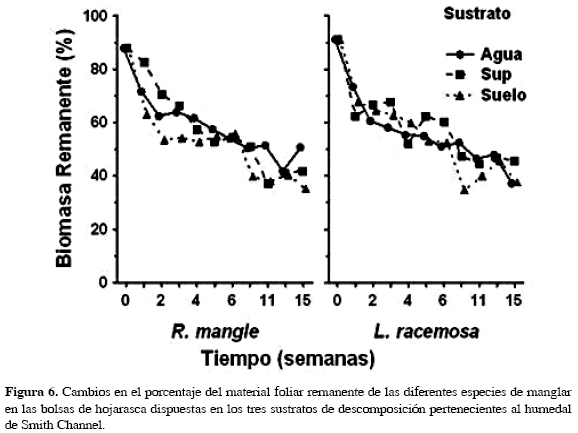
En el humedal de S. Channel se presentan diferencias significativas para los factores sustrato, tiempo y las interacciones sustrato x tiempo y especie x sustrato x tiempo (Tabla 2B). Esta última interacción sugiere que el patrón de pérdida de peso varía entre sustrato y tiempo para ambas especies. En la Figura 6 se observa que R. mangle experimenta una alta tasa de descomposición en el sustrato suelo, que contrasta con aquella del sustrato supericie, sobretodo en las primeras seis semanas de descomposición. No son claras las diferencias en el comportamiento de las curvas para L. racemosa, la tendencia para el sustrato supericie es irregular y se cruza con la de los otros sustratos, lo cual se manifiesta en los resultados de los análisis de varianza con interacciones significativas. Todos los tratamientos poseen una tasa de degradación que oscila entre el 11 y 16 % sem-1.
Hacia la fase final del estudio, para las dos especies las tasas de pérdida de biomasa en los tres sustratos se hacen semejantes y tienden a igualar las cantidades de biomasa remanente (Fig. 6); al final de la semana 15, aproximadamente un 46 % del material vegetal original permanece en las bolsas de nylon (Fig. 6) Para este humedal, no fueron observados invertebrados asociados al material vegetal en descomposición.
Descomposición de la hojarasca en B. Hooker
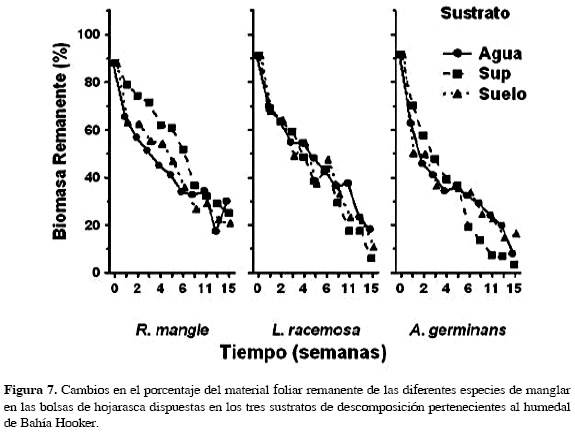
Los factores especie, sustrato y tiempo y sus interacciones dobles influyen significativamente sobre la descomposición de hojarasca (Tabla 2C). La interacción especie x sustrato indica que la degradación foliar cambia entre las especies y es diferencial según el sustrato. La interacción especie x tiempo y sustrato x tiempo demuestran que las diferencias en los patrones de descomposición dependen del sustrato o de la especie con que se halle asociado el período de incubación.
Desde la sexta semana de incubación, las tasas de degradación tienden a disminuir y a mostrar valores de biomasa remanente similares entre sustratos para cada especie (Fig. 7); el porcentaje aproximado de biomasa remanente hacia la semana 15 incrementa en el orden A. germinans (10 %), L. racemosa (13 %), R. mangle (28 %) (Fig. 7). Esta figura muestra que la curva de degradación de R. mangle en general experimenta la menor pendiente, caso opuesto al de A. germinans. Aunque la curva de A. germinans en el sustrato supericie presenta un brusco decaimiento desde la sexta semana de experimentación, en general durante las primeras cinco semanas la tasa de degradación de las especies en el sustrato superficie es similar o más lenta que la de los otros sustratos (Fig. 7).
Los valores de R2 registrados fueron próximos al 90 % Los tratamientos promedian una constante de degradación próxima al 21 % sem-1 (Tabla 1). En algunas ocasiones se detectaron en el material foliar llevado al laboratorio, poliquetos y anfípodos (suborden Gammaridae), los cuales no ocasionaron ruptura de las bolsas de hojarasca.
Comparación de la descomposición de la hojarasca entre humedales
El patrón y la tasa de degradación de la hojarasca de R. mangle difieren significativamente entre los humedales y entre los sustratos (Tabla 2D, Figs. 5, 6 y 7). La interacción significativa sitio x sustrato x tiempo evidencia que la dinámica de descomposición foliar de R. mangle depende del humedal, del sustrato y del tiempo de incubación (Tabla 2D) En los humedales, las tasas medias de degradación para R. mangle se incrementan en el orden S. Channel (13.5 % sem-1), B. Hooker (19.6 % sem-1), El Cove (23.4 % sem-1); así mismo, son muy similares entre los sustratos: superficie (19.5 % sem-1), agua (19 % sem-1), suelo (18 % sem-1) (Tabla 1). El material vegetal remanente de R. mangle, después de la semana 15 de estudio es alrededor de1 10 % en El Cove, 28 % en B. Hooker y 48 % en S. Channel (Figs. 5, 6 y 7).
La dinámica de descomposición de la hojarasca de L. racemosa varía significativamente entre los humedales de B. Hooker y S. Channel durante el período de incubación, independientemente del sustrato en que se halle la hojarasca (Tabla 2E, Figs. 5, 6 y 7). En S. Channel la tasa media de degradación es del 13 % sem-1, y en B. Hooker del 22 % sem-1 (Tabla 1). El tejido vegetal presente de L. racemosa después de la semana 15 de estudio, es próximo al 44 y 13 % en S. Channel y B. Hooker, respectivamente (Figs. 5, 6 y 7).
DISCUSIÓN
Aunque el modelo de regresión frecuentemente empleado y aconsejado en estudios de degradación de hojarasca es el simple exponencial negativo de Wieder y Lang (1982), este modelo no describe adecuadamente la cinética de la descomposición de la hojarasca cuando las tasas relativas de decaimiento varían en el tiempo, como es el caso en que hay una rápida pérdida o una temprana fase de retraso extendido durante la degradación (Harmon et al., 1999). En este estudio, los datos en general, se ajustaron adecuadamente al modelo de regresión simple por raíz cuadrada (Y= a + b * X1/2). La curva general de este modelo, a diferencia del exponencial, posee un patrón inicial de decaimiento mayor, el cual resultó describir con más precisión la dinámica de la fase inicial de la degradación de la hojarasca.
La pérdida rápida inicial de biomasa que caracteriza en general a los tratamientos realizados es atribuible al lavado inmediato del material orgánico soluble y de compuestos inorgánicos (Camilleri y Ribi, 1986). Estos autores han mostrado que entre el 13 y 40 % del material original foliar de A. marina y R. mangle puede liberarse por lixiviación en los primeros tres a nueve días de descomposición, respectivamente. La degradación posterior es mediada por poblaciones microbianas y fúngicas que se desarrollan rápido durante los primeros 30 días de incubación (Benner et al., 1988) El lavado temprano de las muestras se aprecia de forma más conspicua en los sustratos acuático y edáico. Lo anterior se relaciona con el estado de humedad prevaleciente en estos tratamientos; mientras que las muestras acuáticas y edáicas permanecieron anegadas y saturadas respectivamente, el nivel de cobertura de agua para las muestras de superficie fluctuó durante el experimento, persistiendo la mayor parte del tiempo la base de las bolsas de descomposición en directo contacto con agua. Todos los tratamientos a partir de la sexta semana de experimentación, tienden a disminuir la velocidad de degradación y a nivelar el porcentaje de biomasa degradada. Este patrón se explica por la remanencia de materiales refractarios en esta etapa, tales como lignina y fragmentos cuticulares (Steinke et al., 1990). El elevado coeficiente de determinación de las regresiones, así como la alta significancia del factor tiempo y la mayoría de sus interacciones en los análisis de varianza, indican que el tiempo es el factor fundamental en la explicación de la variabilidad en el porcentaje de degradación y que la interdependencia del tiempo con los otros factores determina las diferencias entre los tratamientos.
El bajo R2 del modelo de regresión para el tratamiento de R. mangle en el sustrato suelo para el humedal El Cove sugiere que, además del tiempo, el factor sustrato debe influir sobre la respuesta del cambio en biomasa remanente. El patrón irregular que exhibe la curva de degradación en el sustrato suelo en El Cove es causado principalmente por efectos bióticos. En los muestreos semanales fue común observar cangrejos de la especie Armases ricordi (Sesarmidae) en este humedal, asociados al hábitat edáico, donde cavan sus madrigueras. Estos mismos cangrejos, en especial los pequeños, se encontraron en las bolsas de nylon colectadas mientras se lavaban; aunque no existen pruebas del consumo de hojarasca por parte de este decápodo, en África y Australia se ha establecido que el consumo directo de la hojarasca de manglar por parte de cangrejos de la familia Sesarmidae tiene un notable efecto sobre la descomposición de la hojarasca (Camilleri y Ribi, 1986; Robertson, 1986; Emmerson y McGwynne, 1992; Micheli, 1993; Steinke et al., 1993a; Kathiresan y Bingham, 2001). Por el carácter aleatorio de los muestreos la detección de los cangrejos en las bolsas no fue continua, pero afectó en ocasiones las tres réplicas. El daño a la bolsa y el contacto directo de los cangrejos con la hojarasca probablemente aceleraron la pérdida de biomasa, lo cual se reflejó conspicuamente en el sustrato suelo mientras se examinaban las bolsas de descomposición. Dada la anterior condición, es necesario incorporar en el análisis la actividad de estos invertebrados pues, aunque no se cuantificó su efecto sobre la descomposición de la hojarasca respecto al inducido por los microorganismos y las fuerzas abióticas, todos estos efectos actúan en conjunto para determinar la tasa de degradación del material foliar. De hecho, Middleton y McKee (2001) han indicado que invertebrados como cangrejos y anfípodos triplican la tasa total de degradación y que las hojas ubicadas bajo el suelo experimentan una degradación 2.4 veces más rápida que aquellas dejadas sobre la supericie. Robertson (1986) registró en Australia que cangrejos del género Sesarma (Sesarmidae) remueven más del 28 % de la producción de hojarasca en humedales mixtos de Rhizophora. Recientes estudios en Latinoamérica sugieren también que los cangrejos consumen bastante hojarasca de manglar (Twilley et al., 1997). Las bolsas pertenecientes al tratamiento supericial y acuático también fueron afectadas por estos decápodos, aunque de modo menos recurrente, de acuerdo con las observaciones realizadas durante el procesamiento de las muestras en el laboratorio (Fig. 5). Las condiciones fisicoquímicas de los tres sustratos son muy similares salvo la salinidad, cuyo efecto diferencial sobre la degradación pudo ocultarse por la presencia del efecto biótico.
En S. Channel, si bien las tasas medias de descomposición que presentaron R. mangle y L. racemosa fueron similares entre los sustratos, las constantes de decaimiento pueden no describir con exactitud curvas que presentan muchos altibajos, como en este caso; en cambio, al observar las curvas detalladamente, es posible apreciar que aquella perteneciente al sustrato superficie, para las dos especies, tiende a presentar, durante las primeras y últimas semanas, una pendiente menor. Este fenómeno no es explicable por la medida cuantitativa de los agentes fisicoquímicos, pues éstos no fueron diferentes entre sustratos. Sin embargo, la intensidad del contacto de estos agentes con las bolsas de descomposición sí fue distinto; teniendo en cuenta que las muestras del sustrato agua permanecieron anegadas y las de suelo permanecieron rodeadas por agua intersticial (las lluvias en la época de estudio mantuvieron el suelo húmedo y elevado el nivel freático), pero las muestras del sustrato superficie sólo contactaron el sustrato por su base. Tam et al. (1998) mencionan que la heterogeneidad espacial es un fenómeno común en ambientes de manglares que influye en los procesos de descomposición. El estado de frecuente inundación promueve una mayor lixiviación y mantiene las condiciones de humedad y temperatura aptas para el deterioro saprofítico (Mackey y Smail, 1996). Robertson (1988), en estudios con R. stylosa y A. marina, indica que las densidades bacterianas son entre dos y tres veces más altas en los hábitats sumergidos. Otros trabajos indican que ambientes con limitada disponibilidad de humedad, como la superficie del suelo en la zona intermareal, poseen una mayor fluctuación en el grado de cobertura del agua, sufren altas temperaturas que pueden sobrepasar el nivel óptimo para los descomponedores y consecuentemente afectar negativamente la velocidad de degradación foliar (Flores-Verdugo et al., 1987; Robertson, 1988). El efecto especie específico no fue significativo en este humedal, posiblemente porque los rasgos foliares en ambas especies interactúan de forma similar con el ambiente.
La variación significativa de las tasas de degradación de hojarasca entre las especies y su interacción con el sustrato y el tiempo son vistas claramente en el humedal de B. Hooker, donde A. germinans en el sustrato acuático tiene la mayor pérdida media de biomasa durante las primeras seis semanas, y la menor durante las siguientes semanas. La pérdida inicial acelerada de biomasa en este tratamiento podría explicarse por diferencias en la composición química de las hojas (Robertson, 1988), en la anatomía foliar (Tam et al., 1998) y por la estabilidad ambiental favorable para la acción microbiana, que caracteriza a los microambientes húmedos (Flores-Verdugo et al., 1987; Robertson, 1988). Avicennia germinans posee baja cantidad de taninos, alta cantidad de nitrógeno y baja proporción C:N respecto a R. mangle y L. racemosa, lo cual acelera el proceso de descomposición (Robertson, 1988; Middleton y McKee, 2001). Es sabido que los taninos son sustancias de difícil degradación, tóxicas para microorganismos (Steinke et al., 1990), que inhiben el crecimiento poblacional de la meiofauna (Alongi, 1990) y tienen un efecto de disuasión sobre herbívoros (Kathiresan, 1992). La leve degradación experimentada en las últimas semanas es atribuible a la remanencia de tejidos recalcitrantes de difícil descomposición. La baja consistencia foliar de A. germinans, junto con la baja salinidad (4) registrada en el ambiente superficial, podrían influir en el brusco decaimiento experimentado por este tratamiento en la última semana de muestreo y en consecuencia elevar la tasa de degradación respecto a los otros sustratos. Steinke et al. (1993b) encontraron que la degradación foliar en hojas de A. marina se acentúa en medios con moderadas salinidades Con base en lo anterior, podría explicarse la interesante inversión en la tasa de degradación de A. germinans, particularmente notable para los sustratos acuático y superficial. Las curvas para R. mangle apoyan el notorio efecto positivo que tiene el ambiente acuático sobre la degradación. Trabajos previos como el de Middleton y McKee (2001) han obtenido resultados similares al del presente estudio, ellos señalan que las tasas de pérdida de biomasa en R. mangle, L. racemosa y A. germinans en los humedales de Belice es mucho más rápida en ambientes acuáticos que en zonas secas y que A. germinans presenta la mayor velocidad de degradación.
Al observar el comportamiento entre humedales considerando la misma especie, la interacción significativa sitio x sustrato x tiempo muestra que la dinámica de descomposición foliar de R. mangle depende del humedal, del sustrato y del tiempo de incubación; de modo que la menor pérdida de biomasa para R. mangle experimentada en el humedal de S. Channel, respecto a la de El Cove y B. Hooker, podría estar influida por diversas causas: 1) La fauna asociada a la fragmentación y descomposición foliar. En S. Channel no se registraron animales asociados a la hojarasca, mientras que en El Cove se observaron cangrejos, y un tipo de poliqueto y de anfípodo fueron vistos ocasionalmente en el laboratorio entre los tejidos en descomposición de R. mangle proveniente de B. Hooker. Probablemente esta sea la razón fundamental por la que se dio la marcada diferencia entre las tasas de degradación pues, aunque no se determinó cuantitativamente el efecto de los invertebrados, cualitativamente sí se detectó que la recurrencia de éstos sobre el material en descomposición fue alta en El Cove, media en Bahía Hooker y nula en S. Channel. La presencia o ausencia de esta fauna edáfica podría relacionarse con el carácter de humedal interno de S. Channel y la casi nula salinidad establecida en éste. 2) El pH ligeramente ácido que presentó S. Channel en todos los medios de descomposición, pudo afectar diferencialmente la tendencia de degradación de R. mangle, relacionada principalmente con la acción microbiana. 3) La condición de manglar interno y el mayor desarrollo estructural de S. Channel (García y Gaviria, 1996) podría crear en este humedal un entorno más estable ante fuerzas ambientales que fomentarían el deterioro de la hojarasca, como la incidencia directa del sol, mareas, viento y lluvias (Woitchik et al., 1997). 4) Entre los humedales del estudio, S. Channel posee la mayor producción de hojarasca (R. mangle: 683. 8 g/m2/año; L. racemosa: 746.4 g/m2/año), que además presenta picos máximos en las temporadas de lluvias (García y Gaviria, 1996) como la del presente estudio, lo cual podría provocar la acreción del horizonte orgánico e impedir el contacto directo de las hojas recién caídas con el suelo, retardando así el proceso de descomposición. En el presente trabajo se constató de manera cualitativa (observación en campo) el carácter orgánico del suelo de S. Channel, que contrasta con los suelos principalmente fangosos de B. Hooker y El Cove (García y Gaviria, 1996). 5). El comportamiento irregular y la mayor tasa de degradación del tratamiento acuático en El Cove, probablemente sea reflejo del efecto directo del mar sobre las muestras, del movimiento de las mareas y del contacto con materiales arrastrados por éstas, lo cual en suma pudo intensificar el proceso de degradación. Igualmente, la significativamente mayor oxigenación del ambiente acuático respecto a los otros dos humedales, pudo favorecer la proliferación de bacterias sobre los tejidos en degradación.
La dinámica de la degradación de hojarasca de L. racemosa varía significativamente entre los humedales de B. Hooker y S. Channel durante el período de incubación independientemente del sustrato en que se halle la hojarasca (Figs. 6 y 7, Tabla 2E). Las mismas razones por las que la descomposición de R. mangle es más lenta en S. Channel, son atribuibles a L. racemosa. La no significancia para el factor sustrato en este caso, puede ser efecto de la homogeneidad en los factores fisicoquímicos del microambiente experimentadas por las bolsas de hojarasca en los dos humedales. Estudios en descomposición de hojarasca realizados en otros países (Mitsch y Gosselink, 1993) muestran que para R. mangle el proceso de degradación es más rápido en hábitats de borde, apoyando esto lo observado en este trabajo.
En vista del importante papel que parecen desempeñar los invertebrados en el proceso de degradación de la hojarasca, es conveniente adelantar estudios que establezcan densidades y patrones de forrajeo de estos organismos. Se sugiere que otros trabajos acerca de la descomposición de hojarasca que empleen el método de la bolsa de descomposición, usen un diseño de bolsa más resistente que evite la influencia de factores imprevistos en el experimento.
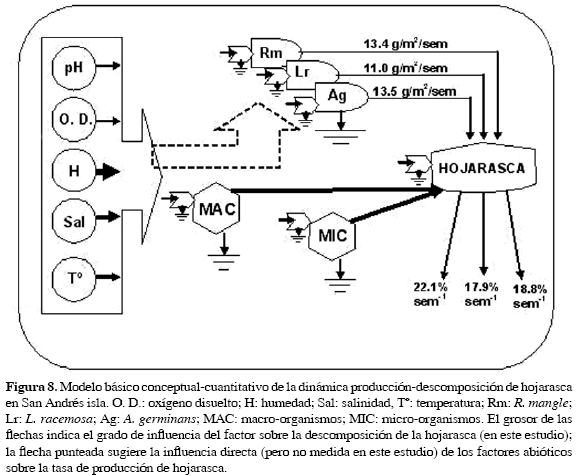
Mediante los resultados obtenidos y aquellos de trabajos previos relacionados con las tasas de producción de hojarasca en los mismos humedales de estudio (García y Gaviria, 1996), se propone un modelo básico conceptual-cuantitativo de la dinámica producción-descomposición de hojarasca en San Andrés isla (Fig 8). Según el modelo planteado, sin incluir tasas de exportación, R. mangle es la especie que contribuiría mayormente a la formación de suelo; aunque su producción promedio sea similar a la de A. germinans y su descomposición semejante a la de L. racemosa y A. germinans, el mangle rojo se halla presente en los seis humedales de manglar de la isla con una importante cobertura (García y Gaviria, 1996), lo cual conllevaría a la acumulación de la hojarasca de esta especie en la turba del humedal. No obstante, es necesario desarrollar investigaciones que midan la tasa de exportación y la actividad de los consumidores de hojarasca e incluir los resultados en futuros modelos.
Implicaciones en el área de estudio
La ganancia externa de sedimentos en la isla de San Andrés es nula, por lo tanto depende de la autodeposición de materia orgánica para mantener el nivel superficial del suelo y la regeneración de nutrientes. La cantidad de materia orgánica acumulada en los humedales de manglar de esta isla está sujeta al balance entre la producción de hojarasca y la descomposición de ésta, junto con procesos físicos como la exportación mareal. Sin embargo, en zonas que están bajo la incidencia potencial de huracanes, como es el caso del archipiélago en que se halla la isla de San Andrés (Santos-Martínez, 2006), la dinámica del carbono y el flujo de nutrientes en los ecosistemas de manglar puede afectarse notablemente tras la repentina incidencia de estos fenómenos naturales, a causa del desprendimiento de grandes cantidades de materia vegetal que liberarían altas cantidades de N y P en los primeros meses siguientes al disturbio (Romero et al., 2005). Conocer que la formación y acumulación de turba en sistemas de humedales tropicales es heterogénea en términos espaciales y temporales y actuar en consecuencia, promoviendo investigaciones relacionadas con la dinámica de la producción y descomposición vegetal que incorporen factores abióticos y bióticos, encaminaría hacia la escogencia de alternativas más propicias en el manejo de estos ecosistemas costeros que no sólo enfrentan disturbios antrópicos constantes sino también eventuales disturbios naturales a gran escala. Los resultados de este estudio tienen implicaciones en la comprensión y predicción de los patrones de acumulación y distribución de la materia orgánica en las islas caribeñas tropicales y por ende en la toma de decisiones locales enfocadas en la protección y explotación racional del valioso recurso que constituyen los humedales de manglar, lo que repercutirá indudablemente sobre las tierras internas que protege este ecosistema.
AGRADECIMIENTOS
Los autores agradecen a Jairo Medina y Peter Lowy por el soporte logistico y los útiles comentarios durante la ejecución de la investigación. El estudio fue apoyado económicamente por el proyecto "Evaluación y seguimiento de los impactos sociales, económicos y ambientales del huracán Beta en la islas de Providencia y Santa Catalina, Caribe colombiano" (código HERMES-UNAL 5344), enmarcado en la iniciativa de Fortalecimiento de las Sedes de Presencia Nacional de la Universidad Nacional de Colombia.
BIBLIOGRAFÍA
1 Alongi D. 1990. Abundances of benthic microfauna in relation to outwelling of mangrove detritus in a tropical coastal region. Mar Ecol. Prog. Ser., 63: 53-63. [ Links ]
2 Alongi, D. 2002. Present state and future of the world's mangrove forests. Environ. Conserv. 29 (3): 331-349. [ Links ]
3 Barriga, E. B., J. C. Hernández., I. T. Jaramillo., R. M. Jaramillo., L. E. Mora., P. E. Pinto y P. M. Ruiz. 1969. La isla de San Andrés: contribuciones al conocimiento de su ecología, flora, fauna y pesca. Dirección de Divulgación Cultural. Universidad Nacional de Colombia, Bogotá. 152 p. [ Links ]
4 Benner, R., R. E. Hodson y D. Kirchman. 1988. Bacterial abundance and production on mangrove leaves during initial stages of leaching and biodegradation. Arch. Hydrobiol., 31: 19-26. [ Links ]
5 Boonruang, P. 1978. The degradation rates of mangrove leaves of Rhizophora apiculata (B1.) and Avicennia marina (Forsk.) Vierh. at Phuket Island, Thailand. Phuket Mar. Biol. Center. Res. Bull., 29: 1-6. [ Links ]
6 Cahoon, D. R. y J. C. Lynch. 1997. Vertical accretion and shallow subsidence in a mangrove forest of southwestern Florida, U. S. A. Mangroves Salt Marshes, 1: 173-186. [ Links ]
7 Cameron, C. C. y C. A. Palmer. 1995. The mangrove peat of the Tobacco Range islands, Belize Barrier Reef, Central America. Atoll Res. Bull., 431: 1-32. [ Links ]
8 Camilleri, J. C. y G. Ribi. 1986. Leaching of dissolved organic carbon [DOC] from dead leaves, formation of flakes from DOC, and feeding on flakes by crustaceans in mangroves. Mar. Biol., 91: 337-344. [ Links ]
9 Emmerson, W. D. y L. E. McGwynne. 1992. Feeding and assimilation of mangrove leaves by the crab Sesarma meinerti de Man in relation to leaf-litter production in Mgazana, a warm-temperate southern African mangrove swamp. J. Exp. Mar Biol. Ecol., 157: 41-53. [ Links ]
10 Escallón, C. y M. Rodríguez. 1986. Aspectos geográficos e importancia ecológica de los manglares con especial referencia a Colombia. Pérez-Arbelaezia, 1 (2): 225-241. [ Links ]
11 Farnsworth, E. J. y A. M. Ellison. 1997. The global conservation status of mangroves. Ambio, 26: 328334. [ Links ]
12 Flores-Verdugo, F. J., J. W. Jr. Day y R. Briseño-Dueñas. 1987. Structure, litter fall, decomposition and detritus dynamics of mangroves in a Mexican coastal lagoon with an ephemeral inlet. Mar Ecol. Prog. Ser., 35: 83-90. [ Links ]
13 García, I. y J. F. Gaviria. 1996. Estudio de los manglares de San Andrés isla: extensión y distribución, estructura, productividad, degradación de hojas y otros análisis. Tesis Biol. Mar., Univ. Jorge Tadeo Lozano, Bogotá. 200 p. [ Links ]
14 Glaser, P. H. 1987. The ecology of patterned boreal peatlands of northern Minnesota: a community profile. Biological Report, 85 (7.14). U.S. Fish and Wildlife Service, Washington, District of Columbia, EE. UU. 98 p. [ Links ]
15 Gornitz, V. 1995. Sea-level rise: a review of recent past and near-future trends. Earth Surf. Process Landf., 20: 7-20. [ Links ]
16 Harmon, M. E., K. J. Nadelhoffer y J. M. Blair 1999. Measuring decomposition, nutrient turnover, and stores in plant litter. 202-240. En: Robertson, G. P., D. C. Coleman, C. S. Bledsoe y P. Sollins (Eds. ). Standard soil methods for long-term ecological research. Oxford University Press, Nueva York. 462 p. [ Links ]
17 Hatcher B. G., R. E. Johannes y A. I. Robertson. 1989. Review of research relevant to the conservation of shallow tropical marine ecosystems. Oceanogr. Mar. Biol. An. Rev., 27: 337-414. [ Links ]
18 Hubach, E. 1956. Aspectos geográficos y geológicos y recursos de las islas de San Andrés y Providencia. Bol. Soc. Geog. Colomb., 12. 37 p. [ Links ]
19 IDEAM, 1995. Datos de las variables climáticas de la isla de San Andrés, Providencia y Santa Catalina. Instituto de Hidrología, Meteorología y Estudios Ambientales, Santafé de Bogotá. 70 p. [ Links ]
20 IGAC. 1986. San Andrés y Providencia: aspectos geográficos. Instituto Geográfico Agustín Codazzi, Bogotá. 156 p. [ Links ]
21 IGAC. 1992. Atlas de Colombia. Instituto Geográfico Agustín Codazzi, Santafé de Bogotá. 321 p. [ Links ]
22 Kathiresan, K. 1992. Foliovory in Pichavaram mangroves. Environ. Ecol., 10 (4): 988-989. [ Links ]
23 Kathiresan, K. y B. L. Bingham. 2001. Biology of mangroves and mangrove ecosystems. Adv. Mar. Biol., 40: 84-193. [ Links ]
24 Lacerda, L. D., V. Ittekkot y S. R. Patchineelam. 1995. Biogeochemistry of mangrove soil organic matter: a comparison between Rhizophora and Avicennia soils in south-eastern Brazil. Estuar Coast. Shelf Sci., 40: 713-720. [ Links ]
25 Macintyre, I. G., M. M. Littler y D. S. Littler. 1995. Holocene history of Tobacco Range, Belize, Central America. Atoll. Res. Bull., 430: 1-18. [ Links ]
26 Mackey, A. P. y G. Smail. 1996. The decomposition of mangrove litter in a subtropical mangrove forest. Hydrobiologia, 332: 93-98. [ Links ]
27 Mancera, J. E. 2003. The contribution of mangrove outwelling to coastal food webs as a function of environmental settings. Tesis doctoral, University of Louisiana at Lafayette, Lafayette, EE. UU. 8 p. [ Links ]
28 Márquez, G., M. E. Pérez., A. D. Britton., J. Archbold y C. Newball. 2006. El Archipiélago posible: Ecología, reserva de biosfera y desarrollo sostenible en San Andrés, Providencia y Santa Catalina (Caribe occidental colombiano). Universidad Nacional de Colombia. Bogotá. 136 p. [ Links ]
29 Micheli, F. 1993. Feeding ecology of mangrove crabs in North Eastern Australia: mangrove litter consumption by Sesarma messa and Sesarma smithi. J. Exp. Mar Biol. Ecol., 171: 165-186. [ Links ]
30 Middleton, B. A. y K. L. McKee. 2001. Degradation of mangrove tissues and implications for peat formation in Belizean island forest. J. Ecol., 89: 818-828. [ Links ]
31 Mitsch, W. J. y J. G. Gosselink. 1993. Wetlands. Van Nostrand Reinhold, Nueva York. 154 p. [ Links ]
32 Primavera, J. H. 2005. Mangroves, fishponds, and the quest for sustainability. Science, 310 (5745): 57-59. [ Links ]
33 Robertson, A. I. 1986. Leaf-burying crabs: their influence on energy flow and export from mixed mangrove forest (Rhizophora spp.) in northeastern Australia. J. Exp. Mar Biol. Ecol., 102: 237-248. [ Links ]
34 Robertson, A. I. 1988. Decomposition of mangrove leaf litter in tropical Australia. J. Exp. Mar. Biol. Ecol., 116: 235-247. [ Links ]
35 Romero, L. M., T. J. Smith y J. W. Fourqurean. 2005. Changes in mass and nutrient content of wood during decomposition in a south Florida mangrove forest. J. Ecol., 93: 618-631. [ Links ]
36 Santos-Martínez, A. 2006. Evaluación y seguimiento de los impactos sociales, económicos y ambientales del huracán Beta en las islas de Providencia y Santa Catalina, Caribe colombiano. Proyecto de Investigación, Universidad Nacional de Colombia - Sede Caribe, Instituto de Estudios Caribeños -Vicerrectoría de Investigaciones, San Andrés. 20 p. [ Links ]
37 Sessegolo, G. C. y P. C. Lana. 1991. Decomposition of Rhizophora mangle, Avicennia schaueriana and Laguncularia racemosa leaves in a mangrove of Paranagua Bay (Southeastern Brazil). Bot. Mar., 34: 285-289. [ Links ]
38 Sokal, R. R. y F. J. Rohlf. 1981. Biometry. W. H. Freeman, Nueva York. 832 p. [ Links ]
39 Spackman, W., C. P. Dolsen y W. Riegel. 1966. Phytogenicorganic sediments and sedimentaryenvironments in the Everglades-mangrove complex Part 1 - Evidence of a transgressing sea and its effect on environments of the Shark River area of southwest Florida. Phalaeontografica, B. 17: 135-152. [ Links ]
39 Steinke, T. D., A. D. Barnabas y R. Somaru. 1990. Structural changes and associated microbial activity accompanying decomposition of mangrove leaves in Mgeni Estuary. S. Afr. J. Bot., 56: 39-48. [ Links ]
40 Steinke, T. D., A. Rajh y A. J. Holland. 1993a. The feeding behaviour of the red mangrove crab Sesarma meinerti de Man, 1887 (Crustacea: Decapoda: Grapsidae) and its effect on the degradation of mangrove leaf litter. S. Afr. J. Mar. Sci., 13: 151-60. [ Links ]
41 Steinke, T. D., A. J. Holland y Y. Sing. 1993b. Leaching losses during decomposition of mangrove leaf litter. S. Afr. Tydskr. Plantk., 59: 21-25. [ Links ]
42 Tam, N. F. Y., Y. S. Wong, C. Y. Lan y L. N. Wang. 1998. Litter production and decomposition in a subtropical mangrove swamp receiving wastewater. J. Exp. Mar. Biol. Ecol., 226: 1-18. [ Links ]
43 Twilley, R. R., M. Pozo, V. H. García, V. H. Rivera-Monroy, R. Zambrano y A. Bodero. 1997. Litter dynamics in riverine mangrove forest in the Guayas River estuary, Ecuador. Oecología, 111: 109-122. [ Links ]
44 UNESCO. 1985. The international system of units (SI) in oceanography. UNESCO Technical Papers No, 45. París. 133 p. [ Links ]
45 Wieder, R. K. y G. E. Lang. 1982. A critique of the analytical methods used in examining decomposition data obtained from litter bags. Ecology, 63: 1636-1642. [ Links ]
46 Woitchik, A. F., B. Ohowa, J. M. Kazungu, R. G. Rao, L. Goeyens y F. Dehairs. 1997. Nitrogen enrichment during decomposition of mangrove leaf litter in an East African coastal lagoon (Kenya); relative importance of biological nitrogen fixation. Biogeochemistry, 39 (1): 15-35. [ Links ]
FECHA DE RECEPCIÓN: 10/07/08 FECHA DE ACEPTACIÓN: 16/03/09
* Trabajo presentado en el XVIII Seminario Nacional de Ciencia y Tecnología del Mar "Las ciencias y las tecnologías marinas al servicio del país". Mayo 20 al 23 de 2008. San Andrés isla, Colombia.