Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Boletín de Investigaciones Marinas y Costeras - INVEMAR
Print version ISSN 0122-9761
Bol. Invest. Mar. Cost. vol.38 no.2 Santa Marta July/Dec. 2009
NOTA:
PRESENCIA DE REMORINA ALBESCENS (PERCIFORMES: ECHENEIDAE) EN EL CARIBE COLOMBIANO, INCLUYENDO UNA CLAVE DE IDENTIFICACIÓN PARA LAS ESPECIES DE LA FAMILIA EN COLOMBIA
OCCURRENCE OF REMORINA ALBESCENS (PERCIFORMES: ECHENEIDAE) IN THE COLOMBIAN CARIBBEAN, INCLUDING A TAXONOMIC KEY FOR SPECIES OF THE FAMILY IN COLOMBIA
Edwin Farfán López1, Arturo Acero P.2 y Marcela Grijalba-Bendeck1
1Universidad de Bogotá Jorge Tadeo Lozano, Facultad de Ciencias Naturales, Programa de Biología Marina. Edificio Mundo Marino, Carrera 2 No. 11-68, El Rodadero - Santa Marta, Colombia, egofar@gmail.com (E.F.L.), marcela.grijalba@utadeo.edu.co (M.G.B.)
2Universidad Nacional de Colombia sede Caribe, CECIMAR/INVEMAR, Cerro Punta Betín, Santa Marta, Colombia, aacero@invernar.org.co
ABSTRACT
The presence of Remorina albescens for the Colombian Caribbean is confirmed, based on a specimen of 165.91 mm of standard length collected in Nenguanje bay at the Tayrona National Natural Park. A taxonomic key for the remoras known from Colombian seas is also included.
KEY WORDS: White suckerfish, Echeneidae, Colombian Caribbean.
Los miembros de la familia Echeneidae, llamados comúnmente remoras, se caracterizan por presentar dos aletas dorsales, la primera modificada en un disco en forma de óvalo situado en la parte superior de la cabeza y origen del tronco. En esta estructura cada lepidotriquia está transformada en una lámina transversal colocada simétricamente a los lados de la cresta media y de un reborde externo; pudiéndose encontrar de 10 a 28 láminas por disco según la especie (Nelson, 2006). El disco les permite adherirse a animales de gran tamaño como tiburones, rayas, tortugas y mamíferos marinos, los cuales usa como transporte, protección y, en la mayoría de los casos, para obtener alimento que se basa en restos de comida o parásitos de sus simbiontes, presentándose en algunas especies de remoras una alta selectividad por su hospedero. El cuerpo es fusiforme, con un cráneo muy deprimido y ancho que proporciona un soporte adecuado para el disco. La mandíbula es prominente con dientes de forma de cepillo, al igual que el vómer, facilitándoles la captura de sus presas (Cervigón, 1993).
La familia Echeneidae se encuentra representada en las aguas colombianas por ocho especies de las subfamilias Echeneinae y Remorinae, la primera incluye los géneros Phtheirichthys y Echeneis, y a la segunda corresponden Remorina y Remora, donde la mayoría de estas especies tiene una amplia distribución en los mares cálidos del mundo. En Colombia se encuentran en el Caribe Echeneis neucratoides, en el Pacífico P. lineatus, Remorina albescens, Remora australis, R. osteochir y R. brachyptera, mientras que E. naucrates y R. remora se encuentran en ambos mares (Franke y Acero, 1990). Este trabajo presenta el primer registro de R. albescens para el Caribe colombiano, la cual fue hallada previamente en el Pacífico por Franke y Acero (1990).
El espécimen se encuentra depositado en la colección de peces de la Universidad de Bogotá Jorge Tadeo Lozano, Santa Marta. Se realizaron contajes de todas las aletas y las medidas fueron tomadas con un calibrador electrónico, siguiendo los criterios de Collette (2002). Su identificación como especie se llevó a cabo con diferentes claves taxonómicas, como las propuestas por Franke y Acero (1990), Cervigón (1993) y Collette (2002).
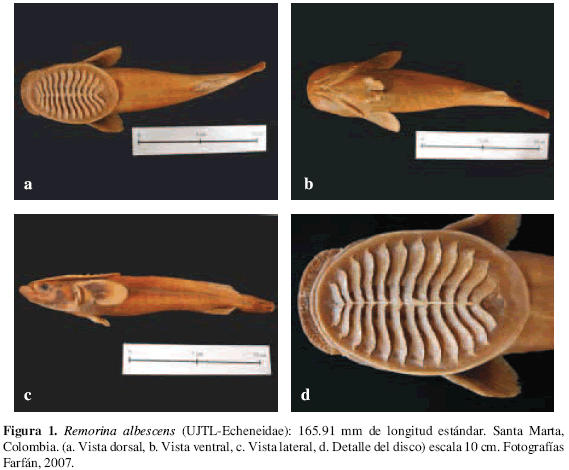
Remorina albescens (Temminck y Schlegel) (Figura 1)
Echeneis albescens Temminck y Schlegel en Siebold, Fauna Japónica, 14: 272, 1850 (Nagasaki, Japón); Day (1878-1888): 258; Cadenat (1950): 265.
Remora albescens, Lozano y Rey (1960): 11-12.
Remorina albescens, Cervigón (1966): 945; Cressey y Lachner (1970): 315-316; Miller y Lea (1972): 144; Martin y Drewry (1978): 239-240; López y Bussing (1982): 16; Eschmeyer et al. (1983): 205; Heemstra (1986): 664; Lachner (1986): 1334; Robins etal. (1986): 158-159; Frankey Acero (1990): 23-30; Cervigón (1993): 47-53; Collette (2002): 1414-1419.
Nombres comunes: Remora blanca, white suckerfish.
Material examinado: Un ejemplar de 165.91 mm de longitud estándar (LE) (UJTL- Echeneidae), recolectado el 10/II/1993 en la bahía de Nenguanje, Parque Nacional Natural Tayrona, Caribe colombiano.
Caracteres merísticos: El individuo presenta 16 radios en la segunda dorsal, 15 en la pectoral, 22 en la anal, una espina y cuatro radios blandos en las pélvicas y 12 láminas en el disco. Según Franke y Acero (1990) y Cervigón (1993), hay una dorsal sin espinas con 16 a 23 radios, anal sin espinas y 21 a 26 radios blandos, pectoral con 16 a 21 radios blandos y 12 a 14 láminas en el disco.
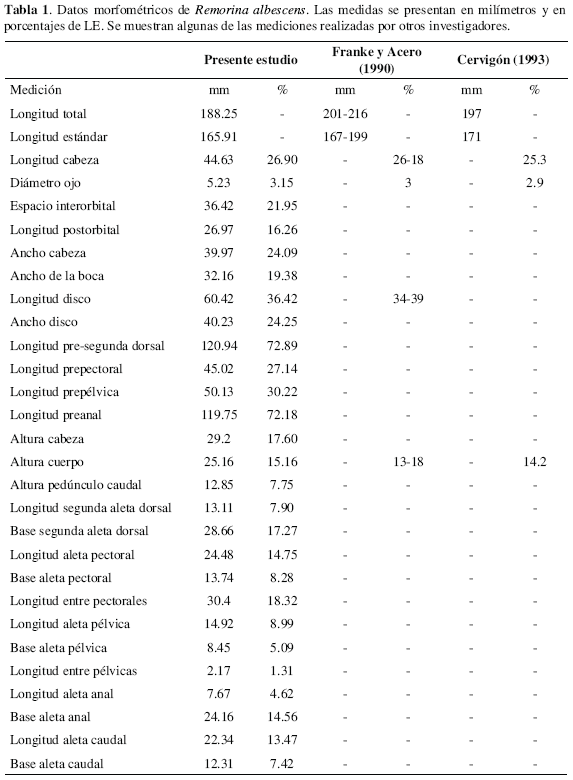
Caracteres morfométricos: La morfometría del ejemplar estudiado se presenta en la Tabla 1.
Coloración: Blanco a gris pálido, en algunos casos con tonalidades amarillas; incluyendo el disco y las aletas; cuerpo más claro hacia la parte dorsal (Cervigón, 1993). En etanol el cuerpo es de color amarillento, más claro en la parte ventral.
Caracteres distintivos: Cuerpo relativamente corto, fusiforme, aletas pélvicas unidas al abdomen por su base, pectorales grandes (Cervigón, 1993). El género es mono típico.
Talla: LE máxima 300 mm (Franke y Acero, 1990).
Hábitat: Pelágicos, marinos, tropicales y subtropicales (Riede, 2004), sus principales simbiontes son mantarrayas (Mobula hypostoma y Manta birostris), pero ocasionalmente se adhiere a tiburones (Sphyrna tudes) (Lozano y Rey, 1960). Se puede encontrar dentro de la cavidad branquial o en la boca de sus simbiontes, también se adhiere al marlín negro (Makaira indica) en la región del Indo Pacífico (Robins et al., 1986) y rara vez se halla nadando libremente (Lachner y Post, 1990).
Distribución: A nivel mundial es una especie conocida de todos los trópicos (Fricke, 1999). En el Atlántico occidental se distribuye desde Florida y el Golfo de México hasta Brasil (Robins et al., 1986), llegando hasta las Rocas de San Pedro y San Pablo en el Atlántico ecuatorial al noreste de Brasil (Lubbock y Edwards, 1981). Presente en el Indico oriental (Fricke, 1999) y en el Pacífico oriental desde San Francisco en California hasta Chile (Eschmeyer et al, 1983), mientras que para el Pacífico colombiano se encuentra en Isla de Gorgona (Franke y Acero, 1990).
CLAVE PARA LAS ESPECIES DE LA FAMILIA ECHENEIDAE PRESENTES EN LOS MARES COLOMBIANOS (Modificada de Robins y Ray, 1986; Franke y Acero, 1990; Cervigón, 1993; Colleté, 2002)
1 a. Cuerpo muy alargado, su altura contenida de 8 a 14 veces en la LE; con 9 a 28 láminas en el disco suctor; aletas pectorales puntiagudas, usualmente con una banda longitudinal oscura a cada lado del cuerpo bordeada de blanco; anal de base larga con 29 a 41 radios blandos; caudal lanceolada en individuos juveniles con radios centrales filamentosos y truncada en adultos (subfamilia Echeneinae).......... 2
1 b. Cuerpo no alargado, su altura contenida de 5 a 8 veces en la LE; 12 a 28 láminas en el disco; pectorales redondeadas y unidas al abdomen; color relativamente uniforme, sin bandas; anal de base corta con 18 a 28 radios; caudal bifurcada en individuos juveniles que es recta o truncada en adultos (subfamilia Remorinae).......... 3
2 a. Disco pequeño con 9 a 11 láminas y 39 a 41 vértebras (dorsal con 29 a 40 radios, anal con 29 a 38 y pectoral con 17 a 21). Asociada a barracudas (S. barracuda) y tortugas (L. olivacea), alcanza 760 mm pero normalmente sólo 450 mm.......... Phtheirichthys lineatus
2 b. Disco grande, con 18 a 28 láminas y 30 vértebras (Echeneis).......... 4
3 a. Aletas pélvicas sólo unidas al abdomen por su base peduncular; 12 a 14 láminas en el disco; 26 vértebras; 16 a 23 radios en la dorsal. Color blanquecino, huésped de mantas.......... Remorina albescens
3 b. Aletas pélvicas ampliamente unidas al abdomen; 14 a 28 láminas en el disco; 27 vértebras; 20 a 34 radios en la dorsal. Color café claro a oscuro, asociada con tiburones y cetáceos (Remora).......... 5
4 a. Disco usualmente con 23 láminas; coloración pálida con las puntas de la dorsal, anal y caudal blancas; modalmente dorsal con 39 radios y anal con 36 a 37; longitud del disco 29 % de la LE.......... Echeneis naucrates
4 b. Con 21 láminas en el disco; coloración blanca; modalmente dorsal con 35 radios y anal con 32; longitud del disco 26 % de LE.......... Echeneis neucratoides
5 a. Con 28 a 37 branquiespinas en el primer arco branquial (disco suctor con 16 a 20 láminas; 21 a 27 radios en la dorsal y 25 a 27 en la pectoral). Longitud del disco menos de la mitad de la longitud del cuerpo. Borde posterior del disco situado delante de los extremos de las aletas.......... Remora remora
5 b. De 11 a 20 branquiespinas en el primer arco branquial.......... 6
6 a. Disco con 24 a 28 láminas; 17 a 20 branquiespinas en el primer arco branquial, longitud del disco casi la mitad de la longitud del cuerpo. Usualmente viven con cetáceos.......... Remora australis
6 b. Con 14 a 19 láminas en el disco; con 11 a 21 branquiespinas; longitud del disco menor que la mitad de la longitud del cuerpo.......... 7
7 a. Borde posterior del disco situado delante de los extremos de las aletas pectorales, longitud del disco 28 a 40 % de la LE, con 14 a 17 láminas; dorsal con 27 a 34 radios, pectoral 23 a 27; número total de branquiespinas en el primer arco branquial menor a 21.......... Remora brachyptera
7 b. Borde posterior del disco situado muy por detrás de los extremos de las aletas pectorales cuando estas están pegadas al cuerpo, longitud del disco corresponde del 37 al 45 % de la LE, con 17 a 19 láminas; dorsal con 21 a 27 radios, pectoral con 20 a 24; con 11 a 13 branquiespinas en el primer arco branquial.......... Remora osteochi
AGRADECIMIENTOS
A la Universidad de Bogotá Jorge Tadeo Lozano sede Santa Marta, por facilitar el material estudiado que se encuentra depositado en su colección ictiológica y el apoyo logístico a este trabajo. Contribución 021 del Grupo de Investigación en Peces del Caribe GIPECA del Programa de Biología Marina.
BIBLIOGRAFÍA
1 Cervigón, F. 1966. Los peces marinos de Venezuela Tomo II. Fund. La Salle Cien. Nat., Monografía 12: 449-951. [ Links ]
2 Cervigón, F. 1993. Los peces marinos de Venezuela Volumen II. Segunda edición. Fund. Cien. Los Roques. Monografía 12, Venezuela. 502 p. [ Links ]
3 Collete, B. 2002. The living marine resources of the Western Central Atlantic. FAO y American Society of Ichthyologists and Herpetologists, Roma, 3: 1414-1419. [ Links ]
4 Cressey, F. y A. Lachner. 1970. The parasitic copepod diet and life history of diskfishes (Echeneidae). Copeia 2: 310-318. [ Links ]
5 Eschmeyer, N., S. Herald y H. Hammann. 1983. A field guide to the Pacific coast fishes of North America. Houghton Mifflin, Boston. 336 p. [ Links ]
6 Franke, R. y A. Acero P. 1990. Remoras (Pisces: Echeneidae) conocidas de los mares colombianos. Bol. Ecotrópica, 23: 23-30. [ Links ]
7 Fricke, R. 1999. Fishes of the Mascarene Islands: an annotated checklist, with descriptions of new species. Koeltz Scientific Books, Koenigstein, Theses Zoologicae, 2 (31): 759 p. [ Links ]
8 Lachner, E. 1986. Echeneididae. In fishes of the North-eastern Atlantic and the Mediterranean. UNESCO, 3: 1329-1334. [ Links ]
9 Lachner, E. y A. Post. 1990. Echeneidae. 725-728. En: Quero, J., C. Hureau, A. Karrer, A. Post y L. Saldaña. Check-list of the fishes of the eastern tropical Atlantic. Vol. 2. JNICT, SEI y UNESCO, Paris. 1524 p. [ Links ]
10 López, M y A. Bussing. 1982. Lista provisional de los peces marinos de la costa Pacífica de Costa Rica. Biología Tropical 30 (1): 5-26. [ Links ]
11 Lozano, L y Rey. 1960. Peces fisoclistos. Subserie torácicos. Tercera parte. Serie de Ciencias Naturales. Tomo XIV. Memorias de la Real Academia de Ciencias Exactas, Físicas y Naturales de Madrid, Madrid. 693 p. [ Links ]
12 Lubbock, R. y Edwards, A. 1981. The fishes of Saint Paul's Rocks. J. Fish Biol., 18: 135-157. [ Links ]
13 Martin, J. y E. Drewry. 1978. Development of fishes of the Mid-Atlantic Bight. Volume III. Stromateidae through Ogcocephalidae. Institute Fish Wildlife Service, Washington D.C. 424 p. [ Links ]
14 Miller, J. y L. Lea. 1972. Guide to the coastal marine fishes of California. California Department Fish and Game. Fish Bull, 157: 235 p. [ Links ]
15 Nelson, J. 2006. Fishes of the world. Cuarta edición. John Wiley y Sons, Inc., Hoboken, New Jersey, EE. UU. 624 p. [ Links ]
16 Riede, K. 2004. Global register of migratory species from global to regional scales. Final report of the R y D. Federal Agency for Nature Conservation, Bonn, Alemania. 329 p. [ Links ]
17 Robins, C. R. y G. Ray. 1986. A field guide to Atlantic coast fishes of North America. Houghton Mifflin Company, Boston. 354 p. [ Links ]
FECHA DE RECEPCIÓN: 10/11/08 FECHA DE ACEPTACIÓN: 22/10/09