Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Boletín de Investigaciones Marinas y Costeras - INVEMAR
Print version ISSN 0122-9761
Bol. Invest. Mar. Cost. vol.40 supl.1 Santa Marta Dec. 2011
DIVERSIDAD, ABUNDANCIA Y AMENAZAS DE LOS OCTOCORALES DE LA ISLA MALPELO, PACÍFICO ORIENTAL TROPICAL, COLOMBIA
DIVERSITY, ABUNDANCE, AND THREATS OF OCTOCORALS AT MALPELO ISLAND, TROPICAL EASTERN PACIFIC, COLOMBIA
Juan A. Sánchez, Carlos E. Gómez, Dairo Escobar y Luisa F. Dueñas
Universidad de los Andes, Facultad de Ciencias, Departamento de Ciencias Biológicas, Laboratorio de Biología Molecular Marina BIOMMAR, Carrera 1E No 18A-10, Bogotá, Colombia. juansanc@uniandes.edu.co (J.A.S.), gomezcar76@gmail.com (C.E.G.), dairoescobar@gmail.com (D.E.), lf.duenas161@uniandes.edu.co (L.F.D.).
RESUMEN
Durante expediciones a la isla Malpelo en 2009 y 2010, se exploró la diversidad, abundancia y estado de los octocorales. Se encontraron siete especies de octocorales: Leptogorgia alba, Pacifigorgia cf. lacerata, Pacifigorgia sp.1 y Pacifigorgia sp.2, Muricea cf. fruticosa, Muricea sp. y la especie invasora Carijoa riisei. Los octocorales forman densas agregaciones en paredes y escarpes rocosos, con su mayor abundancia entre 10 y 20 m, alcanzando densidades máximas de hasta 20 colonias m-2. La especie más abundante fue Pacifigorgia cf. lacerata, con más de un 60 % de predominio en número y una frecuencia de aparición del 100 % para todos los sitios visitados. Para la mayoría de los sitios se determinó la existencia de tres zonas bien definidas de acuerdo a la profundidad. Una zona profunda entre 25 y 40 m, con dominancia exclusiva de L. alba, una estructura somera entre 7 y 20 m, con dominancia de Pacifigorgia spp. y una zona de transición comprendida entre 18 y 25 m, con una mezcla de L. alba y P. cf. lacerata, principalmente. De manera sorpresiva, durante noviembre de 2009 se encontraron poblaciones de Pacifigorgia y Leptogorgia visiblemente afectadas por enfermedades de posible origen fúngico. Después, en febrero de 2010, se visitaron de nuevo las mismas poblaciones de octocorales, en las que se constató una mortalidad de hasta 66 % de las colonias en algunas localidades. Leptogorgia se encontró notablemente menguada en el sector de El Arrecife, mientras que Pacifigorgia cf. lacerata tuvo mortalidades destacadas en La Nevera y El Freezer, y sus colonias se recuperaron en el sector de El Arrecife. Se encontró una disminución drástica de la incidencia de enfermedades para julio 2010, con porcentajes de colonias enfermas menores al 10 %. La especie invasora C. riisei fue observada en La Catedral y el bajo del Monstruo. De esta forma, este estudio amplía considerablemente el conocimiento sobre los octocorales de la isla Malpelo, y es la primera alarma sobre posibles amenazas a sus poblaciones locales, como lo son las enfermedades fúngicas y el octocoral invasor C. riisei.
PALABRAS CLAVE: Malpelo, Octocorales, Enfermedades coralinas, Especie invasora.
ABSTRACT
During three expeditions to the island (2009 and 2010), the diversity, abundance and status of octocorals were explored. Seven species of octocorals were recorded: Leptogorgia alba, Pacifigorgia cf. lacerata, Pacifigorgia sp.1 y Pacifigorgia sp.2, Muricea cf. fruticosa, Muricea sp., and the invasive species Carijoa riisei. Octocorals form dense aggregations in rocky walls and cliffs, with higher abundances between 10 and 20 m, reaching up to 20 colonies m-2. The most abundant species was Pacifigorgia cf. lacerata with a dominance of more than 60 % and a frequency of occurrence of 100 % for all visited sites. According to depth, three well-defined zones were determined for most sites. A deep zone between 25 and 40 m with an exclusive dominance of L. alba, a shallow assemblage between 7 and 20 m dominated by Pacifigorgia spp., and a transition zone between 18 and 25 m with a mixture of L. alba and P. cf. lacerata. Surprisingly, during November 2009, diseases of possible fungal origin visibly affected populations of Leptogorgia and Pacifigorgia. Subsequently, during February 2010 the same populations of octocorals were monitored and up to 66 % of the colonies were already dead in some locations. Leptogorgia had a significant reduction at El Arrecife site, while Pacifigorgia cf. lacerata had high mortality at La Nevera and El Freezer sites, and a recovery in El Arrecife. There was a notable improvement in disease prevalence by July 2010 with less than 10 % of diseased colonies. The invasive species C. riisei was observed in La Catedral and El Monstruo bank. Thus, this information increases considerably the knowledge of octocorals on Malpelo Island and is the first warning of possible threats against local octocoral populations, such as fungal diseases and the invasive octocoral C. riisei.
KEY WORDS: Malpelo, Octocorals, Coral diseases, Invasive species.
INTRODUCCIÓN
Los arrecifes coralinos y rocosos son los ecosistemas marinos más complejos de la tierra y una fuente importante de recursos para muchos países alrededor del mundo que dependen económicamente de sus beneficios (Birkeland, 1997). Los octocorales son uno de los grupos más diversos y con más especies asociadas en los arrecifes coralinos y litorales tropicales, donde proporcionan refugio a una gran cantidad de organismos como moluscos, crustáceos, poliquetos, equinodermos y peces, entre otros (Bayer, 1961; Sánchez et al., 1998). Los octocorales son un componente característico de las aguas tropicales someras de ambas costas de América. A diferencia del Indopacífico, que alberga cientos de corales pétreos (escleractínios) y corales blandos, en el Pacífico Oriental Tropical-POT hay poco desarrollo de corales escleractínios, con menos de 20 especies descritas y una carencia de corales blandos. Sin embargo, para el POT la fauna de octocorales se caracteriza por una gran diversidad de especies y formas, superando las 60 especies descritas (VanOppen et al., 2005). A pesar de la gran diversidad que presentan y de la fauna asociada que albergan, los octocorales, al igual que todo el ecosistema arrecifal, atraviesan por una crisis sin precedentes, tanto por el cambio climático global como por los efectos antropogénicos a los que se ven sometidos (e.g., Knowlton y Jackson, 2008; Mora, 2008).
Una de las principales problemáticas ambientales en la actualidad es la invasión de especies foráneas, que generalmente tienen efectos adversos sobre la biodiversidad nativa (Sax et al., 2005). Carijoa riisei es un octocoral que se presume originario del mar Caribe y que fue introducido al Pacífico por medio de aguas de lastre (Kahng y Grigg, 2005). Habita en ambientes arrecifales y sobre superficies recientemente sumergidas, como barcos o pilares de muelles (Sánchez, 1994), y su alimentación es de tipo generalista (Lira et al., 2009), lo que le confiere una gran ventaja en los nuevos ambientes colonizados. Adicionalmente, su tasa de crecimiento lineal es alta, excediendo 1 cm por semana (Kahng y Grigg, 2005), y presenta una rápida maduración sexual (Kahng et al., 2008). Durante los años 70’s esta especie fue registrada por primera vez en Hawaii, y desde entonces se ha considerado una peste, ya que compite eficientemente por el espacio, desplazando a la fauna nativa, incluso a aquellos organismos de interés económico (Kahng y Grigg, 2005). Las anteriores características hacen de Carijoa un competidor fuerte frente a las especies nativas, por lo tanto una amenaza para la biodiversidad de los arrecifes.
Recientemente, estudios centrados en el cambio global han dado a conocer los posibles impactos del aumento del CO2 atmosférico que repercute directamente en el CO2 de ambientes marinos. Los efectos más graves del incremento del CO2 son la acidificación oceánica y el calentamiento del agua, factores que tienen un mayor efecto sobre organismos marinos calcificadores, como lo son los corales y octocorales (Hoegh-Guldberg et al., 2007). Por su parte, para entender la acidificación oceánica es importante tener en cuenta que los océanos son importantes en la dinámica del CO2 atmosférico, al actuar como secuestradores y almacenadores de este gas, manteniendo un balance océano-atmósfera (The Royal Society, 2005; Kleypas y Langdon, 2006). No obstante, el CO2 antropogénico ha estado acumulándose en la atmósfera por más de un siglo, creando un desbalance en la química marina (Caldeira y Wickett, 2003; Feely et al., 2004) y causando una disminución del pH en el agua (Kleypas et al., 1999; Caldeira y Wickett, 2003; Sabine et al., 2004; Kleypas et al., 2006). Es probable que la saturación del carbonato esté afectando los procesos de calcificación en organismos marinos que dependen de los carbonatos para la elaboración de sus estructuras esqueléticas (Gattuso et al., 1998; Riebesell et al., 2000; Clarke y Warwick, 2003; Orr et al., 2005; Gazeau et al., 2007). Extrapolaciones a partir de estudios previos sugieren que las tasas de calcificación decrecerán hasta un 60 % en el transcurso del presente siglo y, particularmente para los corales, la disminución sería de 10-30 % bajo condiciones que simulan el doble de la concentración de CO2 actual (Gattuso et al., 1998; Langdon et al., 2000; Marubini et al., 2001).
Otra de las principales consecuencias del incremento del CO2 atmosférico es el aumento en la temperatura oceánica (Hoegh-Guldberg et al., 2007). Relacionado con éste, podemos citar consecuencias directas sobre los corales y octocorales como el blanqueamiento coralino y el incremento en la incidencia de enfermedades de origen bacteriano, viral o fúngico (Rosenberg y Ben-Halm, 2002). Entre los factores de deterioro en los octocorales en las últimas décadas está el caso de Aspergillus sydowii, un hongo de origen terrestre que consume los octocorales provocando mortalidades parciales, totales e incluso poblacionales (Kim et al., 2000; Alker et al., 2001). Esta enfermedad, conocida como aspergilosis, ocasionó en 1983 una gran disminución en la poblaciones de Gorgonia ventalina y G. flabellum de las costas caribeñas continentales de Costa Rica, Panamá y Colombia (Nagelkerken et al., 1997). La aspergilosis se caracteriza por la aparición de manchas circulares con bordes púrpura que, al parecer, son el resultado de un mecanismo de defensa del coral al aumentar la producción de escleritos pigmentados en las zonas afectadas (Smith y Weil, 2004; Sutherland et al., 2004). Adicionalmente, se observa degradación y recesión del cenénquima, exposición del esqueleto y, en algunas ocasiones, aparición de agallas (Smith et al., 1998; Smith y Weil, 2004). Aunque inicialmente se consideró que esta enfermedad era el resultado de una interacción específica entre el hospedero y el patógeno, hoy se conoce que, además de G. ventalina y G. flabellum, otras especies de octocorales pueden verse afectadas por esta patología, aunque su estudio ha sido limitado al mar Caribe (Smith y Weil, 2004). Nuestro grupo de investigación tiene evidencia microbiológica de que en el Pacífico colombiano, incluyendo la costa del Chocó, y las islas de Gorgona y Malpelo, especies de abanicos pertenecientes al género Pacifigorgia están siendo afectadas por esta misma enfermedad.
Efectivamente, entre los sitios estratégicos que se han seleccionado o propuesto para implementar con urgencia estudios de monitoreo se encuentra toda la zona que comprende el POT, donde islas como Malpelo se encuentran dentro de un sector sensible a la acidificación oceánica (Kleypas et al., 2006) y la enfermedad de aspergilosis. Particularmente para la isla Malpelo, el único estudio en donde se mencionan los octocorales se remonta a mas de tres décadas, y en él se mencionan dos especies de octocorales, sólo uno de ellos identificado a nivel de especie (Birkeland et al., 1975). La participación de BIOMMAR (Universidad de los Andes) en los cruceros de investigación (SEASCAPE noviembre 2009, febrero 2010 y julio 2010) tuvo como objetivo implementar un estudio base para el monitoreo de las comunidades octocoralinas de la isla Malpelo, con énfasis en estudios de enfermedades y acidificación oceánica. Los objetivos específicos durante las expediciones fueron: (1) realizar un inventario de los octocorales, sus patrones de distribución y reclutamiento; (2) iniciar un monitoreo de las poblaciones y la salud de los octocorales; (3) establecer un monitoreo de la acidificación oceánica y su efecto en el crecimiento de octocorales.
MATERIALES Y MÉTODOS
Diversidad y abundancia de octocorales
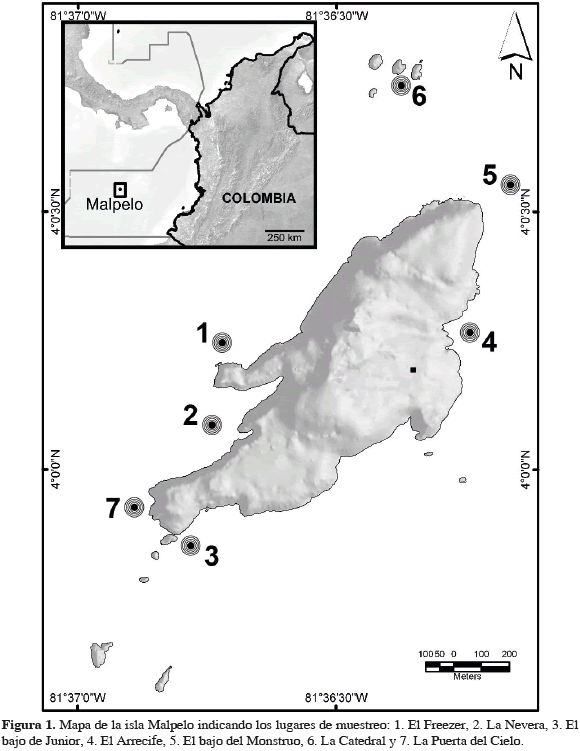
En la isla Malpelo se caracterizaron y monitorearon las comunidades de octocorales en cinco sitios particulares que representan una gran variabilidad de condiciones propicias para el establecimiento y desarrollo de comunidades de octocorales. Por medio de buceo SCUBA se exploraron los siguientes hábitats con fondos duros someros (menores a 30 m de profundidad): El Arrecife, La Nevera, El Freezer, el bajo del Monstruo y el bajo de Junior (Figura 1). En cada lugar se realizaron transectos paralelos y perpendiculares a la línea de costa (Arrecife: tres paralelos y tres perpendiculares; ajo de Junior: dos paralelos y uno perpendicular; Freezer: dos paralelos y uno perpendicular; Nevera: un paralelo y uno perpendicular), de 50 x 0.5 m, con réplicas dentro de cada arrecife y entre arrecifes. En cada transecto, se estimó por medio de foto-cuadrante la abundancia total de organismos por transecto, su densidad promedio (m2 ± error estándar) y la composición de las comunidades de octocorales. De manera selectiva se tomaron pequeñas muestras de tejido, de no más de 1 cm2, para sucesivos análisis de identificación de los ejemplares en el laboratorio mediante análisis de microscopia electrónica, de acuerdo con los métodos empleados por Sánchez (2007). Diferentes colonias, tanto de Pacifigorgia spp. como de Leptogorgia alba, fueron fotografiadas de manera arbitraria, registrando su talla, y teniendo en cuenta su altura y ancho máximos. De la misma manera, se desarrolló un monitoreo independiente de octocorales juveniles menores a 5 cm de altura; (Jamison y Lasker, 2008), registrando su abundancia, densidad y composición. Adicionalmente, se visitó el sitio de buceo La Catedral, con el objetivo de hacer un monitoreo cualitativo de presencia-ausencia del octocoral invasor Carijoa riisei, ya que en ese sitio se había determinado previamente su alta abundancia.
Incidencia de enfermedades
Con ayuda de los foto-cuadrante, a lo largo de los transectos paralelos y perpendiculares de 50 x 0.5 m, se determinó el número de colonias sanas y enfermas (dentro de esta última categoría se tuvo en cuenta aquellas que sólo presentaban signos de pérdida de tejido). Como parte del monitoreo, las colonias marcadas al inicio del estudio fueron permanentemente marcadas con láminas metálicas numeradas, y fueron fotografiadas con una cuadrícula de fondo para estimar su crecimiento y la prevalencia y progresión de la enfermedad. Para este proceso las imágenes fueron segmentadas y cuantificadas con ayuda de ImageJ (NIH). Adicionalmente, se instalaron dos censores de datos para temperatura (termocúpulas: Onset Hobo®) en los sitios de La Nevera y El Freezer, a una profundidad de 15 m, para contar con una medida independiente y constante de la temperatura, que permitiera correlacionarla con las diferentes condiciones de deterioro de los octocorales. Estos almacenadores de datos permiten tomar medidas de temperatura cada 15 minutos, con una capacidad de almacenamiento de hasta un año sin interrupciones.
RESULTADOS
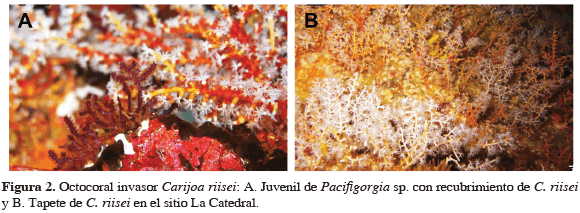
Los octocorales en la isla Malpelo se encuentran por lo general en paredes rocosas con inclinación vertical, donde el fondo está principalmente cubierto por algas coralináceas incrustantes y Balanus peninsularis. Se encontraron seis especies de octocorales para los sectores explorados de la isla: Leptogorgia alba, Pacifigorgia cf. lacerata, Pacifigorgia sp. 1 y sp. 2, Muricea cf. fruticosa, Muricea sp. y Carijoa riisei. Este último octocoral es una especie invasora proveniente del Atlántico, que se observó principalmente en la cueva conocida como La Catedral, donde alcanza coberturas del 100 % entre 7 y 25 m de profundidad (Figura 2). Una pequeña colonia de C. riisei fue observada en la pared del bajo del Monstruo a 27 m. Pacifigorgia sp. es una especie indeterminada aún (posiblemente una nueva especie) que presenta dos morfotipos conspicuos: (1) morfotipo de pólipos blancos y (2) morfotipo de pólipos marrón. Por su parte, Muricea cf. fruticosa es un morfotipo completamente blanco que se encuentra únicamente por debajo de 50 m en el bajo del Monstruo, y Muricea sp. consiste de una única colonia observada en el Freezer a 30 m. L. alba se ubica entre 20 y 40 m hacia zonas de rocas quebradas y más sueltas, mientras Pacifigorgia spp., que son las especies más abundantes, dominan el paisaje de las paredes rocosas entre 5 y 25 m. La abundancia de octocorales se ve interrumpida en zonas con gran desarrollo de corales escleractínios, zonas muy someras con altas densidades de B. peninsularis o en sectores donde el erizo Diadema mexicanum mantiene un halo a su alrededor desprovisto de cualquier invertebrado o alga frondosa.
Estructura de la comunidad de octocorales
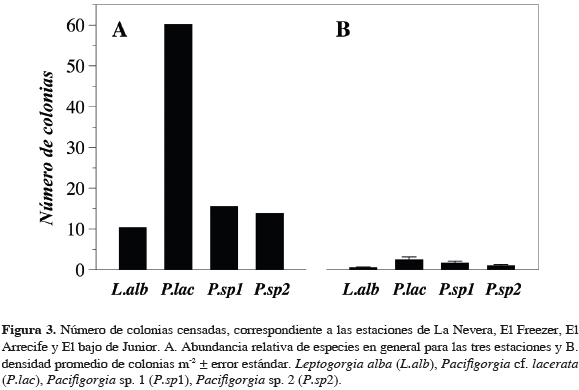
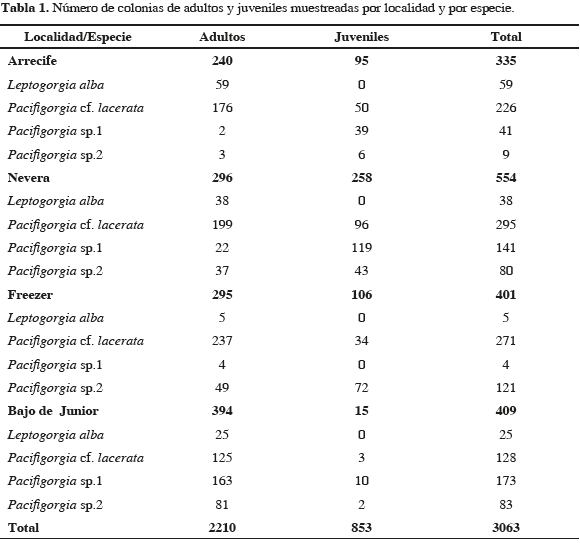
En general, para la totalidad de las estaciones la especie más abundante fue Pacifigorgia cf. lacerata con el 60.2 % (3.94 ± 0.65 col m-2) y la menos abundante fue Leptogorgia alba con el 10.4 % (0.57 ± 0.15 col m-2) (Figura 3). Esta última especie sólo se registró en profundidades superiores a 20 m y se tuvo en cuenta los diferentes morfotipos de Pacifigorgia, que se discriminaron entre morfotipos 1 y 2 (en la gráfica Pacifigorgia sp. 1 y sp. 2, respectivamente). Entre 7 y 20 m, la mayor abundancia de octocorales se registró en el bajo de Junior, seguido por El Freezer (Tabla 1).
Todos los corales juveniles pertenecieron a Pacifigorgia spp., en los cuatro sitios monitoreados. El mayor predominio y abundancia se reportó para P. cf. lacerata (38.61 % de las colonias) con una densidad promedio de 0.34 ± 0.08 col m-2, seguido por Pacifigorgia sp. 1 (dominancia de 35.4 %) con una densidad promedio de 0.34 ± 0.15 col m-2 y Pacifigorgia sp. 2 (25.95 % de las colonias) con una densidad promedio de 0.34 ± 0.06 col m-2 (Tabla 1).
En cuanto a las estaciones de monitoreo, La Nevera presentó la mayor abundancia de juveniles, con un promedio de 64.5 ± 26.4 col/transecto (25 m2), seguida por El Freezer (26.5 ± 2.5 col/transecto) y El Arrecife (23.8 ± 10.6 col/ transecto). La densidad promedio general para todo el estudio fue de 0.91 ± 0.29 colonias m-2.
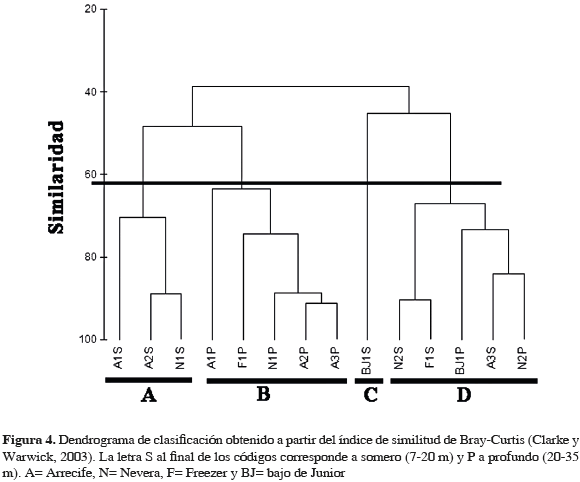
Los transectos perpendiculares de batimetría permitieron definir dos estructuras diferentes de comunidades de octocorales: una profunda (entre 20 y 45 m principalmente), dominada por L. alba y otra somera (entre 7 y 20 m), donde sobresale Pacifigorgia spp. En la Figura 4 se puede observar el resultado del análisis de clasificación a partir del índice de similitud de Bray-Curtis, donde a un nivel de aproximadamente 62 % de similitud se forman tres grupos y una muestra independiente. Los primeros grupos A y B se caracterizaron por presentar una estructura comunitaria bien marcada de acuerdo a la profundidad. El grupo C estuvo conformado por una muestra independiente, que corresponde a la estación del Bajo de Junior, y no se unió a ningún grupo, ya que en la zona comprendida entre 20 y 25 m se encontró una gran abundancia de colonias de Pacifigorgia spp., cambiando de esta forma los valores de similitud entre transectos. Por último, el grupo D reunió cinco transectos y se caracterizó por presentar una mezcla de profundos y someros, sin observarse una estructura muy definida entre estas dos profundidades.
Incidencia de enfermedades
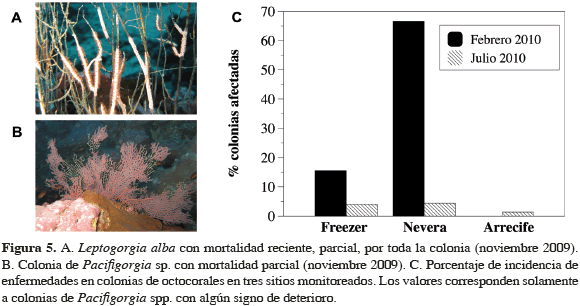
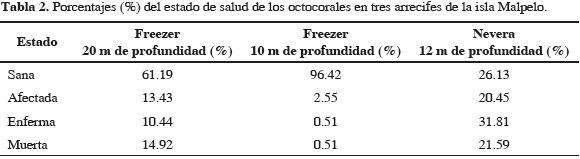
Durante noviembre de 2009 se exploraron las comunidades de octocorales en diversas localidades de la isla Malpelo, y se encontraron dos especies (Leptogorgia alba y Pacifigorgia cf. lacerata) visiblemente afectadas por una enfermedad similar al tipo aspergilosis (Figura 5). Luego, en febrero de 2010 se detectaron mortalidades de hasta 66 % en las colonias de Pacifigorgia spp. En La Nevera incluso se encontraron esqueletos de corales muertos, corales afectados o visiblemente cicatrizados luego de la enfermedad (ver detalles en la Tabla 2). Aunque no dentro de los transectos, también se observaron colonias de L. alba enfermas en noviembre del 2009 y febrero de 2010 (Figura 5).
En los tres sitios monitoreados se encontró una reducción substancial, tanto en la incidencia de la enfermedad como en número de colonias muertas, entre febrero y julio de 2010. En ese período, El Freezer y La Nevera siguieron siendo los sitios con mayor proporción de colonias enfermas y/o muertas. En general se observó que el porcentaje de colonias afectadas no superó el 10 % (julio 2010). Para julio de 2010, La Nevera fue el sitio donde se observó la mayor incidencia de la enfermedad. Sin embargo, solo fue del 4.39 %, seguido por El Freezer con un 4.07 % y finalmente El Arrecife con un 1.43 % (Figura 5). Para el caso del bajo de Junior no se reportó ninguna colonia enferma en los transectos. Vale la pena mencionar que tampoco se reportó ninguna colonia de L. alba con signos de enfermedad en julio de 2010.
DISCUSIÓN
Dadas las condiciones oceánicas de la isla Malpelo, así como su estado de conservación y la ausencia de influencias continentales, se debe considerar la posibilidad de que las enfermedades y la mortalidad de octocorales puedan estar relacionadas con cambios climáticos a nivel global. En el mar Caribe se ha detectado que el hongo que ataca a los abanicos de mar afecta a un mayor número de especies coralinas y, de una manera más virulenta, cuando se elevan las temperaturas del agua por encima de los máximos normales (Ward et al., 2006). En los últimos tres años en el POT se han presentando anomalías térmicas prolongadas por más de seis meses, generalmente entre mayo y octubre. En nuestras investigaciones en curso, hemos detectado mortalidades masivas de octocorales en Gorgona durante 2008 y prevalencia de la enfermedad durante 2007, 2008 y 2009 en Cabo Corrientes, encontrando siempre la enfermedad activa entre los meses de mayo y noviembre. En la isla Malpelo se encontraron octocorales enfermos durante noviembre 2009, pero no se observaban esqueletos muertos o signos de mortalidades masivas. La enfermedad de origen fúngico se observó durante febrero de 2010 con cerca del 70 % de las colonias muertas o altamente afectadas en algunas localidades. Esta preocupación se ha acentuado luego de observar prevalencia de la enfermedad en la localidad de El Freezer hasta febrero de 2011 (J.A. Sánchez y D. Escobar, observación personal). Es una prioridad de investigación el monitoreo de colonias sanas, enfermas o parcialmente afectadas, para determinar la prevalencia de esta enfermedad en el área y su efecto real en la dinámica poblacional, así como conocer sobre los mecanismos naturales de resiliencia frente al cambio climático.
Dadas las condiciones oceánicas de la isla Malpelo, la incidencia de colonias enfermas en el 2008 y 2009 se puede deber más a consecuencias de anomalías térmicas prolongadas, que se han presentado en los últimos tres años en el POT, que a procesos antropogénicos directos. La menor incidencia de enfermedades encontrada en la isla, durante julio de 2010, podría tener una relación con temperaturas menos acentuadas que en el año anterior. Es posible estar hablando de pulsos de infección, seguidos de periodos de recuperación, sobre todo teniendo en cuenta que, normalmente, este tipo de afecciones van acompañadas de una respuesta retardada de tipo fisiológico del coral, que incrementa su resistencia (Kim y Harvell, 2004). Es fundamental hacerle un seguimiento detallado a la temperatura, para de esta forma poder entender de una manera más acertada la dinámica de la enfermedad, así como el comportamiento del hospedero.
Pese a la baja diversidad de especies de octocorales en la isla Malpelo, son evidentes las altas densidades de colonias y es muy probable que algunas de las especies sean endémicas de la isla. A excepción de Leptogorgia alba, una especie muy común en el POT, no ha sido posible realizar la completa identificación de los octocorales encontrados en Malpelo, ya que las especies pertenecientes a los géneros Pacifigorgia y Muricea presentan características morfológicas particulares, no descritas en la bibliografía taxonómica de estos géneros. Particularmente Pacifigorgia sp., que además tiene dos morfotipos, no se ajusta a ninguna especie actualmente descrita. Similarmente, las colonias de Muricea cf. fruticosa en Malpelo son en su totalidad blancas, mientras que en el resto de la costa Pacífica son blancas en la base adquiriendo progresivamente una coloración roja y marrón hacia las puntas de las ramas. Muricea cf. fruticosa se encuentra comúnmente en la costa Pacífica entre 10 y 30 m de profundidad, mientras que en Malpelo ocurre solamente por debajo de 50 m de profundidad. Dadas estas interesantes pero sutiles diferencias, se hace necesario recurrir a métodos genéticos para poder definir si se trata de especies nuevas y diferentes a las de la costa, o si las variaciones observadas son producto de plasticidad fenotípica debida a las diferencias en las condiciones ambientales en las que habitan.
En cuanto a la zonación por profundidad, la baja diversidad de especies en zonas más profundas puede deberse, en parte, a la preferencia de algunas especies de octocorales por superficies rocosas más consolidadas (Goldberg, 1973). En la isla Malpelo, y en especial en la mayoría de sitios monitoreados, por debajo de 25 m la morfología del bentos es cambiante y el sustrato rocoso disponible se encuentra distribuido heterogéneamente, a manera de parches sobre un fondo arenoso. Se ha reportado para otras áreas arrecifales que zonas con un alto nivel de oleaje o con una alta diversidad de corales escleractínios tienden a reducir la diversidad de octocorales (Kinzie, 1973). Sin embargo, debido a la forma que presentan estos abanicos, como en el caso de Pacifigorgia spp., zonas con alto oleaje le facilitan su desarrollo, en comparación con especies más plumosas como lo es L. alba (Sánchez et al., 1998).
Finalmente, en noviembre de 2009, durante la expedición al SFF Malpelo, se constató la presencia de Carijoa riisei (La Catedral), un octocoral invasor proveniente del océano Atlántico. Posteriormente, durante la expedición de febrero 2010, se observó en un sistema rocoso independiente (bajo del Monstruo). Desafortunadamente, durante febrero de 2011 se observaron nuevos brotes de esta especie en El Freezer y dentro de las grutas de La Puerta del Cielo (Figura 1) (J.A. Sánchez y D. Escobar, observación personal), lo que sugiere una reciente expansión a otras localidades de la isla. La introducción de especies, de forma intencional o accidental, es un problema que ha causado graves impactos en diversos ecosistemas marinos alrededor del mundo. Lamentablemente, esta situación ha ido incrementándose en las últimas décadas debido al aumento en la circulación marítima (Coles et al., 2006). Por esta razón, el estudio de las especies invasoras es de gran importancia, como en el caso de C. riisei, un octocoral originario del Atlántico, en donde se distribuye desde Florida hasta Brasil (DeFelice et al., 2001), pero que ha sido visto también en otras localidades del Pacífico colombiano como la isla Gorgona y Cabo Corrientes. Esta es una situación preocupante, ya que C. riisei se caracteriza por su agresividad, llegando a recubrir y a desplazar a otros invertebrados (Lira et al., 2009). Por ejemplo, en Hawaii esta especie reemplazo al 90 % del coral negro, causando un fuerte impacto económico (Kahng y Grigg, 2005). Aunque en Malpelo esta especie parece estar restringida a un par de localidades, las especies de Pacifigorgia son particularmente sensibles al recubrimiento por C. riisei, como lo hemos evidenciado en Gorgona y Cabo Corrientes.
En conclusión, podemos decir que las comunidades de octocorales de la isla Malpelo presentan condiciones únicas en la región del POT, incluyendo posiblemente un componente mayoritario de especies endémicas. Desafortunadamente, se han detectado mortalidades masivas y prevalencia de enfermedades, de índole fúngico, en los octocorales. Debido a las condiciones oceánicas y de conservación de la isla, se presume que el precursor ambiental de estas enfermedades sean las anomalías térmicas que se han presentado en el área durante los últimos tres años. Otra amenaza para los octocorales de Malpelo es la presencia y expansión de Carijoa riisei, especie invasora en el área, la cual ha empezado a recubrir otros octocorales en dos localidades de la isla. Se desconoce si la superioridad de esta especie guarda relación con anomalías térmicas, pero tanto las enfermedades como la expansión de Carijoa hacen importante iniciar un seguimiento detallado de la temperatura del agua y del estado de salud de los octocorales en Malpelo.
AGRADECIMIENTOS
A la Fundación Malpelo (en particular a Sandra Bessudo, Germán Soler y Stan Teillaud): Cruceros SEASCAPE 12, 13, 14 y 16 (Fundación Familia Walton, Asturias Fondos Propios, Mohamed Bin Zayed, y el Fondo Patrimonial); al Departamento de Ciencias Biológicas, al Museo de Historia Natural-ANDES y a la Facultad de Ciencias de la Universidad de los Andes; a los miembros de BIOMMAR, en especial a Juliana Sintura; a la Unidad Administrativa Especial del Sistema de Parques Nacionales Naturales-UAESPNN (SFF Malpelo), por otorgar el permiso de investigación en Biodiversidad Biológica: "Evaluación de las comunidades de octocorales del Santuario de Flora y Fauna Malpelo, Pacífico colombiano" DTSO-M-0100099; a los miembros de SIMAC-INVEMAR; a la tripulación del catamarán Nemo; a la M/N María Patricia y a todos los participantes de las expediciones al SFF Malpelo de noviembre de 2009, y de febrero y julio de 2010. Se agradece a Mateo López, editor del presente volumen, y a dos revisores anónimos, quienes ayudaron a mejorar sustancialmente el manuscrito.
BIBLIOGRAFÍA
1 Alker, A. P., G. W. Smith y K. Kim. 2001. Characterization of Aspergillus sydowii (Thom et Church), a fungal pathogen of caribbean sea fan corals. Hydrobiologia, 460: 105-111. [ Links ]
2 Bayer, F. M. 1961. The shallow-water octocorallia of the west indian region: A manual for marine biologists. Nijhoff, La Haya. 373 p. [ Links ]
3 Birkeland, C. 1997. Symbiosis, fisheries and economic development on coral reefs. Trends in Ecology and Evolution, 12: 364-367. [ Links ]
4 Birkeland, C., D. L. Meyer, J. P. Stames y C. L. Buford. 1975. Subtidal communities of Malpelo Island. 55-68. En: Graham J. B. (Ed.). The biological investigation of Malpelo Island, Colombia. Smithsonian Contr. Zool., Vol. 176. 98p. [ Links ]
5 Caldeira, K. y M. E. Wickett. 2003. Anthropogenic carbon and ocean pH. Nature, 425: 365-365. [ Links ]
6 Clarke, K. y M. Warwick. 2003. Change in marine communities: An approach to statistical analysis and interpretation. PRIMER-V5. Segunda Edición, PRIMER-E Ltd., Plymouth University, Plymouth. 157 p. [ Links ]
7 Coles, S. L., F. L. M. Kandel, P. A. Reath, K. Longenecker y L. G. Eldredge. 2006. Rapid assessment of nonindigenous marine species on coral reefs in the main Hawaiian islands. Pac. Sci., 60 (4): 483-507. [ Links ]
8 DeFelice, R. C., J.T. Carlton, y L. G. Eldredge. 2001. Nonindigenous marine invertebrates. B1-B60. En: Eldredge, L. G. y C. M. Smith. (Eds.) A guidebook of introduced marine species in Hawaii. Bishop Museum Technical Report 21, Honolulu. 65 p. [ Links ]
9 Feely, R. S., C. L. Sabine, K. Lee, W. Berelson, J. Kleypas, V. J. Fabry y F. J. Millero. 2004. Impact of anthropogenic CO2 on the CaCO3 system in the oceans. Science, 305 (5682): 362-366. [ Links ]
10 Gattuso, J. P., M. Frankignoulle, I. Bourge, S. Romaine-Lioud y W. Buddemeier. 1998. Effect of calcium carbonate saturation of seawater on coral calcification. Global Planet Change, 18 (1-2): 37-46. [ Links ]
11 Gazeau, F., C. Quiblier, J. M. Jansen, J. P. Gattuso, J. J. Middelburg y C. H. R. Heip. 2007. Impact of elevated CO2 on shellfish calcification. Geophys. Res. Lett., 34: L07603, doi:10.1029/2006GL028554. [ Links ]
12 Goldberg, W. 1973. The ecology of the coral-octocoral communities off the southeast Florida coast: Geomorpholy, species composition, and zonation. Bull. Mar. Sci., 23 (3): 466-488. [ Links ]
13 Hoegh-Guldberg, O., P. J. Mumby, A. J. Hooten, R. S. Steneck, P. Greenfield, E. Gomez, C. D. Harvell, P. F. Sale, A. J. Edwards, K. Caldeira, N. Knowlton, C. M. Eakin, R. Iglesias-Prieto, N. Muthiga, R. H. Bradbury, A. Dubi y M. E. Hatzioloset. 2007. Coral reefs under rapid climate change an ocean acidification. Science, 318: 1737-1742. [ Links ]
14 Jamison, J. L. y H. R. Lasker. 2008. Identification of octocoral recruits using microsatellite primers: Relationships between recruitment and adult distribution of Pseudopterogorgia spp. Limnol. Oceanogr., 53 (5): 1963-1972. [ Links ]
15 Kahng, S. E., Y. Benayahu, D. Wagner y N. Rothe. 2008. Sexual reproduction in the invasive octocoral Carijoa riisei in Hawaii. Bull. Mar. Sci., 82: 1-17. [ Links ]
16 Kahng, S. E. y R. W. Grigg. 2005. Impact of an alien octocoral, Carijoa riisei, on black corals in Hawaii. Coral Reefs, 24 (4): 556-562. [ Links ]
17 Kim, K., C. D. Harvell, P. D. Kim, G. W. Smith y M. Merkel. 2000. Fungal disease resistence of Caribbean sea fan corals (Gorgonia spp.). Mar. Biol., 136: 259-267. [ Links ]
18 Kim, K. y D. Harvell. 2004. The rise and fall of a six-year coral-fungal epizootic. Am. Nat., 164: S52-S63. [ Links ]
19 Kinzie, R. A. 1973. The zonation of west indian gorgonians. Bull. Mar. Sci., 23 (1): 93-155. [ Links ]
20 Kleypas, J., R. A. Feely, V. Fabry, C. Langdon, C. I. Sabine y L. I. Robbins. 2006. Impacts of ocean acidification on coral reefs and other marine calcifiers: A guide for future research. Reporte de Taller durante 18-20 Abril de 2005. NSF, NOAA, y U.S. Geological Survey. St. Petersburg. 88 p. [ Links ]
21 Kleypas, J. y C. Langdon. 2006. Coral reefs and climate change: Science and management. Coastal Estuarine Stud., 61: 73. [ Links ]
22 Kleypas, J. A., R. W. Buddemeier, D. Archer, J. P. Gattuso, C. Langdon y B. N. Opdyke. 1999. Geochemical consequences of increased atmospheric carbon dioxide on coral reefs. Science, 284: 118-120. [ Links ]
23 Knowlton, N. y J. Jackson. 2008. Shifting baselines, local impacts, and global change on coral reefs. PLoS Biol., 6 (2): 215-220. [ Links ]
24 Langdon, C., T. Takahashi, F. Marubini, M. Atkinson, C. Sweeney, H. Aceves, H. Barnett, D. Chipman y J. Goddard. 2000. Effect of calcium carbonate saturation state on the calcification rate of an experimental coral reef. Global Biogeochem. Cycles, 14: 639-654. [ Links ]
25 Lira, A., J. Naud, P. Gomes y C. Santos-Perez. 2009. Trophic ecology of the octocoral Carijoa riisei from littoral of pernambuco, Brazil. I. Composition and spatio-temporal variation of the diet. J. Mar. Biol. Assoc. U. K., 89 (1): 89-99. [ Links ]
26 Marubini, F., H. Barnett, C. Langdon y M. J. Atkinson. 2001. Dependence of calcification on light and carbonate ion concentration for the hermatypic coral Porites compressa. Mar. Ecol. Prog. Ser., 220: 153-162. [ Links ]
27 Mora, C. 2008. A clear human footprints in the coral reefs of the Caribbean. Proc. R. Soc. London, Ser. B., 275: 767-773. [ Links ]
28 Nagelkerken, I., K. Buchan, G. W. Smith, K. Bonair, P. Bush, J. Garzón-Ferreira, L. Botero, P. Gayle, C. Hereber, C. Petrovic, L. Pors y P. Yoshioka. 1997. Widespread disease in caribbean sea fans: I. Spreading and general characteristics. Proc 8th Int. Coral Reef Symp., Panamá, 1: 679-682. [ Links ]
29 Orr, J. C., V. J. Fabry, O. Aumont, L. Bopp, S. C. Doney, R. A. Feely, A. Gnanadesikan, N. Gruber, A. Ishida, F. Joos, R. M. Key, K. Lindsay, E. Maier-Reimer, R. Matear, P. Monfray, A. Mouchet, R. G. Najjar, G.-K. Plattner, K. Rodgers, C. L. Sabine, J. L. Sarmiento, R. Schlitzer, R. D. Slater, I. J. Totterdell, M. F. Weirig, Y. Yamanaka y A. Yool. 2005. Anthropogenic ocean acidification over the twenty-first century and its impact on calcifying organisms. Nature, 437: 681-686. [ Links ]
30 Riebesell, U., A. T. Revill, D. G. Holdsworth y J. K. Volkman. 2000. The effects of varying CO2 concentration on lipid composition and carbon isotope fractionation in Emiliania huxleyi. Geochim. Cosmochim. Acta, 64 (24): 4179-4192. [ Links ]
31 Rosenberg, E. y Y. Ben-Halm. 2002. Microbial diseases of corals and global warming. Environ. Microbiol., 4 (6): 318-326. [ Links ]
32 Sabine, C. L., R. A. Feely, N. Gruber, R. M. Key, K. Lee, J. L. Bullister, R. Wanninkhof, C. S. Wong, D. W. R. Wallace, B. Tilbrook, F. J. Millero, T. H. Peng, A. Kozyr, T. Ono y A. F. Rios. 2004. The oceanic sink for anthropogenic CO2. Science, 305 (5682): 367-371. [ Links ]
33 Sánchez, J. A. 1994. Presencia de los octocorales Stylatula diadema Bayer (Pennatulacea) y Carijoa riisei (Duchassaing y Michelotti) (Telestacea) en la costa caribe colombiana. An. Inst. Inv. Mar. Punta Betin, 23: 137-147. [ Links ]
34 Sánchez, J. A. 2007. A new genus of atlantic octocorals (octocorallia: Gorgoniidae): Systematics of gorgoniids with asymmetric sclerites. J. Nat. Hist., 41 (9-12): 493-509. [ Links ]
35 Sánchez, J. A., S. Zea y J. M. Díaz. 1998. Patterns of octocoral and black coral distribution in the oceanic barrier reef-complex of Providencia island southwest caribbean. Caribb. J. Sci., 34 (3-4): 250-264. [ Links ]
36 Sax, D. F., J. J. Stachowicz y S. D. Gaines. 2005. Species invasions: Insights into ecology, evolution, and biogeography. Sinauer Associates, Sutherland. 480 p. [ Links ]
37 Smith, G. W., C. D. Harvell y K. Kim. 1998. Response of sea fans to infection with Aspergillus sp. (fungi). Rev. Biol. Trop., 46: 205-208. [ Links ]
38 Smith, G. W. y E. Weil. 2004. Aspergillosis of gorgonians. 279-287. En: Rosenberg, E. y Y. Loya. (Eds.) Coral health and disease. Springer Verlag, Nueva York. 488 p. [ Links ]
39 Sutherland, K. P., J. W. Porter y C. Torres. 2004. Disease and immunity in caribbean and indo-pacific zooxanthellate corals. Mar. Ecol. Prog. Ser., 266: 273-302. [ Links ]
40 The Royal Society. 2005. Ocean acidification due to increasing atmospheric carbon dioxide. The Royal Society, Londres y The Clyvedon Press Ltd, Cardiff. 51 p. [ Links ]
41 VanOppen, M. J. H., J. C. Mieog, C. A. Sánchez y K. E. Fabricius. 2005. Diversity of algal endosymbionts (zooxanthellae) in octocorals: The roles of geography and host relationships. Mol. Ecol., 14 (8): 2403-2417. [ Links ]
42 Ward, J. R., K. Kim y C. D. Harvell. 2006. Temperature affects coral disease resistance and pathogen growth. Mar. Ecol. Prog. Ser., 329: 115-121. [ Links ]
FECHA DE RECEPCIÓN: 08/11/2010 FECHA DE ACEPTACIÓN: 12/10/2011