Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Boletín de Investigaciones Marinas y Costeras - INVEMAR
Print version ISSN 0122-9761
Bol. Invest. Mar. Cost. vol.43 no.2 Santa Marta July/Dec. 2014
EVALUACIÓN DEL CICLO GAMETOGÉNICO DE ARGOPECTEN NUCLEUS (PECTINIDAE, BIVALVIA) EN SISTEMA DE CULTIVO SUSPENDIDO, EN LA BAHÍA DE NENGUANGE, SANTA MARTA, COLOMBIA*
GAMETOGENIC CYCLE ASSESSMENT OF ARGOPECTEN NUCLEUS (PECTINIDAE, BIVALVIA) IN SUSPENDED CULTURE SYSTEM IN NENGUANGE BAY, SANTA MARTA, COLOMBIA
Yucellys P. Daniel-Lemus1, Ernesto J. Acosta-Ortiz2, Félix de Jesús Cuello1 y Javier Gómez-León3
1 Universidad del Magdalena, Programa de Ingeniería Pesquera. Carrera 32 No 22-08, Santa Marta, Colombia. yucellys@gmail.com, felcuello@gmail.com.
2 Wehrheimer Weg 2 Friedberg 61169 (Hessen) Alemania. eracorz77@hotmail.com.
3 Instituto de Investigaciones Marinas y Costeras (Invemar), Calle 25 No. 2-55 Playa Salguero, El Rodadero, Santa Marta, Colombia. javier.gomez@invemar.org.co.
RESUMEN
Entre abril y septiembre de 2010, fue estudiado el ciclo gametogénico del pectínido Argopecten nucleus en la bahía de Nenguange, Parque Nacional Natural Tayrona. Diez organismos fueron colectados cada 14 días y se procesaron sus gónadas para histología; paralelo a esto se realizó un seguimiento de la apariencia morfocromática de la gónada a 55 individuos mantenidos en un sistema de cultivo suspendido, estableciendo cinco estadios así: I = Reposo e indiferenciación; II = Desarrollo inicial; III = Desarrollo avanzado; IV = Maduro y V = Desove. El estadio gonadal predominante fue el III con un promedio de aparición de 60%, seguido del estadio V con 20.7%, después el IV con 13.5% y finalmente los estadios II y I con 5.1 y 0.6% respectivamente. Se encontró una relación significativa entre el índice gonadosomático con la precipitación (p = 0.0001), temperatura (p = 0.0015), salinidad (p = 0.0003) y clorofila a (p = 0.0285). El factor de condición (FC) mostró una correlación con la materia orgánica particulada (MOP; p = 0.0243); sin embargo, al realizar una prueba de regresión simple la MOP no afecta de manera sustancial al FC con un índice de correlación de 4.53.
PALABRAS CLAVES: Argopecten nucleus, ciclo gametogénico, histología, cultivo suspendido.
ABSTRACT
Between April and September 2010, the gametogenic cycle of the scallop Argopecten nucleus was studied in Nenguange Bay in Tayrona National Park. Ten organisms were collected every 14 days and processed for histology of their gonads. Parallel to this, the morfocromatic appearance of the gonads of 55 individuals kept in a suspended culture system was followed, setting up five stages as follows: I = Rest and undifferentiation; II = Initial development; III = Advanced development; IV = Mature; and V = Spawning. The predominant gonadal stage was III with an average of 60%, followed by stage V with 20.7%, followed by IV with 13.5%, and finally stages II and I with 5.1 and 0.6% respectively. We found a significant relationship between the gonadosomatic index and precipitation (p = 0.0001), temperature (p = 0.0015), salinity (p = 0.0003), and chlorophyll a (p = 0.0285). The condition factor (CF) showed a correlation with particulate organic matter (POM; p = 0.0243), however, when performing a simple regression, the test indicated that the MOP will not substantially affect the FC with a correlation index of 4.53.
KEYWORDS: Argopecten nucleus, gametogenic cycle, histology, suspended culture.
INTRODUCCIÓN
Los pectínidos constituyen uno de los grupos más importantes en la acuicultura, ya que presentan un alto potencial como recurso alimentario, generan rentabilidad económica y tienen un crecimiento relativamente rápido (Pereira y Ferreira, 2006), permitiendo de esta manera que su cultivo sea una herramienta que promete proyectarse a escala comercial en Colombia, contribuyendo así a la reducción de la presión sobre los ecosistemas costeros y la diversificación de la acuicultura (Castellanos y Campos, 2007). Estas ventajas han motivado el cultivo de dichos organismos a nivel comercial en países como China y Japón (Patinopecten yessoensis), España (Pecten maximus) Canadá (Argopecten irradians), Francia (P. maximus), Chile y Perú (A. purpuratus), México (Nodipecten subnodosus) y Ecuador (A. ventricosus). Por otro lado, se han realizado cultivos a nivel experimental en Argentina (Aequipecten tehuelchus), Brasil (N. nodosus) y Venezuela (A. nucleus, N. nodosus y Euvola ziczac) (Illanes et al., 1985; Avendaño et al., 2001; Velasco, 2008).
En Colombia, el Instituto de Investigaciones Marinas y Costeras (Invemar) desde 1994 ha llevado a cabo diversas investigaciones en ecología, dinámica poblacional, patrón de abundancia larval en el plancton, captación de semilla y cultivo en campo, con lo cual se ha identificado entre otras, al pectínido A. nucleus como una de las especies nativas con potencial para el cultivo por su rápido crecimiento, alta producción de carne y buen precio en el mercado (Urban, 1999; Valero et al., 2000). Esto ha motivado su cultivo a nivel experimental con la implementación en 1998 por parte de Invemar de una estación en la bahía de Nenguange en el Parque Nacional Natural Tayrona (PNNT) (Urban, 1999) y otra en 2004 en Bahía Portete (La Guajira) (Invemar, 2005, 2009). Así mismo, la Universidad del Magdalena en 2009 instaló una estación en la bahía de Taganga para el cultivo de los pectínidos N. nodosus y A. nucleus; pese a los buenos resultados logrados en estos trabajos, uno de los principales problemas es el abastecimiento de semilla del medio natural, pues para A. nucleus su abundancia es baja, variable y poco predecible (De la Roche y Vélez, 1997; Valero et al., 2000), obteniendo en promedio de tres a cinco organismos por colector (Castellanos y Campos, 2007).
En cuanto a investigaciones referentes al ciclo gametogénico de A. nucleus, son escasas y se limitan tan solo a registros aislados de estadios de madurez con fines de reproducción en laboratorio. Dentro de este contexto Román et al. (2001) señalan que A. nucleus tiene desoves sucesivos durante los meses de enero a junio. Por su parte, Velasco (2008) hizo una modificación de la tabla de estadios de madurez gonadal de Sastry (1963) y Cochard y Devauchelle (1993) para determinar, por medio de la apariencia de la gónada, el grado de madurez de los pectínidos A. nucleus y N. nodosus, con fines de reproducción en laboratorio.
Los estudios histológicos de la gónada en bivalvos nos dan una idea precisa del desarrollo de los gametos y de la ocurrencia de otros fenómenos, como la atresia ovocitaria seguida por la lisis, que en algunas especies parecen formar parte de su estrategia reproductiva. Trabajos de investigación usando la técnica de histología para evaluar ciclos reproductivos en pectínidos son escasos, sin embargo se destacan: Pecten papyraceus, A. purpuratus, A. circularis, P. maximus, A. tehuelchus (Salaya y Pechaszadeh, 1978; Chávez e Ishiyama, 1989; Villalejo-Fuerte, 1992; Jaramillo et al., 1993; Pazos et al., 1996; Narvarte y Kroeck, 2000).
Dentro de la acuicultura de pectínidos, la determinación de los estadios de madurez máxima, al igual que la colecta de semilla proveniente de organismos mantenidos en cultivo, es de vital importancia tanto para la cosecha como para reabastecimiento de los cultivos. Dentro de los principales factores que afectan la producción de óvulos y esperma (gametogénesis) están las variaciones ambientales, siendo la temperatura y la cantidad de alimento los más influyentes (González et al., 1999). Del mismo modo, factores endógenos como el tamaño y la edad de los organismos son importantes en este proceso (Fernández, 1991; Helm et al., 2006). Por lo tanto este trabajo estudió la relación existente de los parámetros ambientales (temperatura, salinidad, transparencia, materia orgánica particulada, clorofila a y precipitaciones) sobre el ciclo gametogénico de A. nucleus, como un aporte de información fundamental para conocer las épocas en las cuales los organismos se encuentran en el máximo grado de madurez sexual, sus picos de desoves y el tiempo más propicio para realizar la colecta de semilla del medio natural.
ÁREA DE ESTUDIO
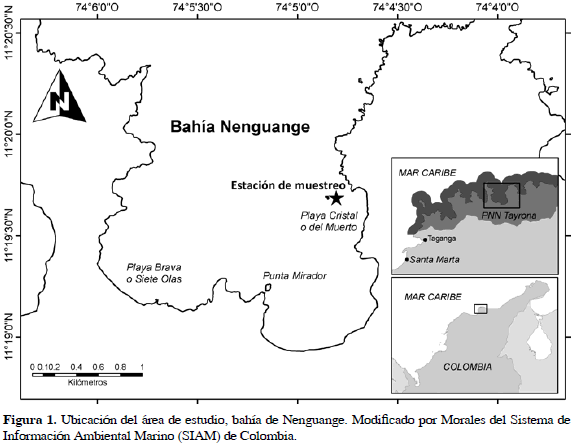
Este estudio se llevó a cabo en la bahía de Nenguange (PNNT; 11°20'N, 74°10'O) (Figura 1), ubicada al nororiente de la ciudad de Santa Marta en el Caribe colombiano (Urban, 1999). El régimen climático regional se caracteriza por ser seco con fluctuaciones entre semidesértico y desértico, comprende una época lluviosa de junio a noviembre intercalada con un corto período seco entre julio y agosto (Veranillo de San Juan) y otro de sequía de diciembre a mayo (Ramírez, 1983). El promedio de la temperatura del agua en la región varía entre 22 y 30 °C, con una salinidad que fluctúa entre 33 y 37, la concentración de seston tiene valores entre 0.93 y 1.73 mg.L-1 y la materia orgánica particulada en el agua oscila entre 0.42 y 0.93 mg.L-1 (Urban, 1999; López, 2008).
MATERIALES Y MÉTODOS
Entre abril y septiembre de 2010 se colectaron un total de 165 organismos, provenientes de una misma cohorte de un experimento de campo del Invemar; estos individuos eran mantenidos en un cultivo suspendido tipo linterna entre 5 y 8 m de profundidad en la bahía de Nenguange (PNNT), con una talla inicial promedio de 40.9 ± 0.5 mm y un estadio de madurez sexual III según la escala de madurez adaptada por Velasco (2008). Los organismos fueron marcados y divididos en dos grupos: el primero, denominado grupo de seguimiento morfocromático, conformado por 55 individuos, que aportaron información con respecto al aspecto de la gónada, al igual que el peso de los organismos. El segundo, llamado de seguimiento histológico conformado por 110 animales, de los cuales se sacrificó una muestra de 10 organismos por muestreo, en intervalos de 14 días (exceptuando el ultimo muestreo que fue de 20 días) con el fin de realizar cortes histológicos y siguiendo la metodología descrita por Gómez-León (2005), se realizaron cortes transversales de 5 mm de grosor de las gónadas previamente fijadas en formaldehido al 4%, para deshidratarlas pasando por una serie sucesiva de baños en etanol de diferente gradación. La eliminación de los restos de alcohol se llevó a cabo en medio soluble de parafina (xileno) y por último se incluyeron en parafina líquida; este procedimiento se realizó en un procesador de tejido automático Shandon Citadel 2000. A continuación se hicieron cortes de 5 µm de espesor utilizando un micrótomo Microm HM 325. Las secciones resultantes se estiraron en un baño de agua destilada a 45 °C, se recogieron en un portaobjetos (dos secciones por portaobjetos) y se secaron al aire. El siguiente paso consistió en el desparafinado de las secciones dispuestas en el portaobjetos y la tinción hematoxilina-eosina. Los cortes se observaron bajo un microscopio con el fin de realizar un análisis cualitativo de la gónada y así obtener una escala propia de madurez sexual, clasificando histológicamente los estadios de desarrollo gonadal, este grupo también fue utilizado para obtener el factor de condición (FC) y el índice gonadosomático (IG). Los animales de ambos grupos fueron mantenidos en sistemas de cultivo suspendido tipo minilinterna, a una densidad constante de 30% de cobertura y profundidad de 5 m.
En cada uno de los muestreos en el lugar de cultivo se registró la temperatura (termómetro de mercurio) a 5 m de profundidad, salinidad (conductímetro YSI-EC 300) y transparencia (disco Secchi) del agua de mar. Además se tomaron muestras de agua para análisis de clorofila a, la cual se determinó por el método de sólidos totales en suspensión seco a 103-105 °C (Garay et al., 2003), y materia orgánica particulada, empleando la técnica descrita por Lorenzen (1967) y adaptada por Garay et al. (2003). También se obtuvo información de la precipitación suministrada por el Instituto de Hidrología, Meteorología y Estudios Ambientales de Colombia (Ideam), para relacionarla con el desarrollo gonadosomático de la especie, con el FC y el IG.
La determinación del FC y del IG se calculó mediante las fórmulas descritas por Villalejo-Fuerte y Ceballos (1996),
FC = B/T*100
donde,
B = Peso húmedo en gramos de las partes blandas
T = Peso húmedo en gramos total del animal
IG = G/B*100
donde,
G = Peso húmedo en gramos de la gónada
Análisis de los datos
Las pruebas estadísticas se efectuaron con el software Statgraphics Centurion XV considerando un α de 0.05. Teniendo en cuenta que durante el período evaluado se presentaron fuertes lluvias, mayores a la registradas en años anteriores, se evaluó si durante el período del ensayo existieron diferentes niveles en las precipitaciones, considerando un nivel de 3 mm como límite entre baja y alta precipitación, para lo cual se probaron los supuestos de normalidad de residuos y homogeneidad de varianzas; en caso de rechazo se empleó la prueba de Kruskal-Wallis.
Para identificar cuáles variables ambientales (materia orgánica particulada, clorofila a, temperatura, salinidad, transparencia y precipitación) tenían correlaciones significativas con el FC y el IG se empleó la prueba de Spearman, luego se efectuó una matriz de regresiones simples con las variables que producen un efecto significativo sobre el FC y el IG. Posteriormente se buscó el modelo más simple que explicara la mayor variabilidad del IG y el FC.
RESULTADOS
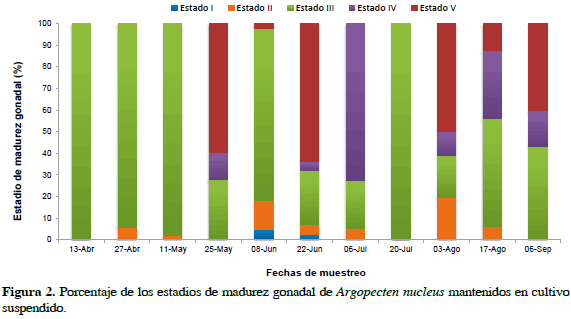
El estadio predominante a lo largo del ensayo fue el III, principalmente en los tres primeros muestreos, con valores que oscilaron entre 93 y 100%, registrando los menores en el muestreo del 25 de mayo (27.7%), 22 de junio (25.0%) y 3 de agosto (19.4%), caracterizados por la presencia de altos porcentajes de organismos desovados a partir del cuarto muestreo (25 de mayo), con 59.6%. En el quinto muestreo (8 de junio), ocurrió una rápida recuperación gonadal, observándose un alto porcentaje de animales en estadio III (79.5%); sin embargo, también se registraron bivalvos en estadios V (2.3%), II (13.6%) y I (4.6%). De igual manera, el estadio de madurez II presentó valores muy bajos a lo largo del muestreo, alcanzando el máximo el 3 de agosto con 19.4% (Figura 2).
En cuanto a los organismos desovados, se observaron en cinco de los once muestreos con porcentajes entre 2.3 y 63.6%, caracterizándose en su gran mayoría por ser desoves parciales (en el cual se nota que la gónada no queda completamente vacía), a excepción del 3 de agosto, en el cual 50% de los organismos desovados desocuparon en su totalidad la gónada, viéndose una gónada completamente translúcida. A pesar de que el máximo estadio madurez sexual (IV) se observó a partir del cuarto muestreo, también se registró en seis de los once con valores relativamente bajos, oscilando entre 4.5% (22 de junio) y 31.2% (17 de agosto), a excepción del 6 de julio en el que el estadio IV fue el dominante con 72.5% de organismos en su máximo estadio de madurez (Figura 2).
Descripción histológica de la gónada
Esta descripción se hizo con base en la tabla morfocromática de madurez sexual de Velasco (2008), adaptándose a los resultados histológicos obtenidos en este estudio.
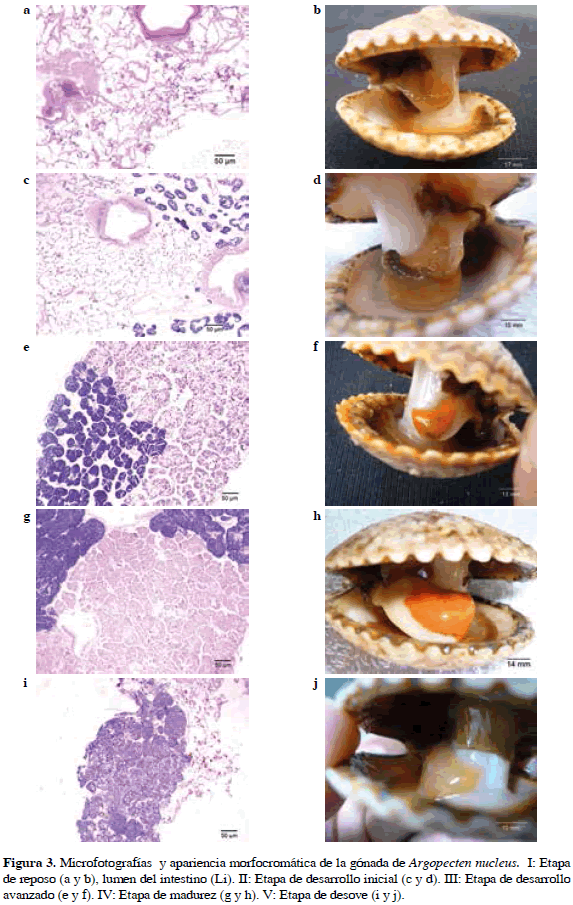
Estadio I o etapa de reposo e indiferenciación. Es la etapa posterior a la emisión total de gametos. En este estadio se inicia la reestructuración de los tejidos de reserva, tanto los folículos como los túbulos seminíferos se encuentran prácticamente vacíos, contraídos, las paredes son gruesas y no tienen células germinales (Figura 3a), por lo tanto el sexo no se puede diferenciar (Figura 3b).
Estadio II o etapa de desarrollo inicial. La gónada se caracteriza por presentar una gran actividad gametogénica, en la que se empiezan a integrar los folículos y los túbulos seminíferos, que están separados por tejidos conectivos (Figuras 3c y d). En las hembras los ovocitos crecen, el núcleo engorda y la cromatina se dispersa en forma de una fina red, para entrar en mitosis; la relación núcleo citoplasma disminuye paulatinamente a medida que los ovocitos se desarrollan, con un diámetro del núcleo de 6.2-8.0 µm. En los machos, al igual que en las hembras, se dan cambios de volumen y morfología nuclear, siendo la cromatina más densa en los espermatocitos que en los ovocitos. En las secciones histológicas, se encuentran diferentes estados de desarrollo: células madres, ovocitos vitelogenéticos adheridos a la pared de los folículos con diámetro promedio folicular de 351 µm y una distancia entre folículos de 122 µm. Espermatocitos dentro de los túbulos seminíferos con diámetro promedio tubular de 293 µm y una distancia entre túbulos de 115 µm. El centro de los folículos y túbulos se encuentra vacío.
Estadio III o etapa de desarrollo avanzado. En esta etapa la foliculogénesis y gametogénesis son intensas, llegando a aparecer los primeros gametos maduros (espermatozoides y ovocitos) (Figuras 3e y f). Los folículos pasan a ocupar la mayor parte de la masa visceral, reduciéndose a la presencia del tejido muscular y conectivo. Los procesos que caracterizan esta fase son la ovogénesis en hembras y la espermatogénesis en machos. Durante la previtelogénesis los ovocitos crecen lentamente, los cromosomas están difuminados y el citoplasma enriquecido con ribonucleoproteínas, aumentando el nucléolo de tamaño y sufriendo la primera división nucleolar cuando se aproxima la vitelogénesis (Lubet, 1959). En la vitelogénesis los ovocitos aumentan de tamaño y acumulan reservas vitelínicas (inclusiones lipídicas, granulación de mucopolisacáridos y plaquetas vitelínicas proteínicas) en el citoplasma. En la espermatogénesis, las espermatogonias van formando una o dos capas periféricas en los acinos gonádicos y al entrar en meiosis se pueden observar todos los estadios espermatogénicos estratificados en capas sucesivas y dirigidas hacia el lumen del túbulo. A medida que avanza el desarrollo, el citoplasma va decreciendo en tamaño y las células van siendo más pequeñas. Las espermatogonias dan origen a los espermatocitos primarios por mitosis, enseguida el espermatocito primario pasa a espermatocito secundario iniciando la meiosis y el paso de espermatocito secundario a espermátidas concluye la segunda división meiótica. Empieza entonces la espermiogénesis, que es la diferenciación de las espermátidas en espermatozoides. En esta etapa los centriolos se disponen perpendicularmente dando lugar a la aparición del flagelo. Empieza entonces la espermiogénesis, que es la diferenciación de las espermátidas en espermatozoides. El centro de algunos folículos se encuentra vacío con diámetro promedio folicular de 219 µm y una distancia entre folículos de 34 µm. Se encuentra una cantidad variable de espermatocitos y espermátides dentro de los túbulos seminíferos con diámetro promedio tubular de 363 µm y una distancia entre folículos de 43 µm.
Estadio IV o etapa de madurez. Período donde los gametos maduran, estando aptos para ser liberados al medio (Figuras 3g y h). La gónada es una masa compacta uniforme, con folículos llenos de ovocitos maduros con diámetro promedio folicular de 517 µm y una distancia entre folículos de 21 µm. Túbulos seminíferos llenos de espermatozoides maduros, con diámetro promedio tubular de 293 µm y una distancia entre folículos de 115 µm. Casi no se observa tejido conectivo. En machos los acinos gonadales contienen principalmente espermatozoides que dirigen sus flagelos hacia el eje central del acino. Las otras formas gametogénicas (espermatogonias, espermatocitos y espermátidas) prácticamente desaparecen. El tejido de reserva intrafolicular desaparece, toda el área gonadal es tomada por gametos maduros.
Estadio V o etapa de desove. Se aprecia la reducción en la cantidad de gametos y la aparición de espacios vacíos en la gónada ocupando un volumen variable en diferentes animales, dependiendo de lo avanzado del desove (Figuras 3i y j). Los folículos generalmente se rompen, se confunden entre sí y los túbulos seminíferos parcialmente vacíos se muestran segregados, disminuyendo drásticamente la cantidad de espermatozoides.
Índice gonadosomático (IG) y factor de condición (FC)
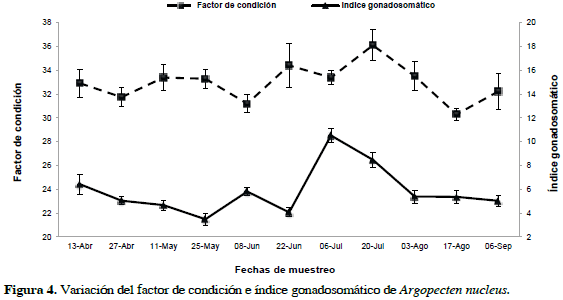
El FC tuvo un promedio de 32.9%, alcanzando un valor máximo de 36.1% durante el muestreo del 20 de julio, a partir de esta fecha y durante los dos siguientes muestreos se registró una disminución constante en el FC, con su valor más bajo (30.3%) el 17 de agosto (Figura 4). Mientras que el IG mostró dos períodos de madurez, con valores mínimos el 25 de mayo (3.5%) y el 22 de junio (4.1%), observando el mayor IG el 6 y 20 de julio con 11 y 8% respectivamente, cuando los individuos se encontraban en un estadio de desarrollo gonadal avanzado y máximo (estadio III y IV) (Figura 3).
Tanto el FC como el IG presentaron similitudes, principalmente entre el primer y segundo muestreo, pero a partir de este último, mientras el FC aumentaba el IG disminuía y viceversa, ya que se ha demostrado que el IG se relaciona de forma inversa al FC debido a una demanda de energía por parte del individuo para procesos reproductivos (González y Oyarzún, 2012), esta tendencia se mantuvo hasta el 6 de julio caracterizado por presentar el máximo estadio de madurez sexual. A partir de ese momento tanto el FC como el IG mostraron una rápida tendencia decreciente, que para el caso del IG se estabilizó a partir del 3 de agosto y para el FC el 17 de agosto (Figura 4).
Variables ambientales
Las variables ambientales presentaron un cambio fuerte después del muestreo del 6 de julio (período caracterizado por presentar el máximo grado de madurez sexual en los organismos), registrándose un rápido incremento en variables como MOP, temperatura y precipitaciones, mientras que la clorofila a, la salinidad y la transparencia presentaron una disminución (Figura 5). El contenido de MOP mantuvo un promedio de 1.11 mg.L-1, fluctuando entre un mínimo de 0.57 mg.L-1 en el muestreo del 22 de junio y un máximo de 1.59 mg.L-1 para el 6 de septiembre (Figura 5a). Sin embargo, la menor concentración de clorofila a se registró el 17 de agosto con 0.16 µg.L-1 y la máxima el 27 de abril con 1.62 µg.L-1, cabe anotar que disminuyó a partir del 6 de julio hasta finalizar el trabajo (Figura 5b). No obstante, el registro más alto de la temperatura fue en julio con 31 °C y el más bajo en mayo y junio con 28.5 °C (Figura 5c). La salinidad presentó su mayor valor en los muestreos del 11 de mayo al 8 de junio con 36, y los menores del 13 al 27 de abril y el 6 de julio con 31 (Figura 5d). En cuanto a la transparencia, su valor mínimo (3.2 m) se registró el 27 de abril y un máximo de 18 m para el 8 de junio, manteniéndose luego desde el 22 de junio hasta el 6 de septiembre entre 5.5 y 7 m (Figura 5e). En la Figura 5f, se muestran los niveles de precipitación, observando bajas precipitaciones de abril a junio (< 3 mm), exceptuando el período del 11 de abril al 10 de mayo cuando la precipitación fue semejante a la registrada en la época de julio a septiembre (> 3 mm), meses que se consideraron de alta precipitación.
Análisis de datos
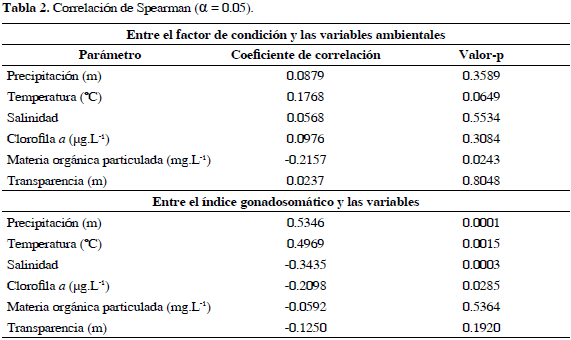
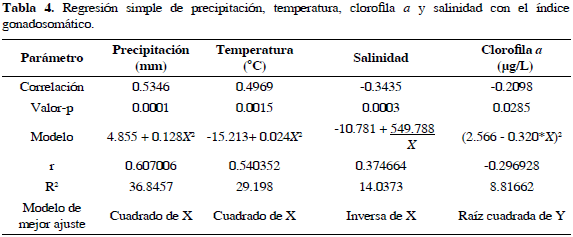
Se encontraron dos niveles de precipitacion significativamente diferentes durante el estudio, uno alto (> 3 mm) y otro bajo (< 3 mm) (Kruskal-Wallis, p = 0.00252; Tabla 1). También se demostró con la prueba de Spearman qué variables influían sobre el FC, observando la MOP como la única que se correlaciona con un p = 0.0243 (Tabla 2). Luego, para ver si la MOP afectaba de manera sustancial al FC se realizó una regresión simple, mostrando que la MOP no causaba cambios significativos al FC, con un índice de correlación de 4.53 (Tabla 3). En cuanto al IG, la precipitación, temperatura, salinidad y clorofila a mostraron una correlación significativa (Tabla 2), siendo la precipitación (p = 0.0001) y la temperatura (p = 0.0015) las que explicaron 36.84 y 29.19% de la variable respuesta (Tabla 4).
DISCUSIÓN
Las observaciones histológicas de las gónadas en el período de desove mostraron que algunos folículos estaban en parte desovados y en parte sin evidencias de evacuación, por lo que es probable que algunos ovocitos conservados en el ovario sean expulsados en uno o varios desoves posteriores. Esta emisión discreta de los gametos podría repetirse hasta producir la evacuación total de la gónada al final de la temporada de desove. También son probables la ocurrencia de más de un ciclo gametogénico durante el período de desove y las emisiones discretas de gametos, las cuales producen espacios vacíos en los folículos, como lo indican Salaya y Penchaszadeh (1978) para Pecten papiraceus de Venezuela.
Comúnmente los ciclos reproductivos incluyen un estadio de reposo tras la puesta, como fue en nuestro caso; sin embargo, existen excepciones en pectínidos, como Pecten novaezelandiae (Williams y Babcock, 2004), Chlamys varia (Iglesias, 2012) y Pecten maximus (Mason, 1958; Paulet, 1990) que mencionan que existe un estadio 0 sin presencia de folículos y sin sexo distinguible, folículos que han disminuido su diámetro, paredes foliculares cubiertas de gonias, gonoductos en su máxima expansión, presencia de numerosas células vesiculares y gran afluencia de amebocitos que fagocitan los gametos residuales. En el estadio II, la relación núcleo-citoplasma disminuye progresivamente a medida que se van desarrollando los ovocitos de A. nucleus (tamaño diámetro del núcleo de 6.2-8.0 µm), resultados comparables a los obtenidos por De la Roche (2008) e Iglesias (2012) para la especie Chlamys varia 6.77 ± 0.41 µm de diámetro. Además, el núcleo de los ovocitos de A. nucleus aumenta durante la ovogénesis; al mismo tiempo la cromatina se va dispersando, como señalan Lucas (1965) y Allarakh (1979). Ambos autores observan mayores tallas nucleares en los ovocitos previtelogénicos. Lucas (1965) describe núcleos de 6 µm en Chlamys varia y Allarakh (1979) de 7.5-10 µm en Aequipecten opercularis. Con este estudio, se confirma también la existencia de un polimorfismo en los ovocitos y en los espermatozoides durante la gametogénesis, dependiendo del estado de desarrollo gonadal, tal como se señala en varias especies de pectínidos: Chlamys varia, P. maximus, Aequipecten opercularis, entre otros (Román y Acosta, 1991; De la Roche, 2008; Iglesias, 2012).
El hecho de encontrar en dos de los once muestreos realizados organismos en estado de madurez sexual I y en porcentajes menores a 5%, y que el estadio predominante haya sido el III con un porcentaje de aparición de 60%, refuerza la idea de que estos animales poseen una alta capacidad de recuperación gonadal, gracias a su alta eficiencia para adquirir energía del alimento, minimizar los costos metabólicos y la pérdida de energía (Velasco, 2006, 2007). La baja frecuencia de animales en estadio I posiblemente indica que la gametogénesis reinició rápidamente y que la mayoría de ellos no declinaron a una etapa de reposo o el tiempo fue muy corto. Este comportamiento puede ser la causa de que en los muestreos se observara una baja y alta proporción de gónadas maduras y/o en proceso de liberación de gametos. Estos resultados concuerdan con los de Baqueiro et al. (1981) y Cáceres et al. (1990), que encontraron en Argopecten ventricosus una fase de reposo sexual corta, siendo pocos los organismos de esta especie que presentan un período de reposo e indiferenciación bien marcado después de los tiempos de desove.
Otra particularidad observada fue la existencia de desoves parciales, en los que se vio que una fracción de la gónada era translucida, mientras que otra aún tenía presencia de ovocitos y esperma; lo cual posiblemente ayudó a que la recuperación gonadal fuera más rápida. Autores como Brown y Guerra (1980) y Akaboshi e Illanes (1983) señalan que en A. purpuratus es difícil encontrar animales completamente desovados. Otros autores mencionan patrones de liberación de gametos parciales y continuos a lo largo de año en las especies: Argopecten ventricosus, Zygochlamys patagónica, Aequipecten tehuelchus y Nodipecten nodosus (Manzoni et al., 1996; Villalejo-Fuerte y Ceballos, 1996; Lasta et al., 1998; Narvarte y Kroeck, 2000). En este estudio se presentó únicamente un desove total para el muestreo del 3 de agosto, del 50% de los individuos, resultados similares a los de Velasco et al. (2007) quienes ensayaron diferentes tipos de inducción al desove, logrando 7% de organismos totalmente desovados, mientras que 93% fueron desoves parciales. Se puede suponer, entonces, que A. nucleus presentó una reproducción habitualmente continua a lo largo del período de estudio, es decir, que tiene varios eventos reproductivos a lo largo de su vida, pero generalmente son de baja intensidad (desoves parciales).
Períodos de maduración y de reproducción en bivalvos suelen coincidir con cambios ambientales (Maru, 1976; Giese y Pearse, 1979), pero también hay que tener en cuenta que el ciclo gametogénico es controlado genéticamente y que, después de alcanzar cierto estado fisiológico en un organismo expuesto a unas condiciones óptimas, se inicia el desarrollo de la gónada; por lo tanto, existen dos factores principales que afectan los eventos reproductivos en bivalvos, llamados factores exógenos y endógenos (Román et al., 2001). Sin embargo, en este trabajo solo se enfatiza en algunos de los factores exógenos a los cuales estuvieron expuestos los organismos en sistema de cultivo suspendido.
En algunos muestreos el IG bajó; según Pereira (1985), la disminución en los valores de los índices gonadosomáticos, se relacionan directamente con períodos de liberación de gametos. Este evento posiblemente se debió a las altas precipitaciones (4.99 mm) que conllevaron a un aumento en los valores de la MOP y en la clorofila a. En esta época de altas precipitaciones posiblemente los individuos guardaron reservas de energía de la gran cantidad de alimento suministrado por el medio, importante en el desarrollo de los gametos, proceso energéticamente costoso que depende fuertemente de la movilización de nutrientes para su cumplimiento; por lo tanto, el ciclo gametogénico y las reservas energéticas son dos procesos diferentes pero íntimamente relacionados (Román et al., 2001).
En agosto hubo 50% de animales desovados totalmente, siendo el único período donde se presentó este caso y una recuperación gonadal lenta, evidenciándose la presencia de diferentes estadios gonadales en los muestreos siguientes; este evento se asocia a un valor de temperatura de 30 °C y MOP de 1.48 mg.L-1, siendo la temperatura considerada como uno de los factores ambientales más importantes que regulan la reproducción en bivalvos (Sastry, 1979). La mayoría de los bivalvos tienden a desovar durante los períodos cuando el alimento está disponible para el desarrollo de la progenie (Bayne, 1976). Por otra parte, Jaramillo et al. (1993), Lodeiros et al. (1998) y Racotta et al. (2003) examinaron la gametogénesis de Z. patagónica, N. nodosus y N. subnodosus, demostrando que probablemente la disponibilidad de alimento está relacionada con el desarrollo gonadal.
A partir del 6 de julio las variables ambientales se comportaron con una tendencia diferente, dado que aumentaron la precipitación, la MOP y la temperatura mientras que la salinidad, la transparencia y la clorofila a bajaron. Además, el aumento de la precipitación produce la descarga de agua dulce, lo que ocasiona el incremento de la temperatura y de la productividad, así como la disminución de la visibilidad y de la salinidad superficial (Freites et al., 1993; Lodeiros et al., 1993); por lo tanto estos factores influyen en los organismos, ya que A. nucleus aparentemente cuando está en su mayor grado de madurez puede desovar frente a un cambio de cualquier parámetro ambiental (Barros, 2004).
En el presente estudio, de las variables que estarían controlando el ciclo gametogénico de A. nucleus en la bahía de Nenguange, la precipitación parece ser la principal, explicando 36.8% (p = 0.0001) en sus variaciones, siguiendo en orden de influencia la temperatura con 29.2% (p = 0.0015), la salinidad con 14.0% (p = 0.0003) y la clorofila a con 8.8% (p = 0.0285) (Tablas 2 y 4). Resultados similares son registrados por otros autores quienes han estudiado el ciclo y acondicionamiento reproductivo de varias especies de pectínidos como P. maximus, A. ventricosus, A. purpuratus y E. ziczac, demostrando que el ciclo gametogénico dentro de cada una de estas especies varia significativamente, dependiendo de las condiciones ambientales de cada lugar; siendo la temperatura y la disponibilidad de alimento uno de los factores de mayor importancia en el inicio y desarrollo del ciclo reproductivo en los bivalvos (Baqueiro et al.,1981; Illanes et al., 1985; Pazos et al., 1996; Borzone et al., 2003; Cantillánez et al., 2005; Magnesen y Christophersen, 2008).
AGRADECIMIENTOS
Los autores expresan sus agradecimientos al Banco de Proyectos de Inversión Nacional por la financiación de este estudio, que hizo parte del trabajo de grado de la primera autora. También al equipo del Laboratorio de Bioprospección Marina del Invemar y a la Línea de Bioprospección Marina del Programa de Valoración y Aprovechamiento de los Recursos donde se llevó a cabo el proyecto.
BIBLIOGRAFÍA
1 Akaboshi, S. y J. Illanes. 1983. Estudio experimental sobre la captación, pre-cultivo y cultivo, en ambiente natural de Chlamys (Argopecten) purpurata, Lamarck 1819, en Bahía Tongoy, IV región, Coquimbo. 233-254. En: Fuentes, H., J. Castillo y L. Disalvio (Eds.). Simposio Internacional Avances y Perspectivas de la Acuacultura en Chile, Coquimbo, Chile. 320 p. [ Links ]
2 Allarakh, C. 1979. Reserches histologiques et experimentales de la différenciation sexuelle et du cycle de reproduction de Chlamys opercularis L. (Mollusque lamellibranche). Tesis doctoral. U. E. R. des Sciences de la Vie et du Comportement. Universidad de Caen, Francia. 148 p. [ Links ]
3 Avendaño, M., M. Cantillánez, M. Le Pennec, C. Lodeiros y L. Freites. 2001. Cultivo de pectínidos iberoamericanos en suspensión. 193-211. En: Maeda-Martínez, A. (Ed.). Los moluscos pectínidos de Iberoamérica: ciencia y acuicultura. Editorial Limusa, México D. F. 501 p. [ Links ]
4 Baqueiro, C., I. Peña y J. Massó. 1981. Análisis de una población sobre explotada de Argopecten circularis (Sowerby. 1835) en La Ensenada de La Paz, B. C. S., México. Cienc. Pesq. Inst. Nal. Pesca, 1 (2): 57-65. [ Links ]
5 Barros, J. 2004. Ensayos de reproducción artificial de la vieira Argopecten nucleus Born, 1780 (Bivalvia: Pectinidae) en condiciones controladas. Tesis Ingeniero Pesquero, Univ. Magdalena, Santa Marta. 90 p. [ Links ]
6 Bayne, B. L. 1976. Marine mussels: Their ecology and physiology. Cambridge University Press, Cambridge. 506 p. [ Links ]
7 Borzone, C., P. Pezzuto e Y. García Tavares. 2003. Características histológicas del ciclo reproductivo de Euvola ziczac (Linnaeus) (Pectinidae, Bivalvia) del litoral sur-este del Brasil. Rev. Bras. Zool., 20 (4): 763-772. [ Links ]
8 Brown, D. y R. Guerra. 1980. Recuperación gonadal en ostión Chlamys (Argopecten) purpurata (Lamarck 1819) luego de evacuación de gametos. Arch. Biol. Med. Exp., 13 (3): 363-368. [ Links ]
9 Cáceres, C., C. Ruiz y M. Rodríguez. 1990. Variaciones estacionales del índice gonádico y muscular de Argopecten circularis (Sowerby, 1835) en la Ensenada de La Paz, B. C. S., México. Invest. Mar. Cicimar, 5 (1): 1-6. [ Links ]
10 Cantillánez, M., M. Avendaño, G. Thouzeau y M. Le Pennec. 2005. Reproductive cycle of Argopecten purpuratus (Bivalvia: Pectinidae) in La Rinconada marine reserve (Antofagasta, Chile): Response to environmental effects of El Niño and La Niña. Aquaculture, 246: 181-195. [ Links ]
11 Castellanos, C. y N. Campos. 2007. Variación espacial y temporal de juveniles de Pinctada imbricata (Röding, 1798) y Argopecten nucleus (Born, 1778) en la región norte del Caribe colombiano. Bol. Inv. Mar Cost., 36: 209-227. [ Links ]
12 Chávez, G. y V. Ishiyama. 1989. Reproducción en Argopecten purpuratus en la bahía Independencia (Pisco, Perú). 295-300. En: Memorias del Simposio Internacional de los Recursos Vivos y las Pesquerías en el Pacífico Sudeste. Revista Pacífico Sur (número especial). 350 p. [ Links ]
13 Cochard, J. C. y N. Devauchelle. 1993. Spawning, fecundity and larval growth in relation to controlled conditioning in native and transplanted populations of Pecten maximus: evidence for the existence of separate stocks. J. Exp. Mar. Exp. Biol., 169: 41-56. [ Links ]
14 De la Roche, J. P. 2008. Ciclo reproductor y anatomía funcional de la gónada de Chamys varia (Linnaeus, 1758). Tesis doctoral, Univ. Santiago de Compostela, Chile. 336 p. [ Links ]
15 De la Roche, J. P. y A. Vélez. 1997. Descripción del desarrollo larval de la vieira "pata de león" Nodipecten nodosus bajo condiciones de laboratorio. 50-55. En: VII Congreso Latinoamericano de Ciencias del Mar (Colacmar), Sao Paulo. 238 p. [ Links ]
16 Fernández, I. 1991. Reproducción y acondicionamiento de bivalvos en el criadero. Consellería de pesca, marisqueo e acuicultura. Editorial Alva A Coruña, Coruña, España. 35 p. [ Links ]
17 Freites, L., A. Vélez y C. Lodeiros. 1993. Crecimiento y productividad de la vieira Euvola (Pecten) ziczac bajo varios sistemas de cultivo suspendido. Mem. IV Congr. Latinoam. Ciencias del Mar, Serie Ocasional, Chile, 2: 259-269. [ Links ]
18 Garay, J., G. Ramírez, J. Betancourt, B. Marín, B. Cadavid, L. Panizzo, L. Lesmes, J. Sánchez, H. Lozano y A. Franco. 2003. Manual de técnicas analíticas para la determinación de parámetros fisicoquímicos y contaminantes marinos: aguas, sedimentos y organismos. Serie de Publicaciones Generales del Invemar No. 13, Santa Marta. 177 p. [ Links ]
19 Giese, A. y J. Pearse. 1979. Introduction: general principles. 1-49. En: Giese, A. y J. Pearse (Eds.). Reproduction of marine invertebrates. Vol. 1, Academic, Nueva York. 546 p. [ Links ]
20 Gómez-León, J. 2005. Estudio epizoótico de agentes patógenos en almeja fina (Ruditapes decussatus) cultivada en Galicia. Tesis de Doctorado en Ciencias Biológicas, Univ. Santiago de Compostela, España. 220 p. [ Links ]
21 González, M., D. López, M. Pérez, V. Riquelme, J. Uribe y M. Le Pennec. 1999. Growth of the scallop, Argopecten purpuratus (Lamarck, 1819), in southern Chile. Aquaculture, 175: 307-316. [ Links ]
22 González, P. y C. Oyarzún. 2002. Biological index variability in Pinguipes chilensis Valenciennes 1833 (Perciformes, Pinguipedidae): Are they correlated? Gayana, 66 (2): 249-253. [ Links ]
23 Helm, M., N. Bourne y A. Lovatelli. 2006. Cultivo de bivalvos en criadero, un manual práctico. FAO Doc. Técn. Pesca No. 471, FAO, Roma. 182 p. [ Links ]
24 Iglesias, P. 2012. Estudio de la reproducción y reclutamiento de los pectínidos de interés comercial de las rías gallegas. Tesis de Doctorado en Ciencias Biológicas, Univ. Santiago de Compostela, Chile 310 p. [ Links ]
25 Illanes, J., S. Akaboshi y E. Uribe. 1985. Efectos de la temperatura en la reproducción del ostión del norte Chlamys (Argopecten) purpuratus en la bahía Tongoy durante el fenómeno El Niño. Invest. Pesq. Chile., 32: 167-173. [ Links ]
26 Invemar. 2005. Informe del Estado de los Ambientes Marinos y Costeros en Colombia: Año 2005. Serie de Publicaciones Periódicas del Invemar No. 8, Santa Marta. 360 p. [ Links ]
27 Invemar. 2009. Cultivo piloto experimental de los bivalvos (Pinctada imbricata, Pteria colymbus y Argopecten nucleus) como sistema productivo alternativo a formas de subsistencia tradicional en Bahía Portete, departamento de La Guajira, Caribe colombiano. Informe final, Invemar, Santa Marta. 120 p. [ Links ]
28 Jaramillo, R., J. Winter, J. Valencia y A. Ribera. 1993. Gametogenic cycle of the Chiloe scallop (Chlamys amandi). J. Shell. Res., 12 (1): 59-64. [ Links ]
29 Lasta, M., N. Ciocco, C. Bremec y A. Roux. 1998. Moluscos bivalvos y gasterópodos. El mar argentino y sus recursos pesqueros. Inidep, 1046 (2): 115-142. [ Links ]
30 Lodeiros, C., L. Freites, M. Núñez y J. H. Himmelman. 1993. Growth of the Caribbean scallop Argopecten nucleus (Born 1970) in suspended culture. J. Shell. Res., 2 (12): 291-294. [ Links ]
31 Lodeiros, C., J. Rengel, L. Freites, F. Morales y J. Himmelmen. 1998. Growth and survival of the tropical scallop Lyropecten (Nodipecten) nodosus maintained in suspended culture at three depths. Aquaculture, 165: 41-50. [ Links ]
32 López, J. 2008. Crecimiento y supervivencia del scallop Nodipecten nodosus (Linnaeus, 1785) (Bivalvia: Pectinidae), en cultivo suspendido, bahía de Nenguange, Parque Nacional Natural Tayrona, Caribe Colombiano. Tesis Ingeniería Pesquera, Univ. Magdalena, Santa Marta. 54 p. [ Links ]
33 Lorenzen, C. J. 1967. Determination of chlorophyll and pheopigments spectronic equations. Limnol. Oceanogr., (12): 343-346. [ Links ]
34 Lubet, P. 1959. Recherches sur le cycle sexual et l'emission des gametes chez le Mytilides et les Pectinides (mollusques bivalves). Rev. Trav. l'Inst. Peches Marit., 23: 387-548. [ Links ]
35 Lucas, A. 1965. Recherche sur la sexualité des mollusques bivalves. Tesis doctoral. Facultad de Ciencias. Universidad de Rénnes, Francia. 136 p. [ Links ]
36 Magnesen, T. y G. Christophersen, 2008. Reproductive cycle and conditioning of translocated scallops (Pecten maximus) from five broodstock populations in Norway. Aquaculture, 285: 109-116. [ Links ]
37 Manzoni, G., C. Poli y G. Rupp. 1996. Período reproductivo del pectínido Nodipecten nodosus (Mollusca: Bivalvia) en los alrededores de la Isla do Arvoredo (27°17'S-48°22'W) Santa Catarina, Brasil. 197-201. En: Silva, A. y G. Merino (Eds.). Acuicultura en Latinoamérica: IX Congreso Latinoamericano de Acuicultura. II Simposio de avances y Perspectivas de la Acuicultura en Chile. Coquimbo, Chile. 245 p. [ Links ]
38 Maru, K. 1976. Studies on the reproduction of a scallop, Patinopecten yessoensis (Joy)-I. Reproductive cycle of the cultured scallop. Sci. Rep. Hokkaido Fish. Exp. Stn., 18: 9-26. [ Links ]
39 Mason, J. 1958. The breeding of the scallop, Pecten maximus (L.), in Manx Waters. J. Mar. Biol. Assoc. U. K., 37: 653-671. [ Links ]
40 Narvarte, M. y M. Kroeck. 2000. Reproducción de la vieira tehuelche A. tehuelchus en el golfo San Matías. 11-15. En: Actas Jornadas Nacionales de Ciencias del Mar. Puerto Madryn, Argentina. 94 p. [ Links ]
41 Paulet, Y. M. 1990. Role de la reproduction dans le déterminisme du recrutement chez Pecten maximus (L) de la baie de Saint-Brieuc. Tesis doctoral. Université de Bretagne Occidentale-Brest, Brest, Francia. 194 p. [ Links ]
42 Pazos, A. J., G. Román, C. P. Acosta, M. Abdal y J. L. Sánchez. 1996. Stereological studies on the gametogenic cycle of the scallops, Pecten maximus, in suspended culture in Ría de Arousa (Galicia NW Spain). Aquaculture, 142: 119-135. [ Links ]
43 Pereira, L. 1985. Reproducción, captación, precultivo y cultivo de Chlamys (Argopecten) purpurata (Lamark, 1819) de ambiente natural en la IV Región. Instituto Profesional de Osorno, Osorno, Chile. 48 p. [ Links ]
44 Pereira, M. y J. Ferreira. 2006. Eficiência comparada do cultivo da vieira Nodipecten nodosus (Linnaeus, 1758) (Bivalvia: Pectinidae) em diferentes densidades e profundiades. Biotemas, 19 (2): 37-45. [ Links ]
45 Racotta, I., J. Ramírez, A. Ibarra, M. Rodríguez, D. Carreño y E. Palacios. 2003. Growth and gametogenesis in the lion-paw scallop Nodipecten (Lyropecten) subnodosus. Aquaculture, 217: 335-349. [ Links ]
46 Ramírez, G. 1983. Características fisicoquímicas de la bahía de Santa Marta. An. Inst. Invest. Mar. Punta Betín, 13: 111-121. [ Links ]
47 Román, G. y C. P. Acosta. 1991. Reproductive and reserve storage cycles in Pecten maximus reared in suspension. I: soft tissue growth and reproduction. 27-59. En: Actes des Colloques 8th Int. Pectinid Workshop. Cherbourg, Francia. [ Links ]
48 Román, G., G. Martínez, O. García y L. Freites. 2001. Reproducción. 27-59. En: Maeda-Martínez, A. N. (Ed). Los moluscos pectínidos de Iberoamérica: Ciencia y acuicultura. Editorial Limusa, México D. F. 501 p. [ Links ]
49 Salaya, J. J. y P. E. Penchaszadeh. 1978. Contribución al conocimiento de la reproducción de la vieira Pecten papyraceus en Venezuela. II Simposio de la Asociación Latinoamericana de Acuicultura, México D. F. 26 p. [ Links ]
50 Sastry, A. N. 1963. Reproduction of the bay scallop, Aequipecten irradians Lamarck. Influence of temperature on maturation and spawning. Biol. Bull., 125 (1): 146-153. [ Links ]
51 Sastry, A. N. 1979. Pelecypoda (excluding Ostreidea). 113-292. En: Giese, A. y J. Pearse (Eds.). Reproduction of marine invertebrates. Academic Press, Nueva York. 546 p. [ Links ]
52 Urban, H. 1999. Cultivo de bivalvos en el Caribe colombiano. Diagnóstico y evaluación de la factibilidad biológica, técnica y económica del cultivo experimental de bivalvos de interés comercial en el Caribe colombiano. Informe técnico final. Instituto de Investigaciones Marinas y Costeras (Invemar), Santa Marta. 212 p. [ Links ]
53 Valero, A., S. Sánchez, C. García, A. Córdoba, J. de La Roche, J. Gómez, C. Castellanos, C. Torres, M. Rueda, C. Hernández, R. Bautista, J. Assmus e Y. Caballero. 2000. Cultivo de bivalvos marinos del Caribe colombiano. Colombia: Cienc. Tecnol., 18 (13): 10-16. [ Links ]
54 Velasco, L. A. 2006. Effect of microalgal concentration and water temperature on the physiology of the Caribbean scallops Argopecten nucleus and Nodipecten nodosus. J. Shellfish Res., 25: 823-831. [ Links ]
55 Velasco, L. A. 2007. Energetic physiology of the Caribbean scallops Argopecten nucleus and Nodipecten nodosus fed with different microalgal diets. Aquaculture, 270: 299-212. [ Links ]
56 Velasco, L. A. 2008. Acondicionamiento reproductivo de los pectínidos de interés comercial de Colombia. 65-85. En: Velasco, L. A. (Ed.). Biología y cultivo de los pectínidos de interés comercial de Colombia. Editorial Unimagdalena, Santa Marta. 258 p. [ Links ]
57 Velasco, L. A., J. Barros y E. Acosta. 2007. Spawning induction and early development of the Caribbean scallops Argopecten nucleus and Nodipecten nodosus. Aquaculture, 272: 767-773. [ Links ]
58 Villalejo-Fuerte, M. 1992. Aspectos reproductivos de la almeja catarina Argopecten circularis (Sowerby 1835) en Bahía Concepción, B. C. S. México. Tesis Maestría Cicimar-IPN, La Paz, México. 75 p. [ Links ]
59 Villalejo-Fuerte, M. y B. Ceballos. 1996. Variaciones de los índices de condición general, gonádica y de rendimiento muscular en Argopecten circularis (Bivalvia, Pectinidae). Rev. Biol. Trop., 44 (2): 591-594. [ Links ]
60 Williams, J. R. y R. C. Babcock. 2004. Comparison of multiple techniques to evaluate reproductive variability in a marine bivalve: application to the scallop Pecten novaezelandiae. Mar. Freshwater Res, 55: 457-468. [ Links ]
FECHA DE RECEPCIÓN: 07/02/2012 FECHA DE ACEPTACIÓN: 21/10/2014
*Contribución No. 1148 del Instituto de Investigaciones Marinas y Costeras (Invemar).