Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Boletín de Investigaciones Marinas y Costeras - INVEMAR
Print version ISSN 0122-9761
Bol. Invest. Mar. Cost. vol.44 no.2 Santa Marta July/Dec. 2015
UNA METODOLOGÍA NO INVASIVA PARA LA EXTRACCIÓN DE ADN DE CORYPHAENA HIPPURUS
A NON-INVASIVE METHOD FOR EXTRACTING DNA FROM CORYPHAENA HIPPURUS
Bruna Rafaela Caetano Nunes Pazdiora1, John Josephraj Selvaraj2, Diego Fernando Marmolejo3, Jaime Eduardo Muñoz2 y Ángela Inés Guzmán2
1 Universidade Federal de Rondônia (UNIR), Departamento de Engenharia de Pesca. Rua da Paz, 4376, Bairro Lino Alves, Presidente Médici, Brasil, CEP: 76916-000. bruna.nunes@unir.br
2 Universidad Nacional de Colombia, sede Palmira, Carrera 32, Chapinero via Candelaria, Palmira, Colombia. jojselvaraj@unal.edu.co, jemunozf@unal.edu.co, aiguzmana@unal.edu.co
3 Universidade Estadual Norte Fluminense Darcy Ribeiro (UENF), Av. Alberto Lamego, 2000. Parque Califórnia, Campos dos Goytacazes, Rio de Janeiro, Brasil, CEP: 28013-602. diegomarmol82@hotmail.com.
RESUMEN
Se evaluó un protocolo de extracción de ADN y el efecto de este en la obtención de muestras de alta cantidad y calidad para estudios moleculares. El ADN de 25 individuos se extrajo de la digestión del músculo y de la aleta dorsal con proteinasa K y el kit de extracción de sangre y tejido animal. Se obtuvo ADN en todos los tipos de muestras; sin embargo, las muestras obtenidas a partir de aletas dorsales mostraron significativamente mayor cantidad de ADN en comparación con las del músculo. Por lo que la definición de una metodología apropiada de extracción de ADN puede contribuir a estudios de la estructura genética de la especie. Por otra parte, la extracción de ADN de aletas dorsales en dorados representa un método no invasivo, haciendo de esta técnica una alternativa ambiental, social y comercialmente viable en la recolecta de muestras, debido a que no requiere el sacrificio del animal y no altera su valor económico.
PALABRAS CLAVE: Aleta dorsal, ADN, Dorado, Pacífico colombiano.
ABSTRACT
A protocol for DNA extraction and effect of the type of tissue material for obtaining DNA from dolphinfish in high quantity and quality for molecular studies was evaluated. The DNA of 25 individuals was extracted from the digestion of the muscle and the dorsal fin, with proteinase K, and the extraction kit for blood and animal tissue. DNA were obtained in all the samples; however, dorsal fins samples showed significantly higher amount of DNA than muscle samples. The definition of an appropriate methodology of DNA extraction can contribute to studies of genetic structure of the species. DNA extraction from dolphinfish dorsal fins, non-invasive method, is an alternative that is environmentally, socially, and commercially viable, where sample collection does not require the sacrifice of the animal and do not alter its economic value.
KEY WORDS: Dorsal fin, DNA, dolphinfish, Colombian Pacific.
Junto con otras especies pelágicas, el dorado (Coryphaena hippurus) es un importante recurso pesquero, suministra seguridad alimentaria y sustento para la pesca artesanal y semindustrial en el Pacífico colombiano (Lasso y Zapata, 1999). Sin embargo, no se conocen estudios regionales de la estructura genética de la especie, de su variabilidad genética dentro o entre la(s) población(es). La identificación de las poblaciones es esencial en los programas de control y conservación de variabilidad genética y, consecuentemente, en programas de manejo y conservación de la especie (Avise, 2000).
La colecta y conservación de las muestras para la obtención de ADN de alta calidad es parte clave de los diferentes protocolos de análisis genéticos. En la obtención de muestras se utilizan métodos invasivos y no invasivos. Los primeros usan muestras de tejidos internos (músculo, hígado, riñón), que pueden producir la muerte del animal, además de dañar la materia prima en la comercialización (Tripp-Váldez et al., 2010). La segunda no necesita sacrificar el animal, el ADN es extraído a partir de tejidos como: aletas, sangre, células bucales, escamas y óvulos que se conservan en alcohol etílico 70 o 100% (Lopera-Barrero et al., 2008).
La aplicación de la biología molecular en especies acuáticas presenta varios inconvenientes, puesto que no existen protocolos estandarizados para trabajar distintos tipos de muestras como músculo, aleta, sangre, de acuerdo con cada especie; principalmente si la especie es escasa en su hábitat, lo recomendable es usar técnicas no invasivas, rápidas, prácticas, de bajo costo, libre de contaminación y de toxicidad, que no dañe los animales y eficaces en cuanto a la calidad y cantidad del ADN. Por lo tanto, el objetivo de la presente investigación fue evaluar un protocolo de extracción de ADN en dos tipos de tejido (aleta o músculo) en C. hippurus.
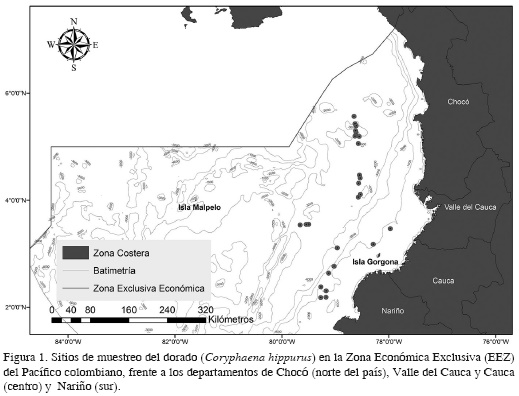
Se recogieron muestras de dorados en los sitios históricamente productivos, identificados por los frentes térmicos (Selvaraj et al., 2011) (Figura 1). Los peces fueron capturados utilizando el palangre de superficie o línea de anzuelos como arte de pesca. Para la estandarización del protocolo de extracción de ADN, se sacó aproximadamente 5 cm de la aleta dorsal y del músculo de 25 individuos adultos de dorado, se preservaron en alcohol etílico a 70% y fueron mantenidos bajo refrigeración (4ºC) hasta su análisis en laboratorio.
El ADN fue extraído a partir de la digestión de la aleta dorsal o del músculo, con proteinasa K, utilizándose el kit de extracción de ADN para sangre y tejido animal DNeasy® Blood&Tissue, Quiagen. La cuantificación del ADN (en ηg/µl) se hizo siguiendo la metodología sugerida por Valentim et al. (2003). La calidad del ADN fue probada utilizando la técnica de PCR (Reacción en Cadena de la Polimerasa), utilizándose cebadores específicos para el gen mitocondrial NADH deshidrogenasa subunidad 1(ND1) del dorado (Wingrove, 2000). La amplificación del fragmento fue realizada siguiendo los protocolos registrados por Díaz-Jaimes et al. (2006).
Para determinar diferencias significativas entre los dos tipos de tejidos, en relación al contenido de ADN extraído, se aplicó una prueba t para muestras independientes (músculo vs. aleta), con el software Statistica 12.0 (Statsoft, 2015). El número de muestras fue 25 (N=25).
En todas las muestras de aleta dorsal y músculos se obtuvieron bandas de ADN. Sin embargo, las muestras de aleta presentaron una mayor cantidad de ADN extraído, donde el promedio de concentración fue de 60 a 100 ηg/µl, mientras que en el músculo fue de 10 a 40 ηg/µl. Esta diferencia fue significativa (p<0.05) (Tabla 1). Por lo tanto, las aletas mostraron mejores resultados que el músculo, y se recomienda para amplificaciones futuras de ADN, y para estudios de variabilidad genética, utilizando por ejemplo el secuenciamiento o marcadores moleculares.
La diferencia en cantidad en la extracción de ADN puede deberse además del tejido usado, a la especie y al protocolo de los procedimientos realizados para cada tejido y para cada especie. Por esta razón es necesaria la estandarización de un protocolo para cada especie, que puede usarse como una guía de trabajo de laboratorio en estudios futuros de conservación genética.
Las muestras de tejidos acondicionadas en alcohol al 70% y mantenidas bajo refrigeración (4ºC) mantuvieron su calidad y buen estado de conservación del ADN después de un largo tiempo de colecta (17-20 meses), haciendo posible los análisis en largo tiempo. Resultados similares fueron obtenidos en la extracción de ADN en peces cartilaginosos, donde las muestras fueron preservadas en etanol, se les adicionó un buffer de extracción sin proteasa, y fueron mantenidas a -20°C (Hleap et al., 2009).
En el presente estudio, el ADN extraído de todas las muestras de aletas lograron amplificación en la metodología de PCR, presentando bandas visibles entre 700 y 800pb, coincidiendo con los resultados esperados para un fragmento de 751pb. Por lo tanto, las muestras de aletas, además de presentar la cantidad de ADN suficiente, también muestran la calidad necesaria para los estudios moleculares. Resultados similares se obtuvieron en la extracción de ADN utilizando escamas de especies en peligro de extinción como: Gibelion catla, Labeo rohita, L. calbasu, L. bata, Cirrhinus cirrhosus, Channa punctata y Cyprinus carpio (Kumar et al., 2007).
La extracción de ADN de calidad de aleta dorsal de dorado (Coryphaena hippurus), metodología no invasiva, es una buena alternativa ambiental y socio-comercial, lo que puede favorecer la cooperación entre investigadores y pescadores, para tomar muestras genéticas y/o no alterar el valor comercial de los peces. En conjunto, toda esta información es de utilidad para futuras investigaciones genéticas, contribuyendo al conocimiento de la estructura de las poblaciones y la conectividad marina, las cuales son importantes en el diseño e implementación de reservas marinas para la protección de especies amenazadas por la sobreexplotación y la degradación de hábitat, especialmente en zonas oceánicas donde la obtención de muestras tiene un costo elevado.
AGRADECIMIENTOS
Los autores agradecen a la Universidad Nacional de Colombia Vicerrectoría de Investigación, Dirección de Investigaciones de Palmira (DIPAL). Al Ministerio de Agricultura y Desarrollo Rural que financió el Proyecto "Identificación y evaluación de nuevas áreas de pesca para grandes pelágicos en el Pacifico colombiano". A la empresa pesquera Sepúlveda Rogers Cía. Ltda. A los pescadores artesanales "Los Amigos" especialmente a Don Guille.
BIBLIOGRAFÍA
Avise, J.C. 2000. Phylogeography: The history and formation of species. Harvard University Press, Cambridge. 447 p. [ Links ]
Díaz-Jaimes, P., M. Uribe-Alcocer, S. Ortega-García y D. Jean-Dominique. 2006. Spatial and temporal mitochondrial DNA genetic homogeneity of dolphinfish populations (Coryphaena hippurus) in the eastern central Pacific. Fish.Res., 80(2006): 333-338. [ Links ]
Hleap, J.S., H. Cárdenas y F. García-Vallejo. 2009. Preservación no criogénica de tejido y extracción de ADN: una aplicación para peces cartilaginosos. Pan-Am. J. Aquat. Sci., 4(4): 545-555. [ Links ]
Kumar, R., P.J Singh, N.S. Nagpure, B. Kushwaha, S.K. Srivastava y W.S. Lakra. 2007. A non-invasive technique for rapid extraction of DNA from fish scales. Indian J. Exp. Biol., 45: 992-997. [ Links ]
Lasso, J. y L. Zapata.1999. Fisheries and biology of Coryphaena hippurus (Pisces: Coryphaenidae) in the Pacific coast of Colombia and Panama. Sci. Mar., 63: 387-399. [ Links ]
Lopera-Barrero, N., J.A. Povh, R.P. Ribeiro, P.C. Gomes, C.B. Jacometo y T.S. Lopes. 2008. Comparación de protocolos de extracción de ADN con muestras de aleta y larva de peces: extracción modificada con cloruro de sódio. Cien. Inv. Agr., 35(1): 77-86. [ Links ]
Selvaraj, J., A.I. Guzmán y A. Martínez. 2011. Guía para identificación de áreas de pesca para grandes pelágicos en el Pacífico colombiano. Universidad Nacional de Colombia y Ministerio de Agricultura y Desarrollo Rural. Palmira, Colombia. 40 p. [ Links ]
Statsoft, Inc. 2015. Statistica Base Edition giving you the statistical and reporting essentials to start improving your analysis. http://www.statsoft.com/Products/STATISTICA/Base. 30/07/2015. [ Links ]
Tripp-Valdez, M.A., F.J. García-León, S. Ortega-García, D. Lluch-Cota, J. López-Martínez y P. Cruz. 2010. Population genetic structure of dolphinfish (Coryphaena hippurus) in the Gulf of California, using microsatellite loci. Fish. Res., 105: 172-177. [ Links ]
Valentim, M., L. Vargas, H.M. Moreira y R.P. Ribeiro. 2003. Comparação de protocolos para extração do DNA de Lernaea sp. (Copepoda: Cyclopoida). Acta Scientiarum, 25(2): 219-222. [ Links ]
Wingrove, R.S. 2000. The population structure of dolphin, Coryphaena hippurus L. 1758, in the western central Atlantic, Gulf of Mexico and eastern Caribbean Sea inferred from mitochondrial DNA variation. Tesis of Mastery, Department of Biology, College of Charleston. Charleston, EE.UU. 92 p. [ Links ]
RECIBIDO: 01/10/2014 ACEPTADO: 06/08/2015