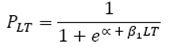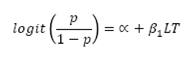INTRODUCCIÓN
La pesca de captura a nivel mundial representó unas 86.6 millones de toneladas en 2012, siendo la captura de camarón con 3.4 millones de toneladas la pesquería que representa una de las principales fuentes de ingresos y alimentos del sector pesquero a nivel mundial, aportando en los últimos años 15.5% del valor total de las exportaciones mundiales de productos pesqueros (FAO, 2014). No obstante, la pesca de captura de camarón por arrastre genera en función de las áreas de pesca no solo un impacto ambiental sobre la fauna asociada al camarón (Girón et al., 2010, Invernar, 2014a), sino un efecto poco evaluado sobre la estructura poblacional de la captura objetivo.
La pesca de arrastre dirigida a la captura de camarones en el Pacífico colombiano se desarrolla desde hace 50 años y representa la actividad pesquera de mayor importancia económica y social para los pobladores del litoral Pacífico (De la Pava y Mosquera, 2001; Girón et al., 2010). Dos flotas ejercen esta actividad, las cuales operan en función de la profundidad, una de ellas extrae camarón de aguas someras (CAS; en profundidades hasta 40 m), teniendo como objetivo el camarón blanco (Litopenaeus occidentalis), capturado secuencialmente por las pesquerías artesanal e industrial con un estado actual de sobre explotación (Rueda et al., 2006). La otra flota por su parte opera en profundidades que van desde 40 hasta 250 m y su objetivo principal es el camarón pink (Farfantepenaeus brevirostris), sin influencia de la pesca artesanal con un estado actual de plena explotación (Rueda et al., 2010; Rodríguez et al., 2012). Farfantepenaeus brevirostris se distribuye desde California hasta Perú y en la costa Pacífica colombiana se encuentra principalmente entre 40 y 160 m, con mayores agregaciones en la región norte (departamento de Chocó; Rodríguez et al., 2012).
La flota del CAP, pese a los problemas de operación que afronta tales como el alto costo de combustible y la inestabilidad de los precios del mercado, en 2014 desembarcó cerca de 372.8 t, de las cuales F. brevirostris representó cerca de 95.2% con ingresos promedios de $32.1 millones por faena (Invernar, 2014b). Este margen de utilidad despierta en años recientes el interés de más armadores para ejercer la actividad sobre este recurso; por tanto, la Autoridad Pesquera ha respondido con algunas medidas para controlar la explotación de este recurso, entre ellas cuotas de pesca, no expedición de más patentes de pesca y veda de camarón. Con fines de evaluar el efecto de esta pesquería sobre la población de F. brevirostris en los últimos años, este estudio aborda un seguimiento a siete años de información sobre los aspectos reproductivos y estructura de tallas de esta especie en el Pacífico colombiano, con fines de brindar información actualizada para diseñar estrategias de manejo basadas en la talla media de madurez y la talla media de captura.
ÁREA DE ESTUDIO
El Pacífico colombiano se caracteriza por diferentes condiciones oceanográficas a lo largo de la costa que delimitan varias zonas en el litoral: I) el área norte que va desde la frontera con Panamá (7° 12' N - 77° 53' O) hasta Cabo Corrientes (5° 29' N), departamento de Chocó, II) el área centro desde Cabo Corrientes hasta Pasacaballos (2° 30' N) y III) el área sur desde Pasacaballos hasta límites con Ecuador (1° 25' N - 78° 54' O; Invernar, 2008) en el departamento de Nariño. La zona norte se caracteriza por la presencia de acantilados, una plataforma profunda y estrecha de aproximadamente 1.8 a 3.7 km con sustrato predominantemente rocoso con presencia de arenas carbonatadas biogénicas y arenas lodosas (Díaz et al., 1997; Beltrán y Ríos, 2000; Zapata, 2000). La zona centro y sur, entre Cabo Corrientes y la Bahía Ancón de sardinas en la frontera con Ecuador, presenta una plataforma más extensa y llena de sedimentos, en su mayoría de origen fluvial provenientes de numerosos ríos que desembocan en la costa (Díaz et al., 1997). La zona de convergencia intertropical es la que regula el clima del Pacífico, con alta nubosidad e intensas lluvias generadas por la inestabilidad de las masas de aire húmedo y caliente que allí se presentan (Tchantsev y Cabrera, 1998; Poveda et al., 2001). Dichas áreas constituyen las zonas de pesca de la flota de arrastre para camarón de aguas profundas (CAP) en el Pacífico cuyo principal objetivo es el camarón pink (Farfantepenaeus brevirostris Kingsley, Figura 1).
MATERIALES Y MÉTODOS
Diseño de muestreo
Entre 2009 y 2015 en los meses de marzo a septiembre que incluye la temporada de pesca de camarón de aguas profundas en el Pacífico colombiano, se realizaron tres monitoreos abordo de ocho días cada uno a faenas de pesca comercial de embarcaciones de la flota industrial de arrastre camaronero seleccionadas al azar, cubriendo un total de 45 lances muestreados por año entre 40 y 250 m de profundidad. La unidad de muestreo fue el lance de una red de arrastre con duración de 2.8 horas en promedio. Las principales motonaves utilizadas para los monitoreos fueron Hifer, Gladiator, Ada Piedad, Gulf Surf, Cristo Rey, Lusitano y Arraijan, las cuales presentaron similares características técnicas (eslora, manga, maquina, puntal y capacidad de bodega) y el mismo diseño de redes de arrastre tipo "flat" hechas en fibra de polietileno (PE) y poliamida (PA) multifilamentos combinados, con relinga superior de 22.86 m y tamaños de malla de 50.8 mm en el cuerpo y 19.05 mm en el bolso (Rueda et al., 2006; Rico-Mejía y Rueda, 2007; Girón et al., 2010). La ubicación de los lances fue seleccionada por los pescadores de acuerdo al comportamiento normal de una faena de pesca comercial (Figura 1). Para este estudio, la mayoría de los lances muestreados se ubicaron en norte del Pacífico lo que denota importantes caladeros de pesca de camarón, especialmente frente a Nuquí en el departamento de Chocó.
Procedimiento abordo: Una vez izadas las dos redes en cubierta, el procedimiento abordo con la captura consistió en la separación de material vegetal, restos orgánicos, congrios y culebras venenosas, además de la separación del camarón objetivo y especies grandes de peces de importancia comercial. La identificación de los organismos se realizó a nivel taxonómico inferior posible, siguiendo las claves para camarones (Fischer et al., 1995; Pérez-Farfante y Kensley, 1997). En cada lance se tomó una muestra de aproximadamente 2.5 kg de camarones, los cuales fueron identificados y medidos in situ registrando su longitud total (LT) desde la punta del rostro hasta la punta del telso con un ictiómetro con precisión a 0.5 mm inferior. Se determinaron estadios de madurez de manera macroscópica para hembras y machos, siguiendo las claves de Velasco y Wolf (2000) y Paramo et al. (2014) como sigue: Estadio I) ovario de color blanco amarillento translúcido; estadio II) ovario con coloración amarillenta opaca en desarrollo; estadio III) ovario con una coloración anaranjada oscuro en maduración se extiende hasta el telso; estadio IV) gónada desarrollada color verde oscuro y algunas veces naranja; y estadio V) ovarios vacíos flácida. Para estimar la talla media de madurez (TMM), se consideraron los estadios I y II como inmaduros y III, IV y V maduros para las hembras, mientras que para los machos la asignación visual de la madurez se basó en el tamaño de las ampollas terminales y se nombraron dos estadios: estadio I) las ampollas terminales son pequeñas y no son claramente visibles a través del exoesqueleto; y estadio II) maduro con ampollas terminales grandes y claramente visibles a través del exoesqueleto (Angulo y Madrid, 2002).
Análisis de la información: Se determinó el porcentaje entre machos y hembras por año de los individuos examinados. Se analizaron las estructuras de las tallas de hembras y machos por años para observar su distribución usando histogramas de frecuencias y calculando la talla media de captura. Se realizó un análisis de varianza (ANOVA) con el fin de determinar la existencia de diferencias significativas de tallas entre sexos y años analizados, igualmente se realizó una comparación de medias por medio del test LSD de Fisher (α = 0.01). Los análisis estadísticos se realizaron usando el paquete estadístico STATISTICA 9. Se obtuvieron los estadios de madurez y se determinó el porcentaje de madurez sexual para machos y hembras en cada año durante el periodo analizado; mientras que la diferencia entre estos para cada año se evaluó con una prueba de Chi-cuadrado. La talla media de madurez (TMM) para hembras y machos de F. brevirostris, se estimó empleando un ajuste del modelo logístico de madurez por mínimos cuadrados, con estimación de intervalos de confianza a 95% para la talla media de madurez mediante la técnica de remuestreo Bootstrap.
Para construir la función de madurez, se desarrolló un vector de datos con la variable longitud total (LT) con intervalos de 20 mm, usando el siguiente modelo logístico (Ogle, 2012):
Dónde: P LT es la proporción de madurez, y αy β 1 son los parámetros de la función logística y LT la longitud total en mm. La transformación requerida es denominada "transformación logit", donde 1 - p es la probabilidad de "fracaso". Para los análisis de madurez se denomina "éxito" cuando el animal está "maduro" y "fracaso" cuando se encuentra en un estado "inmaduro". La transformación logit esta ejemplificada de la siguiente forma:
La estimación de los intervalos de confianza para la TMM mediante Bootstrap consideró 1000 repeticiones. Se hicieron comparaciones entre los parámetros estimados (pendientes y el intercepto) con el fin de identificar si existieron diferencias significativas entre las TMM para ambos sexos. El estadístico de prueba fue una Chi-cuadrado, las diferencias entre los grupos se establecieron mediante la determinación si la variable de interacción es un término significativo en el modelo. La estimación de los parámetros y la construcción de los intervalos, se realizó con la ayuda del software R (R Core Team, 2012), siguiendo el programa de madurez de Northland College (Ogle, 2012), para el cual se utilizaron los paquetes: FSA, NCStats y car, para la versión de R 3.0.2®.
RESULTADOS
Porcentaje de hembras y machos
De los 20262 individuos colectados en los siete años de monitoreos, el porcentaje de hembras observado fue mayor al de los machos en seis de los siete años analizados con un valor promedio de 56.2%. Aunque solo en 2009, el porcentaje de hembras fue menor (50%), la proporción de sexos en cada año no difirió de 1:1 (prueba X2; p > 0.05 en todos los casos). En consecuencia el análisis agrupando todos los años, indicó una proporción hembras: machos de 1:0.8, la cual no fue significativa (X2= 0.81; p > 0.05) (Figura 2).

Figura 2 Porcentaje de hembras y machos de Farfantepenaeus brevirostris, tomados en monitoreos a bordo de la flota industrial de arrastre de camarón de aguas profundas en el Pacífico colombiano entre 2009 y 2015.
Estructura de tallas
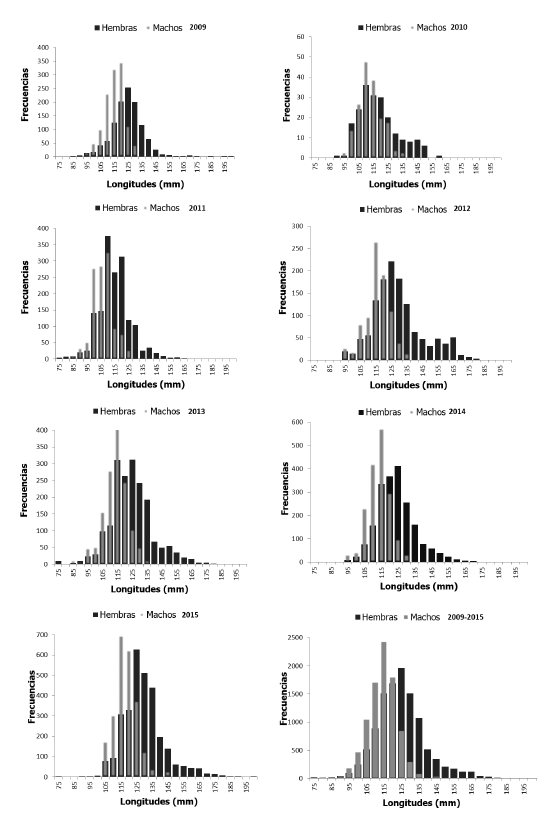
Las estructura de tallas para hembras y machos de F. brevirostris en cada año de estudio mostró que mientras las hembras presentaron un ámbito de distribución normal y unimodal entre 50 y 200 mm con media de 120 mm, los machos presentaron igual patrón de distribución de frecuencia de tallas, pero con menor ámbito (75 a 170 mm) y media de 113 mm (Figura 3). Estas diferencias entre años fueron altamente significativas cuando se compararon las distribuciones de tallas de machos y hembras año por año y agrupando la serie de tiempo 2009-2015 (DN = 0.473; p < 0.0001).
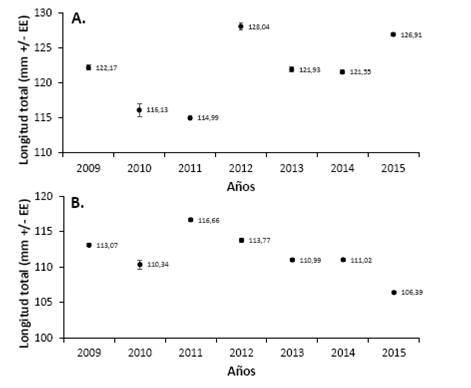
De otro lado, la talla media de captura (TMC) difirió estadísticamente entre años para hembras y machos (F611136 = 204.51; p < 0.0001; F69112 = 244.32; p < 0.0001; respectivamente), observándose para el caso de las hembras la mayor talla media de captura en 2012 (128.04 mm ± 0.463 mm EE) y la menor TMC en 2011 (114.99 ± 0.297 mm EE) (Figura 4)A. Con respecto a la TMC para los machos, se evidenció el mayor valor en 2011 (116.66 ± 0.239 mm EE), mientras que para 2015 se observó el menor valor (106.39 ± 0.165 mm EE) (Figura 4)B. Si bien la TMC de las hembras no mostró tendencia entre años, para los machos se observó una tendencia decreciente entre 2009 y 2015.
Aspectos reproductivos
Las curvas de madurez ajustadas para hembras y machos, agrupando todas las observaciones de probabilidad de madurez por tallas entre 2009 y 2015, se muestran en la Figura 5 (ver parámetros de ajuste en Tabla 1). Dado el gran número de observaciones empleados en los modelos logísticos el patrón de las curvas de madurez para cada año fue similar y se usó para generar intervalos de confianza que dieron cuenta de variabilidad entre años de las funciones de madurez. En consecuencia las curvas de madurez presentadas en este estudio son las curvas medias para toda la serie de tiempo empleada en los ajustes. Las hembras comenzaron a madurar desde 80 mm de longitud total e incrementaron rápidamente la probabilidad de madurez desde 120 mm hasta alcanzar la talla media de madurez (TMM) a 130.6 mm (IC 95% 127.6 - 133.6 mm; Figura 5A). La forma de la curva de madurez de los machos fue más suavizada mostrando individuos madurez antes de 60 mm de longitud total y con un incremento suave de la probabilidad de madurez con la talla, hasta alcanzar la TMM a 83.2 mm (IC 95% 81.2 - 85.2 mm; Figura 5)B. La comparación estadística de las curvas de madurez entre sexos, confirmaron patrones diferentes de madurez (X 2 = 9.832; p < 0.05) y que, en efecto, los machos maduran a menor talla que las hembras.
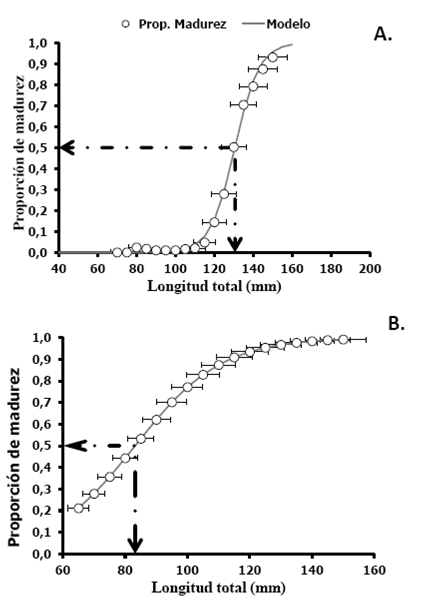
Figura 5: Curvas de madurez del camarón pink (Farfantepenaeus brevirostris), especie objetivo de la pesquería de arrastre industrial de aguas profundas en el Pacífico colombiano: A) Hembras y B) Machos. Se observan los intervalos de confianza bootstrap de tallas para cada proporción de madurez.
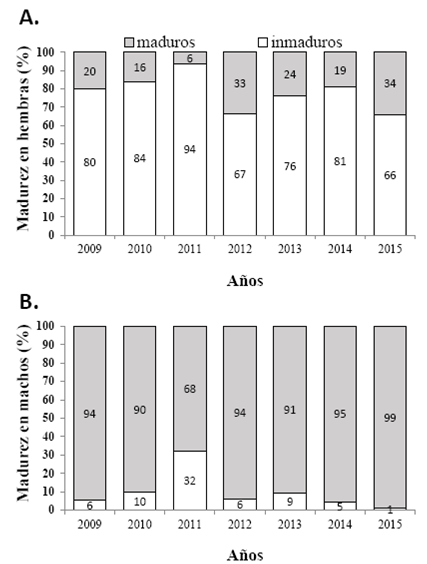
En todos los años de estudio, más de 50% de las hembras de F. brevirostris capturadas por la flota industrial de arrastre en el Pacífico fueron inmaduras (Figura 6)A; no obstante, a partir de 2012 el porcentaje de hembras maduras ha aumentado, siendo 2015 el año con mayor porcentaje de hembras maduras (34%). Caso contrario ocurrió con los machos, los cuales en la mayoría de años el porcentaje de maduros capturados por la flota fue igual o mayor a 90% (Figura 6)B. El año de mayor presión de la pesca sobre el recurso parece fue en 2011, cuando tanto para hembras como para machos se capturó el mayor porcentaje de individuos inmaduros.
DISCUSIÓN
El análisis de más de 20000 individuos de F. brevirostris muestreados a bordo de la flota de arrastre industrial en siete años, permitió determinar el efecto de la pesca sobre la estructura poblacional y condición reproductiva de la especie. Si bien para el periodo de estudio se encontraron para cada año más hembras (56.2% en promedio), la comparación estadística interanual indicó que la proporción entre hembras y machos no difirió de 1:1. Este resultado coincide con lo encontrado por Rueda et al. (2010) en un estudio anterior durante un ciclo anual para la misma especie en el Pacífico; no obstante, diiere de lo encontrado en otra especie de la familia Penaeidae aprovechada comercialmente en el Caribe colombiano, en donde el porcentaje de hembras fue mayor que el de machos (Paramo et al., 2014). Así mismo, estudios reproductivos en el Pacífico mexicano de Farfantepenaeus californiensis muestran mayor proporción de hembras, contribuyendo a una mayor probabilidad de eventos reproductivos para sostener la población sometida a mortalidad por pesca (Romero-Sedano et al., 2004).
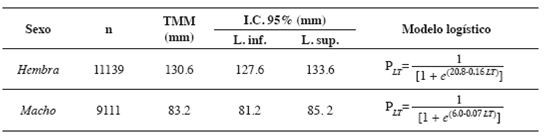
Tabla 1 Funciones de madurez para hembras y machos de Farfantepenaeus brevirostris para el Pacífico de Colombia. Se muestran los parámetros de la función de madurez y la talla media de la primera madurez (TMM) con sus intervalos de confianza bootstrap de 95%.
En forma consistente para cada año estudiado, el ámbito de tallas fue mayor en hembras (50 a 200 mm) que en machos (75 a 170 mm). Esta misma tendencia fue encontrada, aunque con ámbitos más estrechos para la misma especie en el Pacífico colombiano (Invemar, 2014b) y con ámbitos de tallas muy similares para el género estudiado (F. californiensis) en el Pacífico de México (Romero-Sedano et al., 2004). Este patrón de tallas junto con la presencia de un petasma en el primer par de pleópodos en los machos, ejemplifican un carácter distintivo de dimorismo sexual para esta especie (García y Le Reste, 1986). De todos los años estudiados, solo en 2011 (Figura 3) se identificó un mayor efecto de la pesca al encontrarse distribuciones de tallas para hembras y machos con menores valores al resto de la serie de tiempo comparada. Lo anterior puede igualmente ser un efecto combinado de condiciones ambientales adversas al recurso (Rodríguez et al., 2012).
El patrón de madurez de hembras y machos de F. brevirostris fue igual entre años y solo difirió entre sexos con una mayor tasa de madurez en función de la talla en hembras respecto a los machos; no obstante, la talla media de madurez en hembras fue 50 mm mayor que la de los machos (Figura 5). Esto indica parte de la estrategia reproductiva de la especie expresada en su dimorismo sexual en favor de una madurez sexual más temprana en los machos (83.2 mm) frente a las hembras (130.6 mm). En consecuencia, el porcentaje de hembras inmaduras capturadas en la pesquería en siete años osciló entre 66% y 94%, pero los machos han estado disponibles en el área de pesca con porcentajes de madurez entre 68% y 99% (Figura 6).
Diferencias en la forma de la función de madurez entre sexos también han sido determinadas en el Pacífico de México para F. californiensis, donde estimaciones de la TMM fueron similares a las estimadas en este estudio (106.8 mm en machos y 133.3 mm en hembras; Romero-Sedano et al., 2004). Así mismo, la TMM de F. brevirostris estimada en este estudio fue similar a lo registrado por otros autores de esta especie en Colombia (Angulo y Madrid, 2002; Rueda et al, 2010; Rodríguez et al, 2012). No obstante, también hay evidencia de diferencias en la TMM estimada en hembras de F. notialis, donde Ventura-Flores et al. (2014) en Cuba, estimaron la TMM en 96 mm, dando cuenta de diferencias entre latitudes.
En el Pacífico colombiano el desove de F. brevirostris se presenta entre diciembre y abril con picos entre diciembre y febrero (Rueda et al, 2010; Rodríguez et al, 2012), que han llevado a que la Autoridad Pesquera haya establecido una veda reproductiva entre enero y febrero para proteger el desove. Diversos trabajos también ilustran el efecto de variables ambientales y la ocurrencia de El Niño y La Niña en el Pacífico, afectando la condición reproductiva de los camarones (Díaz et al, 1997; Beltrán y Ríos, 2000; Zapata, 2000; Rodríguez et al, 2012). De otro lado, se observó que F. brevirostris es dioica con hembras de mayor tamaño y machos claramente definidos. El dimorismo sexual presente en los machos a través del petasma coniere una estrategia de éxito reproductivo al garantizar la transferencia de espermatóforos al receptáculo seminal de las hembras o télico (García y Le Reste, 1986).
Este estudio contribuyó a generar mayor información sobre el efecto de la pesca de arrastre en la estructura poblacional de F. brevirostris en términos de mayor presión sobre las tallas capturadas de las hembras. En este sentido, se recomienda fortalecer las medidas de manejo actuales como cuotas de pesca y vedas totales por el control de la selectividad de las redes de arrastre con base en las tallas medias de madurez de las hembras que igualmente protegen la población de machos. Así mismo, se debe introducir vedas espacio-temporales como estrategias de cerrar la pesca en ventanas ambientales que cubren hábitats esenciales para la especie (por ejemplo, en el golfo de Tribugá del Pacífico y sus caladeros de Filo, La Roñosa y Morromico). Para todas las medidas de manejo se debe adoptar la activa participación del pescador en el proceso de manejo (e.g. comanejo entre las instituciones y los pescadores industriales y artesanales).