INTRODUCCIÓN
Los ecosistemas fluctúan naturalmente. Por esto, características ecológicas como la competencia, depredación, reclutamiento, colonización y la distribución de las especies podrían fluctuar también (Wallentinus y Nyberg, 2007; Quintana et al, 2013). Adicionalmente, los hábitats se vuelven susceptibles a invasiones ecológicas por especies nativas y no nativas (Valéry et al., 2008). Además, se ha demostrado que las especies nativas también pueden exhibir explosiones demográficas, ocupar rangos más amplios y mostrar un comportamiento invasivo como resultado de perturbaciones naturales y humanas. A pesar de que las "especies invasoras nativas" pueden causar algunos problemas a los ecosistemas (ej. dominancia, extinciones locales y reducción de la biodiversidad) (Parsons y Lalli, 2002; Olden, 2006; Valéry et al, 2009a, 2009b; Carey et al, 2012 y Rilov et al., 2012), han sido poco documentadas en el mundo (Valery et al., 2008, 2009a; Buczkowski, 2010; Carey et al., 2012; Simberloff et al., 2013).
Las explosiones demográficas pueden definirse como un aumento repentino en el número de individuos de una especie (Hawley, 1982). Este incremento, causa desequilibrio en la abundancia de otras especies, disminución en los recursos locales y modifica las características del paisaje (Morelle et al., 2016). Las especies invasoras nativas muestran el mismo comportamiento de rápida expansión que las especies invasoras exóticas (Valery et al., 2009b; Morelle et al., 2016). Por lo tanto, es importante investigar cuáles son las causas que están influyendo en las explosiones demográficas, y las consecuencias de las abundancias excesivas de una especie para los ecosistemas.
Estas especies invasoras nativas también pueden mejorar las condiciones de los ecosistemas. Lo anterior ocurre cuando dichas especies son modificadores ecosistémicos (ecosystem engineers) (Bazterrica et al., 2012). Dichos modificadores, tienden a cambiar la estructura actual del hábitat, modificando las condiciones físicas y modulando la disponibilidad de recursos bióticos y abióticos para otras especies (Jones et al., 1994; Barrios et al., 2009; Bazterrica et al., 2012, 2014). Por ejemplo, los modificadores de ecosistemas pueden crear fácilmente nuevos hábitats, prevenir el reclutamiento de otras especies o aumentar su propia actividad de dispersión y reproducción dentro de las nuevas condiciones creadas (Cuddington y Hastings, 2004; Lambrinos y Bando, 2008).
El conocimiento acerca de invasiones ecológicas es amplio. La mayoría de los estudios previos se han centrado en las invasiones de especies exóticas o foráneas (Luppi y Bas, 2002; Parsons y Lalli, 2002; Bazterrica et al., 2012, 2014; Rilov et al., 2012; Quintana et al., 2013; Urban-Malinga et al., 2013; Shumka et al., 2014; Jaubet et al., 2015). Sin embargo, son escasos los informes de especies invasoras nativas en ecosistemas marinos (Valery et al., 2009a; Buczkowski, 2010; Carey et al., 2012). Las zonas intermareales pueden ser altamente susceptibles a la invasión por diferentes organismos como poliquetos constructores de arrecifes, bivalvos, gramíneas marinas, mejillones y cangrejos, debido a sus condiciones inherentes como el desplazamiento regular del agua, contenido de nutrientes y sustratos óptimos. (Bruschetti et al., 2009). El Pacífico Oriental Tropical (POT) posee grados variables en los rangos mareales, y la costa Pacífica colombiana posee un ámbito meso a macro-mareal (Ramírez-Martínez et al., 2016), que la hace cumplir con estas condiciones previamente mencionadas. Por lo tanto, la hace particularmente propensa a invasiones biológicas.
Los poliquetos son un grupo muy diverso y común en las zonas intermareales (Bouchet, 2006; Appeltans et al., 2012; Valencia et al., 2014). Los sabelláridos (gusanos de peine de miel) pueden producir tubos duros para vivir, y algunos grupos pueden formar colonias que son estructuras duras similares a arrecifes (Pawlik, 1988). Estudios previos han reportado la distribución de los poliquetos constructores de arrecifes en el Océano Pacífico (Barrios et al., 2009; Bastida-Zavala y García-Madrigal, 2012; Alalykina, 2013). En particular, Barrios et al. (2009) estudiaron la distribución de Idanthyrsus cretus en el archipiélago de Las Perlas (Panamá), y Gómez et al. (1997) registró la presencia de esta especie en Oaxaca, México. Sin embargo, no existen estudios en la costa Pacífica colombiana sobre la densidad y cobertura de este poliqueto. Laverde-Castillo (1989) registró sabelláridos, como Phragmatopoma attenuata, I. cretus e I. armatus, en bahía Cobita, bahía Octavia, ensenada de Utria e isla Gorgona. Aunque no midieron la cobertura, las densidades reportadas nunca sobrepasaron más de 11 individuos. Adicionalmente, estudios previos de I. cretus [conocido previamente como I. pennatus en Monro (1933), Fauchald (1977) y Prahl (1979)], mencionaron que pocos individuos difícilmente se encontraban construyendo grandes colonias. Solo cerca de cuatro o cinco individuos vivían en tubos duros individuales, y varios de ellos estaban juntos y acoplados a las piedras. Registros posteriores (Kirtley, 1994; Jaubet et al., 2015), estuvieron de acuerdo con esta observación.
Idanthyrsus cretus Chamberlin (Sabellariidae) es un poliqueto constructor de arrecifes que suele encontrarse en zonas intermareales expuestas al oleaje y a corrientes costeras y superficiales. Idanthyrsus cretus también se puede encontrar a profundidades intermedias bajo el agua en la plataforma continental asociado a corales duros. Estos entornos son perfectos para el desarrollo de este poliqueto debido a que el intercambio regular de arena y sedimentos es alto, permitiéndoles construir sus tubos y colonias (Kirtley, 1994; Bastida-Zavala y Becerril-Tinoco, 2009). Esta especie, al igual que otros Sabeláridos, son animales filtradores que se alimentan de plancton, desechos orgánicos, pequeñas partes de crustáceos y algas (Bastida-Zavala y Becerril-Tinoco, 2009). Por lo general, otros organismos están asociados con los arrecifes que forman los Sabeláridos (Barrios et al., 2009), al igual que otras familias de poliquetos (Luppi y Bass, 2002; Cuddington y Hasting, 2004). Estos organismos asociados, usan estas colonias como refugio y fuente de alimento.
Bastida-Zavala y Becerril-Tinoco (2009) también agregaron que se sabe poco de las relaciones filogenéticas entre las especies de sabelláridos. Según los primeros informes de estos poliquetos realizados por Monro (1933), Hartman (1940), Fauchald (1977) y Prahl (1979) en isla Gorgona, este poliqueto fue considerado como I. pennatus. Sin embargo, después de la revisión taxonómica de Sabeláridos hecha por Kirtley (1997), I. pennatus se corrigió a I. cretus. Así, según referencias bibliográficas, todos los informes anteriores corresponden hoy a I. cretus. Aunque aún no existe algún documento taxonómico que describa a I. cretus en la costa Pacífica colombiana, para este estudio, se consultó a un experto con el fin de identificar correctamente esta especie.
En este artículo se registra por primera vez información sobre los atributos ecológicos, como la cobertura y la densidad, de la reciente explosión demográfica del poliqueto constructor de arrecifes Idanthyrsus cf. cretus (Sabellariidae) en tres sitios de muestreo de isla Gorgona, al sur del Pacífico colombiano. De acuerdo a la información previa, I. cf. cretus nunca ha sido observado construyendo colonias ni formaciones arrecifales como las que se registran aquí para isla Gorgona.
ÁREA DE ESTUDIO
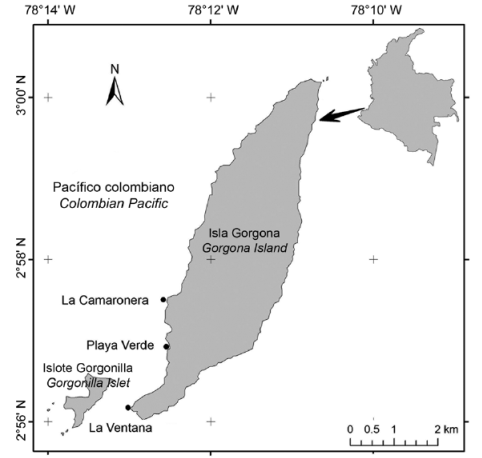
La cuenca del Pacífico colombiano está formada por rocas ígneas y sedimentarias depositadas en antiguos períodos geológicos producidos por erupciones volcánicas (Cantera et al., 1998). Isla Gorgona (2°58 'N - 78°11' O), ubicada a 35 km de la costa, posee una gran variedad de ecosistemas costeros y de aguas poco profundas como playas de arena, arrecifes de coral y arrecifes rocosos (Valencia et al., 2014), lo que la hace una de las localidades con mayor biodiversidad en el Pacífico colombiano (Cantera et al., 1995; Díaz y Acero, 2003).
Este estudio fue llevado a cabo en cada zona intermareal (alta-IA, media-IM y baja-IB) de tres sitios de muestreo (La Camaronera, Playa Verde y La Ventana), donde las costas rocosas son predominantes (Figura 1). La Camaronera y Playa Verde son dos playas rocosas compuestas por arena, grava y algunos grandes bloques de roca entremezclados (zonas intermareales altas y medias). También se pueden encontrar bloques de roca medianos y charcos intermareales (zona intermareal baja). En contraste, La Ventana es una plataforma rocosa de pendiente suave con grandes bloques de roca (intermareal alto), peñascos (intermareal medio) y charcos intermareales, rocas de tamaños medianos y grava (intermareal bajo).
MATERIALES Y MÉTODOS
Estimación de la densidad
Antes del muestreo, se realizaron observaciones cualitativas en cada zona intermareal dentro de cada sitio de muestreo, para describir las colonias que conformaban los arrecifes de los poliquetos y la biota asociada a ellos (algas, moluscos y cangrejos). Se tomaron fotografías de individuos completos y se colectaron algunos para almacenarlos en el Museo de la Universidad del Valle (Cali, Colombia). En cada sitio de muestreo y zona intermareal (IA, IM y IB), una muestra de 100 cm2 de la superficie de las colonias de I. cf. cretus fue extraída aleatoriamente, utilizando un cincel y un martillo (N = 37). Para asegurarnos de que cada colonia fuera completamente muestreada, se cavó hasta encontrar la base de la roca. Por lo tanto, los volúmenes diferían dependiendo del desarrollo colonial. Para el análisis de datos, se utilizó el área en lugar del volumen de la muestra de la colonia. Las colonias fueron cuidadosamente desmenuzadas con el fin de extraer los individuos. Sólo las cabezas de los poliquetos encontrados se contaron para evitar sobreestimación.
Estimación de cobertura
Se realizaron siete transectos aleatorios a lo largo de la costa, en cada zona intermareal (20 m de longitud x 1 m de ancho). Como resultado, se obtuvieron 21 transectos en cada sitio de muestreo, quedando así un total de 63 transectos en todo el estudio. Cada transecto consistió de una cuadrícula de 100 puntos separados cada 5 cm en un cuadrante de 50 cm. Utilizamos esta cuadrícula a ambos lados del transecto para obtener 1 m de ancho (200 puntos), resultando en 4000 puntos bajo los cuales se registraron los datos de presencia/ ausencia de colonias (200 puntos x 20 m).
Análisis de los datos
El análisis de densidad (número de individuos por 100 cm2) sólo consideró los sitios de muestreo. Se excluyeron las zonas intermareales por las siguientes razones: 1) no se encontraron colonias lo suficientemente grandes para muestrear en las zonas de IA e IB en Playa Verde y La Camaronera; y 2) al comparar las zonas intermareales para La Ventana, no se encontraron diferencias significativas. Por lo tanto, la densidad se consideró homogénea en las tres zonas intermareales de este sitio de muestreo. Se utilizó un modelo lineal generalizado con una distribución de probabilidad cuasi-Poisson para evaluar los efectos de los sitios de muestreo sobre la densidad de poliquetos. Este modelo considera la sobre dispersión de los datos (Bilder y Loughin, 2014).
La cobertura (presencia/ausencia de datos) se evaluó utilizando un modelo lineal generalizado con una distribución de probabilidad cuasi-binomial. El modelo ajustado incluyó el sitio de muestreo y la zona intermareal como factores. Fue necesario eliminar la interacción entre factores debido a la presencia de ceros. Por lo tanto, los factores se analizaron independientemente. Todos los análisis estadísticos se realizaron en el programa R versión 3.2.2 (R Core Team, 2015)
RESULTADOS
Un total de 1904 individuos de Idanthyrsus cf. cretus (Fig. 2a-b) fueron colectados de las colonias encontradas en las zonas intermareales (Fig. 2c-e).
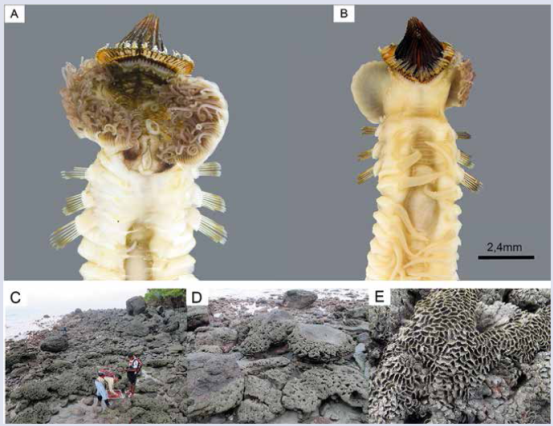
Figura 2 Vista ventral (A), vista dorsal (B), vista general del paisaje (C), morfología de la colonia (D) y vista de la colonia en primer plano (E) del poliqueto Idanthyrsus cf. cretus colectado en la isla Gorgona.
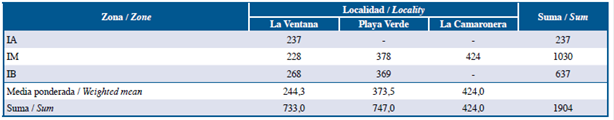
Estos individuos estaban presentes en todas las zonas intermareales de La Ventana. En Playa Verde, se encontraron individuos de I. cf. cretus en el IM e IB, y en La Camaronera sólo en el IM. La menor abundancia se observó en la zona del IA y la más alta en el IM (Tabla 1). El IM en La Camaronera solo representó 22.3% (424 individuos) del total de individuos. La media ponderada del número total de individuos por sitio de muestreo mostró el valor más alto en La Camaronera y el más bajo en La Ventana. Sin embargo, utilizando el índice de dispersión (I), el número de individuos colectados en La Ventana y Playa Verde fue casi similar y mayor que en La Camaronera. Además, se encontró que La Ventana muestra un patrón de distribución aleatorio, mientras que Playa Verde y La Camaronera se observa una distribución irregularo en parches (p«0.001).
Tabla 1 Número total de individuos de Idanthyrsus cf. cretus por sitio de muestreo y nivel intermareal en la Isla Gorgona.
Análisis estadísticos
La cobertura en Playa Verde y La Camaronera fue mayor en las zonas del IM, lo cual refleja el patrón general de cobertura observado (Tabla 2). Además, la cobertura en Playa Verde fue la más alta, en comparación con cualquier otro sitio de muestreo. De hecho, correspondió a 1,6 y 2,0 veces más que en La Camaronera y La Ventana, respectivamente (ver tabla 1, figura 3). Por otra parte, el efecto de la zona intermareal en la cobertura fue aún más notable dado que la cobertura en el IM fue hasta 47,5 y 5,0 veces más alto que en La Ventana y La Camaronera, respectivamente (ver tabla 1, Fig. 4).
Tabla 2 Cobertura de la colonia (%) de Idanthyrsus cf. cretus por sitio de muestreo y nivel intermareal en la Isla Gorgona.
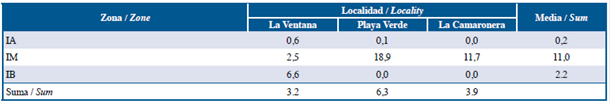
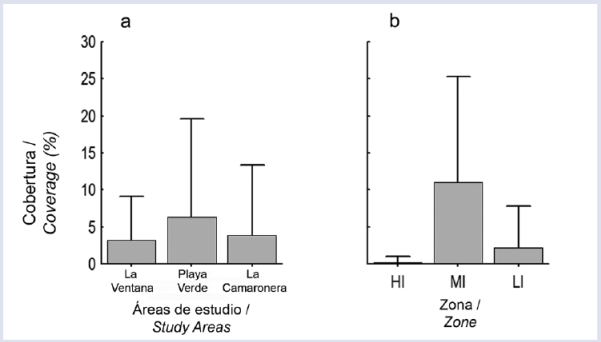
Figura 3 Cobertura media total (+ DE) de las colonias de I. cf. Cretus (a) en cada área de estudio, y zona intermareal (b) en la isla de Gorgona.
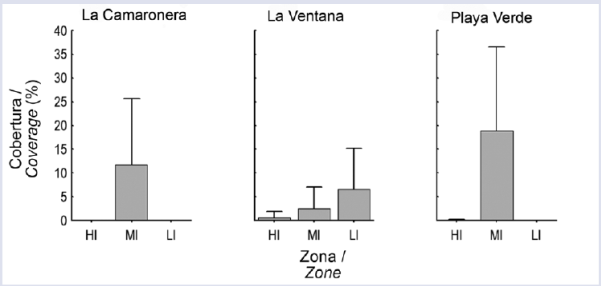
Figura 4 Cobertura media (+ DE) de las colonias de I. cf. cretus para cada sitio de muestreo en cada zona intermareal en la isla de Gorgona.
Por otro lado, los sitios de muestreo no tuvieron un efecto significativo en la cobertura (Fig. 3 a). Sin embargo, Playa Verde fue la localidad con mayor cobertura media, seguida por La Camaronera y La Ventana (Fig. 3a). Se encontraron diferencias estadísticas entre las zonas intermareales. La alta cobertura del IM fue significativamente diferente al IB ( y al IA, mientras que el IB y el IA no fueron estadísticamente diferentes entre ellos (Fig. 3b). Aunque la interacción (localidad x zona intermareal) no se incluyó en el modelo, la agregación de I. cf cretus en el IM de Playa Verde y La Camaronera fue evidente. Por el contrario, La Ventana mostró una tendencia creciente en la cobertura, registrando la más baja en la zona del IA hasta la más alta en la zona del IB (Figura 4).
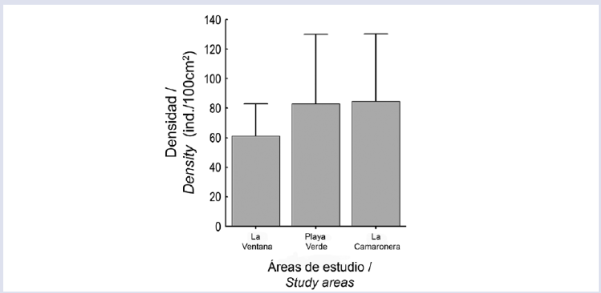
La densidad media (ind./100cm2± DE) fue similar entre los sitios de muestreo . Sin embargo, el sitio de muestreo con menor densidad media fue La Ventana, mientras que Playa Verde y La Camaronera tuvieron densidades similares y más altas (Fig. 5). Estas dos últimas también mostraron una dispersión de datos más amplia (véase el índice de dispersión), lo que podría haber afectado los resultados estadísticos. Además, la densidad entre los niveles intermareales fue evaluada por separado y sólo en La Ventana y Playa Verde. No hubo efectos estadísticos en la densidad de I. cf. cretus entre las zonas intermareales ni en La Ventana ni en Playa Verde.
DISCUSIÓN
Los registros de I. cf. cretus en la Isla Gorgona son raros. Hasta donde se sabe, sólo hay informes de algunos individuos hechos por Monro (I. pennatus e I. armatus, 1933). Sin embargo, Hartman (1940), Fauchald (1977) y Prahl (1979) citaron estos registros en sus estudios, y Kirtley (1994) describió posteriormente a I. pennatus como I. cretus. Por lo tanto, no hay más registros publicados de esta especie además de los estudios mencionados aquí. Adicionalmente, durante viajes constantes a la isla (al menos dos veces al año), no se pudo observar ningún signo de presencia de individuos ni colonias. Por consiguiente, fue evidente que estas colonias aparecieron repentinamente a lo largo de las costas de La Ventana, La Camaronera y Playa Verde. Dado el razonamiento anterior, se reporta con certeza que no hubo informes publicados de colonias anteriores a 2013. Por lo tanto, nuestros resultados de alta cobertura y densidad de I. cf. cretus, sugieren que ha habido una repentina explosión demográfica de esta especie en la isla al menos desde 2014.
Dado la escasez de estudios sobre densidad y cobertura de Idanthyrsus cf. cretus (Sabellaridae), fue difícil comparar nuestros resultados con estudios similares. Sin embargo, los arrecifes de I. cf. cretus estudiados en Gorgona son similares en estructura y características generales a los registrados en áreas cercanas. Por ejemplo, Barrios et al. (2009) registró una densidad en el archipiélago de Las Perlas, en Panamá, de 72 ind./100cm2 (aunque en los resultados registran densidades por 10 cm2, creemos firmemente que se refieren a 100 cm2 ya que en su metodología se indica el uso de cuadrantes de 10 x 10 cm), una densidad casi igual a nuestros resultados (73 ind./100 cm2). Además, Gómez et al (1997) también encontraron esta especie en dos de las cinco bahías muestreadas en Oaxaca, México (La Entrega y Puerto Ángel), pero su densidad fue muy baja comparada con otros sabelláridos registrados en este estudio (seis individuos en 40 transectos de 5 mx1 m). Informes de la abundancia de I. cf. cretus en el Pacífico colombiano incluyen muy poca información sobre las estimaciones de densidad (sólo presencia de especies). En particular, Salazar-Vallejo y Londoño-Mesa, (2004) mencionan que los registros de los poliquetos en la costa del Pacífico colombiano están incompletos o no tienen detalles específicos sobre su morfología. Además, Londoño-Mesa (2017), también explica que en general, los poliquetos en esta región siguen siendo poco estudiados. Con respecto al Pacífico colombiano, nuestros resultados proporcionan detalles importantes sobre los posibles cambios en la ecología poblacional de este poliqueto en isla Gorgona que demandan más investigación.
Durante el muestreo, también se observaron varios organismos asociados a este poliqueto (e.g. algas, moluscos, crustáceos y otros poliquetos), los cuales ya se habían reportado habitando arrecifes creados por poliquetos constructores (Luppi y Bas, 2002; Cuddington y Hastings, 2004; Barrios et al., 2009; Bruschetti et al., 2009). Los arrecifes proporcionan una gran variedad de microhábitats (Hunter y Sayer, 2009), que son utilizados por diferentes organismos. Este es el caso de las colonias formadas por I. cf. cretus. Mientras que esto es cierto, modificadores ecosistémicos (ej. poliquetos constructores de arrecifes; ver Jones et al., 1994) tienden a modificar rápidamente su hábitat alterando el funcionamiento de su ecosistema (Schwindt et al, 2001;Bruschetti et al, 2009). Como consecuencia, esto podría ocasionar graves efectos negativos o positivos sobre los componentes de la comunidad (ej. riqueza y diversidad de especies). Gribben et al, 2013, explica que los modificadores ecosistémicos pueden reducir el crecimiento de la población y la dispersión de otros organismos, especialmente los invertebrados. A pesar de que nuestro conocimiento sobre este poliqueto constructor de arrecifes es muy pobre, y no se obtuvieron datos formales de otros invertebrados, nuestros resultados sugieren que esta dominancia aparente en la mayoría de las zonas intermareales de la isla (tabla 1 y figura 3), podría cambiar las tasas de desarrollo de otros organismos a medida que las colonias se dispersan y crecen. Además, los constructores de ecosistemas también pueden afectar negativamente los componentes de la comunidad infaunal disminuyendo el número de individuos y taxones (Gribben et al., 2013).
La presencia y cobertura de las colonias de I. cf. cretus fueron diferentes entre localidades y zonas intermareales. Se hipotetiza que esto se debe a las características físicas en las que estas colonias están siendo construidas (pendiente de la costa, tipo y heterogeneidad del sustrato, energía de las olas y transporte de sedimentos, Pawlik et al., 1991; Voulgaris et al., 1998; Barrios et al., 2009). En Playa Verde y La Camaronera, el IM está formado por grandes peñascos y bloques de roca que proporcionan lugares adecuados donde los poliquetos pueden establecerse y crecer con seguridad (grietas, hoyos y partes inferiores de las rocas). Además, hay un suministro constante de material de construcción (arena, conchas agrietadas y corales) producido por las fuertes olas que pone en movimiento los sedimentos de las playas, permitiendo que las colonias aumenten su grosor. La ausencia de sustratos adecuados en la zona del IA de Playa Verde y La Camaronera dificultó la formación de colonias. Por otro lado, se observó un patrón diferente en La Ventana donde se encontraron colonias en todos los niveles intermareales (Fig. 4). Sin embargo, estas colonias fueron delgadas y menos abundantes. Esto podría deberse a que este sitio de muestreo se caracteriza por presentar una plataforma de pendiente suave y donde el sustrato está formado por pequeñas rocas y grava. Aunque la playa de arena más grande de la isla se encuentra junto a esta zona, esta plataforma podría restringir el suministro de arena para la formación de colonias. Además, la presencia de una isla más pequeña (islote de Gorgonilla) situada frente a esta localidad y separada sólo por un canal estrecho, podría servir de barrera para el movimiento del agua que impacta la orilla y recircula los sedimentos. En general, aunque las condiciones en La Ventana pueden ser poco aptas para la formación adecuada de colonias, estas condiciones (ej. humedad, suministro de arena) en el IB son ligeramente más adecuadas que en el IA e IM. Como consecuencia, la densidad y cobertura fueron mayores en este nivel intermareal (IB) en La Ventana.
Otra posible explicación para la diferencia en la abundancia y tamaño de las colonias y el hecho de que la densidad de poliquetos no mostró ninguna diferencia estadística entre los niveles intermareales, podría ser el patrón de dispersión de I. cf. cretus en La Camaronera y Playa Verde. Este patrón podría estar sugiriendo que la explosión demográfica comenzó en estos sitios porque nuestros resultados mostraron que la densidad y la cobertura de las colonias fue más altas en ellos, además tenían un patrón de distribución aleatorio. Por otro lado, La Ventana tenía un patrón de distribución irregular o en parches, y las colonias y los valores de densidad fueron pobres en comparación con los otros sitios. Por ende, estos resultados sugieren que la colonización y la explosión demográfica comenzaron en estas dos localidades (Playa Verde y La Camaronera) y va en camino hacia La Ventana. Se sabe que los sabelláridos constructores de arrecifes como I. cf. cretus, se expanden por hábitats marinos dependiendo de las condiciones adecuadas y las corrientes marinas, pero este proceso toma tiempo (ej.Cuddington y Hastings, 2004). Cuddington y Hastings (2004) describieron que las invasiones de modificadores ecológicos (ecosystem engineers) se producen en dos fases: 1) cuando la especie recién se asienta y su crecimiento es muy lento (como ocurre en La Ventana); y 2) cuando la expansión se convierte en una explosión demográfica (como ya ha ocurrido en La Camaronera y en Playa Verde).
CONCLUSIONES
Se registra por primera vez una notable explosión demográfica de I. cf. cretus (Sabellariidae) en la Isla Gorgona. Los resultados concuerdan con los registros de I. cf. cretus en otros lugares (Barrios et al., 2009), donde estos poliquetos han colonizado ambientes bentónicos con altos niveles de movimiento de agua y rocas. Idanthyrsus cf. cretus podría estar modificando las zonas intermareales, debido a su rápida propagación y alta cobertura, monopolizando el espacio y, por lo tanto, afectando a la biodiversidad. Los modificadores ecológicos, como los poliquetos, pueden servir de anfitrión a otras especies de zonas intermareales (Gutiérrez et al., 2003; Bruschetti et al., 2009). Aunque sólo se midió la abundancia y cobertura de este poliqueto, individuos de otras especies se observaron ampliamente dentro o fuera de las colonias (ej. cangrejos pequeños, moluscos y otros crustáceos). Por lo tanto, el efecto de esta invasión repentina sobre la biodiversidad local es incierto y necesita ser más estudiado. Además, es importante reconocer que este poliqueto se ha encontrado previamente en los arrecifes de coral, incluso en isla Gorgona (Monro, 1933); Gorgona parece ser un lugar único y apropiado para que los poliquetos se establezcan dadas las condiciones de la temperatura del agua (Monro, 1933). Por lo tanto, ya que los arrecifes de coral están bajo condiciones marginales en esta Isla, es importante vigilar esta especie invasora nativa, ya que podría ser una posible amenaza debido a su rápida propagación y dominancia (Barrios et al., 2009). Debido a que no hay otros estudios que informen el repentino crecimiento y propagación de I. cf. cretus, es importante y necesario investigar más a fondo esta especie en las costas del Pacífico colombiano para obtener resultados concluyentes sobre esta hipótesis. Específicamente, es necesario estudiar el movimiento del agua y las corrientes, el contenido de sedimentos, la temperatura, etc., ya que estos factores son esenciales para el desarrollo y crecimiento de las especies de Idanthyrsus (Barrios et al., 2009). Así, esto podría ayudar a esclarecer qué cambios ocurrieron desde el último reporte de Monro (1933) y qué pudo causar esta invasión repentina para desarrollar colonias de estos tamaños 80 años después.











 text in
text in