Sumario
Siglas y abreviaturas utilizadas. Introducción. 1. La colisión de derechos en tratados internacionales en Suramérica. 1.1. El derecho a la salud y la patente farmacéutica en la segunda mitad del siglo xx. 1.2. El debate sobre el comercio y los derechos humanos en la salud pública. 2. Impacto del Acuerdo sobre los ADPIC en el acceso a medicamentos esenciales. 2.1. Impacto en Suramérica. 2.2. Solución de controversias sobre patentes farmacéuticas en la OMC. 2.3. Debate sobre acceso a medicamentos en el OSD. 3. Desafíos para Suramérica. 3.1. Unasur y el CSS. 3.2. Cooperación intrarregional y diplomacia transversal. 3.3. Cooperación Sur-Sur y TLC suscritos con normas ADPIC Plus.
3.3.1. La cooperación Sur-Sur y la influencia de Brasil. 3.3.2. TLC suscritos por Chile, Perú y Colombia con Estados Unidos. Conclusiones. Referencias.
SIGLAS Y ABREVIATURAS UTILIZADAS. Acuerdo sobre
los ADPIC |
: A cuerdo sobre los Aspectos de los Derechos de Propiedad Intelectual Relacionados con el Comercio |
AMS |
: Asamblea Mundial de Salud |
CAN |
: Comunidad Andina de Naciones |
CSS |
: Consejo de Salud Suramericano Declaración |
de Doha |
: Declaración relativa al Acuerdo sobre los ADPIC y la Salud Pública |
DIDH |
: Derecho Internacional de los Derechos Humanos |
FDA |
: Food and Drug Administration |
GATT |
: General Agreement on Trade and Tariffs |
ISAGS |
: Instituto Suramericano de Gobierno en Salud |
Mercosur |
: Mercado Común del Sur |
OMC |
: Organización Mundial del Comercio |
OMS |
: Organización Mundial de la Salud |
ONU |
: Organización de las Naciones Unidas |
OSD |
: Órgano de Solución de Diferencias comerciales |
PIDESC |
: Pacto Internacional de Derechos Económicos, Sociales y Culturales |
TLC |
: Tratado de Libre Comercio |
Unasur |
: Unión de Naciones Suramericanas |
UNCTAD |
: Conferencia de las Naciones Unidas sobre Comercio y Desarrollo |
mUNICEF |
: Fondo de las Naciones Unidas para la Infancia |
VIH/SIDA |
: Virus de la Inmunodeficiencia Humana/Síndrome de Inmunodeficiencia Adquirida |
Introducción
El siglo XXI comienza con un encendido debate sobre el comercio y los derechos humanos -trade and human rights debate- a nivel internacional. Sobre la (in)compatibilidad de las reglas y estándares mínimos del comercio internacional, por una parte, y la protección de los derechos humanos, por la otra2. Un ejemplo emblemático lo constituye el debate sobre el acceso a medicamentos esenciales en plena crisis del VIH/SIDA.
Para ser Estado miembro de la OMC los países en desarrollo debieron suscribir el controvertido Acuerdo sobre los ADPIC3, que entró en vigencia el 1.° de enero de 1995.
El Acuerdo sobre los ADPIC fija estándares mínimos de protección de la propiedad intelectual -derechos de autor y derechos conexos; marcas de fábrica o de comercio; indicaciones geográficas; dibujos y modelos industriales; patentes; esquemas de trazado de los circuitos integrados, y protección de la información no divulgada-, y en el caso de las patentes sus efectos son relevantes al fijar como materia patentable “todas las invenciones, sean de productos o de procedimientos, en todos los campos de la tecnología, siempre que sean nuevas, entrañen una actividad inventiva y sean susceptibles de aplicación industrial”4.
Con ello, sus disposiciones también se aplican a la patente farmacéutica, detentada habitualmente por empresas farmacéuticas de nivel global, con casa matriz en Estados unidos o Europa5. Implican derechos de propiedad intelectual de dominio privado que amplían y refuerzan los derechos de sus titulares, al conferirles derechos exclusivos de explotación por un período mínimo de 20 años sobre el nuevo medicamento, retrasando la entrada al mercado del medicamento genérico, aquel que no se encuentra amparado por una patente.
Muy pronto, los Estados miembros de la OMC se ven obligados a formular la Declaración de Doha, de 2001, en la que reconocen las preocupaciones con respecto a sus efectos sobre los precios de los medicamentos y donde afirman que el Acuerdo sobre los ADPIC debe ser interpretado de una manera que apoye el derecho de sus miembros de proteger la salud pública y, en particular, de promover el acceso a los medicamentos para todos.
La tensión en cuanto al acceso a medicamentos esenciales -fármacos antirretrovirales, vacunas y otros medicamentos de alto costo utilizados en programas gubernamentales- se da entre la obligación estatal de facilitar el acceso de la población a medicamentos esenciales, que emana del derecho a la salud consagrado en el artículo 12 del PIDESC de la ONU, de 1966, por una parte, y el fortalecimiento de la patente farmacéutica incluida en las obligaciones internacionales de carácter comercial que asumen los Estados miembros de la OMC en el Acuerdo sobre los ADPIC6.
Ambos corresponden a tratados internacionales vinculantes cuyas obligaciones deben ser aplicadas en el ámbito interno por los doce países de Suramérica, quienes sin excepción los han suscrito y ratificado. En el caso de aquellos productos farmacéuticos que cada país fija en su listado de medicamentos esenciales, estos deben estar disponibles y accesibles en todas sus jurisdicciones, a favor del bienestar de los grupos más desfavorecidos. De acuerdo a las definiciones del Comité de Derechos Económicos, Sociales y Culturales7 del PIDESC, esta obligación es de carácter inderogable y de efecto inmediato, constituyendo para el Estado parte una obligación de cumplir cuya violación se verifica al no adoptarse todas las medidas necesarias que permitan dar efectividad al derecho a la salud.
En este contexto, el objetivo de este trabajo consiste en demostrar, asumiendo una visión suramericana común, la importancia estratégica de que nuestros países se unan, en materia de acceso a medicamentos esenciales, en torno a políticas públicas conjuntas y posiciones comunes en el ámbito internacional.
Para cumplir este objetivo el trabajo consta de tres apartados y una conclusión. El primer apartado aborda la colisión de derechos en ambos tratados internacionales -PIDESC y Acuerdo sobre los ADPIC- en vigencia a lo largo y ancho de Suramérica; el segundo da cuenta del impacto que han supuesto las obligaciones asumidas por los países suramericanos en la OMC respecto del deber de facilitar el acceso de sus poblaciones a medicamentos esenciales; un tercer apartado se ocupa de los desafíos que tiene por delante Suramérica, a partir de las acciones que desarrollan sus países en el marco de Unasur.
Además, en este último apartado se ilustran dos extremos que coexisten a nivel continental, y que precisan ser direccionados lo más armónicamente posible para llevar este desafío suramericano a buen puerto: por una parte, el liderazgo de Brasil en materia de acceso a medicamentos esenciales en el hemisferio sur, y por la otra, los TLC suscritos con Estados unidos por Chile, Perú y Colombia, países que asumen algunas obligaciones con la potencia norteamericana que refuerzan la patente farmacéutica y exceden las obligaciones asumidas por los Estados en el Acuerdo sobre los ADPIC.
1. La colisión de derechos en tratados internacionales en Suramérica
1.1 El derecho a la salud y la patente farmacéutica en la segunda mitad del siglo XX
Con el término de la Segunda Guerra Mundial y la creación de la ONU se fue desarrollando cada vez con mayor vigor el DIDH, sentándose las bases del marco jurídico internacional del derecho a la salud en la Declaración universal de Derechos Humanos8 de 1948.
Desde entonces, este derecho se ha codificado en numerosos tratados internacionales y regionales de derechos humanos de carácter vinculante y en muchas constituciones nacionales, de modo que la mayoría de los países han firmado o ratificado al menos una convención o tratado de carácter general o regional que consagra el derecho a la salud: más de 150 países son Estados parte del PIDESC, 80 han firmado tratados regionales y más de 100 han incorporado el derecho a la salud en su constitución nacional9. Así, en cuatro constituciones nacionales -México, Perú, Filipinas y Siria- se ha reconocido el acceso a los medicamentos esenciales como un derecho fundamental10.
Precisamente, el PIDESC de 1966, que entró en vigencia en 1976, provee la disposición más importante y comprensiva del derecho a la salud del DIDH -el artículo 12, sobre el derecho al más alto nivel posible de salud física y mental-, disposición que hace hincapié en el acceso equitativo a la asistencia sanitaria y en unas garantías mínimas de asistencia sanitaria en caso de enfermedad11. En este contexto, las obligaciones que asumen y declaran los Estados desde un enfoque de derechos humanos se fortalecen en los años 60 y 70.
En 1975 comienza a difundirse por parte de la OMS el concepto de medicamentos esenciales, disponibles a precios razonables en su forma genérica. Esto en referencia a aquellos que no están amparados por una patente farmacéutica, que se comercializan bajo el nombre del principio activo y cuya competencia usualmente conduce a una reducción significativa de los precios y a un mayor acceso de la población mundial.
Luego, en la Declaración de Alma-Ata12 de 1978, efectuada en la ex unión Soviética, en el marco de la Conferencia Internacional sobre Atención Primaria de Salud -patrocinada conjuntamente por la OMS y UNICEF-, se acuña el objetivo mundial de alcanzar el cubrimiento en salud para todos en el año 2000, y se declara que la atención primaria de salud comprende al menos el suministro de medicamentos esenciales.
Todo ello deriva en el Listado de Medicamentos Esenciales, aprobado por la AMS en 1979, con la creación del Programa de Acción sobre Medicamentos Esenciales13. Este listado tiene por objeto fijar aquellos productos considerados, desde el punto de vista sanitario, de primera necesidad, debiendo estar disponibles en los sistemas de salud en todo momento, en cantidades suficientes y a un precio que los pacientes y la comunidad puedan pagar. Fármacos antirretrovirales, vacunas y otros medicamentos de alto costo utilizados en los programas gubernamentales constituyen ejemplos de ello.
Cada Estado formula su propio listado de medicamentos esenciales de acuerdo a sus prioridades sanitarias. En ausencia de aquel listado, serán considerados tales los medicamentos incluidos en la lista modelo de medicamentos esenciales de la OMS, sujeta a cualquier revisión contextual lógica14. Este impulso incluso lleva a la OMS a diseñar plantas farmacéuticas de bajo costo, para la producción de medicamentos genéricos en países en desarrollo, con capacidad para atender una población de tres a cinco millones de personas15.
Por otra parte, el concepto de medicamento esencial generaba, como documenta Greene16, honda preocupación y fuertes críticas por parte de la poderosa industria farmacéutica en Estados unidos y en Europa, asociada en la Federación Internacional de Fabricantes y Asociaciones Farmacéuticas, la que declaraba su rechazo a este concepto, considerándolo inaceptable para sus intereses y comunicando esta postura al Director General de la OMS de la época, Halfdan Mahler.
Las aprehensiones de la industria ante la Dirección General de la OMS documentadas por Greene tenían varias aristas que tradicionalmente han sido motivo de sus preocupaciones, entre ellas: dudas relativas a la capacidad de las autoridades regulatorias para proporcionar garantías sobre la bioequivalencia o intercambiabilidad del suministro de medicamentos dentro de su jurisdicción; las graves repercusiones que generaría desincentivar el uso de medicamentos de marca en la calidad de los productos farmacéuticos; y las reservas sobre la política de medicamentos esenciales y la promoción de medicamentos genéricos frente a medicamentos de marca, considerando que la OMS excedía sus propias capacidades para monitorear normas sobre medicamentos.
Los intereses económicos en discusión eran muy importantes y ya asomaba una industria de medicamentos genéricos en países en desarrollo, como era el caso del gigante suramericano, Brasil, que preocupaba fuertemente a la influyente Asociación de Fabricantes Farmacéuticos de Estados unidos, ante el temor de que pudiera rápidamente expandirse a otros mercados del Sur a través de redes de distribución Sur-Sur y al resto del mundo en desarrollo con genéricos producidos en infracción de sus patentes17.
El trasfondo de la problemática que aquejaba a las poderosas firmas farmacéuticas del Norte en esta época era la ausencia de una legislación internacional que fijara normas mundiales comunes, de manera que un producto farmacéutico de marca patentado en un país en una situación monopólica por el tiempo de duración de la patente, podía al mismo tiempo encontrarse en una zona de competencia genérica en otro país que no concedía patente farmacéutica18.
Esta disconformidad con la heterogeneidad de las normas de propiedad intelectual a nivel internacional se acrecienta una vez que se dicta en Estados unidos, en 1984, la famosa Hatch-Waxman Act19(Drug Price Competition and Patent Term Restoration Act), que tiene el mérito de sentar en Estados unidos las bases de un sistema que logró, por una parte, equilibrar y conjugar una robusta industria de medicamentos genéricos, y por otra, fijar los incentivos necesarios para impactar positivamente en la investigación y desarrollo de productos farmacéuticos a través de empresas farmacéuticas de innovación.
De tal manera, con la entrada en vigencia de la Hatch-Waxman Act se multiplican las exigencias y presiones de parte de las naciones desarrolladas que cuentan con una poderosa industria farmacéutica, para proteger en el resto del mundo de manera adecuada los intereses de este sector. Lo anterior teniendo en cuenta que previo a la creación de la OMC y del establecimiento del Acuerdo sobre los ADPIC en 1995, más de 50 países contemplaban en sus legislaciones la prohibición de patentes sobre productos farmacéuticos20.
1.2. El debate sobre el comercio y los derechos humanos en la salud pública
Si bien la OMC y sus acuerdos anexos comienzan a aplicarse en 1995, es preciso señalar que de acuerdo con Lang el régimen internacional de comercio en el mundo experimentó un "giro neoliberal"21 durante las últimas tres décadas del siglo XX, comenzando a tomar forma institucional concreta el "Estado neoliberal"22, en una variedad de países alrededor del mundo, en los años ochenta y noventa23. Incluso, dicho autor destaca el experimento chileno de mediados de los setenta por el hecho de anticiparse a Estados unidos y el Reino unido, países que proveen el primer laboratorio de ideas neoliberales durante la década de 1980, previo a su extensión a mediados de los noventa, de modo disparejo y parcial, pero aun así de manera reconocible, en el resto del mundo24.
En el comercio internacional, a partir de la Ronda Uruguay de negociaciones del GATT efectuadas entre 1986 y 1994 se logra en Marrakech, en abril de 1994, la creación de la OMC, como un esfuerzo de la comunidad internacional dirigido a promover el multilateralismo en la regulación de los intercambios a escala global. La OMC se expresa fundamentalmente por medio de acuerdos sobre distintas áreas de comercio y servicios, que obligan a los países a mantener sus políticas comerciales dentro de marcos convenidos. Estos acuerdos, "aunque son negociados y suscritos por los gobiernos, su objetivo es regular el comercio internacional en que participan los agentes económicos como productores de bienes y servicios e importadores y exportadores"25.
Los Acuerdos anexos de la OMC abarcan bienes o mercancías26, servicios27 y propiedad intelectual28. Con su creación, el régimen del comercio internacional agregó la propiedad intelectual y el área de servicios a su mandato, con lo que incrementó ostensiblemente su campo de acción e influencia. Desde el inicio de las negociaciones para formar la OMC se manifiestan intereses en pugna entre países desarrollados y países en desarrollo. Como señala Gostin, durante la Ronda Uruguay de negociaciones se genera un acuerdo implícito -"The Grand Bargain"- a través del cual el Norte global consigue acuerdos comerciales en el área de servicios, propiedad intelectual y inversiones, además de la creación de una nueva organización comercial con capacidad para hacer cumplir las decisiones, mientras que el Sur global obtiene acceso a los mercados del Norte en agricultura y manufacturas intensivas en mano de obra29.
Para Susan Sell, en lo que respecta específicamente al Acuerdo sobre los ADPIC, este refleja el interés de empresas globales que intentan ampliar su control sobre la propiedad intelectual:
... amplía los derechos de patente hasta los 20 años; obliga a los países en desarrollo a otorgar protección mediante patente a los productos farmacéuticos; restringe de manera estricta las condiciones en que los Estados pueden expedir licencias obligatorias, y reduce la autonomía de los Estados en el diseño de políticas de propiedad intelectual que se ajusten a sus diversos niveles de innovación y desarrollo económico30.
Las tensiones y conflictos que generó el Acuerdo sobre los ADPIC entre países desarrollados con una poderosa industria farmacéutica y países en desarrollo se reflejan en las controversias suscitadas ante el OSD de la OMC31, como se estudia en el apartado II de este trabajo.
En nuestro concepto, el giro neoliberal que sufre el régimen de comercio internacional al que se refiere Lang, y que deriva en el debate sobre el comercio y los derechos humanos, se manifiesta con nitidez en el acceso a medicamentos esenciales con la Declaración de Doha y el revuelo que genera en la opinión pública32.
Como lo indican Mclnnes y Lee33, la OMC se involucró en la salud global casi por accidente, a través de sus intentos de globalizar los derechos de propiedad intelectual. Debido al efecto negativo del acuerdo sobre los ADPIC sobre el acceso equitativo a los medicamentos, especialmente las terapias antirretrovirales para el tratamiento del VIH/SIDA, la OMC fue objeto de furiosas campañas por parte de organizaciones de la sociedad civil, grupos de pacientes y defensores de los derechos humanos de portadores del VIH/SIDA, por un lado, y empresas farmacéuticas, por el otro.
Esta tensión deriva en la colisión del derecho a la salud con el derecho de propiedad intelectual en tratados internacionales, actualmente en vigencia para todos los Estados de Suramérica que lo suscriben, como se observa en el cuadro a continuación.
Cuadro N°1
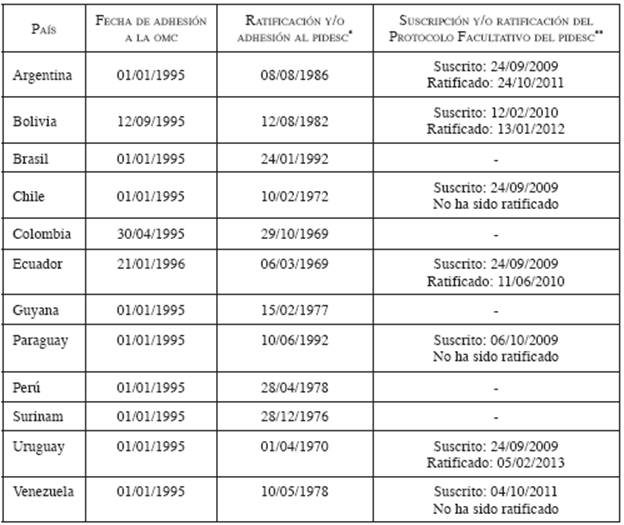
*El PIDSEC fue adoptado y abierto a la firma, ratificación y adhesión por la Asamblea general en su resolución 2200 A (xxi), de 16 de diciembre de 1966, y entró en vigencia el 3 de enero de 1976, de conformidad con el artículo 27. Disponible en: https://treaties.un.org/pages/Treaties.aspx?id=4&subid=A&lang=en
**El protocolo Facultativo del PIDESC fue adoptado en nueva York el 10 de diciembre de 2008 y entró en vigencia el 5 de mayo de 2013, en conformidad con el artículo 18(1).
Fuente: elaboración propia, a partir de datos disponibles en OMC34 y ONU35.
En efecto, para ser miembros de la OMC, los países deben suscribir el Acuerdo sobre los ADPIC, que impone patentes que hacen que los medicamentos sean inaccesibles para los gobiernos y residentes en países de medianos y bajos ingresos, siendo que años antes habían firmado y ratificado el PIDESC de la ONU que los obliga a facilitar el acceso a los medicamentos36.
Para aquilatar la magnitud del impacto que puede generar la colisión de derechos basta considerar que ya a principios de este siglo, de 141 miembros de la OMC que se habían comprometido a aplicar las normas mínimas de protección de la propiedad intelectual en el Acuerdo sobre los ADPIC, 111 habían ratificado el PIDESC37. Actualmente, el PIDESC cuenta con 165 estados parte38 y la OMC con 164 estados miembros39. Los 12 países suramericanos son Estados miembro de la OMC y Estados parte del PIDESC.
2. Impacto del acuerdo sobre los ADPIC en el acceso a medicamentos esenciales
2.1 Impacto en Suramérica
En nuestro concepto, el fortalecimiento de la patente farmacéutica contemplado en el Acuerdo sobre los ADPIC ha provocado dos efectos principales: afectar a las poblaciones vulnerables de los países suramericanos cuyo sistema de seguridad social no logra cubrir los medicamentos esenciales, o bien imposibilitar su financiamiento sostenido por los sistemas de seguridad social crecientemente deficitarios.
Por una parte, limita severamente la capacidad de los países en desarrollo para diseñar políticas de propiedad intelectual que se ajusten a sus diversos niveles de innovación y desarrollo económico40; por la otra, incrementa los derechos exclusivos de explotación de dominio privado que detentan habitualmente empresas farmacéuticas de alcance global. Para ilustrar la importancia económica que han asumido estas empresas en la actualidad es de señalar que entre las 50 compañías transnacionales más rentables en el año 2008, seis de ellas eran gigantes farmacéuticas: Johnson & Johnson (n.° 18), GlaxosmithKline (n.° 31), Roche Group (n.° 33), Novartis (n.° 34), Pfizer (n.° 35) y Merck (n.° 38)41.
Las 10 compañías farmacéuticas más grandes por ventas en 2010 corresponden a empresas trasnacionales con casa matriz en Estados Unidos o Europa42; en su orden: Pfizer, con casa matriz en Estados Unidos; Sanofi Aventis, con casa matriz en Francia; Novartis, con casa matriz en suiza; GlaxosmithKline, con casa matriz en Reino Unido; AstraZeneca, con casa matriz en Reino Unido; 6) Merck & Co., con casa matriz en Estados Unidos; Johnson & Johnson, con casa matriz en Estados Unidos; Eli Lilly & Co., con casa matriz en Estados Unidos; Bristol-Myers Squibb, con casa matriz en Estados Unidos, y Abbott Laboratories, con casa matriz en Estados Unidos. Por si fuera poco, la tendencia en materia de fusiones y adquisiciones provee evidencia de una concentración cada vez mayor al interior de la industria farmacéutica.
El impacto en suramérica desde la entrada en vigencia del Acuerdo sobre los ADPIC ha sido enorme:
1. Para Brasil y Argentina, con capacidad industrial en medicamentos, el Acuerdo sobre los ADPIC significó nada menos que la obligación de implementar la protección de patentes de medicamentos en sus legislaciones nacionales.
Previo al Acuerdo sobre los ADPIC, Brasil y Argentina contemplaban en sus legislaciones la prohibición de patentes sobre productos farmacéuticos. Esto obedecía a razones de salud pública, en especial el temor de que las patentes limitaran el acceso a un bien esencial como es el medicamento43, lo cual les había permitido desarrollar una industria de medicamentos genéricos, especialmente vigorosa en el caso del Brasil, como se dijo en el primer apartado de este trabajo.
En Brasil la Ley de Propiedad Industrial 5.772 de 1971 no incluía el reconocimiento de patentes para productos y procesos farmacéuticos, lo que cambia sustancialmente con la Ley de Propiedad Industrial 9279 de 1996, que fija la obligatoriedad de conceder patentes para el sector farmacéutico impuesta en el Acuerdo sobre los ADPIC. En el caso de Argentina, la patentabilidad de los productos farmacéuticos fue reconocida por medio de la Ley de Patentes y Modelos de Utilidad 24.481 de 1995; esta vino a reemplazar la Ley 111 de 1864, que solo admitía la protección por patentes de los procedimientos para la fabricación de medicamentos.
Como advierte Maskus44, los impactos más destacados de una importación de productos de tecnologías avanzadas se observan precisamente en países que presentan fuertes capacidades de imitación como Brasil, India y Argentina.
El impacto negativo provocado por la introducción del Acuerdo sobre los ADPIC en la industria doméstica de Brasil es notorio, toda vez que uno de sus pilares competitivos se basaba en la comercialización de medicamentos similares -copias de los medicamentos de marca-, no estando en condiciones de competir con los oligopolios internacionales en la producción de medicamentos de innovación45.
2. En el caso de Chile, que no logró desarrollar una industria nacional de medicamentos relevante, con anterioridad al Acuerdo sobre los ADPIC ya contemplaba la protección de medicamentos por medio de patentes farmacéuticas. De tal manera, el impacto del Acuerdo se manifiesta en el incremento de la duración de la patente farmacéutica, para adecuarla al estándar mínimo de 15 a 20 años de protección. La Ley 19.996 de 2005, que introduce reformas a la Ley 19.039 de 1991, sobre propiedad industrial, viene a cumplir con los compromisos contraídos con la OMC en el marco del Acuerdo sobre los ADPIC.
Así las cosas, el tránsito a la entrada en vigencia del Acuerdo sobre los ADPIC es menos dramático para Chile que para Argentina y Brasil, por cuanto su impacto se refiere al incremento en la duración de la patente a favor de las grandes firmas transnacionales, y no a la introducción de la protección de la patente farmacéutica en su legislación.
Como consecuencia de aquello, Chile, en el ámbito farmacéutico, no ha estado involucrado en controversias ante el OSD ni tampoco ha participado en ellas en calidad de tercero. Por el contrario, ha suscrito numerosos TLC, entre ellos el celebrado con Estados Unidos en 2003 y que será abordado en el apartado III.
3. En el caso de Colombia, Ecuador, Perú y Bolivia, que integran la CAN, el impacto también ha sido sustantivo.
Luego de introducir el patentamiento de productos farmacéuticos en 1991, se adoptó la Decisión 344 de 1993, de Régimen Común sobre Propiedad Industrial, de la CAN -"Acuerdo de Cartagena"-, previo a la creación de la OMC y el Acuerdo sobre los ADPIC, cuyo artículo 7 letra e) fijó en carácter de no patentables "las innovaciones relativas a productos farmacéuticos que figuren en la lista de medicamentos esenciales de la Organización Mundial de la salud (OMS)"46.
Sin embargo, como se pudo observar en el cuadro 1, los 4 países de la CAN, para ser Estados miembros de la OMC47, suscribieron, en calidad de Anexo, el Acuerdo sobre los ADPIC. Y por ende, en aras del cumplimiento del Acuerdo48, la excepción a la patentabilidad de los productos farmacéuticos incluidos en la lista de medicamentos esenciales fue dejada sin efecto con la adopción por la CAN de la Decisión 486 de 2000, que sustituyó la Decisión 344.
Así lo refleja Jiménez-Valderrama al referirse a esta Decisión de la CAN que se aplica en Colombia, al indicar:
... en nuestro ordenamiento jurídico, las patentes de invención se regulan a través de la Decisión 486 de 2000 de la Comisión de la Comunidad Andina con vigencia en todo el territorio de la Comunidad (Colombia, Ecuador, Perú y Bolivia). Compartimos de esta forma con los demás países miembros de la Comunidad Andina una regulación jurídica universal que es instrumento necesario para garantizar el establecimiento de un mercado único entre los países miembros sin obstáculos para el intercambio comercial de mercancías y servicios49.
Luego, en el caso de Perú y Colombia, cada uno de ellos procedió a suscribir con Estados Unidos un tratado de libre comercio (Perú en 2009, Colombia en 2012), que incorpora disposiciones que refuerzan los derechos de propiedad intelectual y la patente farmacéutica.
2. 2. Solución de controversias sobre patentes farmacéuticas en la OMC
Una diferencia de gran trascendencia en cuanto a la aplicación y práctica de los tratados internacionales del ámbito del DIDH, por una parte, y del Acuerdo de la OMC, por otra, radica en que este último contempla y aplica con efectividad un mecanismo de solución de diferencias comerciales de carácter vinculante y obligatorio, mientras que para los primeros, si bien ellos contemplan el mecanismo de quejas entre Estados, el mismo nunca se ha implementado, habiéndose aplicado en su lugar el mecanismo de queja o denuncia de particulares en contra de los Estados, con una aplicación mucho más acotada y limitada.
En el caso de la OMC, respecto de cualquier diferencia que pudiere surgir en la interpretación y aplicación de sus acuerdos comerciales, sus Estados miembros disponen del mecanismo de solución de diferencias comerciales ante el OSD.
Este procedimiento se compone de diversas etapas: primero, la solicitud de celebración de consultas, cuando un país reclama contra la conducta de otro y solicita "sentarse a conversar" con él; segundo, de no alcanzar una negociación sobre la diferencia, el reclamante pide la "constitución del Grupo Especial" -panel de expertos-, que elaborará un informe resolviendo la diferencia, haciendo las veces de tribunal de primera instancia; tercero, de existir disconformidad de una parte o de ambas por la resolución del Grupo Especial, el asunto pasa al Órgano de Apelación, cuya decisión final resuelve el litigio y le recomienda al perdedor la aplicación de determinadas medidas a fin de dejar de transgredir el Acuerdo de la OMC; y finalmente, si esta recomendación no se cumple en un plazo determinado, el reclamante puede solicitar la aplicación de sanciones comerciales al perdedor o "retorsiones".
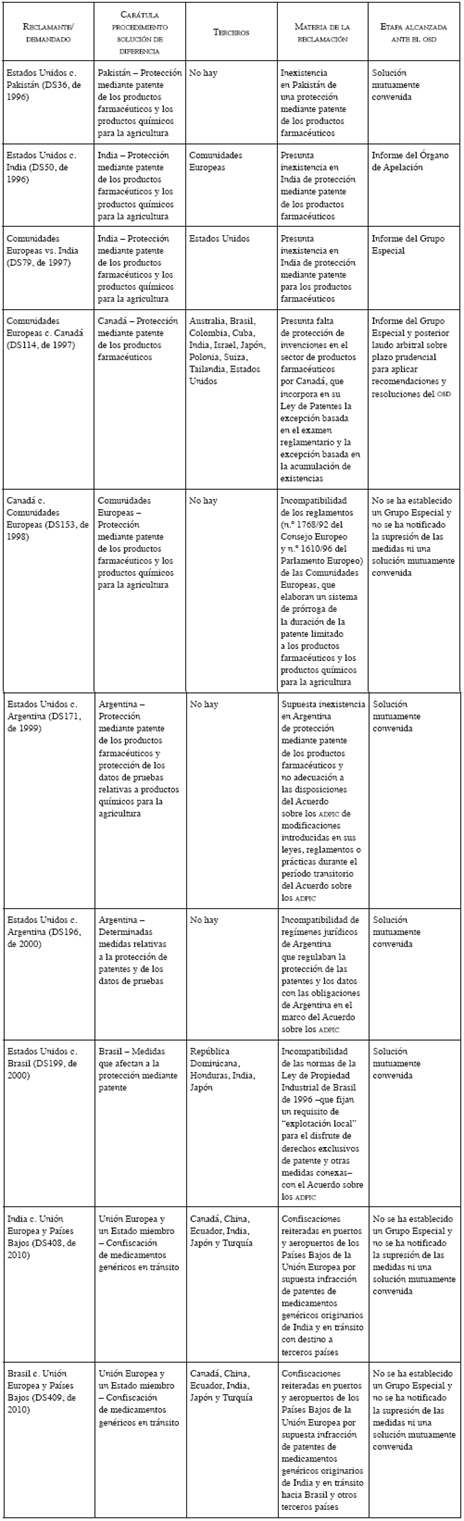
A continuación se sistematizan las 10 reclamaciones de solución de diferencias comerciales referidas específicamente a patentes de productos farmacéuticos50 que hasta la fecha han sido presentadas ante el OSD51.
2.3 Debate sobre el acceso a medicamentos en el OSD
Resulta ilustrativo dar cuenta de los casos sometidos ante el OSD sobre patentes farmacéuticas53, en el ámbito específico del acceso a los medicamentos esenciales, cuya evaluación permite formular las siguientes observaciones principales:
1. En estas controversias suele señalarse el enfrentamiento entre derechos de propiedad intelectual promovidos en defensa de empresas farmacéuticas, por una parte, y requerimientos de protección de la salud pública, por otra, involucrando aspectos cruciales del acceso a los medicamentos54.
En la controversia que enfrentó a las Comunidades Europeas con Canadá (DS114, de 1997) se consagra por el OSD la excepción basada en el examen reglamentario o "cláusula Bolar"55, de mucha relevancia en la actualidad. Esta disputa se origina por la incorporación en la Ley de Patentes de Canadá de la disposición relativa al examen reglamentario -art. 55.2(1)-, dirigida a permitir que un tercero, no titular de la patente, importe, fabrique y utilice un producto patentado antes de su expiración, con el solo objeto de obtener la autorización de comercialización ante la autoridad sanitaria respectiva. Con ello se acelera el proceso de registro sanitario y se facilita la entrada del medicamento genérico en el mercado para su venta tan pronto expire la patente farmacéutica56, disposición que el OSD en definitiva consideró compatible con el Acuerdo sobre los ADPIC. Así se evita un aprovechamiento de la patente farmacéutica por parte de su titular por un período superior a los 20 años contemplados en el Acuerdo sobre los ADPIC.
Por su parte, en la controversia que enfrentó a Estados Unidos con Brasil (DS199, de 2000), en plena crisis del VIH/SIDA en el gigante suramericano, se somete a discusión ante el OSD la facultad de los Estados miembros para incluir disposiciones en su legislación nacional que habiliten la expedición de licencias obligatorias57. Estados Unidos reclama que la disposición incorporada por Brasil en el artículo 68 de la Ley de Propiedad Industrial (Ley 9.279 de 1996) es incompatible con las disposiciones del Acuerdo sobre los ADPIC. Esta norma fija un requisito de "explotación local" -producción en el territorio de Brasil del producto patentado, y no su importación desde el exterior-, que subordina el disfrute de derechos exclusivos de patente sobre el producto (ej.: medicamento) a su producción dentro del territorio brasileño.
En caso contrario, el gobierno de Brasil queda habilitado para conceder eventualmente una licencia obligatoria si el producto no se "explota" en su territorio, impidiendo así el incremento del precio que el titular de la patente genera al importar su producto desde el exterior. En definitiva, en este caso se alcanzó una solución mutuamente convenida entre ambos países, en la que Brasil se comprometió a celebrar conversaciones previas con Estados Unidos en caso de considerar necesario aplicar el artículo 68 para conceder una licencia obligatoria relativa a patentes de empresas de Estados Unidos.
Asimismo, hay dos emblemáticas controversias -India c. Unión Europea y los Países Bajos (DS 408, de 2010) y Brasil c. Unión Europea y los Países Bajos (DS409, de 2010)- que atañen al "corazón" del acceso a medicamentos a nivel internacional, relativo a la producción y exportación de medicamentos genéricos. Ambas se basan en reclamaciones de India y Brasil, respectivamente, por reiteradas confiscaciones de despachos de medicamentos genéricos originarios de India en puertos y aeropuertos de los Países Bajos, cuando se encontraban en tránsito a terceros países, todos países en desarrollo (Nigeria, Colombia, Perú y Brasil, entre otros). Las confiscaciones se basan en la "ficción de la fabricación": medicamentos genéricos fabricados en India y en tránsito a terceros países fueron tratados como si se hubieran fabricado en los Países Bajos, con independencia de la situación de la patente del medicamento en los países de origen y destino. Las patentes presuntamente vulneradas correspondían a Novartis, Glaxo, Merck, Eli Lilly, Sanofi-Aventis y E. I. Dupont de Nemours. Ambas controversias, luego de la solicitud de celebración de consultas, no registraron desarrollo posterior ante el OSD.
2. La gran mayoría de estas controversias dan cuenta de reclamaciones en que se confrontan los intereses de países desarrollados poseedores de una poderosa industria farmacéutica y de países en desarrollo: Estados Unidos c. Pakistán (DS36, de 1996); Estados Unidos c. India (DS50, de 1996); Comunidades Europeas c. India (DS79, de 1997); Estados Unidos c. Argentina (DS171, de 1999); Estados Unidos c. Argentina (DS196, de 2000); Estados Unidos c. Brasil (DS199, de 2000); India c. Unión Europea y Países Bajos (DS408, de 2010); Brasil c. Unión Europea y los Países Bajos (DS409, de 2010).
En ocho de los diez casos se da esta circunstancia de controversias entre países desarrollados y países en desarrollo, siendo importante destacar que en la mitad de ellos (4 de 8) se encuentran involucrados países suramericanos (Argentina en dos controversias y Brasil en otras dos).
3. Varias controversias implican la adecuación y modificación de la legislación interna del Estado miembro de la OMC -en calidad de demandado- a las normas del Acuerdo sobre los ADPIC, lo que da cuenta de las implicaciones y trascendencia de este mecanismo de solución de diferencias comerciales de la OMC, y que no se da en el sistema de derechos humanos en que se han implementado las quejas individuales de particulares contra Estados una vez agotadas las instancias internas de protección, pero no se ha dado aplicación a las quejas entre Estados en el sistema de protección de los derechos humanos. Controversias de este tipo de casos ante el OSD son: Estados Unidos c. India (DS50, de 1996); Comunidades Europeas c. India (DS79, de 1997); Comunidades Europeas c. Canadá (DS114, de 1997); Estados Unidos c. Argentina (DS196, de 2000).
4. Otras controversias dan cuenta de la colisión, en sede comercial, del derecho de propiedad intelectual reivindicado por países desarrollados, por una parte, con el derecho a la salud y la obligación básica de los países en desarrollo de facilitar a su población el acceso a medicamentos esenciales, por la otra . Ejemplos de ello son Estados Unidos c. Brasil (DS199, de 2000); India c. Unión Europea y los Países Bajos (DS 408, de 2010); Brasil c. Unión Europea y Países Bajos (DS409, de 2010), previamente reseñados.
Por tanto, es importante tener en cuenta que el OSD corresponde a sede comercial y no a sede de protección de derechos humanos, toda vez que casos significativos para el acceso a medicamentos pueden quedar sin registro formal de progreso -constitución de Grupo Especial, adopción de una solución mutuamente convenida u otra-, en la OMC -Canadá c. Comunidades Europeas (DS153/1998); India c. Unión Europea y los Países Bajos (DS 408/2010); Brasil c. Unión Europea y los Países Bajos (DS409/2010).
3. Desafíos para Suramérica
3.1. UNASUR y el CSS
Las obligaciones asumidas por todos los Estados de Suramérica en materia de derecho a la salud, y específicamente en lo relativo a facilitar a sus poblaciones el acceso a medicamentos esenciales en el marco del PIDESC, requieren ser enfrentadas por estos países como bloque, de manera convergente e integrada, atendidas las graves dificultades que enfrentan en este ámbito, con un enfoque de derechos para sus habitantes y una voz conjunta ante instancias internacionales.
A la luz de las dificultades mencionadas en este trabajo, primero referidas a la colisión de derechos en tratados internacionales que dificulta el acceso de sus poblaciones a medicamentos esenciales, y luego al impacto que ha generado el fortalecimiento a nivel mundial de la patente farmacéutica, causa expectación el surgimiento de Unasur en el año 2008, y en especial la proyección que pueda generar el CSS, por constituir un espacio de integración diferente a acuerdos regionales como el Mercosur y la CAN, aun cuando su proceso de integración59 parte de la base de los logros y avances del Mercosur y la CAN.
Unasur representa un esfuerzo conjunto sin precedentes al constituir un tratado internacional que incorpora a los doce países de Suramérica, cuenta entre sus objetivos principales la cooperación política en materia de salud, y formula una propuesta de integración regional con base en la definición de la salud como un derecho social. De ahí su relevancia para fortalecer el acceso a medicamentos esenciales, al constituir, como lo destacan Herrero y Tussie60, un espacio de socialización para la construcción de consensos y el establecimiento de intereses comunes.
En definitiva, Unasur recupera la salud no solo como un problema sanitario y de políticas públicas sino, fundamentalmente, como uno de derechos y de gobernanza61. Diferente al enfoque y perspectiva en que se aborda la salud en el Mercosur y la CAN, marcando una diferencia normativa en relación con aquellas experiencias62. Para Riggirozzi y Grugel, Unasur se encuentra desarrollando una forma híbrida de legitimidad que se centra en resultados y se basa en una visión normativa de su papel en la provisión de bienes públicos regionales, a saber, democracia, derechos humanos y la erradicación de la pobreza63.
La relevancia otorgada al acceso a medicamentos esenciales en el CSS queda demostrada al definir su plan de acción coordinado por grupos de trabajo temáticos en cinco programas, siendo uno de ellos el acceso universal a medicamentos64. El agrupar a los doce países en esta instancia, con un enfoque priorizado en el derecho a la salud, en nuestro concepto está llamado a fortalecer, desde la convergencia y la unidad suramericana, la obligación de cumplir que ha suscrito cada Estado signatario del PIDESC de facilitar el acceso a medicamentos esenciales, en sintonía con las directrices emanadas del Comité del PIDESC en su Observación General n.° 14 de 2000.
Para ilustrar las enormes proyecciones de Unasur en materia de acceso a medicamentos esenciales, nos parece necesario distinguir entre las acciones de fomento de la cooperación horizontal o intrarregional que lleva a cabo, por una parte, y aquellas relativas al ejercicio de la diplomacia transversal o extrarregional, por otra65.
3.2. Cooperación intrarregional y diplomacia transversal
A continuación destacamos aquellos desafíos en curso que se encuentran en sintonía con el cumplimiento de obligaciones asumidas por nuestros Estados en el marco del derecho a la salud frente al impacto generado en Suramérica por el cumplimiento de obligaciones internacionales en materia de derechos de propiedad intelectual.
1. La cooperación horizontal o intrarregional. Aquí destaca la adopción de acciones de cooperación y el impulso a políticas comunes al interior del bloque regional, en fase de implementación. En esta línea se insertan alternativas para avanzar hacia una soberanía suramericana de medicamentos en el ámbito del Grupo de Trabajo de Acceso Universal a Medicamentos66.
En ella destaca el Banco de Precios de Medicamentos de Unasur, cuyo objetivo es la creación de una red de información sobre compras que apoye la toma de decisiones en todo el continente y garantice el acceso de la población a medicamentos67. Con ello se pretende fortalecer la capacidad de los países miembros de Unasur en la gestión de los procesos de adquisición de medicamentos, servir de apoyo al control de precios -al disponer de un sistema informatizado de precios de compras de medicamentos y datos vinculados- y, en definitiva, apoyar la capacidad negociadora frente a los oferentes.
También cabe destacar el "Mapa de las capacidades regionales para la producción de medicamentos", dirigido a identificar la capacidad industrial en la región para el diseño de políticas públicas de medicamentos, que permita avanzar hacia una soberanía productiva regional en la producción de medicamentos. Para fomentar el acceso a vacunas y medicamentos a través de políticas comunes de producción de medicamentos, el CSS en su VII Reunión, en octubre de 2012, aprobó la identificación de las capacidades industriales existentes en la región68.
Por último, se proyecta el desarrollo de un complejo de producción de salud que permita el acceso a medicamentos de grupos vulnerables. Para Herrero y Tussie este objetivo es posible de alcanzar, haciendo notar que Argentina ha fortalecido su producción pública de medicamentos y que Brasil es reconocido por su producción de medicamentos genéricos69.
Por tanto, los esfuerzos que Unasur realiza en el ámbito del acceso a medicamentos para vincular la elaboración de políticas con enfoques basados en derechos70 van en la dirección correcta, y nuestros Estados suramericanos deben perseverar en la ejecución de estas acciones de cooperación.
2. Diplomacia transversal o extrarregional. Como destaca Riggirozzi, este aspecto constituye sin lugar a dudas un factor novedoso en relación con el regionalismo del Mercosur o de la CAN, dado que Unasur opera como bloque en decisiones en el marco de la OMS y frente a farmacéuticas internacionales71. Sin duda fortalece las posiciones de Suramérica, de manera que al liderazgo de Brasil en el ámbito internacional, y específicamente en la temática del acceso a medicamentos -como se pudo observar en el apartado I al abordar las controversias ante el OSD-, ahora se suma un poder colectivo que fortalece las posiciones de los Estados de Suramérica en su peso relativo en el concierto global.
De manera que al diseño y desarrollo de políticas comunes en el ámbito de la cooperación horizontal o intrarregional, se suma la participación como bloque regional con posiciones comunes que fortalecen su influencia y peso relativo en las discusiones y negociaciones en el ámbito multilateral de los países de Suramérica.
La influencia regional ahora adopta un peso sustancial relevante que fortalece de mucho mejor manera su peso específico en la OMS, y concretamente en la AMS. Faria, Giovanella y Bermúdez identificaron las resoluciones de la AMS sobre las cuales Unasur presentó posicionamientos comunes en el período comprendido entre 2010 y 2014. En 2010, las dos resoluciones de posición común del CSS estaban relacionadas con la producción de medicamentos. En los años siguientes, ese tema se mantuvo en el foco de los posicionamientos comunes del bloque, pero pasó a ser acompañado de otros, como el Reglamento Sanitario Internacional, en 2011 y 2014; la reforma de la OMS, en 2012 y 2013; y los Objetivos de Desarrollo del Milenio, en 2013 y 201472.
Esta unión permite generar estrategias regionales en apoyo a la coordinación de posiciones comunes de los países de Suramérica en los foros multilaterales, fortaleciendo la actuación en bloque como "jugador" global en salud73.
El CSS tiene un papel instrumental de alto perfil en la diplomacia global desarrollando posiciones comunes ante la OMS74. Como lo corroboran Faria, Giovanella y Bermúdez, gracias a este posicionamiento colectivo el Consejo Suramericano de Salud está ocupando todos los espacios de la OMS a partir de diferentes estrategias operativas. Además de la presentación de posiciones comunes en la AMS, Unasur ha reforzado su representación en su Consejo Ejecutivo. Los Estados miembros de Unasur actualmente ocupan la mitad de las seis vacantes para la región de las Américas. Tiene importancia estratégica el fortalecer la presencia del bloque en el Consejo Ejecutivo para asegurar que aquellos temas considerados prioritarios por los países de Suramérica sean incorporados en tabla en la siguiente sesión de la AMS75.
En definitiva, las acciones de nivel horizontal o intrarregional mencionadas previamente en este apartado complementan una diplomacia transversal o extrarregional exitosa. Por ejemplo, las acciones intrarregionales destinadas a fortalecer la capacidad industrial propia en el marco de Unasur consolidarán las negociaciones conjuntas con compañías farmacéuticas para la adquisición de vacunas y medicamentos.
Los países de Unasur se han comprometido a abstenerse de comprar medicamentos por encima de los precios fijados por el fondo de la Organización Panamericana de la Salud, en un intento por evitar que intereses comerciales circunstanciales se aprovechen del pánico y la incertidumbre provocados por la irrupción de epidemias76.
3.3. Cooperación Sur-Sur y TLC suscritos con normas ADPIC Plus
El desafío en Suramérica es de envergadura en materia de acceso a medicamentos esenciales, en razón del impacto que supuso el Acuerdo sobre los ADPIC. En nuestro concepto, las acciones en Unasur se orientan en la dirección correcta y la fortalecen como bloque regional, unido a la conveniencia de impulsar acciones de cooperación Sur-Sur entre los países de este hemisferio, teniendo en cuenta el predominio de patentes farmacéuticas detentadas por titulares privados del hemisferio norte.
Sin embargo, las actuaciones y obligaciones asumidas por los países de Suramérica en materia de acceso a medicamentos esenciales en este ámbito son disímiles. Para ilustrar esto, a continuación se aborda, primero, el decidido impulso de Brasil a la cooperación Sur-Sur, y por otra parte, el contraste que representa la suscripción por parte de Chile, Perú y Colombia, con Estados Unidos, de un TLC que contiene normas ADPIC Plus en materia de acceso a medicamentos esenciales.
3.3.1. La cooperación Sur-Sur y la influencia de Brasil
A nivel suramericano destacan los esfuerzos desplegados por Brasil para impulsar la influencia del hemisferio sur en el acceso a medicamentos y en el fortalecimiento de la cooperación Sur-Sur. Ha sido un país influyente en el ámbito farmacéutico a nivel mundial por más de 50 años, de manera que no puede extrañar el protagonismo que ha asumido en el contexto del debate sobre el comercio y los derechos humanos.
Junto a India -líder mundial en producción de medicamentos genéricos77-y otros países del hemisferio sur, como Sudáfrica, Brasil fue activo impulsor de la Declaración de Doha ante el OSD con motivo de la interpretación y aplicación de las normas del Acuerdo sobre los ADPIC. Y con India se ha asociado estratégicamente en el ámbito del acceso a medicamentos, como se manifiesta en las controversias sometidas ante el OSD en contra de la Unión Europea y los Países Bajos (DS408 y DS409).
Asimismo, Brasil ha estado presente como actor principal -desde antes del papel asumido por Unasur como bloque regional en el ámbito de la diplomacia transversal o extrarregional-, liderando e influyendo en muchos debates en el ámbito multilateral, especialmente en la OMS. Esto queda de manifiesto en el Grupo de Trabajo intergubernamental sobre Salud Pública, Innovación y Propiedad Intelectual, de la OMS, siendo actor relevante en todas las deliberaciones, discusiones y resoluciones que en el marco de la AMS se han dado y de las cuales da cuenta Howard Zucker, ex representante del Director General de la OMS en Materia de Propiedad Intelectual, Innovación y Salud Pública78. Compartirá causa en estas discusiones y deliberaciones con otros países del hemisferio sur, como Kenia y Tailandia, por ejemplo.
También queda de manifiesto en sus actuaciones en negociaciones sobre diferentes iniciativas en salud con un papel de liderazgo. Impulsa la Iniciativa sobre Política Exterior y Salud Mundial; la implementación del Código Global de la OMS de Práctica en el Reclutamiento de Personal de Salud; y en la Alianza Mundial para la Fuerza Laboral de Salud, entre otras iniciativas de carácter global79.
También cabe mencionar acciones de cooperación internacional Sur-Sur que ha desarrollado Brasil con países de África. Aquí es de señalar la fábrica de producción de medicamentos antirretrovirales para el VIH/SIDA instalada en Mozambique, país sin producción farmacéutica previa, y donde el proyecto impulsado desde el año 2003 ha contado con el apoyo científico y técnico de Brasil80.
De manera que el papel que se encuentra llamado a cumplir Brasil, en razón de su capacidad de producción de medicamentos y de la influencia que ha ejercido en el ámbito de la diplomacia en materia de salud global, es de gran relevancia para Unasur, para la cooperación con el resto de los países del conglomerado, y también para fortalecer e impulsar las relaciones de cooperación Sur-Sur con los países de este hemisferio.
3.3.2. TLC suscritos por Chile, Perú y Colombia con Estados Unidos
En paralelo, algunos países del continente -Chile, Perú y Colombia- han reforzado sus relaciones comerciales con Estados Unidos, mediante la suscripción de TLC de carácter bilateral que generan inquietud en el ámbito de la salud pública, debido a la asimetría de poder económico existente entre un país desarrollado y un país en desarrollo, que permite a Estados poderosos disponer de una vía alternativa para la creación de normas deseadas por ellos que no serían capaces de negociar con éxito a nivel multilateral81.
De tal manera, los TLC que suscriben países en desarrollo con países desarrollados a cambio de la apertura de mercados relevantes, suelen contemplar entre sus disposiciones normas ADPIC Plus82, en ámbitos de interés para sus respectivas industrias, entre ellas, la poderosa industria farmacéutica.
Estas normas hacen referencia a aquellas disposiciones que fijan estándares de propiedad intelectual más elevados que el Acuerdo sobre los ADPIC, o bien que eliminan o limitan las "flexibilidades ADPIC", lo cual inquieta desde la perspectiva del DIDH, al generar potencialmente sistemas de propiedad intelectual incompatibles con las obligaciones que asumen los Estados en virtud de las normas de derechos humanos83.
Como precisa Thomas84, con posterioridad al Acuerdo sobre los ADPIC Estados Unidos comenzó a suscribir una serie de TLC de carácter bilateral, requiriendo a sus contrapartes el cumplimiento de estándares en materia de patentes que exceden las obligaciones que asumen los Estados miembros de la OMC en el Acuerdo sobre los ADPIC.
Ello ha ocurrido en los TLC que Estados Unidos ha celebrado con Chile85 (2003), Perú86 (2009) y Colombia87 (2012), y que se encuentran vigentes. En ellos88 se han incorporado disposiciones relevantes en el capítulo relativo a los derechos de propiedad intelectual, que pueden afectar negativamente el acceso a medicamentos y que van más allá de las obligaciones que asumen los Estados en el Acuerdo sobre los ADPIC89.
En nuestro concepto, destacan en este ámbito las disposiciones referidas al incremento del ámbito de aplicación de la materia patentable; la protección de datos de prueba; la extensión del plazo de protección de la patente por demoras injustificables o retrasos irrazonables durante su otorgamiento, o bien para compensar la reducción injustificada o irrazonable del plazo efectivo de la patente como resultado del proceso de autorización de comercialización del medicamento; y la vinculación del registro sanitario de autorización de comercialización de un medicamento con la patente farmacéutica.
De partida, los TLC de Estados Unidos con Chile, Perú y Colombia contienen una disposición que interpreta el sentido y alcance de los términos "actividad inventiva" y "susceptibles de aplicación industrial" del artículo 27 del Acuerdo sobre los ADPIC90, dirigida a incrementar el ámbito de aplicación de la materia patentable: "Para los efectos de este artículo, una Parte podrá considerar las expresiones 'actividad inventiva' y 'susceptibles de aplicación industrial' como sinónimos de las expresiones 'no evidentes' y 'útiles', respectivamente"91.
Controversial ha resultado la inclusión de disposiciones sobre protección o exclusividad de los datos de prueba por Estados Unidos por la vía de tratados bilaterales. Esta protección pretende mantener por un período de tiempo en secreto los datos de prueba del proceso de investigación de un medicamento. Para Gómez, López y Araújo92, la protección por cinco años perseguida por Estados Unidos tiene por objeto negar el acceso de esta información que fue el elemento sustancial de la creación de las patentes, al otorgar el monopolio por un tiempo determinado a cambio de que el titular de la patente, como contraprestación a la sociedad, suministre información (transferencia tecnológica) que permita el avance científico en el campo, lo que de esta manera termina siendo desvirtuado. Esto acaece en los TLC de los tres países suramericanos con Estados Unidos93.
La extensión del plazo de protección de la patente farmacéutica por demoras injustificadas o retrasos irrazonables durante su otorgamiento94, o bien para compensar la reducción injustificada o irrazonable del plazo efectivo de la patente como resultado del proceso de autorización o aprobación sanitaria de comercialización95, se aborda en los TLC con Estados Unidos, al igual que la vinculación del registro sanitario de autorización de comercialización con la patente farmacéutica96.
Conclusiones
El Acuerdo sobre los ADPIC produjo un fuerte impacto en Suramérica que se manifiesta en las controversias sobre patentes farmacéuticas de Brasil y Argentina ante el OSD de la OMC.
Las normas de este acuerdo comercial provocaron dos efectos principales en la región: la reducción de la autonomía de sus países para diseñar políticas de propiedad intelectual ajustados a sus propios niveles de innovación y desarrollo económico, y el fortalecimiento de los estándares mínimos de protección de las patentes farmacéuticas, habitualmente en manos de empresas farmacéuticas globales con casa matriz en Estados Unidos o Europa.
Sus consecuencias en el acceso a medicamentos esenciales se han hecho sentir, afectando especialmente a la población más vulnerable que no cuenta con seguridad social para adquirirlos, o bien imposibilitando un sostenido financiamiento de los medicamentos esenciales por parte de los sistemas de seguridad social crecientemente deficitarios.
Sostenemos que, desde la perspectiva del derecho internacional de los derechos humanos, la suscripción por países suramericanos de normas ADPIC Plus en TLC y acuerdos comerciales de carácter internacional, que confieren al titular de la patente farmacéutica más derechos que los previstos en el Acuerdo sobre los ADPIC, es incompatible con las obligaciones relativas al acceso a medicamentos esenciales que emanan del artículo 12 del PIDESC, en el marco del derecho a la salud.
La necesidad de invertir en la producción regional de medicamentos esenciales se transforma en una obligación ineludible para los países de nuestra región. De tal manera, los avances en esta dirección del Consejo Suramericano de Salud de UNASUR marcan un rumbo positivo que debe ser profundizado. Esto se encuentra avalado por el posicionamiento común de este bloque regional ante la OMS, y por la intención de desarrollar negociaciones conjuntas con compañías farmacéuticas para la adquisición de vacunas y medicamentos.
Se requieren esfuerzos conjuntos de los países de Suramérica, de carácter permanente y sostenidos en el tiempo, para que puedan cumplir con las obligaciones asumidas con antelación a la creación de la OMC, en el marco del derecho a la salud del PIDESC, relativas a facilitar el acceso a medicamentos esenciales de sus poblaciones.