Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Ingeniería y Universidad
Print version ISSN 0123-2126
Ing. Univ. vol.15 no.1 Bogotá Jan./June 2011
Variables de operación en el proceso de transesterificación de grasas animales: una revisión1
Operation Variables in the Animal-Fat Transesterification Process: a Review2
Variáveis de operação no processo de transesterificação de gorduras animais: uma revisão3
Andrés Rojas-González4
Erika Girón-Gallego5
1Este artículo se deriva del proyecto de investigación denominado Etanólisis de aceites usados provenientes de restaurantes utilizando biocatalizadores nativos de origen vegetal y animal, código QUIPU: 2010100816 y código DIPAL 09CNALPI03, desarrollado por la Universidad Nacional de Colombia, sede Palmira, Colombia.
2Submitted on April 7, 2010. Accepted on June 10, 2011. This article is derived from the research project Ethanolysis of Used Oils from Restaurants through the Use of Local Biocatalysts of both Vegetable and Animal Origin, registration numbers QUIPU: 2010100816 and 09CNALPI033479, developed by the Universidad Nacional de Colombia, sede Palmira, Colombia.
3Data de recepção: 7 de abril de 2010. Data de aceitação: 10 de junho de 2010. Este artigo deriva do projeto de pesquisa denominado Etanólise de óleos usados provenientes de restaurantes utilizando biocatalizadores nativos de origem vegetal e animal, código QUIPU: 2010100816 e código DIPAL 09CNALPI03, desenvolvido pela Universidade Nacional da Colômbia, sede Palmira, Colômbia.
4Ingeniero químico, Universidad Nacional de Colombia, sede Palmira, Colombia. Magíster en Ingeniería Química, Universidad del Valle, Cali, Colombia. Doctor en Ingeniería Química, Universidad del Valle. Correo electrónico: anfrojasgo@unal.edu.co.
5Ingeniera agroindustrial, Universidad Nacional de Colombia. Ingenio Manuelita, Valle del Cauca, Colombia. Correo electrónico: erika.giron@manuelita.com.
Fecha de recepción: 7 de abril de 2010. Fecha de aceptación: 10 de junio de 2010.
Resumen
En este artículo se presentan los resultados de la revisión bibliográfica sobre la influencia de la temperatura y tiempo de reacción, tipo de alcohol, relación molar-alcohol (grasa, tipo y concentración de catalizador, intensidad del mezclado y concentración de ácidos grasos libres y humedad) en el rendimiento de la producción de biodiésel por transesterificación química y biológica de grasas animales. Se encontró que la relación molar-alcohol: grasa utilizada en la transesterificación de grasas animales depende de la grasa y tipo de catálisis empleada en el proceso. También que a presión atmosférica, la temperatura debe ser menor de 50 °C en biocatálisis, de 80 °C en catálisis homogénea y de 250 °C en catálisis heterogénea. Además, la lipasa de la bacteria P. cepacia es la más utilizada en biocatálisis de grasas animales. Conjuntamente, se encontró que para sebo de res el rendimiento está en 50%-95% (tiempo de reacción: 0,75-3 h), grasa de pollo en 33%-99% (0,5-1,5 h), aceite de pescado en 76%-98% (0,17-1,5 h), sebo de pato en 75%-97% (3 h), sebo de carnero en 90%-98% (24 h) y sebo de cerdo en 97% (0,3 h).
Palabras clave: Combustibles diésel, transesterificación, aceites y grasas.
Abstract
This work presents a review of the literature about the influence of parameters such as temperature and time reaction, alcohol type, alcohol: fat molar ratio, catalyst type and concentration, mixed intensity, as well as free fatty acid and moisture concentration, on biodiesel production yield in chemical and biological transesterification of animal fats. It was found that the alcohol: fat molar ratio required by animal fat transesterification depends on the fat and the type of catalysis that are used in the process. It was also found that, under atmospheric pressure, the temperature must be below 50 °C in biocatalysis, 80 °C in homogeneous catalysis, and 250 °C in heterogeneous catalysis. Additionally, lipase from P. cepacia bacteria is the most widely used in biocatalysis of animal fats. It was also found that yield for beef tallow is between 50-95% (reaction time: 0.75-3 h); in the case of chicken fat, between 33-99% (0.5-1.5h); for fish oil, between 76-98% (0.17-1.5 h); for duck tallow, between 75-97% (3 h); for sheep tallow, between 90-98% (24 h), and, for pork tallow, 97% (0.3 h).
Key words: Diesel fuels, transesterification, oils and fats.
Resumo
Neste artigo apresentam-se os resultados da revisão bibliográfica sobre a influência da temperatura e tempo de reação, tipo de álcool, relação molar-álcool (gordura, tipo e concentração do catalisador, intensidade da mistura e concentração de ácidos graxos livres e umidade) no rendimento da produção de biodiesel por transesterificação química e biológica de gorduras animais. Observou-se que a relação molar-álcoool: gordura utilizada na transesterificação de gorduras animais depende da gordura e tipo de catálise empregada no processo, e que a pressão atmosférica também, a temperatura deve ser menor que 50 °C em biocatálise, de 80 °C em catálise homogênea e de 250 °C em catálise heterogênea. Alem disso, a lipasa da bactéria P. cepacia é a mais utilizada em biocatálise de gorduras animais. Em conjunto, observou-se que sebo de res o rendimento está em 50%-95% (tempo de reação: 0,75-3 h), gordura de frango em 33%-99% (0,5-1,5 h), óleo de peixe em 76%-98% (0,171,5 h), sebo de pato em 75%-97% (3 h), sebo de carneiro em 90%-98% (24 h) e sebo de porco em 97% (0,3 h).
Palavras chave: Combustíveis diesel, transesterificação, óleos e gorduras.
Introducción
Debido a la crisis del petróleo de los años setenta (Bielecki, 2002), las investigaciones se han enfocado en buscar fuentes de energía renovables, biodegradables y con mejor calidad de los gases de combustión (Bhatti et al., 2008). Una de estas fuentes es el biodiésel, el cual es una mezcla de alquilesteres de ácidos grasos obtenidos por alcohólisis de aceites y grasas, tanto de origen vegetal (Rojas et al., 2010) como animal. El biodiésel es ambientalmente más amigable que el diésel, ya que no posee compuestos aromáticos ni azufrados y contiene cerca del 11% (p/p) de O2 (Canakci, 2007). Esto hace que los gases de combustión contengan menor cantidad de hidrocarburos, material particulado, CO y SO2 (Sharma et al., 2008; Cheng et al., 2008; Ameeret al., 2009). En la actualidad, el biodiésel se produce por alcohólisis de tres clases de materias primas:
- Aceites vegetales (Rojas et al., 2010): como girasol (Mittelbch, 1990), canola (Leclercq et al., 2001), coco (Tan et al., 2004), palma (Bo et al., 2007), soya (Liu et al., 2008), higuerilla (Benavides et al., 2008), jatrofa (Tamalampudi et al., 2008), ricino y colza (Perin et al., 2008).
- Grasas animales: como sebo de res (Muniyappa et al., 1996; Ma et al., 1998a, 1998b y 1999; Espinosa et al., 2009), pato (Chung et al., 2009) y carnero (Bhatti et al., 2008), manteca de cerdo (Wyatt et al., 2005; Lu et al., 2007; Dias et al., 2009), grasa de pollo (Wyatt et al., 2005; Armenta et al., 2007), aceite de pescado (Armenta et al., 2007; El-Mashad et al., 2008).
- Aceites y grasas usadas (Issariyakul et al., 2007; Ngo et al., 2008).
Pero su producción se ha enfocado en la alcohólisis de aceites vegetales, debido a su gran disponibilidad. Sin embargo, el costo de estas materias primas limita la producción de un biocarburante comercialmente viable. Una alternativa es obtener biodiésel de grasas animales y grasas usadas, ya que su costo es significativamente menor, debido a que son coproductos poco aprovechables de sus respectivas industrias. El biodiésel de estas fuentes tiene un alto poder calorífico y número de cetano. No obstante, su alto punto de nube y punto de obturación del filtro en frío hacen que su uso en climas fríos sea limitado (Canakci et al., 2007).
En Estados Unidos se producen cerca de 5,29 mil millones de toneladas de grasas animales principalmente: sebo no comestible (33,2%), grasas amarillas (22,6%), grasa de pollo (19%), sebo comestible (14%) y grasa y manteca de cerdo (11,2%) (Canakci et al., 2007). El rendimiento, conversión y cinética de la producción de biodiésel de aceites y grasas animales depende del tipo de grasa, el tipo de alcohol, la relación molar-alcohol (grasa, tipo y cantidad de catalizador, tiempo y temperatura de reacción e intensidad de mezclado) (Schuchardt et al., 1998; Sharma et al., 2009).
Los objetivos de este documento son, por un lado, revisar las diferentes variables de proceso que se han reportado en la literatura; por el otro, examinar su efecto en el rendimiento de la transesterificación durante la producción de biodiésel a partir de grasas animales.
1. Producción de biodiésel
Rudolf Diesel, creador del motor de encendido por compresión o motor diésel en 1900, demostró que el aceite de maní se puede utilizar como combustible en estos motores (Nitske et al., 1965). Sin embargo, esto trajo diversos problemas en el motor, como formación de depósitos de carbón y carbonizado en el inyector, dilución del aceite lubricante por contaminación con aceite vegetal y reducción de potencia y eficiencia del motor. Esto es provocado por la alta viscosidad y contenido de ácidos grasos libres, la baja volatilidad, las resinas y gomas y el contenido de cenizas de los aceites. Por lo tanto, para reducir los efectos de los aceites en el motor se ha planteado: (a) el pretratamiento térmico de los aceites para disminuir su viscosidad y tensión superficial, a fin de lograr mejor atomización, o (b) la utilización de mezclas aceite-diésel con modificaciones al motor para que pueda recibir la mezcla. Sin embargo, ninguna de estas opciones es comercialmente viable debido a su ineficacia y poca practicidad (Cervero et al., 2008).
En la actualidad se están modificando químicamente los aceites y grasas y se está creando un combustible con características más apropiadas para los motores diésel (Cervero et al., 2008). Esta modificación se lleva a cabo por un proceso llamado transesterificación (Fuduka et al., 2001; Meher et al., 2006), donde se obtiene un biocombustible más limpio y ambientalmente seguro (Meher et al., 2006). La estequiometría de la reacción muestra que tres moléculas de alcohol reaccionan con una molécula de triglicérido, produciendo tres moléculas de alquilesteres (biodiésel) y una molécula de glicerina, pero debido a que la reacción es reversible, en la práctica se agrega un exceso de alcohol para desplazar la reacción hacia la formación de esteres. Este mismo resultado se obtendría aumentando la temperatura (la reacción es endotérmica) o realizando la extracción simultánea de coproductos durante la reacción. La transesterificación se puede catalizar de forma química o biológica. En la catálisis química se utilizan ácidos (H2SO4 o HCl) (Fukuda et al., 2001; Du et al., 2008) o bases (hidróxidos, carbonatos o alkóxidos) (Schuchardt et al., 1998; Fukuda et al., 2001); mientras que en la catálisis biológica o biocatálisis se utilizan lipasas de diversos microorganismos como Rhizomucor miehei y Rhizopus orizae (Shimada et al., 2002; Du et al., 2008; Demirbas, 2009; Rojas et al., 2010).
2. Variables que afectan el proceso de transesterificación
A continuación se presentan los efectos, reportados en la literatura, de la relación molar-alcohol: grasa, tipo de alcohol, tiempo de reacción, tipo de catalizador, cantidad de catalizador, temperatura de reacción, intensidad de mezclado y contenido de ácidos grasos libres y agua, en el rendimiento de la reacción de transesterificación de grasas animales, a través de catálisis química (homogénea y heterogénea) y biocatálisis.
2.1 Relación molar alcohol:grasa
Por estequiometría de la reacción se requiere una relación molar alcohol:grasa de 3:1 para convertir los triglicéridos a alquilesteres. Sin embargo, como la reacción es reversible, se agrega un exceso de alcohol para favorecer la formación de esteres. Esto fue reportado por (Chung et al., 2009), al transesterificar sebo de pato y obtener rendimientos de 75% y 97% a una relación de 3:1 y 6:1, respectivamente. En la alcohólisis homogénea de grasa de pollo, manteca de cerdo, aceite de pescado y sebo de res, los rendimientos son mayores al 90% a una relación de 6:1 (Armenta et al., 2007; Issariyakul et al., 2007).
Se ha encontrado que una gran cantidad de alcohol disminuye el rendimiento, debido a que actúa como emulsificador del catalizador, haciendo lenta la reacción (Leung y Gou 2006). Tashtoush et al. (2004), al transesterificar grasa animal a relaciones de 6:1, 7,5:1 y 9:1, obtuvo rendimientos del 80%, 73% y 68%, respectivamente. Sin embargo, en catálisis básica heterogénea de sebo y grasa de pollo, se obtuvieron rendimientos mayores al 92% a relaciones de 16,5:1,75 y 60:1, respectivamente (Suppes et al., 2001; Liuet al., 2007). Este aumento de alcohol se debe a que la catálisis heterogénea está limitada por la transferencia de masa entre la fase líquida y la superficie del catalizador, y es necesaria una alta relación alcohol:grasa para aumentar la difusión de los reactantes (Benja-pornkulaphong et al., 2009; Ma et al., 2008).
En biocatálisis se emplean relaciones menores a 4:1 (Watanabe et al., 1999; Hsu et al., 2001; Lu et al., 2007), porque el alcohol insoluble en el aceite puede inactivar las enzimas. Watanabe et al. (1999) utilizaron una relación molar de 4:1 en la etanólisis de aceite de atún, y encontró que la lipasa C. antarctica se inactiva en presencia de 2/3 del alcohol requerido por estequiometría. Por lo tanto, este se agregó en: (a) dos etapas, que alcanzó un rendimiento del 90% en 40 h; y (b) tres etapas, donde a las mismas condiciones de operación, el mismo rendimiento se alcanzó en 60 h. Hsu et al. (2001), en la etanólisis de sebo y grasa con P cepacia en una sola etapa (4:1, 50 °C y 18 h), obtuvieron rendimientos de 91% y 88%, respectivamente.
2.2 Tipo de alcohol
Los alcoholes empleados con mayor frecuencia en la alcohólisis de grasas animales son el metanol y el etanol, aunque se han utilizado otros alcoholes, como dietilenglicol, n-propanol, n-butanol, isobutanol e isopropanol (Hsu et al., 2001). De ellos, el metanol es el más utilizado, por ser económico y permitir obtener mayores rendimientos, debido a la gran reactividad de los metóxidos (Issariyakul et al., 2007). Sin embargo, la solubilidad del metanol en grasas es baja, por lo que la reacción está limitada por la transferencia de masa entre los reactantes. Ma et al. (1998a) encontraron que a 100 °C la solubilidad del metanol en sebo de res fue del 19% (p/p), mientras que con etanol fue del 100 % (p/p), a 68 °C.
A pesar de la alta solubilidad del etanol, este alcohol forma una emulsión después de la reacción, que hace difícil la separación de los productos. Se ha encontrado (Issariyakul et al., 2007; Tashtoush et al., 2004) que los etilesteres de grasas animales presentan mejores características en cuanto al punto de nube, punto de fluidez y menor viscosidad que los metilesteres, pues mejoran las propiedades en frío del biodiésel y su desempeño en el motor. En la catálisis enzimática de grasas animales, Hsu et al. (2001) reportaron que en la alcohólisis de sebo con P. cepacia inmovilizada se obtienen mayores rendimientos (82%-94%) con alcoholes primarios que con alcoholes secundarios (32%-68%).
2.3 Tiempo de reacción
Este parámetro se relaciona principalmente con dos variables del proceso de transesterificación: el tipo de catálisis y el tipo de catalizador utilizado. Alcántara et al. (2000), en la metanólisis de sebo con 1% (p/p) de H2SO4 y NaOCH3, encontraron que en la catálisis ácida, el rendimiento fue del 13% en 48 h y en la catálisis básica fue del 92% en 3 h. Además, el rendimiento es proporcional al tiempo de reacción (Armenta et al., 2007; Balat y Balat, 2008).
Bhatti et al. (2008) estudiaron el efecto del tiempo de reacción en el rendimiento en la metanólisis de grasas de pollo y de carnero con H2SO4, entre 0,75 y 24 h, y encontró que el mayor rendimiento se obtuvo a las 24 h. Sin embargo, después de las primeras 13 h la velocidad de reacción fue más lenta. Watanabe et al. (1999), en la etanólisis de aceite de atún con C. antarctica (rel. molar 3:1, 40 °C y 10% p/p de enzima) evaluaron el rendimiento a 5 y 24 h, que alcanzaron valores de 29% y 35%, respectivamente. En la catálisis biológica, el largo tiempo de reacción es la principal desventaja que limita su aplicación en la industria. Esto se ha evidenciado en la alcohólisis enzimática de aceite de atún, sebo, grasa y manteca de cerdo, donde se han obtenido rendimientos de 35% en 24 h, 93% en 18 h, 94% en 18 h y 87,4% en 10 h, respectivamente (Hsu et al., 2001; Lu et al., 2007).
2.4 Tipo de catalizador
En la transesterificación de grasas animales se han utilizado catalizadores alcalinos como NaOH, KOH, KOCH3, NaOCH3 y NaOC2H5; catalizadores ácidos como H2SO4 y HCl, y catalizadores enzimáticos como C. antarctica y P. cepacia. Los catalizadores básicos y ácidos, al igual que el alcohol, deben ser anhidros (humedad < 0,06%), para evitar la formación de jabón. Al comparar el tiempo de reacción, para una misma cantidad de catalizador, la catálisis alcalina es aproximadamente 4.000 veces más rápida que la catálisis ácida (Fuduka et al., 2001). Esto se confirmó al realizar la metanólisis de sebo con H2SO4 y NaOH, a iguales condiciones de reacción (relación molar 7,5:1, 1% p/p de catalizador, 60 °C y 3 h). Así, se encontró que en la catálisis ácida el rendimiento fue menor del 10%, y en la catálisis básica fue mayor al 95% (Alcántara, 2000). Sin embargo, la catálisis básica es sensible al contenido de agua y a los ácidos grasos libres (AGL) (Sharma et al., 2008). Cuando la acidez de la materia prima es alta (AGL >3% p/p) la catálisis básica es ineficiente debido a que el catalizador reacciona con los AGL para formar jabón.
Tashtoush et al. (2004) alcanzaron un rendimiento del 78% por catálisis ácida (H2SO4) de grasa animal con un contenido de AGL entre 10% y 15% (rel. molar 6:1, 50 °C y 2 h). Issariyakul et al. (2007) y El-Mashad et al. (2008) realizaron experimentos de alcohólisis en dos etapas: una ácida y otra básica.
En la etapa ácida se reduce el contenido de AGL y con la etapa básica se realiza la alcohólisis propiamente dicha. El-Mashad et al. (2008) realizaron la metanólisis de aceite de salmón en dos etapas. Durante la etapa ácida (1% p/p H2SO4), el aceite de salmón disminuyó su acidez de 3,47 a 2,6 mg de KOH/g de aceite. Posteriormente, se realizó la catálisis básica (0,8% p/p de KOH) y alcanzó un rendimiento del 97,6%.
En la catálisis enzimática de aceite de atún (Watanabe et al., 1999), grasa (Hsu et al., 2001) y manteca de cerdo (Lu et al., 2007) se han alcanzado rendimientos del 35%, 94% y 87%, respectivamente. Sin embargo, este tipo de catálisis requiere tiempos largos (18-24 h) para obtener altos rendimientos. Este tipo de catálisis se caracteriza por su baja temperatura de reacción (< 50 °C) y la no formación de jabón.
2.5 Cantidad de catalizador
Con una baja cantidad de catalizador (< 0,1% p/p) (Kim, 2004) o una cantidad excesiva de este (> 50% p/p) (Canacki et al., 2003; Bhatti et al., 2008) es imposible alcanzar máximos rendimientos. Esto fue observado por (Bhatti et al., 2008) en la metanólisis de grasa de pollo a concentraciones de H2SO4 entre 25% y 50% (p/p), donde encontró que el rendimiento es proporcional al incremento en la cantidad de catalizador. Sin embargo, encontró que al utilizar 100% (p/p) de H2SO4, el rendimiento disminuye cerca al 11%. Otros autores (Ma et al., 2008; Wyattet al., 2005) han reportado que los mayores rendimientos se obtuvieron cuando se utilizó una baja concentración de catalizador (0,4% de NaOH).
En la metanólisis de grasa de pollo, sebo y manteca de cerdo se obtuvieron rendimientos del 99,4%, 98,8% y 97,8%, respectivamente, utilizando el 0,4% de NaOH (relación molar 6:1, 60 °C y 30 min) (Wyatt et al., 2005). Cuando se utilizan ácidos, la cantidad de catalizador es mayor que al emplear bases. Así lo confirma (Bhatti et al., 2008) en la metanólisis de sebo de carnero con el 25% (p/p) de KOH y el 50% (p/p) de H2SO4 (relación 30:1, 24 h), quienes encontraron rendimientos del 93,21% y del 90%. En la alcohólisis enzimática de aceite de atún (Watanabe et al., 1999), sebo (Hsu et al., 2001) y manteca de res (Lu et al., 2007), el rendimiento aumentó con la cantidad de enzima agregada. Sin embargo, este incremento fue bajo, lo cual indica que la velocidad de reacción disminuye.
2.6 Temperatura de reacción
El aumento de la temperatura incrementa el rendimiento y la miscibilidad entre los reactantes. Sin embargo, la temperatura no debe ser superior a la temperatura de ebullición del alcohol (que depende de la presión el sistema) para evitar su pérdida y la consecuente disminución del rendimiento. Jeonget al. (2009) en la metanólisis de manteca de cerdo (relación molar 7,5:1, 0,2% KOH, 18 min) evaluaron el rendimiento a 30 y 70 °C, y encontraron rendimientos mayores 55% y 85%, respectivamente. Bhatti et al. (2008) en la metanólisis de grasa de pollo y sebo de carnero (relación molar 30:1 y 50% (p/p) de H2SO4) tuvieron rendimientos para la grasa de pollo del 95%, 94% y 84% a 60, 50 y 40 °C, y para el sebo de carnero del 90%, 75% y 40% a 60, 50 y 40 °C, respectivamente. En la catálisis heterogénea de grasas animales se utilizan temperaturas mayores (95-210 °C) que en la catálisis homogénea (20-80 °C).
En catálisis química heterogénea la temperatura no debe ser superior a los 250 °C, debido a la descomposición de algunos AGL (Muniyappa et al., 1996). Liuet al. (2007), en la metanólisis de grasa de pollo (rel. 30:1, 8 h) con hidrotalcita de Mg-Al (10% p/p), encontraron que a 60 °C la conversión fue del 20%, y a 120 °C fue del 93%. En biocatálisis la temperatura no debe ser mayor a 50 °C, porque se desnaturaliza la enzima y pierde su actividad catalítica. Con P. cepacia se pueden emplear temperaturas hasta de 50 °C, debido a que es más resistente que otras enzimas (Hsu et al., 2001). En la metanólisis de manteca de cerdo con Candida sp., los rendimiento fueron del 87,4% a 40 °C (rel. 3:1, 20% p/p de enzima, 10 h) (Lu et al., 2007).
2.7 Intensidad de mezclado
Debido a que la grasa es inmiscible con la solución alcohol-catalizador, es necesario agitar la mezcla durante la reacción. Ma et al. (1998b) estudió este parámetro sobre el rendimiento de la metanólisis homogénea de sebo de res y halló que no se observó formación de biodiésel en ausencia de agitación. También reportó rendimientos mayores al 92% utilizando una velocidad de agitación de 330 rpm. En la catálisis homogénea y enzimática de grasas animales, la intensidad de agitación se realiza entre 130 y 600 rpm, y en la catálisis heterogénea de sebo, la intensidad de mezcla es mayor (1.417 rpm) (Liu et al., 2007). En la etanólisis de aceite de pescado (Armenta et al., 2007), se evaluó el efecto de utilizar ultrasonido para mezclar los componentes de la reacción, y se encontró que se requieren tiempos más cortos de reacción (10 min) para alcanzar altos rendimientos (95%), que al utilizar el método convencional de agitación.
2.8 Contenido de ácidos grasos libres (AGL) y agua
El contenido de AGL y agua en el medio de reacción, determina el pretratamiento requerido por los reactivos para hacer viable la reacción de transesterificación.
El alto contenido de AGL y humedad forma jabón, reduce la efectividad del catalizador y dificulta la separación y purificación de los productos (Sharma et al., 2008; Meheret al., 2006). Los AGL se reducen pretratando la grasa animal con ácido (esterificación), mientras que el contenido de humedad se reduce utilizando alcohol y catalizador en estado anhídro y calentando el aceite para evaporar el agua.
Ma et al. (1998b) investigaron estos parámetros en la metanólisis de sebo de res con NaOH, y estableció que para obtener altos rendimiento, el contenido de agua y de AGL deben ser inferiores a 0,06% y 0,5%, respectivamente. Cuando se utilizan grasas animales con altos contenidos de AGL, como las grasas amarillas (AGL < 15%), se requiere un pretratamiento con alcohol y H2SO4 para disminuir su grado de acidez y alcanzar mayores rendimientos. Issariyakul et al. (2007) pretrataron grasas de fritura (acidez de 11 mg KOH /g grasa) con 2% p/p de H2SO4 y una relación 3:1, en presencia de metanol a 50 °C y etanol a 60 °C y obtuvo una acidez de 0,5 y 0,8 mg KOH/g grasa, respectivamente.
En la alcohólisis de las grasas sin pretratar se alcanzaron rendimientos cercanos al 50% (1% KOH, rel. 6:1, 25 °C y 30 min); mientras que en la metanólisis y etanólisis de grasas de fritura pretratadas los rendimientos fueron 96% y 97%, respectivamente. En biocatálisis no se requiere un control estricto del contenido de AGL y agua en el medio de reacción, ya que las enzimas tienen una alta especificidad y actúan en la interfase agua-grasa. Se ha encontrado que en la metanólisis de manteca de cerdo con Candida sp. (20% p/p) se alcanzó un rendimiento del 87,4% a 40 °C, al adicionar un 20% p/p de agua (Lu et al., 2007).
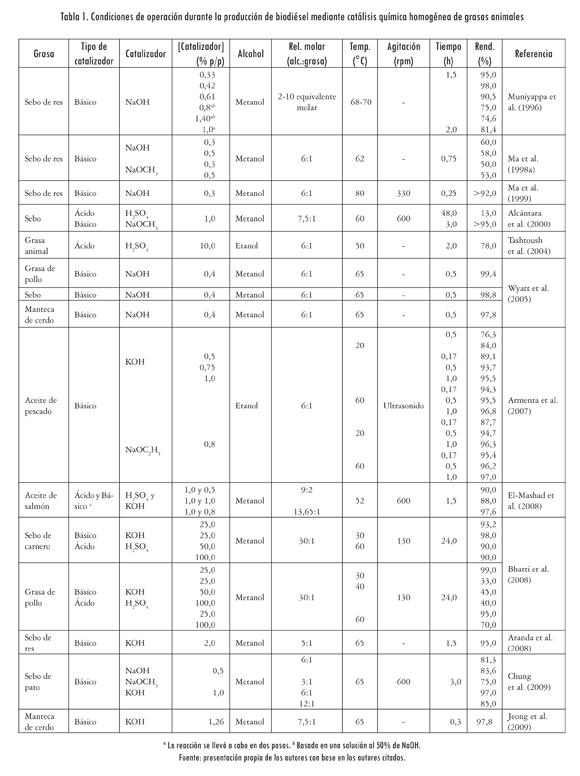
En las tablas 1, 2 y 3 se resumen las condiciones de operación del proceso de síntesis de biodiésel a partir de grasas animales mediante catálisis homogénea, heterogénea química y enzimática, respectivamente, encontradas en la literatura. En ellas se observa que el sebo de res es la grasa animal más utilizada, seguida de la grasa de pollo y la manteca de cerdo. También se indica que el alcohol más utilizado es el metanol, y el tipo de catálisis más empleada es la catálisis homogénea con catalizadores básicos, debido a su efectividad en la obtención de alquilesteres. En la Tabla 1 se observa que el mayor rendimiento (99,4%) se alcanzó en la metanólisis de grasa de pollo utilizando NaOH (0,4% p/p, rel. 6:1, 60 °C y 30 min). Es de notar que en la catálisis homogénea de grasas animales se utiliza generalmente una relación 6:1, una temperatura entre 50 y 80 °C, una cantidad de catalizador entre 0,3% y 0,5% p/p y un tiempo de reacción entre 15 min y 24 h; condiciones de reacción a las cuales se han obtenido los mayores rendimientos.
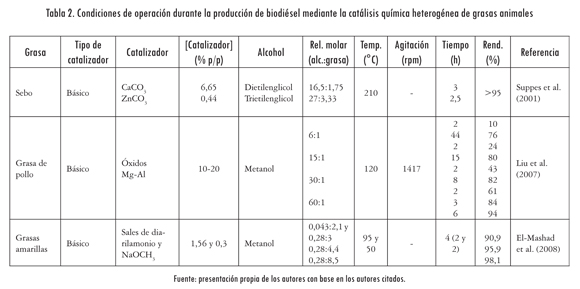
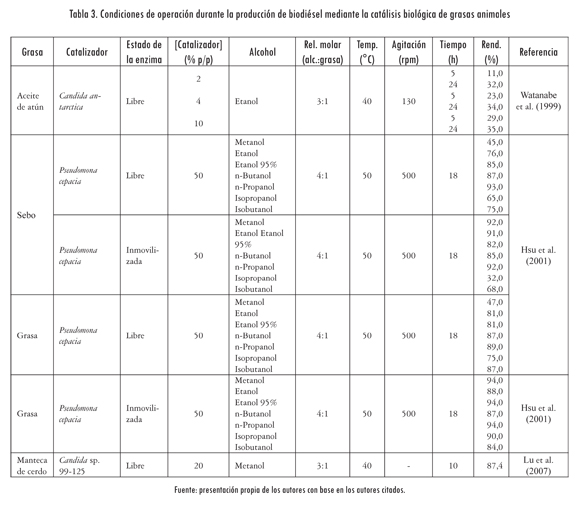
En las tablas 2 y 3 se observa que los estudios realizados en transesterificación heterogénea de grasas animales son pocas, debido principalmente al mayor tiempo de reacción causado por la viscosidad del medio reactante al agregar el catalizador. También se muestra que en la catálisis química y biológica se han alcanzado rendimientos mayores al 98%. En la biocatálisis, la temperatura y la relación alcohol: grasa son menores (rel. 3-4:1 y 40-50 °C) en comparación con las utilizadas en la catálisis química heterogénea (rel. 6-60:1 y 50 a 210 °C), lo cual repercute en el costo del proceso. Sin embargo, se observa que en la catálisis química heterogénea se alcanzan rendimientos superiores al 95% con tiempos de reacción de 3 h, y en la biocatálisis es necesario un tiempo mínimo de reacción de 18 h para obtener rendimientos del 90%.
3. Conclusiones
La alcohólisis de aceites y grasas animales se ha estudiado, principalmente, en laboratorios por catálisis básica homogénea, y se ha encontrado un solo estudio a escala de planta piloto de sebo de res. Esto indica la necesidad de hacer un mayor desarrollo en esta tecnología para el aprovechamiento de los residuos grasos de origen animal, ya que proporciona un bajo costo en materia prima y no se compite por producción de alimentos.
La relación molar alcohol:grasa que se utiliza en la transesterificación de grasas animales, depende de la grasa que se utilice y del tipo de catálisis que se lleve a cabo. Particularmente, en la catálisis enzimática la relación molar de alcohol: grasa óptima está determinada por las características y la resistencia de cada lipasa hacia el alcohol utilizado.
Aunque el metanol es el alcohol más utilizado en la transesterificación de grasas animales, se recomienda utilizar etanol, debido a que proviene de fuentes renovables y se obtienen esteres con mejores propiedades en frío (punto de nube y punto de fluidez). Esto es aplicable tanto a catálisis química como a catálisis biológica.
Se encontró que para sebo de res el rendimiento está entre 50% y 95% (tiempo de reacción entre 0,75 y 3 h); grasa de pollo, entre 33% y 99% (0,51,5 h); aceite de pescado, entre 76% y 98% (0,17-1,5 h); sebo de pato, entre 75% y 97% (3 h); sebo de carnero, entre 90% y 98% (24 h), y para el sebo de cerdo del 97% (0,3 h).
Debido al amplio rango del contenido de agua y ácidos grasos libres presentes en los aceites y grasas animales, es necesario desarrollar un proceso diferente para cada fuente. Sin embargo, el proceso de transesterificación para aceites y grasas animales se puede estandarizar a un proceso de combinado ácido/base para neutralizar los AGL, con una previa evaporación a baja presión del agua.
Referencias
ALCÁNTARA, R. ; AMORES, J. ; CANOIRA, L. ; FIDALGO, E. ; FRANCO, M. J. y NAVARRO, A. Catalytic production of biodiesel from soy-bean oil, used frying oil and tallow. Biomass and Bioenergy. 2000, núm. 18, pp. 515-527. [ Links ]
AMEER, S. D.; RAJA, K. y JEBARAJ, S. A review on biodiesel production, combustion, emissions and performance. Renewable & Sustainable Energy Reviews. 2009, núm. 13, pp. 1628-1634. [ Links ]
ARANDA, A. S.; CANIELAS, L.; ESPINOSA, M.; SHIMITT, F. C.; WEBER, E.; CATALUÑA, V R.; ALVES, M. R. y BASTOS, C. E. Tallow biodiesel: properties evaluation and consumption tests in a diesel engine. Energy & Fuels. 2008, núm. 22, pp. 1949-1954. [ Links ]
ARMENTA, R. E.; VINATORU, M.; BURJA, A. M.; KRALOVEC, J. A. y BARROW, C. J. Transesterification of fish oil to produce fatty acid ethyl esters using ultrasonic energy. JAOCS. 2007, núm. 84, pp. 1045-1052. [ Links ]
BALAT, M. y BALAT, H. A critical review of biodiesel as a vehicular fuel. Energy Conversion and Management. 2008, núm. 49, pp. 2727-2741. [ Links ]
BENAVIDES, A.; BENJUMEA, P. y PASHOVA, V. El biodiesel de aceite de higuerilla como combustible alternativo para motores diesel. DYNA. 2007, núm. 74, pp. 141-150. [ Links ]
BENJAPORNKULAPHONG, S.; NGAMCHARUSSRIVICHAI, C. y BUNYAKIAT, K. Al2O3-supported alkali and alkali earth metal oxides for transesterification of palm kernel oil and coconut oil. Chemical Engineering Journal. 2009, núm. 145, pp. 468-474. [ Links ]
BHATTI, H. N.; HANIF, M. A.; QASIM, M. y REHMAN A. Biodiesel production from waste tallow. Fuel. 2008, núm. 87, pp. 2961-2966. [ Links ]
BIELECKI, J. Energy security, pp. is the wolf at the door? The Quarterly Review of Economics and Finance. 2002, núm. 42, pp. 235-250. [ Links ]
BO, X.; GUOMIN, X.; LINGFENG, C.; RUIPING, W y LIJING, G. Transesterification of palm oil with methanol to biodiesel over a KF/Al2O3 heterogeneous base catalyst. Energy & Fuels. 2007, núm. 21, pp. 3109-3112. [ Links ]
CANAKCI, M. The potencial of restaurant waste lipids as biodiesel feedstocks. Bioresource Technology. 2007, núm. 98, pp. 183-190. [ Links ]
CANAKCI, M. y VAN GERPEN, J. A pilot plant to produce biodiesel from high free fatty acid feedstocks. American Society of Agric. Eng. 2003, núm. 46, pp. 945-954. [ Links ]
CERVERÓ, J. M.; COCA, J. y LUQUE, S. Production of biodiesel from vegetable oils. Grasas y Aceites. 2008, núm. 59, pp. 76-83. [ Links ]
CHENG, C. H.; CHEUNG, C. S.; CHAN, T. L.; LEE, S. C.; YAO, C. D. y TSANG, K. S. Comparison of emissions of a direct injection diesel engine operating on biodiesel with emulsified and fumigated methanol. Fuel. 2008, núm. 87, pp. 1870-1879. [ Links ]
CHUNG, K. H.; KIM, J. y LEE, K-Y Biodiesel production by transesterification of duck tallow with methanol on alkali catalysts. Biomass and Bioenergy. 2009, núm. 33, pp. 155-158. [ Links ]
DEMIRBAS, A. Progress and recent trends in biodiesel fuels. Energy Conversion and Management. 2009, núm. 50, pp. 14-34. [ Links ]
DIAS, J. M.; ALVIM-FERRAZ, C. M. y ALMEIDA, M. F. Production of biodiesel from acid waste lard. Bioresource Technology. 2009, núm. 100, pp. 6355-6361. [ Links ]
DU, W; LI, W; SUN, T.; CHEN, X. y LIU, D. Perspectives for biotechnological production of biodiesel and impacts. Apply Microbiology Biotechnology. 2008, núm. 79, pp. 331-337. [ Links ]
EL-MASHAD, H. M.; ZHANG, R. y AVENA-BUSTILLOS, R. J. A two-step process for biodiesel production from salmon oil. Biosystems Engineering. 2008, núm. 99, pp. 220-227. [ Links ]
ESPINOSA, M.; KRAUSE, L. C.; ARANDA, M. S.; SCHMITT, C.; ASSIS, R.; RODRIGUES, S.; ALVES, M. R. y BASTOS, E. Beef tallow biodiesel produced in a pilot scale. Fuel Processing Technology. 2009, núm. 90, pp. 570-575. [ Links ]
FUKUDA, H.; KONDO, A. y NODA, H. Biodiesel fuel production by transesterification of oils. Journal of Bioscience and Bioengineering. 2001, núm. 92, pp. 405-416. [ Links ]
HSU, A-F.; JONES, K.; MARMER, W N. y FOGLIA, T. A. Production of alkyl esters from tallow and grease using lipase immobilized in a phyllosilicate sol-gel. JAOCS. 2001, núm. 78, pp. 585-588. [ Links ]
ISSARIYAKUL, T.; KULKARNI, M. G.; DALAI, A. K. y BAKHSHI, A. N. Production of biodiesel from waste fryer grease using mixed methanol/ethanol system. Fuel Processing Technology. 2007, núm. 88, pp. 429-436. [ Links ]
JEONG, G.-T.; YANG, H.-S. y PARK, D.-H. Optimization of transesterification of animal fat ester using response surface methodology. Bioresource Technology. 2009, núm. 100, pp. 421-427. [ Links ]
KIM, H.-J.; KANG, B.-S.; KIM, M.-J.; PARK, Y. M.; KIM, D. K.; LEE, S.-J. y LEE, K.-Y. Transesterification of vegetable oil to biodiesel using heterogeneous base catalyst. Catalysis Today. 2004, núm. 93, pp. 315-320. [ Links ]
LECLERCQ, E.; FINIELS, A. y MOREAU, C. Transesterification of rapeseed oil in the presence of basic zeolites and related solid catalysts.JAOCS. 2001, núm. 8, pp. 1161-1165. [ Links ]
LEUNG, D. Y. C. y GUO, Y. Transesterification of neat and used frying oil, pp. optimization for biodiesel production. Fuel Processing Technology. 2006, núm. 87, pp. 883-890. [ Links ]
LIU, X.; PIAO, X.; WANG, Y; ZHU, S. y HE, H. Calcium methoxide as a solid catalyst for the transesterification soybean oil to biodiesel with methanol. Fuel. 2008, núm. 87, pp. 1076-1082. [ Links ]
LIU, Y; LOTERO, E.; GOODWIN, J.G. Transesterification of poultry fat with methanol using Mg-Al hydrotalcite derived catalyst. Apply Catalysis A. General. 2007, 331, pp. 138-148. [ Links ]
LU, J.; NIE, K.; XIE, F. y WANG, F. Enzymatic synthesis of fatty acid methyl esters from lard with immobilized Candida sp. 99-125. Process Biochemistry. 2007, núm. 42, pp. 1367-1370. [ Links ]
MA, F.; CLEMENTS, L. D. y HANNA, M. A. Biodiesel fuel from animal fat. Ancillary studies on transesterification of beef tallow. Industrial & Engineering Chemistry Research. 1998a, núm. 37, pp. 3768-3771. [ Links ]
MA, F.; CLEMENTS, L. D. y HANNA, M. A. The effects of catalyst, free fatty acids, and water on transesterification of beef tallow. Transactions of the ASAE. 1998b, núm. 41, pp. 1261-1264. [ Links ]
MA, F.; CLEMENTS, L. D. y HANNA, M. A. The effect of mixing on transesterification of beef tallow. Bioresource Technology. 1999, núm. 69, pp. 289-293. [ Links ]
MA, H.; LI, S.; WANG, B.; WANG, R. y TIAN, S. Transesterification of rapeseed oil for synthesizing biodiesel by K/KOH/y-Al2O3 as heterogeneous base catalyst. JAOCS. 2008, núm. 85, pp. 263-270. [ Links ]
MEHER, L. C.; SAGAR, D. V. y NAIK. S. N. Technical aspects of biodiesel production by transesterification - a review. Renewable & Sustainable Energy. 2006, núm. 10, pp. 248-268. [ Links ]
MITTELBACH, M. Lipase catalyzed alcoholysis of sunflower oil. JAOCS. 1990, núm. 67, pp. 168-170. [ Links ]
MUNIYAPPA, P R.; BRAMMER, S. C. y; NOUREDDINI, H. Improved conversion of plant oils and animal fats into biodiesel and co-product. Bioresource Technology. 1996, núm. 56, pp. 19-24. [ Links ]
NGO, H. L.; ZAFIROPOULOS, N. A.; FOGLIA, T. A.; SAMULSKI, E. T. y LIN, W Efficient two-step systhesis of biodiesel from greases. Energy & Fuels. 2008, núm. 22, pp. 626-634. [ Links ]
NITSKE, W R. y WILSON, C. M. Rudolf Diesel:pioneer of the age of power. Oklahoma: University of Oklahoma Press, 1965. [ Links ]
PERIN, G. ; ÁLVARO, G. ; WESTPHAL, E. ; VIANA, L. H. y LENARDAO, E. J. Transesterification of castor oil assited by microwave irradiation. Fuel. 2008, núm. 87, pp. 2838-2841. [ Links ]
ROJAS, A. F.; GIRÓN, E. y TORRES, H. G. Variables de operación en el proceso de transesterificación de aceites vegetales: una revisión-catálisis enzimática. Ingeniería e Investigación. 2010, vol. 30, núm. 1, pp. 17-21. [ Links ]
SCHUCHARDT, U.; SERCHELI, R. y VARGAS, R. M. Transesterification of vegetable oils: a review. Journal Brazilian Chememical Society. 1998, núm. 9, pp. 199-210. [ Links ]
SHARMA, Y. C. y SINGH, B. Development of biodiesel: current scenario. Renewable and Sustainable Energy Reviews. 2009, núm. 13, pp. 1646-1651. [ Links ]
SHARMA, Y. C.; SINGH, B. y UPADHYAY, S. N. Advancements in development and characterization of biodiesel: a review. Fuel. 2008, núm. 87, pp. 2355-2373. [ Links ]
SHIMADA, Y; WATANABE, Y; SUGIHARA, A. y TOMINAGA, A. Enzymatic alcoholysis for biodiesel fuel production and application of the reaction to oil processing: Review. Journal of Molecular Catalysis B: Enzymatic. 2002, núm. 17, pp. 133-142. [ Links ]
SUPPES, G. J.; BOCKWINKEL, K.; LUCAS, S.; BOTTS, J. B. y MASON, M.H. Calcium carbonate catalyzed alcoholysis of fats and oils. JAOCS. 2001, vol. 78, núm. 2, pp. 139-146. [ Links ]
TAMALAMPUDI, S.; TALUKDER, R. M.; HAMA, S.; NUMATA, T.; KONDO, A. y FUKU-DA, H. Enzymatic production of biodiesel from jatropha oil: A comparative study of immobilized-whole cell and commercial lipases as a biocatalyst. Biochemical Engineering Journal. 2008, núm. 39, pp. 185-189. [ Links ]
TAN, R.; CULABA, A. B. y PURVIS, M. R. Carbon balance implications of coconut biodiesel utilization in the Philippine automotive transport sector. Biomass & Bioenergy. 2004, núm. 26, pp. 579-585. [ Links ]
TASHTOUSH, G. M.; AL-WIDYAN, M. I. y AL-JARRAH, M. M. Experimental study on evaluation and optimization of conversion of waste animal fat into biodiesel. Energy Conversion and Management. 2004, núm. 45, pp. 2697-2711. [ Links ]
WATANABE, Y; SHIMADA, Y; SUGIHARA, A. y TOMINAGA, Y Stepwise ethanolysis of tuna oil using immobilized. Journal of Bioscience and Bioenergy. 1999, núm. 88, pp. 622-626. [ Links ]
WYATT, V T.; HESS, M. A.; DUNN, R. O.; FOGLIA, T. A.; HAAS, M. J. y MARMER, W N. Fuel properties and nitrogen oxide emission levels of biodiesel produced from animal fat.JAOCS. 2005, vol. 82, núm. 8, pp. 585-591. [ Links ]