Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Boletín Científico. Centro de Museos. Museo de Historia Natural
Print version ISSN 0123-3068
Bol. Cient. Mus. Hist. Nat. Univ. Caldas vol.18 no.1 Manizales Jan./June 2014
CURADURÍA, MORFOLOGÍA E IDENTIFICACIÓN DE ÁFIDOS (HEMIPTERA: APHIDIDAE) DEL MUSEO ENTOMOLÓGICO UNAB. PRIMERA APROXIMACIÓN.*
CURATORSHIP, MORPHOLOGY AND IDENTIFICATION OF APHIDS (HEMIPTERA: APHIDIDAE) DEPOSITED IN THE UNAB ENTOMOLOGICAL MUSEUM . FIRST APPROXIMATION
Ronald Simbaqueba C.1, 2 , 3, Francisco Serna 2, 3 Francisco Javier Posada-Flórez 2, 4
* FR: 16-X-2013. FA: 21-III-2014.
1 Ingeniería Agronómica. Facultad de Ciencias Agrarias. Universidad Nacional de Colombia, Bogotá, Colombia, Cra. 30, #45-03). rrsimbaquebac@unal.edu.co
2 Grupo Sistemática de Insectos Agronomía (SIA). Línea Taxonomía de insectos.
3 Universidad Nacional de Colombia. Facultad de Ciencias Agrarias. Museo Entomológico Universidad Nacional Agronomía Bogotá (UNAB). Cra. 30 # 45-03. Bogotá, Colombia. fjsernac@unal.edu.co
4 Ingeniero Agrónomo. Entomólogo PhD y Postdoctorado. IPM – Tropical Perennial Crop Consultant. 7620 E. Arbory Ct. Laurel, MD. 20707. fjavierposada@hotmail.com
CÓMO CITAR: SIMBAQUEBA C., R., SERNA, F. & POSADA-FLÓREZ, F.J., 2014.- Curaduría, morfología e identificación de áfidos (Hemiptera: Aphididae) del Museo Entomológico UNAB. Primera aproximación. Bol. Cient. Mus. Hist. Nat. U. de Caldas, 18 (1): 222-246.
Resumen
Los áfidos son insectos polífagos succívoros y se alimentan de una importante cantidad de cultivos. Los daños son de importancia económica y pueden ser letales para las plantas, ya que los áfidos están adaptados para transmitir diferentes virus cuando chupan la savia. Viven también en asociación simbiótica con hormigas. Estas, a su vez, los protegen de enemigos naturales y los transportan de un lugar a otro, al mismo tiempo que toman de ellos el excremento azucarado, conocido como rocío de miel. En el presente trabajo se elaboró una colección de referencia de áfidos, que se encuentra almacenada en el Museo entomológico UNAB (Universidad Nacional Agronomía Bogotá), siguiendo un protocolo modificado para el proceso curatorial. Las muestras fueron recolectadas y procesadas a través de diferentes soluciones químicas para la limpieza, aclarado y montaje en portaobjetos de microscopio, en los cuales se incluyeron los datos de colección de las muestras. Este estudio también buscó encontrar caracteres útiles nuevos o previamente registrados para su uso en la morfología descriptiva de Aphididae, y para las claves de identificación. Las ilustraciones y medidas se elaboraron con la ayuda de un microscopio óptico (400 aumentos) y una rejilla. Las fotografías fueron tomadas con una cámara sencilla adaptada a un microscopio, y organizadas en Photoshop. Los áfidos son piriformes, pequeños (4-8 mm), cuerpo blando hemipteroide, con un par de sifúnculos dorsales en el segmento abdominal cinco o seis. La placa genital es el esternito del segmento VII, y la cauda corresponde al terguito del segmento IX. Cabeza opistognatha, con tubérculos frontales o antenales. Esta primera aproximación al proceso curatorial de áfidos de la Colección Taxonómica Central del museo UNAB reúne 18 especies de áfidos, representadas por 579 ejemplares de 18 municipios y un total de 34 plantas hospedantes. Para estas especies, se elaboraron claves taxonómicas, diagnosis e ilustraciones.
Palabras clave: áfidos, curaduría, morfología, taxonomía, claves de identificación, diagnosis.
Abstract
Aphids are succivorous, polyphagous insects that attack an important number of crops. Damages are of economic importance and may be lethal to plants since aphids are adapted to transmit different viruses, while sucking sap juices. Aphids live in symbiotic association with ants. Ants protect and move them from one place to another, and receive honeydew as reward. We developed a voucher collection of aphids housed at the UNAB Museum, following a modified protocol for the curatorial process. Specimens were collected and processed through different chemicals for cleaning, clearing and mounting on microscopic slides, where the collecting data were included in a label. We also pursued to find useful characters both old and new ones for a descriptive morphology of Aphididae, and for the identification keys. Illustrations and measurements were made using an optic microscope (400X), with a grid. Pictures were taken with a simple camera adapted to a microscope, and organized on Photoshop. Aphids are diagnosable as pyriform, small (4-8 mm) soft bodied hemipterans, with a pair of dorsal cornicles or siphuncles on abdominal segment fifth or sixth. Genital plate is the sternite of segment VII, and the cauda corresponds to the tergite of segment IX. Head opisthognathous, with frontal or antennal tubercles. Our first approximation to the curatorial process of the aphids at the Central Taxonomic Collection of the UNAB Museum assembles 18 species, represented by 579 specimens from 18 municipalities and a total of 34 host plants. For these species, we produced identification keys, taxonomic diagnosis, and illustrations.
Key words: aphids, curatorial process, morphology, taxonomy, identification keys, diagnosis.
Los áfidos o "pulgones" causan grandes pérdidas a la agricultura como consecuencia de sus hábitos fitófagos "succívoros". Los daños en la planta pueden presentarse a nivel de raíces, tallos, hojas, flores o inflorescencias y frutos. Este grupo de insectos es uno de los de mayor importancia económica (BUSTILLO & SÁNCHEZ, 1977).
Los síntomas asociados a los daños que causan los áfidos son la deformación o el enroscamiento de los brotes jóvenes, amarillamiento o clorosis, y posterior necrosis de las hojas jóvenes por pérdida de pigmentos fotosintéticos (clorofila a, clorofila b y carotenoides) indispensables para el crecimiento de las plantas (WANG et al., 2004; BALDINI et al., 2008; DAVID et al., 2009), y formación de agallas en tallos y raíces. Los áfidos excretan una sustancia azucarada, conocida como rocío de miel. Esta sustancia posibilita la fijación a la planta de una mezcla de hongos saprofíticos del género Capnodium, azúcares y partículas de polvo y grasa desde el ambiente (DELFINO & BINAZZI, 2002; KAPLAN & EUBANKS, 2002). Tal combinación de elementos produce en la superficie de hojas, tallos, ramas, y frutos un recubrimiento negro, que se conoce como fumagina o negrilla, el cual interfiere con el normal desarrollo de las actividades fotosintéticas de la planta (PATEL et al., 1997; LORENZANA et al., 2004, Ramos y Serna 2004,; SATAR et al., 2005; RUBIN et al., 2006). La producción de rocío de miel le permite también a los áfidos mantener una asociación simbiótica facultativa (no especifica) con hormigas (Hymenoptera: Formicidae) (KAPLAN & EUBANKS, 2002), aunque algunas veces prefieren atender determinadas especies de áfidos (DELNO & BUFFA 1996). Esta asociación mutualista consiste en que las hormigas protegen y transportan los áfidos a diferentes sitios de alimentación (PANCONESI, 1999), y a su vez las hormigas obtienen el recurso energético del rocío de miel (QUEIROZ & OLIVEIRA, 2001), que contribuye a aumentar el potencial de dispersión de los áfidos (RENAULT et al., 2005; LARSEN et al., 2001; KAPLAN & EUBANKS, 2002). Algunas especies de áfidos pueden llegar a tener más de diez generaciones en un año (IVERSEN & HARDING, 2007).
Desde el punto de vista agrícola, lo más importante de los áfidos es su capacidad de infección viral de una planta a otra y la acción tóxica de las secreciones salivares que inyectan durante su proceso de alimentación, y que causan serias alteraciones en el crecimiento de las plantas (MINKS & HARREWIJN, 1987; EASTOP, 1977; BLACKMAN & EASTOP, 2000; KAPLAN & EUBANKS, 2002; MICHELOTTO et al., 2004; WALLIS et al., 2005; QUIROS & EMMEN, 2006; ROBSON et al., 2007; VAN EMDEN & HARRINGTON, 2007; NUESSLY et al., 2008; ZHANG et al., 2008). Además del daño directo en la planta por su alimentación, los daños también provocan una disminución en los rendimientos y calidad de las semillas (YOKOMI et al., 1994; BLACKMAN & EASTOP, 2000; DONALDSON & GRATTON, 2007). Se considera que los áfidos son los responsables de la transmisión del 55-60% de los virus de las plantas (BELDA et al., 1994; CERMELI, 2012), o del 80% al 90% (BUSTILLO & SÁNCHEZ, 1977). Aproximadamente, 4000 especies de áfidos se encuentran descritas y se reporta hasta el momento que 192 transmiten 275 tipos de virosis (NAULT, 1997). Los virus se alojan en los estiletes maxilares o en las glándulas salivares, en el momento de la succión de savia. Esta capacidad de transferencia de virus patogénicos convierte a los áfidos en uno de los grupos de artrópodos más importantes en la Agronomía.
En atención a la importancia agronómica que envuelve este grupo de insectos, a la falta de colecciones de referencia taxonómica y a los pocos estudios morfológicos y taxonómicos en Colombia, el presente estudio pretendió abordar cuatro actividades complementarias: Elaborar una colección de referencia en el Museo Entomológico UNAB (Universidad Nacional Agronomía Bogotá) de áfidos de importancia agrícola, incluyendo su curaduría; analizar la morfología general básica de Aphididae; proponer una clave de identificación para los géneros y especies más comunes en nuestro medio; y presentar las diagnosis taxonómicas ilustradas de las especies hasta ahora curadas en UNAB.
El estudio básico de la morfología de Aphididae permite comprender las transformaciones estructurales que ocurren entre las diferentes especies, el reconocimiento de nuevos caracteres, ya sea para su uso en estudios de filogenia, en la elaboración de nuevas descripciones,diagnosis, claves de identificación, propuestas clasificatorias dentro de la familia, o para el desarrollo de estudios aplicados hacia la relación planta-insecto, fisiología, etc. La morfología permite también revelar las variaciones intraespecíficas (SNODGRASS, 1993, BLACKMAN & EASTOP, (2000); BLACKMAN & EASTOP, (2006).
MATERIALES Y MÉTODOS
Curaduría
Luego de la recolección, sacrificio y separación preliminar de especímenes, las metodologías de curaduría establecidas en el Museo entomológico UNAB comprenden los procesos de aclarado, montaje, rotulación, identificación, catalogación en base de datos digital, etiquetado y preservación en la Colección Taxonómica Central (CTC) de UNAB de las muestras en líquido y en láminas portaobjetos (Figura 1).

Aclarado: Los insectos se sumergen en una solución de KOH [10%] y se calientan al "baño maría" de 5 a 10 minutos. Se transvasan a una caja Petri con solución de agua y ácido acético glacial [1%]. Seguidamente, a cada espécimen se le hace presión con un pincel o pala diminuta para terminar la extracción de los contenidos internos.
Montaje: El procedimiento de montaje en placas (láminas) se basa en BLACKMAN & EASTOP, (2000), el cual se modificó de acuerdo con los resultados más favorables. Los individuos aclarados se depositan en cajas Petri con aceite de clavo para limpiar los restos que quedan de las soluciones anteriores y finalizar el aclarado; cada espécimen se pone en láminas portaobjetos y se le agrega una gota de bálsamo de Canadá; se cubre con una laminilla cubreobjetos. El montaje se flamea con un mechero hasta que las burbujas de aire y restos de aceite se salen del espécimen y de la lámina. Para esto también, en algunos casos, se coloca la lámina en una plancha caliente a 40 grados centígrados por dos días. La lámina cubre-objetos se sella contra el portaobjetos con esmalte transparente.
Rotulado: En un rótulo blanco adherido a la lámina se consigna la siguiente información, para las categorías de división política y otros datos de colección: País, Departamento, Municipio, corregimiento, vereda, georreferencia, elevación (m alt.), especie vegetal asociada, colector y fecha.
Determinación taxonómica: Para este procedimiento se utilizan las claves y descripciones de HOLMAN, (1974); BLACKMAN & EASTOP, (2000); BLACKMAN & EASTOP, (2006) y STOETZEL, (1994). Para la identificación de los áfidos es necesario tener en cuenta un variado número de caracteres morfológicos. Los de mayor uso taxonómico son el número de artejos antenales, el número de rinarios primarios y secundarios, su posición en la antena y si los rinarios primarios están o no acompañados de rinarios accesorios o satélites (COSTA LIMA, 1938); la bifurcación de la vena Media (M), la longitud de los sifúnculos, longitud del estilete y las diversas formas que presenta la cauda.
Etiquetado: En la lámina portaobjeto, y al lado derecho de la laminilla cubreobjeto (cabeza del espécimen hacia adelante) se coloca una etiqueta verde, para los especímenes identificados hasta el nivel de género o especie. En esta etiqueta se se consigna la siguiente información: número de catálogo, familia, género, especie, determinador y año de la determinación. Las placas se almacenan en cajas portaláminas en la Colección Taxonómica Central (CTC) de UNAB (Figura 1) y de ser posible se guarda un respaldo en líquido de cada muestra. Esta colección cuenta con una base de datos electrónica asociada a cada número de catálogo.
Morfología
Para el estudio de la morfología se utilizaron los especímenes preparados en láminas. El estudio y dibujo de las estructuras básicas se basó en SNODGRASS (1993), HOLMAN, (1974); BLACKMAN & EASTOP, (2000); BLACKMAN & EASTOP, (2006) y STOETZEL, (1994).
RESULTADOS.
Curaduría. Colección de referencia y catalogación de los áfidos de UNAB.
En esta fase inicial del estudio de los áfidos, la Colección Taxonómica Central (CTC) de UNAB alcanza 579 especímenes curados, 18 especies determinadas, de 19 municipios ubicados en cinco departamentos (Antioquia, Boyacá, Caldas, Tolima y Cundinamarca), con un total de 34 plantas hospedantes, 26 de estas de importancia agrícola. Para cada especie determinada, a continuación se relacionan respectivamente los números de catálogo asignados en UNAB y sus plantas hospedantes:
Toxoptera aurantii (Boyer de Fonscolombe, 1841) (No. Catálogo 3113: Annona muricata (Annonaceae), Citrus sp., Citrus aurantii, Citrus reticulata (Rutaceae), Theobroma cacao (Malvaceae), Vigna unguiculata (Fabaceae), Coffea arabica (Rubiaceae), Rosa sp. (Rosaceae); T. citricidus (Kirkaldy, 1907) (No. Catálogo 3432, Citrus aurantium, Citrus reticulata, Citrus sp. Rutaceae); Brevicoryne brassicae (Linnaeus, 1758) (No. Catálogo 3467: Brassica oleraceae, Brassica rapa (Brassicaceae), Lactuca sativa (Asteraceae); Rhopalosiphum padi (Linnaeus, 1758) (No. Catálogo 3499: Zea mays (Poaceae); Myzus persicae (Sulzer, 1776) (No. Catálogo 3500, 491: Solanum tuberosum (Solanaceae), Sesamum indicum (Pedaliaceae), Malva sp. (Malvaceae), Myzus ornatus Laing, 1932 (No. Catálogo 3660: Citrus sp. (Rutaceae), Tecoma stans (Bignoniaceae); Greenidia ficicola Takahashi, 1921 (No. Catálogo 3545: Ficus benjamina (Moraceae), Psidium guajava (Myrtaceae); Tuberolachnus salignus (J. F. Gmelin, 1790) (No. Catálogo 3546: Salix babylonica (Salicaceae); Aphis nerii Boyer de Fonscolombe, 1841 (No. Catálogo 3567: Nerium oleander (Apocynaceae); A. gossypii Glover, 1878 (No. Catálogo 3686: Solanum betaceum (Solanaceae), Hibiscus grandiflorus (Malvaceae), Gossypium sp. (Malvaceae); A. craccivora Koch, 1854 (No. Catálogo3685: Vitis sp. (Vitaceae), Mimosa pudica (Fabaceae), Ulex sp. (Fabaceae); Cerataphis brasiliensis (Hempel, 1901) (No. Catálogo 3573: Coccus nucifera (Arecaceae); C. orquidearum (Westwood, 1879) (No. Catálogo 3574: Anguloa sp. (Orquidiaceae); Macrosiphum euphorbiae (Thomas, 1878) (No. Catálogo 3644: Hibiscus grandiflorus (Malvaceae), Rosa sp. (Rosaceae), Tecoma stans (Bignoniaceae); Sipha flava (Forbes, 1884); Carolinaia cyperi Ainsllie, 1915 (No. Catálogo 492; Cyperus sp. (Cyperaceae); Dysaphis apiifolia (Theobald, 1923) (No. Catálogo 493: Arracacia xanthorrhiza (Apiaceae); Picturaphis brasiliensis (Moreira, 1925) (No. Catálogo 494: Phaseolus vulgaris (Fabaceae) y Uroleucon ambrosiae (Thomas, 1878) (No. Catálogo 3687: Tithonia diversifolia (Asteraceae), Taraxacum officinale (Asteraceae).
Insectos en general pequeños (4-8 mm de longitud), delicados, cuerpo ovalado o piriforme (BLACKMAN & EASTOP, 2000), algunas veces cubierto parcial o totalmente por sustancias cerosas (ejemplo Cerataphis spp., Brevicoryne brassicae y Eriosoma spp.).
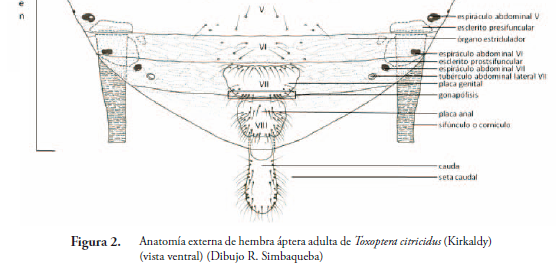
Cabeza. (Figura 2.) De tipo opistognata, con aparato bucal dirigido hacia abajo y hacia atrás (SNODGRASS, 1935). En la mayoría, la cabeza se diferencia claramente del tórax. Partes laterales de la frente protuberantes, dirigidas hacia arriba, formando tubérculos antenales. Frente con diversas formas, según la protuberancia relativa de los tubérculos antenales; algunas veces convexa, transversalmente recta, ligeramente cóncava o sinuosa; aspectos mesiales (interiores) de tubérculos convergentes, paralelos o divergentes. En posición media en la frente, algunas veces se puede encontrar el tubérculo frontal, una proyección más o menos evidente.
En alados y también en la mayoría de los ápteros, se desarrolla el ojo compuesto, y con frecuencia una proyección llamada triommatidio o tubérculo ocular, en margen posterior de la cabeza. Alados: tres ocelos, dos de ellos ubicados en posición dorso-lateral y otro en posición medio-frontal. En ápteros de algunas especies, ojos reducidos solo al triommatidio (como en Cerataphis). Según HOLMAN, (1974), algunas especies con triommatidio fusionado al ojo compuesto o desplazado ventralmente, de manera que no es apreciable desde el dorso.
Aparato bucal de tipo picador-chupador, denominado rostro, rostrum, labium o pico, compuesto de cinco segmentos; segmento apical (V) con frecuencia muy pequeño comparativamente y parcial o totalmente fusionado con el segmento previo (IV). Segmento IV con seis setas, un par lateral, uno dorsal y uno ventral. Este segmento además con dos pequeñas setas basales y dos o más setas adicionales o secundarias en la parte media.
Antena. (Figura 3). Filiforme, compuesta por 5 ó 6 artejos. El escapo se articula con la cápsula cefálica en la fosa antenal. El segundo es el pedicelo. Tres o cuatro (usualmente cuatro) artejos siguientes más delgados y alargados, que conforman el flagelo. Algunos segmentos con sensilias placoideas subcirculares, anulares o transversales, conocidas como rinarios. Último artejo antenal por lo general con adelgazamiento en su tramo distal, conocido como proceso terminal ("processus terminalis"), que va desde la margen distal del primer rinario primario hasta ápice antenal. Caracterización Morfológica de los áfidos. (Figura 2).
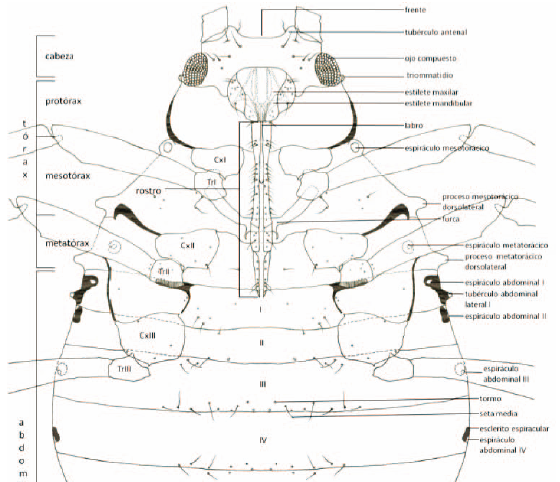
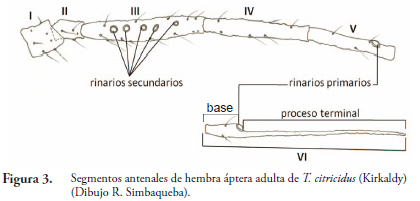
Rinarios primarios presentes en todos los ínstares y en todas las especies. Último y penúltimo segmento antenal con uno a tres rinarios accesorios o satélites, contiguos a los rinarios primarios. Rinarios secundarios desarrollados solo en segmentos III a V de adultos, a menudo solo en segmento III y siempre presentes en alados; menos numerosos en ápteros y sin desarrollo en algunas especies (HOLMAN, 1974).
Tórax. Diferenciado; meso y metatórax fusionados (pterotórax). Primer par de espiráculos anteriados en mesotórax; segundo par en metatórax. Algunas especies con espiráculos rodeados por zona esclerosada (escleritos espiraculares). Varias especies con procesos torácicos dorsomesiales o dorsolaterales (Holman, 1974).
Apéndices torácicos.
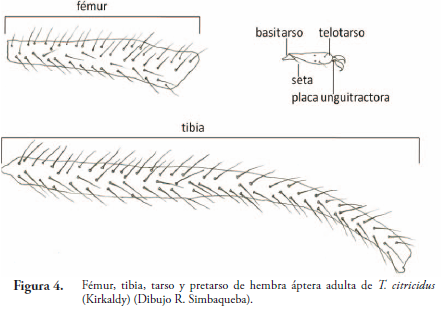
Patas. (Figura 4). De tipo caminador. Tibias más largas que fémures. Tarso con dos segmentos, basitarso y telotarso, basitarso más pequeño; telotarso con una a cinco setas basales; pretarso (podito apical) armado por dos uñas; placa unguitractora entre tarso y pretarso.
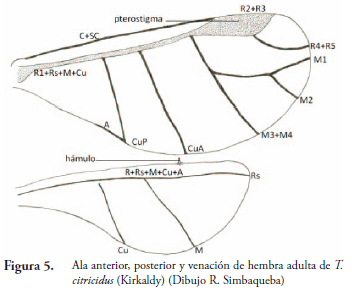
Alas. (Figura 5). Membranosas, anteriores mucho más grandes que las posteriores, con sistema de acople entre sí, por medio de ganchillos (hámulos). Venación con variaciones en las divisiones de la vena Media (M) principalmente, reducción parcial o total del sector radial (Rs), posición relativa de la base cubital (Cu) y reducción de una o varias venas en alas posteriores. Otras diferencias entre especies se presentan en la forma y pigmentación del pterostigma.
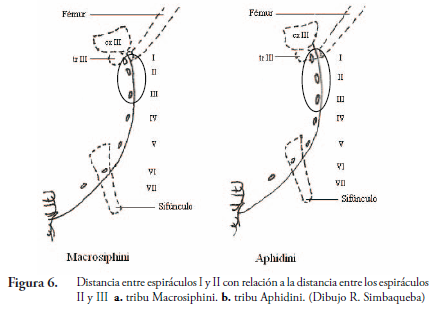
Abdomen. Formado por ocho somitos más terguito del segmento IX (cauda); segmento V o VI con par de órganos corniculares o regiones circulares pareadas dorsales (sifúnculos o cornículos) (Figura 6). Siete pares de espiráculos se distribuyen desde somito I hasta VII, un par en cada uno. Generalmente, en urómeros (segmentos abdominales) I y VII se pueden presentar tubérculos laterales. Algunas especies con proceso abdominal dorsomedial, como tubérculo abdominal dorsal (ejemplo: Tuberolachnus salignus (Gmelin).
Apéndices abdominales.
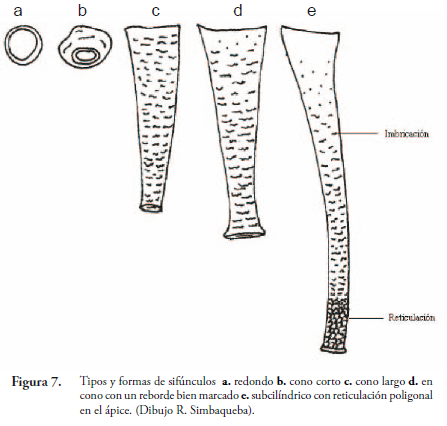
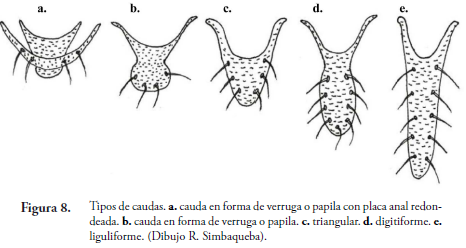
Los sifúnculos son un par de órganos dorsales que se localizan en urómeros V o VI. Su forma varía desde poros simples hasta tubos largos que miden hasta 2/3 de la longitud del cuerpo (ejemplo Greenidea sp.) (Figura 7.). Esternito del segmento VII se conoce como placa genital, se desarrolla solo en formas adultas, ápteras y aladas. Margen posterior de placa genital con grupo de setas denominas "gonapófisis". Cauda corresponde a terguito de segmento IX transformado (Figura 8.),en la mayoría de los áfidos unido al segmento VIII y con movilidad dorso ventral. Cauda y placa anal (esternito del segmento VIII) funcionan probablemente como esfínter anal (Holman, 1974; Zimmerman, 1948).
Setas y escleritos. Cuerpo de especies más ancestrales cubierto por setas finas y espesas. Mayoría de especies con número limitado de setas dorsales, dispuestas más o menos en seis hileras longitudinales: dos mediales (a lo largo de la línea media del cuerpo), dos laterales (una a cada lado del cuerpo) y dos pleurales (una a cada lado entre las hileras mediales y laterales). Segmentos torácicos, y casi todos los abdominales, con seis grupos de setas, cada uno constituido por una o más setas. Setas pleurales sin desarrollo en segmentos V a VIII; segmento VII con frecuencia con solo setas mediales.
Dorso a menudo con placas (áreas esclerosadas) alrededor de la base de las setas, a veces alargadas o fusionadas en algunos grupos, para formar esclerito medial, pleural o marginal. En algunas especies, estos escleritos se fusionan en escleritos o franjas dorsales, que pueden iniciar desde la zona media y terminar en la zona pleural o franjas transversales. Estos últimos incluyen también los escleritos marginales. Las franjas transversales en segmentos abdominales III-V o III-VI pueden unirse para formar placa central o escudo central abdominal. Escleritos marginales de urómeros V y VI representan escleritos presifunculares y postsifunculares correspondientes.
Clave para géneros y especies de áfidos (Hemiptera: Aphididae) más comunes y curados en UNAB.
(En general esta clave aplica para áfidos ápteros. Algunos alados se especificarán en la alternativa respectiva)
1. Setas largas y gruesas en dorso de tórax y abdomen (Figura 23a); último segmento rostral (pico) aproximadamente 0.5 de la longitud del II segmento del tarso posterior; placa anal redondeada (Figura 8a.). .......... ..Sipha flava
1'. Otra combinación de caracteres .. ..2
2. Proceso medidorsal abdominal en forma de cono, entre los sifúnculos (Figura 18c). Sifúnculo en forma de cono bajo (Figura 7b) ...Tuberulacnus salignus
2'. Proceso mediodorsal abdominal ausente .. . .3
3. Sifúnculo en forma de poro (Figura 7a.); cuerpo ovalado (Figura 19a) casi circular, deprimido (en vivo), con cerarios marginales (Figura 19a); cauda en forma de verruga o vesícula (Figura 8a y 8b); formas ápteras carecen de ojos compuestos; procesos frontales pareados, en forma de cuerno (Figura 20b) .Cerataphis 4
3'. Sifúnculos tubulares, subcilíndricos o cónicos (Figura 7b a 7e); cuerpo piriforme u oblongo; cerarios marginales ausentes (Figura 1a.); cauda digitiforme (Figura 8d.), triangular (Figura 8c) o semicircular (Figura 11d.) ... ..5
4. Dos setas frontales gruesas, cortas, en forma de lanza, o incrasada (gruesa) (Figura 19b.).. ...Cerataphis brasiliensis
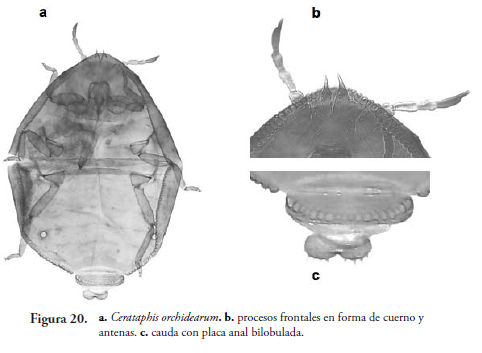
4'. Setas frontales filiformes; proceso frontal (cuerno) más corto que segundo tarsómero de pata posterior (Figura 20b) . Cerataphis orchidearum
5. Sifúnculo 2/3 de la longitud del cuerpo; setas largas y gruesas a lo largo del sifúnculo (Figura 11b); cauda semicircular (Figura 11d) .. ...Greenidea ficicola
5'. Otra combinación de caracteres . . .6
6. Distancia entre espiráculos abdominales I y II grande (mínimo la mitad o la misma distancia entre los espiráculos abdominales II y III (Figura 6b)); tubérculo lateral en protórax (Figura 16c) y papila lateral ("tubérculos marginales") (Figura 9d) en segmentos abdominales I y VII presentes (se pueden presentar papilas laterales en los segmentos abdominales II a VI, pero siempre más pequeñas que en los segmentos I y VII); cabeza no ornamentada (lisa) sin espículas, corrugaciones, asperitos o microtriquias; antenas más cortas que el cuerpo ..tribu Aphidini 7
6'. Distancia entre espiráculos abdominales I y II muy corta (menos de la mitad de la distancia entre los espiráculos abdominales II y III (Figura 6a)); tubérculo lateral protorácico y papila lateral ("tubérculo marginal") en segmentos abdominales I y VII ausentes (de presentarse son de menor tamaño que aquellos de los segmentos abdominales II a VI); antena generalmente más larga que el cuerpo; Cabeza con ornamentación variada (espículas, corrugación, asperitos o microtriquias (Figura 13b) tribu Macrosiphini 12
7. Tubérculo frontal ausente; tubérculo antenal medianamente desarrollado, superficie lateroventral de los segmentos abdominales V y VI con un patrón de cutícula encarrujado (Figura 15c); tibia posterior con pequeñas setas cónicas cortas . . .. ...Toxoptera 8
7'. Tubérculo frontal presente, aunque puede estar poco desarrollado; tubérculo antenal de desarrollo variable; superficie lateroventral de los segmentos abdominales V y VI sin un patrón de cutícula encarrujado; tibia posterior sin pequeñas setas cónicas cortas .. .9
8. Proceso terminal entre tres y cinco veces más largo que el tramo proximal ("base") de su respectivo segmento antenal; cauda digitiforme, con menos de 20 setas; alas anteriores con una sola bifurcación de la vena Media (M) y pterostigma oscuro (Figura 15) . .. .Toxoptera aurantii
8'. Proceso terminal 4.0 - 5.5 veces más largo que el tramo proximal de su respectivo segmento antenal; cauda digitiforme, con más de 20 setas; alas anteriores con doble bifurcación de la vena Media (M) y pterostigma hialino (Figura 16) Toxoptera citricidus
9. Antena de 0.6 - 0.65 de la longitud del cuerpo; sifúnculo 0.13 - 0.20 de la longitud del cuerpo, con reborde apical bien desarrollado y una ligera constricción basal del reborde (Figura 17c); cauda como máximo la mitad de la longitud del sifúnculo, sin constricción alguna y con cuatro o cinco setas (Figura 17) .. .Rhopalosiphum padi
9'. Antena 0.3 - 1.0 de la longitud del cuerpo; sifúnculo 0.15 - 0.25 de la longitud del cuerpo, sin reborde ni constricciones; cauda digitiforme, con 4 a 18 setas ....Aphis 10
10. Cuerpo 1.5 - 2.4 mm de longitud; tubérculo frontal y tubérculo antenal poco desarrollados; antena de 0.6 a 0.8 de la longitud del cuerpo; proceso terminal de 3.5 a 4.5 veces más largo que el tramo proximal de su respectivo segmento antenal. En vivo, áfido de color amarillo intenso o naranja con apéndices de color marrón muy oscuro o negros (Figura 9) ... . . Aphis nerii
10'. Cuerpo 0.9 - 2.7 mm de longitud; tubérculo frontal de desarrollo variable; antena de 0.5-0.7 del longitud del cuerpo; proceso terminal 1.9-3.0 veces más largo que la región proximal ("base") de su respectivo segmento antenal .11
11. Cuerpo 0.9-1.9 mm de longitud; tubérculo frontal medial evidente; antena de 0.5-0.65 de la longitud del cuerpo; sifúnculo 1.3-2 veces más largo que la cauda; cauda digitiforme, con 4 a 7 setas (Figura 21) .. ..Aphis gossypii
11'. Cuerpo de 1.25 a 2.7 mm de longitud; tubérculo frontal y antenal de desarrollo variable; antena de 0.55-0.70 del largo del cuerpo; sifúnculo 0.15-0.25 de la longitud del cuerpo; cauda digitiforme, con 7 setas; escudo o placa dorsal abdominal formada por la fusión de franjas transversales de los terguitos II a VI (Figura 22a) . Aphis craccivora
12. Segmento antenal III muy largo, más largo que los segmentos IV y V conjugados (Imagen 3b); sifúnculo de la misma longitud que la cauda; cauda triangular (Figura 8c), con 6 a 9 setas. En vivo, áfido cubierto por un polvo ceroso de color gris o blanco (Figura 10) . . ....Brevicoryne brassicae
12'. Segmento antenal III aproximadamente igual a la longitud de los segmentos IV y V conjugados; sifúnculo de mayor longitud que la cauda; cauda de otro tipo ...13
13. Ápteros: Antena más corta que la longitud del cuerpo; cabeza ornamentada con numerosas espículas. Alados: Rinarios secundarios en el segmento antenal III únicamente; placa mediodorsal abdominal esclerosada .Myzus 14
13'. Ápteros: Antena más larga que el cuerpo; cabeza lisa o corrugada. Alados: Rinarios secundarios no limitados al segmento antenal III; sin placa central dorso-abdominal esclerosada ....15
14. Ápteros: antena aproximadamente 0.6 de la longitud del cuerpo; proceso terminal 1.8 a 2.5 veces más largo que la región proximal ("base") de su respectivo segmento antenal (Figura 13) ..Myzus ornatus
14'. Ápteros: antena aproximadamente 0.8 de la longitud del cuerpo; proceso terminal tres a cinco veces más largo que la región proximal ("base") de su respectivo segmento antenal (Figura 14) ... ...Myzus persicae
15. Sifúnculo reticulado distalmente (máximo 0.25 de su longitud) (Figura 7e). Áptero: Uno a 36 rinarios secundarios en el segmento antenal III; basitarso siempre con tres setas ..Macrosiphum 16
15'. Sifúnculo reticulado distalmente (0.25 a 0.40 de su longitud). Ápteros: 10-40 rinarios secundarios en segmento antenal III; cada seta dorsal proveniente de un esclerito (pinácula); basitarso con cinco setas .Uroleucon ambrosiae
16. Ápteros: Dos a ocho rinarios secundarios en región proximal del segmento antenal III; sifúnculo oscuro solo distalmente; cauda más oscura que región proximal de los sifúnculos (Figura 12) .. .....Macrosiphum euphorbiae
16'. Ápteros: 10 a 36 rinarios secundarios en el segmento antenal III; sifúnculo oscuro en toda su longitud; cauda de tonalidad más clara que el sifúnculo ...Macrosiphum rosae
Diagnosis para los géneros y especies de áfidos (Hemiptera: Aphididae) más comunes y curados en UNAB.
Aphis nerii Boyer de Fonscolombe, 1841 (Figura 9)
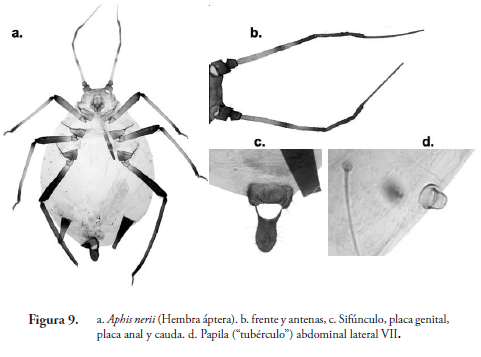
Áfido de color amarillo intenso o amarillo anaranjado, con apéndices de color café muy oscuro o negros. Cuerpo piriforme, de 1.5-2.4 mm de largo. Tubérculo frontal y tubérculo antenal pequeño o poco desarrollado. Antena de 0.6-0.8 de la longitud del cuerpo. Rinario secundario no desarrollado. Proceso terminal de 3.5-4.5 veces mas largo que la parte basal del segmento antenal VI. Rostro (pico) alcanza coxa posterior. Sifúnculo con textura imbricada y muy esclerosado, 0.20-0.25 del largo del cuerpo. Cauda digitiforme, aproximadamente 1,5 veces mas larga que el ancho de su base, con constriccion visible y 9-18 setas. Placa genital con dos setas largas en la parte anterior y de 4 a 8 similares a cada lado del margen posterior. Generalmente habita en Asclepiadaceae y Apocynaceae (Holman, 1974).
Brevicoryne bassicae (Linnaeus, 1758) (Figura 10)
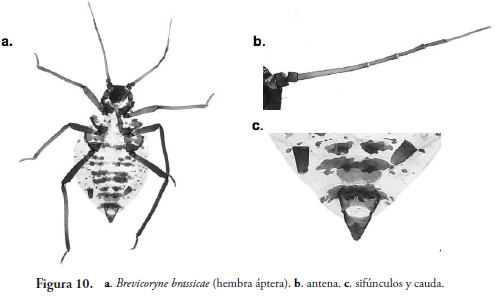
Áfido cubierto por un polvo ceroso de color blanco o gris. Cuerpo ovalado, frente sinuosa, antena de 0.55-0.75 del largo del cuerpo, segmento antenal muy largo, más largo que los segmentos IV y V juntos. Dorso abdominal con escleritos irregulares como base de las setas medias y pleurales; estos a menudo se fusionan formando escleritos mediales-pleurales (Figura 9a) y en terguitos más posteriores forman franjas transversales. Sin tubérculos laterales, 1 ó 2 muy pequeños rara vez se presentan en el segmento IV ó V. Sifúnculos del mismo tamaño que la cauda. Cauda triangular con 6-9 setas. Placa genital con dos setas en la parte anterior y de 11-17 setas a lo largo del margen posterior. Habita generalmente en plantas del género Brassica (Holman, 1974).
Greenidea ficicola Takahashi, 1921 (Figura 11)
Adultos y ninfas ápteras, con cuerpo piriforme, de coloración amarilla parda a café claro. Tubérculo antenal débilmente desarrollado. Antena aproximadamente de igual longitud del cuerpo en ápteros y más largas en alados. Sifúnculo distalmente divergente, recubierto por setas gruesas, completamente reticulado, igual o más largos que las tibias posteriores. (BLACKMAN & EASTOP, 2000). Alados: 17 a 21 rinarios secundarios en el segmento antenal III, dispuestos en una línea a lo largo del segmento; no más de un rinario por sitio. Habita generalmente en Psidium guajava y Ficus sp.
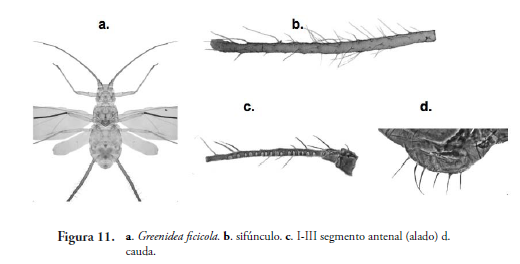
Macrosiphum euphorbiae (Tomas, 1878) (Figura 12)
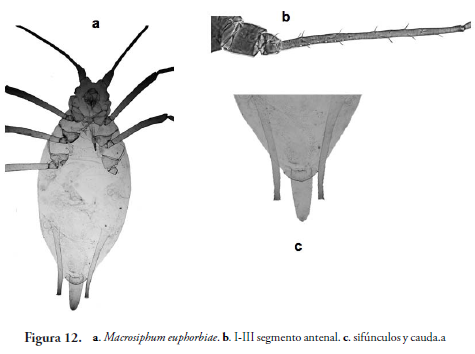
Áfido alargado, delgado, con cuerpo de color verde o rosado, la mayoría de las veces con franjas longitudinales más oscuras, ojos rojos, frente acanalada. Tubérculo antenal desarrollado, antena 1.0-1.5 veces más larga que el cuerpo. Proceso terminal de 5.0-6.5 veces más largo que la longitud de la base del segmento antenal VI. Base del segmento antenal III con 2-7 rinarios secundarios. Apéndices del mismo color del cuerpo, sifúnculo claro en su totalidad y oscuro en su ápice reticulado, de 0.25-0.33 del largo del cuerpo. Cauda liguliforme, con 8-12 setas. Placa genital con 2-4 setas en la parte anterior y algunos a lo largo del margen posterior. Se hospeda habitualmente en Solanaceae, Asteraceae y Cucurbitaceae (HOLMAN, 1974).
Myzus ornatus Laing, 1932 (Figura 13)

Áfidos pequeños; ápteros de color verde claro o verde amarillento, alados con cabeza y tórax oscuro, abdomen verde claro con algunas placas intersegmentales, sifúnculo y cauda oscuros. Dorso con algunas arrugas con apariencia coriácea. Cabeza recubierta por espínulas. Tubérculo antenal bien desarrollado, con el lado interior ligeramente divergente. Antena de la mitad del cuerpo. Proceso terminal de 1.8-2.5 veces más largo que la longitud de la base del segmento antenal VI. Ápteros: rinario secundario no desarrollados; alados: con 4-14 rinarios secundarios en el segmento antenal III. Ápteros: con sifúnculo aproximadamente 0.2 del largo del cuerpo. Aldos: con sifúnculo aproximadamente 0.11-0.2 del largo del cuerpo, imbricado y con reborde ancho. Cauda casi triangular, la mitad de la longitud del sifúnculo o más corta, con 4-6 setas. Placa genital con dos setas en la parte anterior y 8-10 a lo largo del margen posterior. Polífago (Holman, 1974).
Myzus persicae (Sulzer, 1776) (Figura 14)
Áfido de color verde-amarillento claro, verde o rosáceo. Cuerpo de 1.3-2.5 mm de largo. Cabeza con espículas. Tubérculo antenal desarrollado, con excrecencias redondeadas en el margen interior y apariencia convergente. Antena 0.65-0.80 del largo del cuerpo. Proceso terminal 3-5 veces más largo que la longitud de la base del segmento antenal VI. Alados con 7-16 rinarios secundarios, no desarrollados en ápteros. Sifúnculo de 0.20-0.28 del largo del cuerpo. Alados con una placa dorsomedial abdominal esclerosada. Cauda 0.37-0.5 del largo de los sifúnculos, en forma de triángulo alargado, con 5-7 setas. Polífago (Holman, 1974).
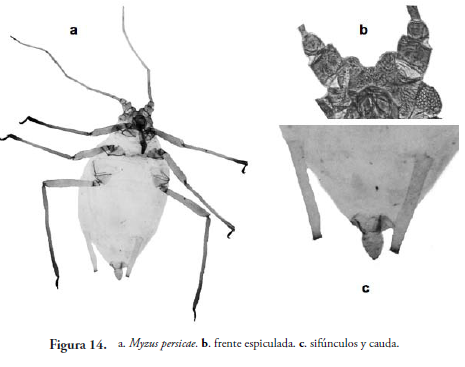
Toxoptera aurantii Boyer de Fonscolombe, 1841 (Figura 15)
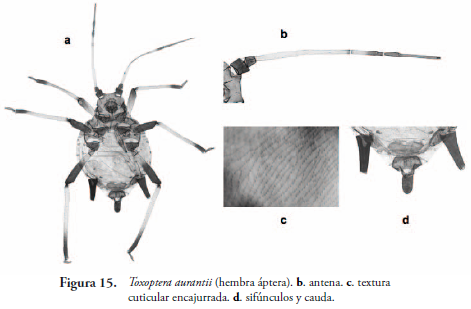
Áfido café oscuro, piriforme, 1.0-2.0 mm de largo. Tubérculo antenal poco desarrollado. Antena de 0.65-0.8 del largo del cuerpo. Proceso terminal 3.3-5.0 veces más largo que la longitud de la base del segmento antenal VI. Rinarios secundarios en número de 2-8 en alados, en los ápteros no se desarrollan. Ala anterior con una sola bifurcación de la vena media (M) y pterostigma oscuro. Sifúnculo igual o un poco más largos que la cauda. Cauda digitiforme con 12-20 setas. Placa genital con 3-8 setas en la parte anterior y de 4-7 setas a cada lado del margen posterior. Superficie lateroventral de los segmentos abdominales V y VI con un patrón de cutícula serrada y endentada. Tibia posterior con setas cónicas y cortas. Polífago, generalmente habita en cítricos (Holman, 1974).
Toxoptera citricidus (Kirkaldy, 1907) (Figura 16)

Áfido de color negro brillante. Característica similares a T. aurantii. Alas anteriores con doble bifurcación de la vena media (M), pterostigma muy claro o hialino. Sifúnculo igual o ligeramente más largo que la cauda. Cauda digitiforme, con más de 20 setas. Superficie lateroventral de los segmentos abdominales V y VI con un patrón de cutícula serrada y endentada. Tibia posterior con setas cónicas y cortas. Polífago, generalmente habita en cítricos (Holman, 1974)
Rhopalosiphum padi (Linnaeus, 1758) (Figura 17)
Piriforme, de 1.5- 2 mm de largo, color verde oscuro, con pigmentaciones rojizas alrededor de la base del sifúnculo. Frente sinuosa, con tubérculo frontal y tubérculo antenal bien desarrollado. Antenas 0.6-0.65 del largo del cuerpo. Proceso terminal 4-5 veces más largo que la longitud de la base del segmento antenal VI. Sifúnculo 0.13-0.18 del largo del cuerpo, reborde bien desarrollado y con ligera constricción anterior. Cauda como máximo la mitad del largo de los sifúnculos, sin constricción alguna, con 4-5 setas. En hojas e inflorescencias de gramíneas (HOLMAN, 1974).

Tuberolachnus salignus (J. F. Gmelin, 1790) (Figura 18)
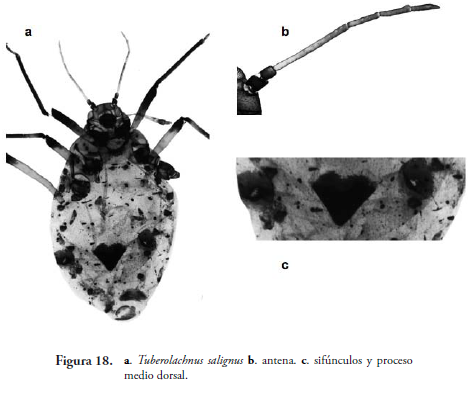
Café oscuro, de 4.0-6.0 mm de largo, cubierto de numerosas setas finas. Tubérculos antenales no desarrollados. Antenas aproximadamente 0.3 del largo del cuerpo. Proceso terminal cónico, 0.35 de la longitud de la base del segmento antenal VI. Rinarios secundarios generalmente no desarrollados en los ápteros. Dorso membranoso con pequeños escleritos. Entre los segmentos IV y V se desarrolla un tubérculo medial grande y cónico. Sifúnculo muy pequeños, setoso, de forma cónica. Cauda no más larga que ancha, con apariencia redondeada (semicircular). En Salix sp. (HOLMAN, 1974).
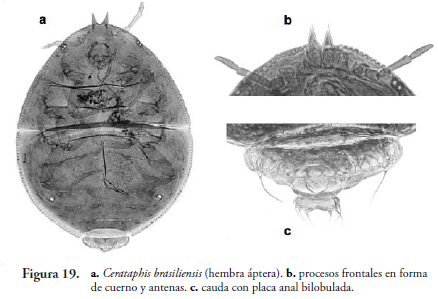
Cerataphis brasiliensis (Hempel, 1901) (Figura 19)
Café oscuro o negro, redondeado y plano. Ápteros: con cuerpo aleirodiforme, con cera blanca alrededor de todo su cuerpo, de 1-1.5 mm de longitud; amplitud 0.75-0.8 del largo del cuerpo. Cabeza fusionada con el pronoto, con un par de procesos anteriores en forma de cuernos puntiagudos y con setas gruesas en la base de estos en forma de daga, ojos reducidos al triommatidio. Antena de 0.15-0.20 del largo del cuerpo. Proceso terminal cónico de 0.3-0.4 de largo de base del segmento antenal VI. Sifúnculo redondo. Cauda en forma de verruga, con 6-8 setas largas. Placa anal bilobulada. En Arecaceae (Holman, 1974).
Cerataphis orchidearum (Westwood, 1879) (Figura 20)
Ápteros con características iguales a C. brasiliensis (color, forma, etc). Cuerpo de 1-1.7 mm de largo. Sin setas gruesas en la base de los procesos anteriores de la cabeza. Cauda en forma de verruga con 8-10 setas. Alados de color café oscuro o negro, ojos compuestos bien desarrollados, sin tubérculos antenales. Antena de 0.3-0.45 del largo del cuerpo, de cinco segmentos, proceso terminal de 0.20-0.25 de largo de la base del segmento antenal VI. Cuerpo de 1.6-2.3 mm de largo. Aproximadamente 30 rinarios secundarios en el segmento antenal III y de 8-15 en el segmento antenal V, en forma de anillos. Cauda en forma de verruga con 10 setas. Placa anal bilobulada. En Orchidaceae (HOLMAN, 1974).
Aphis gossypii Glover, 1877 (Figura 21)

Áfidos de tamaño y color variado, ninfas de tonalidades mas claras. Cuerpo de 0.9-1.9 mm de largo, adultos con frente sinuosa, tubérculo frontal medio evidente. Antena de 0.5-0.65 del largo del cuerpo, de 5-6 segmentos. Proceso terminal de 2-3 veces más largo que la longitud de la base del segmento antenal VI. Sifúnculo de 1.3-2 veces más largo que la cauda. Cauda de 1-1.6 veces más largo que su ancho basal, con 4-7 setas. Generalmente en Cucurbitaceae, Solanaceae y Malvaceae (HOLMAN, 1974).
Aphis craccivora Koch, 1854 (Figura 22)
Áptero café rojizo con dorso abdominal negro brillante, apéndices claros. Cuerpo de 1.25-2.7 mm de largo. Tubérculos antenales poco desarrollados. Antenas de 0.55-0.7 del largo del cuerpo. Proceso terminal 1.9-2.8 veces más largo que la longitud de la base del segmento antenal VI. Rinarios secundarios no desarrollados en los ápteros. Dorso abdominal con franjas transversales que se fusionan desde el segmento II al VI, formando el escudo o placa dorsal abdominal de tamaño irregular. Sifúnculos de 0.15-0.25 del largo del cuerpo. Cauda digitiforme, con 7 setas (rara vez 6 u 8). Placa genital con 2-3 setas largas en la parte anterior y 4-8 a cada lado del margen posterior. Polífago, frecuentemente en Fabaceae (HOLMAN, 1974).

Sipha flava (Forbes, 1885) (Figura 23)

Cuerpo alargado de 1,3-1,9 mm de largo. Antena de cinco segmentos, casi de la mitad del largo del cuerpo, Proceso terminal aproximadamente el doble de la base de su respectivo segmento. Rostro hasta la coxa media, ultimo segmento rostral casi de la mitad del largo del segmento II del tarso posterior. Dorso membranoso, casi liso. Setas dorsales gruesas. Sifúnculo en forma de cono corto. Primeros segmentos tarsales con 5 setas. Alados con escleritos laterales en los segmentos II-IV y VI-VII, algunos más pequeños en segmento V. Rinarios secundarios en número de 2-5, situados en segmento III. En Poaceae (Blackman, y Eastop, 2000).
AGRADECIMIENTOS
Al Museo Entomológico UNAB (Universidad Nacional Agronomía Bogotá) por facilitar las instalaciones, equipos, bibliografía y el uso de las colecciones de referencia. A Valentina Vergara por su permanente asesoría en el proceso de curaduría en UNAB. A Diana Suárez por colaborar en el ejercicio de correr la clave.
BIBLIOGRAFÍA
BALDINI, A., OLTREMARI, J. & HOLMGREN, A. 2008. Efecto de Cinara cupressi (Hemiptera: Aphididae) sobre el ciprés de la cordillera (Austrocedrus chilensis) después de aplicar control químico. Cien. Inv. Agr. 35(3): 341-350. [ Links ]
BELDA, J., AGUIRRE, A., MIRASOL, E. & CABELLO, T. 1994. Dinámica de población de pulgones alados (Hom.; Aphididae) en cultivos del levante de Almería. Bol. San. Veg. Plagas, 20: 329-337. [ Links ]
BLACKMAN, R.L. & EASTOP, V.F. 2000. Aphids on de world's crops. An identification and information guide. Chichester, UK. [ Links ]
BLACKMAN, R.L. & EASTOP, V.F. 2006. Aphids on de world's herbaceous plants and shrubs. Chichester, UK. [ Links ]
BUSTILLO, A. & SÁNCHEZ, G. 1977. Los áfidos en Colombia, plagas que afectan los cultivos agrícolas de importancia económica, ICA. [ Links ]
DAVID G., R.D., QUIROZ G., J.A., YEPES R., F. & SMITH P., A.H. 2009. Nuevo registro de Greenidea ficicola Takahashi (Hemiptera: Sternorrhyncha: Aphididae) en guayabo Psidium guajava (Myrtaceae) en Antioquia, Colombia. Rev. Fac. Nal. Agr. Medellín, 62(1): 4999-5002. [ Links ]
DEFINO, M.A & BUFFA, L.M. 1996. Asociaciones hormigas-ácidos-plantas en la Argentina. Rev. Per. Entomol. 39: 81-84. [ Links ]
DELFINO, M.A. & BINAZZI, A. 2002. Áfidos de Coniferas en la Argentina (Hemiptera: Aphididae). Rev. Soc. Entomol. Argent. 61(3-4): 27-36. [ Links ]
DELFINO, M.A. 2005. Inventario de las asociaciones áfido-planta en el Perú. Ecol. Apl. 4(1,2): 143-158. [ Links ]
DONALDSON, J. R. & C. GRATTON. 2007. Antagonistic effects of soybean viruses on soybean aphid performance. Environ. Entomol. 36: 918-925. [ Links ]
EASTOP V.F. 1977. Worldwide importance of aphids as virus vectors. In: Aphids as Virus Vector. Academic Press, New York. [ Links ]
HOLMAN, J. 1974. Los áfidos de Cuba. Instituto Cubano del Libro. La Habana. [ Links ]
IVERSEN, T. & HARDING, S. 2007. Life table parameters affecting the population development of the woolly beech aphid Phyllaphis fagi. Entomol. Exp. Appl., 123(2): 109-117. [ Links ]
KAPLAN, I. & EUBANKS, M.D. 2002. Disruption of Cotton Aphid (Homoptera: Aphididae) Natural Enemy Dynamics by Red Imported Fire Ants (Hymenoptera: Formicidae). Auburn. Environ. Entomol. 31(6): 1175-1183. [ Links ]
LARSEN, K.J., STAEHLE, L.M., & DOTSETH, E.J. 2001. Tending ants (Hymenoptera: Formicidae) regulate Dalbulus quinquenotatus (Homoptera. Cicadellidae) population dynamics. Environ. Entomol. 30: 757-762. [ Links ]
LORENZANA, A., HERMOSO DE MENDOZA, A., MAGADÁN, J.A. & SECO, M.V. 2004. Respuesta poblacional del pulgón del lúpulo, Phorodon humuli (Schrank, 1801) (Hemiptera, Aphididae) a tratamientos aficidas en diferentes épocas. Bol. San. Veg. Plagas, 30: 427-438. [ Links ]
MICHELOTTO, M.D., ADAIME DA SILVA, R. & BUSOLI, A.C. 2004. Tabelas da vida para Aphis gossypii Glover, 1877 (Hemiptera: Aphididae) em três espécies de plantas daninhas. Bol. San. Veg, Plagas, 30: 211-217. [ Links ]
MINKS, A.K. & HARREWIJN, P. 1987. Aphids: Their Biology, Natural Enemies and Control. Elsevier, New York. [ Links ]
NAULT, L.R. 1997. Arthropod Transmission of Plant Viruses: A new Synthesis. Ann. Entomol. Soc. Am. 90(5): 521-541. [ Links ]
NUESSLY, G.S., NAGATA, R.T., BURD J.D., HENTZ, M.G., CARROLL, A.S. & HALBERT, S.E. 2008. Biology and Biotype Determination of Greenbug, Schizaphis graminum (Hemiptera: Aphididae), on Seashore Paspalum Turfgrass (Paspalum vaginatum). Environ. Entomol. 37(2): 586-591. [ Links ]
PANCONESI, A. 1999. Due mortali nemici del cipresso. Instituto per la Patologia degli Alberi Forestali del C.N.R. di Firenze. Firenze, Italia. Consultado Marzo 2013 en: http://www.catpress.com/fan/scienza/umalat.htm [ Links ]
PATEL, K.I., PATEL, J.R., JAYANI, D.B., SHEKH, A.M. & PATELS, N.C. 1997. Effect of seasonal weather on incidence and development of major pests of okra (Abelmoschus esculentus). Indian Journal of Agricultural Sciences, New Delhi. 67(5): 181-183. [ Links ]
QUEIROZ, J.M., & OLIVEIRA, P.S. 2001. Tending ants protect honeydew-producing whitebies (Homoptera: Aleyrodidae). Environ. Entomol. 30: 295-297. [ Links ]
QUIRÓS, D.I. & EMMEN, D.A. 2006. Diversidad biológica de los áfidos (Hemiptera: Aphididae) de Panamá. Tecnociencia 8(2). [ Links ]
RAMOS, P., A.A. & SERNA C., F.J. 2004. COCCOIDEA DE COLOMBIA, CON ÉNFASIS EN LAS COCHINILLAS HARINOSAS (HEMIPTERA: PSEUDOCOCCIDAE). Revista Facultad Nacional de Agronomía, Medellín, 57(2): 2383-2412. [ Links ]
RENAULT, C.K., L.M. BUFFA & DEFINO, M.A. 2005. An aphid-ant interaction: Effects on different trophic levels. Ecol. Res. 20: 71-74 [ Links ]
ROBSON, J.D., WRIGHT, M.G. & ALMEIDA, R.P. 2007. Biology of Pentalonia nigronervosa (Hemiptera, Aphididae) on Banana Using Different Rearing Methods. Environ. Entomol. 36(1): 46-52. [ Links ]
RUBÍN DE CELIS, V.E., ORTIZ, M.S. & BARLETTA, C.F. 2006. Greenidea ficicola Takahashi (Hemiptera: Aphididae), Nuevo registro para Sudamérica. Rev. Per. de Entomol., 45: 105-107. [ Links ]
SATAR, S., KERSTING, U. & UYGUN, N. 2005. Effect of temperature on development and fecundity of Aphis gossypii Glover (Homoptera: Aphididae) on cucumber. Journal of Pest Science, Heidelberg, 78(3): 133-137. [ Links ]
SNODGRASS, R.E. 1935. Principles of insect morphology. New York [ Links ]
STOETZEL, M.B. 1994. Aphids (Homoptera: Aphididae) of potencial inportance on Citrus in the United States with illustrated keys to species. Proc. Entomol. Soc. Wash. 96(1): 74-90. [ Links ]
VAN EMDEN, H.F. & HARRINGTON, R. 2007. Aphids as Crop Pests. CAB International, Oxford, UK. [ Links ]
WALLIS, C.M., FLEISCHER, S.J., LUSTER, D.F. & GILDOW, E. 2005. Aphid (Hemiptera: Aphididae) Species Composition and Potential Aphid Vectors of Plum Pox Virus in Pennsylvania Peach Orchards. J. Econ. Entomol. 98(5): 1441-1450 [ Links ]
WANG, T., QUISENBERRY, S.S., NI, X. & TOLMAY, V. 2004. Aphid (Hemiptera: Aphididae) Resistance in Wheat Near-Isogenic Lines. Department of Entomology, Montana State University, Bozeman. J. Econ. Entomol. 97(2): 646-653. [ Links ]
YOLOMI, R.K., LASTRA, R., STOETZEL, M.B., DAMSTEEGT, V.D., LEE, R.F., GARNSEY, S.M., GOTTWALD, T.R., ROCHA P., M.A. & NIBLETT, C.L. 1994. Entablishment of Brown citrus aphid (Homoptera: Aphididae) in Cental America and the Caribbean Basin and transmission of citrus tristeza virus. J. Econ. Entomol. 87(4):1078-1085. [ Links ]
ZIMMERMAN, E.C. 1984. Insects of Hawaii. Vol. 5. Homoptera. University Press of Hawaii. [ Links ]













