Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Boletín Científico. Centro de Museos. Museo de Historia Natural
Print version ISSN 0123-3068
Bol. Cient. Mus. Hist. Nat. Univ. Caldas vol.18 no.2 Manizales July/Dec. 2014
REQUERIMIENTOS TÉRMICOS PARA EL DESARROLLO DE Amblyseius sp. (ACARI: PHYTOSEIIDAE)*
THERMAL REQUERIMENTS FOR THE DEVELOPMENT OF Amblyseius sp. (ACARI: PHYTOSEIIDAE)
Natalia Vinasco A.1, Alberto Soto G.2, Luis Fernando Vallejo E.3
* FR: 15-V-2104. FA: 27-X-2014.
1 Ingeniera agrónoma, Universidad de Caldas. Manizales, Caldas, Colombia. E-mail: vinasco.natalia@gmail.com.
2 I.A., M.Sc., Ph.D. Departamento de Producción Agropecuaria. Universidad de Caldas. Manizales, Caldas, Colombia. E-mail: alberto.soto@ucaldas.edu.co.
3 Biólogo, M.Sc., Ph.D. Departamento de Producción Agropecuaria. Universidad de Caldas. Manizales, Caldas, Colombia. E-mail: luis.vallejo_e@ucaldas.edu.co.
CÓMO CITAR: VINASCO A., N., SOTO G., A. & VALLEJO E., L.F., 2014.- Requerimientos térmicos para el desarrollo de Amblyseius sp. (Acari: Phytoseiidae). Bol. Cient. Mus. Hist. Nat. U. de Caldas, 18 (2): 61-66.
Resumen
Se estudiaron las exigencias térmicas de Amblyseius sp., alimentado con Tetranychus urticae en cinco temperaturas constantes (17, 20, 24, 27 y 31 ºC). Los estados de huevo, larva, protoninfa, deutoninfa y periodo de huevo a adulto presentaron temperaturas base de 12,6; 13,1; 11,6; 13,4 y 12,7ºC y constantes térmicas de 26,6; 10,2; 16,1; 13,3 y 66,1 ºD, respectivamente.
Palabras clave: ácaro, biología, constante térmica, fitoseido.
Abstract
Thermal requirements of Amblyseius sp. fed with Tetranychus urticae at five constant temperatures (17, 20, 24, 27 y 31ºC) were studied. The stages of egg, larva, protonymph, deutonymph and adult egg corresponded to temperature thresholds of 12,6; 13,1; 11,6; 13,4 and 12,7 ºC, and thermal constants of 26,6; 10,2; 16,1; 13,3 and 66,1 ºD, respectively.
Key words: mite, biology, thermal constant, phytoseiida
INTRODUCCIÓN
Los ácaros depredadores de la familia Phytoseiidae han recibido gran atención debido a su potencial como agente regulador de poblaciones de ácaros fitófagos (HELLE & SABELIS, 1985; MORAES, 2002; MORAES et al., 2004; SOTO et al., 2011) y pequeños insectos como moscas blancas y trips (ALI, 1998). En diversos países de Europa y América del Norte el control de ácaros fitófagos en invernadero ha sido comúnmente realizado a través de la liberación de ácaros depredadores de la familia Phytoseiidae (VASCONCELOS et al., 2004; ABAD-MOYANO et al., 2010; VAN LEEUWEN et al., 2010). Amblyseius californicus (Acari: Phytoseiidae) se introdujo en el Reino Unido a principios de 1990 como un agente de control biológico contra la araña roja de invernadero Tetranychus urticae (Acari: Tetranychidae) (HARTA et al., 2002). Amblyseius sp. puede presentar buenas perspectivas para el uso en el control biológico aplicado, en especial en condiciones de invernadero, sobre todo para floricultura y cultivo de hortalizas que ofrecen excelentes condiciones para el desarrollo de ácaros fitófagos en Colombia.
T. urticae es una de las principales plagas que ataca cultivos ocasionando pérdidas hasta del 80 % de la producción debido, principalmente, a su alto potencial reproductivo (CHIAVEGATO & MISCHAN, 1981; HELLE & SABELIS, 1985; FADINI & ALVARENGA, 1999; LANDEROS et al., 2004; ANTUNES et al., 2007; SIMÕES et al., 2007; MORAES & FLECHTMANN, 2008; SOTO et al., 2011). Para el control de este fitófago, los agricultores dependen casi exclusivamente de aplicaciones de agrotóxicos organosintéticos. La utilización excesiva e inadecuada de estos productos ha sido relacionada a problemas ecológicos, afectando organismos benéficos, promoviendo el desarrollo de resistencia a agrotóxicos y ocasionando riesgos para la salud de los agricultores y consumidores (GUERRA, 1985; SIBANDA et al., 2000; SAUNYAMA & KNAPP, 2003; PICANÇO et al., 2007).
Por otra parte, varios autores (ZALOM & WILSON, 1982; WILSON & BARNETT, 1983; ZALOM et al., 1983; CHIANG, 1985; GAGE & RUSSEL, 1991; SOTO et al., 2001) indican que la tasa de desarrollo de los artrópodos se basa en la acumulación de unidades calóricas, por lo que se mide en tiempo fisiológico y no cronológico. De acuerdo con CHIANG (1985), el rango óptimo de temperatura para los artrópodos se encuentra entre la temperatura umbral inferior y superior; fuera de este rango la actividad disminuye casi detenerse, sin que necesariamente cause la muerte. El mismo autor señala que la temperatura efectiva es la que se encuentra dentro de este rango y que la constante térmica, expresada en grados día (ºD), es la cantidad de calor que cada especie requiere para completar su ciclo o parte de él, independientemente de la temperatura a que sea expuesto. El conocimiento de los grados días provee una valiosa herramienta para el manejo de plagas tanto para predecir infestaciones como programar medidas de manejo o realizar monitoreo (BARRIENTOS et al., 1998, SOTO et al., 2001).
Existen diversos métodos para calcular la constante térmica (WILSON & BARNETT, 1983; SOTO et al., 1999). Uno de ellos es el método de la temperatura máxima y mínima, el cual consiste en restar la temperatura umbral inferior, o temperatura base, a la temperatura media diaria, mientras que el valor resultante se multiplica por los días que demora el desarrollo (BARRIENTOS et al., 1998; SOTO et al., 2001). El trabajo tuvo como objetivo determinar el periodo de los estados de desarrollo de Amblyseius sp, bajo cinco regímenes térmicos distintos, usando T. urticae como sustrato. Con esta información se calculó la temperatura base de desarrollo y los grados días acumulados (o constante térmica) para completar los estados de desarrollo del depredador. El conocimiento de estos requerimientos térmicos permite mejorar la cría masiva del depredador y de esta manera contribuir con al manejo racional de la plaga.
MATERIALES Y MÉTODOS
Las exigencias térmicas de Amblyseius sp. fueron estudiadas en el Laboratorio de Entomología de la Universidad de Caldas. El ácaro depredador fue obtenido de hojas de fresa (Fragaria x ananassa Duch) infestadas con T. urticae en la granja Tesorito de la misma universidad. La cría fue mantenida en laboratorio a 24 ± 5 ºC y humedad relativa de 70 ± 10 %, utilizando T. urticae como fuente de alimento. El método de cría consistió en sobreponer discos de espuma de polietileno, papel filtro y hojas de frijol infestadas con la presa, sobre una caja petri de 16 cm de diámetro, con agua destilada y circundada con algodón hidrófilo para evitar la fuga de los ácaros. Las hojas fueron renovadas semanalmente.
Biología de Amblyseius sp.
Hembras adultas de Amblyseius fueron transferidas de las colonias de cría a cinco cajas petri con discos de hojas de fríjol infestadas con T. urticae y mantenidas confinadas por 8 h. Después de ese período, las hembras fueron retiradas y los huevos utilizados para instalación del experimento, siendo cada caja petri sometida a las temperaturas constantes de 17, 20, 24, 27 y 31 ºC, humedad relativa de 70 ± 5 ºC y fotofase de 12 h en incubadora tipo B.O.D. Para determinación del tiempo de incubación, los huevos fueron observados cada 12 h. Después de la eclosión, las larvas fueron individualizadas en unidades de cría constituidas por cajas petri de 2,5 cm de diámetro y 1 cm de altura, con tapa que tenía un orificio de 1,5 cm de diámetro cubierto con tela, permitía el paso del aire. El fondo de cada caja petri fue forrado con disco de papel de filtro humedecido con agua destilada, sobre el cual fue colocado un disco de hoja de fríjol con huevos de T. urticae. Las evaluaciones fueron realizadas observándose el estado de desarrollo del ácaro en las unidades de cría cada 12 h.
Exigencias térmicas
Los grados días se calcularon mediante el método de la temperatura media; este método es considerado lineal y se basa en el supuesto de que la tasa de desarrollo es una línea recta, directamente, relacionada con la temperatura (WILSON & BARNETT, 1983). BARRIENTOS et al. (1985) mencionan que existe una relación, aproximadamente, lineal entre la tasa de desarrollo y la temperatura dentro de un rango de temperatura efectiva.Por lo tanto, la constante térmica (expresada en grados días) será la misma, aunque el tiempo variará para cada temperatura. Durante el desarrollo de cada estudio se registraron las temperaturas máximas y mínimas diarias para obtener la temperatura media. SOTO et al. (1999) indican que:
En donde K = constante térmica, n = días que demora el desarrollo, T = temperatura promedio del periodo y Tb = temperatura base. Considerando que la constante térmica es la misma para diversas condiciones de temperatura, finalmente, se puede escribir:
Dada la constancia de K y Tb para cada uno de los estados de desarrollo de Amblyseius sp. se contó con la información de ni en cinco datos de temperatura, mediante un análisis de regresión lineal de 1/ni en función de Ti.
RESULTADOS Y DISCUSIÓN
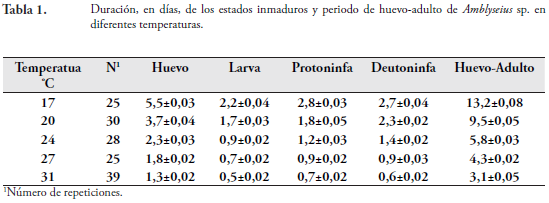
El tiempo medio de desarrollo de los estados inmaduros de Amblyseius disminuyó, progresivamente, con el aumento de la temperatura (Tabla 1). La duración de los estados de huevo, larva, protoninfa y deutoninfa variaron de 5,5 a 1,3; 2,2 a 0,5; 2,8 a 0,7; y 2,7 a 0,6 días, respectivamente, entre 17 y 31ºC (Tabla 1). En la temperatura de 17ºC la duración media de las fases inmaduras y el periodo de desarrollo fueron aproximadamente tres veces mayor que 31 ºC. La media del periodo de desarrollo varió de 13,2 días en la temperatura de 17ºC a 3,1 días 31ºC (Tabla 1).
ALI (1998) verificó la reducción del tiempo de desarrollo de Phytoseiulus macropilis (Acari: Phytoseiidae) con el aumento de la temperatura de 20ºC para 30 ºC, obteniendo resultados de 4,7 y 2,1 días para hembras, respectivamente. PRASAD (1967) evaluó el desarrollo de P. macropilis en la temperatura de 26 ºC, obteniendo resultados de 1,8; 0,5; 0,9 y 1,0 día para las fases de huevo, larva, protoninfa y deutoninfa, respectivamente. Estos resultados son similares a los obtenidos en el presente trabajo. Otros autores, como MORAES & McMURTRY (1981) y MESA & BELLOTI (1986), también verificaron la influencia del aumento de temperatura en la reducción de la duración de estados inmaduros de ácaros fitoseidos. KILINCER et al. (1996) verificaron que Phytoseiulus persimilis (Acari: Phytoseiidae) se desarrolla en 6,4 días en la temperatura de 23 ºC, con duración media del periodo de incubación y de los estados de larva, protoninfa y deutoninfa de 3,0; 0,9; 1,2 y 1,3 días, respectivamente, valores muy próximos a los encontrados en el presente trabajo para Amblyseius sp.
Las especies Amblyseius cucumeris y P. persimilis han sido muy utilizadas en diversos países de Europa y Estados Unidos en el control biológico de ácaros y pequeños insectos, en condiciones de invernadero, constituyendo una alternativa importante en el manejo integrado de plagas de flores y hortalizas (OSBORNE et al., 1985; NIHOUL, 1993; ZHANG & SANDERSON, 1995; KIM et al., 2001; MORAES, 2002).
La temperatura base (Tb) para las fases de huevo, larva, protoninfa, deutoninfa y periodo huevo a adulto fue de 14,5; 15,1; 13,6; 14,9 y 14,5 ºC, respectivamente (Tabla 2). La constante térmica (k) para los estados de huevo, larva, protoninfa, deutoninfa y huevo-adulto fue de 28,9; 10,4; 17,3, 12,2 y 68,8 grados día, respectivamente (Tabla 2).
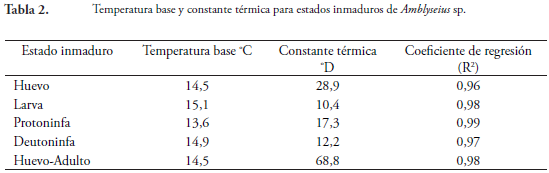
Los altos valores del coeficiente de regresión (R2) (Tabla 2), indican la gran influencia que ejerce la temperatura en la tasa de desarrollo de los estados inmaduros de Amblyseius sp.
BIBLIOGRAFÍA
ABAD-MOYANO, R., PINA, T., PEREZ-PANEDES, J., CARBONELL, E.A. & URBANEJA, A., 2010.- Efficacy of Neoseiulus californicus and Phytoseiulus persimilis in suppression of Tetranychus urticae in young Clementine plants. Experimental and Applied Acarology., 50: 317-328. [ Links ]
ALI, F.S., 1998.- Life tables of Phytoseiulus macropilis (Banks) (Gamasida: Phytoseiidae) at different temperatures. Experimental Applied Acarology, 22: 335-342. [ Links ]
ANTUNES, L.E.C., DUARTE FILHO, J., CALEGARIO, F.F., COSTA, H. & JÚNIOR, C.R., 2007.- Produção integrada de morango (PIMo) no Brasil. Informe Agropecuário, Belo Horizonte, 28 (236): 34-39. [ Links ]
BARRIENTOS, R., APABLAZA, J., NORERO, A. & ESTAY, P., 1998.- Temperatura base y constante térmica de desarrollo de la polilla del tomate, Tuta absoluta (Lepidoptera: Gelechiidae). Ciencia e Investigación Agraria, 25: 133-13. [ Links ]
CHIANG, H.C., 1985.- Insects and their Environment: 128-161 (en) PFAD, R.E. (ed). Fundamentals of Applied Entomology. Macmillan Publishing Company, New York. [ Links ]
FADINI, M.A.M. & ALVARENGA, D., 1999.- Pragas do morangueiro. Informe Agropecuário, Belo Horizonte., 20 (198): 75-79. [ Links ]
FERRAGUT, F. & ESCUDERO, L.A., 2002.- La araña roja del tomate Tetranychus evansi (Acari: Tetranychidae) en España: distribución, biología y control. Phytoma España, 25: 11-113. [ Links ]
GAGE, S.H. & RUSSELL, H.L., 1991.- Pest surveillance systems in the USA. A case study using the Michigan, crop monitoring system (209-223). Crop Loss Assessment and Pest Management., APS Press Minnesota. [ Links ]
GUERRA, M.S., 1985.- Receituário caseiro: alternativa para o controle de pragas e doenças de plantas cultivadas e seus produtos. EMATER, Brasília. [ Links ]
HARTA, A.J., BALEA, J.S., TULLETTA, A.G., WORLANDB, M.R. & WALTERSC, K.F.A., 2002-. Effects of temperature on the establishment potential of the predatory mite Amblyseius californicus McGregor (Acari: Phytoseiidae) in the UK. Journal of Insect Physiology., 6 (48): 593-599. [ Links ]
HELLE, W. & SABELIS, M.W., 1985.- Spider mites: their biology, natural enemies and control. Elsevier, Amsterdam. [ Links ]
KILINCER, N., COBANOGLU, S. & HASS, A., 1996.- Biological characteristics and consumption capacity of the predatory mite Phytoseiulus persimilis Athias-Henriot (Acarina: Phytoseiidae). J. Agric., 20 (2): 107-11. [ Links ]
KIM, J., BROADBENT, B. & GUEI, S., 2001.- Control of the Mass-Reared Predatory Mite, Amblyseius cucumeris (Acarina: Phytoseiidae). J. Asia-Pacific Entomol., 4 (2): 175-179. [ Links ]
LANDEROS, J., GUEVARA, L.P., BADDI, M.H., FLORES, F. & PÁMANES, A., 2004.- Effect of different densities of the twospotted spider mite Tetranychus urticae on CO2 assimilation, transpiration and stomatal behavior in rose leaves. Exp. Appl. Acarology., 32: 187-198. [ Links ]
MESA, N.C. & BELLOTI, A.C., 1986.- Ciclo de vida y hábitos alimenticios de Neoseiulus anonymus, predador de ácaros Tetranychidae en yuca. Rev. Colom. Entomol., 12: 54-60. [ Links ]
MORAES, G.J. & FLECHTMANN, C.H.W., 2008.- Manual de Acarologia: acarologia básica e ácaros de plantas cultivadas no Brasil. Holos., Ribeirão Preto . [ Links ]
MORAES, G.J. & McMURTRY, J.A., 1986.- Suitability of the spider mite Tetranychus evansi as prey for Phytoseiulus persimilis. Entomologia Experimentalis et Applicata., 40: 109-115. [ Links ]
MORAES, G.J., 2002.- Controle biológico de ácaro fitófagos com predadores: 225-237 (en) PARRA, J.P.R., BOTELHO, P.S.M., CORREA-FERREIRA, B.S. & BENTO, J.M.S. (eds.). Controle biologico no Brasil: Parasitoides e predadores. São Paulo, Manole., 635p. [ Links ]
MORAES, G.J., McMURTRY, J.A., DENMARK, H.A. & CAMPOS, C.B., 2004.- A revised catalog of the mite family Phytoseiidae. Zootaxa, 434: 1-49. [ Links ]
NIHOUL, P., 1993.- Controlling glasshouse climate influences the interaction between tomato glandular trichome, spider mite and predatory mite. Crop Prot., 12: 443-44. [ Links ]
OSBORNE, L.S., EHLER, L.E. & NECHOLS, J.R., 1985.- Biological control of the twospotted spider mite in greenhouses. Bulletin 853. Institute of Food and Agricultural Services, University of Florida, Gainesville. [ Links ]
PICANÇO, M.C., SOTO, A., BACCI, L.,FIDELIS, E.G., SILVA, G.A. & DE SENA, M.E., 2007.- Controle biológico das principais pragas de hortaliças no Brasil: 507-537 ZAMBOLIM, L. (ed.). Manejo integrado de doenças e pragas hortaliças. UFV, Viçosa. [ Links ]
PRASAD, V., 1967.- Biology of the predatory mite Phytoseiulus macropilis in: Hawaii (Acarina: Phytoseiidae). Ann. Entomol. Soc. Am., 60: 905-909. [ Links ]
SAUNYAMA, I.G.M. & KNAPP, M., 2003.- The effects of pruning and trellising of tomatoes (Lycopersicon esculentum Mill.) on red spider mite (Tetranychus evansi Baker & Pritchard) incidence and crop yield in Zimbabwe. African Crop Science Journal, 11: 269-277. [ Links ]
SIBANDA, T.,DOBSON, H.M.,COOPER, J.F.,MANYANGARIWA, W. & CHIIMBA, W., 2000.- Pest management challenges for smallholder vegetable farmers in Zimbabwe. Crop Protection, 19: 807-815. [ Links ]
SIMÕES, J.C., FADINI, M.A.M. & VENZON, M., 2007.- Manejo integrado de pragas na cultura do morangueiro. Informe Agropecuário, Belo Horizonte, 28 (236): 56-63. [ Links ]
SOTO, A., APABLAZA, J., NORERO, A. & ESTAY, P., 1999.- Requerimientos térmicos de Trialeurodes vaporariorum (Hemiptera: Aleyrodidae) en tomate (Lycopersicom esculentum). Ciencia e Investigación Agraria., 26: 37-45. [ Links ]
SOTO, A., APABLAZA, J., NORERO, A. & ESTAY, P., 2001.- Requerimientos térmicos para el desarrollo de Encarsia formosa (Hymenoptera: Aphelinidae) criado en Trialeurodes vaporariorum (Hemiptera: Aleyrodidae). Ciencia e Investigación Agraria., 28: 103-109. [ Links ]
SOTO, A., VENZON, M. & PALLINI, A., 2011.- Integración de control biológico y de productos alternativos contra Tetranychus urticae (Acari: Tetranychidae). Revista U.D.C.A. Actualidad y Divulgación Científica., 14 (1): 23-29. [ Links ]
SOTO, A., VENZON, M., OLIVEIRA, R., OLIVEIRA, H. & PALLINI, A., 2010.- Alternative control of Tetranychus evansi Baker & Pritchard (Acari: Tetranychidae) on tomato plants grown in greenhouses. Neotropical Entomology, 39 (4): 363-368. [ Links ]
VAN LEEUWEN, T., WITTERS, J., NAUEN, R., DUSO, C. & TIRRI, D., 2010.- The control of eriophyoid mites: State of the art and future challenges. Experimental and Applied Acarology., 46: 3-6. [ Links ]
VASCONCELOS. J.N., DA SILVA, F., GONDIM, M., BARROS, R. & OLIVEIRA, J., 2004.- Efeito de diferentes temperaturas no desenvolvimento e reprodução de Tetranychus abacae Baker & Printchard (Acari: Tetranychidae) em bananeira Musa sp. Cv. Prata. Neotropical Entomology., 33 (2): 149-154. [ Links ]
WILSON, L. & BARNETT, W., 1983.- Degree-days an aid in crop and pest management. California Agriculture., 37: 4-7. [ Links ]
ZALOM, F. & WILSON, T., 1982.- Degree days in relation to and integrated pest management program. University of California, Davis, CA, USA. 2pp. [ Links ]
ZALOM, F., GOODELL. P., WILSON, L., BARNETT, W. & BENTLEY, W., 1983.- Degree-days: the calculation and use of heat unit in pest management. University of California, Davis, C.A, USA. [ Links ]
ZHANG, Z.Q. & SANDERSON, J.P., 1995.- Twospotted spider mite (Acari: Tetranychidae) and Phytoseiulus persimilis (Acari: Phytoseiidae) on greenhouse roses: Spatial distribution and predator efficacy. J. Econ. Entomol. 88: 352-35. [ Links ]













