Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Boletín Científico. Centro de Museos. Museo de Historia Natural
versión impresa ISSN 0123-3068
Bol. Cient. Mus. Hist. Nat. Univ. Caldas vol.20 no.1 Manizales ene./jun. 2016
https://doi.org/10.17151/bccm.2016.20.1.7
DOI: 10.17151/bccm.2016.20.1.7
ESCARABAJOS COPRO-NECRÓFAGOS (SCARABAEIDAE: SCARABAEINAE) EN DIFERENTES USOS DEL SUELO EN LA RESERVA CAMPESINA LA MONTA ÑA (RCM) EN EL DEPARTAMENTO DEL ATLÁNTICO, COLOMBIA*
COPRO-NECROPHAGOUS BEETLES (SCARABAEIDAE: SCARABAEINAE) IN DIFFERENT LAND USE AT LA RESERVA CAMPESINA LA MONTA ÑA (RCM) IN THE DEPARMENT OF ATLÁNTICO, COLOMBIA.
* FR: 15-II-2016. FA: 30-IX-2016.
1 Semillero de Investigación de artrópodos del Caribe colombiano NEOPTERA, Grupo Biodiversidad del Caribe colombiano. Maestría en Biología, Facultad de Ciencias Básicas, Universidad del Atlántico. Ciudadela Universitaria, Km 7-Vía Puerto Colombia. Barranquilla, Colombia. rangelacosta@gmail.com
2 Grupo de Investigación Biodiversidad del Caribe colombiano. Programa de Biología, Facultad de Ciencias Básicas, Universidad del Atlántico. Ciudadela Universitaria, Km 7- Vía Puerto Colombia. Barranquilla, Colombia. neyjosemartinez@gmail.com
3 Estudiante Doctorado en Ciencias-Biología. Departamento de Biología, Universidad Nacional de Colombia-Sede Bogotá.
CÓMO CITAR:
RANGEL-ACOSTA, J.L., BLANCO-RODRÍGUEZ O.R. & MARTÍNEZ-HERNÁNDEZ N.J., 2016.- Escarabajos copro-necrófagos (Scarabaeidae: Scarabaeinae) en diferentes usos del suelo en la reserva campesina La Montaña (RCM) en el departamento del Atlántico, Colombia. Bol. Cient. Mus. Hist. Nat. U. de Caldas, 20 (1): 78-97. DOI : 10.17151/bccm.2016.20.1.7
Resumen
Se analizó la variación espacio-temporal de los ensamblajes de escarabajos coprófagos (Scarabaeinae) en diferentes usos del suelo (cultivo, potrero, borde e interior del bosque) en la Reserva Campesina La Montaña (RCM) entre las épocas de lluvias y seca de 2009 y 2010. En cada uso del suelo fue ubicado un transecto lineal, donde se marcaron 10 puntos distanciados 50 m, instalándose en cada uno una trampa de caída cebada con una mezcla de excremento de humano, mono (Alouatta seniculus) y pescado en descomposición. Se capturaron 15.636 individuos, agrupados en 12 géneros y 24 especies, de las cuales las más abundantes fueron Canthonaff. morsei y Uroxys deavilai con 7.292 y 3.465 individuos respectivamente, aportando el 69% de la abundancia capturada para el área de estudio. Los valores más altos de riqueza fueron observados durante las lluvias de 2009 y 2010 en todos los hábitats (14-20 especies) y los más bajos en cultivo y potrero en la época seca (7 especies). Con el análisis no métrico multidimensional (nMDS), se determinó que el fragmento de bosque y el borde forman un grupo homogéneo en cuanto a composición de especies que difiere al cultivo y potrero. Se demuestra que estos dos últimos hábitats mantienen un alto número de especies de Scarabaeinae en periodos de lluvias, aunque en la época seca la riqueza y diversidad se reduce drásticamente, evidenciándose que los escarabajos los utilizan de manera estacional.
Palabras clave: Reserva Campesina La Montaña, usos del suelo, Canthon aff. morsei, época seca, fragmento de bosque.
Abstract
The spatio-temporal variation of dung beetles (Scarabaeinae) assemblages in different land use (culture, pasture, edge and interior of forest) at La Reserva Campesina La Montaña (RCM) during the rainy and the dry season in 2009-2010 was analized. For each land use was located a linear transect, where 10 points distanced 50 m each other were marked; with pitfall traps bait human and monkey (Alouatta seniculus) excrement and decaying fish placed in each point. 15.636 individuals distributed in 12 genera and 24 species were captured, of which the most abundant were Canthonaff. morsei and Uroxys deavilai with 3,465 and 7.292 individuals respectively, accounting for 69% of the total abundance for the study area. The highest values of richness were observed during the rainy season in 2009-2010 in all habitats (14-20 species) and the lowest during the dry season (7 species) at culture and pasture. With the non-metric multidimensional analysis (nMDS) was determined that the fragment forest and edge are part of a homogeneous group in terms of species composition that differs to the culture and pasture. It is shown that these last two habitats maintain a high number of species of Scarabaeinae during the rainy season, although during the dry season the richness and diversity is reduced drastically, demonstrating that dung beetles use them seasonally.
Key words: Reserva Campesina La Montaña, land use, Canthonaff. morsei, dry season, forest fragment.
INTRODUCCIÓN
El bosque seco tropical (BST) es uno de los ecosistemas más amenazados y menos conocidos dentro de los bosques tropicales (PORTILLO-QUINTERO & SÁNCHEZ-AZOFEIFA, 2010; DIRZO et al., 2011; GARCÍA et al., 2014). Cerca del 48.5% del BST ha sido transformado para implementación de cultivos, fincas ganaderas y establecimientos de poblaciones humanas, reduciendo así su extensión. El área actual de este ecosistema para América es de 519,597 km2, de las cuales el 51% (268,875 km2) hacen parte de Sudamérica (PORTILLO-QUINTERO & SÁNCHEZ-AZOFEIFA, 2010). Para Colombia, de la cobertura original de BST solo queda el 8% (717,226 ha); de las cuales 3.7% son fragmentos de bosques en estado natural y el restante corresponde a pequeños parches que se encuentran en áreas de intenso uso ganadero y agrícola (GARCÍA et al., 2014).
Aunque los trabajos para el conocimiento del funcionamiento del BST han aumentado (ver PIZANO & GARCÍA, 2014), hay algunos temas que aún quedan por explorar a fondo; uno de los cuales es el rol de los cultivos, potreros y cercas vivas en la conservación de la diversidad biológica. Uno de los grupos utilizados para responder preguntas sobre el aporte de los sistemas productivos en la conservación de la biodiversidad son los escarabajos coprófagos de la subfamilia Scarabaeinae. Estos insectos son un taxón focal muy usado, debido a su fragilidad a los cambios en la estructura de la vegetación de los bosques, la disposición de recursos y a las alteraciones de las variables climáticas productos de la fragmentación (HALFFTER & FAVILA, 1993; FAVILA & HALFFTER, 1997; SPECTOR, 2006; NICHOLS et al., 2007; GARDNER et al., 2008).
Aunque la conversión del BST a zonas de uso ganadero y agrícola es acelerada, la información que se tiene sobre cómo estas áreas contribuyen al mantenimiento y conservación de la diversidad de escarabajos coprófagos en el país es poca (NORIEGA et al., 2015); destacándose los trabajos realizados por BUSTO-GÓMEZ & LOPERA (2003), BARRAZA et al. (2010), NAVARRO et al. (2011) y DELGADO-GÓMEZ et al. (2012). Estos autores demostraron que la fragmentación del BST para implementación de sistemas productivos produce cambios en la composición y estructura de escarabajos coprófagos, observándose una mayor riqueza y diversidad en los fragmentos de bosques, la cual disminuye hacia los hábitats de uso humano. Es probable que la situación encontrada por estos autores sea similar para el departamento del Atlántico, donde la fragmentación del BST ha dejado como resultados fragmentos de bosques inmersos en matrices de uso ganadero y agrícola. Teniendo en cuenta lo anterior nosotros planteamos que independientemente de las épocas de muestreos, los fragmentos de bosque presentan un mayor número de especies y abundancia de escarabajos coprófagos que los potreros, cultivos y borde del bosque; debido a que este ofrece mayor variedad de recursos y condiciones microclimáticas que favorecen el mantenimiento de las poblaciones de estos insectos.
Teniendo en cuenta lo anterior, se evaluó la variación espacio-temporal de los ensamblajes de escarabajos coprófagos en diferentes usos del suelo en la Reserva Campesina La Montaña (RCM), Atlántico, Colombia.
MATERIALES Y MÉTODOS
Área de estudio
La RCM se encuentra ubicada en el municipio de Juan de Acosta, Atlántico, Colombia (Figura 1). Está localizada a 10°46'02,6" N y 75°02'34"; a una altitud que oscila entre 177 y 250m. El área cuenta con una extensión de 365 ha, de las cuales 47 están ocupadas por un fragmento de bosque seco, el cual fue declarado en categoría de zona de reserva campesina (GARCÍA-ATENCIA & MARTÍNEZ-HERNÁNDEZ, 2015). Las hectáreas restantes están distribuidas en pequeñas parcelas rodeadas por cercas vivas, dedicadas a la siembra de policultivos de maíz (Zea mays L.), yuca (Manihot esculenta C.), patilla (Citrullus lanatus M y N.), auyama (Cucurbita moschata D.), sorgo (Sorghum vulgare M.), habichuela (Phaseolus vulgaris L.) y gandul (Cajanus cajan H.) y zona de pastoreo de ganado bovino, equino y caprino (GARCÍA-ATENCIA & MARTÍNEZ-HERNÁNDEZ, 2015).
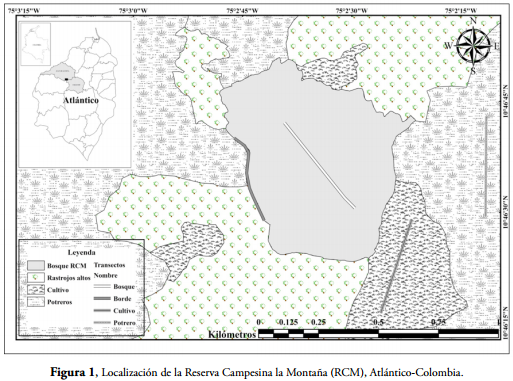
Las zonas hacen parte de una formación higrotropofítica correspondiente a un BST y de acuerdo con BERDUGO-LATKE et al. (2012) estas áreas corresponden a bosques secos dominados por especies de plantas como Hura crepitans L. y Terminalia amazonia L. Teniendo en cuenta la clasificación climática propuesta por RANGEL-CH & CARVAJAL-COGOLLO (2012) para la región Caribe, la reserva está dentro de la unidad climática A, subunidad climática A1 (DS2A zonas semiáridas con marcada deficiencia de agua durante la época seca), donde se presentan montos de precipitaciones anuales de 911 mm. Los meses que presentan la mayor precipitación corresponden a agosto y septiembre (100-580 mm/mes) y enero, febrero y marzo figuran como los de menor precipitación (0-30 mm/mes). La temperatura promedio es de 27.6°C y humedad relativa promedio es de 62 % con pocas variaciones a lo largo del año (GARCÍA-ATENCIA & MARTÍNEZ-HERNÁNDEZ, 2015).
Métodos de muestreo y técnicas de captura
En el área de estudio fueron seleccionados cuatro diferentes usos del suelo: cultivo (Cul), potrero (Pot), borde del fragmento (Bor) y un fragmento de BST (I.B). Se realizó un muestreo mensual en cada hábitat, entre octubre de 2009 y septiembre de 2010, con el fin de abarcar los meses de mayor y menor precipitación. En cada hábitat se marcó un transecto lineal de 450m, donde se marcaron 10 puntos distanciados 50 m. En cada uno se instaló una trampa pitfall (trampa de caída) con modificaciones descritas por MARTÍNEZ et al. (2009), las cuales fueron cebadas con una mezcla de excremento humano, mono (Alouatta seniculus) y pescado en descomposición y permanecieron en campo durante 24 horas. Para el transecto del borde, las trampas fueron colocadas en zigzag, de forma que una trampa era ubicada a cinco metros dentro del bosque y la siguiente a cinco metros fuera de este. La distancia mínima entre transectos fue de 600 m y la máxima de 1,5 Km.
Adicionalmente, en cada punto se midieron variables como humedad ambiente y del suelo (%), temperatura ambiente y del suelo (°C) y pH del suelo; así como la precipitación (mm) con un pluviómetro marca Hellman. Teniendo en cuenta los datos de precipitación en el área de estudio, se estableció que los meses de mayor precipitación fueron octubre y noviembre de 2009 (Lluvias 2009) y marzo, abril, mayo, junio, julio, agosto y septiembre de 2010 (Lluvias 2010), con valores de precipitación mayor a 50 mm; y los meses con menor precipitación (época seca), fueron diciembre (2009) y enero-febrero (2010) con valores inferiores a 50mm.
Las determinaciones fueron realizadas con las claves taxonómicas propuestas por MEDINA & LOPERA (2000) y VAZ-DE-MELLO et al. (2011) hasta el nivel de género y hasta especies con las claves propuestas por KOHLMANN & SOLÍS-BLANCO (1997, 2001), VÍTOLO (2000), SOLÍS-BLANCO & KOHLMANN (2002, 2004), DELGADO & KOHLMANN (2007), GÉNIER (2009), GONZÁLEZ et al. (2009) y EDMONDS & ZÍDEK (2010). La confirmación de las especies se realizó con la colección entomológica del Instituto de Investigaciones Alexander von Humboldt (IAvH). Los ejemplares de cada especie reposan en la colección de referencia de la Universidad del Atlántico (UARC) y la colección entomológica del IAvH.
Análisis de los datos
La riqueza se determinó como el número de especies y la abundancia como el número de individuos recolectados por hábitats y época de muestreo. Para establecer si existe un patrón espacio-temporal de la riqueza y diversidad de escarabajos entre los diferentes usos del suelo, se utilizó un análisis de interpolación y extrapolación propuesto por CHAO et al. (2014), utilizando los números de Hill (HILL, 1973) en unidades del número efectivo de especies siguiendo lo propuesto por JOST (2006). Los órdenes de la diversidad evaluados fueron: OD (riqueza especies), 1D (el exponencial del índice de Shannon) y 2D (el inverso del índice de Simpson). OD no es sensible a la abundancia y tiene en cuenta la presencia de las especies raras. 1D otorga un peso proporcional a las especies teniendo en cuenta su abundancia, por lo tanto puede ser interpretado como el número de especies "comunes" o "típicas" en la comunidad, mientras que 2D puede ser interpretado como el número de especies "muy abundantes" o "dominantes" en la comunidad (JOST, 2006). La diversidad calculada fue comparada usando los intervalos de confianza del 95% (p<0.05) y realizando una comparación visual basada en la superposición de los intervalos de confianza para establecer si existen diferencias entre el fragmento de bosque seco con los otros usos del suelo, durante las épocas de muestreos. El análisis fue realizado con el script iNEXT para R Studios (CHAO et al., 2014) y ejecutado en el programa R versión 3.1.1 (R Development Core Team 2014).
Con el fin de observar la distribución espacial y temporal de la composición de Scarabaeinae en los diferentes usos del suelo, fue realizado un análisis de escalamiento multidimensional no-métrico (nMDS). Para realizar este análisis se utilizó el índice de disimilitud de Bray-Curtis, debido a que sirve para encontrar relaciones de disimilitud entre sitios y distancias ecológicas entre especies (FAITH et al., 1987). El rango de este índice está entre cero (0) y uno (1), donde 0 significa que los dos sitios tienen la misma composición y 1 significa que los dos sitios no comparten ninguna especie. Este análisis fue realizado con el programa R, utilizando los paquetes MASS (VENABLES & RIPLEY, 2002) y VEGAN (OKSANEN et al., 2007). Para determinar si los agrupamientos observados en el nMDS presentan diferencias, se utilizó un ANOSIM a una vía (análisis de similitud), el cual permite detectar diferencias en composición de especies entre grupos y dentro de cada uno, mediante permutaciones realizadas a la matriz original (CLARKE & WARWICK, 2001). Por otro lado, considerando a las especies que aportaron más del 10% de la abundancia total, se determinaron las especies que caracterizaron los hábitats y las épocas según su abundancia rutina SIMPER (porcentajes de similaridades). Para realizar estos análisis se utilizó el programa PRIMER 6.0 (CLARKE & WARWICK, 2001).
Los coleópteros capturados fueron agrupados según la relocalización del alimento, según lo propuesto por DOUBE (1990) en tres grupos: rodadores (R), cavadores (C) y residentes o endocópridos (E) y según el tamaño en pequeños (P) (menor a 10mm) y grandes (G) (mayor a 10 mm) según lo descrito por ESCOBAR (2004). Después de la agrupación por tamaño y método de relocalización del alimento de los escarabajos, se aplicó una ANOVA de Kruskal-Wallis con el fin de establecer si existen cambios en la composición de gremios entre hábitats.
Para determinar el posible efecto de las variables abióticas (humedad del suelo y relativa ambiental, pH, precipitación, temperatura ambiental y del suelo) sobre los cambios de la composición y estructura de los escarabajos copronecrófagos en hábitats y épocas, se empleó un análisis de correspondencia canónica (ACC) con ayuda del programa R y los paquetes MASS (VENABLES & RIPLEY, 2002) y VEGAN (OKSANEN et al., 2007).
RESULTADOS
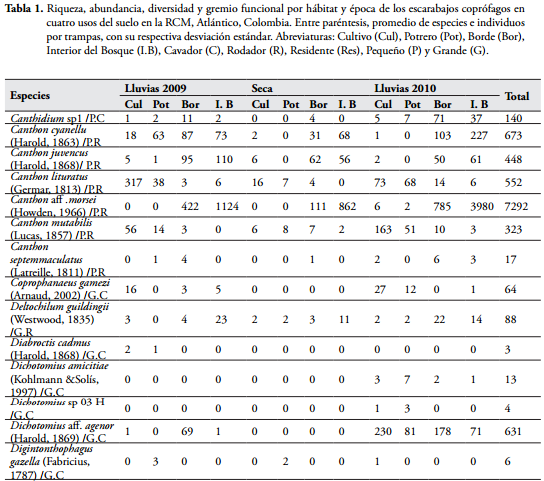
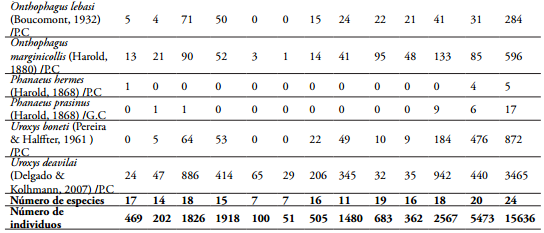
Se capturaron 15.636 individuos agrupados en 12 géneros y 24 especies (Tabla 1). El género que presentó mayor riqueza fue Canthon Hoffmansegg (1817) con seis especies, lo que corresponde al 25% de la riqueza capturada (Tabla 1). Las especies más abundantes fueron Canthonaff. morsei Howden (1966) con 7.292 individuos y Uroxys deavilai Delgado & Kolhmann (2007) con 3.465 individuos, las cuales aportaron el 69% de la abundancia capturada para el área de estudio. La especie C. aff. morsei presentó su mayor pico de abundancia (1.082 individuos) en el interior del fragmento de bosque, mientras que U. deavilai presentó su mayor valor (548 individuos) en el borde del bosque durante la época de lluvias. Las especies menos abundantes fueron Diabroctis cadmus Harold (1868), Dichotomius sp 03 H, Digintonthophagus gazella Fabricius (1787), Malagoniella astyanax (Olivier, 1789) y Phanaeus hermes Harold (1868), las cuales no superaron los diez individuos y solo aportan 0.15% de la abundancia total capturada para el área (Tabla 1).
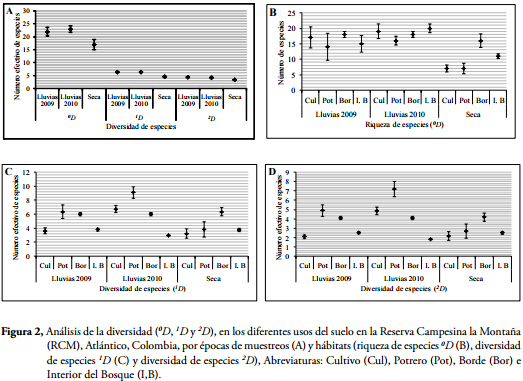
Con el análisis de interpolación y extrapolación se determinó que se obtuvo una completitud del inventario de escarabajos coprófagos en un 100% para la RCM (observadas=24, Chao 1=24). Con este análisis se observó que los mayores valores de riqueza OD (23 especies) y diversidad 1D (6,3 especies efectivas) y 2D (4,2 especies efectivas) se presentaron durante la época de lluvias y los menores durante la época seca (OD=17 especies, 1D=4,5 y 2D= 3,2 especies efectivas) (Figura 2A). Al realizar las comparaciones de los intervalos de confianza al 95%, se determinó que la riqueza y diversidad de especies no presentó diferencias significativas (p>0.05) entre los periodos de lluvias de 2009 y 2010, mientras que estos sí presentaron diferencias con la época seca (Figura 2A).
Con respecto a los hábitats, la mayor riqueza (OD) de especies se observó para interior del bosque durante el periodo de lluvias de 2010 (20 especies) y la menor para época seca para cultivo y potrero con siete especies cada uno. Las comparaciones (intervalo de confianza al 95%) muestran que aunque la riqueza es alta para el interior del bosque en el periodo de lluvias de 2010, esta no difiere con la observada para los otros hábitats tanto para el 2009 y 2010; pero sí son diferentes a los observados para la época seca. Este análisis también muestra que para el periodo seco, la riqueza disminuye drásticamente en todos los hábitats de la RCM, siendo más evidente en el cultivo y el potrero donde desciende hasta el 74% con respecto a la época de lluvias. Sin embargo, hábitats como el borde del bosque exhiben altos números de especies, lo cual fue significativamente mayor a los otros sitios de muestreos durante la época seca (Figura 2B).
Con respecto a la diversidad de especies (1D y 2D), los mayores valores fueron observados en el potrero durante las lluvias de 2010 (1D= 9 y 2D= 7 especies efectivas), mientras que los más bajos se presentaron en el interior del bosque para el mismo periodo (1D =3 y 2D =1.8 especies efectivas) (Figura 2C y 2D). Los altos valores de diversidad observados en potrero presentaron diferencias significativas con los otros hábitats de la RCM, independiente de la época de muestreo.
Con el análisis nMDS, se demostró la formación de grupos que presentan diferencias en composición de especies en cuanto a las épocas de muestreo. El primero formado por el periodo seco y el segundo conformado por los periodos de lluvias de 2009 y 2010. Este segundo grupo presenta un mayor número de especies asociadas que los periodos secos (Figura 3A). En relación con los hábitats, con el nMDS se demuestra que el borde y fragmento de bosque presenta una composición de especies muy similar, pero que difiere a la del potrero y cultivo; estos dos últimos también son altamente homogéneos en cuanto a composición. Este análisis permitió observar que especies como U. deavilai, D. aff. agenor, C. gamezi, C. mutabilis, C. lituratus y E. impresicollis están asociados a hábitats de uso humano como cultivos y potreros; mientras que C. aff. morsei, U. boneti, C. septemmaculatus, C. cyanellus, C. juvencus, E. mexicanus y P. prasinus están asociados a áreas con un mayor grado de cobertura vegetal como el borde y el interior del fragmento (Figura 3B).
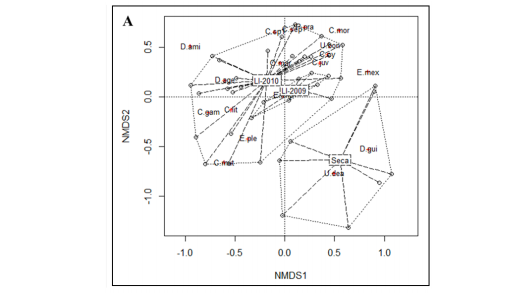
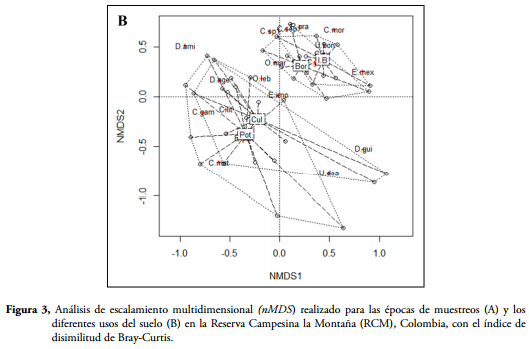
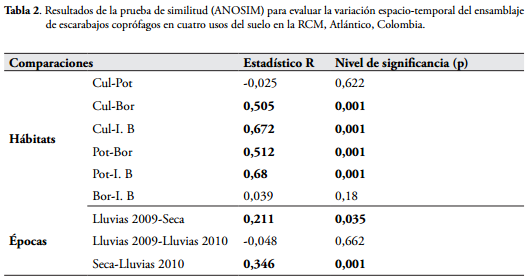
Con la prueba del análisis de similitud (ANOSIM), se demostró que existen diferencias en la estructura de la comunidad entre las épocas de muestreos (R=0,196; p=0,008). Los periodos de lluvias (2009 y 2010) presentaron diferencias con la época seca. En cuanto a los diferentes usos del suelo, se determinaron diferencias significativas en la estructura de la comunidad (R= 0,394; p= 0,001). El interior de bosque y el borde no mostraron diferencias, al igual que potrero con cultivo; mientras que los dos primeros hábitats sí mostraron diferencias con los dos últimos (Tabla 2).
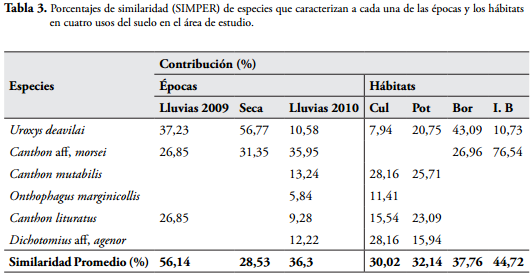
Con la rutina de similaridad (SIMPER), se determinó que la especie U. deavilai estuvo presente en todas las épocas de muestreos y en todos los usos del suelo de la RCM; mientras que C. aff. morsei está presente en todas las épocas de muestreos, pero restringido al borde e interior del fragmento. Con esta rutina también se determinó que C. mutabilis, C. lituratus y O. marginicollis están presentes en cultivo y potrero durante las épocas de lluvias 2009-2010 (Tabla 3).
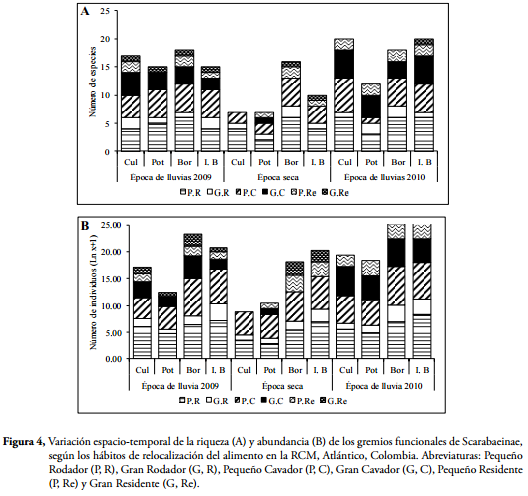
En cuanto a los gremios, los pequeños rodadores y pequeños cavadores presentaron altos valores de riqueza en todos los hábitats sin discriminar la época; caso contrario se observó con los grandes cavadores y rodadores, los cuales mostraron una marcada estacionalidad debido a que solo fueron capturados en las épocas de lluvias en todos los hábitats de la RCM. Por otra parte, se resalta la baja presencia de especies e individuos del gremio pequeños y grandes residentes (Figura 4A). Este comportamiento fue similar tanto para la riqueza como para la abundancia (Figura 4A y 4B). Por último, con la prueba de Kruskal-Wallis se determinó que no existen diferencias en la riqueza (H=10,27; p=0,473) y abundancias (H=11,72; p=0,38) de gremios entre hábitats.
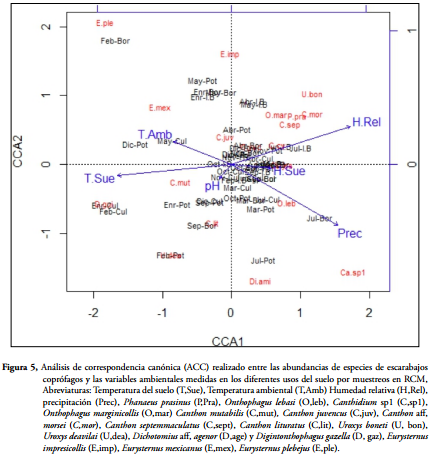
Con el análisis de correspondencia canónica (ACC), se determinó que las variables ambientales medidas explican el 73% de la variación de la comunidad de escarabajos coprófagos en la RCM. Lo anterior se encuentra representado en tres ejes canónicos, de los cuales el primero explica un 34%, el segundo el 21% y el tercero un 18%. En el eje uno, las variables que más aportan a la variación son humedad relativa (0,8848), temperatura del suelo (-0,8474), precipitación (0,7925) y temperatura ambiente (-0,4308). En el eje dos, la variable que más aporta es la precipitación (-0,4511) y en el tercer eje la humedad del suelo (-0,8151) y el pH (0.5014).
Figura 4, Variación espacio-temporal de la riqueza (A) y abundancia (B) de los gremios funcionales de Scarabaeinae, según los hábitos de relocalización del alimento en la RCM, Atlántico, Colombia. Abreviaturas: Pequeño Rodador (P, R), Gran Rodador (G, R), Pequeño Cavador (P, C), Gran Cavador (G, C), Pequeño Residente (P, Re) y Gran Residente (G, Re).
Con el análisis de varianza (ANOVA), se determinó que la variación explicada en el ACC fue significativa (F= 1,551; p= 0,011). Sin embargo, solo las variaciones observadas en el eje uno (F=3,200; p=0,05) y dos (1,952; p=0,015) resultaron significativas. En cuanto a las variables, solo la temperatura del suelo (F=2,685; p=0,002) y la precipitación (F=1,823; p=0,02) pueden explicar la variación del ensamblaje de escarabajos en la RCM. Este análisis también permitió observar que especies como C. morsei, U. boneti, C. septemmaculatus, O. marginicollis y P. prasinus se encuentran correlacionadas con el aumento de la humedad relativa y asociada a sitios como interior del bosque durante las lluvias. Caso contrario sucede con C. lituratus y C. mutabilis, las cuales parecen ser poco afectadas por las condiciones ambientales del cultivo y potrero, haciendo presencia durante las lluvias (Figura 5).
DISCUSIONES
El número de especies reportadas en este estudio corresponde al 34% y 8% de los géneros y especies, reportados por MEDINA et al. (2001) para Colombia. En la escala local, se recolectaron el 92% y 68% de las especies reportadas por MARTÍNEZ et al. (2010) y SOLÍS et al. (2011) respectivamente para fragmentos de BST en el Atlántico. Estos resultados demuestran que los parches de bosques con vegetación nativa inmersos en matrices de uso ganadero y agrícola, así como los potreros y cultivos aledaños a estos contribuyen a mantener una fauna representativa de Scarabaeinae en las tierras bajas del Caribe que anteriormente eran dominadas por grandes extensiones de BST.
En cuanto a lo espacio-temporal, se observó que la riqueza de especies fue similar en los diferentes usos del suelo durante los periodos de lluvias. Es posible que este comportamiento obedezca a la cercanía entre los lugares y a la similitud en las condiciones ambientales (humedad y temperatura ambiente, humedad y temperatura del suelo) durante este periodo en los cuatro hábitats. Lo anterior puede favorecer el desplazamiento de las especies de escarabajos desde el interior del bosque hacía las zonas abiertas, donde hay una mayor cantidad de excrementos de mamíferos introducidos. Por otro lado, los altos valores de riqueza observados en la época de lluvias con respecto a seca, está relacionado con el efecto que causan las precipitaciones; la cual es una variable muy importante en el desarrollo del ciclo de vida y los cambios temporales de estos insectos, así como su incidencia en los cambios determinantes de la fenología y funcionamiento del BST (BUSTO-GÓMEZ & LOPERA, 2003; BARRAZA et al., 2010; MEDINA & GONZÁLEZ, 2014; PIZANO & GARCÍA, 2014).
Los bajos valores de riqueza observados en potrero y el cultivo durante la época seca, se puede atribuir a los bajos niveles de humedad del suelo (0,9%) y las altas temperaturas del suelo (47°C) que se presentaron en estos hábitats durante esta época. Estas condiciones impiden que las cámaras de pupación sean ablandadas y no se presente la emergencia de los escarabajos adultos, lo que se refleja en bajos valores de riqueza y abundancia (SOWIG, 1995; BUSTO-GÓMEZ & LOPERA, 2003). Por otra parte, durante esta época del año la actividad de los Scarabaeinae adultos así como las comunidades de mamíferos nativos se ve restringida a zonas con mayor cobertura vegetal, donde estas condiciones ambientales sean más favorables para su supervivencia (NICHOLS et al., 2007; GARDNER et al., 2008). Por otro lado, aunque la cantidad de excremento en el potrero es mayor por la existencia de ganado vacuno y equino, este se convierte en un recurso poco atractivo en esta época del año; debido a que las altas temperaturas del suelo y ambiental, así como la baja humedad del suelo aceleran la deshidratación de este recurso, endureciéndolo y tornándolo inaccesible a los escarabajos. Caso contrario sucede en las áreas con mayor cobertura (borde e interior del bosque), donde el recurso aportado por los mamíferos nativos tendrá un mayor tiempo de vida para ser colonizados (PECK & FORSYTH, 1982).
Teniendo en cuenta los hábitats, los altos valores de riqueza y abundancia en el borde, se debe a que la transición que hay de un ambiente a otro (interior del fragmento al borde del mismo) no es abrupta; permitiendo que se produzca un efecto ecotono. Esto permite la presencia de microhábitats, tanto de zonas abiertas como de zonas de bosque, favoreciendo la coexistencia de las especies de ambos lugares. Además, la presencia de excremento en el borde, tanto de mamíferos nativos como introducidos; atrae tanto a las especies de interior del bosque como de áreas abiertas, favoreciendo el encuentro de un mayor número de escarabajos representados por muchos individuos; aumentándose la diversidad durante las épocas de muestreos y principalmente en la época seca (MONTES DE OCA, 2001). Estos resultados coinciden con lo propuesto por ESCOBAR (1997), quien registró altos valores de riqueza en los bordes del bosque cuando en sus alrededores se encuentra una matriz de uso ganadero. DÍAZ et al.(2010) considera que los bordes de los fragmentos son lugares transicionales entre dos hábitats, característica que le permite alojar un número altos de especies de ambos ambientes, lo cual también explicaría los resultados obtenidos en este estudio.
Las diferencias en la estructura de la comunidad de Scarabaeinae entre los hábitats intervenidos (Cul y Pot) con los poco intervenidos (Bor e I. B), se puede atribuir a la poca cobertura vegetal que se presenta en los dos primeros. Esta situación permite que en estos lugares se produzcan cambios rápidos en las variables ambientales, los cuales son más notorios durante la época seca. Lo anterior modula la presencia de los escarabajos coprófagos en estos lugares, de tal forma que en estos hábitats se observan pocos escarabajos de interior de bosque que son capaces de tolerar las condiciones de estos usos del suelo (BARRAGÁN et al., 2014; BARNES et al., 2014; BICKNELL et al., 2014). Sin embargo, las condiciones de estos hábitats permiten el rápido establecimiento de especies foráneas, las cuales pueden adaptarse a estos ambientes cambiantes producto de la fragmentación, colonizando y utilizando los recursos que son aportados por mamíferos introducidos (LARSEN et al., 2008). En cuanto al fragmento de bosque, la cobertura vegetal permite la presencia de una mayor variedad de microclimas, presentándose más lugares donde los escarabajos puedan explorar la búsqueda de otro tipo de recursos y sitios de refugios más estables (GILL, 1991; SPECTOR, 2006; SCHOLTZ et al., 2009). Además de las barreras ambientales que imponen lugares de usos humanos, hay muchos escarabajos que no acceden a estos hábitats (Cul y Pot), debido a la preferencia que tienen por ciertos recursos como los excrementos de primates, los cuales son más abundantes en los fragmentos de bosques (GILL, 1991). Además de los recursos ofertados por los primates, en los bosques hay una mayor probabilidad de encontrar otras fuentes de alimento como hongos, frutas, carroña e incluso otro tipo de excrementos proporcionados por mamíferos de tamaño pequeño (roedores), que pueden ser utilizadas por un grupo de escarabajos copro-necrófagos (ANDUAGA & HALFFTER, 1991; GILL, 1991; ANZURES-DADDA et al., 1998; LARSEN et al., 2008).
La presencia de U. deavilai, en todas las épocas de muestreo y todos los hábitats se debe al comportamiento eurifágico de esta especie, lo que le permite aprovechar cualquier recurso disponible. Lo anterior ha sido descrito por DELGADO & KOHLMANN (2007), MARTÍNEZ et al. (2012), RANGEL-ACOSTA et al. (2012), quienes documentaron a esta especie en áreas abiertas y fragmentos de bosques, haciendo uso de varios tipos de recursos alimenticios (excrementos de humano, mono, vaca y asnos). Por otro lado, la presencia de esta especie en todas las épocas se debe posiblemente a varios eventos reproductivos (multivoltino) que la especie presenta durante todo el año, lo cual permite estar presente en ambas épocas de muestreo.
La caracterización de borde e interior de bosque en ambas épocas por C. aff.morsei, se debe a la preferencia de esta especie por hábitats con un alto grado de cobertura vegetal y pocas intervenciones antrópicas. La presencia de esta especie en ambas épocas es producto de varios eventos de reproducción durante el año y su capacidad generalista para consumir recursos alimenticios. Lo anterior ha sido reportado por BEDOUSSAC et al. (2007), HALFFTER & HALFFTER (2009) y RANGEL-ACOSTA et al. (2012), quienes asocian esta especie a necro-trampas cebadas con cadáveres de diplópodos, ratas y copro-trampas cebadas con diferentes excrementos de mamíferos como cerdo (Sus scrofa domestica) y mono (Alouatta seniculus).
Las especies C. mutabilis y C. lituratus caracterizaron a cultivo y potrero, pero en épocas de lluvias diferentes; lo cual evidencia el uso del mismo hábitat de manera alternada. La primera especie tiene sincronizada su emergencia con las primeras lluvias del año, mientras que la segunda presenta su mayor actividad durante las fuertes lluvias; lo cual estaría demostrando que especies muy emparentadas tengan un patrón temporal de actividad diferente con el fin de disminuir la competencia entre ellas. Adicional a esto, el comportamiento que muestran estas especies, evidencia que se ven poco afectados por el constante cambio de las variables ambientales que sufren estos hábitats durante el año; razón por la cual estos taxones no muestran una relación con las variables medidas (SOLÍS-BLANCO & KOHLMANN, 2002).
En el caso de D. agenor y O. marginicollis, caracterizaron hábitats como potrero y cultivo durante los periodos de lluvias. La abundancia de ambas especies mostró una relación directa con la precipitación y con los cambios que este parámetro produce en otras variables ambientales (temperatura ambiente, temperatura del suelo, humedad ambiente y humedad del suelo). Esto evidencia que estas especies tienen sus ciclos reproductivos sincronizados con las épocas donde los valores de precipitación son moderados y muestran una repuesta negativa a valores altos de temperatura del suelo y bajos valores de humedad del mismo. Autores como KOHLMANN & SOLÍS-BLANCO (1997, 2001) han catalogado a estas dos especies como típicas de áreas abiertas, las cuales están presentes con mayor abundancia en periodos húmedos y con una alta afinidad a excrementos de mamíferos introducidos como vacas, caballos y carroña.
La mayor proporción de escarabajos coprófagos pequeños tanto cavadores como rodadores, se debe a que en el bosque seco de las zonas bajas del Caribe colombiano, los ensamblajes están compuestos entre un 50% y 76% de especies de escarabajos pequeños, con aumento de las especies grandes durante la época de lluvias y las cuales desaparecen durante la época seca (BARRAZA et al., 2010; MARTÍNEZ et al., 2010, 2012; NAVARRO et al., 2011; SOLÍS et al., 2011; DELGADO-GÓMEZ et al., 2012; RANGEL-ACOSTA et al., 2012; BARRAZA, 2015).
Trabajos realizados por VERDÚ et al. (2006), VERDÚ et al. (2007), SHEPHERD et al. (2008), encontraron que los escarabajos de mayor tamaño deben mantener una temperatura durante el vuelo inferior a 42°C y en caso de sobrepasar este límite podría causar la muerte de los individuos. Esta situación puede ser la principal causa de la estacionalidad de estas especies y su ausencia durante los periodos secos, cuando las elevadas temperaturas ambientales (>40°C, lugares abiertos) podrían comprometer fácilmente el equilibrio térmico de estos escarabajos. Con el fin de evitar este tipo de situaciones, estos escarabajos presentan mayor actividad durante las noches, al amanecer o al atardecer cuando el clima es más fresco, o en la mayoría de los casos se encuentran asociados a zonas de bosques con altas elevaciones donde la temperatura ambiente es baja (VERDÚ et al., 2006; LARSEN, 2012). Esta situación se asemeja a la observada en este estudio, donde las especies de escarabajos grandes capturadas presentaron hábitos nocturnos y crepusculares, coincidiendo con lo descrito por BARRAZA (2015).
Con relación a las especies pequeñas, ocurre caso contrario, las cuales son ectotermas y dependen del aumento de la temperatura ambiente para su activación. VERDÚ et al., (2006) y LARSEN et al. (2008) describen que estas especies son más activas durante el día, cuando se presentan mayor radiación solar y calor (medio día). El hecho de que las condiciones climáticas afecten poco a estas especies pequeñas les ha permitido colonizar varios tipos de hábitats, tal como es registrado en este trabajo, pues independientemente de la época y del hábitat, los pequeños cavadores y pequeños rodadores están presentes con altos valores de riqueza y abundancia (ARELLANO et al., 2013).
AGRADECIMIENTOS
A la comunidad campesina de la vereda Los Torombolos por facilitar la estancia y permisos en este lugar durante la realización del trabajo de campo, en especial a los señores Santiago Conrado "Chago" y Rafael Conrado "El Mono" y demás familiares, por acogernos en su hogar y colaborarnos con la alimentación. Al Instituto de Investigaciones Alexander von Humboldt por permitir la visita a sus instalaciones y a la Doctora Claudia Medina y Luis Edier Franco por su ayuda para la confirmación de las muestras en el instituto. Al Instituto de Ecología (INECOL), por permitir la estancia durante el curso Análisis de la Diversidad y a los miembros del semillero de investigación NEOPTERA del programa de Biología, en especial a Alcides Mejía & Jeison Barraza por su colaboración en el trabajo de campo y la Facultad de Ciencias Básicas de la Universidad del Atlántico por facilitar los permisos y las instalaciones del laboratorio de zoología para el procesamiento e identificación de las muestras.
REFERENCIAS
ANDUAGA, S. & HALFFTER, G., 1991.- Escarabajos asociados a madrigueras de roedores (Coleoptera: Scarabaeidae, Scarabaeinae).Folia Entomológica Mexicana, 81: 185–196. [ Links ]
ANZURES-DADDA, A., ESTRADA, A. & COATES-ESTRADA, R., 1998.- Monos aulladores (Alouatta palliata), escarabajos coprófagos y la fragmentación de las selvas en los Tuxtlas, Veracruz, México. Neotropical Primates, 6: 111–114. [ Links ]
ARELLANO, L., LEÓN-CORTÉS, J.L., HALFFTER, G. & MONTERO, J., 2013.- Acacia woodlots, cattle and dung beetles (Coleoptera: Scarabaeinae) in a Mexican silvopastoral landscape. Revista Mexicana de Biodiversidad, 84: 650–660. [ Links ]
BARNES, A.D., EMBERSON, R.M., CHAPMAN, H.M., KRELL, F.-T. & DIDHAM, R.K., 2014.- Matrix habitat restoration alters dung beetle species responses across tropical forest edges. Biological Conservation, 170: 28–37. [ Links ]
BARRAGÁN, F., MORENO, C.E., ESCOBAR, F., BUENO-VILLEGAS, J. & HALFFTER, G., 2014.- The impact of grazing on dung beetle diversity depends on both biogeographical and ecological context. Journal of Biogeography, 41: 1991–2002. [ Links ]
BARRAZA, J., 2015.- Patrones de actividad diaria y segregación ecológica en relación al recurso en escarabajos copronecrófagos (Scarabaeidae: Scarabaeinae), en un paisaje de bosque seco tropical en la costa Caribe Colombiana. Maestría, Instituto Venezolano de Investigaciones Científicas I.V.I.C, Caracas-Venezuela. [ Links ]
BARRAZA, J., MONTES, J., MARTÍNEZ, N. & DELOYA, C., 2010.- Ensamblaje de escarabajos coprófagos (Scarabaeidae: Scarabaeinae) del bosque tropical seco, Bahía Concha, Santa Marta (Colombia). Revista Colombiana de Entomología, 36: 285–291. [ Links ]
BEDOUSSAC, L., FAVILA, M.E. & LÓPEZ, R.M., 2007.- Defensive volatile secretions of two diplopod species attract the carrion ball roller scarab Canthon morsei (Coleoptera: Scarabaeidae). Chemoecology, 17: 163–167. [ Links ]
BERDUGO-LATKE, M.L., AVELLA, A. & RANGEL-CH, J.O., 2012.- Patrón biotipológico foliar en un gradiente de precipitación en la Región Caribe de Colombia. En RANGEL-CH, J.O (Editor). Colombia Diversidad Biótica XII: La región Caribe de Colombia, pp. 601–651. Universidad Nacional de Colombia, Bogotá-Colombia. [ Links ]
BICKNELL, J.E., PHELPS, S.P., DAVIES, R.G., MANN, D.J., STRUEBIG, M.J. & DAVIES, Z.G., 2014.- Dung beetles as indicators for rapid impact assessments: Evaluating best practice forestry in the neotropics. Ecological Indicators, 43: 154–161. [ Links ]
BUSTO-GÓMEZ, F.B. & LOPERA, A., 2003.- Preferencia por cebo de los escarabajos coprófagos (Coleoptera: Scarabaeidae: Scarabaeinae) de un remanente de bosque seco tropical al norte del Tolima (Colombia). En ONORE, G., REYES-CASTILLO, P. & ZUNINO, M (Editores). Escarabeidos de Latinoamérica: estado del conocimiento. pp. 59–65. Sociedad Entomológica Aragonesa, Zaragoza-España. [ Links ]
CHAO, A., GOTELLI, N.J., HSIEH, T.C., SANDER, E.L., MA, K.H., COLWELL, R.K. & ELLISON, A.M., 2014.- Rarefaction and extrapolation with Hill numbers: a framework for sampling and estimation in species diversity studies. Ecological Monographs, 84: 45–67. [ Links ]
CLARKE, K. R. & WARWICK, R. M., 2001.- Change in marine communities: an approach to statistical analysis and interpretation, 2nd ed. PRIMER-E, Plymouth. Inglés, United Kingdom. [ Links ]
DELGADO-GÓMEZ, P., LOPERA, A. & RANGEL-CH, J.O., 2012.- Variación espacial del ensamblaje de escarabajos coprófagos (Scarabaeidae: Scarabaeinae) en remanentes de bosque seco en Chimichagua (Cesar, Colombia). En Rangel-Ch, J.O. (Editor) Colombia Diversidad Biótica XII: La región Caribe de Colombia, pp. 833–849. Universidad Nacional de Colombia, Bogotá-Colombia. [ Links ]
DELGADO, L. & KOHLMANN, B., 2007.- Revisión de las especies del género Uroxys Westwood de México y Guatemala (Coleoptera: Scarabaeidae: Scarabaeinae). Folia Entomológica Mexicana, 46: 1–36. [ Links ]
DÍAZ, A., GALANTE, E. & FAVILA, M.E., 2010.- The effect of the landscape matrix on the distribution of dung and carrion beetles in a fragmented tropical rain forest. Journal of Insect Science, 10: 1–10. [ Links ]
DIRZO, R., YOUNG, H.S., MOONEY, H.A. & CEBALLOS, G., 2011.- Seasonally dry tropical forests: ecology and conservation. Island Press, Washington, DC. [ Links ]
DOUBE, B.M., 1990.- A functional classification for analysis of the structure of dung beetle assemblages. Ecological Entomology, 15: 371–383. [ Links ]
EDMONDS, W.D. & ZÍDEK, J., 2010.- A taxonomic review of the neotropical genus Coprophanaeus Olsoufieff, 1924 (Coleoptera: Scarabaeidae, Scarabaeinae). Insecta Mundi, 0129: 1-111. [ Links ]
ESCOBAR, F., 1997.- Estudio de la comunidad de coleópteros coprófagos (Scarabaeidae) en un remanente de bosque seco al norte del Tolima, Colombia. Caldasia, 19: 419–430. [ Links ]
ESCOBAR, F., 2004.- Diversity and composition of dung beetle (Scarabaeinae) assemblages in a heterogeneous Andean landscape. Tropical Zoology, 17: 123–136. [ Links ]
FAITH, D.P., MINCHIN, P.R. & BELBIN, L., 1987.- Compositional dissimilarity as a robust measure of ecological distance. Vegetatio, 69: 57–68. [ Links ]
Favila, M.E. & Halffter, G., 1997.- The use of indicator groups for measuring biodiversity as related to community structure and function. Acta Zoológica Mexicana, 72: 1–25. [ Links ]
GARCÍA-ATENCIA, S. & MARTÍNEZ-HERNÁNDEZ, N., 2015.- Escarabajos fitófagos (Coleoptera: Scarabaeidae) del departamento del Atlántico, Colombia. Acta Zoológica Mexicana (nueva serie), 31: 89–96. [ Links ]
GARCÍA, H., CORZO, G., ISAACS, P. & ETTER, A., 2014.- Distribución y estado actual de los remanentes del bioma de bosque seco tropical en Colombia: insumos para su gestión. En PIZANO, C. & GARCÍA, H (Editores). El bosque seco tropical en Colombia, pp. 229–251I. Instituto de Investigación de Recursos Biológicos Alexander von Humboldt (IAvH), Bogotá-Colombia. [ Links ]
GARDNER, T.A., HERNÁNDEZ, M.I., BARLOW, J. & PERES, C.A., 2008.- Understanding the biodiversity consequences of habitat change: the value of secondary and plantation forests for neotropical dung beetles. Journal of Applied Ecology, 45: 883–893. [ Links ]
GÉNIER, F., 2009.- Le genre Eurysternus Dalman, 1824 (Scarabaeidae: Scarabaeinae: Oniticellini), revision taxonomique et clés de determination illustrées. Pensoft, Francia. [ Links ]
GILL, B.D., 1991.- Dung beetles in tropical American forests. En Hanski, I. & Cambefort, Y. (Editores). Dung beetle ecology, pp. 211–229. Princeton University Press, New Jersey. [ Links ]
GONZÁLEZ, F.A., MOLANO, F. & MEDINA, C.A., 2009.- Los subgéneros Calhyboma Kolbe 1893, Hybomidium Shipp 1897 y Telhyboma Kolbe 1893 de Deltochilum (Coleoptera: Scarabaeidae: Scarabaeinae) en Colombia. Revista Colombiana de Entomología, 35: 253-274. [ Links ]
HALFFTER, G. & FAVILA, M.E., 1993.- The Scarabaeinae (Insecta: Coleoptera) an animal group for analyzing, inventorying and monitoring biodiversity in tropical rainforest and modified landscapes. Biology International, 27: 15–21. [ Links ]
HALFFTER, V. & HALFFTER, G., 2009.- Nuevos datos sobre Canthon(Coleoptera: Scarabaeinae) de Chiapas, México. Acta zoológica mexicana, 25: 397–407. [ Links ]
HILL, M.O., 1973.- Diversity and Evenness: A Unifying Notation and Its Consequences. Ecology, 54: 427. [ Links ]
JOST, L., 2006.- Entropy and diversity. Oikos, 113: 363–375. [ Links ]
KOHLMANN, B. & SOLÍS-BLANCO, A., 1997.- El género Dichotomius (Coleoptera: Scarabaeidae) en Costa Rica. Giornale Italiano di Entomologia, 8: 343–382. [ Links ]
KOHLMANN, B. & SOLÍS-BLANCO, A., 2001.- El género Onthophagus (Coleoptera: Scarabaeidae) en Costa Rica. Giornale Italiano di Entomologia, 9: 159–261. [ Links ]
LARSEN, T.H., LOPERA, A. & FORSYTH, A., 2008.- Understanding Trait-Dependent Community Disassembly: Dung Beetles, Density Functions, and Forest Fragmentation. Conservation Biology, 22: 1288–1298. [ Links ]
LARSEN, T.H. 2012.- Upslope Range Shifts of Andean Dung Beetles in Response to Deforestation: Compounding and Confounding Effects of Microclimatic Change. Biotropica, 44: 82–89. [ Links ]
MARTÍNEZ, N.J., GARCÍA, H., PULIDO, L.A., OSPINO, D. & NARVÁEZ, J.C., 2009.- Escarabajos coprófagos (Coleoptera: Scarabaeinae) de la Vertiente Noroccidental, Sierra Nevada de Santa Marta, Colombia. Neotropical Entomology, 38: 708–715. [ Links ]
MARTÍNEZ, N.J., CAÑAS, L.M., RANGEL, J.L., BARRAZA, J., MONTES, J. & BLANCO, O., 2010.- Coleópteros coprófagos (Scarabaeidae: Scarabaeinae) en un fragmento de bosque seco tropical en el departamento del Atlántico, Colombia. Boletín del Museo de Entomología de la Universidad del Valle, 11: 21–30. [ Links ]
MARTÍNEZ, N., SALCEDO, G., SIERRA, K. & BARRAZA, J., 2012.- Escarabajos coprófagos (Coleoptera: Scarabaeinae) asociados a excrementos de mamíferos en un fragmento de bosque seco tropical en el departamento del Atlántico, Colombia. Ecología austral, 22: 203–210. [ Links ]
MEDINA, C.A. & GONZÁLEZ, F.A., 2014.- Escarabajos coprófagos de la subfamilia Scarabaeinae. En PIZANO, C & GARCÍA, H (Editores). El bosque seco tropical en Colombia, pp. 194–213. Bogotá-Colombia. [ Links ]
MEDINA, C.A. & LOPERA, A., 2000.- Clave ilustrada para la identificación de géneros de escarabajos coprófagos (Coleoptera: Scarabaeinae) de Colombia. Caldasia 22, 299–315. [ Links ]
MEDINA, C.A., LOPERA, A., VÍTOLO, A. & GILL, B., 2001.- Escarabajos coprófagos (Coleoptera: Scarabaeidae: Scarabaeinae) de Colombia. Biota Colombiana, 2: 131–144. [ Links ]
MONTES DE OCA, E., 2001.- Escarabajos coprófagos de un escenario ganadero típico de la región de los Tuxtlas, Veracruz, México: importancia del paisaje en la composición de un gremio funcional. Acta Zoológica Mexicana (nueva serie), 82: 111–132. [ Links ]
NAVARRO, I.L., ROMAN, A.K., GÓMEZ, F.H. & PÉREZ, A., 2011.- Variación estacional en escarabajos coprófagos (Coleoptera: Scarabaeidae: Scarabaeinae) de la Serranía de Coraza, Sucre (Colombia). Revista Colombiana de Ciencia Animal, 3: 102–110. [ Links ]
NICHOLS, E., LARSEN, T., SPECTOR, S., DAVIS, A.L., ESCOBAR, F., FAVILA, M. & VULINEC, K., 2007.- Global dung beetle response to tropical forest modification and fragmentation: a quantitative literature review and meta-analysis. Biological Conservation, 137: 1–19. [ Links ]
NORIEGA, J.A., CAMERO, E., ARIAS-BURITICÁ, J., LOCARNO, L.C.P., MONTES, J.M., ACEVEDO, A., ESPARZA, A., MURCIA, B., GARCÍA, H. & SOLÍS, C., 2015.- Grado de cobertura del muestreo de escarabajos coprófagos (Coleoptera: Scarabaeidae: Scarabaeinae) en Colombia. Int. Jour. Trop. Bio and Cons, 63: 97–125. [ Links ]
OKSANEN, J., KINDT, R., LEGENDRE, P., O'HARA, B., STEVENS, M.H.H., OKSANEN, M.J. & SUGGESTS, M., 2007.- The vegan package. Community ecology package. Community ecology package. Disponible en: http://cran.r-project.org/web/packages/vegan/vegan.pdf; última consulta: 6 de dic.2015. [ Links ]
PECK, S.B. & FORSYTH, A., 1982.- Composition, structure, and competitive behaviour in a guild of Ecuadorian rain forest dung beetles (Coleoptera; Scarabaeidae). Canadian Journal of Zoology, 60: 1624–1634. [ Links ]
PIZANO, C. & GARCÍA, H., 2014.- El bosque seco tropical en Colombia. Instituto de Investigación de Recursos Biológicos Alexander von Humboldt (IAvH), Bogotá-Colombia. [ Links ]
R CORE TEAM., 2014.- R: a language and environment for statistical computing. R foundation for Statistical Computing. Vienna, Austria. Disponible en: http://www.R-project.org/.
Última consulta 6 de dic. 2015. [ Links ]
PORTILLO-QUINTERO, C.A. & SÁNCHEZ-AZOFEIFA, G.A. 2010.- Extent and conservation of tropical dry forests in the Americas. Biological Conservation, 143: 144–155. [ Links ]
RANGEL-ACOSTA, J.L., BLANCO-RODRÍGUEZ, O.R., GUTIÉRREZ-RAPALINO, B.P. & MARTÍNEZ-HERNÁNDEZ, N.J., 2012.- Coleópteros coprófagos (Scarabaeidae: Scarabaeinae) asociados a excrementos de mamíferos de la Reserva Natural Luriza (RNL), Departamento del Atlántico, Colombia. Boletín de la SEA, 50: 409–419. [ Links ]
RANGEL-CH, J.O. & CARVAJAL-COGOLLO, J.E., 2012.- Clima de la Región Caribe Colombiana. En RANGEL-CH, J.O. (Editores). Colombia Diversidad Biótica XII: La región Caribe de Colombia, pp. 67–129. Universidad Nacional de Colombia, Bogotá-Colombia. [ Links ]
SCHOLTZ, C.H., DAVIS, A.L.V. & KRYGER, U., 2009.- Evolutionary biology and conservation of dung beetles. Pensoft Pub., Bulgaria. [ Links ]
SHEPHERD, B.L., PRANGE, H.D. & MOCZEK, A.P. 2008.- Some like it hot: Body and weapon size affect thermoregulation in horned beetles. Journal of Insect Physiology, 54: 604–611. [ Links ]
SOLÍS-BLANCO, A. & KOHLMANN, B., 2002.- El género Canthon(Coleoptera: Scarabaeidae) en Costa Rica. Giornale Italiano di Entomologia, 10: 1–68. [ Links ]
SOLÍS-BLANCO, A. & KOHLMANN, B., 2004.- El género Canthidium (Coleoptera: Scarabaeidae) en Costa Rica. Giornale Italiano di Entomologia, 11: 1–73. [ Links ]
SOLÍS, C., NORIEGA, J.A. & HERRERA, G., 2011.- Escarabajos coprófagos (Coleoptera: Scarabaeinae) en tres bosques secos del departamento del Atlántico Colombia. Boletín del Museo de Entomología de la Universidad del Valle, 12: 33–41. [ Links ]
SOWIG, P., 1995.- Habitat selection and offspring survival rate in three paracoprid dung beetles: the influence of soil type and soil moisture. Ecography, 18: 147–154. [ Links ]
SPECTOR, S., 2006.- Scarabaeine dung beetles (Coleoptera: Scarabaeidae: Scarabaeinae): An invertebrate focal taxon for biodiversity research and conservation. The Coleopterists Bulletin, 60: 71–83. [ Links ]
VAZ-DE -MELLO, F.Z., EDMONDS, W.D., OCAMPO, F.C. & SCHOOLMEESTERS, P., 2011.- A multilingual key to the genera and subgenera of the subfamily Scarabaeinae of the New World (Coleoptera: Scarabaeidae). Zootaxa, 2854: 1–73. [ Links ]
VENABLES, W.N. & RIPLEY, B.D., 2002.- Modern applied statistics with S. Springer. Disponible en: http://cran.r-project.org/web/packages/MASS/MASS.pdf. última consulta 6 de dic.2015. [ Links ]
VERDÚ, J.R., ARELLANO, L. & NUMA, C., 2006.- Thermoregulation in endothermic dung beetles (Coleoptera: Scarabaeidae): Effect of body size and ecophysiological constraints in flight. Journal of Insect Physiology, 52: 854–860. [ Links ]
VERDÚ, J.R., ARELLANO, L., NUMA, C. & MICÓ, E., 2007.- Roles of endothermy in niche differentiation for ball-rolling dung beetles (Coleoptera: Scarabaeidae) along an altitudinal gradient. Ecological Entomology, 32: 544–551. [ Links ]
VITÓLO, A., 2000.- Clave para la identificación de los géneros y especies phaenaeinas (Coleóptera: Scarabaeidae: Corpinae: Phanaeini) de Colombia. Rev. Acad. Colomb. Cienc 24: 591–601. [ Links ]














