Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Boletín Científico. Centro de Museos. Museo de Historia Natural
Print version ISSN 0123-3068
Bol. Cient. Mus. Hist. Nat. Univ. Caldas vol.20 no.2 Manizales July/Dec. 2016
https://doi.org/10.17151/bccm.2016.20.2.6
DOI: 10.17151/bccm.2016.20.2.6
BIOLOGICAL ACTIVITY OF ENTOMOPATHOGENIC FUNGI AND BACTERIA ON Diatraea saccharalis Fabricius (LEPIDOPTERA: CRAMBIDAE)
* FR: 23-IX-16. FA: 18-X-16.
1 Ingeniero Agrónomo. Universidad de Caldas, Manizales, Colombia. E-mail: meissen.3@hotmail.com; ORCID: 0000-0002-9288-8515
2 I.A., M.Sc., Ph.D. Departamento de Producción Agropecuaria, Universidad de Caldas, Manizales, Colombia. E-mail: alberto.soto@ucaldas.edu.co; ORCID: 0000-0002-9727-8919
3 I.A., Ph.D. Departamento de Desarrollo Rural y Recursos Naturales, Universidad de Caldas, Manizales, Colombia. E-mail: gabocruz@ucaldas.edu.co ORCID: 0000-0003-1550-6517
Diatraea saccharalis es considerada la plaga más limitante del cultivo de caña de azúcar en América, causando grandes pérdidas en la producción. El objetivo del trabajo fue evaluar el efecto de hongos entomopatógenos comerciales y nativos y de la bacteria Bacillus thuringiensis var. kurstaki como potenciales controladores biológicos de este insecto plaga. Se evaluó la patogenicidad y virulencia de 6 hongos entomopatógenos comerciales, 1 hongo nativo (Bb-HN1) y la bacteria Bacillus thuringiensis sobre larvas de primer instar de Diatraea; bajo condiciones de laboratorio y semicampo. Los productos Safer mix®, Dipel®, Insecbiol® y el aislamiento nativo Bb-HN1 presentaron mortalidad del 100, 100, 62 y 70%, respectivamente. Los tratamientos más virulentos de acuerdo a su tiempo letal y concentración letal media fueron Dipel® (1,3 días y 1,64 ui/ml), Safer mix® (12,5 días y 5,35 ui/ml) y Bb-HN1 (22,3 días y 1,66 ui/ml) respectivamente. También se evidencio un posible sinergismo entre el hongo B. bassiana y la bacteria B. thuringiensis, y una disminución del daño causado por las larvas a las semillas de caña panelera tratadas con los productos Dipel® y Bb-HN1 en condiciones de semicampo. El producto B. thuringiensis (Dipel®) en mezcla con el hongo Bb-HN1 se presentan como alternativa para el manejo integrado de la plaga.
Palabras clave: control biológico, manejo integrado de plagas, caña panelera, Bacillus thuringiensis.
AbstractDiatraea saccharalis is considered the most limiting pest of sugarcane crops in America generating great losses in production. The main aim of this study was to evaluate the effect of commercial and native entomopathogenic fungi and the bacterium Bacillus thuringiensis var. kurstaki as potential biological controls of this insect pest. The pathogenicity and virulence of six commercial entomopathogenic fungi, one native fungus (Bb-HN1) and the bacterium Bacillus thuringiensison first instar larvae of Diatraea under laboratory and field conditions was evaluated. The commercial products mix®, Dipel® and nsecbiol® as well as the native isolate Bb-HN1 showed mortality rates of 100, 100, 62 and 70%, respectively. The most virulent treatments according to their lethal and median lethal concentration were Dipel® (1.3 days and 1.64 IU/ml), Safer mix® (12.5 days and 5.35 IU/ml) and Bb-HN1 (22.3 days and 1.66 IU/ml) respectively. A possible synergism between the fungus B. bassiana and the bacterium B. thuringiensis, and a damage reduction caused by the larvae to sugarcane seeds treated with the products and a damage reduction caused by the larvae to sugarcane seeds treated with the products Dipel® and Bb-HN1 under semi-field conditions was also found. The product B. thuringiensis (Dipel®) mixed with the fungus Bb-HN1 is presented as an alternative for the integrated management of the pest.
Key words: biological control, integrated pest management, sugarcane, Bacillus thuringiensis.
Diatraea saccharalis (Lepidoptera: Crambidae) es una de las principales plagas que ataca la caña, causando grandes perjuicios a la producción final y su control implica directamente el aumento de la productividad (GALLO et al., 2002; POLANCZYK et al., 2004; VARGAS et al., 2013). Las larvas de D. saccharalis ocasionan disminución en la germinación de la semilla, corazones muertos en las plantas jóvenes, cogollos muertos en las plantas más viejas, tallos quebrados y crecimiento reducido de los tallos atacados que sobreviven al ataque (MENDONÇA, 1996; BOTELHO & MACEDO, 2002; GALLO et al., 2002; PARRA et al., 2002; PINTO et al., 2006).
Las pérdidas ocasionadas por D. saccharalis y la importancia que presenta el cultivo de caña panelera en nuestro país, conllevan a buscar alternativas para su manejo que sean ecológica y económicamente viables (MOJICA & PAREDES, 2004).
La necesidad de adoptar nuevas tecnologías para el control de plagas ha orientado las investigaciones hacia el uso de bioinsecticidas que, actuando de manera similar a los plaguicidas convencionales, no ocasionan problemas como la resurgencia de plagas, la inducción de nuevas plagas y la contaminación del medio ambiente, entre otras (CABRERA & PINEDO, 1994; ESTRADA et al., 2004; BADII et al., 2006; CRANSHAW, 2014).
Varios métodos de control son utilizados para minimizar las pérdidas ocasionadas por acción de la plaga, como el control cultural, por medio de la rotación de cultivos y de la siembra de variedades resistentes; además de estos, el control biológico con los parasitoides Trichogramma exiguum (Hymenoptera: Trichogrammatidae), Cotesia flavipes (Hymenoptera: Braconidae), Billaea claripalpis y Lydella minense (Díptera: Tachinidae), con la bacteria Bacillus thuringiensis (Bt), o con hongos entomopatógenos como Metarhizium anisopliae y Beauveria bassiana (ALVES et al., 1985; LECUONA et al., 1996; WENZEL et al., 2006; OLIVEIRA et al., 2008a, b; ZAPPELINI et al., 2010; GUO et al., 2012; SVEDESE et al., 2013; ZHANG et al., 2013). Diversos estudios de compatibilidad con productos fitosanitarios son realizados, en condiciones de laboratorio, para evaluar su selectividad a microrganismos y potencializar su acción en el manejo integrado de plagas (YASEM et al., 2008; ISLAM et al., 2010; BLANFORD et al., 2011; SABBOUR & ABDEL-RAHMAN, 2013; ZAHRAN et al., 2013).
El objetivo del presente trabajo fue evaluar el efecto de hongos entomopatógenos comerciales y nativos y de la bacteria Bacillus thuringiensisvar. kurstaki para el control de D. saccharalis, con el fin de incrementar la productividad del cultivo, además de asegurar el crecimiento sustentable del país.
MATERIALES Y MÉTODOSEl estudio se realizó en el Laboratorio de Entomología y en el Centro de Investigación y Cría de Enemigos Naturales de la Universidad de Caldas, ubicado en el municipio de Manizales (Coordenadas: 5° 05'N y 75° 40' W). Se evaluaron los siguientes productos comerciales sobre larvas de primer instar de D. saccharalis: Metaril® (M. anisopliae), Insecbiol® (B. bassiana, M. anisopliae, P. fumosoroseus, P. lilacinus, B. thuringiensis, Baculovirus), Bauberiasil® (B. bassiana), Micosplag® (P. lilacinus, M. anisopliae, B. bassiana), Safer mix® (B. bassiana, M. anisopliae, L. lecanii, B. thuringiensis), Micosis® (B. bassiana), Dipel® (B. thuringiensis var. kurstaki) y Bb-HN1 (Cepa nativa de B. bassiana aislada de larvas de Diatraea, suministrada por el Centro Bekdau de la Universidad de Caldas).
Evaluación de la patogenicidadSe determinó la patogenicidad que ejercen dichos productos microbiológicos sobre larvas de Diatraea, para lo cual se infestaron 5 larvas de primer instar de Diatraea por caja Petri previamente esterilizada, por tratamiento, y se aplicaron los productos a una concentración de 2 x 106 unidades infectivas/ml (ui/ml) de agua, para lo cual se utilizó un hemocitómetro marca Boeco para el conteo de las esporas. La cepa del hongo nativo (Beauveria bassiana Bb-HN1) se aplicó a la misma concentración de los productos comerciales (2 x 106 ui/ml de agua). La inoculación de las larvas se realizó mediante la inmersión de las mismas en la suspensión correspondiente al tratamiento evaluado durante un minuto, salvo el tratamiento testigo cuyos insectos se sumergieron en agua destilada estéril. Las larvas se ubicaron en una incubadora marca Scientific a temperatura de 26±1°C y humedad relativa de 70±10%. Se utilizó un diseño completamente al azar con 10 repeticiones por tratamiento. Para el análisis estadístico se utilizó el programa SAS 9.1 y se realizaron pruebas de Tukey al 5%.
Evaluación de la virulenciaA los tratamientos que presentaron mayor patogenicidad en la fase anterior, se les evaluó la virulencia ocasionada a las larvas de Diatraea, para lo cual se infestaron 10 larvas de primer instar de Diatraea por caja Petri, por tratamiento, y se aplicaron los productos a concentraciones de 5 x 105, 1 x 106, 2 x 106 y 4 x 106 ui/ml de agua, para lo cual se usó un hemocitómetro marca Boeco para el conteo de las esporas. Igual que en el experimento anterior, la inoculación de las larvas se realizó mediante la inmersión de las mismas en la suspensión correspondiente al tratamiento evaluado durante un minuto, salvo el tratamiento testigo cuyos insectos se sumergieron en agua destilada estéril. Las larvas se ubicaron en una incubadora marca Scientific a temperatura de 26±1oC y humedad relativa de 70±10. Se utilizó el diseño completamente al azar, con 7 repeticiones por tratamiento y se realizaron pruebas de Tukey al 5%. Los datos se procesaron por los modelos de regresión Probit y Logit, y se utilizaron los programas estadísticos SAS 9.1 y Curve Expert Profesional 2.0.
Evaluación del sinergismo ocasionado por los productosDebido a que los productos utilizados están compuestos por mezcla de hongos entomopatógenos y otro producto a base de la bacteria B. thuringiensis, se evaluó el posible sinergismo que existe entre ellos. Los productos a base de hongos se ajustaron a una concentración de 2 x 108 ui/ml (CL90), y el producto que contenía la bacteria se aforó a una concentración de 1 x 104 ui/ml. Se emplearon 10 larvas por caja Petri, con 10 repeticiones por tratamiento, las cuales se ubicaron en incubadora marca Scientific a 26±1°C de temperatura y humedad relativa del 70 ±10%. La inoculación de las larvas se realizó mediante la inmersión en la suspensión correspondiente al tratamiento evaluado durante un minuto, los insectos correspondientes al tratamiento testigo se sumergieron en agua destilada estéril durante un minuto. Se utilizó el diseño completamente al azar y para el análisis los programas estadísticos SAS 9.1 y Curve Expert Profesional 2.0.4.
RESULTADOS Y DISCUSIÓNPatogenicidad de los aislamientos
Todos los tratamientos evaluados fueron patogénicos a las larvas de D. saccharalis, ocasionando mortalidad entre el 30 y 100%. El 25% de los tratamientos del bioensayo ocasionaron más del 95% de mortalidad (Safer mix® y Dipel®), mientras que el otro 75% no superaron el 70% de mortalidad (Insecbiol, Bauberiasil, Micosplag, Micosis y Bb-HN1); el producto Metaril no superó el 50% de larvas muertas de Diatraea.
En cuanto a la mortalidad de las larvas de D. saccharalis ocasionada por los diferentes productos en la fase de laboratorio, el análisis de varianza indica que se presentaron efectos estadísticamente diferentes de los tratamientos (Pr < 0.0001). Los productos Safer mix, Dipel, Bb-HN1 e Insecbiol ocasionaron la mayor mortalidad a las larvas de D. saccharalis (100, 100, 70 y 62%), respectivamente. Aunque estadísticamente los productos Insecbiol y Bb-HN1 no presentaron diferencia estadística significativa con respecto a los tratamientos Micosis, Miscosplag y Bauberiasil. El tratamiento con menor acción bioinsecticida fue Metaril, ya que ocasionó el 30,92% de mortalidad (Tabla 1).
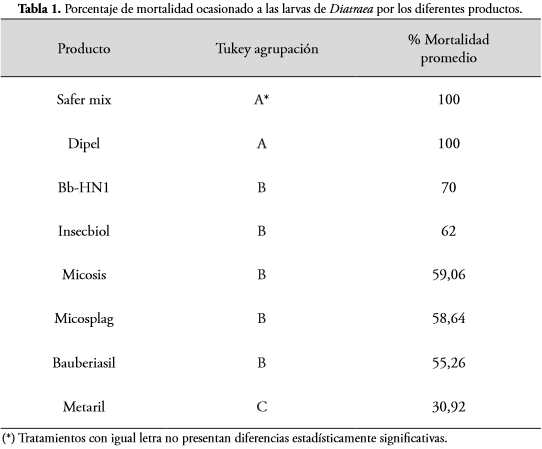
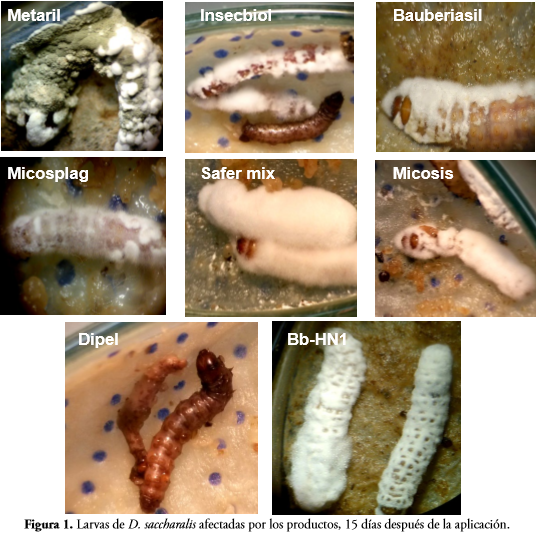
En la Figura 1 se puede observar el efecto de las aplicaciones de los productos sobre las larvas de D. saccharalis. En todas las larvas esporuló el hongo B. bassiana.
Virulencia de los productos
De acuerdo con el tiempo letal 50 (TL50) a una concentración de 2x106, los productos Dipel y Safer mix presentaron mayor virulencia, menor a 13 días (Figura 2). Un menor tiempo letal indica no solo una mayor virulencia, sino que también reduce el daño causado por la plaga hasta el momento de la muerte.
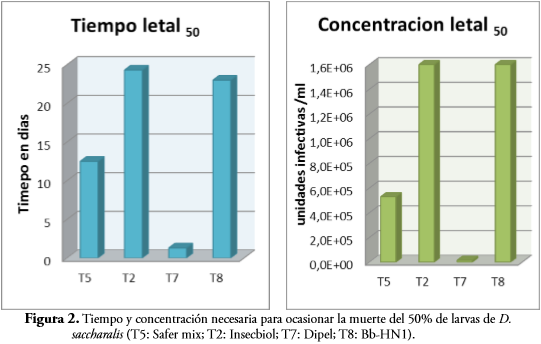
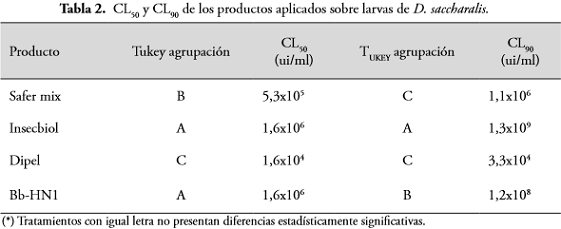
Los productos Safer mix y Dipel, con CL50 de 5,3x105 y 1,6x104, respectivamente, presentaron mayor virulencia que los productos Insecbiol y Bb-HN1con CL50 de 1,6x106 cada uno (Tabla 2). Una menor CL50 indica una mayor virulencia del producto, de manera que se requiere una menor concentración para eliminar el 50% de la población plaga.
Para controlar el 90% de la población, los productos que presentan mayor virulencia son el Dipel y el Safer mix a concentraciones de 3,3x104 y 1,1x106 ui/ml, respectivamente. El producto que requiere aplicar la mayor concentración es el Insecbiol a 1,3x109 ui/ml (Tabla 2).
En investigación realizada por RAMOS et al., (2004) obtuvo una mortalidad del 90% con la aplicación del producto Dipel sobre larvas de D. saccharalis; también observó que a una concentración subletal del producto se ejerce un efecto negativo sobre el crecimiento de las larvas, afectando directamente la capacidad para completar con éxito el proceso de metamorfosis, además influye sobre su viabilidad y por lo tanto en la población del insecto. En la presente investigación se observó que el único hongo en donde se cumplieron los postulados de Koch sobre las larvas de D. saccharalis fue B. bassiana, lo que indica que este hongo es patogénico para el insecto, y por lo tanto se debe tener en cuenta para involucrarlo en el manejo integrado de la plaga.
WENZEL (2006) obtuvo mortalidad de larvas de D. saccharalis entre el 65 y 89% con la aplicación de dos aislamientos de B. bassiana a concentraciones de 5x107, 1x108 y 5x108 ui/ml; igualmente obtuvo CL50 con la aplicación de 1,58 x 107 ui/ml. SANTILLANA (2002) registró un 26%, 32% y 40% de mortalidad sobre larvas de D. saccharalis con la aplicación de B. thuringiensis en la Dl50 a las 24h, incrementándose a 88, 99 y 100% la mortalidad a los 7 días después de la aplicación. ARGUETA et al. 2011 obtuvo resultados similares con los de la presente investigación, concluyendo que el bioplaguicida más efectivo para el control de D. saccharalis fue Dipel (B. thuringiensis var. kurstaki), el cual alcanzó 90% de mortalidad sobre la población tratada, aproximadamente a los 5 días después de aplicación. En trabajos realizados por RAMOS et al., (2004), afirman que B. thuringiensis variedad kurstaki es un excelente biocontrolador de larvas de D. saccharalis.
ESTRADA et al (1997), en aplicación de B. bassiana para el control de D. saccharalis en un cultivo de caña, obtuvo 30% menos de infestación de la plaga y 27% menos de daño a las plantas, lo que demuestra que este microorganismo disminuye las poblaciones del insecto, y por consiguiente, reduce los niveles de daño producidos en el cultivo.
Sinergismo entre B. bassiana y B. thuringiensisCuando se aplicaron los productos en mezcla: Dipel (1x104 ui/ml) con Bb-HN1 (2x108 ui/ml) y Dipel (1x104 ui/ml) con Micosis (2 x 108 ui/ml), ocasionaron mortalidad a las larvas de Diatraea del 100 y 77,14%, respectivamente. Los productos aplicados de manera individual en las mismas concentraciones anteriores (Dipel, Bb-HN1 y Micosis), ocasionaron mortalidad a las larvas del 44,28; 20,14 y 8,5%, respectivamente (Tabla 3). Los resultados anteriores indican que existe sinergismo entre la bacteria B. thuringiensis y el hongo entomopatógeno en el control de la plaga.
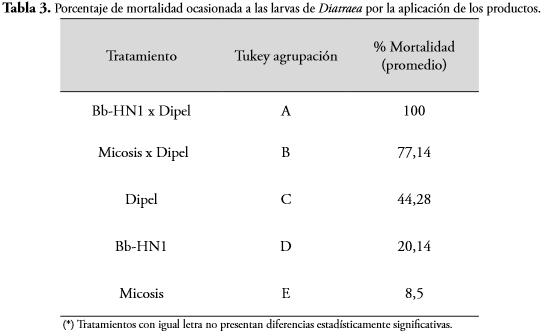
Con respecto al TL50, cuando se aplicó la mezcla de los productos Bb-HN1 x Dipel, en las concentraciones anteriores, el 50% de la muerte de las larvas de Diatraea se alcanzó a los 7,07 días después de la aplicación, mientras que los productos Micosis, Bb-HN1 y Dipel aplicados de manera individual, la mortalidad de las larvas se presentó a los 23,57; 15,14 y 13,21días, respectivamente (Tabla 4).
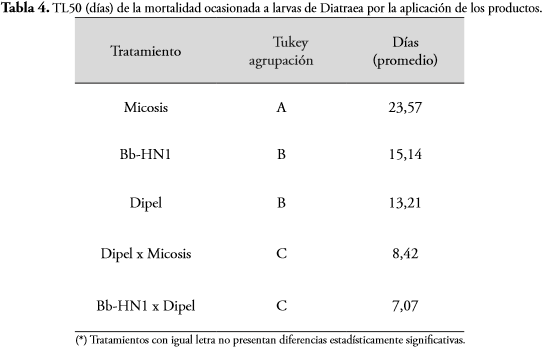
Es evidente observar la viabilidad que se presenta al aplicar la mezcla del hongo entomopatógeno con la bacteria B. thuringiensis para el control de D. saccharalis, ya que se incrementa el control del insecto, aspecto que se debe tener en cuenta al momento de implementar el manejo integrado de la plaga.
AGRADECIMIENTOSA la Vicerrectoría de Investigaciones y Postgrados de la Universidad de Caldas y al Proyecto "Implementación del Centro de Investigación, Innovación y Tecnología al sector Panelero del departamento de Caldas-Centro BEKDAU" por el financiamiento de la investigación.
ALVES, S.B., PADUA, L.E., MILWARD DE AZEVEDO, E.M.V. & ALMEIDA, M.C., 1985.- Controle da broca da cana-de-açúcar pelo uso de Beauveria bassiana. Pesq. Agrop. Bras., 20 (4): 403-407. [ Links ]
ARGUETA A.E. & HERNANDEZ, W., 2011.- Parasitoidismo y control Microbiano del Barrenador (Diatraea saccharalis F.) De la Caña de Azúcar (Saccharum officinarum L.), en el Departamento de Sonsonate, El Salvador, 2009. (Tesis Ingeniero Agrónomo, Universidad de El Salvador). 64p. [ Links ]
BADII, M.H. & ABREU, J.L., 2006.- Control biológico una forma sustentable de control de plagas. Biological control a sustainable way of pest control. Internacional Journal of Good Conscience, 1(1): 82-89. [ Links ]
BLANFORD, S., SHI, W., CHRISTIAN, R., MARDEN, J.H., KOEKEMOER, L.L. & BROOKE, B.D., 2011.- Lethal and pre-Lethal effects of a fungal biopesticide contribute to substantial and rapid control of malaria Vectors. Plos One. 6(8): e23591. [ Links ]
BOTELHO, P.S.M. & MACEDO, N., 2002.- Cotesia flavipes para o controle de Diatraea saccharalis. In: PARRA, J.R.P.; BOTELHO, P.S.M.; CORRÊA-FERREIRA, B.S.; BENTO, J.M.S. (eds.) Controle Biológico no Brasil: Parasitóides e Predadores. Manole: Barueri, p.409-447. [ Links ]
CABRERA, J.C. & PINEDO, E., 1994.- El hongo Beauveria bassiana en el control de algunas plagas agrícolas. Revista Peruana de Entomología, Departamento de Entomologia. UNALM. 37 (1): 107-110. [ Links ]
CRANSHAW, W.S., 2014.- Bacillus thuringiensis. Colorado State University Extension, A division of the office of engagement. Fac Sheet No 5.556. p 2. [ Links ]
ESTRADA, M.E. & GUELMES, J., 2004.- Persistencia de Beauveria basasiana (bálsamo) Vuillemin en las hojas de la caña de azúcar (Saccharum sp. híbrido). Fitosanidad, 8 (4): 53-56. [ Links ]
ESTRADA, M.E., ROMERO, M. & SNOWALL, M., 1997.- Aplicacion de Beauveria bassiana en la lucha biológica contra Diatraea saccharalis. Caña de Azúcar, 15(1): 39-43. [ Links ]
GALLO, D., NAKANO, O., SILVEIRA NETO, S., CARVALHO, R.P.L., BATISTA, G.C., BERTI FILHO, E., & VENDRAMIM, J.D., 2002.- Entomologia Agrícola. São Paulo, Ceres. [ Links ]
GUO, Z., CHENG, Y., HUANG, F., LUTTRELL, R. & LEONARD, R., 2012.- Microarray analysis of global gene regulation in the Cry 1Ab- resistant and Cry1Ab- susceptible strais of Diatraea saccharalis. Pest Manag. Sci. 68: 718-730. [ Links ]
ISLAM, M.D.T., CASTLE, S.J. & REN, S., 2010.- Compatibility of the insect pathogenic fungus Beauveria bassiana with neem against Sweet potato whitefly, Bemisia tabaci, on eggplant. Entomol Exp Appl. 134(1): 28-34. [ Links ]
LECUONA, R.E., TIGANO, M.S. & DIAZ, B.M., 1996.- Characterization and pathogenicity of Beauveria bassiana against Diatraea saccharalis (F.) (Lepidoptera: Pyralidae) in Argentina. Anais da Sociedade Entomológica do Brasil, 25 (2): 299-307. [ Links ]
MENDONÇA, A.F., 1996.- Pragas da Cana-de-açúcar. Maceió: Insecta, 239p. [ Links ]
MOJICA, A. & PAREDES, J., 2004.- El cultivo de la caña panelera y la agroindustria panelera en el departamento de Santander. Centro Regional de Estudios Económicos, Bucaramanga. Banco de la República, Colombia. 26p. [ Links ]
OLIVEIRA, M.A.P de., MARQUES, E.J., WANDERLEY-TEIXEIRA, V. & BARROS, R., 2008a.- Efeito de Beauveria bassiana (Bals.) Vuill. e Metarhizium anisopliae (Metsch.) Sorok. sobre características biológicas de Diatraea saccharalis F. (Lepidoptera: Crambidae). Maringá, 30: 220-224. [ Links ]
OLIVEIRA, M.A.P., WANDERLEY-TEIXEIRA, V., MARQUES, E.J., ALBUQUERQUE, A.C., SANTOS, F.A.B., BARROS, R. & TEIXEIRA, A.A.C., 2008b.- Dinâmica hemocitária em Diatraea saccharalis F. (Lepidoptera: Crambidae) desafiada imunologicamente pelos fungos Beauveria bassiana (Bals.) Vuill. e Metarhizium anisopliae (Metsh.) Sorok. Arq. Inst. Biol. 75: 173-179. [ Links ]
PARRA, J.R.P., BOTELHO, P.S.M., CORRÊA-FERREIRA, B.S. & BENTO, J.M.S., 2002.- Controle biológico no Brasil: Parasitóides e Predadores. Manole: Barueri. 609p. [ Links ]
PINTO, A.S., CANO, M.A. & SANTOS, E.M., 2006.- A broca da cana de açúcar Diatraea saccharalis: 15-20 (en) PINTO, A.S. Controle de pragas da cana de açúcar. Biocontrol, Sertaozinho. [ Links ]
POLANCZYK, R.A., ALMEIDA, L.C., PADULLA, L. & ALVES, S.B., 2004.- Pragas de cana-de-açúcar X métodos alternativos de controle. Revista Biotecnologia & Desenvolvimento. 33: 14-17. [ Links ]
RAMOS, F.C., CARMONA, A., BÉRES, M. & MÉNDEZ, N., 2004.- Evaluación de aislamientos de Bacillus thuringiensis tóxicos a Diatraea saccharalis (Lepidoptera: Pyralidae). Bioagro. 16(3): 183-188. [ Links ]
SABBOUR, M.M. & ABDEL-RAHMAN, A., 2013.- Efficacy of isolated Nomuraea rileyi and Spinosad against corn pests under laboratory and field conditions in Egypt. Ann Rev Res Biol. 3(4): 903-912. [ Links ]
SANTILLANA, E de J., 2002.- Desarrollo de formulaciones de Bacillus thuringiensis a partir de gelatina y o pectina y evaluación tóxica contra el barrenador del tallo de la caña de azúcar Diatraea saccharalis Fabricius. Tesis Maestría en Ciencias con especialidad en Microbiología. Universidad Autónoma de Nuevo León. 128 p. [ Links ]
SVEDESE, V.M., TIAGO, P.V., BEZERRA, J.D.P., PAIVA, L.M.; LIMA, E.A.L.A. & PORTO, A.L.F., 2013.- Pathogenicity of Beauveria bassiana and production of cuticle-degrading enzymes in the presence of Diatraea saccharalis cuticle. African Journal of Biotechnology, 12(46): 6491-6497. [ Links ]
VARGAS, G., LASTRA, L.A., VILLEGAS, A. & BARCO, L.E., 2013.- Diatraea tabernella: Nueva especie de barrenador del tallo en el valle del rio Cauca. Importancia y perspectivas de manejo. Serie divulgativa N° 16. Cali. Cenicaña, Cali. [ Links ]
WENZEL, I.M., GIOMETTI, F.H.C. & ALMEIDA, J.E.M., 2006.- Patogenicidade do isolado IBCB 66 de Beauveria bassiana à broca da cana-de-açúcar Diatraea saccharalis em condições de laboratório. Arquivos do Instituto Biológico, 73: 259 -261. [ Links ]
YASEM, M., SALVATORE, A., LÓPEZ, G. & WILLINK, E., 2008.- Presencia natural de hongos hyphomycetes en larvas invernantes de Diatraea saccharalis F. en caña de azúcar en Tucumán, Argentina. Rev. Ind. y Agric. de Tucumán, 85 (2): 39-42. [ Links ]
ZAHRAN, H.E.D.M., KAWANNA, M.A. & BOSLY, H.A., 2013.- Larvicidal Activity and Joint Action Toxicity of Certain Combating Agents on Culex pipiens L. Mosquitoes. Ann Rev Res Biol. 3(4): 1055-106. [ Links ]
ZAPPELINI, L.O., ALMEIDA, J.E.M., BATISTA FILHO, A. & GIOMETTI, F.H.C., 2010.- Seleção de isolados do fungo entomopatogênico Metarhizium anisopliae (Metsch.) Sorok. visando o controle da broca da cana-de-açúcar Diatraea saccharalis (Fabr., 1794). Arquivos do Instituto Biológico. 77: 75-82. [ Links ]
ZHANG, L., HUANG, F., ROGERS, L.B., CHEN, M., CLARK, T., ZHU, Y.C., WANGILA, D.S., YANG, F. & NIU, Y., 2013.- Susceptibility of cry 1Ab maize -resistant and- susceptible strains of sugarcane borer (Lepidoptera: Crambidae) to four individual cry proteyns. J. Invertebr. Pathol. 112: 267-272. [ Links ]














