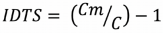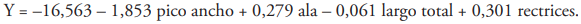Introducción
El dimorfismo sexual se considera que es explicado principalmente por las presiones selectivas que surgen al momento de la elección de pareja, donde los machos compiten entre ellos por hembras para la reproducción (Darwin, 1871). El grado de dimorfismo sexual varía según el sistema de apareamiento de la especie; así, aquellas con estrategias polígamas incluyendo Leks, presentan la diferencia más acusada de fenotipos entre sexos (Webster, 1992; Székely et al., 2000). En especies monógamas estas diferencias tienden a ser tan pocas (Delestrade, 2001; Radford y Du plessis, 2004) que en algunos casos no es posible diferenciar el sexo entre los individuos (Cuthill et al., 1999).
Aunque el dimorfismo sexual en las aves se ha explicado principalmente por el sistema de apareamiento (Owens y Hartley, 1998), el tamaño corporal no se determina solo por selección sexual; otras presiones selectivas influyen en el tamaño de las especies (Andersson, 1994; Blanckenhorn, 2000; 2005). Por ejemplo, se ha planteado que la mortalidad puede afectar de forma distinta a los sexos según su tamaño corporal, además características de historia natural independientes del tamaño corporal, como la morfología y la conducta, pueden estar afectándolos diferencialmente y conllevar al dimorfismo sexual (Blanckenhorn, 2005). El alimento es otra presión selectiva importante sobre el tamaño de un organismo, la hipótesis de partición de recursos plantea que la presión por recursos puede llevar a diferencias en caracteres morfométricos entre los sexos, que relajen la competencia intra especifica al no explotar los mismos recursos (Blanckenhorn, 2005; Székely et al., 2007). En las aves uno de los caracteres que más se ha estudiado en relación con la hipótesis de división de recursos es el pico (Frith, 1997; Moorhouse et al., 1999; Nebel, 2005; Radford y Duplessis, 2003; Suhonen y Kuitunen, 1991; Temeles et al., 2000), ya que su forma y tamaño influye en la dieta, estrategias y sitios de alimentación empleado por los individuos según el sexo (Nebel, 2005; Radford y Du Plessis, 2003).
Conocer el sexo es indispensable para desarrollar investigaciones en áreas como la ecología, historias de vida, comportamiento y conservación de las aves (Dechaume-Moncharmont et al., 2011). Aspectos como defensa territorial, cuidado y socialización de crías, defensa contra depredadores, existencia de cópulas extra pareja (González-Solís et al., 2007; Gunness y Weatherhead, 2002; Hughes, 1998), proporción de sexos a través del tiempo (Yan-Ping et al., 2006), diversidad de hábitats necesarios para la especie (Catry et al., 2006) y patrones evolutivos (Donald, 2007) son algunos de los temas que requieren distinción del sexo entre los individuos y son de gran importancia a la hora del diseño de planes completos para la conservación de especies.
Aunque en especies aparentemente monomórficas se puede identificar el sexo por comportamiento reproductivo (Delestrade, 2001), presencia de parche de incubación o protuberancia cloacal (Gray y Hamer, 2001; Møller, 2002; Lishman, 1985; Suthers, 1994; Yamazaki et al., 1994); estos caracteres son útiles de forma limitada debido a que no aplican para individuos no activos reproductivamente o juveniles. Otras alternativas como laparoscopias (Greenwood, 1983; Jones et al., 1984; Richner, 1989), el análisis de vocalizaciones (Bourgeois et al., 2007) y métodos moleculares (Dubiec y Zagalska-Neubauer, 2006), tienen limitaciones por costos, tiempo requerido, equipos o lo invasivo del procedimiento. La determinación de sexo basada en la morfometría es una alternativa económica y rápida (Dechaume-Moncharmont et al., 2011) que usa un modelo matemático denominado función discriminante (Dechaume-Moncharmont et al., 2011) y se ha demostrado que tienen un alto grado de exactitud en muchas especies (Alarcos et al., 2007; Blanco et al., 1996; Bosch, 1996; Cruz-Bernate et al., 2013; Donohue y Dufty, 2006; Frey et al., 2008; Mawhinney y Diamond, 1999; Wilson, 1999; Zavalaga y Paredes, 1997).
Sicalis flaveola es una especie monógama y social que suele alimentarse en grupos en hábitats abiertos (Marcondes-Machado, 1982; 1997). Es abundante en zonas urbanas y suburbanas y acepta fácilmente cajas nido para su reproducción, lo cual ha facilitado su estudio principalmente en zonas templadas del sur (León et al., 2014; Marques-Santos et al., 2018; Palmerio y Massoni, 2009; 2011; Saldívar y Massoni, 2018; Saldívar et al., 2019). Se conocen cinco subespecies que se distribuyen en Suramérica y están divididas taxonómicamente en dos grupos: a) Pelzeni con S. f. pelzeni (Argentina, Bolivia, Brasil, Paraguay, Uruguay y Chile), S. f. brasiliensis (Brasil) y S. f. koenigi (Argentina) (Rising et al., 2011); y b) Flaveola con S. f. valida (Ecuador y Perú) y S. f. flaveola (Colombia y Venezuela) (Rising et al., 2011). En el grupo Pelzeni hay diferencias en el patrón de coloración del plumaje entre machos y hembras, mientras que en el grupo Flaveola, no. El macho de grupo Flaveola tiene coronilla naranja y una coloración general amarilla con tonos oliváceos en el dorso, alas y cola, y la hembra es similar al macho con la coronilla aparentemente menos brillante (Hilty y Brown, 2001; Rising et al., 2011), pero esta diferencia no es siempre apreciable en campo. Tampoco se aprecian diferencias morfológicas como en el tamaño corporal entre sexos. Pese a los avances en el conocimiento sobre la especie en la zona templada, su amplia distribución y los primeros trabajos en Colombia (Burnham, 2019; Espinosa et al., 2017), aún no hay estudios que aborden las diferencias puntuales en morfometría de los adultos en la subespecie del norte de Suramérica. El objetivo de este estudio fue determinar si existían diferencias morfométricas entre los sexos en el S. flaveola flaveola y proponer una función discriminante lineal que permitiera la identificación del sexo de manera rápida en campo.
Métodos
Áreas de estudio
El trabajo se desarrolló entre 2017 y 2019 en el campus universitario de la Universidad del Valle, Cali y zonas verdes de la ciudad de Jamundí, Valle del Cauca (Figura 1).
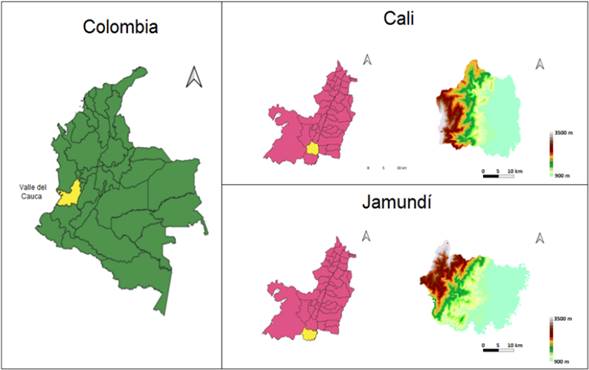
Fuente: elaboración propia.
Figura 1 Áreas de estudio, municipios de Cali y Jamundí, Departamento del Valle del Cauca, suroccidente de Colombia.
Universidad del Valle
El campus de la universidad está situado en el municipio de Cali, departamento del Valle del Cauca (3° 22’ N, 76° 32’ W, 970 m). El promedio anual de las temperaturas mensuales fue de 24.1°C y la humedad relativa promedio fue del 73%. La precipitación anual promedio para el periodo entre 1965 y 2001 fue 1471 mm, con dos picos anuales de lluvia, de marzo a mayo y de septiembre a noviembre. De acuerdo con sus características climáticas, corresponde a la Zona Natural de Vida bosque seco tropical (bs-T), según el sistema de clasificación de Holdridge (Espinal, 1967). El campus tiene un área de aproximadamente 100 ha, de las cuales 8.5 ha están ocupadas por edificaciones, 44 ha por árboles, 45.5 ha por prados y pastizales y 1 ha por dos lagos (Ardila-Téllez y Cruz-Bernate, 2014).
Jamundí
La investigación incluyó áreas de vegetación urbana del municipio de Jamundí, departamento del Valle del Cauca (3° 15’ N, 76° 33’ W, 998 m). La precipitación promedio anual fue de 1777 mm, con dos períodos de lluvias con sus máximos en abril y noviembre y una época seca con un mínimo en junio. El promedio anual de las temperaturas mensuales fue de 23.7 °C sin presencia de diferencias acusadas entre sus meses (Estación Meteorológica La independencia, CVC, 2019). De acuerdo con sus características climáticas, esta región corresponde a la zona natural de vida Bosque húmedo Tropical (bh-T), según el sistema de clasificación de Holdridge (Espinal, 1967).
Métodos de campo
Para la captura de los individuos, se instalaron periódicamente diez redes de niebla (12 m x 2.5 m y ojo de malla de 30 mm) entre las 07:00 - 15:00 h en el campus de la Universidad del Valle y entre las 17:00 - 19:00 h en Jamundí. Además, se capturaron parejas que se encontraron reproduciéndose en las cajas nido instaladas en el campus universitario. Para las capturas de estas, se usó una puerta móvil ubicada en la entrada del nido durante la fase de alimentación de los polluelos. Se logró capturar 198 individuos que recibieron una combinación única de anillos en la región del tibio tarso para su reconocimiento individual (Figura 2).

Fuente: Esther Vallejo Santamaría.
Figura 2 Adulto de Sicalis flaveola con combinación de anillos metálico y de color en el tibio tarso para su reconocimiento individual, Departamento del Valle del Cauca, Colombia.
Morfometría
A cada adulto se le midieron 12 caracteres morfológicos: masa corporal; largo, ancho y alto del pico; comisura; narinas; ala; distancia primarias-secundarias; tarso-metatarso; halux; rectrices, y largo total. Para la masa corporal se empleó una balanza digital con ± 0,01 de precisión. Se utilizó un calibrador digital ((± 0,01 mm) para medir el largo del pico desde su base hasta el extremo distal. El ancho del pico se registró como la distancia horizontal a nivel de las narinas, alto del pico como la distancia vertical a nivel de las narinas, comisura como la mayor distancia horizontal a nivel de la base del pico y narinas se consideró como la distancia entre fosas nasales (Figura 3). El ala se midió desde la muñeca hasta la primaria más larga sin aplanar su curvatura; distancia primarias-secundarias fue medida como la distancia entre los extremos distales de la primaria y la secundaria más larga del ave con el ala en posición de reposo; tarso-metatarso se midió como las distancia entre la articulación intertarsal y la articulación con las falanges. El halux se midió como el largo de la falange sin incluir la longitud de la uña, la longitud de las rectrices se tomó desde la base de las plumas centrales hasta la pluma más larga. Con una regla (± 0,1 mm) se midió el largo total, que correspondió a la distancia entre la cabeza y el extremo distal de las rectrices, con el ave en reposo en una superficie horizontal. Los tres investigadores contribuyeron con la toma de medidas de los individuos. A todos los individuos se les suministró suplemento nutricional líquido como compensación por la energía gastada durante la medición y se liberaron en el mismo lugar de captura.

Fuente: Lorena Cruz-Bernate.
Figura 3 Medidas morfométricas a) largo del pico, b) narinas, c) ancho del pico y d) comisura en adultos de Sicalis flaveola en el Departamento del Valle del Cauca, Colombia.
Para determinar las variables morfométricas que explicaron mejor el fenómeno de variación entre los sexos se realizó un análisis de función discriminante lineal, después de evaluar los supuestos de normalidad (Anderson-Darling) y homogeneidad de varianzas en las matrices de covarianza con la prueba M de Box (Morrison, 1976; Thode, 2002). El análisis de la función discriminante se realizó excluyendo una a una las variables morfométricas para obtener la combinación de variables óptima en la determinación del sexo. Se estimó la precisión de la ecuación con la validación cruzada, con el método de Jackknife (Venables y Ripley, 2002). Se evaluó el nivel de significancia estadística de la función discriminante, utilizando los criterios estadísticos Lambda de Wilks, un método para la selección de variables por pasos del análisis discriminante que selecciona las variables para su introducción en la ecuación basándose en cuánto contribuyen a disminuir la Lambda de Wilks (Sokal y Rohlf, 1995). Todos los análisis estadísticos se ejecutaron en el paquete de libre acceso denominado R (R CORE TEAM 2019).
Además, se empleó el índice de dimorfismo sexual en tamaño (IDTS), propuesto por Lovich y Gibbons (1992):
Donde, Cm = promedio de la medida corporal del sexo más grande.
C = promedio de la medida corporal del sexo opuesto.
Un IDTS de 0.05 es equivalente a una diferencia de 5% en el tamaño promedio entre ambos.
Determinación del sexo
Se empleó tanto determinación morfológica como molecular del sexo. La determinación morfológica consistió en la inspección visual de los individuos para la identificación de caracteres como parche de incubación para las hembras y protuberancia cloacal para los machos (Figura 4). La determinación molecular se efectuó mediante el método propuesto por Ellegren (1996) e implementado para la especie por Espinosa et al. (2017). Consistió en la amplificación de un intrón comprendido entre el nucleótido 2550 y 2718 del gen CDH1 (Dominio Cromo-Helicasa) ubicado en los cromosomas sexuales de las aves (W, Z). Para ello se tomó muestra sanguínea de 10 µl, con la punción de la vena braquial. La muestra se conservó en un microtubo con buffer de lisis en el Laboratorio de Ornitología y Comportamiento Animal-OYCA de la Universidad del Valle. El protocolo para la extracción del ADN fue el denominado extracción por sales o “Salting Out” (Gustincich et al., 1991). Para la reacción en cadena del ADN polimerasa (PCR) se emplearon los iniciadores 2550F-2718R (Fridolfsson y Ellegren, 1999). Los productos amplificados se separaron en geles de agarosa al 1% (Sambrook y Russell, 2001) (Figura 5).

Fuente: Camilo Espinosa Bravo e Isabel Castro.
Figura 4 Caracteres morfológicos de individuos reproductivamente activos. A. Parche de incubación en hembras. B. Protuberancia cloacal en machos de Sicalis flaveola en el Departamento del Valle del Cauca, Colombia.
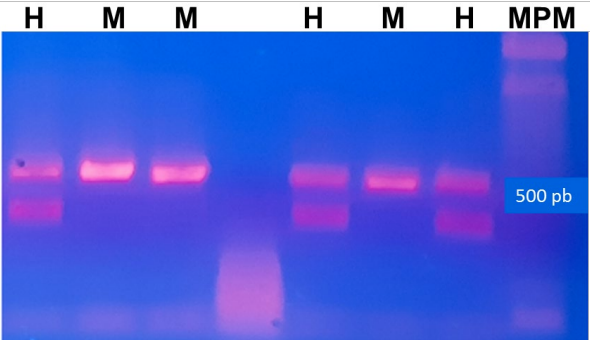
Fuente: Camilo Espinosa Bravo.
Figura 5 Gel de agarosa al 1% productos de la amplificación del intrón comprendido entre el nucleótido 2550 y 2718 del gen CHD1 de Sicalis flaveola, Departamento del Valle del Cauca, Colombia. MPM = marcador de peso molecular de 100 pb; H = hembras con dos bandas CHD1Z y CHD1W (600 y 450 pb respectivamente) y M = machos con una banda CHD1Z (600 pb).
Resultados
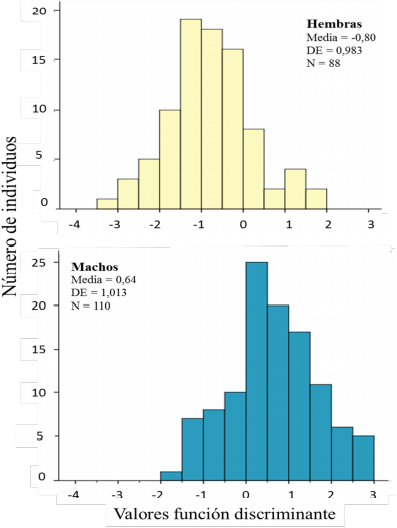
Se capturó un total de 198 individuos, 20 en Jamundí y 178 en Cali, correspondientes a 88 hembras y 110 machos. La identificación del sexo por caracteres morfológicos y comportamiento reproductivo correspondió 100% con el método molecular. Todas las medidas morfométricas (Tabla 1) cumplieron el supuesto de normalidad y homogeneidad de varianzas entre las matrices de covarianza (Box M Aprox = 1,791, gl1 = 10, gl2 =164521,152, p = 0,056), excepto por el Halux. Los machos presentaron alas y rectrices significativamente más largas que las hembras, mientras que las hembras presentaron un pico más ancho que los machos (Tabla 1). La distancia entre primarias-secundarias presentó diferencias significativas pero con un grado de precisión del 91,8% y sin embargo, fue la única medida corporal con diferencias importantes en el IDTS (Tabla 1). Esto significa que los machos presentan diferencias, entre sus plumas de vuelo, 13% más grandes que las hembras.
Tabla 1 Comparación de masa corporal (g), medidas morfométricas (mm) (media ± DE) e Índice de Dimorfismo Sexual en Tamaño (IDTS), en machos y hembras de Sicalis flaveola, Departamento del Valle del Cauca, suroccidente de Colombia.
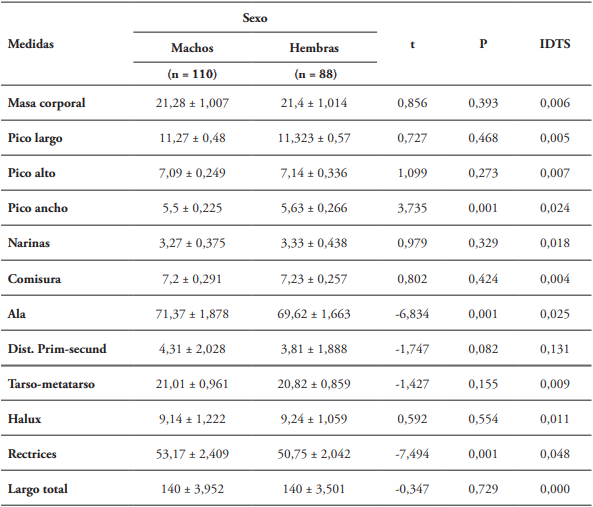
Fuente: elaboración propia.
Las variables que mejor explican las diferencias morfométricas y permiten distinguir entre sexos está dada por la siguiente función discriminante:
Si y < 0 el ave se clasifica como hembras, y si y > 1 se considera macho (Figura 6). La ecuación permitió identificar correctamente el 77,8 % de los individuos. Con lo anterior se puede constatar que la especie posee un dimorfismo críptico y se propone una función discriminante que permite clasificar a los individuos según el sexo con base en sus medidas morfológicas.
Discusión
La variación en el tamaño corporal entre los sexos de S. flaveola es pequeña. Los machos presentaron mayores medidas relacionadas con el desplazamiento aéreo como alas y rectrices (variables altamente correlacionadas); mientras que las hembras tuvieron mayores dimensiones en aspectos óseos como el ancho del pico. A pesar de que S. flaveola no presenta la magnitud de la diferencia esperada para paserinos monógamos donde los machos tienen alas 5% más grandes que las hembras (Delestrade, 2001; Kissner et al., 2003; Regosin y Pruett-Jones, 2001); ellos sí tienen alas significativamente más largas que las hembras, solo que en una proporción de 2,5 %. La especie posee otra característica importante respecto a la diferenciación entre sexos; los machos tienen mayores diferencias en la longitud entre las plumas secundarias y primarias en comparación con las hembras. Se ha demostrado que esta medida de relación de aspecto se relaciona con las habilidades de desplazamiento de los individuos, como por ejemplo durante el comportamiento migratorio (Baldwin et al., 2010; Lockwood et al., 1998), dispersión natal (Dawideit et al., 2009; Derryberry et al., 2011) y capacidad diferencial de vuelo (Claramunt et al., 2012; Dawideit et al., 2009).
Los machos de S. flaveola flaveola tienen territorios exclusivos que defienden de sus congéneres a lo largo del año, lo cual implica desplazamiento rápido, oportuno y preciso hasta el límite de su territorio donde se aproxima al contendor, en varias ocasiones emitiendo vocalizaciones (Espinosa, 2015). Es probable que el papel que desempeña el macho en esta actividad se vea favorecido por las características de relación de aspecto de sus alas. Norberg (1995) argumenta que el largo de la cola y la forma del ala influyen en la velocidad y eficiencia energética del vuelo. Así, una mayor eficiencia en vuelo puede ser una adaptación que compense la inversión energética que invierte el macho en vocalizaciones y defensa del territorio, especialmente en la etapa de incubación.
Durante la época reproductiva se observa que las alas desempeñan un papel protagónico en los despliegues de cortejo por parte del macho. Ellos las agitan vigorosamente frente a la hembra lo cual puede desencadenar aceptación o no por parte de ella. Las rectrices por su parte, se posicionan hacia arriba de tal manera que equilibran al individuo durante sus despliegues. Se ha demostrado que diferencias en la longitud de las rectrices contribuyen con las manobras de cortejo, balance, eficiencia energética, capacidad de vuelo y aceleración entre otras (Norberg, 1995; Thomas, 1996; 1997; Thomas y Taylor, 2001; Warrick et al., 2002). Proponemos que la mayor longitud de las alas y las rectrices pueden estar involucradas también en la transmisión de señales acerca del individuo cortejante durante la elección de pareja en S. flaveola, como ocurre en otras especies tales como Hirundo rustica, Panurus biarmicus y Euplectes progne; quienes durante el establecimiento del vínculo de pareja presentan preferencias sexuales por individuos con diferencias en la expresión del carácter: longitud de rectrices (Andersson, 1982; Andersson y Andersson, 1994; Cuervo et al., 1996; Romero-Pujante et al., 2002; Møller et al., 2006).
Aunque la selección sexual se plantea como la principal fuerza de selección sobre el dimorfismo sexual (Blanckenhorn, 2005; Székely et al., 2007), existen otras presiones que afectan el tamaño corporal. Por ejemplo, las diferencias en la dimensión y forma del pico pueden responder a dietas distintas o diferentes estrategias para obtener el alimento (Gosler, 1987; Radford y Du Plessis, 2003) encontrándose incluso en Parus major, cambios anuales en la forma del pico en respuesta al alimento disponible según la estación (Gosler, 1987). Se plantea que el mayor ancho del pico en las hembras de S. flaveola, puede estar relacionado con diferencias en la dieta o con estrategias empleadas para alimentarse, de manera que se relajaría la competencia intersexual. Partición en el uso del hábitat es un aspecto a tener en cuenta cuando de diseño de estrategias de conservación de especies se refiere.
La ecuación del análisis discriminante lineal para la especie en el suroccidente colombiano tiene una precisión del 77,8 % y se convierte es una herramienta útil para investigación en campo, cuando no se tiene la posibilidad de hacer la determinación del sexo por métodos morfológicos relacionados con la condición reproductiva o por análisis moleculares con ADN. Se debe considerar evaluar otras medidas morfométricas no convencionales, que sean lo suficientemente informativas y que ayuden aumentar la precisión de la ecuación, como en Vanellus chilensis (Cruz-Bernate et al., 2013). Además, la edad del ave es una variable que se debe tener en cuenta debido a que la morfometría de las aves puede variar con la edad; por ejemplo, en Icteria virens el largo del ala aumenta en cada muda (Francis y Wood, 1989).
La implementación de la ecuación en otras poblaciones debe hacerse con análisis previos, debido a que se conoce que existen variaciones geográficas en el tamaño corporal en las poblaciones de aves (Conklin et al., 2011; Symonds y Tattersall, 2010). En el caso de Leucophaeus atricilla se tuvo que modificar el número de variables morfométricas incluidas en el análisis discriminante lineal para lograr aplicación y precisión de la ecuación en otra población (Evans et al., 1993). Debido a la amplia distribución de la especie (Rising et al., 2011), sería interesante hacer estudios de variaciones geográficas y determinar si existen diferencias en la biología conductual que se relacionen con las diferencias morfológicas en diferentes regiones del país, e inclusive en otros países donde se encuentra distribuida la subespecie como por ejemplo en Venezuela. Ya se tiene evidencia de diferencias morfométricas entre las subespecies S. f. flaveola y S. f. pelzeni; esta última con distribución en Argentina, es tres gramos más liviana, y con tarso 3,5 mm más pequeño en promedio que S. f. flaveola en Colombia (Palmerio, 2012; Espinosa et al., 2017).
Concluimos que la subespecie S. f. flaveola, con distribución en el territorio colombiano, presenta diferencias morfológicas pequeñas entre sexos, lo que significa que presenta dimorfismo sexual críptico. Se sugieren presiones de selección sexual y competencia por recursos alimenticios como moldeadores del dimorfismo para la especie. Las diferencias, que no son fáciles de detectar a la vista, pueden ser utilizadas para la determinación del sexo con la ecuación matemática aquí propuesta, con una precisión del 77,8%.