Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Biotecnología
Print version ISSN 0123-3475
Rev. colomb. biotecnol vol.13 no.1 Bogotá Jan./June 2011
ARTÍCULO DE INVESTIGACIÓN
Efecto de diámetro de esfera y densidad celular en la producción de etanol con levadura inmovilizada en alginato
Effect of pellet diameter and cell density on ethanol production with alginate immobilized yeast
Título corto: Producción de etanol con levadura inmovilizada
Martha V. Jiménez * , Gabriella G. Zarkovic * , Gretty K. Villena * , Marcel Gutiérrez-Correa *
* Investigadores del Laboratorio de Micología y Biotecnología, Universidad Nacional Agraria La Molina, Lima, Perú. gkvch@lamolina.edu.pe mgclmb@lamolina.edu.pe
Recibido: diciembre 06 de 2009 Aprobado: mayo 09 de 2011
Resumen
Las células inmovilizadas tienen aplicación potencial en la producción de biocombustibles posibilitando la reutilización de biomasa, el empleo de diversas configuraciones de reactores y sistemas de cultivo, el manejo de altas densidades celulares alcanzando altas productividades volumétricas, y la simplificación de operaciones de procesamiento de salida. El objetivo del presente estudio fue evaluar la influencia del diámetro de las perlas y la densidad celular en la producción de etanol con Saccharomyces uvarum inmovilizada en alginato al 2% (p/v). Para ello se evaluaron tres diámetros de perlas de 2, 2,5 y 3 mm. Las células inmovilizadas fueron cultivadas en medio con 12% (p/v) de glucosa en biorreactores de columna sin agitación a 28 ºC, y se operaron cuatro lotes consecutivos de 48 horas cada uno. En cada lote se cuantificó el consumo de glucosa y se determinó la cantidad de etanol producido. Los rendimientos máximos de etanol para las esferas de 2, 2,5 y 3 mm de diámetro fueron 81, 83 y 97% del rendimiento teórico. La máxima productividad volumétrica de etanol fue 1,2 g/L-1/h-1 con un consumo de glucosa de 99,8% al término del lote, correspondiente a las columnas con perlas de 3 mm y con una producción de 0,017 g de etanol por esfera. La producción de etanol acumulada en cada sistema fue 178, 189 y 200 g/L-1 para 2, 2,5 y 3 mm respectivamente, encontrándose una relación directa con el diámetro de perla e inversa respecto a la densidad celular. Los rendimientos de etanol obtenidos son superiores a los reportados para la misma especie.
Palabras clave: inmovilización, alginato, Saccharomyces uvarum, etanol, lote repetido.
Abstract
Immobilized cells have a potential use in biofuel production. They also allow re-using biomass, using diverse reactor configurations and culture systems, handling high cell densities to obtain high volumetric productivities and to simplify the downstream processing. The purpose of this work was to evaluate the influence of bead diameter and cell density on ethanol production using immobilized Saccharomyces uvarum in 2% (w/v) alginate. For that, three bead diameters (2, 2.5 and 3 mm) were evaluated. Immobilized cells were cultured on a 12% (w/v) glucose medium in column bioreactors without agitation at 28 °C for four 48 h–repeated batches. For each batch, both glucose consumption and ethanol produced were measured. Maximum yields for 2, 2.5 and 3 mm bead diameters were 81, 83 and 97% of theoretical yield. Maximum volumetric productivity of ethanol was 1.2 g/L-1/h-1 with 99.8% glucose consumption at the end of the batch, corresponding to the 3 mm bead diameter and the ethanol production per bead was 0.017 g. Accumulated ethanol production for each system was 178, 189 and 200 g/L-1 for 2, 2.5 y 3 mm bead diameter, respectively, being this directly related to bead diameter and inversely related to cell density. Ethanol yields were higher than those reported for the same species.
Key words: Immobilization, alginate, Saccharomyces uvarum, ethanol, repeated batch.
Introducción
La inmovilización de células tiene múltiples aplicaciones en biotecnología, biomedicina y ambiente. Entre las principales ventajas que ofrecen las células inmovilizadas se incluyen: la posibilidad de llevar a cabo reacciones complejas o acopladas, la reutilización de biomasa, una mayor estabilidad del biocatalizador, mayor productividad, la facilidad operativa, el bajo consumo de energía, y la baja contaminación ambiental, entre otras (Martynenko y Gracheva, 2003; Freeman y Lily, 1998; Salter y Kell, 1991). Se considera que los sistemas de células inmovilizadas pueden separarse en totalmente artificiales y naturales (Junter y Jouenne 2004), aunque la inmovilización "natural" o "pasiva" es realmente un proceso biológico que da lugar a una biopelícula (Gutiérrez-Correa y Villena, 2003). Por tanto, la inmovilización de células se debe referir solamente a un sistema de ingeniería para la retención artificial de células sobre o dentro de un soporte o matriz.
Para la inmovilización de células por atrapamiento, los geles de alginato de calcio son los más utilizados (Manojlovic et al., 2006). Entre las ventajas de este método están la facilidad para manipular las propiedades gelificantes y la resistencia del gel (Sree et al., 2000). Además, cuando la inmovilización se realiza en perlas de alginato, estas pueden ser resolubilizadas, con lo que se obtienen células libres para su conteo o evaluación. La diferencia del alginato con otros geles como el agar, radica en que el primero es térmicamente irreversible, lo que permite trabajar a temperaturas elevadas (Guiseley, 1989). De otro lado, este es un sistema ideal para la reutilización del biocatalizador y su utilización en diversos tipos de fermentación (Sree et al., 2000).
Una de las aplicaciones más destacables de la inmovilización de células es la producción de etanol (Nuñez y Lema, 1987). Debido a la creciente demanda de este biocombustible, se incrementa la necesidad de emplear tecnologías económicas y microorganismos con altos rendimientos (Lin y Tanaka, 2006). En este aspecto, la fermentación alcohólica con células inmovilizadas ofrece un mayor rendimiento con un menor empleo de recursos, en comparación con la fermentación con células libres; además, tiene una tasa más alta de fermentación, ya que permite operar a una alta densidad celular por unidad de volumen, y permite la recuperación in situ de células, con lo que se facilitan las operaciones de recuperación de biomasa y producto. Esto, a su vez, incrementa la tolerancia de los microorganismos al etanol y reduce costos de producción de inóculo (Sree et al., 2000; Norton y D’Amore, 1994).
Históricamente, los microorganismos más utilizados en la producción de etanol han sido las levaduras. Entre ellas, Saccharomyces puede producir hasta 18% de etanol y crece en glucosa o sacarosa, por lo que es comúnmente utilizada para la producción de etanol. En general, el género Saccharomyces es reconocido como GRAS (generally recognised as safe) y puede emplearse en forma segura como aditivo alimenticio, producción de bebidas alcohólicas e industria de panificación (Lin y Tanaka, 2006).
Si bien el método de inmovilización de células por atrapamiento en geles tiene varias ventajas, posee también como desventajas la escasa permeabilidad a moléculas de sustrato con elevado peso molecular y, en general, limitaciones en la transferencia de materiales a las células. En tal sentido, el objetivo del presente estudio fue evaluar el efecto del diámetro de las perlas de alginato y la densidad celular sobre la producción de etanol con células inmovilizadas de Saccharomyces uvarum.
Materiales y métodos
Microorganismo. Se utilizó la cepa Saccharomyces uvarum NRRL Y-11877, la cual se mantuvo en cuñas de agar Saboraud.
Inmovilización de células en esferas de alginato
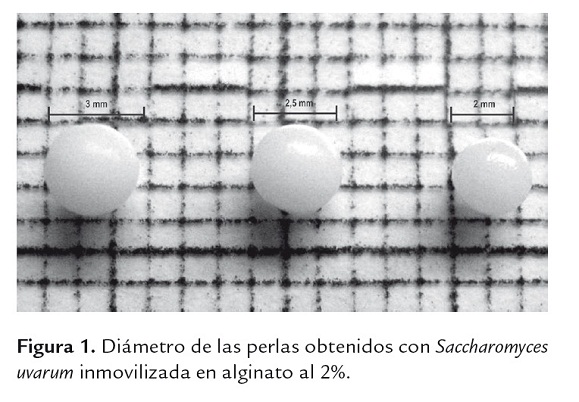
Las células de levadura utilizadas para inmovilización se obtuvieron a partir de cultivos de 24 horas de crecimiento en matraces de 250 mL conteniendo 20 mL de caldo saboraud a 28 ºC con agitación de 175 rpm. Para separar las células, el medio de cultivo fue centrifugado a 4000 rpm durante 12 minutos descartando el sobrenadante y lavando la biomasa con 30 mL de una solución de NaCl al 0,85% (p/v) por 3 veces. La biomasa obtenida, de aproximadamente 25 mg de peso fresco, según la densidad por probar, se resuspendió con 5 mL de NaCl al 0,85% y se le agregaron 5 mL de solución de alginato al 4% (p/v). La mezcla homogénea fue absorbida con jeringas estériles de diferentes tamaños de aguja para obtener diferentes diámetros de perla, como se muestra en la figura 1. La mezcla se dejó gotear sobre una solución de CaCl2 0,05 M para permitir la gelificación de las perlas de alginato. Una vez formadas, las perlas se mantuvieron en refrigeración por 12 h en CaCl2 0,05 M. Finalmente, se lavaron con suero fisiológico estéril 3 veces antes de ser transferidas a los microbiorreactores.
Determinación de la densidad celular por perla
Para determinar la densidad celular, cada perla se colocó en un tubo de microcentrífuga que contenía 1,5 mL de buffer citrato 0,1 M a pH 4,8 y se incubó por 15 min a temperatura ambiente para solubilizar el alginato. Luego, se agitó vigorosamente el tubo para obtener una solución líquida homogénea. El conteo celular se realizó en una cámara de Neubauer. Se realizaron cuatro repeticiones para cada diámetro de perla.
Medio de cultivo. El medio de fermentación para la producción de etanol tuvo la siguiente composición: KH2PO4 1 g/L; MgSO4·7H2O 1 g/L y glucosa 120 g/L; con un pH final de 4,5.
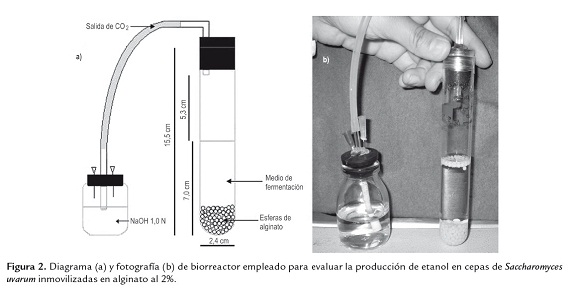
Biorreactor. Se utilizaron biorreactores de columna construidos con tubos de vidrio de 15 cm de longitud y 2,4 cm de diámetro, cada uno conectado a un frasco colector de CO2 como se muestra en la figura 2. La altura del líquido fue de 7 cm y el espacio de cabeza 5,3 cm.
Condiciones del cultivo. Los biorreactores contenían, cada uno, 20 mL de medio de fermentación y se operaron durante 4 lotes consecutivos de 48 horas cada uno, a 28 °C, sin agitación. Luego, el medio de fermentación de cada lote fue reemplazado por un volumen igual de medio fresco. Los frascos colectores de CO2 fueron reemplazados cada 24 horas.
Análisis
La concentración de etanol fue determinada mediante oxidación con dicromato de potasio utilizando una reacción de titulación redox (Pilone, 1985; Archer et al., 2007; Seo et al., 2009). Se preparó una solución de dicromato de potasio en ácido sulfúrico diluido (0,1 M Cr2O72- en H2SO4 5 M). Un mL de muestra de etanol contenida en un vial de plástico se introdujo en un matraz de 250 mL con 15 mL de la solución de dicromato de potasio. El vial se mantuvo suspendido al interior y el matraz fue sellado e incubado a 50 oC por una noche. En estas condiciones, el etanol se evaporó entrando en contacto con el dicromato. La solución resultante fue titulada con una solución de tiosulfato de sodio al 0,03 M. Por relación estequiométrica, 1 mol de tiosulfato de sodio fue equivalente a 0,25 moles de etanol.
El CO2 producido fue cuantificado por titulación con BaCl2 de acuerdo con lo descrito por Sugama y Okasaki (1979). El CO2 fue colectado en frascos con 30 mL de una solución 1,0 N de NaOH. Para la titulación, el contenido de cada frasco fue transferido a un matraz de 250 mL y se le añadieron 10 mL de una solución al 10% (p/v) de BaCl2. La mezcla se tituló con HCl 1,0 N, utilizando fenolftaleína como indicador. La medición de CO2 se hizo cada 24 horas. La glucosa residual en el medio de fermentación se determinó mediante el ensayo de azúcares reductores de Miller (1959).
Análisis estadístico. Los resultados fueron analizados por el software Statistical Analisis System® (Version 8.1) (SAS Institute, Inc., Cary, NC, USA), teniendo en cuenta el análisis de varianza por el procedimiento de Modelos Lineales Generales y la prueba de Duncan de rangos múltiples. Para los análisis estadísticos se consideraron cuatro repeticiones.
Resultados
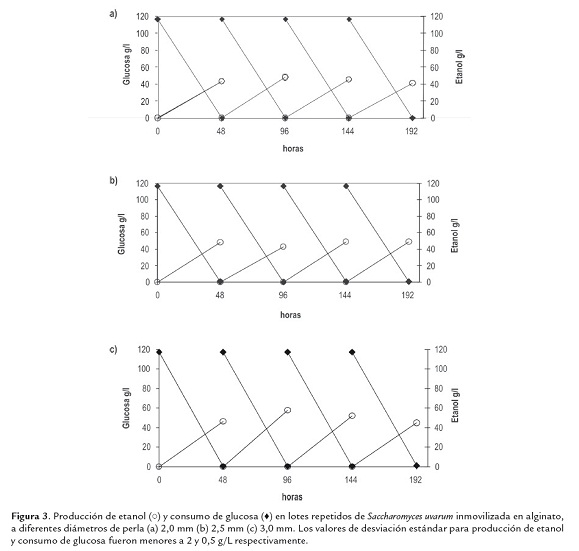
Se cultivó Saccharomyces uvarum NRRL Y-11877 (Saccharomyces bayanus) inmovilizada en perlas de alginato en microrreactores para la producción de etanol (figura 2). La figura 3 muestra producción de etanol y consumo de glucosa. La producción de etanol fue variable en el tiempo respecto al diámetro de perlas. Para las perlas de 2 mm de diámetro (figura 3a) se alcanzó una producción máxima de etanol de 48,02 g/L-1 en el segundo lote (48-96 horas de incubación), disminuyendo en 7 y 15% en los dos últimos lotes respectivamente. En las perlas de 2,5 mm de diámetro (figura 3b), la producción de etanol se mantuvo casi constante, con un máximo de 49,27 g/L-1 correspondiente al cuarto lote (144-192 horas de incubación). La producción de etanol en las perlas de 3 mm de diámetro (figura 3c) fue la máxima registrada alcanzando 57,75 g/L-1, con un rendimiento del 97% correspondiente al segundo lote (48-96 horas de incubación), disminuyendo en los lotes sucesivos hasta en un 22%. El consumo de glucosa fue similar en todos los casos.
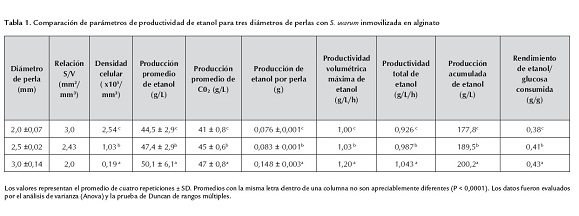
Con los datos obtenidos se comparó la producción de etanol respecto a la relación superficie/volumen (S/V) y densidad celular para los diferentes diámetros. Los resultados se muestran en la tabla 1. De acuerdo con esto, la relación S/V es inversa al diámetro de las perlas obteniéndose una menor relación S/V para las perlas de 3 mm. Sin embargo, debido a la menor densidad celular obtenida en este diámetro de perla se consiguió una mayor producción de etanol. Con base en ello, la producción promedio de etanol mostró una relación directa con el diámetro de perla e inversa respecto a la densidad celular, resultando una mayor producción promedio de etanol de 50,1 g/L para las perlas de 3 mm de diámetro. Así también, la producción acumulada de etanol durante los 4 lotes fue de 177,8, 189,,5 y 200,2 g/L para las perlas de 2, 2,5 y 3 mm de diámetro respectivamente, encontrándose una relación lineal (R2 = 0,99). Asimismo, el CO2 producido en cada sistema fue concordante con la producción de etanol.
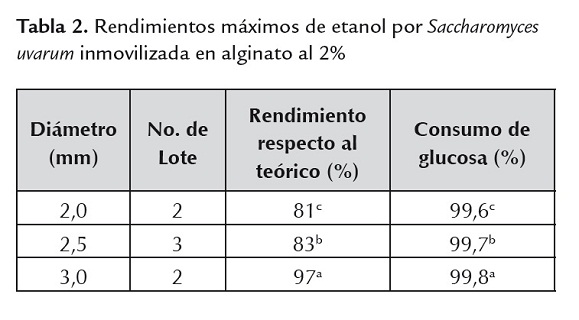
En concordancia con la producción de etanol, la mayor productividad volumétrica alcanzada correspondió a los biorreactores con perlas de 3 mm, siendo 1,2 g/L/h. Además, la productividad total alcanzada por este mismo sistema (1,043 g.L.h) fue significativamente mayor respecto a los diámetros de 2,,5 y 2 mm (0,98 g/L/h y 0,926 g/L/h, respectivamente). Por último, en la tabla 2 se presentan los rendimientos máximos para cada diámetro de perla, observándose que la producción de etanol por perla es superior en aquellas de 3 mm de diámetro para el segundo lote, alcanzando un 97 % del rendimiento teórico.
Discusión
Aunque S. cerevisiae es la principal responsable en la fermentación alcohólica, otras especies de Saccharomyces sensu stricto, como S. bayanus (S. uvarum) y S. paradoxus pueden actuar también como cultivos iniciadores de la fermentación (Querol et al., 2003; Redzepovic et al., 2002). Se ha reportado que algunas especies de S. bayanus tienen características de fermentación inusuales y específicas, con altas tasas de crecimiento y mejor fermentación a bajas temperaturas en comparación a S. cerevisisae, además de su alta capacidad de producción de aromas (Masneuf et al., 1998; Querol et al., 2003). Sin embargo, existen pocos reportes sobre su comportamiento en inmovilización (Mc Ghee et al., 1982).
La inmovilización de células por atrapamiento en gel tiene algunas limitaciones, principalmente referidas a las restricciones difusionales internas, por lo que el tamaño de perla es un parámetro importante por considerar. La estrategia más común para mejorar la transferencia interna de masa es reducir el diámetro de perla, lo cual conlleva una situación de compromiso de elegir el menor tamaño posible, manteniendo las características operativas de las perlas (Norton y D’Amore, 1994).
Los problemas difusionales y, por tanto, el diámetro de perla también tienen influencia en la producción de etanol (Lin y Tanaka, 2006). Se han reportado problemas difusionales con diámetros mayores a 3,5 mm (Norton y D’Amore, 1994). Los resultados obtenidos en este estudio con S. uvarum (S. bayanus) coinciden con esto, ya que se registró un aumento en la producción y rendimiento de etanol hasta un diámetro de 3 mm, pero se obtuvo lo contrario a lo obtenido en un estudio semejante con Saccharomyces cerevisiae (Göksungur et al., 2001), en el cual la producción de etanol disminuyó a medida que se incrementó el diámetro de las perlas, obteniendo producciones de 42,7, 46,2 y 38,1 g/L para los diámetros 1,3 – 1,,7, 2,0 – 2,4 y 2,8 – 3,2 mm, respectivamente. Aunque al aumentar el tamaño de las perlas disminuye el área superficial disponible para la transferencia de masa de sustrato dentro y a través de las perlas (Goksungur et al., 2001), se han reportado cambios fisiológicos y metabólicos relacionados con procesos de inmovilización celular. Estos cambios podrían atribuirse a una modificación en el entorno físico y químico de las células inmovilizadas, estrechamente asociados a limitaciones en transferencia de masa al interior del sistema, lo cual puede contrarrestarse por el empleo de monocapas celulares o trabajando a bajas densidades celulares (Norton y D’Amore, 1994). Según esto, los resultados obtenidos en el presente estudio para las perlas de 3 mm de diámetro en las que se obtuvo la mayor productividad de etanol a pesar de tener menor relación S/V, mostrarían un importante efecto de la densidad celular para la transferencia de masa, lo cual no ha sido evaluado en los estudios mencionados. De acuerdo con el diseño de los experimentos, la densidad celular fue menor conforme se aumentó el diámetro de las perlas, con lo cual esta resulta ser el parámetro más significativo en relación con los problemas difusionales (cuadro 1).
Desde el punto de vista operativo, el diámetro de 3 mm es aún manejable, mantiene su resistencia y permite la fácil separación de biomasa. Otros autores han reportado diámetros óptimos de 1 a 1,6 mm para contrarrestar problemas difusionales en la producción de etanol (Norton y D’Amore, 1994). Otro aspecto también importante en la inmovilización en alginato, es la concentración del mismo. En otros estudios realizados se menciona la importancia de la dureza y la rigidez de las perlas en relación con la concentración de alginato. Trabajando con Saccharomyces cerevisiae inmovilizada con soluciones de alginato al 1,5, 2, 3 y 6 %, la solución de alginato al 2% resultó la más adecuada para evitar inconvenientes en la difusión de los nutrientes a altas tasas de actividad celular y con buenas características de resistencia del gel durante todo el tiempo de cultivo (Najfpour et al., 2004). Estos resultados coinciden con los del presente estudio, ya que la utilización de alginato al 2% permitió mantener la integridad de las perlas durante los cuatro lotes de cultivo con rendimientos máximos de etanol cercanos al valor teórico.
Otras variables importantes en la inmovilización de levaduras para la producción de etanol incluyen el soporte de la inmovilización, del tipo de cultivo utilizado, el sistema de cultivo (cultivo en lote o cultivo continuo), la concentración y el tipo de azúcar, y la temperatura de fermentación.
Altas concentraciones de glucosa muestran un efecto inhibitorio en la producción de etanol, aunque se ha sugerido un menor efecto en células inmovilizadas (Lin y Tanaka, 2006). En el presente estudio, los valores de rendimiento máximo de etanol (cuadro 2) para todos los diámetros de perla probados a una concentración de 12% de glucosa confirman esta ventaja en células inmovilizadas. Asimismo, Mc Ghee et al. (1982) utilizaron Saccharomyces uvarum, Saccharomyces cerevisiae y Zymomonas mobilis inmovilizadas en alginato para producción de etanol en cultivo continuo, para lo cual probaron concentraciones de glucosa de 1, 3, 5, 10 y 20%. En estas condiciones no se observó una gran variación en la producción de etanol entre las concentraciones de 1, 3, 5 y 10% en columnas empaquetadas con las perlas; pero cuando la concentración de glucosa se incrementó del 10 al 20%, la producción de etanol de las cepas disminuyó. En cambio, en columnas con una distribución uniforme de perlas, la producción de etanol de S. uvarum aumentó. Tomando en cuenta esto, y considerando un bajo empaquetamiento del reactor usado en este estudio (figura 2), los resultados coinciden con lo encontrado por estos autores para S. uvarum (S. bayanus), por lo cual se puede sugerir una concentración de 12% de glucosa para la producción de etanol con Saccharomyces uvarum en reactores no empacados. Concentraciones mayores podrían producir inhibición en la producción de etanol, como fue demostrado para otras especies como Saccharomyces cerevisiae (Sree et al., 2000).
Respecto a la temperatura, se conoce que este parámetro también tiene una marcada influencia en la productividad la cual, en el caso de S. cerevisiae, disminuye al disminuir la temperatura de fermentación (Bakoyianis et al., 1997). Sin embargo, S. uvarum (S. bayanus) mantiene su capacidad fermentativa a bajas temperaturas (Querol et al., 2003). En este estudio la temperatura fue controlada a 28 oC por lo cual no se evaluó el efecto de esta variable.
Finalmente, la productividad máxima de etanol obtenida en el presente trabajo con Saccharomyces uvarum inmovilizada fue de 1,2 g/L/h, equivalente a 57,8 g/L para una concentración inicial de glucosa de 120 g/L, valores comparables o mayores a los obtenidos por otros autores. Así, la producción y el rendimiento alcanzados en este estudio utilizando un sistema de lotes repetidos fueron mayores a los alcanzados por Mc Ghee et al. (1982) en cultivos continuos con 10% de glucosa para S. cerevisiae (47 g/L) y S. uvarum (40 g/L), y semejantes a los valores de productividad de 60,3 g/L/día obtenidos por Bakoyianis et al. (1997), con Saccharomyces cerevisiae alcohol-resistente, y criotolerante que fue inmovilizado en alginato de calcio en un medio de fermentación con 12,0 ºBe (equivalentes aproximadamente a 240 g/L de azúcar).
Debido a los pocos estudios realizados con Saccharomyces uvarum (S. bayanus) inmovilizada para la producción de etanol, los resultados obtenidos en el presente estudio son de utilidad para considerar a esta especie como una buena alternativa en la producción de etanol.
Conclusiones
De acuerdo con los resultados obtenidos, el rendimiento y la producción de etanol con Saccharomyces uvarum (S. bayanus) inmovilizada en 2% de alginato están directamente relacionados con el diámetro de esferas e inversamente con la densidad celular. Para los tres diámetros evaluados, las perlas con mayor diámetro y menor densidad celular (3 mm) mostraron el mayor rendimiento y la mayor producción; mientras que las esferas de menor diámetro y mayor densidad celular (2 mm) tuvieron los menores valores para estas variables. Asimismo, por los rendimientos obtenidos, S. uvarum NRRL Y-11877 inmovilizada en alginato muestra una buena capacidad fermentativa para la producción de etanol.
Agradecimientos
El presente trabajo fue subvencionado por el Laboratorio de Micología y Biotecnología (LMB), Universidad Nacional Agraria La Molina, Perú. Los autores desean expresar su reconocimiento al señor Mario García por su asistencia técnica.
Referencias bibliográficas
1 Archer, M., De Vos, B.-J., Visser, M. S. 2007. The preparation, assay and certification of aqueous ethanol reference solutions. Accreditation and Quality Assurance 12: 188-193. [ Links ]
2 Bakoyianis, V., Koutinas, A. A., Agelopoulos, K., Kanellaki, M. 1997. Comparative study of kissiris, -alumina, and calcium alginate as supports of cells batch and continuous wine - making at low temperatures. Journal of Agriculture and Food Chemistry 45: 4884-4888. [ Links ]
3 Freeman, A., Lilly, M. D. 1998. Effect of processing parameters on the feasibility and operational stability of immobilized viable microbial cells. Enzyme and Microbial Technology 23: 335-345. [ Links ]
4 Goksungur, Y., Zorlu, N. 2001. Production of ethanol from beet molasses by ca - alginate immobilized yeast cells in a packed - bed bioreactor. Turkish Journal Biology 25: 265-275. [ Links ]
5 Guiseley, K. B. 1989. Chemical and physical properties of algal polysaccharides used for cell immobilization. Enzyme and Microbial Technology 11: 706 - 716. [ Links ]
6 Gutiérrez-Correa M., Villena G.K. 2003. Surface adhesion fermentation: a new fermentation category. Revista Peruana de Biología 10: 113-124. [ Links ]
7 Junter, G.-A., Jouenne, T. 2004. Immobilized viable microbial cells: from the process to the proteome. . . or the cart before the horse. Biotechnology Advances 22: 633-658. [ Links ]
8 Lin, Y., Tanaka, S. 2006. Ethanol fermentation from biomass resources: current state and prospects. Applied Microbiology and Biotechnology 69: 627-642. [ Links ]
9 Manojlovic, V., Djonlagic, J., Obradovic, B., Nedovic, V., Bugarski, B. 2006. Investigations of cell immobilization in alginate: rheological and electrostatic extrusion studies. Journal of Chemical Technology and Biotechnology 81: 505-510. [ Links ]
10 Martynenko, N. N., Gracheva, I. M. 2003. Physiological and biochemical characteristics of immobilized champagne yeasts and their participation in champagnizing processes: A review. Applied Biochemistry and Microbiology 39: 439-445. [ Links ]
11 Masneuf, I., Hansen, J., Groth, C., Piskur, J., Dubourdieu, D. 1998. New hybrids between Saccharomyces sensu stricto yeast species found among wine and cider production strains. Applied and Environmental Microbiology 64: 3887-3892. [ Links ]
12 Mc Ghee, J. E., Julian G. S. T., Detroy, R. W., Bothast, R. J. 1982. Ethanol production by immobilized Saccharomyces cerevisiae, Saccharomyces uvarum, and Zymomonas mobilis. Biotechnology and Bioengineering 24: 1155-1163. [ Links ]
13 Miller, G. L. 1959. Use of dinitrosalicylic acid reagent for the determination of reducing sugar. Analytical Chemistry 31: 426-428. [ Links ]
14 Najafpour, G., Habibollah, Y., Syahidah, K. 2004. Ethanol fermentation in an immobilazed cell reactor using Saccharomyces cerevisiae. Bioresource Technology 92: 251-260. [ Links ]
15 Norton, S., D'Amore, T. 1994. Physiological effects of yeast cell immobilization: Applications for brewing. Enzyme and Microbial Technology 16: 365-375. [ Links ]
16 Núñez, M. J., Lema, J. M. 1987. Cell immobilization: Application to alcohol production. Enzyme and Microbial Technology 9: 642-651. [ Links ]
17 Pilone, G. J. 1985. Determination of ethanol in wine by titrimetric and spectrophotometric dichromate methods: collaborative study. Journal of the Association of Official Analytical Chemists 68: 188-90. [ Links ]
18 Querol, A., Fernández-Espinar, M. T., Del Olmo, M., Barrio, E. 2003. Adaptive evolution of wine yeast. International Journal of Food Microbiology 86: 3-10. [ Links ]
19 Redzepovic, S., Orlic, S., Sikora, S., Majdak, A., Pretorius, I. S. 2002. Identification and characterization of Saccharomyces cerevisiae and Saccharomyces paradoxus strains isolated from Croatian vineyards. Letters in Applied Microbiology 35: 305-310. [ Links ]
20 Salter, G. J., Kell, D. B. 1991. New materials and technology for cell immobilization. Current Opinion in Biotechnology 2: 385-389. [ Links ]
21 Seo, H. B., Kim, H. J., Lee, O. K., Ha, J. H., Lee, H. Y., Jung, K. H. 2009. Measurement of ethanol concentration using solvent extraction and dichromate oxidation and its application to bioethanol production process. Journal of industrial Microbiology and Biotechnology 36: 285-92. [ Links ]
22 Sree, N. K., Sridhar, M., Suresh, K., Banat, I. M., Rao, L. V. 2000. High alcohol production by repeated batch fermentation using an immobilized osmotolerant Saccharomyces cerevisiae. Journal of Industrial Microbiology and Biotechnology 2: 222-226. [ Links ]
23 Sugama, S., Okasaki, N. 1979. Growth estimation of Aspergillus oryzae cultured on solid media. Journal of Fermentation Technology 57: 408-412. [ Links ]