Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Biotecnología
Print version ISSN 0123-3475
Rev. colomb. biotecnol vol.13 no.1 Bogotá Jan./June 2011
ARTÍCULO DE INVESTIGACIÓN
Acumulación de mercurio (Hg) por caña flecha (Gynerium sagittatum) (Aubl) Beauv. in vitro
Accumulation of mercury (Hg) by arrow cane (Gynerium sagittatum) (Aubl) Beauv. in vitro
Rafael Esteban Ortega-Ortega 1 , Javier Darío Beltrán-Herrera 1 , José Luis Marrugo-Negrete 2
1 Universidad de Sucre, Facultad de Educación y Ciencias, Departamento de Biología. Grupo de Investigación Biotecnología Vegetal (Biovus). raesortega@gmail.com
2 Universidad de Córdoba, Grupo de Aguas, Química Aplicada y Ambiental.
Recibido: octubre 24 de 2010 Aprobado: mayo 23 de 2011
Resumen
En este estudio se evaluó, in vitro, la capacidad de acumulación de mercurio (Hg) que pueda poseer la caña flecha (Gynerium sagittatum) (Aubl) Beauv. como una alternativa viable de ser implementada para la rehabilitación de suelos contaminados. Este estudio fue realizado en el laboratorio de Biotecnología Vegetal de la Universidad de Sucre (9º18’ N, 75º23’ O). Se usó un diseño experimental de bloques al azar, un análisis de varianza para comparación de medias, una prueba de Tukey (p≤0,05) para la establecer las diferencias significativas entre los tratamientos, pruebas de normalidad (Kolmogorov-Smirnov) y test de homogeneidad de varianza de Bartlett. Los análisis de mercurio se realizaron en un espectrofotómetro de absorción atómica Thermo Electron S4, provisto de una celda con ventanas de cuarzo, por el método de espectroscopia de absorción atómica con vapor frío. Los resultados muestran que la parte de la planta que presenta mayor acumulación es la raíz con 55,98 µg g-1 HgT, seguida de los tallos-hojas con 14,84 µg g-1 HgT, valores relacionados con el grado de concentración del metal en el medio de cultivo. Además, la acumulación de mercurio en raíces y tallos aumentó con el tiempo. En conclusión, in vitro esta planta acumula Hg debido a las altas concentraciones en sus tejidos sin afectar la viabilidad de las plantas.
Palabras clave: fitorremediación, remoción, metales pesados.
Abstract
In this in vitro study was evaluated the potential for accumulation of mercury (Hg) that can hold the cane arrow (Gynerium sagittatum) (Aubl) Beauv. as a viable alternative to be implemented for the rehabilitation of contaminated soils. This study was conducted at the Plant Biotechnology Laboratory, University of Sucre (9º 18' N, 75° 23' W). An experimental design was randomized block, an analysis of variance to compare means, Tukey test (p ≤ 0.05) to establish significant differences between the treatments, tests of normality (Kolmogorov-Smirnov) and homogeneity test Bartlett variance. The mercury analyses were performed on atomic absorption spectrophotometer Thermo Electron S4, a cell equipped with quartz windows, by the method of atomic absorption spectrometry with cold steam. The results show that the plant part that presents the greatest accumulation is the root with 55.98 mg g-1 HgT, followed by the stems, leaves 14.84 g g-1 HgT and these values are related to the degree of metal concentration in the culture medium. Furthermore, the accumulation of mercury in roots and stems increased with time. In conclusion, in vitro this plant accumulates due to the high Hg concentrations in their tissues without affecting the viability of plants.
Key words: Phytoremediation, removal, heavy metals.
Introducción
Los metales pesados son quizás los agentes tóxicos más conocidos desde la antigüedad, no han perdido interés, y en los últimos años se ha incrementado el conocimiento concerniente a los potenciales efectos tóxicos y mecanismos de acción de los iones metálicos, los compuestos inorgánicos y organometálicos, que constituyen parte de los productos y subproductos tecnológicos (Repetto, 1995; Kosnett, 2010). El mercurio (Hg) genera uno de los mayores problemas ambientales actuales debido a su alta toxicidad y capacidad para bioacumularse y biomagnificarse (Zheng et al., 2008), por lo que altera el equilibrio ecológico y genera graves problemas de salud pública. Este contaminante está relacionado con daños severos al sistema nervioso central, teratogénesis, así como con afecciones del hígado y los riñones (Magos, 2003; Bocayuva et al., 2005; Nóvoa et al., 2008).
En Colombia, la mayor zona de explotación minera de oro se encuentra ubicada entre el norte de Antioquia y sur de Bolívar, con más de 12.400 minas en explotación que involucran un número de personas superior a 50.000 las cuales reciben influencia directa o indirecta de esta actividad (Unidad de planeación minera energética, 2001). La cantidad de mercurio liberado al ambiente en esta actividad no ha sido calculada con exactitud, pero se ha estimado en cerca de 80 a 100 toneladas al año. El manejo inadecuado de este metal ha conllevado la contaminación de suelos, sedimentos, cuerpos de agua y demás compartimientos ambientales (Olivero y Johnson, 2002).
De aquí surge el interés y la necesidad de colaborar con la naturaleza para revertir el efecto de los contaminantes en los ecosistemas colombianos y, debido a los problemas de salud humana que representa el contacto con suelos contaminados con metales pesados, se evalúan alternativas de tratamiento de estos mediante la extracción de los metales del suelo y su recuperación usando la fitorremediación (Ibáñez y Montoro, 1996; Behne et al., 1998; Barregard et al., 1999; López et al., 2005).
Entre las diferentes opciones técnicas de remediación, la fitorremediación ocupa un lugar importante porque es una tecnología emergente basada en la acción combinada de plantas (terrestres o acuáticas), dado su bajo impacto medioambiental, bajo costo, eficiencia y gran aceptabilidad entre el público para extraer los contaminantes del suelo, y disminuir o eliminar su toxicidad (Prabha y Loretta, 2007; Ghaderian et al., 2007; Malikova et al., 2008).
La Gynerium sagittatum (Aubl) Beauv pertenece a la familia de las Poaceae, comprende un gran número de especies —alrededor de 5.000— pertenecientes a más de 700 géneros. Se trata de plantas herbáceas, perennes o anuales, con tallo (hueco en los entrenudos y muy nudoso), en algunos casos lignificado (Bambuseae). En algunas áreas tienden a dominar, llegando incluso a constituir bandas de vegetación muy extendidas que confieren una fisonomía propia al territorio (prado, estepa, sabana) (Kalliola et al., 1992). Aunque se conocen algunos antecedentes de otras gramíneas para la eliminación de metales pesados y de residuos orgánicos como el carrizo (Phragmites australis), en la actualidad no se conocen estudios realizados sobre la capacidad fitorremediadora de metales pesados (Hg) que pueda poseer la Gynerium sagittatum (Aubl) Beauv, lo cual se puede considerar como una desestimación del potencial que tiene esta especie pudiendo ocupar un lugar importante en esta tecnología emergente (Martínez et al., 2005); Gynerium sagittatum es un recurso existente en la zona indígena de los departamentos de Córdoba y Sucre, la costa norte y valles de muchos ríos colombianos (Sehuanes y Flórez, 2003).
La investigación en cultivos in vitro tiene potencial para el estudio práctico de los procesos y mecanismos implicados en la fitorremediación, se ha aplicado en numerosos estudios encaminados a identificar la capacidad de las células vegetales a tolerar, asimilar, desintoxicar, metabolizar, almacenar y eliminar productos formados de una amplia variedad de orgánicos y xenobióticos contaminantes, eliminando los efectos de la actividad microbiana. Debido a que crecen relativamente rápido, y una vez establecidos, estos cultivos in vitro se pueden propagar de forma indefinida, se puede asegurar la estabilidad genética en los tejidos usados y están disponibles siempre que se requieran, garantizando la reproducibilidad de los resultados (Rezek et al., 2007; Podlipna et al., 2008; Coniglio et al., 2008).
En contraste, las plantas in vivo o en sistemas hidropónicos tienen una vida útil limitada y cada planta necesita ser reemplazada y restablecida después de cada experimento, en consecuencia, el tiempo necesario para llevar a cabo los montajes experimentales se puede reducir sustancialmente usando plantas in vitro en lugar de las plantas in vivo (Gujarathi et al., 2005; Wevar Oller et al., 2005; Doran, 2009). Los cultivos in vitro se mantienen libres de contaminación microbiana, y pueden ser utilizados para distinguir las respuestas y las capacidades metabólicas de las células vegetales de las de los microorganismos que normalmente están presentes en la rizosfera de plantas o de tejidos in vivo. El papel clave del uso del cultivo de tejidos in vitro en la investigación en fitorremediación es un sistema modelo para establecer el potencial de acumulación, la comprensión de los mecanismos metabólicos y la tolerancia con que funcionan en las plantas in vivo (Chaudhry et al., 2005; Lebeau et al., 2008).
Por tanto, el objetivo de este estudio fue evaluar el potencial acumulador de Hg y establecer la posible fitotoxicidad en esta especie en condiciones in vitro.
Materiales y métodos
Material vegetal. Las plantas de Gynerium sagittatum (Aubl) Beauv c.v "criolla" fueron obtenidas del banco de germoplasma del laboratorio de Biotecnología Vegetal de la Universidad de Sucre, propagadas utilizando el medio básico de Murashige y Skoog (MS) (1962). suplementado con: tiamina-HCl 1 mg/L-1; mio-inositol 100 mg/L-1 piridoxina-HCL 0,5 mg/L-1; nicotinamida 0,5 mg/L-1; glicina 2 mg/L-1; sacarosa 2500 mg/L-1; agar 4,5 g/L-1; 1 mg/L-1 de 6-bencilaminopurina (BAP); el pH se ajustó en un rango de 5,7-5,8 y se llevaron al cuarto de incubación en donde se mantuvieron a una temperatura promedio de 25 ± 3 ºC, con una intensidad lumínica de 50 ± 5 µMol m-2 s-1, con un foto periodo de 12 horas día/noche y una humedad relativa del 60%, hasta que las plantas alcanzaron un tamaño de 8 a 10 cm.
Montaje de las pruebas con el mercurio. Se realizó la preparación de los diferentes ensayos partiendo de una solución patrón de Hg(NO3)2 con una concentración de 500 mg/L-1 en la cual se hicieron las diluciones pertinentes para obtener una concentración final según la tabla 1, en un volumen de 250 mL por tratamiento adicionado al medio de cultivo Murashige y Skoog (1962). Para cada experimento se utilizó un diseño completamente al azar, realizando un procedimiento de muestreo aleatorio simple; se contó con cinco repeticiones por tratamiento y cada ensayo se realizó por duplicado en 20, 40 y 60 días de evaluación.
Muestreo y análisis de las plantas. Una vez las plantas tuvieron un sistema radicular se transfirieron a los frascos a razón de una planta por frasco el cual contenía 15 mL de medio de cultivo líquido cada uno. Se inició la evaluación de los tratamientos a los 20, 40 y 60 días. Para el análisis se tomaron las raíces y los tallos con sus hojas y fueron digeridos con una solución de HNO3:H2SO4 (3:1, v/v). Los análisis de mercurio se realizaron en un espectrofotómetro de absorción atómica Thermo Electron S4, provisto de una celda con ventanas de cuarzo, por el método de espectroscopia de absorción atómica con vapor frío adaptado de Sadiq et al., (1991) y United States Environmental Protection Agency (1994), previamente validado en el laboratorio de Aguas de la Universidad de Córdoba. Los datos analíticos cumplieron los criterios de control de calidad que debe poseer un procedimiento analítico: linealidad, exactitud, precisión y límite de detección, para garantizar una alta confiabilidad (Miller y Miller, 2000). Los análisis fueron realizados por duplicado y los resultados se reportaron en mg Hg kg-1 peso seco.
Fitotoxicidad. El porcentaje de plantas necróticas se valoró mediante la cuantificación del desarrollo de las plantas expresadas en características morfológicas como el porcentaje de hojas cloróticas y tallos, contrastando con la concentración de Hg adicionada al medio de cultivo (Kabata y Pendías, 2001).
Manejo y análisis de datos. El resultado del análisis de HgT para cada muestra de raíz, tallo-hojas y el efecto fitotóxico en las plantas es presentado como la media (‾X) +/- error estándar (SEM) de las determinaciones por las cinco repeticiones de cada tratamiento. Para evaluar la existencia de diferencias significativas entre las concentraciones medias de mercurio de las exposiciones a las diferentes soluciones (grupos de datos) se empleó una prueba de Tukey. De otra parte, para examinar la presencia de diferencias entre más de dos medias se utilizó el análisis de varianza (Anova), el cual asume que los datos siguen una distribución normal y que las varianzas de las poblaciones son iguales. Por consiguiente, antes de realizar este análisis fue indispensable aplicar el test de normalidad de Kolmogorov-Smirnov y el test de homogeneidad de varianza de Bartlett por medio del paquete estadístico Statgraphics Centurion XVI. Para todos los análisis estadísticos el criterio de significancia fue establecido en P<0,05 (Walpole y Myers, 1992).
Resultados y discusión
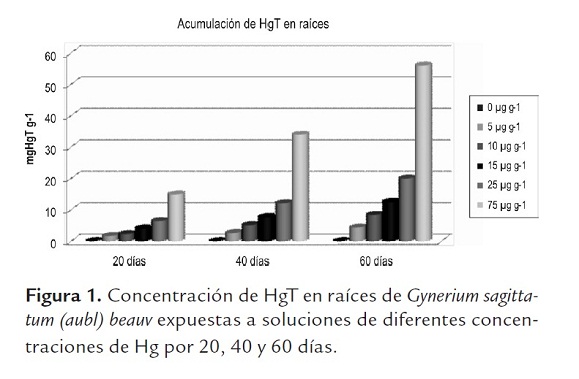
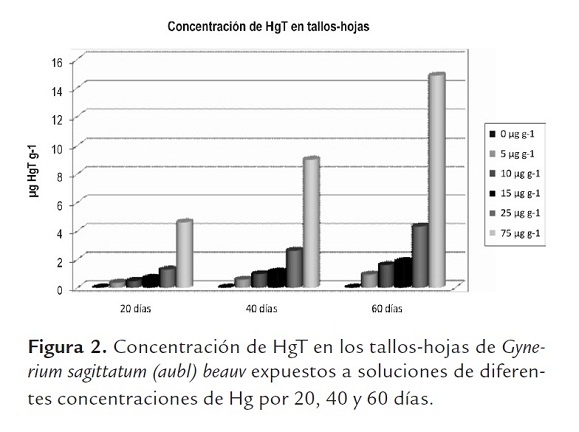
Acumulación de mercurio en tejidos. Al analizar las plantas en las diferentes concentraciones de mercurio suministradas al medio de cultivo se obtuvieron los siguientes resultados de Hg total (HgT) en las raíces (figura 1) y tallos-hojas (figura 2) evaluadas a los 20, 40 y 60 días.
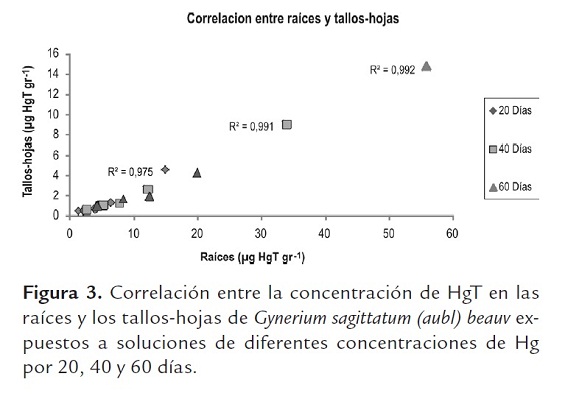
Al correlacionar la concentración de HgT en raíces con la obtenida en tallos y hojas, esta presenta altos valores de R, indicando una relación directa entre dichas concentraciones como se muestra en figura 3.
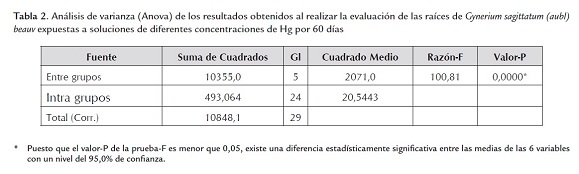
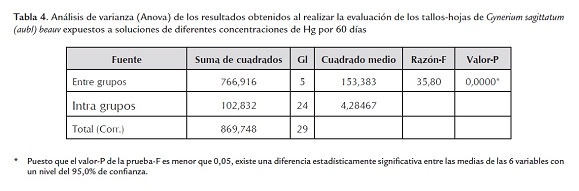
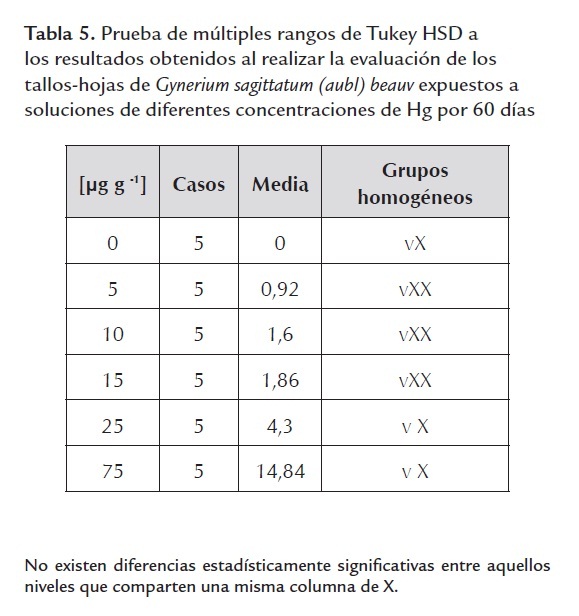
De acuerdo con el análisis de varianza (P<0,05) la concentración media del HgT resultó ser diferente entre las concentraciones en el estudio para cada tiempo de evaluación y también para cada una de las concentraciones en los tres tiempos evaluados; por su parte, la prueba de Tukey (P<0,05) arrojó diferencias significativas entre los tratamientos 15 µg g-1, 25 µg g-1 y 75 µg g-1 para las raíces y los tallos-hojas, indicando que el tiempo de exposición favorece el aumento de la concentración en las raíces hasta llegar a 55,98 µg g-1, seguida de los tallos-hojas con 14,84 µg g-1; comparándola con pteris longuifolia que presenta acumulación promedio de HgT en raíz de 26,22 µg g-1 de mercurio y Adiantum sp con 17,91 µg g-1 en tallos determinadas en un estudio de Mina Santa Cruz, municipio Barranco de Loba, departamento de Bolívar (Pérez, 2010), Gynerium sagittatum (aubl) beauv. presenta una alta acumulación de HgT en sus tejidos.
La mayor parte del mercurio acumulado está atrapado en las raíces y solo una pequeña cantidad puede ser traslocada a los tallos-hojas. La captación principalmente se realiza en la punta de la raíz, antes de la formación de la banda de Caspary (Agrasar y Sánchez, 1989; Giraldo, 2005), la cual constituye una barrera que impide al metal pasar por apoplasto, forzándola a través del citoplasma que es selectivamente permeable (simplasto) (Matilainen et al., 2001; Wang, 2004). La banda de Caspary es una capa de suberina impermeable que se extiende sin sucesión de continuidad a lo largo de las paredes radiales y transversales, y constituye una barrera eficaz contra el movimiento pasivo de metales pesados en la estela, incidiendo de este modo en la acumulación de metal (MacFarlane y Burchett, 2000; Lux et al., 2004; Wang, 2004; Alassimone et al., 2010). La endodermis divide el apoplasto de la raíz en dos compartimentos, lo que resulta muy conveniente para el desplazamiento selectivo de iones, minerales y agua. Los iones presentes en la solución se pueden difundir libremente en todo el córtex, pero no pueden atravesar la banda de Caspary. Para entrar al cilindro vascular, es decir, a la corriente transpiratoria, deben cruzar la membrana plasmática de una célula endodérmica, y así la planta controla qué iones pasan y qué iones son excluidos (Pulford y Watson, 2003; Wang, 2004; Alassimone et al., 2010).
Fitotoxicidad del Hg en las plantas de Gynerium sagittatum (aubl) beauv.
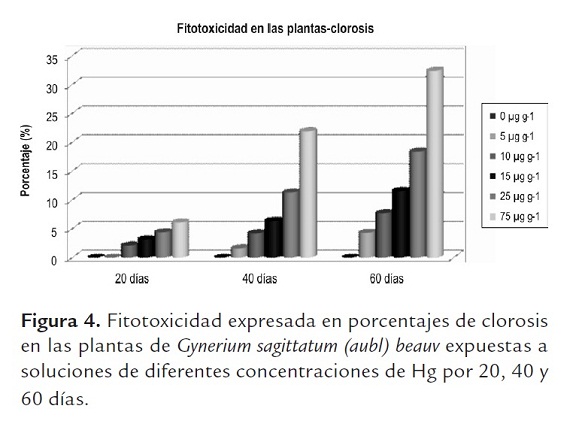
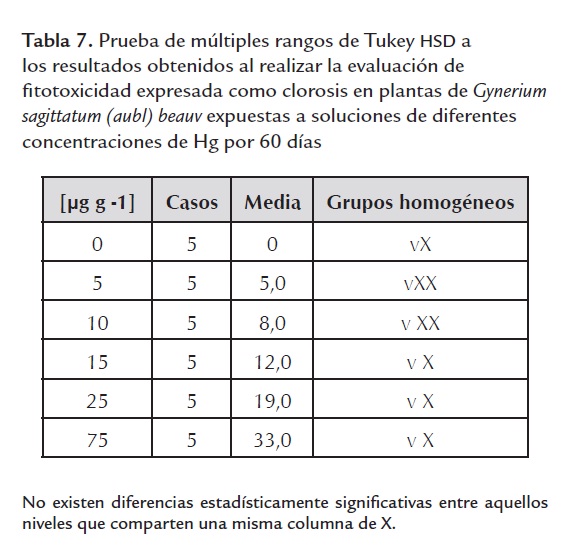
Los efectos de requerimientos nutricionales y tóxicos de los metales se estudian en condiciones controladas con el fin de diferenciarlos de aquellos que pueden ser producto de interacciones con microorganismos que están presentes en condiciones in vivo (Ross, 1994; Liu et al., 2009). La sensibilidad de las especies vegetales a los metales pesados varía considerablemente a través de reinos y familias, siendo las plantas vasculares ligeramente más tolerantes y las diferentes respuestas a los metales pesados pueden ser atribuidas a factores genéticos y fisiológicos (Calow, 1993; Ci et al., 2009), los efectos de la clorosis de las plantas se muestran en la figura 4 y los de necrosis se muestran en la figura 5.
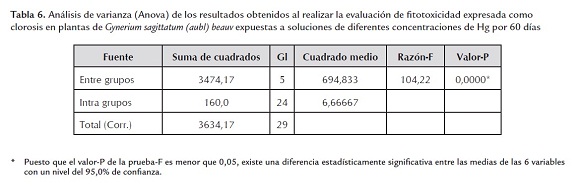
De acuerdo con los resultados se observa una marcada clorosis que se expresa directamente proporcional al aumento de la concentración del Hg. El análisis de varianza (P<0,05) mostro que la media de la clorosis en las plantas resultó ser diferente entre los tratamientos en cada una de las combinaciones y para cada tiempo de acumulación y al realizar la prueba de Tukey (P<0,05) a los resultados arrojaron diferencias significativas entre los tratamientos. En los tratamientos donde la concentración de Hg es más alta (75 µg g-1) se obtuvo el mayor porcentaje de plantas cloróticas, llegando a 32,5% del total de plantas evaluadas.
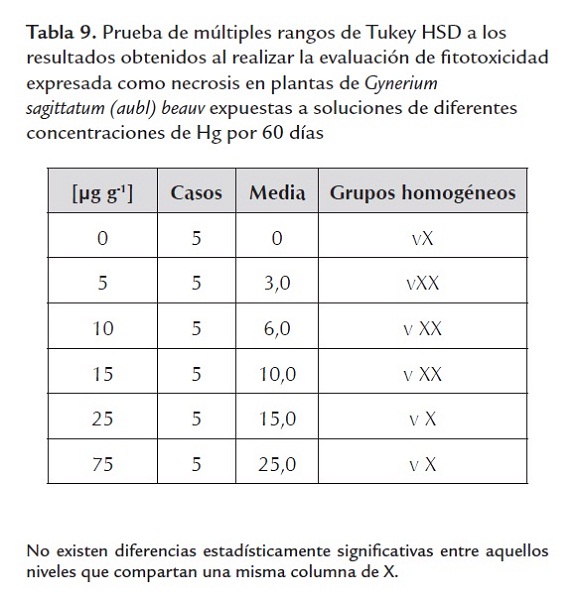
En este estudio se presentó la muerte prematura de células, tejidos, órganos y plantas completas, comportamiento directamente proporcional a la concentración de Hg a la que fueron sometidas: a menor concentración menor porcentaje de muerte (3,4% hasta llegar a 25,2% en 75 µg g-1) del total de las plantas evaluadas. El análisis de varianza (P<0,05) mostró que la media de la necrosis en las plantas resultó ser diferente entre los tratamientos en cada una de las combinaciones y para cada tiempo de evaluación, y al realizar la prueba de Tukey (P<0,05) los resultados mostraron diferencias significativas entre los tratamientos.
El análisis de varianza (P<0,05) mostró que la media de la necrosis en las plantas resultó ser diferente entre los tratamientos en cada una de las combinaciones y para cada tiempo de evaluación, y al realizar la prueba de Tukey (P<0,05) los resultados mostraron diferencias significativas entre los tratamientos.
De acuerdo con los resultados, se observa una marcada necrosis que se comporta directamente proporcional al aumento de la concentración del metal; en los tratamientos donde la concentración de Hg es más alta (75 µg g-1) se obtuvo el mayor porcentaje de plantas necróticas llegando a 25,2% del total de plantas evaluadas en los 60 días. Varios autores reportan concentraciones promedio de HgT en suelos contaminados por mercurio debido a la minería, dentro del rango de 0,02 a 30 µg g-1 (Carrasquero y Adams, 2003; Terzano et al., 2010; Vidal, 2010; Santos et al., 2011), donde las plantas de Gynerium sagittatum (aubl) beauv podrían tener una mortalidad por debajo del 15%.
El estado electroquímico y la especiación química de elementos contaminantes pueden contribuir a su movilidad desde las raíces a los brotes. En el caso del mercurio se consideran las especies más móviles: el mercurio elemental y el ión mercurio II. La mayoría del mercurio Hg(II) que es capturado permanece ligado a los tejidos de la raíz, mientras que el mercurio Hg(0) capturado por las raíces y por las hojas es reducido a Hg(II) y permanece ligado a los tejidos (Moreno et al., 2005). Una vez el tóxico ha sido transportado a las partes superiores de la planta, este se concentra y se almacena; este paso requiere de la transformación a especies más o menos reactivas que favorezcan esta acumulación. Las plantas en general son capaces de secuestrar los iones tóxicos en complejos en el citoplasma para defenderse de su fitotoxicidad. El control de estas dos variables maximiza el almacenamiento de los elementos en las hojas, los tallos y los tejidos vasculares, así el mercurio es trasportado como Hg(0) a las partes superiores de las plantas, donde los niveles de peroxidasa y catalasa oxidan el Hg(0) a Hg(II). El Hg(II) es altamente reactivo y forma productos particularmente estables con tioles reducidos que pueden almacenarse en las plantas en grandes cantidades (Meagher y Heaton, 2005).
Los posibles mecanismos causales de la toxicidad del mercurio son los cambios en la permeabilidad de la membrana celular, reacciones de sulfhidrilo (-SH) con cationes, la afinidad para reaccionar con grupos fosfato y grupos de ADP o ATP, y la sustitución de los iones esenciales, principalmente grandes cationes, e intervenir la fotosíntesis, la absorción de nutrientes minerales y la transpiración (Barber et al., 1973; Godbold y Hütterman, 1988; Godbold, 1991; Patra y Sharma, 2000).
Conclusiones
La Gynerium sagittatum (aubl) beauv es una especie que acumula Hg en sus tejidos, siendo la raíz la parte de la planta que presenta mayor concentración, seguida de los tallos-hojas. La capacidad de acumulación en las raíces está relacionada con la concentración que se presente en el medio de cultivo, y la capacidad de acumulación en los tallos-hojas está relacionada con la capacidad de translocación del Hg a través de las raíces.
Se pudo establecer que cuando las plantas de Gynerium sagittatum (aubl) beauv fueron sometidas a concentraciones elevadas de Hg, presentaron bajos porcentajes de clorosis y necrosis indicando pocos efectos fitotóxicos.
Las altas tasas de acumulación de HgT del medio de cultivo en los tejidos de Gynerium sagittatum (aubl) beauv en 60 días de evaluación implican que esta especie tiene capacidad de remoción y un alto potencial para ser empleada en fitorremediación de suelos contaminados con Hg, debiendo realizar los respectivos estudios en condiciones in vivo.
Agradecimientos
Agradecemos al soporte financiero del proyecto Colciencias código 1112-489-25604 Contrato 472 Colciencias - Universidad de Córdoba, y a su Grupo de Aguas, Química Aplicada y Ambiental; a la Universidad de Sucre y a su Grupo de Investigación en Biotecnología Vegetal (Biovus) por el apoyo en la presente investigación.
Referencias bibliográficas
1 Alassimone, J,. Naseer, S., Geldner, N. 2010. A developmental framework for endodermal differentiation and polarity. PNAS, 107 (11): 5214-5219. [ Links ]
2 Agrasar, Z., Sánchez, E. 1989. Estudios sobre el género Digitaria. I. Anatomía de Digitaria phaeothrix y especies afines. Bol. Soc. Argent. Bot. (26): 107-118. [ Links ]
3 Barber, J., Beauford, W., Shieh, Y. 1973. Some aspects of mercury uptake by plant, algal and bacterial systems in relation to its biotransformation and volatilization. In: Miller, M. W., Clarkson, T. W. (eds.). Mercury, mercurials, and mercaptans. Illinois: Charles D. Thomas Publisher. pp. 325-345. [ Links ]
4 Barregard, L., Svalander, C., Schütz, A. 1999. Cadmium, mercury, and lead in kidney cortex of the general swedish population: a study of biopsies from living kidney donors. Environ Health Perspect. (197): 867-871. [ Links ]
5 Behne, D., Hammel, C., Pfeifer, H. 1998. Speciation of selenium in the mammalian organism. Analys. (123): 871-873. [ Links ]
6 Bocayuva, L., Magalhães, V., Malm, O., Oleivera, E. 2005. Performance on neurological development tests by riverine children with moderate mercury exposure in Amazonia. Brazil Cad Saúde Pública, 21 (4): 1160-1167. [ Links ]
7 Calow, P. 1993. Handbook of ecotoxicology. London: Blackwell Science (1): 478 [ Links ]
8 Carrasquero, A., Adams, M. 2003. Fraccionamiento de mercurio en suelos de áreas contaminadas de El Callao, estado de Bolívar-Venezuela. Agronomía Tropical, 53(3): 331-345. [ Links ]
9 Chaudhry, Q., Blom-Zandstra, M., Gupta, S., Joner, E. 2005. Utilising the synergy between plants and rhizosphere microorganisms to enhance breakdown of organic pollutants in the environment. Environ Sci Pollut Res. (12): 34-48. [ Links ]
10 Ci, D., Jiang, D., Dai, T., Jing, Q., Cao, W. 2009. Effects of cadmium on plant growth and physiological traits in contrast wheat recombinant inbred lines differing in cadmium tolerance. Chemosphere, 77 (11): 1620-5. [ Links ]
11 Coniglio, M., Busto, V., González, P., Medina, M., Milrad, S., Agostini, E. 2008. Application of Brassica napus hairy root cultures for phenol removal from aqueous solutions. Chemosphere (72): 1035-1042. [ Links ]
12 Doran, P. 2009. Application of plant tissue cultures in phytoremediation research: incentives and limitations. Biotechnol Bioeng. 103 (1): 60-76. [ Links ]
13 Ghaderian, S., Mohtadi, A., Rahiminejad, R., Reeves, D., Baker, A. 2007. Hyperaccumulation of nickel by two Alyssum species from the serpentine soils of Iran. Plant Soil (293): 91-97. [ Links ]
14 Giraldo, D. 2005. The Colombian species of the genus Digitaria (Poaceae: Panicoideae: Paniceae). Caldasia 27 (1): 25-87. [ Links ]
15 Godbold, D. 1991. Mercury induced root damage in spruce seedlings. Water Air and Soil Pollution (56): 823-831. [ Links ]
16 Godbold, D., Hütterman, A. 1988. Inhibition of photosynthesis and transpiration in relation to mercuryinduced root damage in spruce seedlings. Physiologia Plantarum (74): 270-275. [ Links ]
17 Gujarathi, N., Haney, B., Park, H., Wickramasinghe, S., Linden, J. 2005. Hairy roots of Helianthus annuus: A model system to study phytoremediation of tetracycline and oxytetracycline. Biotechnol Prog. (21): 775-780. [ Links ]
18 Ibáñez, N., Montoro, R. 1996. Trace element food toxicology: an old and evergrowing discipline. Critical reviews in Food Science and Nutrition (36): 299-320. [ Links ]
19 Kabata, A., Pendías, H. 2001. Trace Elements in Soils and Plants. 3 ed. Boca Ratón: CRC Press. [ Links ]
20 Kalliola, R., Puhakka, M., Salo, J. 1992. Interspecific variation, and the distribution and ecology of Gynerium sagittatum (Poaceae) in the western Amazon. Flora 186 (3-4): 153-167. [ Links ]
21 Kosnett, M. 2010. Chelation for heavy metals (arsenic, lead, and mercury): protective or perilous? Clin Pharmacol Ther. 88 (3): 412-5. [ Links ]
22 Liu, W., Wang, K., Wang, M. 2009. Physiological responses of different peanut (Arachis hypogaea L.) varieties to cadmium stress. Ying Yong Sheng Tai Xue Bao Chinese, 20 (2): 451-9. [ Links ]
23 López, E., Rivera, S., Vargas, M. 2005. Tratamientos pasivos de drenajes ácidos de mina: estado actual y perspectivas de futuro. Boletín Geológico y Minero (113): 3-21. [ Links ]
24 Lebeau, T., Braud, A., Jezequel, K. 2008. Performance of bioaugmentation assisted phytoextraction applied to metal contaminated soils. Environ Pollut. (153): 497-522. [ Links ]
25 Lux, A., Sottníková, A., Opatrná, J., Greger, M. 2004. Differences in structure of adventitious roots in Salix clones with contrasting characteristics of cadmium accumulation and sensitivity. Physiologia Plantarum 120 (4): 537-545. [ Links ]
26 MacFarlane, G., Burchett, M., 2000. Cellular distribution of copper, lead and zinc in the grey mangrove, Avicennia marina (Forsk.) Vierh. Aquatic Botany (68): 45-59. [ Links ]
27 Magos, L. 2003. Neurotoxic character of thimerosal and the allometric extrapolation of adult clearance half-time to infants. J Appl Toxicol. 23 (4): 263-9. [ Links ]
28 Malikova, I., Ustinov, T., Anoshin, G., Badmaeva, Z., Malikov, Y. 2008. Mercury in soils and plants in the area of Lake Bol"shoe Yarovoe (Altai Territory). Russian Geology and Geophysics, 49 (1): 46-5. [ Links ]
29 Martínez, S., Gallegos, M., Pérez, L., Gutiérrez, M. 2005. Mecanismos de fitorremediación de suelos contaminados con moléculas orgánicas xenobióticas. Rev. Int. Contam. Ambient., 21 (2): 91-100. [ Links ]
30 Matilainen, T., Verta, M., Korhonen, H., Uusi-Rauva, A., Niemi, M. 2001. Behaviour of mercury in soil profiles: Impact of increased precipitation, acidity, and fertilization on mercury methylation. Water, Air and Soil Pollution, 125 (1-4): 105-119. [ Links ]
31 Meagher, R., Heaton, A. 2005. Strategies for the engineered phytoremediation of toxic element pollution: mercury and arsenic. Journal of Industrial Microbiology and Biotechnology (32): 502-513. [ Links ]
32 Moreno, F., Anderson, C., Stewart, R., Robinson, B. 2005. Mercury volatilisation and phytoextraction from base-metal mine tailings. Environmental Pollution (136): 341-352. [ Links ]
33 Miller, J., Miller, J. 2000. Statistics and chemometrics for analytical chemistry. 4 ed. London: Prentice Hall. [ Links ]
34 Murashige, T., Skoog, F. 1962. A revised medium for rapid growth and bioassays with tobacco tissue culture. Physiol. Plant. (15): 473-497. [ Links ]
35 Nóvoa, J., Pontevedra, X., Martínez, A, García, E. 2008. Mercury accumulation in upland acid forest ecosystems nearby a coal-fired power-plant in southwest Europe España. Science of the Total Environment, 394 (2-3): 303-12. [ Links ]
36 Olivero, J., Johnson, B. 2002. El lado gris de la minería del oro: la contaminación con mercurio en el norte de Colombia. Colombia: Ed. Universitaria. [ Links ]
37 Patra, M., Sharma, A. 2000. Mercury toxicity in plants. The Botanical Review, 66 (3): 379-421. [ Links ]
38 Pérez, L. 2010. Evaluación de la capacidad acumuladora de mercurio de especies vegetales establecidas en mina Santa Cruz, sur de Bolívar, Colombia. Sistema de Universidades Estatales del Caribe Colombiano, SUE-CARIBE. Tesis Maestría. [ Links ]
39 Podlipna, R., Falova, Z., Vanek, T. 2008. Toxic effect of nitroesters on plant tissue cultures. Plant Cell Tiss Organ Cult. (94): 305-311. [ Links ]
40 Prabha, K., Loretta, L. 2007. Phytorremediation technology: hyperacumulation metals in plants. Water air soil pollut. (180): 207-216. [ Links ]
41 Pulford, I., Watson, C. 2003. Phytoremediation of heavy metal-contaminated land by trees a review. Environmental International (29): 529-540. [ Links ]
42 Repetto, M. 1995. Toxicología avanzada. Madrid: Díaz de Santos. [ Links ]
43 Rezek, J., Macek, T., Mackova, M., Triska, J. 2007. Plant metabolites of polychlorinated biphenyls in hairy root culture of black nightshade Solanum nigrum SNC-9O. Chemosphere (69): 1221-1227. [ Links ]
44 Ross, S. 1994. Toxic metals in soil-plant systems. Chichester: John Wiley. [ Links ]
45 Sadiq, M., Zaidi, T., Al-mohana, M. 1991. Bulletin of Environmental Contamination and Toxicology (47): 335-341. [ Links ]
46 Santos, F., García, A., Alonso, P., Contreras, F., Adams, M. 2011. Distribution and mobility of mercury in soils of a gold mining region, Cuyuni river basin, Venezuela. J Environ Manage, 92(4): 1268-76. [ Links ]
47 Sehuanes, I., Flórez, H. 2003. Micropropagación in vitro de la caña flecha (Gynerium sagittatum) (aubl) beauv. c.v. "criolla" mediante el uso de segmentos nodales. Tesis de grado. Facultad de educación y ciencia. Departamento de Biología. Universidad de Sucre. Sincelejo. [ Links ]
48 Terzano, R., Santoro, A., Spagnuolo, M., Vekemans, B., Medici, L., Janssens, K. et al. 2010. Solving mercury (Hg) speciation in soil samples by synchrotron X-ray microspectroscopic techniques. Environ Pollut. 158 (8): 2702-9. [ Links ]
49 Unidad de Planeación Minera Energética (UPME). 2001. Estadísticas minero energéticas, 13. [ Links ]
50 United States Environmental Protection Agency (Usepa). 1994. Ground Water Modeling Compendium. 2 ed. EPA 500-B-94-004. [ Links ]
51 Vidal, J., Marrugo, J., Jaramillo, B., Pérez, L. 2010. Remediación de suelos contaminados con mercurio utilizando guarumo (Cecropia peltata). Revista Científica de Ingeniería y Desarrollo, 27. [ Links ]
52 Wang, Y. 2004. Phytoremediation of mercury by terrestrial plants. Tesis doctoral. Department of Botany, Stockholm University. pp. 1- 41. [ Links ]
53 Walpole, R., Myers, R. 1992. Probabilidad y estadística. 4 ed. México: McGraw-Hill Interamericana. [ Links ]
54 Wevar oller, A., Agostini, E., Talano, M., Capozucca, C., Milrad, S., Tigier, H., Medina, M. 2005. Overexpression of a basic peroxidase in transgenic tomato (Lycopersicon esculentum Mill. cv. Pera) hairy roots increases phytoremediation of phenol. Plant Sci. (169): 1102-1111. [ Links ]
55 Zheng, Y., Liu, Y., Hu, H., He, J. 2008. Mercury in soils of three agricultural experimental stations with long-term fertilization in China. Chemosphere, 72 (9): 1274-8. [ Links ]