Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Biotecnología
Print version ISSN 0123-3475
Rev. colomb. biotecnol vol.13 no.2 Bogotá July/Dec. 2011
ARTÍCULO DE INVESTIGACIÓN
Quorum sensing en la asociación beneficiosa de las bacterias con las plantas
Quorum sensing in beneficial plant-bacteria associations
Marcia M. Rojas Badía1.
1Departamento de microbiología y virología, Facultad de Biología, Universidad de La Habana, Cuba. marcia@fbio.uh.cu
Recibido: marzo 05 de 2010 Aprobado: noviembre 30 de 2011
Resumen
Se conoce que el quorum sensing es un atributo común de muchas especies bacterianas y que puede ser un carácter universal de las bacterias. Actualmente se están describiendo a un paso más rápido nuevas señales y nuevos sistemas de regulación por quorum sensing y se han desarrollado las investigaciones acerca de la comunicación célula-célula en bacterias basada en el mecanismo de quorum sensing. En los ambientes naturales existen muchas bacterias que viven juntas y utilizan varias clases de moléculas señales. Dentro de las señales especie específicas predominan las acilhomoserín lactonas (AHLs), pero ya se han descrito una amplia diversidad de moléculas involucradas en la señalización célula-célula. Numerosos bioensayos y sistemas sensores se han desarrollado para la detección, caracterización y cuantificación de las AHLs. Se han obtenido evidencias de la acción de estas moléculas señales en la colonización de la rizosfera, el swarming, las interacciones simbióticas y la capacidad de interrumpir el proceso de señalización de otras bacterias que convivan en el mismo ambiente. Todas estas potencialidades de las bacterias que involucran el mecanismo de quorum sensing, pudieran ser utilizadas para fortalecerla acción estimuladora del crecimiento vegetal y el control biológico de patógenos en los agroecosistemas sostenibles.
Palabras clave: comunicación celular, PGPB, control biológico, moléculas señal
Abstract
The quorum sensing is a common attribute in some bacterial species. Currently, several signals and new regulation systems are describing and the researchers are very interested in the cell-cell communication based on quorum sensing mechanism. In the natural environments several bacteria are living together, then several types of signal molecules are using. The acylhomoserines lactones (AHLs), are predominant, but a wide range of molecules are involved in cell-cell communication. To detect, characterization and quantification of signals numerous bioassays and sensors systems were developed. It were demonstrated the action of signals molecules in the rhizosphere colonization, swarming, symbiotic interactions and the capacity to break the signaling process of another microorganism in the same environment. These potentialities of bacteria would be used to improve the plant growth stimulation and biological control of pathogens in sustainable agricultural.
Key words: celular communication, PGPB, biological control, signals molecules
Introducción
El descubrimiento de que las bacterias tienen la capacidad de comunicarse entre ellas cambió la percepción de que son sencillos y simples organismos que habitan en nuestro mundo. En lugar del lenguaje, las bacterias usan moléculas señales, las cuales son secretadas al ambiente, y la concentración de los compuestos químicos está en dependencia de la densidad de la población.
Hace 40 años se publicaron 2 artículos que llevaron a una conclusión importante: las bacterias individuales pueden usar señales químicas para comunicarse y coordinar actividades como población.
Una de ellos estaba relacionado con la bacteria Gram positiva Streptococcus pneumoniae, quien controla factores de competencia genética por la producción de una sustancia química llamada factor de competencia. El otro artículo describe el control de la luminiscencia en la bacteria marina Gram negativa, Photobacterium fischeri (anteriormente denominado Vibrio fischeri), por diferentes señales que se describieron como autoinductores (Fuqua and Greenberg, 2002). Se conoce que el quorum sensing es un atributo común de muchas especies bacterianas y que puede ser un carácter universal de las bacterias. Actualmente se están describiendo a un paso más rápido nuevas señales y nuevos sistemas de regulación por quorum sensing (Fuqua y Greenberg, 2002).
En nuestros días el término de quorum sensing se usa para describir el fenómeno en el cual la acumulación de moléculas señales permite a una célula individual percibir el número de bacterias (densidad celular) que tiene a su alrededor por la detección y reacción con estos compuestos, esto es suficiente para que las bacterias inicien la expresión coordinada de genes específicos, lo que implica un cambio en su comportamiento hacia una fase multicelular. Esto ocurre bajo condiciones apropiadas y cuando están en un número que supera un nivel crítico. Este fenómeno también se conoce como comunicación célula-célula y autoinducción.
Los cambios en el comportamiento resultan en la activación de genes específicos en respuesta a la señal. El propósito del cambio es que la población de bacterias pueda cooperar para explotar el ambiente de formas que no pueden hacer las células individuales. Por ejemplo, una célula de una bacteria patógena que intenta invadir su hospedero tiene pocas posibilidades de entrar debido al sistema de defensa de la planta, entonces, para evadir la respuesta defensiva temprana de la planta, los patógenos retrasan la expresión de factores de virulencia.
En los ambientes naturales existen muchas bacterias que vivien juntas y utilizan varias clases de moléculas señales. Como emplean diferentes lenguajes no necesariamente pueden interactuar con otras bacterias.
Existen dos grandes grupos de señalización por quorum sensing: la intraespecífica y la interespecífica. Dentro de las señales especie específicas en las bacterias Gram negativas predominan las acilhomoserín lactonas (AHLs) y en las Gram positivas este mecanismo es mayormente mediado por pequeños péptidos (March and Bentley, 2004).
Los cuerpos de fructificación y el “swarming” son las formas más espectaculares en que las bacterias se pueden manifestar de manera colectiva similar a un tejido, pero la agregación celular, la formación de microcolonias y biopelículas son las formas de expresión más ampliamente distribuidas del comportamiento colectivo de las bacterias (Morris and Monier, 2003).
Para tener éxito en su nicho ecológico las bacterias deben ser capaces de sobrevivir y competir en complejas comunidades microbianas. Esto es especialmente cierto para las interacciones bacteria-bacteria y bacteria-planta en la rizosfera. Estas interacciones dependen de la expresión apropiada de genes específicos que estén involucrados en ellas. Muchas bacterias han desarrollado mecanismos de regulación de genes que les permiten detectar y responder a las diversas condiciones ambientales, incluyendo la presencia de competidores y plantas o animales hospedadores. Entre esos sistemas destacan los sistemas de autoinducción. En varias bacterias del grupo Gram negativo se han identificado diversos sistemas de regulación por autoinducción mediados por AHLs. Entre ellas se encuentran Agrobacterium tumefaciens, Erwinia carotovora, Pantoea stewartii, Ralstonia solanacearum, Pseudomonas aureofaciens y Rhizobium leguminosarum, aunque ya se han estudiado algunas otras moléculas que intervienen en el quorum sensing.
En el presente trabajo nos proponemos exponer los principales avances en el estudio del mecanismo de quorum sensing en bacterias beneficiosas asociadas a plantas, así como la importancia de este mecanismo en el estudio de esta interacción y su utilización en beneficio de la agricultura sostenible.
Diversidad estructural de las moléculas señales
Investigaciones recientes han mostrado la amplia diversidad de moléculas involucradas en la señalización célula-célula. Las más estudiadas para varias especies de bacterias son las acilhomoserín lactonas (AHLs). Además se han descrito otros sistemas como péptidos autoinductores (AIP) en Staphylococcus aureus (Waters and Bassler, 2005), γ-butirolactonas en Streptomyces (Waters and Bassler, 2005), dipéptidos cíclicos (Holden et al., 1999) y quinolonas en Pseudomonas (Venturi, 2006).
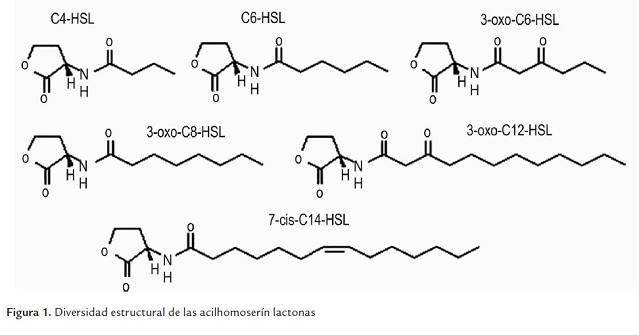
Las AHLs son las más difundidas y en muchos casos se han estudiado a profundidad química, bioquímica, fisiológica y molecularmente. En general las AHLs están compuestas por una cadena acil-grasa ligada a una homoserina lactonizada a través de una unión amida (Fuqua y Greenberg, 2002) (figura 1). El largo de la cadena acílica puede variar entre 4 y 16 átomos de carbono en números pares (Whitehead et al., 2001), aunque Lithgow et al. (2000) identificaron una acilhomoserín lactona con 7 átomos de carbono en la cadena acílica, pero la fuente de esta cadena con número impar aún no se ha dilucidado. El tercer carbono en la cadena acílica puede ser un carbonil totalmente oxidado, llevar un grupo carboxilo o estar totalmente reducido, variedad que se debe a la derivación de la cadena acílica de la biosíntesis del ácido graso. Dos de las acilhomoserín lactonas más largas descritas tienen una simple unión insaturada en el medio de la cadena acílica (Gray et al., 1996; Puskas et al., 1997).
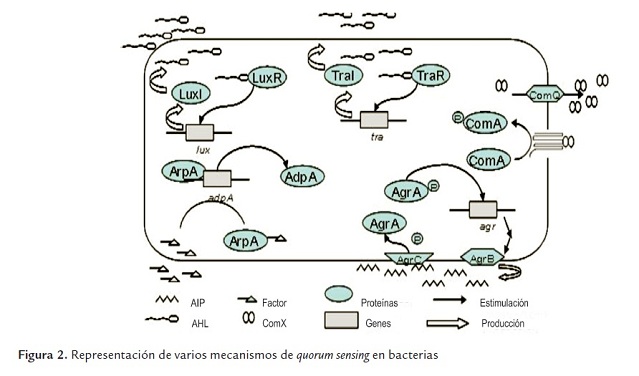
En estos momentos se han secuenciado más de veinte proteínas homólogas a LuxR y LuxI en diferentes microorganismos. LuxR es un polipéptido de 250 aminoácidos que requiere de la presencia de chaperonas moleculares GroESL para que pase a su forma activa a (Whitehead et al., 2001) (figura 2).
Los aislamientos de las secuencias de aminoácidos revelan sorprendentemente poca identidad. Solo 5 residuos se conservan totalmente en las secuencias que están actualmente disponibles. Las dos terceras partes de la región amino-terminal de LuxR actúan como sitio de unión de AHLs, de ahí que se requieran altas concentraciones de estas moléculas para la inducción de este tipo de proteína (Whitehead et al., 2001).
LuxI es una familia de proteínas que directamente participa en la síntesis de la molécula señal, tiene una cadena de 190-230 aminoácidos, los cuales coparten entre 30-35% de pares de bases de identidad. En la mayoría de proteínas tipo LuxI existen 10 residuos conservados en los 110 aminoácidos amino-terminales. Desafortunadamente no se puede predecir cuál AHLs será sintetizada por los diferentes homólogos de LuxI teniendo en cuenta solamente el análisis de las secuencias (Fuqua y Greenberg, 2002).
De hecho distintas cepas pertenecientes a la misma especie pueden sintetizar diferentes tipos de AHLs dependiendo del hábitat en el que se encuentren. De manera similar los análisis de secuencias de LuxR homólogas no ofrecen información acerca de cuál puede ser la AHLs que se una a cada proteína (Eberl, 1999).
Se considera que el transporte de las AHLs de cadenas cortas se da por simple difusión, mientras que para las AHLs de cadenas de más de 12 átomos de carbono, ocurre una transportación activa a través de un sistema de exflujo o influjo como se ha estudiado en Pseudomonas aeruginosa (Pearson et al., 1999).
Por otra parte, los péptidos autoinductores (AIP) producidos por Staphylococcus aureus, que por lo general es microbiota normal de la piel en humanos y en ocasiones un patógeno oportunista, también se ha encontrado en la rizosfera y el interior de diferentes plantas. Estas bacterias usan como señales un sistema de dos componentes, tipo sensor unido a membrana como receptor histidín quinasa. La producción y el control de estos péptidos están codificados en los genes agr (Waters and Bassler, 2005) (figura 2).
Se ha estudiado la producción de γ-butirolactonas por Streptomyces, uno de los principales géneros reservorios de metabolitos secundarios en el suelo. El primer compuesto descrito, Factor A (2-isocapriloil-3R-hidroxi-metil-γbutirolactona), producido por S. griseus, controla la diferenciación morfológica y la producción del antibiótico streptomicina mediante la regulación de la expresión del activador transcripcional AdpA (Waters and Bassler, 2005) (figura 2).
Se han descrito dipéptidos cíclicos como moléculas señal en gran número de bacterias, tanto Gram positivas como Gram negativas (Holden et al., 1999). La producción de surfactina, un lipopéptido cíclico, está a cargo de Bacillus subtilis y está regulada por la densidad de población por la ferormona ComX (Fraser and Hughes, 1999) (figura 2).
En el género Pseudomonas se produce una molécula señal tipo quinolona, que pertenece a la familia de 4-hidroxi-2-alkilquinolonas, la cual es conocida por su actividad antimicrobiana y que resulta necesaria para incrementar la solubilidad y potenciar la producción de biosurfactantes de Pseudomonas aeruginosa (Venturi, 2006). Esta señal actúa además como una unión regulatoria entre los circuitos de quorum sensing Las y Rhl. El mecanismo molecular que interviene en la expresión de los genes es aún desconocido.
Identificación y cuantificación de las moléculas señales
Numerosos bioensayos y sistemas sensores se han desarrollado para la detección, caracterización y cuantificación de las AHLs.
La cepa CV026 de Chromobacterium violaceum es uno de los sistemas más utilizados en este sentido. Esta cepa es una mutante mini-Tn5 de la cepa tipo de esta especie ATCC 31532, en la cual la producción de AHL está involucrada en la síntesis de violaceína, lo que permite su detección (McClean et al, 1997).
Otro sistema muy conocido para la detección de AHLs es el que utiliza Agrobacterium tumefaciens NTL4 (pZLR4) como organismo indicador (Cha et al., 1998). Esta construcción consiste en la inserción del gen que codifica para la β-glucoronidasa, lo que permite la detección de la producción de la molécula por la cepa a probar.
La extracción de sobrenadantes para cromatografía en capa delgada con acetato de etilo acidificado (con 0,5% de ácido fórmico) tiene mayor eficiencia que con acetato de etilo solo. Utilizando el primero y realizando 3 extracciones queda un remanente de AHLs sin extraer del 20-30% en el sobrenadante. Esta cromatografía en capa delgada se lleva a cabo en un sistema de solvente metanol/agua en una proporción 60:40 (v/v) (Ravn et al., 2001).
La cromatografía en capa delgada tiene una gran versatilidad y no requiere de reactivos caros, como el equipamiento del HPLC o el uso de películas o luminómetro.
Recientemente, De Angelis et al. (2007) obtuvieron un biosensor basado en Agrobacterium tumefaciens (pAHL-Ice), el cual permite detectar la producción de AHLs en las comunidades microbianas intactas de la rizosfera y el suelo en general.
Estos métodos descritos son utilizados para la detección e identificación de las moléculas señales, pero rara vez aparecen en la literatura estudios sobre la cinética de producción de las AHLs, así como diferentes metodologías para cuantificar estas moléculas señales.
La cuantificación de la producción de violaceína utilizando la cepa de Chromobacterium violaceum CV026 permite tener una medida indirecta de la producción de molécula señal por la cepa probada en medio líquido. Esto se calcula como la relación entre la absorbancia del extracto de violaceína en butanol (585 nm) sobre la densidad del cultivo (600 nm), multipicado por 1000, refiriendo el valor obtenido como actividad en unidades de violaceína (Blosser and Gray, 2000).
Hay varias especies bacterianas en las que los genes lux se han encontrado separados de los genes fenotípicos regulados por las AHLs, entre las que se encuentra Rhizobium leguminosarum (Gray et al., 1996). En estas bacterias la regulación de los genes lux puede seguir un patrón diferente al de la respuesta fenotípica. Resumiendo, existen muchos casos en que la producción de AHLs parece ser constitutiva, pero también está ocurriendo una regulación positiva del fenotipo a través del mecanismo de quorum sensing.
Influencia del quorum sensing en la colonización y el movimiento de las bacterias en la rizosfera
En la naturaleza, la colonización de la rizosfera por una mezcla de poblaciones bacterianas es un proceso muy común. Entre estos microorganismos existe una gran diversidad de interacciones físicas y metabólicas necesarias para la adhesión, crecimiento y supervivencia, incluso cuando las condiciones ambientales son adversas. Estas comunidades microbianas generalmente se encuentran adheridas a la superficie de las raíces, organizadas en una comunidad denominada biopelícula (Colón-González y Membrillo-Hernández, 2003).
Se ha demostrado la formación de una biopelícula homogénea en la cepa salvaje de Pseudomonas putida mientras que la mutante en los genes ppuI y ppuA forma biopelículas con características de microcolonias y con canales llenos de agua (Steidle et al. (2002), lo que demuestra la regulación de la formación de esta estructura mediante el mecanismo de quorum sensing.
Varios factores abióticos influyen sobre las asociaciones de las biopelículas en la raíz, como son: las variaciones físico-químicas a lo largo de la superficie de la raíz, la disponibilidad de nutrientes, la temperatura, la humedad relativa, entre otros (Stanley and Lazazzera, 2004).
Los exudados radicales sirven como principal factor disparador de la colonización de la raíz (Lugtenberg et al., 1999) y las asociaciones de biopelículas (Walker et al., 2004). Sin embargo, como plantean Rudrappa et al. (2008), no se conoce específicamente cuál es el compuesto orgánico secretado por la raíz que determina la estructura de la biopelícula, lo que resulta necesario para comprender mejor la interacción de las bacterias con la planta.
Rudrappa et al. (2008) propusieron un esquema hipotético de formación de biopelículas a lo largo de la raíz, donde en las regiones superiores ocurre la formación de la biopelícula en los tejidos del xilema. En esta región se forman agregados de células a través del cilindro del xilema para absorber los nutrientes que pasan por estos fluidos (Koutsoudis et al., 2006). En la región media de la raíz madura se forma una biopelícula mejor estructurada como resultado de mayores fluctuaciones de nutrientes (Shrout et al., 2006). En el extremo de la raíz, donde la disponibilidad de nutrientes es menor y se pueden excretar sustancias antimicrobianas, se forma una biopelícula más plana (Shrout et al., 2006).
La regulación del swarming por quorum sensing presumiblemente conlleva a una óptima diseminación de las células bacterianas cuando la población debe alcanzar un hábitat extenso (Whitehead et al., 2001).
El swarming bacteriano es un tipo de traslocación donde el movimiento está guiado por el flagelo en presencia de un muscílago extracelular, a través del cual la bacteria puede diseminarse como una biopelícula sobre la superficie. Este mucílago está formado por una mezcla de carbohidratos, proteínas, péptidos, surfactantes, etc. (Fraser and Hughes, 1999; Sharma and Anad, 2002).
Este fenómeno se ha descrito en géneros asociados a plantas como Bacillus, Chromobacterium, Azospirillum, Serratia, Burkholderia, Pseudomonas y Sinorhizobium y otras bacterias patógenas de diferentes hábitats (Proteus, Vibrio, Clostridium, Escherichia, Salmonella, Aeromonas, Yersinia).
La sobreproducción de flagelina en variantes fenotípicas de Pseudomonas fluorescens F113, trae como resultado un flagelo más largo que mayor cantidad de flagelos. Además, estas células colonizan preferencialmente la parte distal de la raíz y reflejan una especialización en la colonización de diferentes partes de la raíz en comparación con la cepa salvaje (Sánchez-Contreras et al., 2002).
Se han obtenido evidencias indirectas para el swarming mediado por quorum sensing por la observación de varios compuestos similares a moléculas señales como diketopiperazinas (Holden et al., 1999), furanonas halogenadas (Rasmussen et al., 2000) y sustancias secretadas por plantas (Teplitski et al., 2000, Bauer and Teplitski, 2001) que pueden influir en diferentes bacterias.
Influencia del quorum sensing en las interacciones simbióticas
Las interacciones simbióticas entre los rizobios fijadores de nitrógenos y las leguminosas son el resultado de una serie de señales que se producen entre la bacteria y la planta hospedera. El inicio del proceso de simbiosis se produce cuando existe una determinada concentración de bacterias alrededor de las raíces de la planta, por tanto, no fue una sorpresa para los investigadores el hecho de que este proceso estuviera mediado por el mecanismo de quorum sensing.
Además de las moléculas estudiadas tradicionalmente que están involucradas en el proceso de nodulación (flavonoides, factores de nodulación, exopolisacáridos), actualmente se están incluyendo en este tipo de estudios las AHLs (González and Marketon 2003). Estos autores han señalado que el quorum sensing regula varios fenómenos de la simbiosis como son la eficiencia de nodulación, el desarrollo del simbiosoma, la producción de exopolisacáridos y la fijación de nitrógeno, todas las cuales son imprescindibles en el establecimiento de la simbiosis.
Se han descrito varias moléculas de la familia de las AHLs producidas por rizobios y se ha logrado determinar, en algunas de ellas, el fenómeno específico que regula. Entre los rizobios, el fenómeno de quorum sensing mejor caracterizado es el de Rhizobium leguminosarum bv. viciae, el cual tiene varios sistemas de quorum sensing (rai, rhi, cin y tra) y se ha identificado las vías de regulación de la mayoría de estos sistemas. Inicialmente se estudió el sistema rhi, compuesto por genes análogos a LuxI y LuxR, y que forma un operón (rhiABC) localizado en el plásmido simbiótico pRL1JI (Cubo et al., 1992, Rodelas et al., 1999). Estos genes se expresan en la rizosfera pero no en los bacteroides, algunos de ellos intervienen en la eficiencia de nodulación (Cubo et al., 1992, Rodelas et al., 1999), otros en la transferencia del plásmido simbiótico (Wilkinson et al., 2002) y de algunos aún no se conoce su función. El locus cinIR controla una compleja cascada de bucles de autoinducción con otros tres sistemas de autoinducción con sus correspondientes AHLs. Estos sistemas incluyen raiI/raiR (Rosemeyer et al., 1998), traI/traR y rhi/rhiR. Otras cepas de rizobios parecen compartir algunos de estos loci de autoinducción, pero no todos los loci han sido encontrados en todas las cepas.
En Sinorhizobium meliloti se han descrito varias AHLs reguladas por el sistema traR/traI, relacionadas con la transferencia del plásmido simbiótico y el sistema sinR/sinI que controla la producción de exopolisacáridos EPSII (Marketon and González, 2002).
Otro tipo de molécula señal diferente de las AHLs se describió para Bradyrhizobium sp., la bradyoxetina, que interviene en la activación de los genes nod (Loh et al., 2001, Loh et al., 2002). Esta es una molécula de bajo peso molecular que tiene una estructura similar a ciertos antibióticos y sideróforos.
González and Marketon (2003) consideran que los rizobios constituyen un modelo excelente para el estudio del quorum sensing, debido al conocimiento bioquímico, fisiológico y molecular que existe de los fenómenos que ocurren en la simbiosis entre la bacteria y la planta.
Utilización de la disrupción del quorum en el control biológico de patógenos
Como hemos venido analizando a lo largo del trabajo, la señalización basada en las AHLs entre bacterias Gram negativas está muy difundida. Las moléculas de la familia de las AHLs son muy similares, incluso muchos microorganismos utilizan la misma molécula para regular diferentes fenotipos, esto nos permite predecir que puede existir una comunicación interespecífica en los ecosistemas donde cohabitan especies que produzcan la misma molécula señal; esto posibilitaría su utilización con diferentes fines.
La primera aplicación de disrupción del quorum con el propósito de controlar una enfermedad fue la introducción de los genes iiA clonados de Bacillus sp. en plantas transgénicas de tabaco y papa (Dong et al., 2001). Muchas especies de Bacillus secretan la enzima AiiA, que es extremadamente específica, puede clivar los anillos de lactona de la cadena acílica de las AHLs y, por tanto, obtenerse una molécula señal inactiva (Dong et al., 2000). La expresión de estos genes y la producción de AHLs lactonasa por la planta modificada genéticamente paraliza el sistema de quorum sensing de la bacteria fitopatógena Erwinia carotovora, resultando en un incremento de la resistencia de la planta a enfermedades.
Recientemente se ha descubierto la existencia de estrategias de competencia en el ecosistema del suelo dirigidas específicamente contra los sistemas de autoinducción. Así, Bacillus sp. (240B1) es capaz de producir la inactivación enzimática de estas N - acil homoserin lactonas mediante la expresión del gen aiiA, que codifica una proteína con actividad lactonasa (AiiA) y con capacidad de destruir el anillo lactónico de las AHLs. De esta forma, su actividad determinaría bajos niveles de autoinductores, suprimiendo cualquier tipo de regulación por autoinducción. Bacillus sp. no se ve afectado por esta enzima ya que se trata de una bacteria Gram positiva que no posee sistemas de autoinducción regulados por AHLs (Dong et al., 2000).
Molina et al. (2003) demostraron que la cepa A24 de Bacillus tiene la capacidad de degradar las AHLs producidas por los patógenos de plantas Erwinia carotovora y Agrobacterium tumefaciens y presenta un amplio espectro de actividad que reduce significativamente las enfermedades producidas por estos patógenos en tomate y papa. Además, se ha demostrado que el gen responsable de esta actividad de disrupción del quorum se encuentra ampliamente distribuido en este género.
Recientemente se ha demostrado que la capacidad de control biológico de B. subtilis sobre Pseudomonas syringae pv. tomato DC3000 se ve favorecida por la formación de biopelícula y la producción de surfactina (Bais et al., 2004).
Leadbetter and Greenberg, (2000) aislaron del suelo una cepa de Variovorax paradoxus que tiene la capacidad de utilizar varias AHLs como única fuente de energía y nitrógeno, fundamentalmente a través de una lactonasa que se ha propuesto rendir al final de la degradación propionato. Esta actividad puede romper el proceso de señalización de otras bacterias que convivan en el mismo ambiente, lo cual puede ser explotado para interrumpir actividades reguladas por quorum sensing como la patogenicidad de determinados hongos del suelo.
Por otra parte, se conoce que un gran número de bacterias asociadas con eucariontes regulan fenotipos por quorum sensing como son: la producción de exoenzimas, exopolisacáridos y antibióticos. Como estas bacterias producen señales moleculares que regulan estos mecanismos, potencialmente deben existir hospederos eucarióticos que pueden romper este mecanismo de regulación mediante la producción de compuestos similares a las señales bacterianas (González and Marketon, 2003).
Se ha demostrado que el guisante (Pisum sativum) y otras plantas producen compuestos similares a las AHLs, denominadas AHLs mimics, que interfieren en el mecanismo de regulación por quorum sensing de varias cepas bacterianas (Teplitski et al., 2000).
Recientemente se demostró que las furanonas halogenadas producidas por determinadas plantas, modulan la actividad de LuxR a través de la degradación acelerada del activador transcripcional por bloqueo o desplazamiento de la unión de la señal acil homoserínlactona, ya que actúa como un inhibidor competitivo (Manefield et al., 2002).
Consideraciones Finales
En la última década se han desarrollado las investigaciones acerca de la comunicación célula-célula en bacterias basada en el mecanismo de quorum sensing.
En estos momentos ya se puede comprender cómo pueden “hablar” las bacterias a través de señales mensajeras como las AHLs. Ha existido un gran progreso en la descripción molecular de los mecanismos genéticos que regulan este fenómeno, lo cual ha permitido analizar los procesos fisiológicos regulados por quorum sensing.
Son muchas las bacterias descritas que utilizan el mecanismo de quorum sensing para controlar numerosos procesos fisiológicos, pero en los próximos años continuaremos incrementando tanto la lista de las bacterias como las funciones involucradas.
La era de la Biología Molecular, la Proteómica y la Bioinformática nos permitirá no solo continuar profundizando en el conocimiento de los mecanismos involucrados, sino también en la búsqueda de alternativas viables para controlar la interacción de los microorganismos y los organismos eucariontes, como las plantas, los animales y el hombre, a través de la explotación del quorum sensing como estrategias anti-quorum sensing.
Desde el punto de vista aplicado, el comportamiento de las bacterias influenciado por swarming y el establecimiento de las biopelículas, puede ayudar a controlar la colonización de la raíz y la permanencia de las bacterias en los tejidos vegetales y la rizosfera, lo cual puede tener importantes aplicaciones en la agricultura, ya que puede ser utilizado en el control biológico de patógenos y la estimulación del crecimiento vegetal.
Referencias Bibliográficas
1 Bais, H. P., Fall, R. and Vivanco, J. M. 2004. Biocontrol of Bacillus subtilis against infection of Arabidopsis roots by Pseudomonas syringae is facilitated by biofilm formation and surfactin production. Plant Physiol 134: 307-319. [ Links ]
2 Bauer, W. D. and Teplitski, M. 2001. Can plants manipulate bacterial quorum sensing? Australian Journal Plant Physiologi 28: 913-921. [ Links ]
3 Blosser, R. S. and Gray, K. M. 2000. Extraction of violacein from Chromobacterium violaceum provides a new quantitative bioassay for N-acyl homoserine lactone autoinducers. Journal of Microbiological Methods 40: 47-55. [ Links ]
4 Colón-González, M. y Membrillo-Hernández., J. 2003. Comunicación entre bacterias. Microbios en línea. [ Links ]
5 Cubo, M. T., Economou, A., Murphy, G., Johnston, A. W. and Downie., J. A. 1992. Molecular characterization and regulation of the rhizosphere-expressed genes rhiABCR that can influence nodulation by Rhizobium leguminosarum biovar viciae. Journal of Bacteriology 174: 4026-4035. [ Links ]
6 Cha, C., Gao, P., Chen, Y. C., Shaw, P. D. and Farrand, S. K. 1998. Production of acyl-homoserine lactone quorum-sensing signals by gram-negative plant-associated bacteria. Molecular Plant-Microbe Interactions 11: 1119-1129. [ Links ]
7 De Angelis, K. M., Firestone, M. K. and Lindow, S. E. 2007. Sensitive whole-cell biosensor suitable for detection a variety of N-acyl homoserine lactones in intact rhizosphere Microbial communities. Applied Environmental Microbiology 73 (11): 3724-3727. [ Links ]
8 Dong, Y. H., Wang, L. H., Xu, J. L., Zhang, H. B., Zhang, X. F. and Zhang, L. H. 2001. Quenching quorum-sensing-dependent bacterial infection by an N-acyl homoserine lactonase. Nature 411: 813-17. [ Links ]
9 Dong, Y. H., Xu, J. L., Li, X. Z. and Zhang, L. H. 2000. AiiA, an enzyme that inactivates the acylhomoserine lactone quorum-sensing signal and attenuates the virulence of Erwinia carotovora. Proceedings of the National Academy of Sciences of the United States of America 97: 3526-3531. [ Links ]
10 Eberl, L. 1999. N-acyl homoserine lactones-mediated gene regulation in Gram negative bacteria. Systematic and Applied Microbiology 22: 493-506. [ Links ]
11 Fraser, G. M. and Hughes, C. 1999. Swarming motility. Current Opinion in Microbiology 2: 630-635. [ Links ]
12 Fuqua, C. and Greenberg, E. P. 2002. Listening in on bacteria: Acyl-homoserine lactone signalling. Molecular Cell Biology 3: 685-695. [ Links ]
13 Gonzalez, J. E. and Marketon, M. M. 2003. Quorum sensing in nitrogen-fixing rhizobia. Microbiology and Molecular Biology Reviews 67 (4): 574-592. [ Links ]
14 Gray, K. M., Pearson, J. P., Downie, J. A., Boboye, B. E. A. and Greenberg, E. P. 1996. Cell-to-cell signalling in the symbiotic nitrogen-fixing bacterium Rhizobium leguminosarum: autoinduction of a stationary phase and rhizosphere expressed genes. Journal of Bacteriology 178: 372-376. [ Links ]
15 Holden, M. T., Chhabra, S. R., Nys, R. d., Stead, P. and Bainton, N. J. 1999. Quorum-sensing cross talk: isolation and chemical characterization of cyclic dipeptides from Pseudomonas aeruginosa and other gram-negative bacteria. Molecular Microbiology 33: 1254-66. [ Links ]
16 Koutsoudis, M. D., Tsaltas, D., Minogue, T. D. y Bodman, S. B. v. 2006. Quorum-sensing regulation governs bacterial adhesion, biofilm development, and host colonization in Pantoea stewartii subspecies stewartii. Proceedings of the National Academy of Sciences of the United States of America 103: 5983-5988. [ Links ]
17 Leadbetter, J. R. and Greenberg, E. P. 2000. Metabolism of Acyl-Homoserine Lactone quorum-sensing signals by Variovorax paradoxus. Journal of Bacteriology 182 (24): 6921-6926. [ Links ]
18 Lithgow, J. K., Wilkinson, A., Hardman, A., Rodelas, B., F. Wisniewski-Dye, Williams, P. and Downie., J. A. 2000. The regulatory locus cinRI in Rhizobium leguminosarum controls a network of quorum-sensing loci. Molecular Microbiology 37: 81-97. [ Links ]
19 Loh, J., Carlson, R. W., York, W. S. and Stacey, G. 2002. Bradyoxetin, a unique chemical signal involved in symbiotic gene regulation. Proceedings of the National Academy of Sciences of the United States of America 99: 14446-14451. [ Links ]
20 Loh, J. T., Yuen-Tsai, J. P., Stacey, M. G., Lohar, D., Welborn, A. and Stacey, G. 2001. Population density-dependent regulation of the Bradyrhizobium japonicum nodulation genes. Molecular Microbiology 42: 37-46. [ Links ]
21 Lugtenberg, B. J. J., Kravchenko, L. V. and Simons, M. 1999. Tomato seed and root exudate sugars: composition, utilization by Pseudomonas biocontrol strains and role in rhizosphere colonization. Environmental Microbiology 1: 439-446. [ Links ]
22 Manefield, M., Rasmussen, T. B., Henzter, M., Andersen, J. B., Steinberg, P., Kjelleberg, S. and Givskov, M. 2002. Halogenated furanones inhibit quorum sensing through accelerated LuxR turnover. Microbiology 148: 1119-1127. [ Links ]
23 March, J. C. and Bentley, W. E. 2004. Quorum sensing and bacterial cross-talk in biotechnology. Current Opinion in Biotechnology 15: 495-502. [ Links ]
24 Marketon, M. M. and González, J. E. 2002. Identification of two quorum-sensing systems in Sinorhizobium meliloti. Journal of Bacteriology 184: 3466-3475. [ Links ]
25 McClean, K. H., Winson, M. K., Fish, L., Taylor, A., Chhabra, S. R., Camara, M., Daykin, M., Lamb, J. H., Swift, S., Bycroft, B. W., Stewart, G. S. and Williams, P. 1997. Quorum sensing and Chromobacterium violaceum: exploitation of violacein production and inhibition for the detection of N-acylhomoserine lactones. Microbiology 143: 3703-3711. [ Links ]
26 Molina, L., Constantinescu, F., Michel, L., Reimmann, C., Duffy, B. and Défago, G. 2003. Degradation of pathogen quorum-sensing molecules by soil bacteria: a preventive and curative biological control mechanism. FEMS Microbiology Ecology 45: 71-81. [ Links ]
27 Morris, C. E. and Monier, J.-M. 2003. The ecological significance of biofilm formation by plant-associated bacteria. Annual Review of Phytopathology 41: 429-453. [ Links ]
28 Pearson, J. P., Delden, C. v. and Iglewski, B. H. 1999. Active efflux and diffusion are involved in transport of Pseudomonas aeruginosa cell-to-cell signaling. Journal of Bacteriology 181: 1203-1210. [ Links ]
29 Puskas, A., Greenberg, E. P., Kaplan, S. and Schaefer, A. L. 1997. A quorum-sensing system in the free-living photosynthetic bacterium Rhodobacter sphaeroides. Journal of Bacteriology 179: 7530-7537. [ Links ]
30 Rasmussen, T. B., Manefield, M., Kumar, L., Labbate, M., England, D., Rice, S., Givskov, M., Saldmon, G. P., Steward, G. S., Bycroft, B. W., Kjelleberg, S. and Williams, P. 2000. How Delinea pulcra furanones affect quórum sensing and swarming motility in Serratia liquefaciens MG1. Microbiology 146: 3237-3244. [ Links ]
31 Ravn, L., Christensen, A.B., Molin, S., Givskov, M. and Gram, L. 2001. Methods for acylated homoserine lactones produced by Gram-negative bacteria and their application in studies of AHL-production kinetics. J. Microbiol. Methods 44 : 239-251. [ Links ]
32 Rodelas, B., Lithgow, J. K., Wisniewski-Dye, F., Hardman, A., Wilkinson, A., Economou, A., Williams, P. and Downie, J. A. 1999. Analysis of quorum-sensing-dependent control of rhizosphere-expressed (rhi) genes in Rhizobium leguminosarum bv. viciae. Journal of Bacteriology 181: 3816-3823. [ Links ]
33 Rudrappa, T., Biedrzycki, M. L. and Bais, H. P. 2008. Causes and consequences of plant-associated biofilms. FEMS Microbiology Ecology: 1-14. [ Links ]
34 Rosemeyer, V., Michiels, J., Verreth, C. and Vanderleyden, J. 1998. luxI-and luxR-homologuous genes of Rhizobium etli CNPAF512 contribute to synthesis of autoinducer molecules and nodultaion of Phaseolus vulgaris. J. Bacteriol.180:815-821. [ Links ]
35 Sánchez-Contreras, M., Martín, M., Villancieros, M., O´Gara, F., Bonilla, I. and Rivilla, R. 2002. Phenotypic selection and phase variation occur during alfalfa root colonization by Pseudomonas fluorescens F113. Journal of Bacteriology 184: 1587-1596. [ Links ]
36 Sharma, M. and Anad, S. K. 2002. Swarming: a coordinated bacterial activity. Indian J. Med. Sci. 83: 707-715. [ Links ]
37 Shrout, J. D., Chopp, D. L., Just, C. L., Hentzer, M., Givskov, M. and Parsek, M. R. 2006. The impact of quorum sensing and swarming motility on Pseudomonas aeruginosa biofilm formation is nutritionally conditional. Molecular Microbiology 62: 1264-1277. [ Links ]
38 Stanley, N. R. and Lazazzera, B. A. 2004. Environmental signals and regulatory pathways that influence biofilm formation. Molecular Microbiology 52: 917-924. [ Links ]
39 Steidle, A., Allesen-Holm, M., Riedel, K., Berg, G., Givskov, M., Molin, S. and Eberl, L. 2002. Identification and characterization of an N-acylhomoserine lactone-dependent quorum-sensing system in Pseudomonas putida strain IsoF. Applied and Environmental Microbiology 68: 6371-6382. [ Links ]
40 Teplitski, M., Robinson, J. B. y Bauer, W. D. 2000. Plants secrete substances that mimic bacterial N-acyl homoserine lactone signal activities and affect population density-dependent behaviors in associated bacteria. Molecular Plant-Microbe Interactions 13: 637-648. [ Links ]
41 Venturi, V. 2006. Regulation of quorum sensing in Pseudomonas. FEMS Microbiology Reviews 30: 274-291. [ Links ]
42 Walker, T. S., Bais, H. P., Deziel, E., Schweizer, H. P., Rahme, L. G., Fall, R. and Vivanco, J. M. 2004. Pseudomonas aeruginosa-Plant Root Interactions. Pathogenicity, Biofilm Formation, and Root Exudation. Plant Physiology 134: 320-331. [ Links ]
43 Waters, C. M. and Bassler, B. L. 2005. Quorum Sensing: Cell-to-Cell Communication in bacteria. Annual Review Cell and Developmental Biology 21: 319-46. [ Links ]
44 Whitehead, N. A., Barnard, A. M., Slater, H., Simpson, N. J. and Salmond, G. P. 2001. Quorum sensing in Gram-negative bacteria. FEMS Microbiology Reviews 25: 365-404. [ Links ]
45 Wilkinson, A., Danino, V., Wisniewski-Dye, F., Lithgow, J. K. and Downie, J. A. 2002. N-Acyl-homoserine lactone inhibition of rhizobial growth is mediated by two quorum-sensing genes that regulate plasmid transfer. Journal of Bacteriology 184: 4510-4519. [ Links ]