Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Biotecnología
Print version ISSN 0123-3475
Rev. colomb. biotecnol vol.13 no.2 Bogotá July/Dec. 2011
ARTÍCULO CORTO
Concentración mínima inhibitoria de higromicina B en callos embriogénicos de arroz (Oryza sativa L.)
Minimum inhibitory concentration of higromycin B in rice embryogenic calli (Oryza sativa L.)
Iván Darío Barbosa Cepeda1 , Alejandro Chaparro Giraldo2
1Biólogo, estudiante MSc. en Biología-Genética, Grupo de Ingeniería Genética de Plantas, Departamento de Biología, Universidad Nacional de Colombia, Bogotá. idbarbosac@unal.edu.co
2Ph.D., profesor asociado, director Grupo de Ingeniería Genética de Plantas, Departamento de Biología, Universidad Nacional de Colombia, Bogotá. achaparrog@bt.unal.edu.co
Recibido: marzo 15 de 2011 Aprobado: noviembre 25 de 2011
Resumen
Uno de los elementos imprescindibles en la ingeniería genética de plantas es un sistema de selección eficiente. El propósito de este trabajo fue evaluar la sensibilidad al marcador de selección higromicina B, de callos embriogénicos obtenidos a partir del escutelo de semilla de tres variedades colombianas de arroz (FEDEARROZ 2000, FEDEARROZ 50 y FEDEARROZ 369). Además, se validó la respuesta de estas variedades al protocolo de regeneración empleado. Se probaron cuatro concentraciones del antibiótico (25 mg/L, 50 mg/L, 75 mg/L y 100 mg/L) más un control sin higromicina B. Los resultados obtenidos mostraron que una concentración de 50 mg/L de antibiótico en el medio de regeneración es adecuada para la selección. Con esta concentración se impide la formación de brotes, aunque los callos no mueren completamente. Por otra parte, se estableció que el protocolo de regeneración utilizado es de baja eficiencia y, por consiguiente, es necesario optimizarlo para poder usarlo en procesos de ingeniería genética de cultivares colombianos de arroz.
Palabras clave: variedades colombianas de arroz, FEDEARROZ 2000, FEDEARROZ 50, FEDEARROZ 369, sistema de selección, antibiótico.
Abstract
An efficient selection system is one of the most important elements of plant genetic engineering. The purpose of this study was to evaluate the sensitivity of scutellum-derived embriogenic calli obtained from three colombian rice varieties (FEDEARROZ 2000, FEDEARROZ 50 and FEDEARROZ 369), to the selection marker hygromycin B. Aditionally, the response of these varieties to the regeneration protocol was measured. Four antibiotic concentrations were tested (25 mg/L, 50 mg/L, 75 mg/L and 100 mg/L) plus one control without hygromycin B. The results show that 50 mg/L of antibiotic in the regeneration medium is adequate for selection. This concentration prevents the formation of shoots, though the calli do not die. It was also established that the regeneration protocol is a low-efficiency system and it needs to be improved, in order to use it for colombian rice genetic engineering.
Key words: rice Colombian varieties, FEDEARROZ 2000, FEDEARROZ 50, FEDEARROZ 369, selection system, antibiotic.
Introducción
El arroz (Oryza sativa L.) es uno de los cultivos de mayor importancia en el mundo, tanto por su impacto económico como por su papel en la seguridad alimentaria (Kathuria et al ., 2007). Debido al aumento poblacional, en los próximos años se espera una mayor demanda. No obstante, para lograr suplir este incremento, es necesario obtener variedades nuevas que puedan enfrentar el reto de producir más con menos tierras disponibles para agricultura, y bajo la presión ejercida por el calentamiento global (Sharma et al ., 2005; Kathuria et al ., 2007; Wahid et al ., 2007; FAO, 2008).
Colombia no es uno de los grandes productores de arroz a nivel mundial. Sin embargo, a nivel continental ocupa el tercer lugar en producción después de Estados Unidos y Brasil, y es el mayor productor en la región andina. Si bien entre 1991 y 2005 las importaciones de grano han superado a las exportaciones, el país cuenta con la posibilidad de autoabastecerse completamente de arroz gracias a la disponibilidad de tierras, a la tecnificación de la producción y a la obtención de variedades mejoradas. El cultivo de arroz tiene un impacto importante en la economía, de él depende el sostenimiento de muchas familias campesinas y constituye cerca del 11% del valor total de la actividad agrícola colombiana (Espinal et al ., 2005).
En Colombia, el incremento en la producción por hectárea logrado hasta hoy, se ha conseguido fundamentalmente con la aplicación de buenas prácticas agrícolas junto con la producción de variedades con características productivas, agronómicas y culinarias óptimas, mediante la utilización de técnicas convencionales de mejoramiento (Diago, 2003). Sin embargo, el mejoramiento convencional se encuentra limitado por la naturaleza misma del método y por la falta de germoplasma disponible para cruces, que va asociada a la estrechez de la base genética actual de gran parte de los cultivos de seguridad alimentaria (Morgante and Salamini, 2003; Ashraf and Akram, 2009; Ashraf, 2010). Por estas razones es pertinente explorar alternativas biotecnológicas para ampliar la diversidad genética del arroz y obtener nuevas variedades (Diago, 2005).
La ingeniería genética de plantas es una de las herramientas biotecnológicas que puede emplearse para la obtención de nuevas variedades en diferentes cultivos. Mediante esta técnica es posible transferir un gen o un pequeño grupo de genes provenientes de cualquier fuente, a un organismo de interés (Chaparro, 2005; Sharma et al ., 2005). Uno de los elementos imprescindibles en el desarrollo de plantas transgénicas, es la disponibilidad de un sistema de selecciónque permita recuperar plantas potencialmente trans- formadas de una población de explantes (Chaparro, 2005).
Entre los diferentes tipos de agentes de selección actualmente disponibles, uno de los más ampliamente utilizados en arroz es la higromicina B. Este antibiótico de tipo aminoglicósido, obtenido a partir de Streptomyces hygroscopicus, tiene un amplio espectro de acción sobre procariotas y eucariotas, pues inhibe la síntesis de proteínas interfiriendo con la translocación de mRNAs y ribosomas (Borovinskaya et al ., 2008). Aunque en los cereales se han probado diferentes agentes de selección como kanamicina y fosfinotricina (Wakasa et al ., 2009), se ha encontrado que la higromicina B es uno de los más efectivos. Bajas concentraciones del antibiótico son capaces de eliminar totalmente células o explantes en condiciones in vitro; mientras que los cereales en general parecen ser altamente sensibles a los efectos tóxicos de la higromicina B, existe un consenso relativo en cuanto a la tolerancia parcial a la kanamicina, lo que la hace menos útil como agente de selección (Dekeyser et al., 1989; Zhuo et al ., 2009).
El objetivo del presente estudio fue el establecimiento de la concentración mínima inhibitoria de higromicina B en condiciones in vitro, sobre callos embriogénicos obtenidos a partir de tres genotipos colombianos de arroz. Este trabajo hace parte de un proceso más amplio de investigación, en el que se pretende lograr la generación de líneas transgénicas de variedades comerciales en Colombia.
Materiales y métodos
Material biológico
Como material biológico se emplearon semillas maduras de las siguientes variedades de arroz indica (Oryza sativa L.): FEDEARROZ 2000, FEDEARROZ 50 y FEDEARROZ 369, facilitadas por la Federación Nacional de Arroceros.
Protocolo de desinfección y obtención de callos embriogénicos
El sistema de cultivo de tejidos para regeneración utilizado fue el sugerido por Saharan et al . (2004), con algunas modificaciones puntuales. Se realizaron cambios en el proceso de esterilización de semillas, en el método de desecación de callos, en la temperatura de cultivo y en el tipo de recipiente usado durante la regeneración. Este protocolo fue escogido mediante ensayos previos llevados a cabo por el Grupo de Ingeniería Genética de Plantas de la Universidad Nacional de Colombia (datos no publicados), y está orientado a la obtención de callos embriogénicos derivados del escutelo de embriones maduros. Las semillas de las tres variedades mencionadas fueron descascaradas manualmente y desinfectadas con un lavado en etanol al 70% por 30 segundos, seguido por tres lavados con agua destilada estéril, un lavado con hipoclorito de sodio al 3% y Tween-20 (40 mL en 40 mL de hipoclorito), y varios lavados con agua destilada estéril para remover la espuma. Posteriormente, las semillas fueron secadas sobre papel absorbente estéril y sembradas en cajas de Petri plásticas con medio de inducción de callos (sales y vitaminas MS más 30 g/L de sacarosa, 0,5 g/L de prolina, 0,5 g/L de caseína hidrolizada, 2,5 mg/L de 2,4-D y 2,5 g/L de gelrite). El pH del medio fue ajustado a 5,8. Las semillas fueron dejadas a 28 °C y 70% de humedad relativa, en oscuridad total. A las tres semanas de cultivo, se determinó el porcentaje de formación de callos ([No. de callos formados / No. de semillas sembradas]*100%), se removieron los brotes y endospermos de los callos, y estos fueron colocados en cajas de Petri de vidrio con una hoja de papel Whatman No. 1 para desecarlos, durante 48 horas a 28 °C y 70% de humedad relativa, en oscuridad total.
Curva de sensibilidad a higromicina B
Los callos desecados fueron transferidos a cajas de Petri plásticas con medio de regeneración (sales y vitaminas MS más 30 g/L de sacarosa, 0,5 g/L de prolina, 0,5 g/L de caseína hidrolizada, 2,0 mg/L de kinetina, 0,5 mg/L de ANA y 6 g/L de gelrite). El pH del medio fue ajustado a 5,8. Para establecer la sensibilidad a la higromicina B, se aplicaron cuatro concentraciones de antibiótico al medio de regeneración (25 mg/L, 50 mg/L, 75 mg/L y 100 mg/L) más un control sin higromicina B. Por cada tratamiento se sembraron 80 callos de cada variedad (diez por caja). Los callos fueron colocados a 28 °C y 70% de humedad relativa, en fotoperiodo de 16 horas de luz y 8 horas de oscuridad. A las tres semanas se evaluó la sensibilidad estableciendo el peso seco (biomasa) de los diez callos de cada caja, el porcentaje de callos con brotes ([No. de callos con brotes / No. de callos sembrados]*100%) y el porcentaje de callos necróticos ([No. de callos necróticos / No. de callos sembrados]*100%). Para la evaluación de la necrosis se consideró que un callo era necrótico si más de la mitad del explante estaba oxidado (con una coloración parda o negra).
Resultados Y Discusión
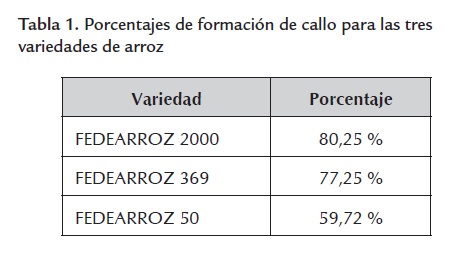
Formación de callo
Los resultados de formación de callo están reportados en la tabla 1 . Las diferencias entre las tres variedades, particularmente entre FEDEARROZ 50 y las otras dos, indican que la respuesta a las condiciones in vitro es dependiente del genotipo con el que se trabaja. Esta situación se encuentra documentada; actualmente existe un consenso amplio en cuanto a que las variedades de arroz de la subespecie indica son recalcitrantes al cultivo de tejidos y su respuesta depende fuertemen- te del genotipo con el que se trabaja (Kathuria et al ., 2007). Saharan et al . (2004) obtuvieron porcentajes de formación de callo de 60,5% para la variedad HKR-46 y de 83,5 para la variedad HKR-126. En este sentido, puede considerarse que los porcentajes obtenidos en este trabajo no son bajos. No obstante, es necesario considerar el ajuste futuro de las condiciones de formación de callo, particularmente para FEDEARROZ 50, con el fin de optimizar el sistema de obtención de callos embriogénicos aptos para transformación genética.
Sensibilidad de los callos a la higromicina B
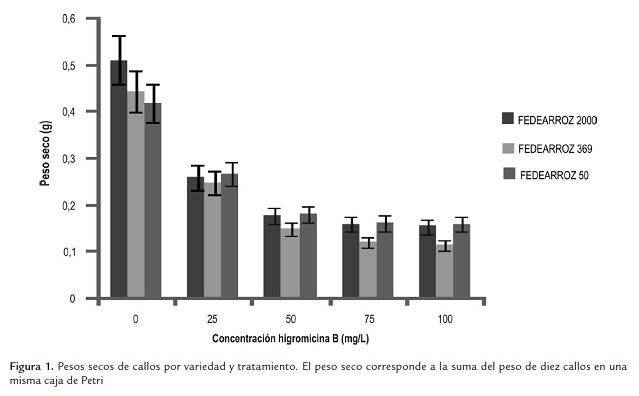
Para establecer la sensibilidad de los callos al antibiótico, se evaluaron diferentes variables como la biomasa de los callos, el número de callos con brotes y el número de brotes por callo. En las tres variedades se observa una disminución importante en la biomasa de los callos desde el tratamiento con 25 mg/L (figura 1). A partir de los 50 mg/L, las pérdidas en peso seco de los callos no son tan importantes, lo cual puede ser un indicio de que al usar esta concentración, se impide totalmente el crecimiento del callo en el medio de regeneración, con respecto a los callos que no fueron tratados con higromicina B. Debido a que la acción fundamental del antibiótico es la disrupción de la síntesis de proteínas por la alteración del funcionamiento de los ribosomas (Borovinskaya et al ., 2008), es de esperarse que uno de los efectos más evidentes sobre el desarrollo de los callos sea impedir su proliferación.
Por otra parte, queda claro que las variedades evaluadas no se sustraen a la tendencia generalizada de alta susceptibilidad de los cereales a la toxicidad de la higromicina B (Dekeyser et al ., 1989; Zhuo et al ., 2009).
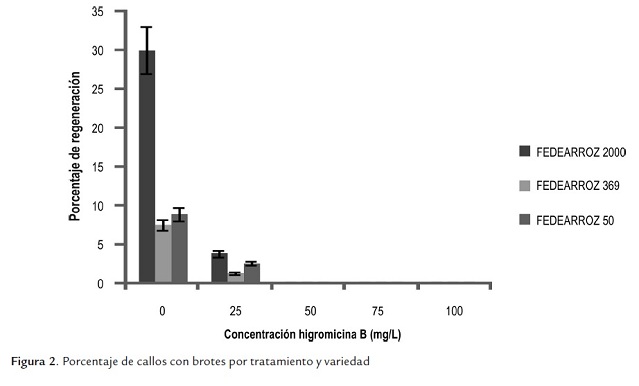
Los porcentajes de regeneración no fueron altos para ninguna de las tres variedades en el control con 0 mg/L de higromicina B (figura 2). La variedad con el porcentaje más alto fue FEDEARROZ 2000 (30,00%), seguida por FEDEARROZ 50 (8,89%) y FEDEARROZ 369 (7,50%). Estos datos son importantes por dos razones. En primer lugar, existe una notable diferencia entre los valores que aquí se reportan y los encontrados por Saharan et al . (2004), cuando utilizaron el mismo protocolo con las variedades indica recalcitrantes HKR- 46 y HKR-126 (63,70 y 82,00% respectivamente). En segundo lugar, la diferencia entre los porcentajes de regeneración de las tres variedades también es alta, especialmente si se compara FEDEARROZ 2000 con las otras dos. Ambas situaciones se explican por la fuerte dependencia genotípica de las variedades indica a las condiciones in vitro, lo cual dificulta el desarrollo de protocolos de regeneración eficientes para procesos de ingeniería genética; un protocolo que funciona muy bien con una variedad puede resultar poco eficiente con otra (Saharan et al ., 2004; Kathuria et al ., 2007). Debido a que los porcentajes de regeneración son bajos, el sistema evaluado, tal como se presenta, es de poca utilidad si se pretende desarrollar material transgénico a partir de estas tres variedades. Uno de los elementos críticos dentro de todo proceso de ingeniería genética de plantas es contar con un sistema de regeneración altamente eficiente; independientemente de que la inserción del casete de expresión en el genoma de la célula sea exitoso, si no es posible obtener un brote a partir de células transformadas, la transformación genética carecerá de valor práctico (Sharma et al ., 2005).
En cuanto a los porcentajes de regeneración para los tratamientos con higromicina B, se observa una fuerte caída a partir de los 25 mg/L, donde FEDEARROZ 2000 alcanza un valor de 3,75%, seguida por FEDEARROZ 50 con 2,50% y FEDEARROZ 369 con 1,25%. La fuerte disminución de la capacidad de regeneración de los callos es un nuevo indicador de la alta toxicidad que el antibiótico tiene sobre los explantes. No obstante, debido a que se presentan escapes, la concentración de selección efectiva para estas tres variedades es de 50 mg/L, donde ya no se encuentra ningún brote. En este sentido, los resultados concuerdan con la mayoría de trabajos de ingeniería genética de arroz, en los que generalmente se utiliza dicha concentración para lograr la selección sobre los explantes [para una revisión amplia de los reportes, véase Bajaj and Mohanty, (2005) y Kathuria et al ., (2007)].
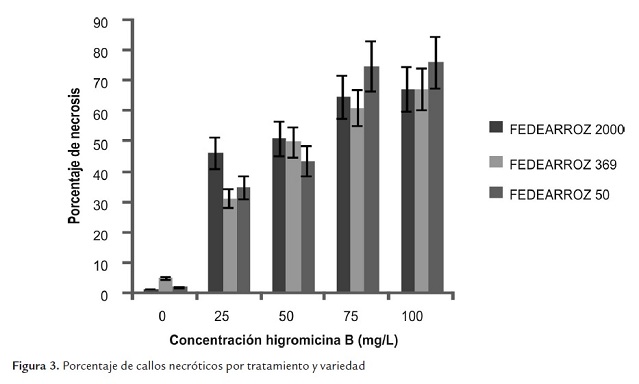
La oxidación y necrosis de los explantes es un fenómeno que se presenta en el cultivo de tejidos vegetales como respuesta a condiciones de estrés en el medio de cultivo o en el ambiente en el que se encuentra el explante (Pérez Molpe Balch et al ., 1999). En ese sentido, los valores bajos de callos necróticos en el tratamiento sin higromicina B para las tres variedades, son un resultado esperable (figura 3). A partir de los 25 mg/L de antibiótico, los porcentajes de necrosis se elevan considerablemente por efecto de la higromicina B. Estos resultados coinciden con lo observado en la disminución del peso seco y del porcentaje de regeneración, y en su conjunto demuestran la alta sensibilidad de los callos al agente de selección. Por otro lado, se resalta que, si bien los porcentajes de necrosis más altos se logran con la más alta concentración de antibiótico, estos no alcanzan a ser del 100%. Es posible que los callos resistan de alguna manera la acción tóxica de la higromicina B, puesto que no todos mueren; sin embargo, el hecho de que sean totalmente incapaces de regenerar a partir de los 50 mg/L de antibiótico en el medio, hace que esta concentración sea suficiente para establecer un sistema de selección adecuado.
Conclusiones
De manera general, los resultados obtenidos en este trabajo permiten concluir que la higromicina B es un agente de selección adecuado para el desarrollo de trabajos de ingeniería genética en variedades colombianas de arroz. Los datos obtenidos para todas las variables evaluadas durante la etapa de regeneración indican que con una concentración de 50mg/L de antibiótico, es posible evitar completamente la formación de brotes sobre los callos e impedir la aparición de escapes cuando se haga transformación genética.
Este trabajo fue financiado por la Federación Nacional de Arroceros (FEDEARROZ) - Fondo Nacional del Arroz y la Universidad Nacional de Colombia.
Referencias bibliográficas
1 Ashraf, M. 2010. Inducing drought tolerance in plants: Recent advances. Biotechnology Advances 28: 169-183. [ Links ]
2 Ashraf, M. and Akram, N. A. 2009. Improving salinity tolerance of plants through conventional breeding and genetic engineering: An analytical approach. Biotechnology Advances 27: 744-752. [ Links ]
3 Bajaj, S. and Mohanty, A. 2005. Recent advances in rice biotechnology-towards genetically superior transgenic rice. Plant Biotechnology Journal 3: 275-307. [ Links ]
4 Borovinskaya, M.A., Shoji, S., Fredrick, K. and Cate, J. H. D. 2008. Structural basis for hygromycin B inhibition of proteína biosynthesis. RNA 14: 1590-1599. [ Links ]
5 Chaparro, A. 2005. Elementos para entender la tecnología transgénica. En: Chaparro, A. Introducción a la ingeniería genética de plantas (editor). Bogotá: Unibiblos. pp. 11-22. [ Links ]
6 Dekeyser, R., Claes, B., Marichal, M., van Montagu, M. and Caplan, A. 1989. Evaluation of selectable markers for rice transformation. Plant Physiology 90: 217-233. [ Links ]
7 Diago, M. 2003. Compendio de Resultados de Investigación 2001- 2002. Colombia: Fedearroz-Fondo Nacional del Arroz. [ Links ]
8 Diago, M. 2005. Compendio de Resultados de Investigación 2003- 2005. Colombia: Fedearroz-Fondo Nacional del Arroz. [ Links ]
9 Espinal, C. F., Martínez, H. J. y Acevedo, X. 2005. La cadena del arroz en Colombia: una mirada global de su estructura y dinámica, 1991-2005. Documento de Trabajo Nº 89. Bogotá: Ministerio de Agricultura y Desarrollo Rural, Observatorio Agrocadenas Colombia, p. 47. Disponible en http://www.agrocadenas.gov.co. [ Links ]
10 FAO. 2008. Climate change and food security: a framework docuMent, Roma: Food and Agriculture Organization, p. 107. [ Links ]
11 Kathuria, H., Giri, J., Tyagi, H. and Tyagi, A. 2007. Advances in Transgenic Rice Biotechnology. Critical Reviews in Plant Sciences 26: 65-103. [ Links ]
12 Morgante, M. and Salamini, F. 2003. From plant genomics to breeding practice. Current Opinion in Plant Biology 14: 214-219. [ Links ]
13 Pérez Molpe Balch, E. M., Ramírez Malagón, R., Núñez Palenius, H. G. y Ochoa Alejo, N. 1999. Introducción al Cultivo de Tejidos Vegetales. México: Universidad Autónoma de Aguas Calientes, p. 170. [ Links ]
14 Saharan, V., Yadav, R. C., Yadav, N. R. and Chapagain, B. P. 2004. High frequency plant regeneration from dessicated calli of indica rice (Oryza sativa L.). African Journal of Biotechnology 3 (5): 256-259. [ Links ]
15 Sharma, K. K., Bhatnagar-Mathur, P. and Thorpe, T. A. 2005. Genetic transformation technology: status and problems. In Vitro Cellular and Developmental Biology-Plant 41: 102-112. [ Links ]
16 Wahid, A., Gelani, S., Ashraf, M. and Foolad, M. R. 2007. Heat tolerance in plants: An overview. Environmental and Experimental Botany 61: 199-223. [ Links ]
17 Wakasa, Y., Ozawa, K. and Takaiwa, F. 2009. Higher-level accumulation of foreign gene products in transgenic rice seeds by the callus-specific selection system. Journal of Bioscience and Bioengineering 107 (1): 78-83. [ Links ]
18 Zhuo, Q., Piao, J-H., Tian, Y., Xu, J. and Yang, X-G. 2009. Large-scale purification and acute toxicity of hygromycin B phosphotransferase. Biomedical and Environmental Sciences 22: 22-27. [ Links ]