Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Biotecnología
Print version ISSN 0123-3475
Rev. colomb. biotecnol vol.14 no.1 Bogotá Jan./June 2012
ARTÍCULO DE INVESTIGACIÓN
LSSP-PCR para la identificación de polimorfismos en el gen cry1Ben cepas nativas de Bacillus thuringiensis
LSSP-PCR to identify polymorphisms in the gene cry1B of Bacillus thuringiensis native strain
Martha Ilce Orozco Mera1, Jaime Bernal Villegas2, y Javier Hernández-Fernández3.
1 Centro de Biología Molecular, Gimnasio Campestre. Escuela de Bacteriología y Laboratorio Clínico, Facultad de Salud, Universidad del Valle, Calle 3a No. 36 B 05 Edificio 134. Espacio 206
2 Instituto de Genética, Pontificia Universidad Javeriana, Carrera 7 No. 40-62 Edificio 32, Bogotá, Colombia.
3 Universidad Jorge Tadeo Lozano, Facultad de Ciencias e Ingeniería. Grupo de investigación: GENBIMOL, Genética, Biología Molecular & Bioinformática. Carrera 4 No 22-61, Bogotá-Colombia. Autor para correspondencia: javier.hernandez@utadeo.edu.co
Recibido: abril 12 de 2011 Aprobado: junio 26 de 2012
Resumen
Se estandarizó la técnica LSSP-PCR (reacción en cadena de la polimerasa con un único oligonucleótido en condiciones de baja astringencia), para identificar polimorfismos del gen cry1B en aislamientos nativos de Bacillus thuringiensis (Bt) . Se evaluaron 164 aislamientos nativos colombianos identificándose el gen cry1Ba en 11 de estos aislamientos. Los 11 fragmentos amplificados, junto con el de la cepa de referencia Bt subsp. aizawai HD137, se analizaron por LSSP-PCR y los patrones electroforéticos obtenidos se compararon cualitativamente. Con los productos amplificados mediante el oligonucleótido directo se construyó un dendrograma utilizando UPGMA que mostró tres agrupamientos con similitud de 83, 79 y 68%. La agrupación con 68% de similaridad correspondió al aislamiento nativo BtGC120 que presentó el patrón de bandas más variable. Con el oligonucleótido reverso el aislamiento BtGC120 mostró una menor variabilidad (43%). La secuencia nucleotidica obtenida de este fragmento de 806 pares de bases mostró una identidad de 93% con la secuencia de los genes cry1Bc1 de Bt morrisoni y cry1Bb1 de la cepa BT-EG5847. Se predijo del marco de lectura +3 una proteína de 268 residuos aminoácidicos, con 88% de identidad con la proteína Cry1Bc. Esta secuencia reveló dos dominios, una endotoxina N implicada en la formación del poro y otra endotoxina M relacionada en el reconocimiento del receptor. La evaluación biológica del aislamiento BtGC120 sobre larvas de primer instar del insecto plaga Spodoptera frugiperda, mostró una CL50 de 1,896 ng de proteína total por cm2. Este estudio muestra que la LSSP-PCR es una técnica que permite identificar de una manera específica variaciones en las secuencias de los genes cry de Bt, con potencialidad de encontrar nuevos genes con novedosas actividades biológicas.
Palabras clave: Bacillus thuringiensis, genes cry1B, delta-endotoxinas, Spodoptera frugiperda, BTGC120.
Abstract
LSSP-PCR (low stringency specific primer-PCR), technique was standardized for polymorphisms in native isolates cry1B genes Bacillus thuringiensis (Bt) identify. 164 isolates were evaluated by identifying the gene colombian native cry1Ba, in 11 of these isolates. The 11 amplified fragments, along with the reference strain Bt subsp. aizawai HD137 were analyzed by LSSP-PCR and electrophoretic patterns obtained were compared qualitatively. With the amplified products with direct oligonucleotide was constructed using UPGMA dendrogram showed three clusters with similarity of 83, 79 and 68%. The group with 68% similarity corresponded to the isolation BtGC 120 native who introduced the variable pattern of bands. With the isolation BtGC 120 reverse oligonucleotide showed less variability (43%). The nucleotide sequence obtained from this fragment of 806 bp showed 93% identity with the sequence of the genes of Bt morrisoni cry1Bc1 and cry1Bb1 BT-strain EG5847. Predicted reading frame of 268 +3 a protein amino acid residues with 88% identity with the protein Cry1Bc. This sequence revealed two domains, an N endotoxin involved in the formation of the pore and other related M endotoxin in receptor recognition. The biological evaluation BtGC120 insulation on first instar larvae of Spodoptera frugiperda insect pest, showed an LC50 of 1.896 ng of total protein per cm2. This study shows that the LSSP-PCR is a technique that identifies a specific way variation in the sequences of cry genes of Bt, with the potential to find new genes with novel biological activities.
Keywords: Bacillus thuringiensis, cry1B genes, delta-endotoxins, Sodoptera frugiperda, BTGC120.
Introducción
Bacillus thuringiensis (Bt) es un bacilo Gram positivo esporoformador, el cual está ampliamente distribuido en el suelo (Schnepf et al. 1998). Produce una o más proteínas Cry en forma de inclusión cristalina paraesporal, las cuales son tóxicas sobre diferentes órdenes de insectos, entre estos: lepidóptera, díptera, coleóptera, himenóptera, homóptera, ortóptera y malófaga, y aún contra otros organismos como platelmintos, nemátodos, protozoos y ácaros (Hofte and Whiteley, 1989; Feitelson et al., 1992; Bravo et al., 1992, 1998; García-Robles et al., 2001; Xue et al., 2004). Aunque muchas proteínas Cry presentan similaridad en su estructura y función, su diversidad y potencial insecticida es altamente variable. A la fecha, se han identificado más de 500 toxinas Cry clasificadas dentro de 70 grupos según su secuencia aminoacídica (.http://www.biols.susx.ac.uk/home/Neil_Crickmore/Bt/toxins2.html 2012). De estos, el grupo cry1 presenta el más alto nivel de biodiversidad con 187 genes reportados, y a su vez, la mayor frecuencia en la naturaleza (Bravo et al., 1998; Porcar y Juárez-Pérez, 2003). Por más de 40 años se han identificado diferentes cepas de Bt con proteínas Cry novedosas, las cuales se han empleado como insecticidas biológicos y los genes codificantes en la generación de cultivos transgénicos autorresistentes al ataque de insectos, con reducción de los costos de producción y menores riesgos para la salud y el ambiente (Bravo et al., 1998; Porcar y Juárez-Pérez, 2003).
La reacción en cadena de la polimerasa (PCR) y otras herramientas moleculares junto con bioensayos, han permitido la caracterización de cepas de Bt portadoras de genes que codifican para las toxinas Cry y que poseen actividad insecticida. Se han adoptado algunas técnicas moleculares con base en PCR, las cuales presentan desventajas como dificultades técnicas, falta de especificidad y sensibilidad para la identificación de nuevos genes, etc. De hecho, siempre hay dificultad para una caracterización rápida y específica en grandes colecciones de cepas. Una clase de PCR, es la denominada PCR con un sólo oligonucleótido en baja astringencia (LSSP-PCR), la cual es útil para detectar cambios en la secuencia de DNA dentro de un multibandeo denominado, señal genética. Esta técnica ha tenido aplicaciones en la detección de enfermedades genéticas humanas y en la tipificación genética de agentes infecciosos (Pena et al., 1994; Villa et al. 1995; Barreto et al., 1996; Gomes et al., 1997; Vago et al., 1996, 2000; Ferreira et al., 2007; Márquez et al., 2007; Brito et al., 2008; Mejía et al., 2009; Baptista et al., 2009).
Se ha realizado búsqueda de nuevas cepas de Bt portadoras de nuevos genes cry, con el fin de descubrir proteínas con un nuevo espectro de acción y toxicidad sobre diferentes insectos plaga, que podrían ser útiles en el manejo de aparición de resistencia. Es importante identificar nuevas toxinas que logren ser utilizadas apropiadamente en combinación con otras toxinas de Bt para el control de diferentes insectos plaga y de esta manera retrasar la aparición de resistencia. Algunas cepas portadoras de los genes cry1Bse han sugerido como herramientas para un control efectivo y manejo de resistencia de muchas especies de insectos plaga lepidópteros importantes agronómicamente, como Spodoptera frugiperda, Plutella xylostella, Lymantria dispar, Diatrea saccharalis y Chilo suppressalis (Chambers et al. 1991, Fiuza et al. 1996, Tang et al. 1996, Peyronnet et al. 1997, Bohorova et al. 1997, Monnerat et al. 2006). La presencia del gen cry1Bjunto a otros genes cry, se ha relacionado con un aumento en la toxicidad debido a que se une a receptores diferentes del intestino medio de las larvas (Peyronnet et al. 1997, Luo et al. 1999). Igualmente, las cepas portadoras del gen cry1Bse han evaluado como una fuente de nuevas proteínas para ampliar el espectro de acción debido a su actividad dual contra órdenes de insectos Lepidóptera y Coleóptera (Bradley et al. 1995, Zhong et al. 2000, Rosas et al. 2004).
El objetivo de este estudio fue evaluar molecularmente mediante LSSP-PCR 164 aislamientos nativos colombianos con el fin de determinar la presencia de genes cry1Be identificar polimorfismos. Cepas que contengan genes cry1Bcon polimorfismos podrían producir nuevas proteínas insecticidas que permitirán ampliar el espectro de acción de los insecticidas basados en Bt o ampliar su uso para la producción de plantas transgénicas resistentes al ataque de insectos lepidópteros plaga.
Materiales y métodos
Cepas de B. thuringiensis
Se utilizaron 164 aislamientos de Bt aislados a partir de muestras de suelo del Centro y Caribe colombiano. Se empleó como control en la amplificación y ensayo biológico, la cepa de referencia Bt subsp. aizawai HD137, la cual fue donada por la unidad de biotecnología y control biológico de la Corporación para Investigaciones Biológicas (Medellín, Antioquia). Todas las cepas fueron cultivadas en medio Luria Bertani durante 7 días a 30°C y se verificó la presencia de esporas y cristales paraesporales mediante observación microscópica (Olympus E-600) con tinción safranina-verde de malaquita. Estas cepas se criopreservaron a -20°C en glicerol al 30% (v/v).
Extracción de DNA plasmídico y amplificación del gen cry1 mediante PCR
La extracción de DNA plasmídico se realizó utilizando el método de Kotchoni et al., (2003) y se visualizó en gel de agarosa al 1% (Sambrook et al., 2001). Las cepas nativas de Bt fueron caracterizadas molecularmente para determinar la presencia de genes cry1 mediante PCR utilizando oligonucleítidos generales diseñados previamente (Bravo et al., 1998). Los productos de amplificación de aproximadamente 550 pb se visualizaron mediante electroforesis en geles de agarosa al 1%.
Diseño de oligonucleótidos para el gen cry1B
Se diseñó un par de oligonucleótidos específicos para el gen cry1Bque amplificaran una región variable de aproximadamente 1000 pb considerando 11 secuencias nucleótidicas del gen cry1Bpublicadas en la base de datos de GenBank. Se realizó alineamiento de las secuencias con el programa ClustalW (EMBL-EBI; http://www.ebi.ac.uk/clustalw/) (Thompson et al., 1994) para determinar regiones variables representativas del gen. Con esta región y utilizando el programa Primer3 (HHMI;http://frodo.wi.mit.edu/cgi-bin/primer3/primer3_www.cgi) (Rozen & Skaletsky, 2000) se generaron varios oligonucleótidos candidatos, de los cuales se seleccionó un par que se analizó con el programa BLASTN para determinar su especificidad (NCBI; http://www.ncbi.nlm.nih.gov/gorf/gorf.html). Los oligonucleótidos fueron sintetizados por la casa comercial Invitrogen (USA).
Amplificación del gen cry1Bmediante PCR
Las reacciones de PCR para identificar genes cry1B, se realizaron con los oligonucleótidos específicos diseñados y bajo las siguientes condiciones: 0.5 pmol de oligonucleótidos, 0.2 mM de dNTPs, 1X Buffer PCR (20 mM de Tris-HCl, pH 8.4; 50 mM KCl), 1 U de Taq DNA polimerasa, 1.5 mM de MgCl2 y 50 ng de DNA. El programa utilizado fue: 95°C por 5 m, 35 ciclos de 94°C por 1 m, 52°C por 1 m, 72°C por 1 m y una extensión final a 72°C por 6 m. El producto de amplificación se analizó en gel de agarosa al 1% (Sambrook et al., 2001).
Amplificación del gen cry1Bmediante LSSP-PCR
La banda del producto del gen cry1B, se recuperó a partir de un gel de agarosa al 1% (p/v) y se disolvió en una proporción 10:1 con agua destilada desionizada estéril para obtener una dilución de DNA. 3 µL de esta mezcla se utilizó como DNA molde para la reacción de LSSP-PCR. La reacción se llevó a cabo en un volumen final de 25 µL, utilizando 5 pmol de un sólo oligonucleótido (directo y/o reverso), 0.2 mM de dNTPs, 1X PCR Buffer (20 mM de Tris-HCl, pH 8.4; 50 mM KCl), 4 U de Taq DNA polimerasa, 2.5 mM de MgCl2. El programa utilizado fue: 94°C por 5 m, 35 ciclos de 94°C por 1 m y 40°C por 1 m. El producto de amplificación se analizó en gel de poliacrilamida al 6% (p/v) y se tiñó con nitrato de plata (Sambrook et al., 2001).
Análisis de los geles
Los perfiles de las cepas se analizaron cualitativamente mediante la observación de los geles y utilizando el programa ImageJ (Rasband W.S., U.S. National Institute of Health, Bethesda, Maryland, U.S.A., http://rsb.info.nih.gov/ij/, 1997-2007). Este programa genera electroferogramas, en los cuales la altura del pico indica la presencia de la banda, y el ancho su intensidad. Con las bandas identificadas se construyó una matriz de presencia o ausencia. La matriz se analizó utilizando el programa NTSYS (Rohlf, 1999). Entre los perfiles de bandas se calculó el grado de similitud mediante el coeficiente de Dice (Dice, 1945) y a partir de la matriz de similaridad se construyó un dendograma mediante el algoritmo UPGMA (Unweighted Pair Group Method with Arithmatic Mean) (Sneath and Sokal, 1973). También se evaluó la consistencia de los agrupamientos representados en el dendograma, para lo cual se determinó el valor de correlación entre la matriz de los valores cofenéticos de los datos de similaridad y la misma matriz de similaridad.
Secuencia nucleótidica
Un fragmento amplificado del gen cry1Bde la cepa BtGC120 se purificó y secuenció, en un secuenciador automatizado (ABI Prism 310, APPLIED BIOSYSTEMS). La secuencia, se comparó con las publicadas en la base de datos de GenBank utilizando los programas BLASTN y BLASTX (Altschul et al., 1997). Posteriormente, se realizó un alineamiento con el fragmento homologo de las 11 secuencias del gen cry1Bpublicadas en GenBank, mediante el programa ClustalW (Thompson et al., 1994) (EMBL -EBI; http://www.ebi.ac.uk/clustalw/) y se construyó un dendograma con el programa Phylip, a partir de las distancias evolutivas de pares de bases utilizando el método de Neighbour-Joining (Saitou and Nei, 1987) y su confiabilidad se estimó con el método de bootstrap con 1000 repeticiones.
Bioensayos
La cepa de referencia Bt subsp. aizawai HD137 y el aislamiento nativo que presentó perfil de LSSP-PCR más variable, se incubaron en agar LB a 30°C por 7 días. A partir de este cultivo se preparó un extracto crudo de esporas y cristales en agua destilada desionizada estéril. La proteína total se cuantificó utilizando el método de Bradford (1976). Las concentraciones se ajustaron en un rango entre 0 y 1500 ng/cm2, empleando 6 dosis con una diferencia de 250 ng/cm2 cada una. Se utilizó un testigo absoluto sin tratamiento. Los ensayos biológicos se realizaron sobre larvas del primer instar de S. frugiperda, las cuales se habían colectado de un cultivo de maíz ubicado en el Municipio de El Espinal, Tolima, Colombia. La cría se mantuvo bajo condiciones de laboratorio a una temperatura de 25 +/- 3°C y 65 +/- 5% de humedad relativa. La aplicación de los tratamientos se realizó por el método de contaminación superficial propuesto por Aranda y colaboradores (1996), con un volumen de 400 µl de cada tratamiento sobre el haz y el envés de recortes de hojas de higuerilla (Ricinus communis) de 15 cm2, desinfectadas previamente con NaClO al 0.5% y tres enjuagues en agua destilada estéril por 5 minutos cada uno. Posteriormente, se ubicó una toalla de papel húmeda estéril en recipientes plásticos y sobre ésta la hoja de higuerilla con el tratamiento aplicado y una larva de primer instar de S. frugiperda proveniente de la cría del laboratorio.
Se evaluaron tres repeticiones del experimento cada uno con 25 larvas de primer instar. Estas se alimentaron durante 96 horas y se evalúo la mortalidad cada 24 horas. Los datos obtenidos en el bioensayo se analizaron para estimar la CL50 con un límite de confiabilidad del 95%, empleando el análisis estadístico de regresión logarítmico Probit del programa POLO-PC (Finney, 1971).
Resultados y discusión
Los 164 aislamientos nativos de bacilos esporulados se evaluaron de acuerdo a la capacidad para producir cristales paraesporales mediante la tinción diferencial safranina-verde de malaquita. Se observaron diferentes formas y cantidades de cristales paraesporales, la forma más común fue la bipiramidal pero se observaron cristales redondos, ovalados y triangulares. La mayoría de cepas presentaron menos de 10 cristales por campo óptico (65%), otras presentaron de 10 a 20 (27%) y solo unas pocas mostraron más de 20 cristales (8%). Es bien conocida la importancia de la caracterización de los cristales debido a su naturaleza proteica, la cual se ha relacionado con la actividad biopesticida potencial de las cepas (Schnepf et al. 1998; Hernández et al., 2010).
Se obtuvo DNA plasmídico de los 164 aislamientos nativos y se utilizó para la amplificación por PCR de un fragmento de genes cry1. Esta caracterización permitió identificar 70 aislamientos nativos positivos para la presencia de genes cry1, los cuales representan un 46% del total de los aislamientos (figura 1). Estos resultados fueron consistentes con estudios previos en los cuales se publicó para el gen cry1 una frecuencia con un rango entre 40 y 70% (Bravo et al., 1998; Uribe et al., 2003; Porcar et al., 2003; Hernández et al., 2010).
Diseño de oligonucleótidos y amplificación del gen cry1Bmediante PCR
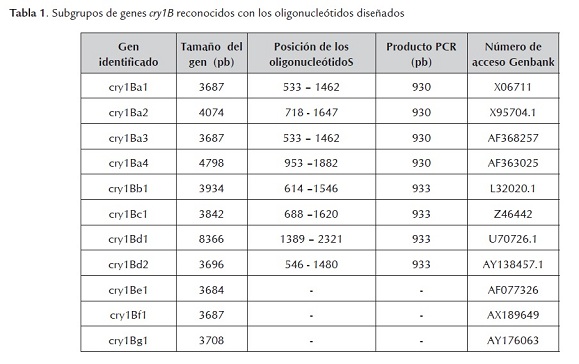
Los genes cry poseen regiones conservadas y variables que son reflejo de la estructura aminoácidica que ellos codifican, específicamente las toxinas Cry1 presentan 5 bloques conservados separados por secuencias de diferente longitud con alta variabilidad (Hofte y Whiteley, 1989; De Maagd et al., 2003; Hussain et al., 2010). Se realizaron alineamientos con el programa ClustalW (EMBL -EBI; http://www.ebi.ac.uk/clustalw/) (Thompson et al., 1994) de once secuencias de los genes cry1Bprovenientes de NCBI (tabla 1), y se seleccionó una región variable codificante ubicada entre los bloques conservados 1 y 3 de la secuencia aminoácidica, siendo está región útil para el diseño de oligonucleótidos y el subsiguiente análisis por LSSP-PCR. Además, esta región aminoácidica tiene importancia en la función de reconocimiento y unión a receptores localizados en el intestino medio de insectos susceptibles, lo cual es un determinante en la especificidad de la toxina (De Maagd et al. 1999; Hussain et al., 2010 ).
Cuando se analizaron los oligonucleótidos con el programa BLASTN (NCBI; http://www.ncbi.nlm.nih.gov/gorf/gorf.html), se determinó una mayor similaridad con los genes cry1Bde Bt que con otros microorganismos que podrían ser detectadas potencialmente. Los oligonucleótidos específicos se nombraron CRY1BF directo (5'-TGGTATATGCTCAAGCTGCAA-3') y CRY1BR reverso (5'-CACTACGATGCGTCCAAGAA-3').
Para obtener buenos perfiles en la LSSP-PCR se debe tener una concentración de DNA entre 50 y 150 ng aproximadamente (Pena et al. 1994, Wannia et al., 2003; López et al., 2006). Por esto, se hizo necesario optimizar la reacción de PCR para amplificar el fragmento del gen cry1Bde 930 pb, utilizando primero la variable temperatura de anillaje y luego se procedió a estandarizar las condiciones correspondientes a las concentraciones de MgCl2, oligonucleótidos y DNA plasmídico (resultado no presentado).
Se confirmó la especificidad de los oligonucleótidos diseñados, CRY1BF y CRY1BR, al obtener amplificaciones con la cepa B. thuringiensis subsp. aizawai, la cual contiene el gen cry1B, y no se presentó amplificación con otros genes cry1B, como los de las cepas B. thuringiensis subsp. kurstaki y B. thuringiensis subsp. israeliensis. Por lo tanto, estos oligonucleótidos permitieron la detección del gen cry1Ben forma específica.
Se evaluaron los 70 aislamientos nativos caracterizados previamente para el gen cry1, bajo condiciones estandarizadas para la reacción de PCR utilizando el par de oligonucleótidos diseñados que amplifican el fragmento del gen cry1B. Las amplificaciones resultaron en una banda única y de buena intensidad (figura 2). La reproducibilidad se evaluó realizando al menos tres veces la PCR para cada una de los aislamientos bajo las mismas condiciones, instrumentos y reactivos y siempre se obtuvo idénticos resultados.
Se amplificó un fragmento de 930 pb en 11 aislamientos nativos positivos para la presencia del gen cry1B, los aislamientos BtGC14, BtGC36, BtGC82, BtGC91, BtGC94, BtGC102, BtGC112, BtGC120, BtGC130, BtGC207 y BtGC240, los cuales representan un 16% de los 70 aislamientos que amplificaron previamente un fragmento del gen cry1 (figura 2). Estos resultados fueron similares a estudios en las colecciones de cepas de México, España, Reino Unido y Colombia, en los cuales el porcentaje de aislamientos portando el gen cry1Bes bajo (30, 13, 17 y 35% respectivamente) (Cerón et al. 1995; Perani et al. 2000; Martínez et al. 2005; Hernández et al., 2010).
LSSP-PCR de los fragmentos amplificados del gen cry1B
Desde principios de los 90's, se desarrollaron diferentes herramientas moleculares con la capacidad de detectar variaciones en la secuencia de DNA, obviamente la secuenciación es el método más sensible e informativo, pero para caracterizar grandes colecciones de microorganismos es importante generar metodologías rápidas y eficientes que puedan utilizarse rutinariamente. La técnica denominada PCR con un sólo oligonucleótido en baja astringencia (LSSP-PCR por sus siglas en inglés: low stringency single primer-PCR), fue propuesta por varios investigadores por su sensibilidad, especificidad y capacidad de detección de cambios en una secuencia de nucleótidos de longitud de por lo menos 1000 pb (Pena et al., 1994). Con la LSSP-PCR, se traslada la secuencia de DNA a un multibandeo denominado: señal genética. Cambios tan pequeños como mutaciones en una base alteran significativamente la señal produciendo un fenotipo que es diagnóstico de la alteración en particular (Pena et al., 1994; Villa et al., 1995; Barreto et al., 1996; Gomes et al., 1997; Vago et al., 2000; López et al., 2006). De esta manera es posible identificar cambios en la secuencia de genes específicos relacionados con funciones relevantes.
El gen cry1Bde Bt ha sido clasificado de acuerdo a su secuencia aminoácidica codificada en 7 subgrupos (desde cry1Ba1 hasta cry1Bg1) mostrando una variación grande (http://www.lifesci.sussex.ac.uk/home/Neil_Crickmore/Bt/, 2011). Por esta razón, en este estudio se analizaron por LSSP-PCR los productos de amplificación de los genes cry1Bde los 11 aislamientos nativos de Bt, con el fin de determinar la variación en el perfil electroforético que indicará la presencia de polimorfismos en la secuencia nucleótidica al compararlo con la cepa de referencia Bt subsp. aizawai.
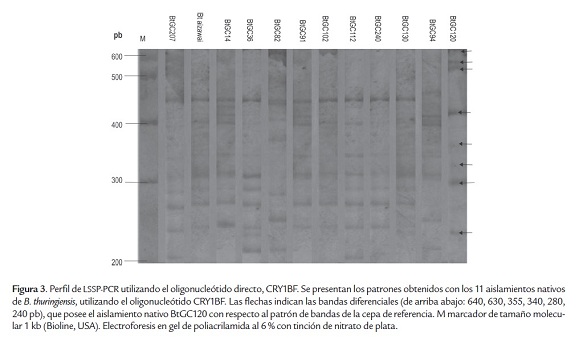
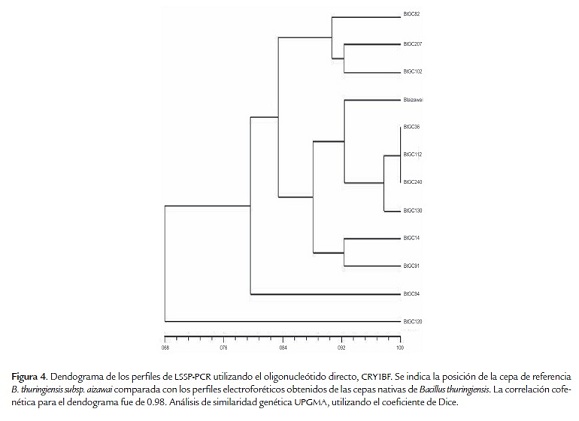
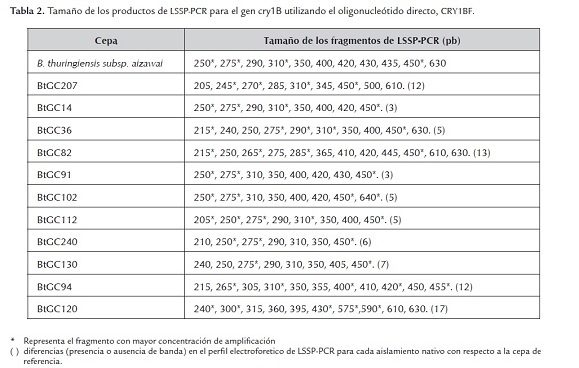
La LSSP-PCR con el oligonucleótido directo, CRY1BF presentó perfiles que variaron desde 7 hasta 12 bandas, con pesos entre 200 y 600 pb. La cepa de referencia presentó un perfil electroforético que consistió en 11 bandas (figura 3, tabla 2). Los aislamientos nativos presentaron perfiles similares pero con diferencias, algunos con ausencia o presencia de otras bandas y variación en la intensidad de las mismas. Se observó una gran variabilidad al no presentarse perfiles idénticos al de la cepa de referencia Bt subsp. aizawai (figura 3, tabla 2). El dendograma obtenido para los perfiles de LSSP-PCR con este análisis mostró la presencia de 10 agrupamientos, de los cuales únicamente uno comprende 3 aislamientos con un 99% de similaridad: BtGC36, BtGC112 y BtGC240 y los 9 restantes están formados por un solo aislamiento (figura 4). El valor de correlación cofenética global calculado fue 0.98, indicando un buen nivel de confiabilidad. La figura 4 muestra la presencia de 2 subgrupos, el primero se divide en dos ramas, una rama con similaridad de 83%, que corresponde a los aislamientos BtGC82, BtGC207, BtGC102, la cepa de referencia Bt subsp. aizawai, BtGC36, BtGC112, BtGC240, BtGC130, BtGC14, BtGC91 y la segunda rama con una similaridad de 79%, que corresponde al aislamiento BtGC94. Al segundo subgrupo sólo pertenece el aislamiento BtGC120, con una similaridad de 68% con respecto a los demás aislamientos. Esta baja similaridad del producto amplificado del aislamiento BtGC120 lo identificó como el fragmento más variable del gen cry1Bentre los 11 aislamientos evaluados (figura 3).
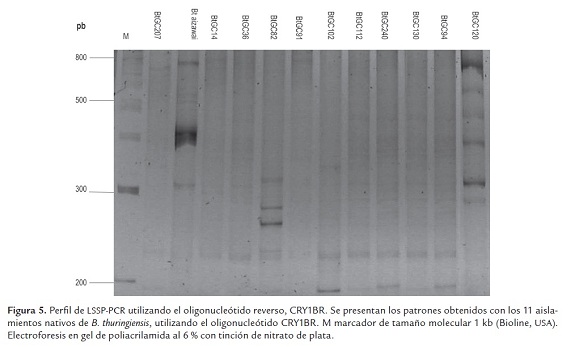
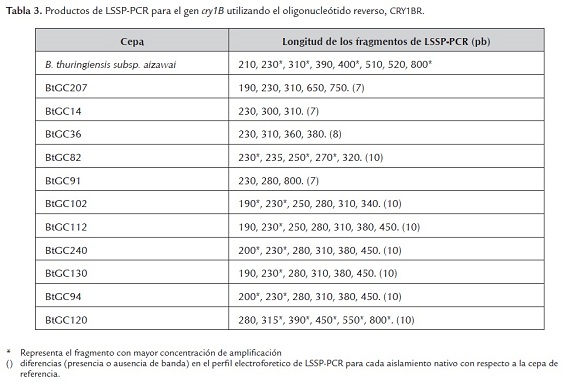
Los perfiles electroforéticos obtenidos cuando se amplificó por LSSP-PCR utilizando el oligonucleótido reverso, CRY1BR, presentaron fragmentos que variaban en tamaño desde 190 a 800 pb. El perfil electroforético de LSSP-PCR para la cepa Bt subsp. aizawai consistió en 8 bandas aproximadamente de 210, 230, 310, 390, 400, 510, 520 y 800 pb. Los perfiles generados para cada uno de los amplificados para los 11 aislamientos nativos de Bacillus thuringiensis presentaron bandas con menor intensidad y su número fue limitado (de 3 a 8) (figura 5 y tabla 3 ). Los aislamientos nativos BtGC94 y BtGC240 presentaron idéntico perfil a la cepa de referencia (figura 5, tabla 3).
El dendograma obtenido para los perfiles de LSSP-PCR con el oligonucleótido reverso reveló la misma tendencia que el obtenido con el oligonucleótido directo, puesto que se muestra la presencia de 10 agrupamientos, de los cuales 8 están formados cada uno por un sólo aislamiento y los dos restantes por dos aislamientos con un 99% de similaridad (BtGC130 con BtGC36 y BtGC240 con BtGC112) (figura 6). El valor de correlación cofenética global calculado fue de 0.97, indicando un buen nivel de confiabilidad. En la figura 6, se muestra la presencia de 2 subgrupos, el primer subgrupo se divide en dos ramas, la primera con una similaridad de 52%, que corresponde a los aislamientos BtGC94, BtGC207, BtGC102, BtGC14 y BtGC91 y la segunda con una similaridad de 43%, que corresponde al aislamiento BtGC120. De todos los aislamientos de este subgrupo, BtGC120 presentó la menor similaridad con respecto a los demás, lo cual significa que este produce el perfil más divergente del gen cry1B(figuras 4 y 6). El segundo subgrupo se divide en dos ramas, una primera rama con una similaridad de 64%, la cual corresponde a la cepa de referencia Bt subsp. aizawai y 4 aislamientos muy similares entre ellos (BtGC130, BtGC36, BtGC240 y BtGC112) y la segunda rama con una similaridad de 58%, la cual corresponde al aislamiento BtGC82.
Al utilizar la técnica LSSP-PCR, el oligonucleótido directo fue más informativo que el oligonucleótido reverso porque permitió distinguir los aislamientos nativos debido a que evidenció mayor número de bandas polimórficas (figuras 3 y 5), siendo este resultado consistente con estudios previos en los cuales se encontró mayor número de perfiles al utilizar uno de los dos oligonucleotidos (Pena et al., 1994; Vago et al., 2000; López et al., 2006).
Para seleccionar los aislamientos nativos de Bt que portaran variaciones en la secuencia, se tuvo como criterio la presencia de un menor porcentaje de similaridad en los dendrogramas deducidos de los perfiles de LSSP-PCR con cada uno de los dos oligonucleótidos evaluados. Los aislamientos nativos de Bacillus thuringiensis BtGC82, BtGC94 y BtGC120 presentaron la mayor variación entre sus secuencias amplificadas del gen cry1B(figuras 3 y 5). Entre estos aislamientos, el producto amplificado del gen cry1Bde BtGC120 presentó el menor porcentaje de similaridad. Además, los aislamientos nativos que presentaron el menor grado de variación entre sus secuencias, fueron: BtGC130, BtGC36, BtGC240 y BtGC112. Por este motivo se decidió analizar el fragmento amplificado por PCR-LSSP del aislamiento nativo de Bacillus thuringiensis BtGC120.
Secuencia nucleotídica
Se purificó el producto de amplificación del fragmento del gen cry1Bdel aislamiento BtGC120 y se secuenció en ambos sentidos en un equipo automatizado ABI Prism 310 (Applied Biosystems) utilizando los oligonucleótidos diseñados, CRY1BF y CRY1BR, según Sanger et al., (1977). La secuencia obtenida presentó un tamaño de 806 pb y 93% de identidad con los genes cry1Bc1 de Bt morrisoni (GenBank Z46442) y cry1Bb1 de la cepa BT-EG5847 (GenBank L32020). La similitud entre la secuencia de aminoácidos deducida del aislamiento BtGC120 y la proteína Cry1Bc (GenBank CAA86568.1) se evidenció entre el aminoácido 232 hasta el 464 región 5' terminal del gen. Se confirmó una alta similaridad de la secuencia del fragmento del gen cry1Bdel aislamiento BtGC120 con la región homologa del gen cry1Ba1, de la cepa de referencia Bt subsp. aizawai, encontrándose 148 cambios en la secuencia del aislamiento nativo BtGC120 representadas por 5 deleciones, 134 cambios de bases (70 transversiones y 64 transiciones) y 9 inserciones. Con estos cambios se predijo que posiblemente codifica para el extremo N- terminal de la secuencia de la proteína Cry1Bc, lo que representa aproximadamente el 65% del dominio II de esta secuencia y el 22% de la proteína completa. Esto muestra que la LSSP-PCR puede implementarse para discriminar variaciones en la secuencia de genes cry amplificados por PCR obtenidos de aislamientos nativos de Bt. Además, los cambios nucleotídicos podrían participar en modificaciones funcionales, como se ha reportado en estudios previos con la proteína Cry1A, en la cual han correlacionado los cambios nucleotídicos con un aumento de la toxicidad (Estela et al., 2004; Hussain et al., 2010). Estos cambios son muy frecuentes en los aislamientos de Bt, debido a su alta diversidad en los genes cry cuya variación se debe a la presencia en plásmidos conjugativos, movilización asociada a secuencias de inserción y transposones, además del frecuente intercambio de dominios y la coevolución con sus diferentes hospederos (Schnepf et al., 1998; de Maagd et al., 2001, 2003; Hernández et al., 2010; Hussain et al., 2010).
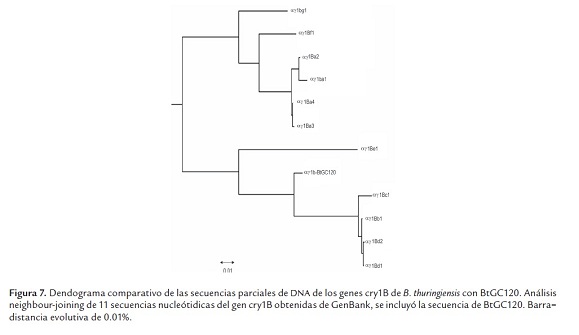
Por otro lado, la secuencia del fragmento del gen cry1Bdel aislamiento BtGC120 se comparó con el fragmento homologo en las 11 secuencias del gen cry1Breportadas en GenBank. Se realizó un alineamiento utilizando el programa ClustalW y se obtuvo un dendograma donde se muestran dos agrupamientos claramente separados: el primero formado por los genes cry1Bg1, cry1Bf1, cry1Ba2, cry1Ba1, cry1Ba4 y cry1Ba3 y el segundo formado por los genes cry1Be1, cry1Bc1, cry1Bb1, cry1Bd2, cry1Bd1 junto con la secuencia del aislamiento BtGC120 (figura 7). Estos datos son indicativos de que la secuencia del aislamiento BtGC120 presenta una relación más cercana a los genes del segundo agrupamiento con una similitud de 93%, reafirmando los resultados anteriores.
En la región amplificada del gen cry1Bdel aislamiento BtGC120 se presentan diferencias importantes respecto de los genes hasta el momento publicados. Las variaciones en la secuencia de nucleótidos y en la de aminoácidos deducidos hacen de este gen un buen candidato a nuevo gen cry, esto se debe validar clonando y secuenciando completamente el gen de este aislamiento nativo.
Bioensayos
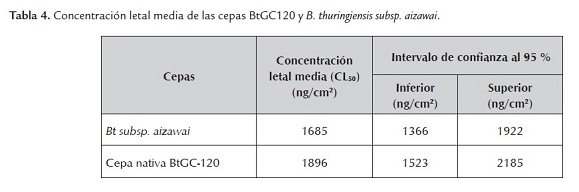
Se realizó un análisis de varianza con los datos de la mortalidad acumulada al quinto día de la cepa de referencia Bt subsp. aizawai HD137, en el cual se encontraron diferencias significativas entre las concentraciones de proteína empleadas. En la tabla 4, se presentan los resultados mediante el análisis Probit, mostrando que el valor de la concentración letal media del aislamiento nativo BtGC120 obtenido para larvas de primer instar de S. frugiperda fue superior al de la cepa de referencia Bt subsp. aizawai. Sin embargo, la prueba de comparación t-student determinó que estas cepas no presentaron diferencias significativas en cuanto a la variable respuesta CL50 (t=18, gl= 22, a=0.05). Esta respuesta sugiere que el aislamiento nativo es virulento y altamente promisorio para el control de larvas de S. frugiperda en campo.
Al comparar la CL50 de las cepas BtGC120 y Bt subsp. aizawai sobre larvas de primer instar de S. frugiperda, se infiere que las modificaciones de la proteína de BtGC120 como consecuencia de los cambios mutacionales posiblemente se encuentran en regiones de la proteína Cry que no producen alteraciones importantes en la interacción con el receptor de S frugiperda.
Este es el primer reporte de la utilización de la técnica LSSP-PCR para la identificación de polimorfismos dentro de los genes cry de Bt, metodología con la cual es posible, evaluar colecciones de esta bacteria para encontrar genes cry diferentes a los descritos en la literatura, y por ende, identificar proteínas con nuevas actividades, o mayor toxicidad sobre insectos plaga de importancia agronómica.
Agradecimientos
Los autores agradecen al doctor Sergio Orduz por el suministro de la cepa de referencia.
Bibliografía
1 Altschul, S., T. Madden, A. Schaffer, J. Zhang, Z. Zhang, W. Miller and D. Lipman. 1997. Gapped BLAST and PSI-BLAST: a new generation of protein database search programs. Nucleic Acids Res. 25: 3389-3402. [ Links ]
2 Aranda, E., J. Sánchez, M. Peferoen, L. Guereca, and A. Bravo. 1996. Interaction of Bacillus thuringiensis crystal protein with the midgut epithelial cells of Spodoptera frugiperda (Lepidoptera: Noctuidae). J. Invertebr. Pathol. 68: 203-212. [ Links ]
3 Baptista, C., A. Schubach, M. Madeira, C. Leal, M.Pires, F. Oliveira, F. Conceicao-Silva, C. Rosalino, M. Salqueiro and R. Pacheco. 2009. Leishmania (Viannia) braziliensis genotypes identified in lesions of patients with atypical or typical manifestations of tegumentary leishmaniasis: evaluation by two molecular markers. Exp. Parasitol. 121(4): 317-322. [ Links ]
4 Bohorova, N.; Cabrera M.; Abarca C.; Quintero R.; Maciel A.; Brito R.; Hoisington D. and Bravo A. 1997. Susceptibility of four tropical lepidopteran maize pest to Bacillus thuringiensis CryI type insecticidal toxins. J. Econ. Entomol. 90:412-415. [ Links ]
5 Bradford, M. 1976. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Anal. Biochem. 72,: 248-254. [ Links ]
6 Bradley, D.; Harkey M.; Kim M.; Biever K. and Bauer L. 1995. The insecticidal cry1Bcrystal protein of Bacillus thuringiensis ssp. thuringiensis has dual specificity to coleopteran and lepidopteran larvae. J. Invertebr. Pathol. 65(2): 162-173. [ Links ]
7 Bravo A., Hendrickx K., Jansens S. and Peferoen M. 1992. Immunocytochemical analysis of specific Binding of Bacillus thuringiensis Insecticidal Crystal Proteins to Lepidopteran and Coleopteran Midgut Membranes. J. Invertebr. Pathol. 60: 247-253. [ Links ]
8 Bravo, A.; Sarabia S.; López L.; Ontiveros H.; Abarca C.; Ortiz A.; Ortiz M.; Lina L.; Villalobos F.; Peña G.; Nuñez-Valdez M.; Soberon M. and Quintero R.1998. Characterization of cry genes in a Mexican Bacillus thuringiensis strain collection. Appl. Environ. Microbiol. 64(12): 4965-4972. [ Links ]
9 Brito C., M. Lima, O. Sarquis, M. Pires, C. Coutinho, R. Duarte, R. Pacheco. 2008. Genetic polymorphism in Trypanosoma cruzi I isolated from Brazilian Northeast triatomines revealed by low stringency single specific primer polymerase chain reaction. Parasitol. Res. 103(5): 1111-1117. [ Links ]
10 Cerón, J.; Ortiz A.; Guereca L. and Bravo A. 1995. Specific PCR reaction primers directed to identify cryI and cryIII genes with a Bacillus thuringiensis strain collection. Appl. Environm. Microbiol. 61(11): 3826-3831. [ Links ]
11 Chambers, J.; Jelen A.; Gilbert M.; Jany C.; Johnson T. and Gawron-Burke C. 1991. Isolation and characterization of a novel insecticidal crystal protein gene from Bacillus thuringiensis subsp. aizawai. J. Bacteriol. 173(13): 3966-3976. [ Links ]
12 Crickmore Neil. Bacillus thuringiensis toxin nomenclature. 2012. En: http://www.lifesci.sussex.ac.uk/Home/Neil_Crickmore/Bt/. (Consultado el 10 de mayo de 2012). [ Links ]
13 De Maagd, R., A. Bravo and N. Crickmore. 2001. How Bacillus thuringiensis has evolved specific toxins to colonize the insect world. Trends Genet. 17: 193-199. [ Links ]
14 De Maagd, R., A. Bravo, C. Berry, N. Crickmore and H. Schnepf. 2003. Structure, diversity, and evolution of protein toxins from spore forming entomopathogenic bacteria. Annu. Rev. Genet. 37: 409-433. [ Links ]
15 Dice, L. 1945. Measures of the amount of ecological association between species. Ecology. 26: 297-302. [ Links ]
16 Estela, A., B. Escriche and J. Ferré. 2004. Interaction of Bacillus thuringiensis toxins with larval midgut binding sites of Helicoperva armigera (Lepidoptera : Noctuidae). Appl. Environ. Microbiol. 70: 1378-1384. [ Links ]
17 Feitelson J., J. Payne and L. Kim. 1992. Bacillus thuringiensis: insects and beyond. Biotechnology. 10 (5): 271-275. [ Links ]
18 Ferreira G., F. Soares, S. Vasconcellos, E. Rodrogues, R. Werkhauser, M. de Brito and F. Abath. 2007. Discrimination of Leishmania braziliensis variants by kDNA sigNatures produced by LSSP-PCR. J. Parasitol. 93(3): 712-714. [ Links ]
19 Finney, D. 1971. Probit analysis. Cambridge University Press. Cambridge. [ Links ]
20 Fiuza, L.; Nielsen-Leroux C.; Goze E.; Frutos R. and Charles J. 1996. Binding of Bacillus thuringiensis Cry1 Toxins to the midgut Brush Border Membrane Vesicles of Chilo suppressalis (Lepidoptera: Pyralidae): evidence of shared binding sites. Appl. Environ. Microbiol. 62(5): 1544-1549. [ Links ]
21 Garcia - Robles, I., J. Sanchez, A. Gruppe, A. Martinez-Ramírez, C. Rausell, M. Real and A. Bravo. 2001. Mode of action of Bacillus thuringiensis PS86Q3 strain in hymenopteran forest pests. Ins. Biochem. Molec. Biol. 31: 849-856. [ Links ]
22 Hernández-Fernández J., L. Ramírez, N. Ramírez, L. S. Fuentes y J. Jiménez. 2010. Molecular and biological characterization of native Bacillus thuringiensis strains for controlling tomato leafminer (Tuta absoluta Meyrick) (Lepidoptera: Gelechiidae) in Colombia. World J Microbiol Biotechnol. 27, ( 3): 579-590, DOI: 10.1007/s11274-010-0493-5 [ Links ]
23 Hofte H. and H. Whiteley. 1989. Insecticidal crystal proteins of Bacillus thuringiensis. Microbiol. Rev. 53 (2): 242-255. [ Links ]
24 Hussain Syed-Rehan A., Flórez Álvaro M., Dean Donald H., Alzate Óscar. 2010. Preferential Protection of Domains II and III of Bacillus thuringiensis Cry1Aa Toxin by Brush Border Membrane Vesicles. Rev. Colomb. Biotecnol. 12 (2): 14-26. [ Links ]
25 Kotchoni, S.; Gachomo E.; Betiku E. and Shonukan O. 2003. A home made kit for plasmid DNA mini-preparation. Afric. J. of biotechnol. 2(4): 88-90. [ Links ]
26 López Pazos Silvio, Javier Hernández Fernández, Jaime Bernal Villegas. 2006. Identificación y secuenciación parcial de un nuevo gen cry1ab en aislamientos nativos de Bacillus thuringiensis por LSSP-PCR. El Astrolabio, Revista de Investigación y Ciencia, 5( 2): 14-21. [ Links ]
27 Luo, K.; Banks D. and Adang M. 1999. Toxicity, binding, and permeability analyses of four Bacillus thuringiensis Cry1 delta-endotoxins using border membrane vesicles of Spodoptera exigua and Spodoptera frugiperda. Appl. Environ. Microbiol. 65(2): 457-464. [ Links ]
28 Márquez D., L. Ramírez, J. Moreno, A. Pedrosa and E. Lages. 2007. Trypanosoma rangeli: RAPD-PCR and LSSP-PCR analyses of isolates from southeast Brazil and Colombia and their relation with KPI minicircles. Exp. Parasitol. 117(1): 35-42. [ Links ]
29 Martin, P. and Travers, R. 1989. Worldwide abundance and distribution of Bacillus thuringiensis isolates. AEM. 55: 2437-2442. [ Links ]
30 Martinez, C.; Ibarra J. and Caballero P. 2005. Association analysis between serotype, cry gene content, and toxicity to Helicoperva armigera larvae among Bacillus thuringiensis isolates native to Spain. J. Invertebr. Pathol. 90(2): 91-97. [ Links ]
31 Mejía, A., S. Arboleda, I. Rodríguez, C. Cura, A. Salazar, J. del Mazo, O. Triana and A. Schijman. 2009. Geographical clustering of Trypanosoma cruzi I groups from Colombia revealed by low stringency single specific primer PCR of the intergenic regions of spliced leader genes. Parasitol. Res. 104(2): 399-410. [ Links ]
32 Monnerat, R.; Martins E.; Quiroz P.; Ordúz S.; Jaramillo G.; Benintende G.; Cozzi J.; Real M.; Martinez-Ramírez A.; Rausell C.; Cerón J.; Ibarra J.; Del Rincón-Castro M.; Espinoza A.; Meza-Basso L.; Cabrera L.; Sánchez J.; Soberon M. and Bravo A.. 2006. Genetic variability of Spodoptera frugiperda Smith (Lepidoptera: Noctuidae) populations from Latin America is associated with variations in susceptibility to Bacillus thuringiensis Cry toxins. Appl. Environ. Microbiol. 72(11): 7029-7035. [ Links ]
33 Pena, S.; G. Barreto; A. Vago; L. De Marco; F. Reinach; E. Días Neto and A. Simpson. 1994. Sequence-specific "gene sigNatures" can be obtained by PCR with single specific primers at low stringency. Proc. Natl. Acad. Sci. USA. 91: 1946-1949. [ Links ]
34 Perani, M.; Bishop A. and Vaid A. 1998. Prevalence of ß-exotoxin, diarrhoeal toxin and specific delta-endotoxin in natural isolates of Bacillus thuringiensis. FEMS Microbiol. Lett. 160(1):55-60. [ Links ]
35 Peyronnet, O.; Vachon V.; Brousseau R.; Baines D.; Schwartz J. and Laprade R. 1997. Effect of Bacillus thuringiensis toxins on the membrane potential of lepidopteran insect midgut cells. Appl. Environ. Microbiol. 63(5): 1679-1684. [ Links ]
36 Porcar, M. and Juárez-Pérez V. 2003. PCR-based identification of Bacillus thuringiensis pesticidal crystal genes. FEMS Microbiol. Rev. 26(5):419-32. [ Links ]
37 Rasband, W. ImageJ 1,29x. National Institute of Health USA. (Consultado 2007 enero). Disponible en: http://rsb.info.nih.gov/ij/. [ Links ]
38 Rohlf, F. 2000. NTSYS-pc: numerical taxonomy and multivariate analysis system, version 2.1. Exeter Software: Setauket, N.Y. [ Links ]
39 Rosas-Garcia, N.; Pereyra B.; Arevalo K.; Galn-Wong L. and Morales L. 2004. Novel toxicity of native and HD Bacillus thuringiensis strains against to the sugarcane borer Diatrea saccharalis. Biocontrol. 49(4): 455-465. [ Links ]
40 Rozen, S. and Skaletsky H. 2000. Primer3 on the WWW for general users and for biologist programmers. In: Krawetz S., Misener S. (eds) Bioinformatics Methods and Protocols: Methods in Molecular Biology. Humana Press, Totowa, NJ, pp. 365-386. [ Links ]
41 Saitou, N. and M. Nei. 1987. The neighbor-joining method: a new method for reconstructing phylogenetic trees. Mol. Biol. Evol. 4: 406-425. [ Links ]
42 Sambrook, J.; Russell, D. and Sambrook, J. 2001. Molecular Cloning: A Laboratory Manual. Tercera edición. Cold Spring Harbor Laboratory Press, N.Y. [ Links ]
43 Schnepf, E.; Crickmore, N.; Van Rie, J.; Lereclus, D.; Baum, J.; Feitelson, J.; Zeigler, D. and Dean, D. 1998. Bacillus thuringiensis and Its Pesticidal Crystal Proteins. Microbiol. Mol. Biol. Rev. 62: 775-806. [ Links ]
44 Sneath, P. and R. Sokal. 1973. Numerical taxonomy. Nature. 193: 853-860. [ Links ]
45 Tang, J.; Shelton A.; Van Rie J.; De Roeck S.; Moar W.; Roush R. and Peferoen M. 1996. Toxicity of Bacillus thuringiensis spore and crystal protein to resistant diamondback moth (Plutella xylostella). Appl. Environ. Microbiol. 62(2): 564-569. [ Links ]
46 Thompson, J., D. Higgins and T. Gibson. 1994. CLUSTAL W: Improving the sensitivity of progressive multiple sequence alignment through sequence weighting, position-specific gap penalties and weight matrix choice. Nucleic Acids Res. 22: 4673-4680. [ Links ]
47 Uribe, D. 2004. Ecología y distribución de Bacillus thuringiensis. Pp. 101-122 Bacillus thuringiensis en el control biológico. Bravo, A. y Cerón, J. (eds). Universidad Nacional de Colombia. Bogotá, Colombia. [ Links ]
48 Uribe, D.; Martínez W. and Cerón J. 2003. Distribution and diversity of cry genes in native strains of Bacillus thuringiensis obtained from different ecosystems from Colombia. J. Invertebr. Pathol. 82(2): 119-127. [ Links ]
49 Vago, A., L. Andrade, A. Leite, D. d'Avila Reis, A. Macedo, S. Adad, S. Tostes Jr., M. Moreira, G. Filho and S. Pena. 2000. Genetic Characterization of Trypanosoma cruzi Directly from Tissues of Patients with Chronic Chagas Disease. Differential Distribution of Genetic Types into Diverse Organs. American Journal of Pathology. 156(5): 1805-1809. [ Links ]
51 Wania S. Carvalho; Silvana Spindola de Miranda; Kátia M. Costa; José G.V.C. Araújo; Claudio J. Augusto;João B. Pesquero; Jorge L. Pesquero; Maria A. Gomes. 2003. Low-Stringency Single-Specific-Primer PCR as a Tool for Detection of Mutations in the rpoB Gene of Rifampin-Resistant Mycobacterium tuberculosis. Journal of Clinical Microbiology, 41 ( 7): 3384-3386,. [ Links ]
52 Xu Z.; B. Yao; M. Sun and Z. Yu. 2004. Protection of mice infected with Plasmodium berghei by Bacillus thuringiensis crystal proteins. Parasitol. Res. 92: 53-57. [ Links ]
53 Zhong, C.; Ellar D.; Bishop A.; Johnson C.; Lin S. and Hart E. 2000. Characterization of a Bacillus thuringiensis delta-endotoxin which is toxic to insects in three orders. J. Invertebr. Pathol. 76:131-139. [ Links ]