Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Biotecnología
Print version ISSN 0123-3475
Rev. colomb. biotecnol vol.14 no.2 Bogotá jul./Dec. 2012
ARTÍCULO DE INVESTIGACIÓN
Identificación de bacterias productoras de Polihidroxialcanoatos (PHAs) en suelos contaminados con desechos de fique
Identification of polyhydroxyalkanoate-producing bacteria in soils contaminated with fique wastes
Silvia Alexandra Sánchez Moreno1 , Mauricio Alejandro Marín Montoya2 , Amanda Lucía Mora Martínez3 , María del Socorro Yepes Pérez4 .
1 Bacterióloga, Magíster en Biotecnología, Laboratorio de Venenos Naturales, Universidad Nacional de Colombia sede Medellín. silvie07@gmail.com
2 Ingeniero Agronómo, Ph.D. en Fitopatología, Docente Facultad de Ciencias, Laboratorio de Biología Celular y Molecular, Universidad Nacional de Colombia Sede Medellín. mamarinm@unal.edu.co
3 Química, D.Sc. en Química, Docente Facultad de Ciencias, Laboratorio de Procesos Ambientales, Universidad Nacional de Colombia Sede Medellín. almora@unal.edu.co
4 Química, M.Sc. en Química, Docente Facultad de Ciencias, Laboratorio de Venenos Naturales, Universidad Nacional de Colombia Sede Medellín. msyepes@unal.edu.co
Recibido: septiembre 24 de 2012 Aprobado: noviembre 29 de 2012
Resumen
Los Polihidroxialcanoatos (PHAs) son biopolímeros con características similares a los plásticos sintéticos, pero rápidamente biodegradables dado su origen microbiano. En esta investigación se aislaron 248 colonias bacteriales de suelos contaminados con residuos del beneficio de fique en Guarne (Antioquia), evaluándose su capacidad como productoras de PHAs. Se realizaron tinciones con rojo y azul de Nilo y detección por PCR del gen PhaC. Las bacterias positivas a dichas pruebas, fueron identificadas utilizando análisis filogenético de secuencias de 16S del ADNr y pruebas bioquímicas. Finalmente, se evaluó, mediante cromatografía de gases con detector selectivo de masas GC-MS/SIM, la naturaleza química del biopolímero, a partir de la biomasa generada en un ensayo de fermentación en cultivo sumergido, con medio mínimo de sales suplementado con glucosa como fuente de carbono. Cuatro cepas de los morfotipos bacteriales encontrados, presentaron potencial para producir PHAs, de los cuales dos fueron identificados como miembros de la especie Bacillus megaterium, uno como B. mycoides y el otro como Gordonia sp. El gen PhaC se detectó en los dos aislamientos de B. megaterium. El análisis cromatográfico permitió detectar al Polihidroxibutirato (PHB) como el principal componente de los PHAs presentes en B. megaterium, cuantificándose entre 63.8 mg/g y 95.3 mg/g de PHB en los ensayos de fermentación. Las bacterias aisladas tienen potencial en la producción de PHAs a partir de residuos agroindustriales, incluyendo el jugo de fique, lo que contribuiría a la reducción de su condición contaminante.
Palabras clave: ADNr 16S, Bacillus, biopolímeros, Furcraea bedinghausii, PhaC.
Abstract
Polyhydroxyalkanoates (PHAs) are biodegradable biopolymers of bacterial origin with properties similar to conventional plastics. In this work, bacteria were isolated from soils contaminated with fique wastes in the municipality of Guarne (Antioquia) and their ability to produce PHAs was evaluated. Bacteria were stained with Nile blue and Nile red and the PhaC gene detected by PCR. Positive bacteria were identified by phylogenetic analysis of 16S rDNA and biochemical tests. The chemical nature of the biopolimers was determined by gas chromatography GC-MS/SIM using biomass produced in a submerged fermentation in a minimal media supplemented with glucose as sole carbon source. Four bacterial morphotypes identified as Bacillus megaterium (2), B. mycoides (1) and Gordonia sp. (1) showed potential to produce PHAs. However, the PhaC gene was detected in B. megaterium. Chromatographic analysis showed polyhydroxybutirate (PHB) to be the main component in the PHAs produced by B. megaterium with levels between 63.8 mg/g and 95.3 mg/g in the fermentation test. The isolated bacteria have potential to produce PHAs, generating added value to the Agro-industrial waste, as in the fique industry, and reducing its contamination impact.
Key words: 16S DNAr, Bacillus, biopolymer, Furcraea bedinghausii, PhaC.
Introducción
Los polihidroxialcanoatos (PHAs) son bioplásticos termoestables, sintetizados por bacterias que los acumulan como reservas de carbono y energía, en forma de gránulos intra-citoplasmáticos. Dependiendo de la especie bacteriana, del sustrato utilizado y de la fase de crecimiento microbiana, éstos pueden llegar a representar entre el 45% y el 85% del peso seco celular (Reddy et al., 2003). Los PHAs se clasifican de acuerdo a la composición de sus monómeros en tres clases: (a) de cadena corta (PHASCL), conformados por monómeros de 3 a 5 carbonos, como el Poli-3-hidroxivalerato ([P(3HV)] y el Poli-3-hidroxibutirato [P(3HB)] o poli-hidroxibutirato (PHB); (b) de cadena mediana (PHAMCL), constituidos por monómeros de 6 a 14 carbonos, como el copolímero poli-3(HB-co-HV) y, (c) de cadena mixta (PHAMCM), que combinan los dos anteriores y que por tanto, constan de monómeros entre 3 y 14 carbonos, como es el caso del Poli (3HB-co-3HV-co-3HHx) (Sttube y Tian, 2003). Desde el punto de vista industrial, se destacan el PHB y el copolímero Poli 3(HB-co-HV) (Dionisi et al., 2004).
Los PHAs son sustitutos atractivos de los poliésteres de origen petroquímico, dado que tienen propiedades similares a las de varios termoplásticos y elastómeros, con la ventaja de ser totalmente biodegradables (Sttube y Tian, 2003; Dionisi et al., 2004). En la naturaleza, los microorganismos son capaces de degradarlos hasta CO2 y agua, en condiciones aerobias, y hasta metano, en condiciones anaerobias, por acción de las enzimas PHA despolimerasas y PHA hidrolasas (Barbosa et al., 2005). Otra ventaja de estos biopolímeros está asociada con los sustratos utilizados para su síntesis, mientras para la producción de plásticos sintéticos se requiere materia prima de origen petroquímico, los PHAs se pueden obtener a partir de diferentes desechos agroindustriales, que constituyen materiales orgánicos de bajo costo (Vishnuvardhan et al., 2009; Thirumala et al. 2010).
Uno de los PHAs más empleados en el campo médico es el PHB, gracias a su biocompatibilidad, siendo la base para la elaboración de filamento de suturas, vehículo para fármacos y constructos para el crecimiento celular, entre otros (Chen y Wu, 2005). Además, se ha utilizado en el campo industrial para la producción de botellas, películas protectoras, fibras para empaques de alimentos y cubiertas agrícolas (López et al. 2012).
Hasta el momento, se conocen aproximadamente 300 especies bacterianas productoras de PHAs, incluyendo diversas bacterias Gram negativas y Gram positivas, pero solo unas pocas se utilizan industrialmente, dadas sus altas eficiencias en la transformación de los sustratos y concentración final del biopolímero en sus células (Barbosa et al., 2005; López et al. 2012). Entre las bacterias Gram negativas se destacan Cupriavidus necator (antes Alcaligenes eutrophus), Alcaligenes latus, Pseudomonas putida, P. oleovorans y Azotobacter vinelandii; además, una cepa de Escherichia coli recombinante que contiene el operón de la biosíntesis de PHAs de C. necator (Barbosa et al., 2005). Con respecto a las bacterias Gram positivas, se han reportado como productoras de PHAs varias especies del género Bacillus, incluyendo B. megaterium y B. cereus (Yilmaz et al., 2005; Reddy et al., 2009), así como también actinomycetes del género Streptomyces (Franco-Correa et al., 2009).
La organización de los genes involucrados en la biosíntesis de PHAs varía dependiendo de los microorganismos, hasta ahora se han detectado cuatro arreglos genéticos principales (Solaiman et al. 2000; McCool y Cannon, 2001). En el primer sistema, denominado tipo I y tipificado por el operón pha de C. necator, se incluyen el gen PHA sintasa phaC, y los genes phaA y phaB, que se presentan adjuntos y codifican para β-cetotiolasa y acetoacetil-CoA reductasa, dos enzimas relacionadas con la biosíntesis de PHAs de cadena corta. La segunda clase (tipo II), consiste de dos genes sintasa (phaC1 y phaC2) separados por el gen que codifica para la despolimerización de PHAs (phaZ), este sistema es comúnmente encontrado en bacterias del género Pseudomonas. El sistema genético tipo III, se encuentra en Chromatium vinosum, Synechocystis sp. y Thiocystis violaceae; en estos microorganismos la enzima sintasa consta de dos subunidades de polipéptidos codificadas por los genes phaE y phaC. Los genes phaA y phaB también se localizan en este operón, pero son frecuentemente transcritos en forma divergente de los genes phaE y phaC. Finalmente, el tipo IV se presenta en Bacillus sp. y se caracteriza porque la PHA sintasa esta conformada por dos subunidades, PhaC y PhaR, codificadas por el operón phaRBC (McCool y Cannon, 2001).
La fuente de carbono empleada en el cultivo de los diferentes microorganismos para la producción de PHAs, afecta el contenido, composición y propiedades del polímero y constituye un factor importante en el costo de su producción (Reddy et al., 2003). Existen diversos sustratos que por su naturaleza de desechos, podrían incidir favorablemente en los costos de producción de los biopolímeros. Entre los sustratos económicos más usados se encuentran: la melaza de caña, la cual requiere una fermentación acidogénica previa a la producción de PHAs, residuos de la industria del arroz y los lactosueros (Almeida et al., 2004). Otras fuentes de carbono frecuentes son los ácidos grasos volátiles (acético, butírico y propiónico), obtenidos de la degradación de algunos desechos orgánicos lipídicos, pero que deben utilizarse en bajas concentraciones, debido a su toxicidad celular (Yan et al., 2003).
Para países como Colombia, donde la actividad agrícola tiene una participación importante en la economía nacional y al mismo tiempo genera grandes cantidades de desechos sólidos y líquidos, algunos con características recalcitrantes y contaminantes, la exploración de alternativas para realizar un manejo ambientalmente-sostenible de dichos residuos agroindustriales es una prioridad.
En este sentido, la cadena productiva del fique es una de las actividades agroindustriales más tradicionales en Colombia. En departamentos como Cauca, Nariño, Antioquia y Santander, los cultivos superan las 21000 ha y generan cerca de 13000 empleos rurales directos y 60000 empleos en el eslabón artesanal, destinado a la producción de hilos, tejidos, empaques, biomantos, entre otros. Del bagazo también se puede obtener papel, fibra reforzada y aglomerados para diferentes usos, y del jugo se podrían extraer saponinas (hecogenina y tigogenina) de utilidad en las industrias farmacéutica y cosmética (Ministerio de Agricultura y Desarrollo Rural, 2008). Sin embargo, en la gran mayoría de explotaciones dichos materiales no son aprovechados y por el contrario, establecen fuentes importantes de contaminación de aguas y suelos.
Ya que la utilización de procesos de biorremediación microbiana se constituye en una alternativa biológica para el manejo de residuos e incluso, para generar valor agregado en la agroindustria del fique, en este trabajo se aislaron e identificaron, mediante técnicas moleculares y bioquímicas, bacterias productoras de PHAs presentes en suelos contaminados con desechos del proceso de beneficio de la fibra de fique (Furcraea bedinghausii) en el municipio de Guarne (Antioquia).
Materiales y métodos
Muestras
El sitio para el muestro de suelos, ubicado en la vereda El Salado, municipio de Guarne (Antioquia) (06°16′50"N y 75°26′37"O), fue seleccionado por corresponder a una zona de producción de fique en pequeñas parcelas, bajo arreglos mixtos con diversos cultivos de hortalizas y plantas medicinales. Se tomaron cinco muestras de suelos que incluyeron dos con bagazo de fique en fermentación, uno contaminado con jugo de fique, uno de suelo con fibra de fique incorporada y uno con bagazo superficial.
Aislamiento y detección de bacterias productoras de PHAs
Para el aislamiento microbiano se utilizó inicialmente la preparación de diluciones seriadas del suelo (Capuccino y Sherman, 2007), con siembra posterior en medio de sales minerales (MSM) pH 7.0, y glucosa como fuente de carbono. Para detectar las colonias potencialmente productoras de PHAs, se empleó rojo de Nilo al 0.1%, que permitió hacer la diferenciación a una longitud de onda de 340 nm (Spiekermann et al., 1999). Los cultivos se incubaron a una temperatura de 30°C durante tres días y se monitorearon cada 24 h bajo luz ultravioleta.
A los cultivos que dieron positiva la prueba del rojo de Nilo, se les realizó la tinción confirmatoria con azul de Nilo, siguiendo la metodología de Ostle y Holt (1982), para lo cual se utilizó un microscopio de fluorescencia (Axiolab-Zeiss, Alemania), a una longitud de onda de 450 nm y un aumento de 1000X. Las bacterias que presentaron fluorescencia rojo-naranja, indicativo de la presunta producción de PHAs, se purificaron en Agar Nutritivo y se sometieron al proceso de tinción de Gram (Capuccino y Sherman, 2007), para luego proceder a la confirmación mediante PCR, de la presencia del gen phaC.
Detección por PCR de phaC
La presencia del gen phaC se evaluó por PCR, utilizando diferentes juegos de cebadores dirigidos a los diversos arreglos genéticos registrados para la biosíntesis de PHAs (Tabla 1). El ADN de las bacterias se obtuvo por lisis térmica (Revelo et al. 2007). Las reacciones de PCR se realizaron en un volumen total de 25 µL e incluyeron: 0.1 µM de cada cebador (Tabla 1), 1 U de Taq ADN polimerasa (Fermentas, Lituania), 0.2 mM de cada dNTP, 1X de buffer de enzima, 2.5 mM MgCl2, 5% DMSO (v/v) y 3 μL del lisado bacteriano. El programa de amplificación consistió en una desnaturalización inicial a 94°C por 4 min, seguida de 35 ciclos a 94°C por 30 s, 60°C por 45 s, 72°C por 75 s y una extensión final a 72°C por 10 min.
Los productos de PCR se separaron en gel de agarosa al 1.5% en buffer TBE 1X, suplementado con 3 µL de bromuro de etidio [10 mg/mL]. La visualización de las bandas se realizó bajo luz ultravioleta, utilizando el sistema digital de análisis Bio Doc Analyze (Biometra, Alemania). Los amplicones del tamaño esperado fueron purificados mediante el Kit QIAquick PCR Purification (Qiagen, Alemania), para proceder a su secuenciación directa en ambas direcciones, utilizando los cebadores empleados en su amplificación, mediante el sistema Big Dye Terminator Cycle Sequencing Ready Reaction (PE Applied Biosystems, EEUU). Su corrido y separación se realizó en un secuenciador ABI Prism 3730xl (PE Applied Biosystems) de la compañía Macrogen (Corea del Sur). Se editaron las secuencias obtenidas con cada cebador y los consensos generados con el programa BioEdit 6.0.6 (Hall, 1999). Su identidad se evaluó por comparación con las bases de datos moleculares mediante BlastN (http://www.ncbi.nlm.nih.gov/BLAST/Blast.cgi).
Identificación taxonómica de las bacterias productoras de PHAs
Una vez detectadas las bacterias potencialmente productoras de PHAs, se procedió a determinar su identidad taxonómica mediante la amplificación por PCR y secuenciación de una porción de la subunidad pequeña del ADNr (16S), utilizando los cebadores PA y Pc5B (5’ AGA GTT TGA TCC TGG CTC AG 3’ y 5’ TAC CTT GTT ACG ACT T 3´) (Kuske et al., 1997). Las PCRs, así como la separación de los amplicones y su secuenciación, fueron similares a las descritas anteriormente.
Las secuencias obtenidas con cada cebador fueron editadas mediante BioEdit 6.0.6 (Hall 1999) y comparadas con GenBank mediante BlastN. Con base en dicha información, se obtuvieron secuencias de diferentes especies representando el rango de variación bacterial detectado en el estudio, así como también secuencias de grupos externos, realizándose un alineamiento mediante Clustal W (Larkin et al., 2007). La matriz generada fue utilizada para obtener un árbol filogenético basado en máxima parsimonia, utilizando la opción Heuristic search del programa PAUP 4.0b, con la orden tree-bisection reconnection (TBR) (Swofford, 1998). El soporte de la topología interna de los dendrogramas fue determinada por análisis de bootstrap con 1000 remuestreos (Felsenstein, 1985).
Los resultados taxonómicos, obtenidos mediante las pruebas moleculares, para las cepas seleccionadas como potenciales productoras de PHAs, se confirmaron con base en características fenotípicas, para lo cual se efectuaron diversas evaluaciones morfológicas y bioquímicas. Inicialmente se realizaron pruebas de tinción de Gram, seguidas de tinción de esporos con verde de malaquita y caracterización macroscópica de las colonias. Las bacterias que resultaron Gram positivas y esporuladas, se caracterizaron bioquímicamente mediante el sistema API 50CHB (Biomérieux, Francia). La bacteria que resultó Gram positiva, pleomórfica y no esporulada, se evaluó bioquímicamente a partir de una batería de diez pruebas que incluyó: TSI, LIA, RM, VP, PPA, SIM, Ureasa, movilidad, citrato y malonato. De forma adicional, a esta cepa se le realizaron pruebas de oxidasa, catalasa y coloración de Zielh-Neelsen (Capuccino y Sherman, 2007).
Caracterización química de PHAs
Para las bacterias en las que se detectó el gen PhaC, se procedió con la detección monomérica de los polihidroxialcanoatos (PHAs) mediante GC-MS. Los microorganismos se sometieron a fermentaciones en cultivo sumergido, utilizando erlenmeyers de 250 mL de capacidad, con 50 mL de MMS suplementado con glucosa como fuente de carbono. Se utilizó un inóculo microbiano al 10% (v/v). Para cada una de las bacterias seleccionadas, se prepararon dos erlenmeyers de reacción y un control negativo, sin inóculo. Las incubaciones se llevaron a cabo a temperatura controlada de 30°C y bajo agitación (150 rpm), durante 72 h. Trascurrido este tiempo, se procedió a centrifugar el caldo de fermentación y a separar la biomasa, que luego se liofilizó y se sometió a extracción con solventes, para recuperar el biopolímero.
El aislamiento y purificación del PHA, se realizó de acuerdo a la metodología propuesta por Moreno et al. (2006); ésta consistió en adicionar un (1) mL de hipoclorito de sodio comercial al 5% (p/v) y un (1) mL de cloroformo al 50% (v/v) por cada 0.02 gramos de biomasa liofilizada. La mezcla se agitó por 1 h a temperatura ambiente (28°C-29°C), para luego centrifugar a 10000 rpm, durante 10 min, y separar la fase orgánica. A partir de ésta, se precipitó el biopolímero, adicionando 1 mL de metanol y reposando la mezcla por 12 h a 4ºC. El precipitado se separó y se secó en estufa a 60°C, durante 24 h.
La determinación y cuantificación de los PHAs, se llevó a cabo mediante cromatografía de gases (modelo 6890 series plus, Agilent Technologies, EEUU) con detector selectivo de masas (Agilent Technologies), operado en el modo de monitoreo de ión(es) seleccionados (GC-MS/SIM, por su abreviatura en inglés). Las muestras se inyectaron en modo splitless (Viny= 1 µL) para su preparación se aplicó la norma ISO 5509, por la cual los PHAs fueron hidrolizados y sus productos, derivatizados a sus metilésteres con BF3/MeOH. Se utilizó PHB como material de referencia, ácido benzoico como estándar interno (ISDT) y una columna DB-WAX [60m x 0.25mm x 0.25 µm]. La selección del PHB se basó en estudios previos que identificaron que los gránulos de PHAs de B. megaterium contenían 97.7% de PHB, y mínimas proporciones de fosfolípidos (0.46%) y proteínas (0.47%) (Sttube y Tian, 2003).
Resultados y discusión
Aislamiento y detección de bacterias productoras de PHAs
En total se obtuvieron 248 colonias bacteriales, a partir de las diferentes muestras de suelos y diluciones seriadas realizadas. A pesar del alto número de aislamientos, fue posible agruparlos en siete morfotipos coloniales diferentes: F1) colonias sin borde definido traslúcidas, fuertemente adheridas al agar, F2) colonias con aspecto rizoide de color blanco, F3) colonias puntiformes traslúcidas, F4) colonias redondas mucosas de color crema brillante, F5) colonias puntiformes de color crema, F6) colonias redondas convexas de color blanco y F7) colonias redondas de color crema y opacas.
Es de anotar que el suelo corresponde a uno de los hábitats donde se han detectado mayor número de especies bacteriales productoras de PHAs (Barbosa et al; 2005); sin embargo, en este estudio se encontró una baja diversidad de microflora bacterial asociada a los suelos sometidos a desechos de fique. Esto puede sugerir un efecto selectivo de dichos residuos, dado que el jugo de fique contiene diferentes compuestos fenólicos, esteroides y saponinas, que resultan extremadamente tóxicos para un amplio espectro de macro y microorganismos (Peinado et al., 2006); así por ejemplo, en un bioensayo realizado con peces en el departamento de Nariño, se encontró una concentración letal media de los jugos de fique de 1 mg/L para alevinos de trucha arco iris y una concentración crítica 3 mg/L, que causó la muerte de todos los peces expuestos. Estas cantidades superaron la toxicidad del fungicida Mancozeb y el herbicida propanil (Martínez y Caicedo, 2002).
La condición de contaminante recalcitrante que presenta el jugo de fique, hace fundamental la búsqueda de alternativas ambientalmente sostenibles para su disposición final o su utilización en la generación de valor agregado para la cadena productiva del fique y su industria. La versatilidad metabólica bacteriana brinda alternativas para su tratamiento, siendo la producción de PHAs una excelente opción, dadas sus múltiples aplicaciones biotecnológicas.
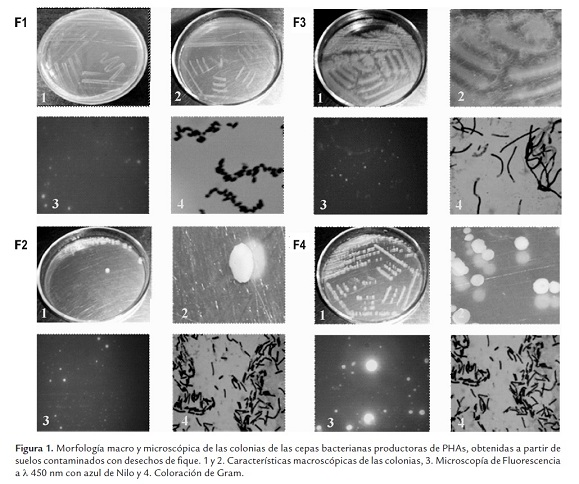
En este estudio se encontró que las cepas representando los morfotipos F1, F2, F3 y F4, dieron emisión de fluorescencia en las pruebas con el rojo de Nilo y por ende, se consideraron potencialmente productores de PHAs. Este resultado se confirmó por microscopía de fluorescencia a λ de 450 nm, empleando azul de Nilo para la tinción (Figura 1). Las cepas F1 y F2 procedían de suelo con bagazo en fermentación, mientras que F3 y F4 fueron obtenidas de suelo contaminado con jugo de fique.
Detección por PCR de phaC
Con el fin de superar los inconvenientes que pueden presentarse con las pruebas de fluorescencia durante la selección de microorganismos productores de PHAs, diversos autores han recomendado el uso de pruebas moleculares como la amplificación por PCR del gen phaC, el cual codifica para la enzima PHA sintasa. Esta prueba permite seleccionar específicamente los microorganismos productores de PHAs, minimizando los posibles falsos positivos de las coloraciones tradicionales, que por su inespecificidad pueden teñir también lípidos celulares (Sheu et al., 2000).
De las cuatro cepas preseleccionadas (F1, F2, F3 y F4) mediante fluorescencia con azul de Nilo, F3 y F4 amplificaron por PCR con el juego de cebadores B-1F y B-1R, dirigido al arreglo genético del operón de biosíntesis de PHAs tipo IV, obteniéndose un fragmento de un tamaño aproximado de 600 pb. Las evaluaciones de PCR en las que se emplearon los otros tres pares de cebadores, no arrojaron los amplicones esperados en ninguno de los microorganismos. La secuenciación de los amplicones obtenidos y su posterior comparación con las bases de datos moleculares, permitió confirmar la presencia del gen phaC en las cepas F3 y F4, presentando un nivel de identidad del 98%, valor e=0.0 y cobertura de la comparación del 99%, con una región codificante para PHA sintasa ubicada entre las posiciones 5920 y 6497 de un cluster secuenciado por McCool y Cannon (2001) en Bacillus megaterium (Accesión AF109909).
Con base en trabajos previos realizados por Shamala et al. (2003), quienes reportan que los cebadores diseñados para amplificar el gen PhaC de B. megaterium, también son efectivos para obtener amplicones en otras especies de Bacillus, no es posible definir la identidad taxonómica inequívoca de las bacterias bajo estudio, por lo que en este trabajo de investigación se secuenció la región 16S del ADNr. Estos investigadores señalan también que en una cepa identificada como B. licheniformes, no lograron la obtención del fragmento de phaC con dichos cebadores, aunque se detectó químicamente la producción del biopolímero. Lo anterior indica, que es necesario continuar con la secuenciación del operón de biosíntesis de PHAs en diferentes miembros de éste género, de manera que sea posible la obtención de cebadores universales o en su defecto, la definición de nuevos tipos de arreglos genéticos al interior del género Bacillus. Por esto, la ausencia de amplificación en las cepas F1 y F2 obtenidas en este estudio y detectadas como positivas para PHAs en las pruebas con colorantes, no conduce a su descarte, sino más bien, a la necesidad de realizar estudios moleculares más detallados como Southern-blot y Genome-walking, que permitirían determinar inequívocamente la presencia y características del operón responsable de la biosíntesis de PHAs en estas bacterias.
En este sentido, es importante indicar que existen diversos métodos para identificar organismos productores de PHAs (Spiekermann et al., 1999). En la mayoría se utilizan colorantes lipofílicos como el negro Sudán, el azul de Nilo y rojo de Nilo, que se unen al polímero emitiendo fluorescencia (Solaiman et al., 2000). Aunque estas metodologías son muy sensibles, no son completamente efectivas para la selección, porque los colorantes pueden formar complejos fluorescentes con compuestos afines a los biopolímeros, como lo son las inclusiones lipídicas. Además, la producción de PHAs depende de las condiciones nutricionales del medio de crecimiento, especialmente de las relaciones C/N y C/P. Otro factor que incide, es la naturaleza del sustrato, a tal punto que aunque los genes del operón bacteriano existan, no logran expresarse, dando lugar a falsos negativos (Solaiman et al., 2000; Shamala et al., 2003). Debido a estos inconvenientes, el complemento de estudios como el aquí presentado, con la detección directa por PCR y secuenciación del gen phaC y/o de otros componentes del operón de biosíntesis de PHAs, resulta deseable para darle un mayor soporte a las evaluaciones fenotípicas.
Identificación taxonómica de las bacterias productoras de PHAs
Las amplificaciones de PCR realizadas mediante el empleo de los cebadores PA y P5CB, permitieron obtener los fragmentos esperados de aproximadamente 1440 pb, en las cuatro cepas microbianas seleccionadas. La comparación de las secuencias de los amplicones con las bases de datos moleculares, indicaron para las cepas F3 y F4 niveles de identidad del 100% (valor e: 0.0) para la región 16S del ADNr con aislamientos de Bacillus megaterium de diferentes fuentes y regiones geográficas. La secuencia de la cepa F2 presentó niveles de identidad del 100% con diferentes especies de Bacillus, incluyendo B. mycoides, B. weihenstephanensis y cepas no identificadas a nivel de especie.
Por su parte, la secuencia de la cepa F1 presentó un 100% de identidad (valor e: 0.0) con la especie Gordonia westfalica, reportada por Linos et al. (2002) en el desarrollo de un trabajo en el que se evaluaban bacterias degradadoras de caucho. Esta cepa bacteriana también presentó valores del 99% de identidad con varios aislamientos de Gordonia sp. procedentes de suelos contaminados con fenol, aguas de neumáticos y esputo.
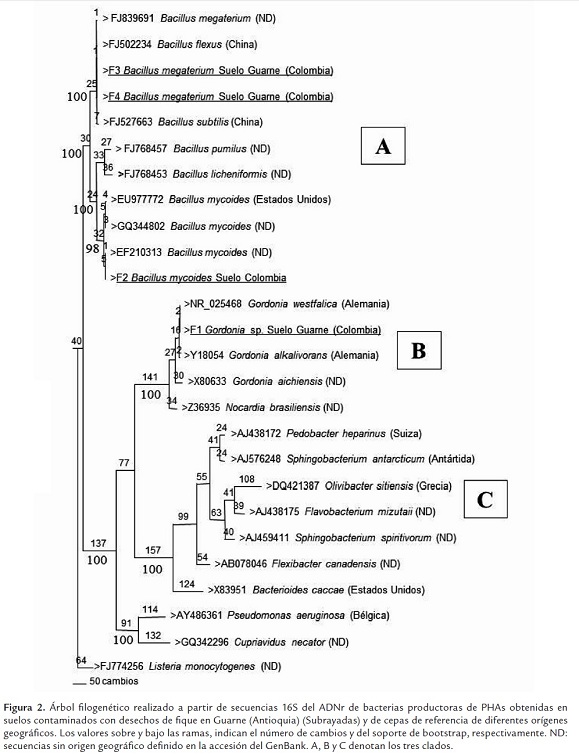
Para brindar mayor soporte a los resultados generados por BlaST, se realizó un análisis filogenético basado en 1425 caracteres del ADNr 16S. De estos, 583 resultaron informativos para el análisis de parsimonia, 723 fueron constantes y 119 variables pero no informativos. El dendrograma generó tres clados (A, B, C) soportados por un valor de bootstrap de 100% (Figura 2). El clado A agrupó todas las cepas del género Bacillus, incluyendo las denominadas F3 y F4, que fueron identificadas como B. megaterium, y la cepa F2, que se ubicó en un subgrupo con tres aislamientos de referencia de B. mycoides, fuertemente soportado por el análisis de bootstrap (98%). El clado B se presentó con dos subgrupos que dividían las cepas de diferentes especies de Gordonia y esfingobacterias de diferentes géneros. La cepa F1 se agrupó en el primer subclado con Gordonia sp., con un valor del 100% de bootstrap. El clado C correspondió a las cepas Gram negativas Pseudomonas aeruginosa y Cupriavidus necator, utilizadas como productoras de referencia de PHAs, las cuales se presentaron muy distantes de los dos grupos anteriormente mencionados. El árbol presentó como secuencia basal, la de Listeria monocytogenes (grupo externo de análisis).
Finalmente, las evaluaciones de tinción de Gram y del API 50 CH para bacilos positivos esporulados, permitió confirmar la identidad de la cepa F2 como B. mycoides y de las F3 y F4 como B. megaterium (Figura 1). Por otra parte, la cepa F1, identificada molecularmente como Gordonia sp., presentó una tinción Gram positiva y una coloración naranja intensa en el medio de cultivo (Figura 1), además de los siguientes resultados en la batería bioquímica, TSI: k/k, LIA: k/k, PPA: -, RM: -, VP: -, Ureasa: +, SIM: -, movilidad: -, Citrato: -, Malonato: -, Catalasa: +, Oxidasa: -, Coloración ZN: no se presentaron bacilos ácido-alcohol resistentes. Sin embargo, ante la gran versatilidad metabólica de las bacterias de este género, con esta información no fue posible su clasificación a nivel de especie, siendo necesario evaluar otros aspectos como la longitud de sus ácidos micólicos y el tipo de menaquinonas (Cuesta, 2004).
Caracterización química de PHAs
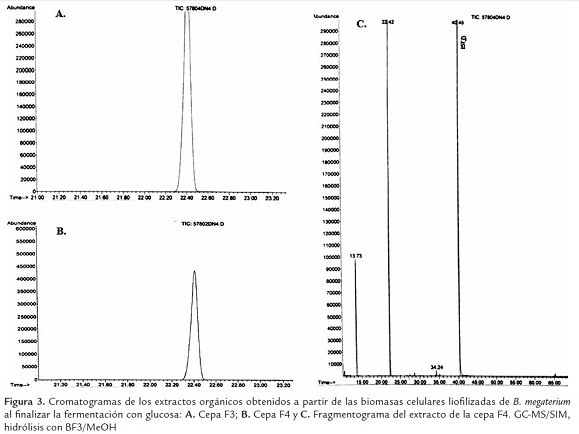
De acuerdo con los perfiles cromatográficos, el PHB fue el principal monómero de los PHAs producido a partir de las cepas F3 y F4 de B. megaterium. Los metilésteres formados al someter el PHB comercial a hidrólisis y posterior derivación con BF3/MeOH, se identificaron por GC-MS/SIM como metiléster del ácido-2-butenoico, metiléster del ácido-3-hidroxibutanoico y metiléter del ácido-3-hidroxibutírico (Figura 3). Este último compuesto se detectó mayoritariamente a un tiempo de retención de 22.44 min, por lo que fue utilizado para estimar la concentración de PHB en las muestras de origen microbiano; calculándose una concentración de 63.8 mg/g y 95.3 mg/g de PHB para los extractos biopoliméricos de las cepas F3 y F4, respectivamente.
Los resultados obtenidos en esta investigación, coinciden con los de trabajos previos que reportan la capacidad de B. megaterium para producir PHB a partir de glucosa, glicerol, sacarosa y diferentes desechos agroindustriales como melaza de caña (López et al., 2012). Vishnuvardhan et al. (2009), por ejemplo, utilizando una cepa de B. megaterium aislada de lodos de alcantarillado, obtuvieron PHB con rendimientos del 62.4% y 58.6%, a partir de glicerol y glucosa, respectivamente; este potencial puede direccionarse para lograr su empleo a escala industrial, para la generación de valor agregado a partir de bioproductos de la industria del biodiesel, como lo es el glicerol (López et al. 2012).
Es de anotar que la ausencia de membrana externa en las bacterias Gram positivas, como Bacillus sp., les hace más promisorias que las Gram negativas en la producción de biopolímeros con aplicaciones biomédicas, porque no presentan la condición de endotoxinas que generan algunos de los liposacaridos (LPS) presentes en esta membrana (López et al., 2012). Otra ventaja de las cepas de Bacillus sp., es su rápido crecimiento sobre diferentes sustratos, incluyendo residuos agroindustriales. Sin embargo, en términos prácticos, presentan el inconveniente de que los mismos desbalances nutricionales (C vs N; C vs P) asociados a la producción de PHAs, inducen su esporulación, reduciendo su eficiencia en la síntesis de los biopolímeros (Wu et al., 2001); no obstante, recientemente se reportó que la eficiencia puede mejorarse sustancialmente, implementando sistemas de fermentación por lotes y estrategias experimentales para determinar los tiempos y condiciones de aporte de los nutrientes (López et al. 2012). Esto se aprecia en el trabajo de Sabra y Aboud-Zeid (2008), en el que lograron reducir casi completamente la esporulación de una cepa de B. megaterium y generar 65% de PHB en peso seco celular, controlando principalmente la concentración de amonio (0.2-0.4 g/L) en un sistema de fermentación por lotes.
En el presente trabajo de investigación se identificaron cuatro cepas bacteriales aisladas a partir de suelos tratados con diferentes residuos sólidos y líquidos del proceso de beneficio de fique, en una región tradicionalmente productora de esta fibra, como lo es Guarne (Antioquia). Pruebas indirectas de coloración con tintes y PCR para el gen PhaC y directas, a partir de análisis cromotográfico de gases, confirmaron la capacidad de dos de las bacterias para producir PHB. Estas bacterias se identificaron molecular y bioquímicamente como miembros de la especie B. megaterium y representan una alternativa para transformar directamente el jugo de fique en productos de valor agregado, como los biopolímeros. Además, podrían evaluarse su eficiencia en la producción de PHB a partir de diferentes residuos agroindustriales convencionales (melazas y bagazos de caña de azúcar, lactosueros, residuos de palma, glicerina) y no convencionales, como los que se generan de los procesos de producción de pulpas de frutas, aceites comestibles y estiércol de animales.
Las otras dos cepas identificadas como Gordonia sp. y B. mycoides, también han sido reportadas como productoras de PHAs (Cuesta, 2004; Fernández y Ortiz, 2006), aunque su eficiencia es aparentemente menor en relación con B. megaterium.
Por otra parte, en trabajos preliminares realizados por nuestro grupo, se ha encontrado que el jugo de fique es una matriz que inhibe el crecimiento microbiano, por lo que se requiere emprender estudios que evalúen las condiciones de fermentación que se adapten mejor a un medio enriquecido con este extracto, que incluyan pretratamientos físicos y químicos que disminuyan su acción deletérea para las bacterias.
Conclusiones
Para la selección de bacterias productoras de Polihidroxialcanoatos (PHAs) es importante considerar un conjunto de pruebas y técnicas biológicas y químicas, que van desde las tinciones con rojo y azul de Nilo, para la preselección de los microorganismos, hasta el análisis cromatográfico (GC/MS/SIM), que permite identificar y cuantificar el biopolímero, pasando por la identificación molecular y bioquímica de las cepas. La aplicación de este conjunto de pruebas, permitió en este trabajo reconocer y seleccionar dos cepas de B. megaterium, una de B. mycoides y una de Gordonia sp., aisladas de suelos contaminados con residuos del proceso de beneficio de fique en el municipio de Guarne (Antioquia), como promisorias para la producción industrial de PHAs a partir de residuos agroindustriales generados en el país, incluyendo los derivados de la cadena productiva del fique.
Agradecimientos
Esta investigación fue financiada por la Universidad Nacional de Colombia Sede Medellín a través del proyecto DIME Código 20101007214. Se agradece al Centro de Cromatografía y Espectrometría de Masas de la Universidad Industrial de Santander, por los análisis cromatográficos.
Referencias bibliográficas
1 Almeida, A., Ruiz, J., López, N. 2004. Bioplásticos: Una alternativa ecológica. Revista Química Viva. 3: 122-133. [ Links ]
2 Barbosa, M., Moreno, N., Espinosa, A., Malagón, D. 2005. Producción de poli-B-hidroxibutirato (PHB) por Ralstonia eutropha ATCC 17697. Revista de la Facultad de Ciencias Pontificia Universidad Javeriana. 10: 45-54. [ Links ]
3 Capuccino, J., Sherman, N. 2007. Microbiology: A Laboratory Manual. New York: Benjamin Cummings. 544 p. [ Links ]
4 Chen, G.Q., Wu, Q. 2005. The application of polyhydroxyalkanoates as tissue engineering materials. Biomaterials. 26: 6565-6578. [ Links ]
5 Cuesta, G. 2004. Detección y caracterización por métodos fenotípicos y moleculares de mycolata formadores de espumas en estaciones depuradoras de aguas residuales domésticas con sistemas de fangos activos. Tesis Doctoral. Valencia: Universidad Politécnica de Valencia. Departamento de Biotecnología. [ Links ]
6 Dionisi, D., Majone, M., Papa, V., Beccari, M. 2004. Biodegradable polymers from organic acid by using actived sludge enriched by aerobic periodic feeding. Biotechnology and Bioengineering. 85: 569-579. [ Links ]
7 Felsenstein, J. Confidence limits on phylogenies: an approach using the bootstrap. Evolution. 39: 783-791. [ Links ]
8 Fernández, P., Ortíz, F. 2006. Influencia de fuentes de carbono y nitrógeno en el crecimiento bacteriano y en la síntesis de copolímero Poli-(hidroxibutirato-co-hidroxivalerato) de una cepa silvestre de Bacillus mycoides. Universidad y Salud. 1: 34-42. [ Links ]
9 Franco, M., Gómez, D., Medina, N., Rendón, M. 2009. Polihidroxialcanoatos en actinomicetos nativos de suelos colombianos. Revista Peruana de Biología. 16: 115- 118. [ Links ]
10 Hall, T.A. 1999. BioEdit: a user-friendly biological sequence alignment editor and analysis program for Windows 95/98/NT. Nucleic Acids Symposium Series. 41: 95-98. [ Links ]
11 Kuske, C.R., Bams, S.M., Busch, J.D. 1997. Diverse uncultivated bacterial groups from soils of the Arid Southwestern United States that are present in many geographic regions. Applied Environmental Microbiology. 63: 3614-3621. [ Links ]
12 Larkin, M., Blackshields, G., Brown, N.P., Chenna, R., McGettigan, P.A., McWilliam, H., Valentin, F., Wallace, I.M., Wilm, A., López, R., Thompson, J.D., Gibson, T.J., Higgins, D.G. 2007. Clustal W and Clustal X version 2.0. Bioinformatics 23: 2947-2948. [ Links ]
13 Linos, A, Berekaa, M.M., Steinbüchel, A., Kim, K.K., Sproer, C., Kroppenstedt, R.M. 2002. Gordonia westfalica sp. nov., a novel rubber degrading actinomycete. International Journal of Systematic and Evolutionary Microbiology. 52: 1133-1139. [ Links ]
14 López, J.A., Naranjo, J.M., Higuita, J.C., Cubitto, M.A., Cardona, C.A., Villar, M.A. 2012. Biosynthesis of PHB from a new isolated Bacillus megaterium strain: outlook on future developments with endospore forming bacteria. Biotechnology and Bioprocess Engineering. 17: 250-258. [ Links ]
15 Martínez, A., Caicedo, T. 2002. Bioensayo de toxicidad de los jugos de fique en peces en el municipio de Tambo (Nariño). Tesis especialización de Salud Ambiental. Bogotá: Universidad del Bosque. 26 p. [ Links ]
16 Mccool, G., Canoon, M. 2001. PhaC and PhaR are required for polyhydroxyalkanoic acid synthase activity in Bacillus megaterium. Journal of Bacteriology. 183: 4235-4243. [ Links ]
17 MINISTERIO DE AGRICULTURA Y DESARROLLO RURAL - MADR. 2008. Cadena agroindustrial del fique. Bogotá, Colombia. p 8. [ Links ]
18 Moreno, N., Malagón, D., Cortázar, J., Espinosa, A. 2006. Recuperación de poli-b-hidroxihexanoato-co-octanoato sintetizado por Pseudomonas putida mediante el uso de dispersiones hipoclorito-cloroformo. Revista de la Facultad de Ciencias Pontificia Universidad Javeriana. 11: 41-48. [ Links ]
19 Ostle, A.G., Holt, J.G. 1982. Nile Blue A as a fluorescent stain for poly-beta-hydroxybutyric acid. Applied and Environmental Microbiology. 44: 238-241. [ Links ]
20 Peinado, J.E., Ospina, L.F., Rodríguez, L., Miller, J., Cruz, D., Medina, R., Toscano, D., Toro, I., Medina, R. 2006. Guía Ambiental del Subsector fiquero. Bogotá: Ministerio de Ambiente, Vivienda y Desarrollo Territorial. 121 p. [ Links ]
21 Reddy, C., Ghai, R., Kalia, V.C. 2003. Polyhydroxyalcanoates: an overwiew. Bioresource Technology. 87: 137-146. [ Links ]
22 Reddy, S.V., Thirumala, M., Mahmood, S.K. 2009. Production of PHB and P (3HB-co-3HV) biopolymers by Bacillus megaterium strain OU303A isolated from municipal sewage sludge. World Journal of Microbiology and Biotechnology. 25: 391-397. [ Links ]
23 Revelo, D. 2007. A most effective method for selecting a broad range of short and medium chain-length polyhidroxyalcanoate producing microorganisms. Electronic Journal of Biotechnology. 10: 348-357. [ Links ]
24 Sabra, W., Aboud-Zeid, D.M. 2008. Improving feeding strategies for maximizing polyhydroxybutyrate yield by Bacillus megaterium. Research Journal of Microbiology. 3: 308-318. [ Links ]
25 Shamala, T.R. 2003. Identification of polyhydroxyalkanoate (PHA)-producing Bacillus spp. using the polymerase chain reaction (PCR). Journal of Applied Microbiology. 94: 369-374. [ Links ]
26 Sheu, D.S., Wang, Y.T., Lee, C.Y. 2000. Rapid detection of plyhydroxyalkanoate-accumulating bacteria isolated from the environment by colony PCR. Microbiology. 146: 2019-2025. [ Links ]
27 Solaiman, D.K., Ashby, R.D., Foglia, T.A. 2000. Rapid and specific identification of medium-chain-length Polyhydroxyalkanoate synthase gene by polymerase chain reaction. Applied Microbiology and Biotechnology. 53: 690-694. [ Links ]
28 Spiekermann, P., Rehm, B.H., Kalscheuer, R., Baumeister, D., Steinbuchel, A. 1999. A sensitive, viable-colony staining method using Nile Red for direct screening of bacteria that accumulate polyhydroxyalkanoic acids and other lipid storage compounds. Archives for Microbiology. 171: 73-80. [ Links ]
29 Stubbe, J., Tian, J. 2003. Polyhydroxyalkanoate (PHA) homeostasis: the role of the PHA synthase. Natural Products Reports. 20: 445-457. [ Links ]
30 Swofford, D.L. 1998. PAUP*: Phylogenetic Analysis Using Parsimony (and other methods). Sunderland: Sinauer Associates. [ Links ]
31 Thirumala, M., Reddy, S.V., Mahmood, S.K. 2010. Production and characterization of PHB from two novel strains of Bacillus spp. isolated from soil and activated sludge. Journal of Industrial Microbiology and Biotechnology. 37: 271-278. [ Links ]
32 Vishnuvardhan, S., Reddy, C., Thirumala, M., Mahmood, S.K. 2009. Production of PHB and P (3HB-co-3HV) biopolymers by Bacillus megaterium strain OU303A isolated from municipal sewage sludge. World Journal of Microbiology and Biotechnology. 25: 391-397. [ Links ]
33 Yan, Q., Du, G., Chen, J. 2003. Biosynthesis of polyhydroyalcanoates (PHAs) with continuos feeding of mixed organics acids as carbon sources by Ralstonia eutropha. Process Biochemistry. 39: 387-391. [ Links ]
34 Yilmaz, M., Beyatli, Y. 2005. Poly-B-hydroxybutyrate (PHB) production by a Bacillus cereus M5 strain in sugarbeet molasses. Zuckerindustrie. 130: 109-112. [ Links ]
35 Wu, Q., Huang, H., Hu, G., Chen, J., Ho, K.P, Chen, G.Q. 2001. Production of poly-3-hydroxybutyrate by Bacillus sp. JMa5 cultivated in molasses media. Antonie Van Leeuwenhoek. 80: 111-118. [ Links ]