Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Biotecnología
Print version ISSN 0123-3475
Rev. colomb. biotecnol vol.15 no.1 Bogotá Jan./June 2013
ARTÍCULO DE INVESTIGACIÓN
Caracterización del perfil quimiosensibilidad y del estado de ampliación génica de un panel de líneas celulares de origen tumoral pulmonar
Amplificación génica y quimiosensibilidad en líneas celulares de cáncer de pulmón
Characterization of chemosensitivity profile gene amplification status of a panel of lung cancer cell lines
Sandra Johanna Morantes1 , Sandra Perdomo2 , Edward Fabián Carrillo3 , Fabio Aristizábal4.
1 cPhD Ciencias Farmacéuticas, Departamento de Farmacia, Facultad de Ciencias, Universidad Nacional de Colombia. sjmorantesm@unal.edu.co
2 PhD Ciencias Biológicas, Pontificia Universidad Javeriana, Unidad de Investigación Básica Oral, Universidad el Bosque sperdomo@javeriana.edu.co
3 PhD Ciencias Farmacéuticas, Departamento de Farmacia, Facultad de Ciencias, Universidad Nacional de Colombia, Instituto de Investigaciones Biomédicas Universidad Libre-Cali efcarrillob@unal.edu.co
4 PhD en Ciencias Biológicas, Profesor Titular, Departamento de Farmacia, Facultad de Ciencias, Universidad Nacional de Colombia. faaristizabalg@unal.edu.co
Recibido: noviembre 28 de 2012 Aprobado: junio 15 de 2013
Resumen
En este trabajo se presentan los resultados de un análisis de amplificación génica y de sensibilidad a fármacos antineoplásicos, realizado para un panel de líneas celulares de origen tumoral pulmonar. Para los ensayos de quimiosensibilidad las células fueron tratadas durante 48 h con concentraciones variables de taxol, cisplatino, doxorrubicina y 5-fluoracilo. La citotoxicidad de los fármacos se cuantificó usando el ensayo de reducción de resazurina y se reportó en valores de concentración inhibitoria 50 (CI50). Para los análisis de amplificación génica se emplearon sondas TaqMan® dirigidas contra los genes AKT2, PIK3CA, ERBB2, EGFR, c-REL y genes de la familia MYC. El número de copias para cada gen fue calculado usando el método de doble delta Ct, empleando ACTB como gen de referencia y la línea MRC-5 como muestra control. Los resultados mostraron que la viabilidad de todas las líneas celulares se afectó por el tratamiento con taxol, cisplatino y doxorrubicina, pero no con el tratamiento con 5-fluoracilo. Las CI50 calculadas se ubicaron entre 0,38 ± 0,03 µM y 111,3 ± 3,58 µM, siendo el taxol y la doxorrubicina los fármacos más potentes. Del panel evaluado las células NCI-H292 resultaron ser las más sensibles y las células LSPG8G las más resistentes a los fármacos. Interesantemente en las células NCI-H292 ningún gen se encontró amplificado; por el contrario en las células LSPG8G los genes cMYC, MYCN, MYCL y AKT2 mostraron un aumento en el número de copias con respecto al de las células control. Estos resultados sugieren que eventos de amplificación génica podrían contribuir con el fenómeno de quimioresistencia en líneas celulares de cáncer de pulmón, sin embargo otros estudios deben realizarse para confirmar esta hipótesis.
Palabras clave: cáncer de pulmón, citotoxicidad in vitro, dosis génica, NCI-H292, LSPG8G.
Abstract
In this paper, we show results of anticancer drug sensitivity assays and studies of gen amplification performed for a panel of lung cancer cell lines. For the chemosensitivity assays the cells were treated for 48 h with different concentrations of taxol, cisplatin, doxorubicin and 5-fluorouracil. The cytotoxic effect of each drug was determined using the resazurin reduction assay and reported in terms of inhibitory concentration 50 (IC50). For the analysis of gene amplification we used TaqMan® probes designed against AKT2, PIK3CA, ERBB2, EGFR, REL and MYC family members. Copy number for each gene was calculated using the delta-delta-CT method, employing ACTB as reference gen and MRC-5 cell line as control sample. In the chemosensitivity assays, we observed a clear decrease in cell viability in the cells treated with taxol, cisplatin and doxorubicin but not in the cells treated with 5-fluorouracil. IC50 values ranging between 0,38± 0,03 µM and 111,3 ±3,58 µM, being the taxol and doxorubicin the most potent drugs. NCI-H292 cell line was the most sensitivity and LSPG8G cell line was the most resistant. Interestingly, NCI-H292 cells did not show increase in the copy numbers for the gene evaluated, in contrast, we observed changes in the gene dosage for cMYC, MYCN, MYCL and AKT2 in LSPG8G cells. These results suggest that gene amplification could contribute to drug resistance in lung cancer cell lines; however, more studies are needed to confirm this hypothesis.
Key words: lung cancer, in vitro cytotoxicity, gene dosage, NCI-H292, LSPG8G.
Introducción
Las líneas celulares derivadas desde tumores humanos han constituido uno de los modelos preclínicos más empleados para estudiar las bases genéticas y moleculares del cáncer de pulmón. Antes de su establecimiento, la mayoría de las investigaciones alrededor de esta enfermedad progresaban lentamente, sin embargo con su desarrollo, hoy ya se conocen diferentes cambios a nivel molecular relacionados con la transformación tumoral, el desarrollo de metástasis y la aparición de quimioresistencia (Miller, 2005).
La quimioresistencia es uno de los principales obstáculos para el tratamiento del cáncer de pulmón (ŠKarda et al., 2008) y puede presentarse en respuesta al tratamiento (resistencia adquirida) o al momento del diagnóstico (resistencia intrínseca). La selección de clones quimioresistentes a partir de líneas celulares expuestas a concentraciones crecientes de fármacos antitumorales, es una de las aproximaciones más empleadas para estudiar la resistencia adquirida. En estos ensayos un criterio que define las diferencias entre la sensibilidad de la línea parental (no tratada) y la línea resistente (tratada), es el valor de la concentración inhibitoria 50 (CI50). Sin embargo, para realizar estas comparaciones hay ciertos aspectos que deben considerarse, pues se ha demostrado que este valor, puede cambiar dependiendo de los tiempos de duplicación de la línea celular empleada, los tiempos de exposición al fármaco, el número de células tratadas y el método usado para cuantificar la viabilidad celular (Sumantran, 2011; Ari et al., 2010; Zumpe et al., 2010; Ulukaya et al., 2008).
La amplificación génica es uno de los mecanismos más frecuentes de activación de oncogenes en los tumores sólidos (Starczynowski et al., 2011). Es un evento a nivel celular que se caracteriza por un incremento en el número de copias de un gen o región cromosómica y se asocia comúnmente con sobreexpresión de los genes implicados (Albertson, 2006). En cáncer de pulmón y otros tumores sólidos se ha reportado que los oncogenes MYC, MYCN, MYCL, EGFR, AKT-2, ERBB2, PIK3CA y REL pueden estar amplificados (Santarius et al., 2010; Alvarez et al., 2012). Por otro lado, la relación de dosis génica y respuesta a fármacos se ha establecido en algunos trabajos, aunque la mayoría se enfocan en genes que codifican para dianas terapéuticas (Cappuzzo et al., 2005) y/o proteínas transportadoras (Yasui et al., 2004).
En este trabajo se establecieron las condiciones para realizar pruebas de quimiosensibilidad a 48 h de exposición, usando líneas celulares de cáncer de pulmón con diferentes tiempos de duplicación y empleando el ensayo de reducción de resazurina como método indirecto para evaluar viabilidad celular. Se compara el perfil de sensibilidad frente a fármacos antineoplásicos con diferentes mecanismos de acción y se caracteriza el estado de amplificación génica (número de copias promedio por genoma) para el grupo de oncogenes atrás descritos. Al final se identifican líneas celulares sensibles y resistentes a quimioterapéuticos y se presentan resultados que pueden servir de soporte para comenzar estudios de amplificación génica en modelos in vitro de resistencia adquirida.
Materiales y métodos
Líneas celulares y condiciones de cultivo
Se emplearon las líneas celulares LSPG8G (aislada en el laboratorio a partir de un carcinoma anaplásico de célula grande) A549 (adenocarcinoma), NCI-H520 (carcinoma escamocelular), NCI-H727 (carcinoide), NCI-H292 (carcinoma mucoepidermoide), NCI-H460 (carcinoma anaplásico de célula grande) y MRC-5 (fibroblastos normales de pulmón). Todas las células fueron propagadas en frascos de cultivo celular de 75 cm2, a 37°C, en atmósfera con 5% de CO2 y medio RPMI-1640, suplementado con 10% de Suero Fetal Bovino, penicilina 100 U/ml y estreptomicina a 100 mg/ml.
Fármacos
Se emplearon las formas comerciales de los fármacos: paclitaxel, cisplatino, doxorrubicina HCl y 5-fluorouracilo. Se evaluaron cinco diluciones seriadas en diferentes rangos de concentración y cada dilución se evaluó por triplicado. La concentración de partida se modificó dependiendo del fármaco, para el taxol la concentración inicial fue de 100 µM, para cisplatino, doxorubicina y 5-fluorouracilo fue de 300 µM.
Selección de densidades de trabajo para los ensayos de quimiosensibilidad
Para garantizar un crecimiento exponencial de las células durante el tiempo de exposición a los fármacos, se calculó la densidad celular óptima de trabajo. Para calcularla, se tuvo en cuenta el tiempo de duplicación poblacional de las células, el porcentaje de confluencia en las placas de 96 pozos después de 48 h y 72 h de cultivo y los resultados de linealidad obtenidos a partir del ensayo de reducción de resazurina. La densidad se seleccionó a partir de un grupo de 6 densidades (5 x103, 7,5 x 103, 12,5 x 103, 1,5 x 104 y 2 x 104 células por pozo). Cada densidad celular fue sembrada en triplicado usando 100 μl de medio de cultivo, e incubadas bajo las mismas condiciones en las que se realizan los ensayos de quimiosensibilidad (descritos adelante). Luego se realizó el ensayo de reducción de resazurina y se verificó si se mantenía una relación lineal entre la fluorescencia emitida por las células que metabolizaron la resazurina y las densidades sembradas en los pozos.
Ensayos de Quimiosensibilidad
Las células en fase de crecimiento exponencial, fueron tripsinizadas, contadas en cámara de Neubauer y sembradas en las densidades celulares seleccionadas. Las placas se incubaron por 24 h a 37ºC para permitir la adhesión al soporte. Transcurrido este tiempo la monocapa celular fue expuesta durante 48 h a 100 µL de las diluciones de cada fármaco. Luego se cuantificó el efecto citotóxico mediante el ensayo de reducción de resazurina. Cada ensayo de quimiosensibilidad se realizo por triplicado, en semanas diferentes.
Ensayo de reducción de resazurina
Para realizar este ensayo el medio con los tratamientos se remplazó por 100 ml de medio con resazurina a una concentración final de 44 µM. Las placas se incubaron por 4 horas y la fluorescencia emitida por las células viables y/o metabólicamente activas se cuantificó usando un espectroflourómetro a una longitud de onda de excitación de 535 y una de emisión de 595 (O"Brien et al., 2000). Las unidades de fluorescencia emitidas por las células tratadas se transformaron a porcentajes de supervivencia normalizando con las unidades de fluorescencia emitidas por las células control (células sin tratamiento). En todos los casos se asumió un 100% de supervivencia en las células sin tratamiento, al final la respuesta celular se graficó en función del logaritmo de la concentración y a partir de la curva dosis-respuesta se calcularon los valores de CI50, usando el programa estadístico GraphPad Prism® versión 5 (GraphPad Software Inc).
Extracción de ADN genómico para análisis moleculares
Las células en un 80% de confluencia fueron lavadas con PBS y tratadas con una solución de tripsina (0,025%) - EDTA (0,03%) durante 5 minutos. La suspensión obtenida se centrifugó a 1200 rpm x 5 minutos y se descartó el sobrenadante. El botón celular obtenido se resuspendió en 200 μl de una solución de Tris-HCl 50mM pH 8.0, acetato de calcio 2 mM con 200 μg de proteinasa K. La mezcla se incubó a 55°C por una hora y luego a 95°C por 5 minutos para inactivar la enzima. Inmediatamente después el ADN se recuperó por extracción con fenol:cloroformo:alcohol isoamílico (25:24:1) y precipitación con etanol. Su cuantificación se realizó por métodos espectrofotométricos.
Análisis de número de copias o dosis génica
Los análisis se realizaron por PCR en tiempo real empleando el sistema ABI® 7500 Prism (Applied Biosystems), en un volumen final de 25 μl y en mezclas de reacción multiplex preparadas con 0,04 μM de cebadores, 0,375 μM de sondas, 1x de Master Mix y 20ng de ADN. El programa de PCR utilizado para la detección de los fragmentos incluyó un ciclo de 10 min a 95°C, seguido por 40 ciclos 15 s a 95°C y 1 min a 61°C. La dosis génica fue determinada empleando el método comparativo de doble delta Ct (2-ΔΔCt). En todos los ensayos se usó el gen ACTB como gen referencia y ADN de las células MRC-5 (fibroblastos normales de pulmón) como muestra control. Un valor de 2-ΔΔCt mayor a 2 se consideró como amplificación génica (Huang et al., 2007). La secuencia de las sondas TaqMan® y los cebadores usados en este ensayo se reportan en estudios previos (Perdomo et al., 2012; Alvarez et al., 2012) y se muestran en la tabla 1.
Resultados
Selección de densidades de trabajo para ensayos quimiosensibilidad
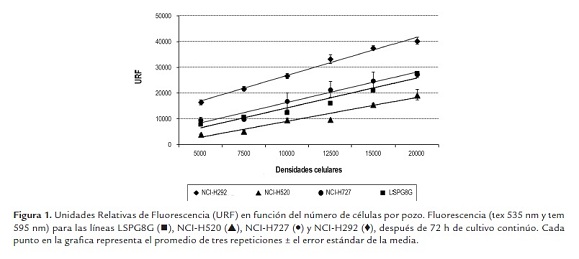
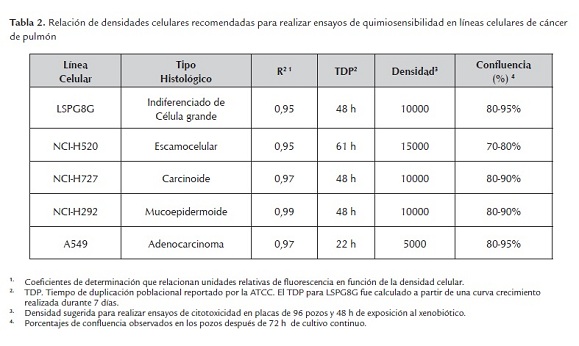
Al graficar las unidades relativas de fluorescencia (URF) en función de las densidades celulares se determinó que las líneas LSPG8G, NCI-H292, NCI-H520 y NCI-H727 después de 72 h de crecimiento continuo, muestran una respuesta lineal frente a la reducción de resazurina cuando se siembran entre 5000 y 20000 células por pozo (figura 1). Para la línea A549 se mantiene la tendencia lineal solo entre 5000 y 12500 células por pozo. En densidades mayores se pierde esta tendencia y a las 48 h se observa un 100% de confluencia, un nivel que no garantiza el crecimiento exponencial de las células durante el tiempo de tratamiento y por tanto la confiabilidad de los resultados de los ensayos de citotoxicidad. Para el resto de las líneas, en densidades menores a 15000 células por pozo, se observaron niveles de confluencia entre un 50 - 70% a las 48 h y entre el 70 y 95% a las 72 h de cultivo; la mayor confluencia a las 72 h se observa para las células con mayor tamaño (LSPG8G) y con tiempos de duplicación cortos (A549). La menor confluencia se observó para la línea NCI-H520, una línea con un tiempo de duplicación de 61 h y en general más pequeña que el resto de células del panel. En el tabla 2 se resumen los resultados del análisis de linealidad, se muestran los valores R2 y los porcentajes de confluencia observados a las 72 h de cultivo para las densidades de trabajo seleccionadas. Una densidad de trabajo de 15000 células por pozo se recomendó para las células NCI-H460 en un estudio previo (Prieto & Aristizábal, 2009).
Ensayos de quimiosensibilidad
Los resultados de tres experimentos independientes muestran que bajo nuestras condiciones de ensayo, los fármacos cisplatino, taxol y doxorrubicina HCl, afectan la actividad metabólica de todas las líneas en rangos de concentración del orden µM. Al probar rangos del orden nanomolar, las células conservan la capacidad de metabolizar la resazurina y los valores de fluorescencia emitidos por las células tratadas son comparables a los valores observados en las células sin tratamiento. Cuando las células fueron tratadas con 5-fluoracilo, la reducción de la capacidad metabólica y/o viabilidad celular solo fue evidente en concentraciones mayores a 1mM.
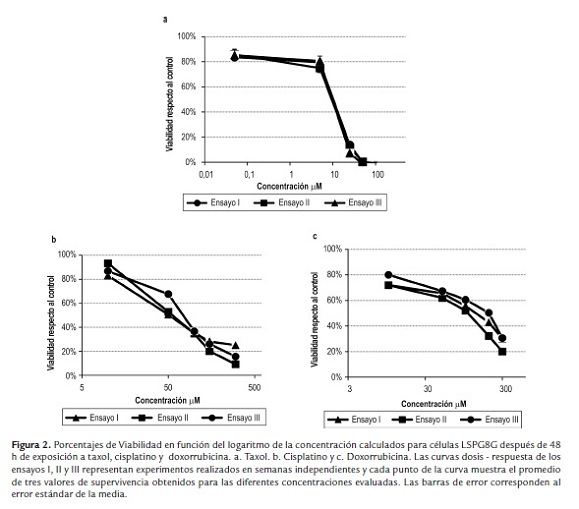
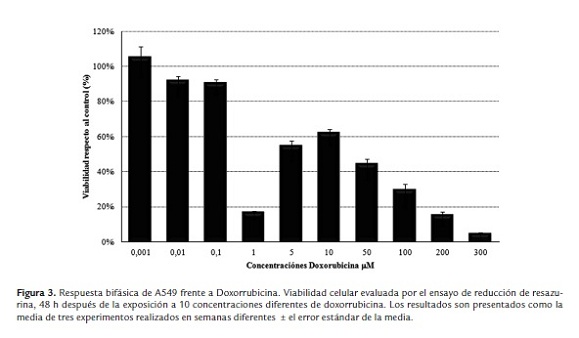
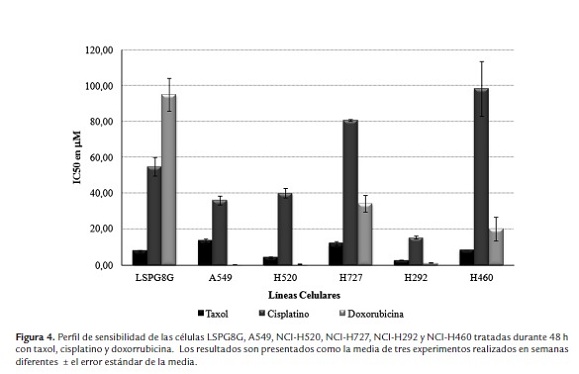
En general la actividad citotóxica de los fármacos fue dependiente de la concentración, aunque no en todos los casos se observó una respuesta lineal. En la figura 2 se observa la tendencia de las curvas dosis-respuesta obtenidas para las células LSPG8G tratadas con taxol, cisplatino y doxorrubicina. Una tendencia que fue similar en la mayoría de las líneas. En la figura 3 se grafica el comportamiento bifásico observado en las células A549 tratadas por 48 h con doxorrubicina, una tendencia que fue reproducible sólo en esta línea. En cuanto a la sensibilidad frente a los fármacos se pudo ver que la línea NCI-H292 es una de las más sensibles, especialmente a taxol y doxorubicina y las células LSPG8G y NCI-H460 tienden a ser las más resistentes, especialmente a doxorubicina. Los valores de las CI50 calculados para todas las líneas se muestran en la figura 4.
Análisis de amplificación génica (dosis génica)
Empleando el método de doble delta Ct, se calculó la dosis génica para c- MYC, MYCN, MYCL, EGFR, AKT-2, ERBB2, PIK3CA y c-REL para un panel de líneas celulares de origen tumoral pulmonar. Para validar el uso de este método previamente se verificó que la eficiencia de amplificación de los genes problema fuera comparable a la eficiencia del gen control (ACTB) (Perdomo et al., 2012).
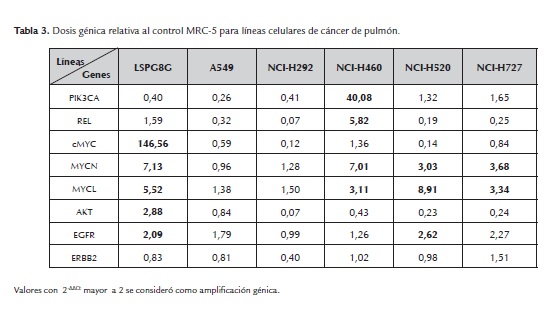
Los resultados mostraron que ningún gen se encuentra amplificado en las células A549 y NCI-H292, por el contrario un claro aumento en el número de copias fue observado para las líneas LSPG8G, NCI-H460, NCI-H520, NCI-H727, siendo común la amplificación de MYCN y MYCL en estas líneas. El mayor cambio en la dosis génica se registró para el gen cMYC en las células LSPG8G y para el gen PIK3CA en las células NCI-H460. Coincidencialmente en estas dos últimas líneas se observó el mayor número de genes amplificados y mostraron ser de las más resistentes del panel. En la tabla 3 se muestra la dosis génica calculada para todas las líneas celulares.
Discusión
Los análisis de quimiosensibilidad muestran que las líneas celulares responden diferente frente a los fármacos. Bajo nuestras condiciones de ensayo, algunas líneas fueron muy sensibles a doxorrubicina (CI50 < 1 µM), otras mostraron una sensibilidad intermedia frente taxol (CI50 entre 1 y 10 µM) y la mayoría fueron resistentes a 5-fluoracilo y cisplatino (CI50 > 10 µM) (Noro et al., 2006; Søndergaard et al., 2010).
Estas diferencias de sensibilidad y en general la respuesta in vitro frente a un fármaco o un xenobiótico, puede ser el resultado de una interacción entre diferentes variables, entre estas; las características de la línea, el mecanismo de acción del fármaco y las condiciones de ensayo. Dentro de las características de la línea vale la pena resaltar la influencia que pueden tener las alteraciones genéticas o epigenéticas que presentan las células, su origen tumoral primario, tipo histológico, los tiempos de duplicación poblacional y hasta el número de pases en el que se encuentre la línea al momento del análisis.
Al comparar los valores de CI50 calculados en este trabajo con los publicados en la literatura, se observa que estos valores son más altos para algunas células. También fue evidente que las CI50 difieren entre estudios, aunque se utilice la misma línea y el mismo fármaco. Al parecer la densidad celular, el tiempo de exposición, el vehículo en el que se disuelve el compuesto y el ensayo que se use para cuantificar el efecto citotóxico (XTT, MTT, Resazurina, ( 3H) timidina, ensayo luminiscencia de ATP) también pueden influir sobre la determinación de los valores de CI50 (Zumpe et al., 2010; Ulukaya et al., 2008). Para el paclitaxel por ejemplo, algunas investigaciones muestran que este fármaco ejerce su actividad citotóxica sobre las células A549 en rangos del orden de nanomolar (Buey et al., 2005; Breen et al., 2008), otros trabajos reportan CI50 del orden micromolar (Ulukaya et al., 2008). Por otro lado, Liebmann et al., (1993) demuestran que la actividad citotóxica del paclitaxel es menor sobre A549 cuando las células son tratadas con el compuesto disuelto en Cremophor EL® (diluente empleado en la formulación clínica) y mayor cuando está disuelto en DMSO; en contraste, Georgiadis et al., (1997) demuestran que el vehículo no influye sobre la actividad citotóxica del paclitaxel. En nuestro estudio se empleó la formulación clínica de paclitaxel (disuelto Cremophor EL) y se obtuvieron valores de CI50 del orden (µM) para todas las líneas celulares.
La respuesta bifásica frente a un fármaco ha sido discutida previamente para varias líneas celulares (Yeung et al., 1999), sin embargó la tendencia de la curva dosis respuesta observada para células A549 tratadas con doxorrubicina no se encontró reportada previamente. Para el taxol se ha descrito que este comportamiento bifásico es un indicativo de que el fármaco puede estar ejerciendo su actividad citotóxica por dos mecanismos diferentes; apoptosis a bajas concentraciones y necrosis a altas concentraciones (Yeung et al., 1999).
La amplificación génica es uno de los cambios genéticos más comunes que ocurre en las neoplasias humanas. En tumores y en líneas celulares se ha detectado con frecuencia un aumento en la dosis génica de genes que codifican para proteínas que participan en la inhibición de la apoptosis, favorecen la proliferación y/o estimulan el crecimiento celular. También se ha descrito que la magnitud del aumento en el número de copias puede depender del origen primario (colon, seno, pulmón, estomago, etc), del tipo histológico y que puede estar correlacionada con la agresividad de tumor (Knuutila et al., 1998).
En este estudió las líneas celulares LSPG8G y NCI-H460, exhibieron el mayor número de genes amplificados e interesantes cambios en el número de copias para los genes cMYC y PIK3CA. Coincidencialmente las dos líneas fueron derivadas del mismo tipo histológico y mostraron los rangos más altos de quimioresistencia, especialmente a doxorubicina.
El oncogen c-MYC es un miembro de la familia MYC, relacionado funcionalmente con la síntesis de ADN (Mørkve et al., 1992) y la regulación de la expresión de genes involucrados en crecimiento celular (Mitani et al., 2001). Se ha visto amplificado en leucemias y linfomas (Mørkve et al., 1992), en cáncer de pulmón de célula pequeña y carcinoma escamocelular, entre otros tumores (Mitani et al., 2001; Carrillo et al., 2009; Alvarez et al., 2012). En nuestro estudio este gen se vio claramente amplificado en las células LSPG8G, una línea derivada desde un tumor anaplásico de célula grande, un tipo histológico, altamente indiferenciado y extremadamente agresivo (Pardo et al., 2009) Los otros dos miembros de la familia MYC, los genes MYCL y MYCN mostraron un modesto cambio en el número de copias en cuatro de las seis líneas evaluadas. Estos genes se ha visto amplificados en neuroblastoma, retinoblastoma y también en muestras de cáncer de pulmón (Lu et al., 2003; Alvarez et al., 2012).
El gen PIK3CA codifica para una de las subunidades de la proteína PI3K y se ha reportado amplificado en tumores del tracto urinario, cáncer de ovario, cérvix y cabeza y cuello (Frendi et al., 2009). La ganancia en el número de copias para este gen, se ha correlacionado con aumentos en la expresión de PI3K y respuesta a fármacos (Heinonen et al., 2008).
Los genes EGFR y ERBB2 son dos miembros de la familia ERBB, que funcionan como receptores transmembrana y que junto con sus ligandos participan activamente en la estimulación del crecimiento y proliferación celular (Herbst et al., 2008). El aumento en el número de copias para EGFR ha sido reportado para gliomas, cáncer de seno y de vejiga, también hay algunos reportes para cáncer de pulmón de célula pequeña (Knuutila et al., 1998). La amplificación de EGFR ha sido relacionada con la respuesta a erlotinib y gefitinib, debido a que son fármacos que se asocian al dominio intracelular de este receptor (Pao et al., 2004). En nuestro trabajo este gen se encontró amplificado en las células NCI-H520, una línea celular derivada de un carcinoma escamocelular. Para ERBB2 se ha descrito que se encuentra amplificado en cáncer de seno, ovario, estómago y colon (Knuutila et al., 1998), en nuestro estudio este gen no se vio amplificado.
AKT es un gen serina/treonina que funciona como efector de la ruta de señalización activada por PIK3CA, regula procesos celulares que controlan tamaño, crecimiento y proliferación celular y se ha encontrado amplificado en cáncer de seno y ovario (Cheng et al., 1992; Bellacosa et al., 1995). En cuanto a su relación con la sensibilidad a fármacos, se ha reportado que líneas celulares de pulmón, ovario y gliomas resistentes a cisplatino, activan constitutivamente el gen AKT y sugieren que esta activación puede ser un posible mecanismo de resistencia a cisplatino (Huang & Hung, 2009). En nuestros resultados las células en general muestran ser resistentes a cisplatino, sin embargo solo la línea LSPG8G muestra un ligero aumento en la dosis génica.
c-Rel es un importante factor de transcripción de la familia cRel/NF-kB, participa activamente en la expresión de genes involucrados en el desarrollo, proliferación y supervivencia de células linfoides (Houldsworth et al., 1996). El aumento en su dosis génica se ha asociado con el desarrollo de linfomas (Gilmore et al., 2004) y algunos tumores sólidos (Romieu-Mourez et al., 2003). En este trabajo se registró un aumento en el número de copias relativas de este gen para la línea NCI-H460, sin embargo no se encontraron otros reportes que soporten este resultado.
Conclusiones
Los resultados obtenidos en este trabajo indican que la línea NCI-H292 es una de las más sensibles a taxol, cisplatino y doxorrubicina y la líneas LSPG8G y NCI-H460 son de las más resistentes, especialmente a doxorubicina. Los análisis moleculares sugieren que la amplificación génica puede ser una alteración frecuente en células resistentes, sin embargo otros análisis deben realizarse para probar esta hipótesis.
Referencias bibliográficas
1 Ari, F., Ikitimur, E., Ulukayama, E. 2010. The ATP Assay, but not the MTT assay, Detects Further Cytotoxicity of the Combination of Anthracycline-based Therapy with Histone Deacetylase Inhibitor (Valproic Acid ) in Breast Cancer Cells. Turkish Journal of Biochemistry. 35 (4): 293-299. [ Links ]
2 Albertson, D. 2006. Gene Amplification in Cancer. Trends in Genetics. 22 (8): 447-455. [ Links ]
3 Alvarez, A., Perdomo, S., Palacios, D., Cariillo, E., Garcia, L., Camacho, F., Ojeda, P., Aristizabal F. 2012. Detection of Gene Dosage in Circulating Free Plasma DNA as Biomarker for Lung Cancer. Journal of Cancer Therapy. 3: 343-351. [ Links ]
4 Bellacosa, A., De Feo, D., Godwin, A. K., Bell, D. W., Cheng, J. Q., Altomare, D. A., et al. 1995. Molecular alterations of the AKT2 oncogene in ovarian and breast carcinomas. International Journal of Cancer. 64: 280-285. [ Links ]
5 Breen, L., Murphy, L., Keenan, J., Clynes, M. 2008. Development of Taxane Resistance in a Panel of Human Lung Cancer Cell Lines. Toxicology in vitro. 22:1234-1241. [ Links ]
6 Buey, R., Barasoain, I., Jackson, E., Meyer, A., Giannakakou, P., Paterson, I., Mooberry, S., Andreu, J., Díaz J. 2005. Microtubule Interactions with Chemically Diverse Stabilizing Agents: Thermodynamics of Binding to the Paclitaxel Site Predicts Cytotoxicity. Chemistry & Biology. 12: 1269-1279. [ Links ]
7 Cappuzzo, F., Varella-Garcia, M., Shigematsu, H., Domenichini, I., Bartolini, S., Ceresoli, G.L. Rossi, E., et al. 2005. Increased HER2 Gene Copy Number Is Associated with Response to Gefitinib Therapy in Epidermal Growth Factor Receptor-positive Non-small-cell Lung Cancer Patients. Journal of Clinical Oncology. 23 (22): 5007-5018. [ Links ]
8 Carrillo, E., Arias, Y., Perdomo, S., Aristizábal, F., Ojeda, P., Palacios, D.M. 2009. Oncogene Amplification as Tumor Marker in a Group of Colombian Lung Cancer Patients. Colombia Medica. 40: 148-157. [ Links ]
9 Cheng, J., Godwin, A., Bellacosa, A., Taguchi, T., Franke, T., Hamilton, T., Tsichlis P, Testa J. 1992. AKT2, a putative oncogene encoding a member of a subfamily of protein-serine/threonine kinases, is amplified in human ovarian carcinomas. Proceedings of the National Academy of Sciences of the United States of America. 89: 9267-9271. [ Links ]
10 Frendi A., Khabir A., Mnejja W., Al E. 2009. PIK3CA amplification is predictive of poor prognosis in Tunisian patients with nasopharyngeal carcinoma. Cancer Science. 100: 2034-2039. [ Links ]
11 Georgiadis, S., Gazdar, F., Russell, K., Johnso, E. 1997. Paclitaxel Cytotoxicity Against Human Lung Cancer Cell Lines Increases with Prolonged Exposure Durations. Clinical Cancer Research. 3: 449-454. [ Links ]
12 Gilmore, T., Kalaitzidis, D., Liang, M., Starczynowski, D. 2004. The c-Rel Transcription Factor and B-cell Proliferation: a Deal with the Devil. Oncogene. 23 (13) : 2275-86. [ Links ]
13 Heinonen, H., Nieminen, A., Saarela, M., Kallioniemi, A., Klefström, J., Hautaniemi, S., Monni, O. 2008. Deciphering Downstream Gene Targets of PI3K/mTOR/p70S6K Pathway in Breast Cancer. BMC Genomics. 9 : 348. [ Links ]
14 Herbst, R., Heymach, J., Lippman. S. 2008. Lung Cancer. The New England Journal of Medicine. 359 (13): 1367-80. [ Links ]
15 Houldsworth, J., Mathew, S., Rao, P., Dyomina, K., Louie, D., Parsa, N., Offit, K., Chaganti, R. 1996. REL Proto-oncogene Is Frequently Amplified in Extranodal Diffuse Large Cell Lymphoma. Blood. 87 (1) : 25-29. [ Links ]
16 Huang, C., Yang L., Li, Z., Yang. J., Zhao J, Dehui X et al. 2007. Detection of CCND1 Amplification Using Laser Capture Microdissection Coupled with Real-time Polymerase Chain Reaction in Human Esophageal Squamous Cell Carcinoma. Cancer Genetics Cytogenetics. 175(1):19-25. [ Links ]
17 Huang, W., Hung M. 2009. Induction of Akt Activity by Chemotherapy Confers Acquired Resistance. Journal of the Formosal Medical Association. 108 (3): 180-194. [ Links ]
18 Knuutila, S., Bjorkqvist, A., Autio, K., Tarkkanen, M., Wolf, M., Monni, O, et al. 1998. DNA Copy Number Amplifications in Human Neoplasms. American Journal of Pathology. 152 (5): 1107-1123. [ Links ]
19 Liebmann, J., Cook, J., Lipschultz, C., Teague, D., Fisher, J., Mitchell, J. 1993. Cytotoxic studies of paclitaxel (Taxol) in human tumour cell lines. British Journal of Cancer. 68(6):1104-1109. [ Links ]
20 Lu, X., Pearson, A., Lunec. J. 2003. The MYCN Oncoprotein as a Drug Development Target. Cancer Letters. 197 : 125-130. [ Links ]
21 Miller, Y. 2005. Pathogenesis of Lung Cancer: 100 Year Report. American Journal of Respiratory Cell and Molecular Biology. 33 (3): 216-23. [ Links ]
22 Mitani, S., Kamata, H., Fujiwara, M., Aoki, N., Tango, T., Fukuchi, K., Oka, T. 2001. Analysis of c-MYC DNA Amplification in Non-small Cell Lung Carcinoma in Comparison with Small Cell Lung Carcinoma Using Polymerase Chain Reaction. Clinical and Experimental Medicine. 2: 105-111. [ Links ]
23 Mørkve, O., Halvorsen, O., Stangeland, L., Gulsvik, A., Laerum. O. 1992. Quantitation of Biological Tumor Markers (p53, C-myc, Ki-67 and DNA Ploidy) by Multiparameter Flow Cytometry in Non-small-cell Lung Cancer. International Journal of Cancer. 52 (6): 851-855. [ Links ]
24 Noro, R., Gemma, A., Kosaihira, S., Kokubo, Y., Chen, M., Seike, M., Kataoka, K., et al. 2006. Sensitive Lung Cancer Cell Lines Show Phosphorylation of Akt Without Ligand Stimulation. BMC Cancer. 6 (6): 277. [ Links ]
25 O"Brien, J., Wilson, I., Orton, T., Pognan F. 2000. Investigation of the Alamar Blue (resazurin) Fluorescent Dye for the Assessment of Mammalian Cell Cytotoxicity. European Journal of Biochemistry. 267 (17) : 5421-5426. [ Links ]
26 Pao, W., Miller, V., Zakowski, M., Doherty, J., Politi, K., Sarkaria, I., Singh, B. et al. 2004. EGF Receptor Gene Mutations Are Common in Lung Cancers from "Never Smokers" and Are Associated with Sensitivity of Tumors to Gefitinib and Erlotinib. Proceedings of the National Academy of Sciences of the United States of America. 101 (36): 13306-13311. [ Links ]
27 Pardo, J., Martinez-Peñuela, A., Sola, J., Panizo, A., Gúrpide, A., Martinez-Peñuela, J., Lozano, M. 2009. Large Cell Carcinoma of the Lung: An Endangered Species? Applied Immunohistochemistry & Molecular Morphology. 17 (5): 383-392. [ Links ]
28 Perdomo, S., Morantes, J., Aristizábal, F. 2012. Development and Validation of a TaqMan PCR Assay for the Gene Dosage Quantification in Cancer. Revista Colombiana De Ciencias Químico Farmaceúticas. 42: xx-xx. En prensa. [ Links ]
29 Prieto, S., Aristizábal, F. 2009. Perfil De Sensibilidad De HEpG2 Como Modelo Para Evaluación De Actividad Citotóxica de Xenobióticos Bioactivados via CYP450." Vitae. 16 (2): 219-227. [ Links ]
30 Romieu-Mourez, R., Kim, D., Shin, S., Demicco, E., Landesman-Bollag, E., Seldin, D., Cardiff, R., Sonenshein, G. 2003. Mouse Mammary Tumor Virus C-rel Transgenic Mice Develop Mammary Tumors. Molecular And Cellular Biology. 23 (16): 5738-5754. [ Links ]
31 Santarius, T., Shipley, J., Brewer, D., Stratton, M., Cooper, C. 2010. A Census of Amplified and Overexpressed Human Cancer Genes. Nature Reviews Cancer. 10: 59-64. [ Links ]
32 SKarda, J., Hajdúch, M., Vítezslav K., 2008. "Drug Resistance in Lung Cancer." Cancer Therapy. 6: 377-388. [ Links ]
33 Starczynowski, D., Lockwood, W., Deléhouzée, S., Chari, R., Wegrzyn, J., Fuller, M., Tsao M. et al. 2011. TRAF6 Is an Amplified Oncogene Bridging the RAS and NF-kB Pathways in Human Lung Cancer. The Journal of Clinical Investigation. 121 (10): 4095-4105. [ Links ]
34 Sumantran, V. 2011. Cellular Chemosensitivity Assays: An Overview. En: Cancer Cell Culture Methods in Molecular Biology. Portsmouth UK, Humana Press. p. 437. [ Links ]
35 Søndergaard, J., Nazarian, R., Wang, Q., Guo, D., Hsueh, T., Mok, S., Sazegar, H., et al. 2010. Differential Sensitivity of Melanoma Cell Lines with BRAFV600E Mutation to the Specific Raf Inhibitor PLX4032. Journal of Translational Medicine. 8: 39. [ Links ]
36 Ulukaya, E., Ozdikicioglu, F., Oral, A., Demirci, M. 2008. The MTT Assay Yields a Relatively Lower Result of Growth Inhibition Than the ATP Assay Depending on the Chemotherapeutic Drugs Tested. Toxicology in vitro. 22 (1): 232-239. [ Links ]
37 Yasui, K., Mihara, S., Zhao, C., Okamoto, H., Saito-Ohara, F., Tomida, A., Funato, T., Yokomizo, A., Naito, S., Imoto, I., Tsuruo, T., Inazawa, J. 2004. Alteration in Copy Numbers of Genes as a Mechanism for Acquired Drug Resistance Drug Resistance. Cancer Research. 64: 1403-1410. [ Links ]
38 Yeung, T., Germond, C., Chen, X., Wang, Z. 1999. The Mode of Action of Taxol: Apoptosis at Low Concentration and Necrosis at High Concentration. Biochemical and Biophysical Research Communications. 263 (2): 398-404. [ Links ]
39 Zumpe, C., Bachmann, C., Metzger, A., Wiedemann, N. 2010. Comparison of Potency Assays Using Different Read-out Systems and Their Suitability for Quality Control. Journal of Immunological Methods. 360 (1-2) : 129-140. [ Links ]