Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Biotecnología
Print version ISSN 0123-3475
Rev. colomb. biotecnol vol.15 no.1 Bogotá Jan./June 2013
ARTÍCULO DE INVESTIGACIÓN
Nueva alternativa para la micropropagación en inmersión temporal del cultivar de plátano vianda "INIVITPV-2011"(AAB)
New alternative for micropropagation in temporary immersion system of plantain cultivar "INIVITPV-2011" (AAB).
Milagros Basail Pérez1,2 , Victor Medero Vega1 , Marlenys Torres Delgado1 , Jorge López Torres1 , Arletys Santos Pino1 , Aymé Rayas Cabrera1 , Maricel Bauta Toledo1 , Yoel Beovidez García1 y Alexi Ortega Ortiz1.
1Instituto Nacional de Investigaciones en Viandas Tropicales (INIVIT), Apartado 6, Santo Domingo CP. 53000, Villa Clara, Cuba.
2MSc. Autor para correspondencia: e-mail: sit.biotec@inivit.cu. Cuba.
Recibido: marzo 19 de 2013 Aprobado: junio 24 de 2013
Resumen
El trabajo fue desarrollado en el Laboratorio de Biotecnología Vegetal del Instituto de Investigaciones en Viandas Tropicales (INIVIT) con el objetivo de incrementar el coeficiente de multiplicación en el cultivar de plátano vianda "INIVITPV-2011" (AAB) en el Sistema de Inmersión Temporal (SIT). Se estudiaron diferentes tiempos de inmersión (10, 20 (control) y 30 minutos) y frecuencias de inmersión (3, 6 (control) y 8 horas) en frascos Nalgene de 10 L de capacidad, se estudió además el volumen de medio de cultivo por explante (20, 40 (control) y 60 ml de medio de cultivo/explante), así como el tiempo de subcultivo (15, 18, 21 (control) y 25 días) y la densidad de explantes por frasco (20, 40 (control), 60 y 80 explantes/frasco de cultivo). Se utilizó el medio de cultivo de multiplicación MS suplementado 2,0 mg.L-1 de 6-BAP; 3,5 mg.L-1de AIA; 30,0 g.L-1 de sacarosa; 10,0 mg.L-1 de ácido ascórbico. Los resultados obtenidos permitieron establecer una metodología para la micropropagación en el Sistema de Inmersión Temporal del cultivar de plátano vianda "INIVITPV-2011" (AAB) la cual consistió en utilizar un tiempo de inmersión de 10 minutos con una frecuencia cada 3 horas, es decir, 8 inmersiones al día, además para cada frasco de 10 L se inocularon 60 explantes y la renovación con 3600 ml de medio de cultivo y un tiempo de cultivo de 18 días permitió alcanzar la mayor productividad del material en fase de multiplicación. Estos resultados, utilizando el Sistema de Inmersión Temporal permitieron establecer una metodología eficiente para la micropropagación del cultivar de plátano vianda "INIVITPV-2011" (AAB).
Palabras clave: propagación in vitro, tiempo, frecuencia, inmersión, multiplicación.
Abstract
This work was developed at the Plant Biotechnology Laboratory from the Research Institute of Tropical Root and Tuber Crops (INIVIT) in order to increase the multiplication coefficient in plantain cultivar "INIVITPV-2011" (AAB) in Temporary Immersion Systems (TIS). Different immersion times (10, 20 (control) and 30 minutes) and immersion frequencies (3, 6 (control) and 8 hours) in 10 L Nalgene flasks, and culture medium volume per explants (20, 40 (control) and 60 ml culture medium / explants) were studied, as well as, subculture time (15, 18, 21(control) and 25 days) and explants density per flask (20, 40 (control), 60 and 80 explants / culture flask). The multiplication culture medium MS supplemented with 2.0 mg.L-1 6-BAP, 3.5 mg.L-1 IAA, 30.0 gL-1 sucrose, 10.0 mg.L-1 ascorbic acid was used. Results obtained allowed to establish a methodology for micro-propagation of plantain cultivar "INIVITPV-2011" (AAB) in temporary immersion system, which consisted of using a 10 minute immersion time with 3 hour frequency (8 immersions per day). Besides, 60 explants were inoculated in each 10 L flask, and the renewal with 3600 ml culture medium and 18 day culture time allowed to obtain the highest productivity in the multiplication stage. These results, using the temporary immersion system allowed to establish a method for micro-propagation of plantain cultivar "INIVITPV-2011" (AAB).
Key words: in vitro propagation, time, frequency, immersion, multiplication.
Introducción
El cultivo del plátano (Musa spp) es una importante fuente de alimento para una gran parte de la población mundial, localizada principalmente en países subdesarrollados de Asia, África, América Central y del Sur, la producción anual se estimó en 43,4 millones de toneladas y los rendimientos en 73,28 ton.ha-1 (FAO, 2010).
En Cuba los plátanos tipo vianda constituyen un cultivo estratégico de elevada prioridad dentro del programa alimentario nacional debido a su capacidad de producir todos los meses del año, su elevado potencial de rendimiento, arraigados hábitos de consumo y diversidad de usos (Rodríguez, 2008).
A pesar de ocupar el cuarto lugar entre las principales fuentes de alimentos (después del arroz, la leche y el trigo), son fuente importante de carbohidratos (35%), proteínas (1,2%) y fibras (6-7%); adicionalmente aportan potasio, magnesio, fósforo, calcio y vitamina A y C (Kodym y Zapata, 1999).
Dentro de las técnicas de cultivo de tejidos, la micropropagación es una alternativa desarrollada para la producción a gran escala de plantas, que ha sido utilizada con éxito desde los años 60 del siglo pasado, pero sus principales desventajas son: bajos coeficientes de multiplicación, alto costo por mano de obra y la escasa posibilidad de automatización que brinda el proceso (Kitto, 1997).
En los últimos tiempos se han desarrollado investigaciones sobre la automatización en la propagación de plantas, que incluyen el diseño de nuevos sistemas para la micropropagación, ya que reducen el costo por explantes, permiten una mayor optimización biológica por los altos coeficientes de multiplicación que se obtienen y un mejor comportamiento de las vitroplantas ex vitro por mayor metabolismo autotrófico durante la fase in vitro (Aitcken-Christie et al., 1995).
Los Sistemas de Inmersión Temporal (SIT) además de solucionar las dificultades de los cultivos en medios líquidos estáticos, abren la posibilidad de semiautomatizar algunas etapas del cultivo in vitro (Alvard et al., 1993), permiten mayor facilidad de escalado y aumentan la eficiencia biológica y productiva del material propagado (Jiménez et al., 1999; Castro, 2001). Al mismo tiempo la morfología y el comportamiento fisiológico de los cultivos en los Sistemas de Inmersión Temporal son muy semejantes a los que presentan las plantas en condiciones ex vitro, lo que permite una mayor tasa de supervivencia (Escalona et al., 1999).
De esta forma, el cultivo en Inmersión Temporal puede constituir una alternativa de micropropagación a corto plazo, mientras, a largo plazo se venzan obstáculos biológicos que permitan la obtención eficiente de plantas y embriones somáticos en biorreactores (Escalona et al., 1999).
Teniendo en cuenta lo anterior el presente trabajo se realizó con el objetivo de incrementar el coeficiente de multiplicación en el cultivar de plátano vianda "INIVITPV-2011" (AAB) utilizando el Sistema de Inmersión Temporal.
Materiales y métodos
La investigación se realizó en el laboratorio de Cultivos de Tejidos de plantas del Instituto de Investigaciones en Viandas Tropicales (INIVIT); ubicado en Santo Domingo, Villa Clara, Cuba.
Material vegetal
Como material vegetal se utilizaron plantas de plátano vianda "INIVITPV-2011" (AAB) (Musa spp., AAB) cultivadas in vitro, en fase de multiplicación con tres subcultivos en medio de cultivo semisólido. Estas procedían del banco de germoplasma de plátanos y bananos del Instituto de Investigaciones en Viandas Tropicales (INIVIT).
Medios de cultivo
En este experimento se utilizó el medio de cultivo de multiplicación MS suplementado 2,0 mg.L-1 de 6-BAP; 3,5 mg.L-1de AIA; 30,0 g.L-1 de sacarosa; 10,0 mg.L-1 de ácido ascórbico (López et al., 2010). Para la fase de establecimiento y multiplicación hasta tercer subcultivo se utilizó como agente gelificante el agar-agar a razón de 4.5 g.L-1. En los frascos de cultivo de capacidad 200 ml de volumen total se dosificó un volumen de 30 ml de medio de cultivo semisólido (fase de establecimiento y multiplicación) y en los Sistemas de Inmersión Temporal el volumen de medio de cultivo cambio acorde al diseño de los distintos experimentos.
Condiciones de cultivo in vitro
Luz artificial: se utilizó un fotoperíodo de 16 horas de luz y una densidad de flujo de fotones fotosintéticos (DFFF) de 62-68 µmol m-2 s-1, temperatura 27±2°C.
Los controles utilizados para los diferentes ensayos corresponden a condiciones establecidas previamente en el Instituto de Investigaciones de Viandas Tropicales para otros cultivos por Basail y Santos (2010)
Componentes del Sistema de Inmersión Temporal
Este tipo de sistema de cultivo estuvo compuesto por dos frascos de cultivo tipo Clearboys (Compañía Nalgene, E.U.A) de 10,0 L de capacidad, uno para el crecimiento de los brotes y el otro como reservorio de medio de cultivo. Estos frascos de cultivo se conectaron entre sí por una manguera de silicona de seis milímetros de diámetro mediante conectores que atravesaron la tapa. En la parte interna se colocó una manguera, la cual descendió hasta el fondo en ambos recipientes. El medio de cultivo circuló de un frasco de cultivo a otro en dependencia de la apertura o cierre de dos electroválvulas de tres vías, las cuales estaban conectadas a un temporizador programable para determinar el tiempo y frecuencia de la inmersión. A la entrada de los frascos de cultivo se colocaron filtros hidrofóbicos (0,22 µm, MIDISART 2000, de la compañía SARTORIUS) para garantizar la esterilidad del aire. La presión del aire de 2,0 atm proveniente de un compresor que fue regulada por un manómetro.
Efecto del tiempo y frecuencia de inmersión en el Sistema de Inmersión Temporal
Efecto del tiempo de inmersión
Para estudiar el tiempo de inmersión en la fase de multiplicación se estudiaron tres tratamientos (10, 20 (control, y 30 minutos). En este experimento se utilizó el medio de cultivo de multiplicación MS suplementado 2,0 mg.L-1 de 6-BAP; 3,5 mg.L-1de AIA; 30,0 g.L-1 de sacarosa; 10,0 mg.L-1 de ácido ascórbico. El volumen de medio de cultivo en la fase de multiplicación fue de 2000 ml por Sistema de Inmersión Temporal. La frecuencia de inmersión fue de cuatro inmersiones por día (cada seis horas). Las evaluaciones se realizaron a los 21 días de cultivo y se emplearon 40 explantes por frasco de cultivo y tres repeticiones por tratamiento (Ventura et al., 2002).
Efecto de la frecuencia de inmersión
Con el objetivo de evaluar el efecto de la frecuencia de inmersión en la fase de multiplicación se estudiaron tres frecuencias de inmersión, cada 3.0, 6.0, y 8.0 horas por día, con el mejor tiempo de inmersión obtenido como resultado en las variables en el experimento anterior (10 minutos de inmersión).
Se utilizaron las mismas condiciones del experimento efecto del tiempo de inmersión, así como el medio de cultivo. Se adicionaron 2000 ml de medio de cultivo por frasco.
Determinación del volumen de medio de cultivo en el Sistema de Inmersión Temporal
Para determinar el efecto del volumen de medio de cultivo por explante se utilizaron tres tratamientos (20, 40 (control) y 60 ml/explante). Se utilizó el mejor tiempo y frecuencia de inmersión obtenido como resultado para las variables evaluadas en los experimentos anteriores.
Determinación del momento de subcultivo en el Sistema de Inmersión Temporal.
Se constituyeron cuatro tratamientos: 15; 18; 21 (control) y 25 días de cultivo. Se emplearon las mismas condiciones de los experimentos anteriores así como el mejor volumen de medio de cultivo obtenido.
Determinación de la densidad de explantes por frasco
A partir de los resultados obtenidos en el Sistema de Inmersión Temporal con condiciones predeterminadas por las experiencias en el manejo de los mismos, se estudió la densidad de inóculo con el objetivo de mejorar las condiciones de cultivo, así como la calidad del proceso. Se evaluó la influencia de cuatro densidades de inóculo: 20; 40 (control, utilizado por otros investigadores); 60 y 80 explantes por frasco y un volumen de medio de cultivo por batería de 1200 ml; 2400 ml; 3600 ml y 4800 ml en la producción de explantes Para determinar la densidad de inóculo se utilizó el mejor resultado obtenido en el experimento anterior así como las condiciones experimentales.
Se realizaron tres repeticiones por tratamiento y se evaluó:
- Coeficiente de multiplicación (unidades). Se determinó por el número de brotes finales con respecto al número de brotes iniciales.
- Altura de los brotes de yemas axilares (cm). Se realizó con una regla graduada y se midió desde la base del pseudotallo hasta la inserción de la primera hoja.
Grado de oxidación según escala de Novak et al. (1994)
Grado 0: no hubo oxidación, coloración del explante de blanco-amarillo crema.
Grado 1: Incipiente coloración carmelita sin llegar a la necrosis del tejido.
Grado 2: 25% de tejido necrótico en la base del explante.
Grado 3: 50% de tejido necrótico en la base del explante.
Grado 4: 75% de tejido necrótico en la base del explante con penetración.
Grado 5: 100% de tejido necrótico en la base del explante con penetración y se necesitan cortes profundos para lograr que la asimilación de nutrientes sea efectiva. - Diámetro del pseudotallo de los brotes de yemas axilares (cm). Se realizó con el auxilio de una regla graduada y se midió el diámetro de la base del pseudotallo.
- Número de hojas de los brotes de yemas axilares (unidades). Se contaron las hojas que estaban abiertas.
Procesamiento estadístico
Con los criterios de estadística descriptiva se realizaron las tablas que expresan los resultados procesados con estadística inferencial paramétrica (análisis de varianza de clasificación simple). La comparación múltiple de media se realizó según Tukey cuando se encontró homogeneidad de varianza, (Lerch, 1977). Se utilizó el paquete estadístico MSTAT-C de la Universidad de Micchigan (Bricker, 1993, citado por Guzmán y Castaño, 2002).
Resultados y discusión
Efecto del tiempo y frecuencia de inmersión en el Sistema de Inmersión Temporal
Efecto del tiempo de inmersión
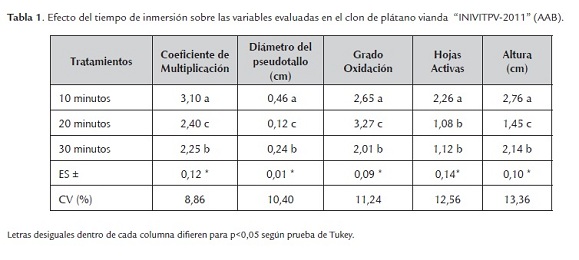
El tiempo de inmersión en el Sistema de Inmersión Temporal influyó de forma significativa. Con un tiempo de inmersión de 10 minutos y una frecuencia cada 6 horas (4 inmersiones al día) se alcanzaron los mejores resultados para las variables evaluadas (coeficiente de multiplicación (3,10), diámetro del pseudotallo (0,46), grado de oxidación (2,65), número de hojas activas (2,26) y altura del explantes (2,76) con diferencias significativas respecto al resto de los tratamientos (tabla 1).
Investigadores como Martre et al. (2001) han descrito que prolongados períodos de inmersión afectan el desarrollo del material vegetal a causa de un incremento de la hiperhidricidad y estrés oxidativo. Roels et al. (2005) cuando incrementaron el tiempo de inmersión de 12 minutos a 22 minutos de inmersión observaron que los brotes presentaron hiperhidricidad, inferior longitud y menor número de hojas.
El tiempo de inmersión es considerado un factor importante en la respuesta morfogenética del material vegetal a micropropagar. Al respecto, Escalona et al. (1999) en el cultivo de la piña (Ananas comosus (L) Merr.) encontró que con un tiempo de inmersión de dos minutos/hora y una frecuencia de tres horas se incrementó el coeficiente de multiplicación y por lo tanto se facilitó una mayor eficiencia en la asimilación de nutrientes por los explantes.
Dottin (2000) con el empleo de siete minutos de inmersión de los explantes obtuvo un elevado coeficiente de multiplicación (13,80) en el cultivo de la malanga (Xanthosoma sagittifolium (L) Schott) con respecto al clon de Malanga INIVITMC-2001 (10,45) en Sistema de Inmersión Temporal.
Lo anterior demuestra la necesidad de determinar el tiempo de inmersión para cada una de las especies y fases de cultivo en la micropropagación, pues del ajuste del tiempo de inmersión depende en gran medida la eficiencia del empleo de los Sistemas de Inmersión Temporal (Berthouly y Etienne, 2005; Escalona, 2006).
Efecto de la frecuencia de inmersión
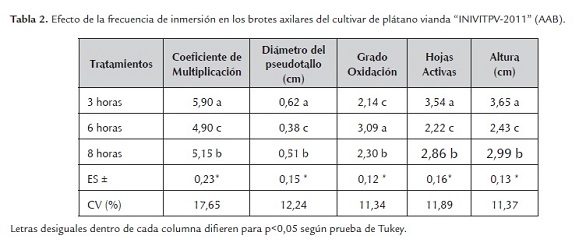
Al utilizar una frecuencia de 3 horas y 10 minutos de inmersión se obtienen los máximos valores para el coeficiente de multiplicación (5,90), diámetro del pseudotallo (0,62), número de hojas activas (3,54) y altura del explante (3,65) con diferencias significativas respecto al resto de los tratamientos excepto con el grado de oxidación donde se obtiene el menor valor (2,14) sin la presencia de brotes hiperhidratados (tabla 2).
Ha sido descrito por McAlister et al. (2005) y Mehrotra et al. (2007) que el tiempo y la frecuencia de inmersión influyen según el estado de desarrollo del material vegetal cultivado en la renovación de la atmósfera interna del frasco de cultivo, así como en la asimilación por el material vegetal de los nutrientes del medio de cultivo. Por lo que se hace necesario determinar el tiempo y la frecuencia de inmersión según la fase de cultivo para satisfacer los requerimientos del material vegetal (Escalona, 2006).
Colmenares y Jiménez (2003) en el banano "Gran Enano" (AAA) con inmersiones de dos minutos cada cuatro horas obtuvieron un coeficiente de multiplicación de 7,5 y para veinte minutos cada cuatro horas un índice de multiplicación de 8,0 en frascos de 10,0 L.
Castro (2001) señaló que durante la fase de multiplicación de brotes de Eucaliptus grandis, al emplear una frecuencia de 24 horas con una duración de tres minutos el número de brotes por explantes fue significativamente superior al obtenido con un minuto de inmersión, sin embargo, en ambos se observó la presencia de brotes hiperhidratados.
Quiala et al. (2006) en el cultivo de la caña santa (Cymbopogon citratus (D.C.) Staff) obtuvieron los mejores resultados para el peso fresco y el coeficiente de multiplicación al utilizar seis inmersiones por día (cada cuatro horas) en Sistemas de Inmersión Temporal de un litro de capacidad.
Por el contrario, Cabrera (2009) con las frecuencias de inmersión cada doce y veinticuatros horas, en el clon de ñame "Pacala Duclos" tuvieron menos posibilidades para asimilar nutrientes y acumular sustancias de reserva en comparación al tratamiento con cuatro inmersiones al día, en el cual los microtubérculos alcanzaron los mayores porcentaje de masa seca.
Los tiempos y frecuencias de inmersión que se ensayaron según las posibilidades de automatización, demostraron que con diez minutos de inmersión y tres horas empleados en los experimentos, se obtuvieron los mejores resultados en cuanto a la producción y calidad de los brotes.
Determinación del volumen de medio de cultivo en el Sistema de Inmersión Temporal
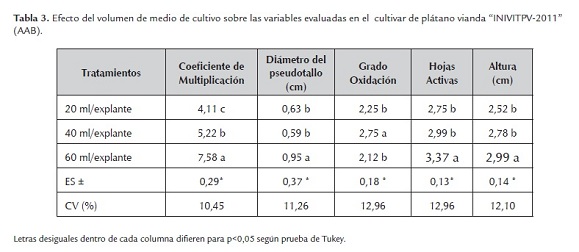
El volumen de medio de cultivo tuvo influencia sobre todas las variables evaluadas con la adición de 40 explantes por frasco de cultivo de 10 litros de volumen total. Los mayores valores en cuanto a las variables evaluadas se alcanzaron cuando se empleó una relación de 60 ml de medio de cultivo por explante obteniéndose los mejores resultados para el coeficiente de multiplicación (7,58), diámetro del pseudotallo (0,95), número de hojas activas (3,37) y altura del explantes (2,99) con diferencia significativa con los demás tratamientos no siendo así en cuanto al grado de oxidación donde se obtienen el menor valor (2,12) (tabla 3).
Berthouly y Etiennen (2005) han señalado que el volumen de medio de cultivo por explante utilizado en los frascos de cultivo de Inmersión Temporal es uno de los principales factores a evaluar para utilizar eficientemente este tipo de sistema de cultivo. Lo cual se evidencia en los resultados del presente trabajo para la formación de microtubérculos de ñame en Sistema de Inmersión Temporal.
Cabrera (2009) en la medida que incrementó el volumen de medio de cultivo por planta in vitro se incrementó el número y la masa fresca de los microtubérculos de ñame en el clon ´Pacala Duclos´. Los mejores resultados se alcanzaron al emplear un volumen de 60 y 90 mL de medio de cultivo por planta in vitro.
Berthouly y Etienne (2005) con 40 y 50 mL de medio de cultivo por explante obtuvieron los mejores resultados en la multiplicación de brotes de yemas axilares, debido a que se garantizó durante esta fase de cultivo un adecuado equilibrio entre las necesidades de nutrientes de los brotes de yemas axilares y la disponibilidad de los mismos en el medio de cultivo, en comparación con los volúmenes de 20 y 30 ml/explante de medio de cultivo. Lo que demuestra la necesidad de ajustar el volumen de medio de cultivo por explantes cultivados en el SIT, sin renovación del medio de cultivo.
Ziv (2005) al utilizar 1250 ml de medio de cultivo en biorreactores de 2500 ml de volumen total obtuvo un coeficiente de multiplicación (15,10) con la adición de 20 explantes de bananos.
Según Castro y González (2002) para lograr un mismo desarrollo en las técnicas de cultivo de tejidos es necesario proveer a las plantas con suficientes cantidades de nutrientes esenciales (incluyendo la sacarosa y carbono como fuentes de energía bajo condiciones heterotróficas y mesotróficas), de tal manera que los nutrientes no sean un factor limitante para la multiplicación en el desarrollo de las plantas. De acuerdo con los resultados obtenidos (Eucalyptus grandis Hill ex Maiden) demostraron que con el empleo de un volumen de 500 mL de medio de cultivo con 9 explantes se logró un coeficiente de multiplicación de 10,5 brotes y la mejor calidad de los brotes en términos de una mayor producción de masa seca. Es importante notar que en la medida que se incrementó el volumen de medio de cultivo se obtuvo un mayor coeficiente de multiplicación, sin embargo, la calidad de los brotes constituyó un factor importante, el cual permitió definir un volumen adecuado de medio de cultivo, que minimiza el estrés hídrico en los brotes, particularmente en las primeras etapas del cultivo.
Determinación del momento de subcultivo en el Sistema de Inmersión Temporal
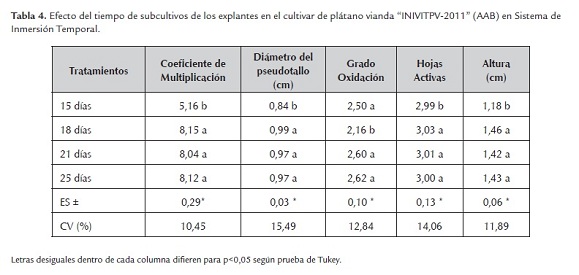
A partir de los 18 días de realizado el subcultivo hubo un incremento del coeficiente de multiplicación (8,15), diámetro del pseudotallo (0,99), número de hojas activas (3,03) y altura del explante (1,46), siendo este superior pero sin diferencias significativas en cuanto a los demás tratamientos pero sí con el de 15 días de cultivo. Al analizar la variable grado de oxidación se obtiene el menor resultado (2,16) con diferencias respecto al resto. Por lo tanto el tiempo de subcultivos es a partir de los 18 días, pues a través de este período de proliferación se puede obtener una mayor cantidad de explantes en un menor tiempo y el material está menos expuesto a riesgo de contaminación (tabla 4).
Williams (1995) demostró que hay diversos cultivares de boniato (Ipomoea batatas, Lam) que con poco período de proliferación comienza un incremento, alcanzando el número y calidad de los brotes deseados.
Escalona et al. (1999) para el cultivo de la piña demostraron que períodos prolongados promovieron la deformación de los brotes y por lo tanto afectaron el número de brotes que se podía obtener.
Los resultados alcanzados en el presente trabajo con el uso del Sistema de Inmersión Temporal durante un período de 18 días de incubación, constituye una vía efectiva para incrementar el coeficiente de multiplicación en el cultivar de plátano vianda "INIVITPV-2011" (AAB).
Determinación de la densidad de explantes por frasco
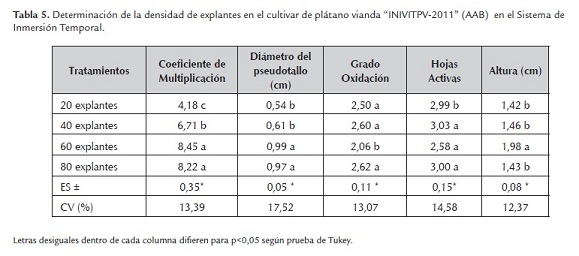
La densidad de explantes por frasco también influyó en las variables evaluadas (tabla 5), el mejor resultado se obtuvo con 60 explantes por frasco de 10 litros de capacidad, con los mayores valores numéricos en cuanto al coeficiente de multiplicación (8,45), diámetro del pseudotallo (0,99) y altura del explante (1,98) con diferencias significativas con todos los demás tratamientos excepto en cuanto al grado de oxidación (2,06) y el número de hojas activas (2,58) donde se obtienen el menor valor con diferencias significativas con los demás tratamientos.
A partir de los resultados obtenidos se seleccionó la densidad de 60 explantes por frasco de cultivo, pues hay una mayor asimilación de los nutrientes que componen el medio de cultivo y por tanto un mejor aprovechamiento de los frascos de cultivo Nalgene de 10 litros de capacidad (figura 1).
En el cultivar "Gran Enano" (AAA), empleando los Sistemas de Inmersión Temporal de 5 litros de capacidad, Albany (2001) señala que la variable que determina un incremento en el coeficiente de multiplicación, peso de los brotes, peso final y peso útil, es la densidad de inóculo, obteniendo los mejores resultados con 25 explantes.
Según Posada et al. (2003) los mejores resultados para la multiplicación de los cultivares de banano "FHIA 01" y "FHIA 18" se alcanzaron con la densidad de cinco explantes y una frecuencia de inmersión de tres veces durante un minuto cada 24 horas, en frascos de Inmersión Temporal (Sistema RITA).
Orellana (1998), puntualizó la necesidad de valorar experimentalmente la densidad de explantes por frasco porque este parámetro pudiera ocasionar deficiencias en el sistema; ya que una baja densidad ocasionaría pérdidas de espacio y de medio de cultivo, y con ello la subutilización de los recipientes; mientras que una alta densidad propicia un crecimiento limitado de los brotes e insuficiente proliferación con subcultivos más frecuentes.
De Feria et al. (1998), recomendaron para los recipientes de los Sistemas de Inmersión Temporal una densidad de 40 brotes de caña de azúcar, la cual les permitió obtener mayor coeficiente de multiplicación (10,92) y un peso promedio de 5,74 mg por brote.
Los experimentos desarrollados permitieron incrementar de forma significativa el coeficiente de multiplicación en el cultivar de plátano vianda "INIVITPV-2011" (AAB) en Sistema de Inmersión Temporal de 3,5 a 8,45 obteniendo plantas con características muy superiores a las obtenidas por el método de propagación convencional.
Conclusiones
Se estableció una metodología que permitió incrementar el coeficiente de multiplicación a 8,45 y la calidad del material micropropagado en el cultivar de plátano vianda "INIVITPV-2011" (AAB). A través del Sistema de Inmersión Temporal con un tiempo de 10 minutos de inmersión y una frecuencia cada 3 horas (8 inmersiones al día), con una densidad de inóculo de 60 explantes, un volumen de 3600 ml de medio de cultivo y un tiempo de cultivo de 18 días se garantizó el mejor comportamiento del material.
Referencias bibliográficas
1 Aitken-Christie, J., Davies, H.E., Kubota, C., Kosai, T. 1995. Automation in Plant Tissue Culture. General introduction overview: Automation and environment control in Plant Tissue Culture Kluwer, Academic Publisher, Dordrech, pp.1-19. [ Links ]
2 Albany, N. 2001. Efectos de retardantes del crecimiento en la micropropagación de bananos en medios de cultivo líquidos en agitador orbital y sistemas de inmersión temporal. Tesis para optar por el Grado Científico de Master en Biotecnología Vegetal. Instituto de Biotecnología de las Plantas. Santa Clara, pp. 34-36. [ Links ]
3 Alvard, D., Cote, F., Teisson, C. 1993. Comparison of methods of liquids medium culture for banana micropropagation. Effects of temporary inmersion of explants. Plant Cell Tissue and Organ Culture 2: 55-61. [ Links ]
4 Basail, M. y Santos, A. 2010. Comunicación personal. [ Links ]
5 Berthouly, M., Etienne, H. 2005. Temporary immersion systems: a new concept for use liquid medium in mass propagation. En: Hvoslef-Eide A. K. y Preil W. (Ed). Liquid Culture Systems or in vitro Plant Propagation, pp. 165-195. [ Links ]
6 Cabrera, M. 2009. Formación de microtuberculos de ñame (Dioscorea alata L.) clon "Pacala duclos" en Sistema de Inmersión Temporal como material vegetal de plantación. Tesis para aspirar al Grado Científico de Doctor en Ciencias Agrícolas. Universidad de Santa Clara, Instituto de Biotecnología de las Plantas. Cuba. [ Links ]
7 Castro, D. 2001. Propagación mixotrófica de Eucalipto grandis Hill ex Maide en biorreactores de inmersión temporal. Tesis para aspirar al Grado Científico de Doctor en Ciencias Agrícolas. Universidad de Ciego de Ávila, Centro de Bioplantas. Cuba. [ Links ]
8 Castro, D. R., González, J. 2002. Eucalyptus (Eucalyptus grandis Hill ex Maiden) micropropagation in a temporary immersion system. Agricultura sostenible, 62(1): 68-78. Colombia. [ Links ]
9 Colmenares, M., Jiménez, C. 2003. Multiplicación in vitro Musa spp mediante el sistema de inmersión temporal. www.revfacagronluz.org.ve. Venezuela, pp. 468-477. Consultada el 22 de Julio/2011 [ Links ]
10 De Feria, M., Jiménez, E., Chávez, M. 1998. Influencia de la densidad de inóculo y la renovación del medio de cultivo en la propagación in vitro de la caña de azúcar (Saccharum officinarum) utilizando sistema de inmersión temporal. III Encuentro Latinoaméricano de Biotecnología Vegetal. REBIO"98. 1-5 Junio, La Habana, Cuba. Libro de Resúmenes, p.42. [ Links ]
11 Dottin, M. 2000. Propagación in vitro de la malanga (Xanthosoma sagittifolium (L) Schoott). Tesis presentada para optar por el grado científico de Doctor en Ciencias Agrícolas. Universidad Central de Las Villas. Santa Clara, Cuba. [ Links ]
12 Escalona, M., Cid, M., Lezcano, Y., Capote, I., Yánez, E., González, J. 1999. Propagación de la piña (Ananas comosus (L.) Merr.) en biorreactores de inmersión temporal. Efecto de la frecuencia de inmersión y el paclobutrazol. BioVeg"99. Ciego de Avila, Cuba. Libro de resúmenes, p. 28. [ Links ]
13 Escalona, M. 2006. Temporary immersion beats traditional techniques on all fronts. Prophyta anual. pp. 48-50. [ Links ]
14 FAO. 2010. Boletín trimestral FAO de Estadísticas. [ Links ]
15 Guzmán, O. A., Castaño, J. 2002. Reconocimiento de nemátodos fitopatógenos en plátanos ´Dominico hartón´ (Musa AAB, Simmonds), ´Africa´, ´FHIA-20´ y ´FHIA-21´ en Colombia. InfoMusa. 11 (2): 34-35. [ Links ]
16 Jiménez, E., Pérez, N., de Feria, M., Barbón, R., Capote, A., Chávez, M., Quila, E., Pérez, J. C. 1999. Improved production of patato microtubersusing a temporary inmersión system. Plant Cell, Tissue and Organ Culture. 59: 19-23. [ Links ]
17 Kitto, M. 1997. Commercial Micropropagation. HorScience. 32(6): 1-3. [ Links ]
18 Kodym, A., Zapata, F. 1999. Natural light as alternative light source for the in vitro culture of banana (Musa acuminate cv. ´Grande Naine´, AAA). Plant Cell Tissue and Organ Culture. 55: 141-145. [ Links ]
19 Lerch, G. 1977. La experimentación en las Ciencias Biológicas y Agrícolas. Ed. Científica y Técnica. La Habana, p. 288. [ Links ]
20 López, J., Montano, N., Reynaldo, D., Medero, V., Basail, M., Rayas, A. 2010. Micropropagación de clones de banana cv. ´FHIA-25´ en Biorreactor de inmersión temporal. Biotecnología Vegetal. 3(5): 101-107 [ Links ]
21 Martre, P., Lacan, D., Just, D., Teison, C. 2001. Physiological effects of temporary immersion on Hevea brasiliensis callus. Plant Cell Tissue and Organ Culture. 67: 25-35. [ Links ]
22 McAlister, B., Finnie, J., Watt, M., Blakeway, F. 2005. Use of the temporary immersion bioreactor system (RITA®) for production of commercial Eucalyptus clones in Mondi Forests (SA). A.K. Hvoslef-Eide and W. Preil (Eds.). Liquid Culture Systems for in vitro Plant Propagation, pp. 425-442. [ Links ]
23 Mehrotra, S., Manoj, G., Arun, K., Bhartendu, M. 2007. Efficiency of liquid culture systems over conventional micropropagation: A progress towards commercialization. African Journal of Biotechnology. 6 (13): 1484-1492. [ Links ]
24 Murashige, T., Skoog, F. 1962. A revised medium for rapid growth and bioassays with tobacco Tissue Cultures. Physiologia Plantarum. pp. 473-497. [ Links ]
25 Novak, F., Afza, R., Duren, M. 1994. Fiel evaluation of tissue-culture bananas in grade oxidation. Australian Journal of Experimental Agriculture. 30: 569-574. [ Links ]
26 Orellana, P. 1994. Tecnología para la micropropagación in vitro de clones de Musa spp. Tesis en opción al grado científico de Doctor en Ciencias Agrícolas. Universidad Central de Las Villas, Santa Clara, Cuba, 96p. [ Links ]
27 Orellana, P. 1998. Introducción a la propagación masiva. En: Pérez, J. N. 1998. Propagación y mejora genética de plantas por Biotecnología (Eds), Instituto de Biotecnología de las plantas, Universidad Central de Las Villas, J. N. Pérez Ponce (Ed.), Santa Clara, Cuba, pp.83-295. [ Links ]
28 Posada, P. L., Gómez, R., Reyes, M., Álvarez, L. 2003. Empleo de los sistemas de inmersión temporal (RITA) en la propagación de plantas vía organogénesis en caña de azúcar y bananos. Biotecnología Vegetal. 3(1): 6-8. [ Links ]
29 Quiala, E., Barbón, R., Jiménez, E., De Feria, M., Chávez, M., Capote, A., Pérez, N. 2006. Biomass production of Cymbopogon citratus (D.C.) Stapf., a medicinal plant, in temporary immersion systems. In vitro Cellular and Developmental Biology - Plant. 42: 298-300. [ Links ]
30 Rodríguez, S., Folgueras, M., Medero, V. 2008. El plátano en Cuba. Informativo del Consorcio Latinoamericano y del Caribe de Apoyo a la Investigación. Colombia. 2. Agosto, 5p. [ Links ]
31 Roels, S., Noceda, C., Escalona, M., Sandoval, J., Canal, M., Rodríguez, R., Debergh, P. 2005. Optimization of plantain (Musa AAB) micropropagation by Temporary immersion System. Plant Cell Tissue and Organ Culture. 82: 57-66. [ Links ]
32 Sigma. 1991. Catalogue.Sigma Chemical Company. EUA. [ Links ]
33 Ventura, J., Medero, V., López, J., García, M., Rodríguez, S., García, J., Reynaldo, D., Rayas, A., Basail, M., Santos, A. 2002. Tecnología para la producción de plátanos y bananos. Memorias en CD. Evento de AGRONAT. Universidad de Cienfuegos. ISBN 959-257-046-02. [ Links ]
34 Williams, R. 1995. The chemical microenviroment In: Jaitken-Christie., T. Kozait., M. A. L. Smith (Eds). Automation and Environmental control in Plant Tissue Culture. Kluwer Academic Publishers. pp. 405- 438. [ Links ]
35 Ziv, M. 2005. Simple bioreactor for mass propagation of plant. Plant Cell, Tissue and Organ Culture. 81: 277-285. [ Links ]