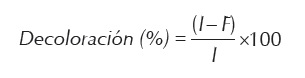Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista Colombiana de Biotecnología
versão impressa ISSN 0123-3475
Rev. colomb. biotecnol vol.16 no.1 Bogotá jan./jun. 2014
https://doi.org/10.15446/rev.colomb.biote.v16n1.33172
http://dx.doi.org/10.15446/rev.colomb.biote.v16n1.33172
ARTÍCULO CORTO
Consorcio microbiano nativo con actividad catalítica para remoción de índigo y surfactantes en agua residual industrial textil a través de una matriz de inmovilización
Microbial consortium native catalytically active for removal of indigo and surfactants in textile industry wastewater through an immobilization matrix
Título corto: Consorcio microbiano nativo con actividad catalítica para remoción de índigo
Liliana Guerrero Porras3, Elizabeth Serna3, Santiago Cardona Gallo1, Gloria Cadavid -Restrepo3, Camilo Suárez2 y Luz Quintero-Rendón2.
1 Departamento de Geociencias y Medio Ambiente.
2 Departamento de Procesos y Energía Facultad de Minas. gecadavi@unal.edu.co, casuarezmendez@unal.edu.co, laquinte@unal.edu.co
3 Facultad de Ciencias. Grupo de Microbiodiversidad y Bioprospección, Facultad de Ciencias. Universidad Nacional de Colombia Sede Medellín. Tel: (57-4) 425 51 20. lguerre@unal.edu.co, esernao@unalmed.edu.co, scardona@unal.edu.co
Recibido: marzo18 de 2013 Aprobado: mayo 7 de 2014
Resumen
El siguiente estudio tuvo como objetivo aislar seis diferentes cepas bacterianas provenientes de las descargas de agua utilizadas en la tintura de hilo con colorante índigo, que tuviesen capacidad de degradación de compuestos orgánicos del tinte índigo y tres surfactantes de tipo no iónicos. Igualmente, se evaluaron diferentes medios de soporte para inmovilizar las cepas seleccionadas. Las cepas con mejor capacidad de decoloración se combinaron para conformar cuatro consorcios (I, II, III, y IV) con el fin de potenciar el proceso de decoloración, considerando que la sinergia y el complemento de actividades metabólicas de cultivos mixtos dentro de una comunidad microbiana incrementan la eficiencia de remoción de carga orgánica. Los porcentajes de remoción que se alcanzaron fueron 64, 73, 76 y 59 %, respectivamente. Los cultivos individuales no presentaron porcentajes de remoción superiores a los reportados por los consorcios, lo que permite pensar en su utilización para la remoción de tintes índigos en aguas residuales.
Palabras clave: aislamiento, biodegradación, índigo, surfactantes no iónicos, consorcio bacteriano.
Abstract
The aim of this study was isolate six different bacterial strains from water discharges used in dyeing yarn with indigo, capable of degradation of organic compounds with indigo dye and three type nonionic surfactants. Similarly, various supporting media were evaluated for immobilizing the selected strains. Strains with better capacity were combined to form four consortia (I, II, III, and IV) in order to enhance the bleaching process, whereas synergy and complement metabolic activities of mixed cultures within a community increase microbial removal efficiency of organic load. Removal percentages were achieved which were 64, 73, 76 and 59%, respectively. Individual cultures showed no higher than rates reported by consortia removal, which suggests in its use for the removal of indigo dyes in wastewater.
Key words: Isolation, biodegradation, indigo, nonionic surfactants, bacterial consortium.
Introducción
La industria textil es uno de los sectores que más contribuye en la contaminación medio ambiental, pues maneja grandes volúmenes de agua por unidad de producto, así como una composición química y orgánica de alto riesgo para los cuerpos de agua receptores (Ministerio del Medio Ambiente, 2002). Los principales contaminantes químicos presentes en aguas residuales textiles son los tintes que contienen aminas cancerígenas, metales pesados tóxicos, pentaclorofenol, blanqueadores con cloro, compuestos orgánicos halogenados absorbibles (AOX), surfactantes, formaldehído libre, biocidas, retardantes de fuego, suavizante no neutros y sales (Correia et al., 1994).
Esta industria emplea una gran variedad de tintes entre los que se encuentran los de tipo tina, usados ampliamente para teñir tejidos de algodón (particularmente el índigo es el tinte comúnmente usado para la manufactura del denim). Para este tipo de tintes se estima que queda sin fijarse entre el 5 y el 20% de ellos en las tinas y son desechados. Algunos de estos tintes y subproductos son carcinógenos y mutagénicos, deterioran estéticamente los cuerpos de agua e impactan negativamente la flora y la fauna (Robinson et al., 2002). Numerosos estudios se han enfocado en el tratamiento de los efluentes textiles centrándose principalmente en el desarrollo de un proceso de degradación eficiente y rentable. Los métodos actualmente utilizados incluyen procesos físicos, químicos y biológicos. Para el tratamiento de aguas residuales contaminadas con colorantes se ha empleado una amplia gama de procesos como son adsorción, neutralización, coagulación, degradación química, y degradación fotocatalítica, ozonación, filtración por membrana e intercambio iónico (Forgacs et al., 2004). Sin embargo, en la mayoría de las ocasiones estos tratamientos tienen problemas operacionales, generan grandes cantidades de lodo y poseen altos costos, además de generar subproductos que pueden llegar a ser más tóxicos que el contaminante inicial (Robinson et al., 2001).
Los tratamientos biológicos han sido reconocidos como métodos efectivos para el proceso de decoloración y degradación de colorantes en aguas residuales industriales altamente contaminadas. Adicionalmente, se consideran muy efectivos ya que son tratamientos amigables con el medio ambiente, de baja producción de lodos y competitivos con relación a los costos requeridos (Banat et al., 1996). Entre las diversas técnicas, la biodegradación es considerada actualmente la alternativa menos costosa para transformar contaminantes presentes en diversos ecosistemas, teniendo en cuenta que gran variedad de bacterias cuentan con la maquinaria enzimática para transformar los compuestos xenobióticos persistentes, y éstas pueden ser aisladas de lugares donde ha existido previa exposición al contaminante (Tony et al., 2009). Actualmente, para la decoloración y mineralización de los colorantes presentes en dichas aguas, son usados sistemas aerobios, anaerobios y combinados (Shaw et al., 2002), con hongos (Prigione et al., 2008; Kaushik y Malik, 2009) y bacterias (Jadhav et al., 2010). Se han reportado estudios en donde se emplean bacterias capaces de remover tintes, ya sea en cultivos puros o en consorcios (Pearce et al., 2003; Khehra et al., 2005). La utilización de consorcios microbianos ofrece considerables ventajas sobre el uso de cultivos puros en la degradación de tintes sintéticos (Moosvi et al., 2006). Las distintas cepas pueden atacar la molécula de colorante en diferentes posiciones, o pueden utilizar los productos de la descomposición de la molécula del tinte (Kuhad et al., 2004). En investigaciones realizadas con un tratamiento aerobio se logró la remoción de 80 - 96 % de color para tintes tipo azo con glucosa como co-sustrato a una concentración de 1.3 g/l empleando un consorcio bacteriano proveniente de una planta de tratamiento de agua industrial textil (Tony et al., 2009). Khehra et al. (2005) logaron la decoloración de tintes tipo azo sin la utilización de co-sustratos alcanzando hasta 99% de remoción de color. Se han empleado tratamientos anaerobios, donde se alcanza la decoloración total del efluente con índigo carmín en un periodo de 18 días, empleando una población mixta de bacterias y usando como co-sustrato acetato, un aditivo que es frecuentemente usado en la industria textil (Fisher-Colbrie et al., 2005). En la búsqueda del escalado del proceso también se ha estudiado el proceso a nivel piloto, donde se utilizó un sistema combinado que consta de un reactor aerobio de tanque agitado continuo y un biorreactor de película fija alimentado con índigo (C.I.Vat Blue 1), los biorreactores fueron inoculados por un consorcio microbiano aclimatado; este sistema alcanzo el 97,5 % de remoción de color (Khelifi et al., 2008).
Materiales y métodos
En este trabajo se determinaron los parámetros más importantes para la decoloración de un efluente textil simulado, empleando un consorcio bacteriano para potenciar la remoción de color del efluente, el cual es considerado un medio de alta complejidad química ya que los métodos para fijar el color índigo son mecanismos de óxido reducción difíciles debido a la insolubilidad del índigo en agua. El índigo puede ser reducido por agentes reductores fuertes como el ditionito de sodio (llamado también hidrosulfito de sodio - Na2S2O4) usado para la preparación del agua sintética (Prideaux, 2003). La reducción se da en presencia de un medio alcalino alto (pH 11-14) por hidróxido de sodio, sales metálicas, y solución de potasio. Se utilizaron surfactantes no iónicos etoxilados para mantener soluble el índigo en agua. Para la simulación del efluente utilizado en este trabajo se emplearon tres tensoactivos no iónicos: surfactante A, surfactante B y surfactante 1, los que se denominaron disp. A, disp. B y disp. 1, respectivamente.
Este estudio incluye, además, el análisis de los parámetros físicos y químicos del proceso de decoloración. Para lo cual se realizaron diferentes ensayos de decoloración, empleando seis cepas aisladas de un efluente textil real, que fueron posteriormente cultivadas en un efluente simulado y de allí se seleccionaron las cepas con mayor porcentaje de remoción en cultivo individual. A continuación, se combinaron para seleccionar el consorcio que alcanzara el mejor porcentaje de remoción, con el objetivo de llevarlo a un siguiente tratamiento en una planta piloto de un sistema trifásico llevado a caben un biorreactor de lecho fluidizado.
Colorantes y químicos
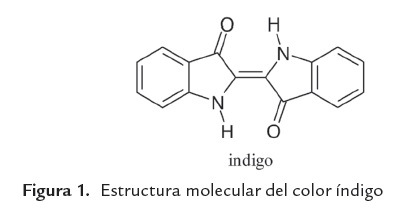
- Tinte: C.I.Vat Blue 1, color índigo, de fórmula química C16H10N2O2 y estructura molecular presentada en la figura 1, C.I. No. 73000, CAS No. 482-89-3; fabricado por INDIGO_ASH_PACIFIC y proporcionado por la industria textilera Fabricato (Medellín, Colombia).
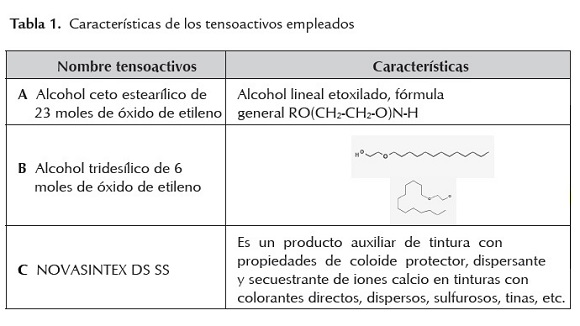
- Surfactantes: Surfactante A: Alcohol ceto estearílico de 23 moles de óxido de etileno, de fórmula química C34H72O2. Surfactante B: Alcohol tridesílico de 6 moles de óxido de etileno. Surfactante 1: NOVASINTEX DS SS. Los tres surfactantes fueron proporcionados generosamente por Colorquímica S.A. (Medellín, Colombia). En la tabla 1 se presentan las características de cada uno de ellos.
- Ditionito de Sodio: Producido y adquirido en Químicos JM, (Medellín, Colombia).
- Los componentes del medio de cultivo fueron cedidos gentilmente por el Laboratorio de Microbiología Industrial, Universidad Nacional, Sede Medellín.
Medio de cultivo
Se preparó el medio de crecimiento BH (Bushnell Haas Broth) (pH 7.0 a 25°C) con los siguientes reactivos en g/l: MgSO4, 0.2; K2HPO4, 1.0; CaCl2, 0.02; FeCl3, 0.05; (NH4)2NO3, 1.0. Dado que el medio no contiene fuente de carbono orgánica, se adicionó el color índigo (contaminante) como fuente de carbono y energía al 1% y 10% V/V. Este medio se preparó en forma sólida y líquida. El índigo y el medio suplementado fueron esterilizados a 121°C y 15 psi durante 15 minutos y luego inoculados con la muestra del efluente.
Bacterias para decoloración de efluente textil
Para desarrollar el consorcio microbiano nativo capaz de decolorar tinte índigo, se tomaron muestras de líquido y sedimento del efluente de una planta de teñido de índigo. Las muestras fueron conservadas en glicerol al 20% en una proporción 1:1 a una temperatura de -20°C. Se realizaron diluciones seriadas de dichas muestras hasta 10-3 en medio BH suplementado al 1% y 10% V/V con índigo y a dos pH diferentes, 7,9 y 11, ajustado con hidróxido de sodio. El tinte índigo fue adicionado posteriormente al medio, luego de su esterilización a través de un filtro de tamaño de poro de 0.22 micras esterilizada a 120°C y 15 psi por 15 minutos. Estas muestras fueron mantenidas en medio aerobio a una agitación constante de 130 rpm y a una temperatura de 30°C por dos semanas. Los tubos se examinaron diariamente y fueron comparados con un blanco que no contenía el inóculo de la muestra de agua. Las diluciones 10-1 y 10-2 fueron cultivadas por dispersión en medio sólido BH alrededor de 10 días utilizando 20% de agar para la siembra en placa. Éste procedimiento se realizó por triplicado y se monitoreó el crecimiento a las 48 y 72 horas. A partir de las placas se inoculó por el método de siembra de dispersión 2 µl/placa y se realizó una siembra en placa para lograr disminución de densidad y diferenciación morfológica.
Aislamiento y caracterización
Con los cultivos primarios obtenidos, se realizó el aislamiento bacteriano a partir del crecimiento en placa de cuatro cepas a pH 7 suplementado con índigo filtrado. Se tomaron las colonias aisladas para aumentar su densidad poblacional y realizar caracterización morfológica a través del test tinción de Gram. Las cepas aisladas fueron guardadas en glicerol al 20%.
Ensayos de decoloración
Las cepas aisladas fueron crecidas en los medios y las condiciones de cultivo descritos anteriormente, por períodos de tiempo establecidos. Los ensayos se desarrollaron centrifugando las muestras durante 15min a 8000g y colectando el sobrenadante. La lectura de la absorbancia se realizó usando un espectrofotómetro a una longitud de onda máxima de 650nm sugerida para el color índigo, utilizando agua destilada como blanco y empleando una curva de calibración construida con el agua residual sintética de concentración conocida.
Evaluación del consorcio
Medio de cultivo
Se utilizó el medio de cultivo BH (Bushnell Haas Broth) (pH 7.0 a 25°C) adicionando como fuente de carbono el color índigo sintético preparado en baño de tina y tres surfactantes. Las concentraciones de los componentes en el efluente sintético variaron en los experimentos realizados. Las relaciones óptimas utilizadas en los últimos ensayos que cumplían con las características del efluente real fueron: Na2S2O4, 150 mg/l, surfactante A sólido 16 mg/l, surfactante B liquido 12 mg/l, surfactante 1, dispersión 12 mg/l e índigo a 50 mg/l. El efluente sintético fue utilizado en los experimentos en medio sólido y medio líquido. El efluente y el medio suplementado fueron esterilizados a 121°C y 15 psi durante 15 minutos.
Selección de cepas con mejor actividad de decoloración
Los aislamientos seleccionados fueron reactivados en medio sólido Luria-Bertani (LB) durante un periodo de 24 a 48 horas. Se tomó muestra de cada una de las cepas y se realizó siembra en 15 ml de medio BH enriquecido con índigo a 50 mg/l, los viales se incubaron a 30° y 130 rpm. El número de viales que se incubaron fue igual al número de muestras tomadas, de forma que cada vial se abrió una sola vez. El control no inoculado se incubó también para comprobar la decoloración abiótica del medio de contraste.
La eficiencia de decoloración de los aislamientos
La longitud de onda de absorción máxima del tinte índigo, 670 nm, fue espectrofotométricamente medida rastreando el espectro visible entre 400 y 700 nm y utilizando agua destilada como blanco, con el espectrofotómetro DR 2700 marca HACH. Los experimentos de decoloración con las cepas aisladas fueron llevados a cabo en cultivo discontinuo por 21 días de tratamiento. En este procedimiento solo se tomaron dos mediciones a cada una de las cepas, al inicio y al final del proceso. La eficiencia de decoloración de las diferentes cepas se determinó por la siguiente ecuación (Robinson et al., 2002).
Donde
I: absorbancia inicial
F: absorbancia del medio decolorado (final)
Desarrollo del consorcio
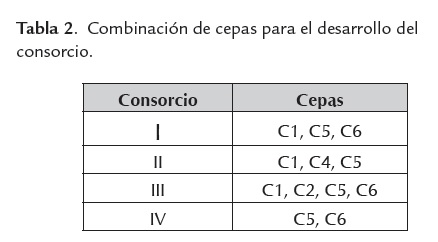
A partir del ensayo anterior, se seleccionaron los aislamientos que presentaron los mayores porcentajes de remoción de color, los cuales se nombraron C1, C2, C3, C4, C5 y C6, y se utilizaron para el desarrollo del consorcio. Cada uno de los aislamientos se cultivó en caldo LB durante 48h con el fin de tener una alta concentración celular en menor tiempo, se ajustó la concentración celular del inoculo a 1.0 (DO) leída a 540 nm. En la tabla 2 se presentan las combinaciones de cepas para la construcción del consorcio. Se sembró 1 ml de cada una de las cepas en un volumen final de 30 ml de caldo BH enriquecido con índigo a 50 mg/l. Posteriormente, se incubó a 30°C y 130 rpm. De esta prueba se seleccionó el consorcio que pudiese alcanzar el más alto porcentaje de remoción de color.
Ensayo de biodegradabilidad de los surfactantes en el efluente sintético
Los surfactantes presentes en la solución, por su naturaleza orgánica, representan otra fuente de carbono para las bacterias. Por esta razón se realizó el siguiente ensayo: se sembró cada una de las cepas en medio BH enriquecido con cada uno de los surfactantes y en una mezcla de estos, en medio sólido, a las mismas concentraciones de la preparación del efluente simulado, surfactante (A) sólido 16 mg/l, surfactante (B) liquido 12 mg/l, surfactante (1), dispersión 12 mg/l. La medición de crecimiento se realizó de manera cualitativa por un periodo de 12 días a temperatura ambiente (25°C).
Evaluación de material de soporte
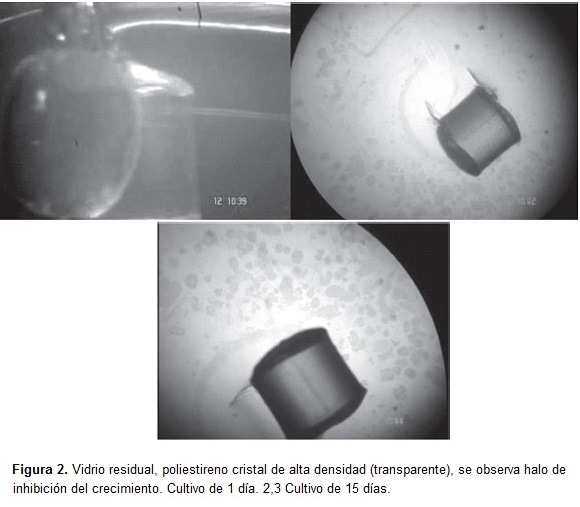
Se evaluó el comportamiento bacteriano de los siguientes materiales propuestos para ser utilizados en el reactor biológico de lecho fluidizado. Vidrio residual (poliestireno cristal de alta densidad, transparente, homopolímero obtenido directamente de la polimerización del estireno, figura 2), plástico reciclado (de colores y de baja densidad), plástico reciclado (color negro, baja densidad y poroso) y carbón antracita.
El poliestireno cristal (vidrio residual) y los plásticos fueron esterilizados a 120ºC y 15 psi por 15 min. Dos tipos de experimentos fueron llevados a cabo. El primero de los ensayos se desarrolló impregnando sobre el material de soporte dispuesto sobre un medio sólido un pre inoculo en medio BH acondicionado por 15 días a una agitación y temperatura constante (130 rpm y 30ºC). El segundo ensayo se desarrolló agregando al pre-inóculo desde su momento inicial de cultivo el material de soporte a una agitación de 130 rpm y a una temperatura de 30ºC constante durante 15 días y luego se colocaron en condiciones estériles sobre el medio BH sólido. La evaluación del material de soporte con respecto al crecimiento bacteriano se realizó cualitativamente.
La antracita fue evaluada tomando una mezcla de las 6 cepas aisladas, esta mezcla se reactivó en medio LB durante 12h, se agregó al medio de cultivo el soporte de inmovilización. Previamente la antracita fue lavada en repetidas ocasiones, incinerada a 550° C por 1 hora, lavada nuevamente, secada a 105° C y esterilizada a 121°C y 15 psi durante 15 minutos. Se incubó durante 48 h el medio de cultivo inoculado en presencia de antracita. Posterior a este período, se tomaron partículas de soporte y se llevaron a medio LB sólido para observar el crecimiento sobre y alrededor del soporte.
Resultados y discusión
Aislamiento de cepas
A partir del muestreo inicial del efluente se obtuvieron dos muestras, denominadas líquido y sedimento, que fueron activadas y cultivadas en medio BH. Sin embargo, se decidió trabajar en sus etapas posteriores con la muestra procedente de medio líquido debido a que proporcionó una mayor variedad bacteriana.
Análisis posteriores de los experimentos realizados en laboratorio, permitieron implementar la fuente alterna de carbono esterilizada en autoclave como otra forma de garantizar la desinfección en vez de usar el índigo filtrado como sugieren varios autores. A partir de las diluciones seriadas se determinó que para posteriores experimentos solo es necesario diluir hasta 10-2.
Los resultados de los protocolos microbiológicos permiten proponer que se requiere un periodo de adaptación en cultivo en suspensión alrededor de 15 días a temperatura de 30 °C y 130 rpm, ya que las cepas iniciales en índigo filtrado fueron repicadas en medio sólido, cambiando el pH de 7 a 11 sin una adaptación previa en cultivo en suspensión y de este proceso, aproximadamente la mitad de las bacterias se adaptaron al cambio de pH, las demás no presentaron crecimiento.
Con el aumento del pH en el medio sólido se evidenció un pardeamiento gradual, este hecho se presentó posiblemente debido a la oxidación de los metales del medio, lo que se observó en el medio líquido como una mayor precipitación de sales. El crecimiento de las cepas se presentó con rapidez a los pH 7 y 9; lo que no sucedió a pH 11, contrario a lo que se esperaba según las condiciones de alcalinidad en el efluente comercial (pH 11.78). Para la identificación de las bacterias, se trabajó a un pH de 7 tanto para medio sólido como para medio líquido y se propuso como el pH óptimo para trabajar en las técnicas de bioestimulación y en la operación de la planta de tratamiento de agua residual.
Los tiempos de cultivo en placa con el cambio de índigo filtrado a índigo esterilizado en autoclave se duplicaron a un promedio de 10 días. Además por resultados previos la adaptación en suspensión se presenta a los 15 días.
Aislamiento y caracterización
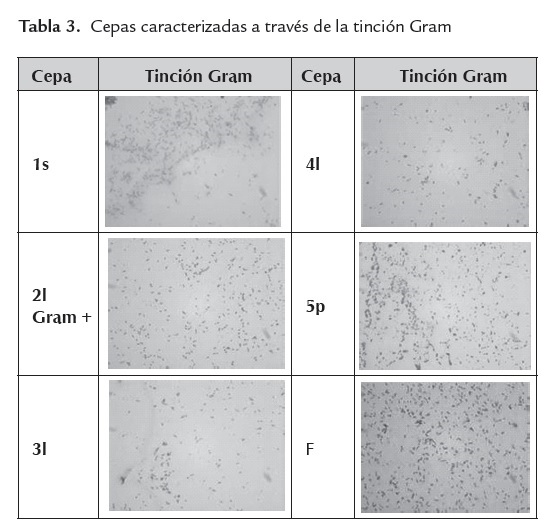
Fueron aisladas seis cepas, cuyo desarrollo se presenta en la tabla 3. Estas cepas presentaron buen crecimiento a los pH 7 y 11 con las siguientes características:
1s: Puntiforme, borde regular, brillante, muy pequeña y no forma agregados.
2L: Borde irregular, cremosa, elevación acuminada, borde ondulado. Mayor tamaño.
3l: Borde entero, brillante, elevación convexa evidencia de un poco acuminada.
4l: Circular, convexa, borde entero, brillante y cremosa-
5p: Puntiforme y brillante. La de menor tamaño, borde entero
F: Con apariencia igual a 2L. En la tinción Gram se verificó su diferencia.
La realización del frotis y la fijación de la muestra para tinción de Gram fueron determinantes para la identificación bacteriana, ya que las bacterias encontradas que usaron el índigo como fuente de carbono tuvieron un tamaño particularmente pequeño. En la tinción de Gram se obtuvieron cinco cepas Gram negativas y una Gram positiva (tabla 3).
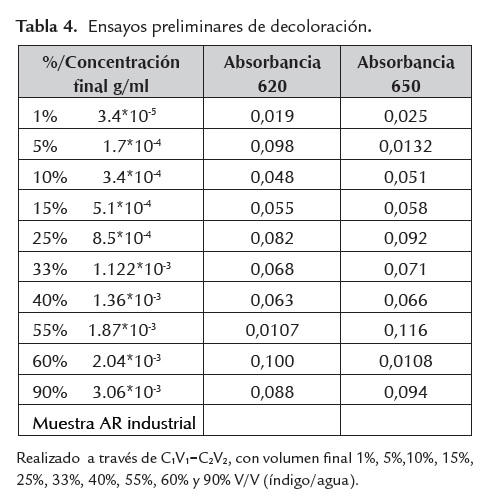
Ensayos preliminares de decoloración
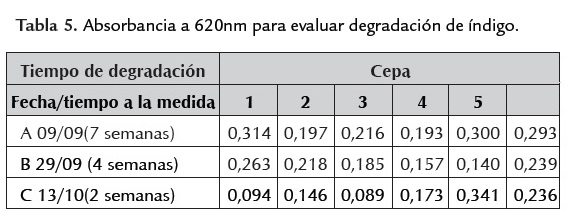
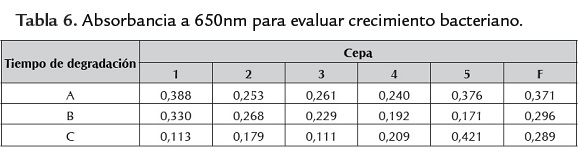
Para obtener el consorcio microbiano óptimo se implementó un ensayo inicial de decoloración con 4 cepas. La medición de absorbancia a 610 y 600 nm en periodos de 24 horas de cultivo, tiempos de (0, 24, 48) fue registrada. El blanco usado para esta prueba fue el tiempo cero. Los resultados con datos negativos sugirieron implementar un blanco con una concentración baja (posiblemente agua destilada), ya que los resultados, que se presentan en las tablas 4, 5, 6, dificultan la interpretación de los datos.
Evaluación de consorcio
Selección de cepas con mejor actividad de decoloración
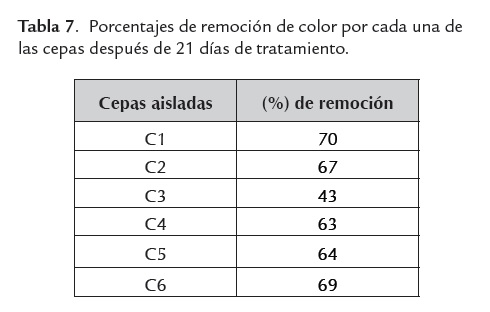
Las cepas seleccionadas fueron revisadas por su capacidad para decolorar índigo C.I.Vat Blue 1 (50 mg/l) en el caldo BH. Los aislamientos no identificados alcanzaron los porcentajes de remoción que muestra la tabla 7. No se verificó acumulación de tinte por las bacterias manteniéndose la hipótesis de que usan como fuente de carbono tanto el colorante como los dispersantes presentes en el efluente simulado. La eficiencia en la decoloración del tinte por las cepas aisladas de muestras tomadas del efluente de una planta de teñido de índigo, indica la adaptación natural de estos microorganismos para sobrevivir en la presencia de colorantes tóxicos. Este resultado es similar al reportado por Chen et al. (2003), quienes reportaron el aislamiento y la detección de microorganismos capaces de decolorar tintes tipo azo a partir de diferentes muestras de lodo recogido de una planta de tratamiento de aguas residuales.
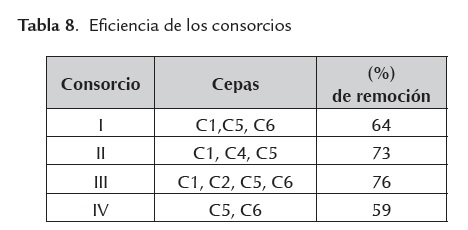
Remoción de color por los consorcios
La combinación de cepas (consorcios) basados en diferentes combinaciones de cinco de los seis aislamientos fueron probados para determinar su eficiencia en la decoloración del efluente simulado. Los resultados presentados en la tabla 8 muestran que el consorcio, denominado III, aumentó significativamente la eficiencia de decoloración de índigo a 50 mg/l. El consorcio III alcanzó un porcentaje de decoloración de 76 % mientras que la cepa pura que mayor porcentaje alcanzó fue de 70%, por lo cual el consorcio es una muy buena alternativa. El potencial de actividad metabólica concertada de las poblaciones microbianas para decolorar aguas residuales de la industria textil ha sido reportado por Manu y Chaudhari (2003), donde con un tratamiento anaerobio, empleando un cultivo mixto, se alcanzó una decoloración de hasta un 90% del colorante índigo añadido.
Selección del consorcio con mejor actividad de remoción de color
El consorcio que alcanzó mayor porcentaje de remoción de color, fue el Consorcio III. Este consorcio es el seleccionado para llevar a cabo el tratamiento a escala semi-piloto en un reactor trifásico de lecho fluidizado en un estudio posterior.
Ensayo de biodegradación de los surfactantes presentes en el efluente simulado
Los agentes activos superficiales o surfactantes son moléculas que contienen un segmento liposoluble y otro hidrosoluble. De acuerdo a los estudio de Olmos et al. (2003) donde la solubilidad parcial tanto en agua como en aceite permite al surfactante ocupar la interface. En este estudio se utilizaron para la simulación del efluente, tres tensoactivos de tipo no iónico etoxilados (disp. A, disp. B y disp. 1), que mantienen soluble el índigo y por ende el agua coloreada. En este ensayo se quiso verificar si las cepas asimilaban como fuente de carbono los surfactantes presentes en el efluente tratado, para despejar la hipótesis de mecanismos de decoloración por parte de las bacterias. El resultado de este ensayo se presenta en la tabla 10. Donde puede observarse que todas las bacterias mostraron crecimiento en al menos un tipo de tensoactivo, lo que indica que pueden ser tomados como fuente de carbono y se corrobora la hipótesis de decoloración por desestabilización del complejo índigo-surfactantes, lo que causa la insolubilidad del índigo y posterior precipitación del colorante dando como resultado un efluente decolorado. Similar a lo reportado por Patoczka y Pulliam (1990), quienes mostraron la biodegradación de surfactantes etoxilados reflejado en la disminución de DQO y toxicidad del efluente después del tratamiento.
Evaluación de material de soporte
Los experimentos con el material de soporte (vidrio residual y plástico de baja densidad) fueron llevados a cabo con una mezcla de bacterias aisladas a partir del efluente textil. El vidrio residual exhibió una clara inhibición de crecimiento bacteriano, el plástico de baja densidad de mayor tamaño y porosidad fue comparado al tiempo t= 1 día con el plástico reciclado de colores y presentó un menor crecimiento (figuras 1a, 2a y 3).
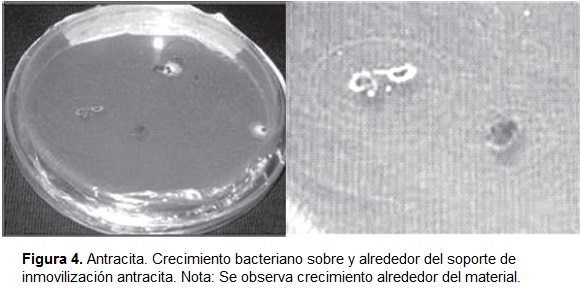
Los experimentos con el material de soporte antracita fueron llevados a cabo con la mezcla de las seis cepas determinadas a partir del efluente textil. En la figura 4 se muestra el crecimiento alrededor del soporte de inmovilización después de 3 días de ser colocado sobre medio LB sólido, lo que indica que este tipo de material no inhibe el crecimiento bacteriano y puede ser exitosamente utilizado en el reactor trifásico de lecho fluidizado para un posterior tratamiento.
Se observa crecimiento alrededor del material.
Conclusiones
Aislamiento
Se obtuvieron seis cepas bacterianas con capacidad de consumo de índigo como fuente única de carbono y energía, con potencial degradativo útil en el tratamiento biológico.
Para este estudio, los parámetros de cultivo que favorecen el crecimiento microbiano, a escala de laboratorio fueron: pH 7, una agitación de 130 rpm y una temperatura óptima de crecimiento dentro de un rango de 25-30 °C.
Consorcio
En este estudio se llevó a cabo la decoloración de un efluente industrial simulado de la industria textil el cual está principalmente compuesto por índigo (C.I.Vat Blue 1), ditionito de sodio (Na2S2O4) y tres surfactante no iónicos.
La actividad metabólica del consorcio III, conformado por cuatro cepas bacterianas, arrojó como resultado un aumento de la eficiencia de decoloración del tinte índigo en comparación con la presentada por las distintas cepas en cultivos axénicos.
Se ensayó mineralizar el colorante con el objetivo de remover el color del efluente, sin embargo el estudio mostró que el proceso de decoloración puede darse principalmente por la desestabilización del complejo surfactantes-índigo generada por la acción bacteriana sobre los surfactantes. Lo que añade interés sobre el consorcio desarrollado, ya que potencialmente puede actuar sobre surfactantes presentes en aguas residuales industriales textiles. Por otra parte, se alcanzó el objetivo del estudio ya que a temperaturas en un rango de 25 - 30°C, agitación en un rango de 120 - 130 rpm y pH entre 7.0 - 7.5 se alcanzó el 76 % de remoción de color utilizando el consorcio desarrollado. Una decoloración significativamente alta, lo que indica la aplicabilidad de este método para el tratamiento de aguas residuales textiles.
Material de soporte
De los cuatro materiales de soporte evaluados, se llega a la elección de la antracita como material de soporte de inmovilización, debido a que no presentó inhibición en el crecimiento bacteriano, lo que permitiría su utilización como medio de soporte en un proceso de tratamiento empleando un biorreactor trifásico de lecho fluidizado.
Agradecimientos
Este trabajo fue financiado a través de los proyectos de investigación: "Identificación y preparación de consorcio microbiano nativo con actividad catalítica para decoloración de índigo en agua residual industrial textil a través de una matriz de inmovilización" (Convocatoria DIME pregrado, código QUIPU 20201007812) y "Evaluación del tratamiento biológico para remoción de color índigo de agua residual industrial textil por un consorcio microbiano en lecho fluidizado" (Convocatoria DIME Bicentenario, código QUIPU 2020100773) de la Universidad Nacional de Colombia, Sede Medellín.
Referencias bibliográficas
1 Banat I.M., Nigam P., Singh D., Marchant R. 1996. Microbial decolorization of textile-dyecontaining effluents: A review. Bioresource Technology. 58 (3): 217- 227. [ Links ]
2 Chen K.C., Wu J.Y., Liou D.J., Hwang S.C.J. 2003. Decolorization of the textile dyes by newly isolated bacterial strains. Journal of Biotechnology. 101(1): 57-68. [ Links ]
3 Correia V.M., Stephenson T., Judd S.J. 1994. Characterization of textile wastewaters: A review. Environmental technology. 15(10): 917-929. [ Links ]
4 Fischer-Colbrie G., Maier J., Robra K.H., Guebitz G.M. 2005. Degradation of the indigo carmine dye by an anaerobic mixed population. En: Environmental Chemistry (pp.289-294). Springer Berlin Heidelberg. [ Links ]
5 Forgacs E., Cserhati T., Oros G. 2004. Removal of synthetic dyes from wastewaters: A review. Environment International. 30(7): 953-971. [ Links ]
6 Jadhav J.P., Kalyani D.C., Telke A.A., Phugare S.S., Govindwar S.P. 2010. Evaluation of the efficacy of a bacterial consortium for the removal of color, reduction of heavy metals, and toxicity from textile dye effluent. Bioresource Technology. 101(1):165-173. [ Links ]
7 Kaushik P., Malik A. 2009. Fungal dye decolourization: Recent advances and future potential. Environment International. 35(1): 127-141. [ Links ]
8 Khehra M.S., Saini H.S., Sharma D.K., Chadha B.S., Chimni S.S. 2005. Decolorization of various azo dyes by bacterial consortium. Dyes and Pigments. 67(1): 55-61. [ Links ]
9 Khehra M.S., Saini H.S., Sharma D.K., Chadha B.S., Chimni S.S. 2005. Comparative studies on potential of consortium and constituent pure bacterial isolates to decolorize azo dyes. Water Research. 39(20): 5135-5141. [ Links ]
10 Khelifi E., Gannoun H., Touhami Y., Bouallagui H., Hamdi M. 2008. Aerobic decolourization of the indigo dye-containing textile wastewater using continuous combined bioreactors. Journal of Hazardous Materials. 152(2): 683-689. [ Links ]
11 Kuhad R.C., Sood N., Singh T., Ward O.P. 2004. Development in microbial methods for the treatment of dye effluents. Advances in Applied Microbiology. 56: 185-213. [ Links ]
12 Ministerio del Medio Ambiente. 2002. Guía Ambiental "Formulación de planes de pretratamiento de efluentes industriales". Bogotá, Colombia. Consultado en http://www.minambiente.gov.co/documentos/Efluentes_industriales.pdf y en http://www.minambiente.gov.co/documentos/Efluentes_industriales_parte_2.pdf [ Links ]
13 Moosvi S., Kher X., Madamwar D. 2006. Isolation, characterization and decolorization of textile dyes by a mixed bacterial consortium JW-2. Dyes and Pigments. 74(3):723 -729. [ Links ]
14 Olmos R.R., Sepulveda R.M., Villalobos F.M. 2003. Agua en el ambiente: muestreo y análisis. Baja California, México. Ed. Plaza y Valdés S.A. [ Links ]
15 Patoczka J., Pulliam W.G. 1990. Biodegradation and secondary effluent toxicity of ethoxylated surfactants. Water Research. 24(8): 965-972. [ Links ]
16 Pearce C.I., Lloyd J.R., Guthrie, J. T. 2003. The removal of colour from textile wastewater using whole bacterial cells: a review. Dyes and Pigments. 58(3): 179-196. [ Links ]
17 Prideaux V. 2003. Handbook of Indigo Dyeing. Search Press Limited. Kent: United Kingdom. [ Links ]
18 Prigione V., Tigini V., Pezzella C., Anastasi A., Sannia G., Varese G.C. 2008. Decolourisation and detoxification of textile effluents by fungal biosorption. Water Research. 42(12): 2911-2920. [ Links ]
19 Robinson T., McMullan G., Marchant R., Nigam P. 2001. Remediation of dyes in textile effluent: A critical review on current treatment technologies with a proposed alternative. Bioresource Technology. 77(3): 247-255. [ Links ]
20 Robinson T., Chandran B., Naidu G.S., Nigam P. 2002. Studies on the removal of dyes from a synthetic textile effluent using barley husk in static-batch mode and in a continuous flow, packed-bed, reactor. Bioresource Technology. 85(1): 43 - 49. [ Links ]
21 Shaw C.B., Carliell C.M., Wheatley A.D. 2002. Anaerobic/aerobic treatment of coloured textile effluents using sequencing batch reactors. Water Research. 36(8):1993-2001. [ Links ]
22 Tony B. D., Goyal D., Khanna S. 2009. Decolorization of textile azo dyes by aerobic bacterial consortium. International Biodeterioration & Biodegradation. 63(4):462 - 469. [ Links ]