Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Biotecnología
Print version ISSN 0123-3475
Rev. colomb. biotecnol vol.16 no.2 Bogotá July/Dec. 2014
https://doi.org/10.15446/rev.colomb.biote.v16n2.47237
http://dx.doi.org/10.15446/rev.colomb.biote.v16n2.47237
ARTÍCULO DE INVESTIGACIÓN
Detección molecular de potyvirus en hojas y minibulbillos de ajo, Allium sativum, asociados a un programa de producción de semilla limpia
Molecular detection of potyvirus in leaves and small bulbs of garlic, Allium sativum, associated a clean seed production program
Parra-Fuentes, M.1, Reyes-Perdomo, C.2, Hernández-Fernández, J.1
1 Universidad Jorge Tadeo Lozano, Facultad de Ciencias e Ingeniería. Centro de Biosistemas. Grupo de Investigación, Desarrollo en Horticultura Sostenible.
2 Universidad Jorge Tadeo Lozano, Facultad de Ciencias e Ingeniería. Grupo de Investigación GENBIMOL "Genética, Biología Molecular y Bioinformática", Cra. 4 No 22-61, Bogotá, D.C., Colombia. Autor para correspondencia: javier.hernandez@utadeo.edu.co
Recibido: octubre 18 de 2013 Aprobado: octubre 1 de 2014
Resumen
El ajo (Allium sativum L) se reproduce vegetativamente utilizando bulbillos, condición que favorece la propagación de enfermedades, especialmente bacterias, hongos y virus que afectan la calidad y el rendimiento del cultivo. Por este motivo se implementó la identificación molecular por RT-PCR de los potyvirus LYSV y OYDV en el sistema de producción de semilla limpia de ajo en tres clones nacionales. En la fase de producción de semilla limpia mediante micropropagación, se estandarizó el establecimiento de meristemos de ajo. La presencia de potyvirus se analizó en 586 plántulas mediante ELISA y en 70 por RT-PCR. Para la RT-PCR se extrajo ARN a partir de microbulbillos y hojas de plántulas, obteniéndose 1.7 a 226 ng/microlitro de ARN y se sintetizó entre 35 a 50 ng de cADN. Los resultados obtenidos mostraron que el protocolo de desinfección produjo una viabilidad del 73.6%. El análisis ELISA presentó un saneamiento del 96.1% de las plántulas a potyvirus, mientras que con RT-PCR se identificó la presencia de LYSV en el 8.6% de las muestras evaluadas. El virus del enanismo amarrillo de la cebolla (OYDV) no fue detectado en ninguna de las muestras. Los resultados muestran que el cultivo in vitro de meristemos de ajo es una excelente alternativa para la producción de semilla, mostrando un 92% de eficiencia. Además, validan el diagnóstico eficiente del potyvirus LYSV en hojas y microbulbillos de ajo.
Palabras clave: Allium sativum, ELISA, micropropagación, LSYV, potyvirus, OYDV, RT-PCR.
Abstract
Garlic (Allium sativum L), reproduces vegetatively using bulbils, condition that favors the spread of diseases, especially bacteria, fungi and viruses, which affect the quality and crop yield. For this reason, the molecular identification by RT-PCR of potyvirus: LYSV and OYDV in the production system of clean seed garlic of three national clones were implemented. In the production phase of clean seed was establishing garlic meristems micropropagation. Potyvirus presence in 586 seedlings was analyzed by ELISA and for RT-PCR in 70. RNA was extracted from leaves and small bulbs, yielding 1.7 to 226 ng/μl, and with this RNA, between 35 to 50 ng of cDNA. The results showed that the disinfection protocol produced a 73.6% viability of plants. ELISA analysis showed 96% sanitation of seedling to potyvirus, whereas, Leek Yellow Strip Virus, LYSV was identified in 8.6% of samples used RT-PCR methodology. Onion yellow dwarf virus (OYDV) was not detected in any sample. The results show that the in vitro culture of meristem of garlic, is an excellent alternative for seed production, showing a 92% efficiency. Moreover, efficient diagnostics of LYSV potyvirus was validated in leaves and small bulbs of garlic.
Key words: Allium sativum, ELISA, micropropagation, LSYV, potyvirus, OYDV, RT-PCR.
Introducción
El ajo (Allium sativum L) contiene sustancias nutritivas como calcio, hierro y vitamina C, además de alicina y diferentes sulfatos que lo hacen atractivo a nivel culinario, agroindustrial y medicinal Metwally et al., 2012). El ajo es una especie de reproducción agámica que no posee semilla botánica, siendo estrictamente apomíctica (Mújica y Mogollón, 2004; Pardo et al., 2011). Su propagación se realiza de manera vegetativa a través de bulbillos (Torres et al., 2000; Pardo et al., 2011; Metwally et al., 2012), lo cual favorece la transmisión y acumulación de virus (Davis, 1995; Lunello et al., 2005) hongos, bacterias y nematodos (Burba, 1992), produciendo enfermedades sistémicas entre generaciones. El Ministerio de Agricultura y Desarrollo Rural reportó para el año 2007 en Colombia, 375 ha sembradas con una producción de 4.300 t y un rendimiento de 11.5 t ha-1. Pese a la poca área cultivada hay un aumento notable en el consumo, el cual ha llevado a la importación de más del 90% del ajo para consumo interno (Pinzón, 2009).
En el cultivo de ajo, los patógenos, especialmente los virus se acumulan dentro de los tejidos y se propagan durante cada ciclo, reduciendo el rendimiento y afectando la calidad de los bulbos (Torres et al., 2000; Fajardo et al., 2001). Por lo general, la presencia de virus se presenta como un complejo viral compuesto por dos o más carlavirus y/o potyvirus (Van Dijk, 1993; Melo Filho et al., 2004) que causan un mosaico de síntomas y generan en la planta una infección crónica, más no mortal. La familia Potyviridae que debe su nombre al grupo de Potato Virus, o virus de la papa, es la más grande dentro de los grupos de virus de importancia económica (Chung et al., 2008; Danci et al., 2009), que causan enfermedades en una amplia gama de cultivos (Shukla et al., 1994). Los virus de los 6 géneros de Potyviridae (Adams et al., 2005) son transmitidos por insectos vectores como áfidos, mosca blanca, hongos y ácaros eriófidos, o a través de las estructuras reproductivas de la especie vegetal (Berger, 2001). Los potyvirus son el género más grande de esta familia con más de 100 especies y se transmiten por áfidos, e inclusive, por medios mecánicos (Danci et al., 2009).
El virus del enanismo amarrillo de la cebolla (OYDV por sus siglas en inglés Onion Yellow Dwarf Virus) y el rayado amarrillo del puerro (LYSV por sus siglas en inglés Leek Yellow Strip Virus) son los potyvirus que más afectan cultivos del genero Allium (Van Dijk, 1993; Barg et al., 1997; Chen et al., 2001), siendo difíciles de eliminar una vez infectan la planta (Walkey, 1989; Bai et al., 2010). Las enfermedades causadas por virus reportan perdidas en el rendimiento del 25-50%, dependiendo del cultivar (Messiaen et al., 1981; Lot et al., 1998; Haque, 2003) y disminución en el peso y tamaño de los bulbillos a causa de OYDV del 24-60% y por LYSV del 17-54% (Lot et al., 1998).
Actualmente, se ha desarrollado un gran interés por la obtención de semilla limpia y libre de virus de acuerdo a los estándares de calidad, mercadeo y presentación de los productos a nivel internacional (Lunello et al., 2005). Entre las diversas técnicas que permiten eliminar estos agentes infecciosos se encuentran el cultivo de meristemos, aplicación de termoterapia (Hernández y Mancipe, 1995; Varés y Iglesias, 2005) o electroterapia (Hernández et al., 1997) y el cultivo de meristemos combinado con termoterapia (Verbeek et al., 1995). La técnica de cultivo de tejidos a través del aislamiento de meristemos permite la propagación de plántulas libres de patógenos bajo condiciones de asepsia (Pérez, 1998) y favorece la posibilidad de obtener semilla limpia de alta calidad, aumentando la producción y rendimiento de los cultivos (Conci et al., 1986; Walkey et al., 1987; Conci y Nome 1991; Verbeek et al., 1995). La termoterapia es un método eficaz y de fácil aplicación para la erradicación de patógenos (bacterias, hongos, nematodos, virus y fitoplasmas) en material vegetal utilizado en la reproducción vegetativa (Varés et al., 2009), sin embargo, la sensibilidad de algunos cultivares a las altas temperaturas y la ineficiencia en la erradicación de ciertos patógenos (Guillen, 2007) limitan el uso de este tratamiento.
La aplicación de técnicas de diagnóstico como la prueba inmunoenzimática conocida como ELISA (Enzyme- Linked ImmunoSorbent Assay), así como, el análisis ISEM (microscopia electrónica de inmunoabsorbancia) permiten identificar el estado fitosanitario de las plántulas obtenidas por cultivo in vitro (Hernández et al., 2002). Sin embargo, aunque la técnica ELISA es favorecida por el análisis rápido y el fácil uso para procesar una gran cantidad de muestras, su detección es limitada y frecuentemente produce falsos negativos (Conci, 1997), mientras que la técnica ISEM desarrolla un escrutinio de una gran cantidad de muestras en poco tiempo (Walkey et al., 1990), pero requiere personal calificado y laboratorios equipados (Salazar, 1995).
La transcripción reversa acoplada a la reacción en cadena de la polimerasa (RT-PCR) consiste en la síntesis de ADN complementario (cADN) a partir de ARN, utilizando una transcriptasa reversa retroviral (Prediger, 2001). La RT-PCR es un método sensible que permite identificar virus en plantas (Dovas et al., 2001; Melo Filho et al., 2004). Con esta técnica se han desarrollado varias investigaciones sobre detección de virus en ajo (Tsuneyoshi y Sumi, 1996; Takaichi et al., 1998; Ayabe y Sumi, 2001; Dovas et al., 2001; Shiboleth et al., 2001; Lunello, 2004; Park et al., 2005; Arya et al., 2006; Majumder et al., 2008; Oleas, 2013). La RTPCR es considerada una alternativa novedosa para la detección de virus en bajas concentraciones (Lunello, 2005).
El objetivo de este estudio fue identificar molecularmente los potyvirus LYSV y OYDV utilizando RT-PCR para certificar la producción, por cultivo in vitro de meristemos, de semilla limpia de ajo en tres clones nacionales.
Materiales y métodos
Material vegetal: se utilizaron tres clones nacionales de ajo provenientes de Cerrito (Santander), Santa Rosa de Viterbo (Boyacá) y la Sabana de Bogotá, cuya semilla fue seleccionada con los agricultores en las zonas de producción luego de evaluar la apariencia y estado sanitario, así como las características agronómicas de producción y rendimiento. Los bulbillos se desinfectaron con solución jabón antibacterial comercial al 10% durante 5 min, etanol al 70% durante 30 s, hipoclorito de calcio (1gL-1) por 10 min e hipoclorito de sodio (0.1%) por 15 min. Los meristemos aislados del segmento basal de los bulbillos se inocularon asépticamente en medio de cultivo formulado con sales MS (Murashige y Skoog, 1962), suplementado con 0.5 mgL-1 de ácido naftalen acético (ANA), 0.6 mgL-1 de 2-Isopentil adenina (2ip), 3% de sacarosa y 9.5 gL-1 de agar PTC (PhytoTechnology Laboratories). El crecimiento de los explantes se realizó a una temperatura de 25±3°C y fotoperiodo de 16 horas luz.
Identificación de potyvirus mediante ELISA: se utilizó el kit Potyvirus Group CAB 27200/0500 (Agdia inc®, Elkart, E.U.A.) para determinar mediante la técnica inmunoenzimática ELISA indirecto (Koenig, 1981) la presencia de potyvirus en 586 muestras foliares de plántulas in vitro y en 6 muestras foliares de plantas cultivadas en campo como control positivo. El análisis se realizó por duplicado para confirmación de resultados.
Análisis molecular por RT-PCR
Material biológico: 70 muestras de hojas y bulbillos de ajo cultivados in vitro se conservaron en RNALater (Ambion Inc. Woodwart St. Austin, Texas, USA) para evitar la degradación del ARN.
Aislamiento y purificación del ARN: se extrajo ARN a partir de fragmentos de tejido de aproximadamente 60 a 100 mg. El tejido fue macerado en morteros de porcelana estériles utilizando nitrógeno líquido bajo una cámara de flujo horizontal LABCONCO Class II Tipo A2 (Kansas, E.U.A.) en condiciones de asepsia. El tejido pulverizado se utilizó para la extracción del ARN utilizando el Kit NucleoSpin RNA/Protein (Macherey- Nagel, Düren, Germany), siguiendo las especificaciones de la casa comercial fabricante. El ARN se observó después de una electroforesis en gel de agarosa al 1%, teñido con bromuro de etidio (2 μg/ml). El gel se fotografió empleando el fotodocumentador UVP GelDoc-It™ System y se analizó con el programa VisionWorks LS Image Acquisition and Analysis Software (UVP, Upland, E.U.A.). A continuación, se determinó la concentración de ARN con el equipo NanoDrop 1000 Spectrophotometer y se registró con el programa ND-
1000 V3.7.1 (Thermo Scientific, Denver, E.U.A.).
Síntesis de ADN complementario (cADN): el cADN fue sintetizado utilizando el kit RETROscript Reverse Transcription for RT-PCR (Ambion Inc., Woodwart St., Austin-Texas, E.U.A.), preparado en un volumen final de 30 μl, el cual contenía 1.2 μM de oligo (dT), 1X de tampón de RT (Tris-HCl 100 mM, pH:8.3; KCl 500 mM y MgCl2 15 mM), 2.5 mM de la mezcla de deoxinucleotidos (dNTP´s), 10 unidades del inhibidor de RNase y 100 unidades de la enzima RT-MMLV (Reverse Transcriptase - Moloney Murine Leukemia Virus). La reacción se llevó a cabo en un termociclador de bloque PTC-100 Peltier Thermal Cycler (M.J. Research, Waltham, E.U.A.) utilizando un programa que comprendió 30 min a 44°C, 15 min a 50°C y finalmente 15 min a 55°C. Posteriormente, se incubó 10 min a 92°C para inactivar la enzima.
PCR para la detección de virus: se realizó la estandarización de las concentraciones de la enzima Taq Polimerasa y de cADN requeridas para la adecuada amplificación de la banda específica para los virus LYSV y OYDV. Se evaluó la amplificación de 2 muestras de ajo en una reacción de PCR con concentraciones de Taq polimerasa entre 1 a 2.5 U y entre 0,5 y 0,8 mg/ml de cADN. Además, se adicionaron 2.5 mM de dNTP´s y 1 μM de oligonucleótidos directo 1OYDV (5´ TTA CAT TCT AATACC AAG CA 3´) y reverso 2OYDV (5´GCA GGA GAT GGG GAG GAC GC 3´) para identificar el virus del enanismo amarrillo de la cebolla (OYDV) y de los oligonucleótidos directo 1LYSV (5´TCA CTG CAT ATG CGC ACC AT 3´) y reverso 2LYSV (5´GCA CCA TAC AGT GAA TTG AG 3´), para identificar el virus del rayado amarrillo del puerro (LYSV) previamente descritos (Fajardo et al., 2001). Se utilizó como control positivo para los virus LYSV y OYDV la muestra de cDNA obtenida a partir de una planta de ajo cultivada en campo que presentaba los síntomas virales característicos. Con las concentraciones de Taq Polimerasa y cADN estandarizadas se realizó la evaluación de presencia de los virus a las muestras de microbulbillos.
La reacción se llevó a cabo en un termociclador de bloque PTC-100 Peltier Thermal Cycler (M.J. Research, Madison, E.U.A.) utilizando un programa que comprendió una fase inicial de desnaturalización de 94°C por 4 min y 35 ciclos de amplificación de 94°C por 30 s, 50°C por 1 min y 72°C por 1 min. Los productos de amplificación se revelaron en una cámara de electroforesis Gel XL ultra V-2 (Labnet international, Inc. Bioscience Research, New Jersey, E.U.A.) utilizando geles de agarosa al 1% (Seaken), corridos por 30 min a 100 v. Los geles fueron fotografiados con el fotodocumentador UVP Gel-Doc-ITTM imaging system (UVP LSC. Upland, E.U.A.) y se analizaron con el programa VisionWorks LS Image Acquisition and Analysis Software (UVP, Upland, E.U.A.).
Resultados y discusión
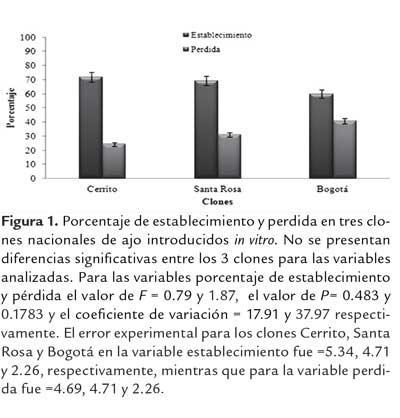
Un total de 730 meristemos fueron introducidos. La desinfección realizada a los bulbillos produjo 100% de explantes libres de contaminación bacteriana o fúngica. Se presentaron pérdidas en 31% de los explantes introducidos, 18% de los meristemos se perdieron por muerte del tejido o viabilidad (figura 1). Los porcentajes de establecimiento permiten validar la producción in vitro de ajo en los clones Cerrito, Santa Rosa y Bogotá (figura 1). El 71% de las plántulas establecidas en medio de cultivo suplementado con los reguladores 2ip y ANA, mostraron después de cuatro semanas una adecuada formación y vigor conforme a los requerimientos de la etapa, presentando características deseables como una altura promedio de 1.5 cm, y el desarrollo de plántulas con 2.5 hojas por plántula y sin raíces.
Los resultados obtenidos con el análisis ELISA, mediante anticuerpos policlonales contra el grupo potivirus, identificaron 23 plántulas infectadas (3.9%), las restantes 563 plántulas (96.1%) dieron negativo para la presencia de potyvirus, mostrando un resultado satisfactorio del tratamiento realizado. De otra parte, las plantas provenientes de campo fueron positivas para la presencia de potyvirus, confirmando la infección del material inicial. Este resultado está de acuerdo con estudios previos, donde semilla de ajo colombiano de las variedades Rubí-1 y Criollo presentaban 100% de la semilla donante infectada con potyvirus (Parra, 2006), así mismo, Torres et al. (2000) identificaron que el material donante de semilla del clon Amarante se hallaba infectado 100% por virus, mientras que Alvarado (2001) detectó la presencia de potyvirus en el 57 y 75% en los materiales donantes de ajo Chino,California y Perla. El alto porcentaje de saneamiento alcanzado en esta fase de este estudio, permite concluir inicialmente que el proceso de producción de plántulas por cultivo in vitro de meristemos permite la obtención de semilla limpia.
En otros estudios realizados, en donde también se utilizó el cultivo de meristemos in vitro y ELISA para evaluar la presencia de potyvirus, se observó un saneamiento en las variedades de ajo Rubí-1 en 87% y de ajo criollo en un 66% (Parra, 2006), resultado que está de acuerdo con los obtenidos en este estudio. Por el contrario, Pérez et al. (2008) encontraron porcentajes de infección de 78 y 90% de los potyvirus OYDV y LYSV, respectivamente, en diferentes materiales obtenidos a partir de meristemos.
Debido a que el proceso de saneamiento viral a través del cultivo de meristemos no es 100% eficiente (Shiboleth et al., 2001), es necesario el análisis para cada uno de los virus a fin de detectar las plantas que están realmente libres de virus. Adicionalmente, las concentraciones de los virus en las plántulas "in vitro" son muy bajas, por ello, es importante utilizar métodos de diagnóstico de alta sensibilidad e incluso utilizar técnicas combinadas (Conci, 2004).
Análisis molecular
El método utilizado en este estudio buscaba detectar la presencia de bajas concentraciones de potyvirus a través de oligonucleótidos específicos, en plántulas cultivadas a partir de cultivo de meristemos, para ello, se realizó la extracción de ARN de 70 muestras de ajo, obteniéndose concentraciones entre 1.7 y 226 ng/μl. Se observó que a partir de muestras de bulbillo se obtienen concentraciones de ARN adecuadas para la identificación de los virus (entre 30 y 226 ng/μl), contrario a la concentración de ARN obtenida a partir de hojas (entre 1.7 y 20 ng/μl).
Se obtuvieron cADNs a partir de los ARN con concentraciones entre 0.3 y 2.533 ng/μl, mostrando una alta variación de acuerdo con las concentraciones obtenidas de ARN total. Aunque las concentraciones bajas de ARN no permitieron obtener una buena cantidad de cADN, estas pueden producir cADN de mejor calidad con el uso de cantidades más altas de dNTP's al mejorar la detección de las transcripciones específicas (Williams et al., 1992).
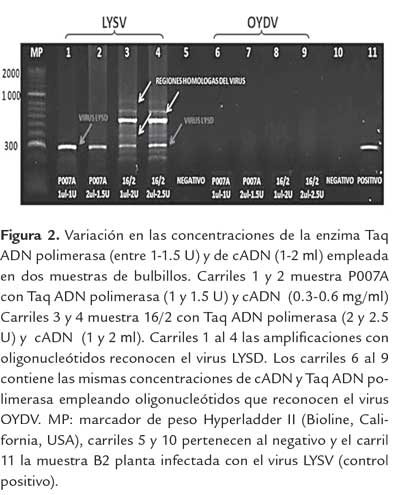
Para la amplificación de la secuencia de los virus LYSV y OYDV se realizó una estandarización utilizando diferentes concentraciones de la enzima Taq Polimerasa y de cADN. Las mejores condiciones de amplificación se lograron con el uso de 1U de Taq Polimerasa y 0.3- 0.6 mg/μl de cADN, produciendo una banda intensa y definida (figura 2, carril 2) para el virus LYSV. Para el virus OYDV ninguna de las combinaciones de Taq y cADN evaluadas generó la presencia de una banda especifica del virus, lo cual pudo deberse a la ausencia del virus en las muestras analizadas, a la necesidad de realizar ajustes en los parámetros de amplificación para el virus o que la secuencia de los oligonucleótidos no amplifican la región especifica del virus en las muestras, siendo necesario diseñar otros oligonucleótidos.
Para la identificación del virus LYSV, los resultados obtenidos permitieron observar la amplificación de una banda de aproximadamente 335 pb (figura 2, carriles 1 y 4 flecha oscura) que identifica la presencia del virus LYSV en 2 muestras de bulbillos. También se observaron bandas inespecíficas (figura 2, carriles 3 y 4 flechas claras) posiblemente generadas debido a la mayor concentración de cADN y de Tag Polimerasa utilizadas. En los carriles 6-9 no se produjo ningún producto de amplificación que comprueba que estas plantas no contienen infección con ARN del virus OYDV.
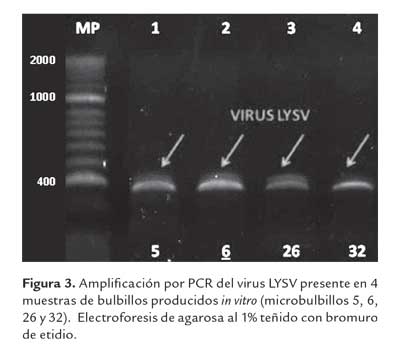
Korkmaz y Cevik (2009) utilizando los oligonucleótidos 1LYSV y 2LYSV (Fajardo et al., 2001), los mismos utilizados en este estudio, y analizando plantas de puerro (Allium porrum) en Turkia, obtuvieron por RT-PCR una banda amplificada de 308 pb que al ser secuenciada y comparada por blastn tenía 93% de similaridad con el virus LYSV reportado en Argentina. Teniendo estandarizada la reacción de RT-PCR se procedió a evaluar 70 de las 592 plántulas provenientes de cultivo in vitro de tejidos (586) y de casa de malla (6) seleccionadas al azar. Se obtuvieron amplificaciones por PCR en cuatro de las muestras de cultivo in vitro y en dos bulbillos cultivados en casa de malla. La figura 3 muestra la amplificación específica obtenida para las plantas 5, 6, 26 y 32 procedentes de cultivo in vitro. Se observa claramente una banda de peso aproximado de 335 pb que identifica infección por virus LYSV.
El muestreo y análisis de cada una de las plántulas establecidas de ajo mediante test ELISA permitió detectar aquellas plántulas con presencia de potyvirus antes de realizar el proceso de multiplicación, sin embargo, se identificó y detectó el virus del rayado amarillo del puerro (LYSV) utilizando el método molecular RT-PCR. También se confirmó, que las muestras evaluadas no contienen el virus del enanismo amarillo de la cebolla (OYDV). Las concentraciones óptimas para la producción de cADN se obtuvieron, en todos los casos, a partir de muestras de bulbillos, mientras que las concentraciones a partir de muestras de hojas fueron muy bajas. Se recomienda la utilización de esta metodología para la evaluación masiva del material obtenido tanto de plantas in vitro sometidas a tratamientos de limpieza o saneamiento, como de las plantas provenientes de casa de malla o campo, que requiera la identificación y detección del virus LYSV, a fin de garantizar que la propagación y el cultivo de plántulas se encuentre libre de patógenos a lo largo del proceso de producción in vitro.
Conclusión
El método de detección por RT-PCR de potyvirus puede ser utilizado con éxito para supervisar un programa de producción de semilla de alta calidad de ajo libre de potyvirus asociado a un programa eficaz de erradicación de virus de ajo por cultivo de meristemos.
Agradecimientos
Los autores agradecen a Julio Cesar Martínez por su apoyo en el análisis de algunas muestras por RT-PCR.
Referencias bibliográficas
1. Adams, M.; Antoniw, J.; Fauquet, C. M. 2005. Molecular criteria for genus and species discrimination within the family Potyviridae. Archives of virology. 150 (3): 459-479. [ Links ]
2. AGDIA. Indirect ELISA, alkaline phosphatase label. Disponible en internet: http://www.agdia.com/cgi_bin/catalog.cgi?m23. [ Links ]
3. Alvarado, R.; Moreno, A.; Martínez, M. 2001. Obtención de semilla de Ajo (Allium sativum) libre de patógenos. Disponible en internet: http://www.ciu.reduaz.mx/investigacion/Agropecuarias/WORD/ap02-002.doc. [ Links ]
4. Arya, M.; Baranwal, V. K.; Ahlawat, Y. S.; Singh, L. 2006. RT-PCR detection and molecular characterization of Onion yellow dwarf virus associated with garlic and onion. Current Science. 91(9): 1230-1234. [ Links ]
5. Ayabe, M.; Sumi, S. 2001. A novel and efficient tissue culture method–" stem-disc dome culture"–for producing virus-free garlic (Allium sativum L.). Plant Cell Reports. 20 (6), 503-507. [ Links ]
6. Bai, Y.; Zhang, W.; Li, X.; Shen, Y.; Gao, Y.; Fan, G.; Geng, H.; Meng, X. 2010. Advances in research of garlic virus diseases. Jornual of Northeast Agricultural University. 17(2): 85-92. [ Links ]
7. Barg, E.; Lesemann, D.; Vetten, H.; Green, S. 1997. Viruses of alliums and their distribution in different Allium cops and geographical regions. Acta Horticulturae. 433: 607-616. [ Links ]
8. Berger, P. 2001. Potyviridae. En: Encyclopedia of Life Science DOI:10.1038/npg.els.0000755. Disponible en internet: http://onlinelibrary.wiley.com/doi/10.1038/npg.els.0000755/abstract?deniedAccessCustomisedMessage=&userIsAuthenticated=false . [ Links ]
9. Burba, J. 2009. Mejoramiento genético y producción de "semilla" de ajo. Posibilidades de adaptación a diferentes ambientes. Revista Colombiana de Ciencias Hortícolas. 3 (1): 28-44. [ Links ]
10. Burba, J. 1992. Producción, poscosecha, procesamiento y comercialización de ajo, cebolla y tomate. Santiago de Chile, Chile: FAO, pp 23-25, 63-127. [ Links ]
11. Chen, J.; Adams, J. 2001. Molecular Characterisation of a Complex mixture of viruses in garlic with mosaic symptoms in China. Archives of Virology. 146: 1841-1853. [ Links ]
12. Chung, B.; Miller, W.; Atkins, J.; Firth, A. 2008. An overlapping essential gene in the Potyviridae. Proceedings of the National Academy of Sciences. 105 (15): 5897-5902. [ Links ]
13. Conci, V.; Moriconi, D.; Nome S. 1986. Cultivo de meristemas apicales de seis tipos clonales de ajo (Allium sativum L.). Phyton. 46 (2): 187-194. [ Links ]
14. Conci, V.; Nome, S. 1991. Virus free garlic (Allium sativum L.) plants obtained by thermotherapy and meristem tip culture. Journal of Phytopathology. 132 (3): 186-192. [ Links ]
15. Conci, V. 1997. Virus y Fitoplasmas de ajo. En: Burba, JL (Ed.). 50 temas sobre producción de ajo. Mendoza, Argentina: EEA-INTA La Consulta. 3: 267-291. [ Links ]
16. Conci, V. 2004. Obtención de plantas libres de virus. En: Echenique V., Rubinstein C., Mroginski L. (Eds.). Biotecnología y Mejoramiento Vegetal. Buenos Aires, Argentina: Ediciones INTA, Parte VIII, Cap. 5: 303-312. ISBN 987-521-138-9. [ Links ]
17. Danci, O.; Ziegler, A.; Torrance, L.; Gasemi, S.; Danci, M. 2009. Potyviridae family-short review. Journal of Horticulture, Forestry and Biotechnology. 13: 410-420. [ Links ]
18. Davis, R. 2008. Diseases Caused by Viruses and phytoplasmas. En: Schwartz H., Mohan S. (Eds.). Compendium of onion and garlic diseases and pest. Minnesota, USA: APS Press. p 78. ISBN 978- 0-19-89054-357-3 [ Links ]
19. Dovas, C.; Hatziloukas, E.; Salomon, R.; Barg, E.; Shiboleth, Y.; Katis, N. 2001. Incidence of viruses infecting Allium spp. in Greece. European journal of plant pathology. 107 (7): 677-684. [ Links ]