INTRODUCCIÓN
A nivel mundial el cáncer de cuello uterino representa la cuarta causa de incidencia y mortalidad por cáncer en las mujeres (Siegel et al., 2016). En Colombia, esta enfermedad es la segunda causa de morbi-mortalidad, afectando principalmente mujeres entre 15 y 39 años (INS, 2011). Aunque, se han obtenido descensos en las tasas de mortalidad por este cáncer durante los últimos años, aún las cifras en Colombia se sitúan por encima del promedio mundial.
El cáncer del cuello uterino se puede detectar a tiempo, siempre y cuando se realicen periódicamente las pruebas de tamización, tales como la citología vaginal, técnicas de inspección visual del cuello uterino y pruebas de detección molecular del ADN-VPH. Esta última técnica fue incluida en el País, a través del acuerdo 029 de 2011 de la comisión de regulación en salud (Comisión de Regulación en Salud, 2011) y reglamentada por el plan decenal de cáncer en Colombia 2012-2021 (Gaviria et al., 2013), en donde se anota que la prueba molecular del VPH se debe realizar en mujeres de 30 a 65 años y con una periodicidad de cada 5 años.
El proceso carcinogénico del CaCU comienza a través de la infección de las células epiteliales escamosas del cuello uterino por parte del Virus del Papiloma Humano (VPH), generando posteriormente lesiones intraepiteliales de bajo y alto grado hasta continuar con la aparición del CaCU infiltrante (Woodman et al., 2007; Walboomers et al., 1999). Sin embargo, este proceso no siempre es continuo y por el contrario aproximadamente un 60% de las lesiones intraepiteliales de bajo grado regresan y solo un 10% de los casos progresan a lesiones intraepiteliales de alto grado (Ostor, 1993). Por lo tanto, sería de gran importancia poder identificar algunos biomarcadores, que nos permitan focalizar y predecir aquellas mujeres con mayor probabilidad de progresión de su lesión preneoplásica cervical.
Por todo lo anterior, se planteó en éste estudio identificar 7 posibles biomarcadores involucrados en la progresión de las lesiones cervicales, teniendo como antecedente un estudio previo en donde se detectó un grupo de genes hipermetilados y subexpresados en muestras de tejido cervical de pacientes Colombianas, con diferentes grados de lesiones preneoplásicas, cáncer invasor y muestras sin ningún grado de lesión cervical (García et al., 2011). A pesar de estudios previos sobre biomarcadores tales como: DAPK1, TWIST y MGMT, éstos han sido estudiado en población asiática y europea y con datos inconsistentes con relación al porcentaje de metilación en las lesiones preneoplásicas y cancerosas del cuello uterino (Kalantari et al., 2014). En un estudio realizado por el grupo se analizó el perfil de metilación de aproximadamente 14000 promotores asociados con progresión en cáncer cervical, allí se analizaron los distintos estadíos de la carcinogénesis cervical donde se incluyó LIEBG (CIN I), LIEAG (CIN II y III) y cáncer invasivo, además de pacientes sanos, luego del análisis bioinformático y estadístico, se propone como posibles biomarcadores un set de 40 genes, los cuales presentaron bajo nivel de metilación en pacientes sanos y con LIEBG comparado con altos niveles de metilación en LIEAG y cáncer invasivo (García et al., 2017), basados en éstos resultados, el objetivo del presente estudio fue analizar la expresión del mARN de los genes incluídos en el estudio como SFRP1, PTPRN, CDO1, EDNRB, CDX2, EPB41L3 y HAND1 en muestras negativas para lesiones intraepiteliales cervicales, muestras con lesiones intraepiteliales de bajo grado y alto grado.
MATERIALES Y MÉTODOS
Muestra
El presente estudio fue descriptivo de corte transversal observacional, con muestras correspondientes a biopsias de cérvix conservadas en parafina, que presentaran un diagnóstico histopatológico con Hematoxilina & Eosina realizado por dos médicos patólogos, los diagnósticos fueron normalidad o proceso inflamatorio cervical (n=9), LIEBG (n=10) y LIEAG (n=11), durante los años 2009 a 2014. El estudio contó con aprobación del comité de ética de la Facultad de Odontología de la Pontificia Universidad Javeriana. La disponibilidad de los tejidos embebidos en parafina estuvo a cargo de "Estudios Anatomopatológicos Ltda" quien actúa como custodio de las muestras incluidas en el presente estudio.
A partir de cada bloque se realizaron dos cortes de 5µm para pruebas moleculares, y un corte final de 3µm para confirmar con tinción de hematoxilina & Eosina la presencia o no de lesión. Teniendo precaución de cambiar la cuchilla para cada muestra, para evitar contaminación con ácidos nucleicos residuales.
Extracción de ARN
Los cortes de 5um fueron utilizados para la extracción de ARN mediante el Kit AllPrep DNA/RNA/ Protein Qiagen. A partir de ARN total se realizó el proceso de retrotranscripción y síntesis de cADN con el kit Super Script VILO de Invitrogen. Finalmente, se cuantificó la concentración de cADN de cada una de las muestras a través de nanodrop 1000® y se conservó el material a -70°C.
qRT-PCR
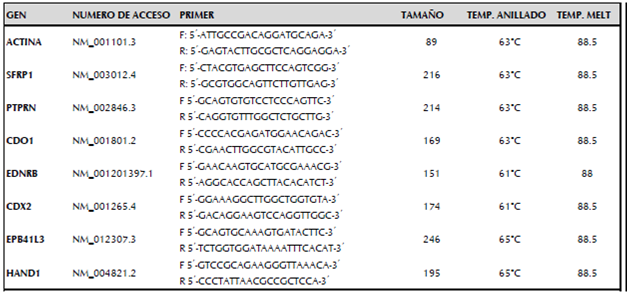
Para realizar la PCR en tiempo real se utilizó 1X de Fast SybrGreen de Kappa, 200nM de cada iniciador para todos los genes de estudio (p-ACTINA, PTPRN, CDO1, EDNRB, CDX2, EPB41L3 y HAND1) y 10ng de cADN para un volumen final de 10uL, cada muestra fue analizada por duplicado en el equipo CFX96 Biorad. El gen correspondiente a p-actina fue utilizado como gen calibrador. En la tabla 1 se observan las secuencias de los iniciadores para cada gen utilizado en el estudio.
Las condiciones de termociclado fueron 95°C 3 minutos, seguido por 35 repeticiones de 95 °C por 3 segundos y 61°C para EDNRB y CDX2 ó 63°C para ACTINA; SFRP1, PTPRN y CDO1 ó 65°C para EPB41L3 y HAND1 durante 45 segundos, finalmente se realizó curva de melting.
Luego se consolidaron los resultados obtenidos del ciclo umbral (CT) y curva Melting, de cada uno de los genes, para corroborar las replicas de los ensayos y que el producto detectado fuese el esperado.
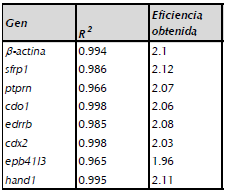
El análisis de expresión génica, fue realizado mediante el método de cuantificación relativa, para ello se hicieron curvas de eficiencia para cada gen, a través de ADN de la línea celular HeLa con las siguientes concentraciones: 100ng; 20ng; 4ng; 0.8ng y 0.16ng. La eficiencia se calculó con la fórmula (10 (-1/pendiente)) y coeficiente de correlación (R2) obtenido para cada gen, donde los dos valores se detalla en la tabla 2. El cálculo de expresión fue calculado con el método 2 "ACT teniendo en cuenta las eficiencias obtenidas para cada set de iniciadores. La expresión relativa de los genes de interés fue basado en la siguiente fórmula: (Eactina)CT/ (Egen de interés) CT (Pfaff, 2001; Thomas et al., 2013).
Tabla 2 Eficiencias de los pares de primers b-actina, SFRP1, PTPRN, CDO1, EDNRB, CDX2, EPB41L3 y HAND1 utilizando DNA de línea celular HeLa
Análisis estadístico
El análisis estadístico de los valores de expresión relativa para cada gen entre los tres grupos de análisis (negativo para lesión cervical, LIEBG y LIEAG) mediante la prueba no paramétrica de ANOVA. Un valor de p< 0.05 fue considerado como una diferencia estadísticamente significativa. El programa estadístico utilizando fue GraphPad Prism 6.
RESULTADOS
De acuerdo a los resultados previos descritos por García y colaboradores en el 2017, fueron seleccionados siete posibles biomarcadores asociados a progresión en cáncer cervical que presentaban alteraciones epigenéticas como la hipermetilación de sus promotores, genes que fueron incluidos en el presente estudio analizando en muestras embebidas en parafina la expresión del mARN, donde se espera encontrar bajos niveles de expresión, ya que la hipermetilación se asocia en la mayoría de los casos a una baja expresión génica.
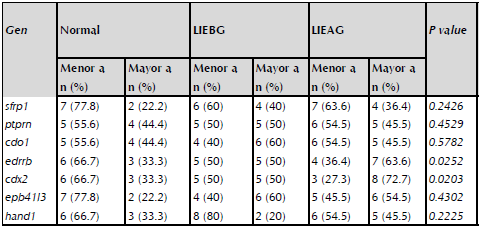
En la tabla 3 se observa que al comparar SFRP1 con respecto al gen calibrador P-Actina se observó disminución en la expresión de SFRP1 en el 60% de las muestras con LIEBG y un 63.6% en las correspondientes a LIEAG. En el grupo normal se observó disminución en la expresión en un 77.8%. Sin embargo no hubo diferencia estadísticamente significativa (p=0,2426), para el gen CDO1, mostró niveles de expresión muy similares entre LIEAG y el grupo normal, encontrándose una menor expresión con respecto al gen calibrador, del 54.5% y 55.6%, respectivamente. En el grupo de LIEBG, el porcentaje de casos con disminución de expresión fue del 40%, para esté gen tampoco se observó diferencia estadísticamente significativa (p=0,5782). El gen CDX2, tuvo menores niveles de expresión con respecto al gen calibrador en el 66,7% de los casos normales, 50% en LIEBG y 27,3% en LIEAG, encontrando diferencia estadísticamente significativa entre la expresión de las muestras de LIEAG en comparación con la expresión de LIEBG y normal (p= 0,0203). El gen EDNRB, registró menor expresión con respecto al gen calibrador en un 66,7% en el grupo normal, en el grupo de LIEBG el porcentaje fue 50% y en el grupo de LIEAG el 36,4%. Hubo diferencia estadísticamente significativa entre la expresión de este marcador en las muestras de LIEAG en comparación con la expresión de LIEBG y normal (p= 0,0252). Adicionalmente, el gen EPB41L3, mostró menor expresión en los grupos de LIEBG y LIEAG en un 40% y 45,5%, respectivamente., mientras que en el grupo normal hubo menor expresión en 77,8% de los casos (p=0.4302). Con respecto al gen HAND1, hubo menor expresión en un 80% en el grupo de LIEBG; 54.5% en LIEAG y 66.7% en el grupo normal (p=0.2225). Finalmente, los niveles de expresión de PTPRN fueron similares entre los tres grupos de análisis: normal (55.6%), LIEBG (50%) y LIEAG (54.5%). Ver tabla 3, que contiene el resumen de resultados de qRT-PCR para cada uno de los genes.
DISCUSIÓN
Teniendo en cuenta la historia natural de la infección por VPH a nivel cervical, se observa que ésta es una causa necesaria más no suficiente para el desarrollo de las lesiones premalignas y malignas de cuello uterino y que en general la aparición del cáncer invasor del cérvix es una consecuencia poco frecuente de la infección por VPH. Por lo anterior, varios trabajos de investigación se ha realizado con el propósito de encontrar nuevos biomarcadores a nivel de VPH y de la célula hospedera, que permita predecir de una mejor manera la probabilidad de progresión o regresión de las lesiones premalignas del cuello uterino.
De manera específica con el cáncer del cuello uterino, son varios los genes que han sido estudiados desde el punto de vista epigenético como posibles biomarcadores. Kim y colaboradores en el 2010 estudiaron varios genes como factor pronóstico de progresión a LIEAG, algunos de los genes fueron: CHH1, DAPK, GSTP1 y MGMT entre otros, evidenciáron que al analizar simultaneamente los genes RAR-beta/Twist/MGMT encontraron una especificidad del 82,2% y una sensibilidad del 78,7% de distinguir muestras con LIEAG o CaCU en comparación a las muestras normales y LIEBG.
También se ha observado inconsistencia entre el porcentaje de metilación por ejemplo, para MGMT con un 11,9% en muestras de LIEAG (Kim et al., 2010), en comparación al trabajo de Iliopoulos et al., 2009, en donde el porcentaje de metilación para el mismo gen fue de 75% en muestras de LIEAG.
En un estudio previo reportado por García y colaboradores en el 2017, realizado en población Colombiana, se analiza la metilación de aproximadamente 14.000 regiones promotoras, en mujeres sin lesiones intraepiteliales cervicales y con lesiones grado 1 (LIEBG), grados 2 y 3 (LIEAG) además de mujeres diagnósticadas con cáncer invasivo, en muestras de citologías en base líquida. En dicho estudio se reporta un listado de 40 genes que podrían servir como biomarcadores asociados a progresión, ya que se encontraron hipermetilados en LIEAG y cáncer cervical invasivo comparado con LIEBG y tejido normal. En el presente estudio se seleccionaron siete (7) genes candidatos del listado previo de 40 posibles biomarcadores, para analizar en muestras de tejido embedidas en parafina con diagnóstico histopatológico confirmado como: a. Normalidad ó sin cambios displásicos, b. LIEBG y c. LIEAG, y evaluar los niveles de expresión de los siete biomarcadores seleccionados, puesto que normalmente la hipermetilación en las regiones promotoras de los genes conlleva a la disminución en su expresión génica.
Contrario a lo que esperábamos, encontramos mayor expresión con respecto al gen calibrador de P-actina para los genes EDNRB y CDX2, en el grupo de LIEAG, en comparación con LIEBG y normal, encontrando diferencias estadísticamente significativas. Qu y colaboradores en el 2013, realizan una revisión exhaustiva de la literatura, con el fin de describir alteraciones epigenéticas asociadas a cáncer gástrico, en su búsqueda mencionan varios genes implicados, entre ellos reportan a EDNRB y CDX2 como posibles biomarcadores en ésta patología. Adicionalmente otros estudios también reportan hipermetilación en estos dos genes principalmente EDNRB en cáncer cervical (Lin et al., 2016) y CDX2 en cáncer colorrectal (Wang et al., 2016).
El gen EDNRB (Endothelin receptor type B) se encuentra localizado en el cromosoma 13 (13q22) y codifica para un receptor ligado a la proteína G para la Endotelina 3. EDNRB está aceptado como uno de los genes responsables de la enfermedad de Hirschsprung, debido a que interviene para el normal desarrollo del tejido ganglionar entérico, el cual juega un papel muy importante durante el desarrollo embriogénico de la población celular de la cresta neural. La hipermetilación del promotor del EDNRB, se ha visto implicada en el carcinoma escamocelular esofágico, leucemia, cáncer gástrico, carcinoma nasofaríngeo, melanoma, cáncer de pulmón y también en CaCU (Lin et al., 2016; García et al., 201 7; Brentnall et al., 2015; Watanabe et al., 2014; Vasiljevic et al., 2014). En nuestro trabajo se evidenció mayor expresión de EDNRB en 7 de 11 muestras (63,6%), resultados que al contrastarlos con otros autores como Vasiljevic et al., en el 2014, pueden parecer contradictorios, debido a que ellos describen hipermetilación en EDNRB en pacientes diagnósticados con LIEAG. Por otra parte, el estudio realizado por Watanabe y colaboradores, en el 2014, encontraron que la baja expresión de EDNRB está asociada a un peor pronóstico en cáncer de próstata, y que en tumores malignos como el melanoma la sobre-expresión actúa como factor pronóstico desfavorable, adicionalmente, en otro estudio realizado por Cruz-Muñoz y colaboradores en el 2012, reportan que el aumento en la expresión de EDNRB en el mismo tipo de tumor se asocia al incremento en la metástasis, lo que nos sugiere que el aumento en la expresión de EDNRB es de mal pronóstico y que posiblemente en la patología cervical se relacione con procesos de progresión de LIEAG hacia cáncer cervical invasivo.
En cuanto al gen CDX2 (Caudal - type Homeobox Transcription Factor 2) es un factor de transcripción esencial para el desarrollo embrionario de los tejidos. CDX2 es un gen localizado en el cromosoma 13 (q12.2) y juega un papel esencial en el desarrollo del intestino, inhibiendo la proliferación y promoviendo la diferenciación y expresión de genes específicos del Intestino, así como regula negativamente la vía wnt (Liu et al., 2012). CDX2 se ha utilizado como un biomarcador para algunos tipos de cáncer gastrointestinal y también pulmonar. La mayoría de los cánceres colorrectal muestran una fuerte expresión nuclear y solo entre 1030% de los casos muestran pérdida o pobre expresión del CDX2. Esta pérdida de expresión del CDX2 se correlaciona con el grado de diferenciación nuclear, localización proximal del tumor, mutación del BRAF y menor sobrevida de los pacientes con cáncer de colon (Camilo et al., 2014). En nuestro estudio, CDX2 tuvo mayor expresión en las muestras con LIEAG en el 72,7%. Es importante anotar que el incremento en la expresión de CDX2 en las lesiones tumorales gastrointestinales les confiere un mejor pronóstico a los pacientes (Camilo et al., 2014), por lo tanto, podría plantearse la posibilidad que CDX2 en LIEAG, también le pudiera brindar cierto factor pronóstico favorable, que estaría representado en la regresión de la lesión intraepitelial escamosa de alto grado hacia una lesión de bajo grado.
Teniendo en cuenta que la hipermetilación normalmente conlleva a la disminución en la expresión génica, se esperaba encontrar menor expresión de EDNRB y CDX2 en los casos de LIEAG. Una posible explicación a estos hallazgos, sugieren que pueden existir otros mecanismos distintos a la hipermetilación que afecten la expresión de éstos dos genes, entre los cuales podemos mencionar los miARNs que pueden alterar la expresión de algunos genes implicados en procesos celulares importantes en la carcinogénesis cervical, un estudio realizado por Kim y colaboradores en el 2015, describen el perfil de miARN en cáncer cervical y observan que alteraciones en la expresión de miARNs, por ejemplo la baja expresión de miR-125b, 2195, 2196a, 199a, y 376c conlleva al incremento de los niveles de expresión de genes como CDKN2A, CCNE1, CCNE2, E2F3, RARB, e IGFBP3, promoviendo proliferación celular, invasión y metástasis. Así mismo Kriegel y colaboradores en el 2015, en un modelo de hipertensión describe que la familia de miR-92 puede afectar la expresión del gen EDNRB y Teng y colaboradores en el 2018, describen que miR-361-3p afecta la expresión de CDX2, en un modelo células esofágicas infectadas y transformadas con Helicobacter pylori, donde observan baja expresión del miARN y por ende un incremento en los niveles de expresión de CDX2. Es así, como nuestros resultados motivan en futuros trabajos de investigación que determinen el estado de metilación de EDNRB y CDX2 simultáneamente con los niveles de expresión tanto de los genes en mención como de los miARNs miR-361-3p y los de la familia de miR-92.
En relación al gen SFRP1 (Secreted frizzled-related protein1), se encuentra ubicado en el cromosoma 8(p.11.21) y codifica una proteína (SFRP1) que actúa como modulador de la vía de señalización Wnt, la cual juega un papel importante en el desarrollo embrionario, diferenciación celular y proliferación celular y se ha evidenciado la alteración de esta vía de señalización en varias entidades tumorales malignas en el ser humano, tales como cáncer colorrectal, de seno, hepático, próstata y pulmonar. SFRP1 se ha encontrado hipermetilado en varios tipos de cánceres tales como leucemia, colon-recto, gastrointestinal, seno y carcinoma esofágico (Sova et al., 2006; Chung et al., 2009). En el presente estudio no se observaron diferencias significativas en la expresión de SFRP1 entre los grupos de análisis, encontrándose que en más del 50% de las muestras de todos los grupos registró baja expresión posiblemente debido a una hipermetilación, sin embargo es importante en estudios posteriores analizar la metilación de dicho gen en muestras con distinto tipo de lesiones intraepiteliales cervicales.
El gen PTPRN (Protein-tyrosine phosphatase, receptor -type N), se encuentra localizado en el cromosoma 2, q35 y codifica una proteína que actúa como receptor y posee un solo dominio trans-membranal. Además participa en procesos de fosforilación que están involucrados en señales de transducción, proliferación y diferenciación celular. PTPRN, se ha asociado con la presencia de diferentes tipos de tumores malignos tales como: esófago, seno, próstata, colon, pulmón, linfoma T y tumores neuroendocrinos. También se ha relacionado el estado de metilación de PTPRN como factor pronóstico de sobrevida libre de enfermedad, posterior al tratamiento con quimioterapia en pacientes con cáncer de ovario (Lu et al., 1994; Bauerschlag et al., 2011). En el presente estudio, aunque no hubo diferencias significativas en la expresión de PTPRN entre los grupos de LIEBG y LIEAG, se observó que más del 50% de las muestras en todos grupos analizados hubo baja expresión de éste gen posiblemente debido a una hiper-metilación, sin embargo es importante en estudios posteriores analizar su estado de metilación, con distintos tipos de lesiones intraepiteliales cervicales.
Con respecto a CDO1 (Cysteine Dioxygenase type 1) se localiza a nivel del cromosoma 5 (q22.3) y codifica una proteína que participa en la via metabólica del Piruvato y varios componentes sulfurados, además participa en la regulación celular de las concentraciones de Cisteína, especialmente a nivel hepático y de la médula ósea. La enzima Cisteina Dioxigenasa es vital para el ser humano, debido a que participa en la biodegradación de la Cisteína tóxica y por lo tanto, regula la concentración de esta enzima a nivel corporal. Alteración en la expresión de este gen ha sido estudiado e implicado en tumores de tipo colorrectal, pulmonar, mamario, esofágico, gástrico y con los linfomas cutáneos de linaje T. Dado que en estas patologías se ha encontrado a CDO1 hipermetilado y con disminución en su expresión de mARN, se le ha postulado como un gen supresor tumoral (Brait et al., 2012). Para el caso de éste gen en nuestro estudio encontramos baja expresión en muestras negativas para lesiones cervicales y LIEAG, sin embargo en sólo el 40% de los casos de LIEBG se encontró disminuída su expresión, resultado que sugiere que la hipermetilación de CDO1 no está estrechamente relacionado con la progresión en cáncer cervical.
Para el gen EPB41L3 (erythrocyte membrane protein band 4.1-like 3), se localiza en el cromosoma 18 (p11-32) y codifica una proteína localizada en la membrana citoplasmática, que interviene en la vía de señalización Tight Juntion, la cual participa en la regulación del citoesqueleto. En condiciones normales éste gen es altamente expresado en tejido nervioso, testicular, placentario, adiposo y renal. Se ha reportado que EPB41L3 tiene función supresora tumoral, inhibiendo la proliferación tumoral y promoviendo la apoptosis y se ha observado la sub-expresión de este gen en patología tumoral maligna, tales como: carcinoma de próstata, meningioma y carcinoma pulmonar de célula pequeña (Vasiljevic et al., 2014). En el caso del presente estudio observamos baja expresión de éste gen en muestras negativas para lesiones intraepiteliales cervicales, mientras que muestras con LIEBG y LIEAG la mayoría de las muestras presentaban alta expresión de éste gen, lo que nos permite sugerir que éste gen posiblemente pueda servir como biomarcador pero por mecanismos distintos a la metilación que induzcan sobre expresión génica.
Finalmente para el gen HAND1 (Heart And Neural Crest Derivatives Expressed 1), se localiza en el cromosoma 5 (q33.2), codificando una proteína que se encuentra involucrado en procesos de morfogénesis, especialmente a nivel cardiaco (ventrículo derecho y arco aórtico). Este gen ha estado implicado en anomalías congénitas del corazón como la tetralogía de Fallot y también hay estudios donde reportan alteraciones epigenéticas de HAND1 con cáncer de origen colorectal, mamario, pulmonar y hepático (Yagi et al., 2010). En el presente estudio observamos que en más del 50% de las muestras analizadas en cada grupo de análisis la expresión de éste gen se encontraba disminuida, similar a lo encontrado para los genes PTPRN y SFRP1 y al igual que en ellos es importante en estudios posteriores analizar la metilación en muestras con distinto tipo de lesiones intraepiteliales cervicales.