INTRODUCCIÓN
Factores, como el sedentarismo y el consumo de alimentos poco saludables, han hecho que aumenten las cifras de la población que padece de las denominadas enfermedades no trasmisibles (ENT), en las que se destaca la obesidad, la diabetes Mellitus, los problemas cardiovasculares y la hipertensión (OPS/OMS, 2016). El riesgo de enfermedades crónicas ha ido creciendo, a medida que las pautas alimentarias de la población cambiaban y se incorporaban cada vez más alimentos procesados ricos en grasas, azúcares o con alto contenido de ácidos grasos trans (AGT), de producción industrial (Bejarano-Roncancio et al. 2015)
Recientes estudios han comprobado que el consumo de alimentos ricos en grasas trans, sal y carbohidratos favorecen el incremento de peso y de los factores de riesgo de contraer alguna enfermedad, del tipo ENT (Parodi, 2009).
El aceite de aguacate (Persea americana) es rico en ácidos grasos mono-insaturados, además posee tocoferoles de gran beneficio al ser consumidos; es fuente importante de vitaminas, contiene 12 de las 13 vitaminas existentes, (Barbosa-Martín et al. 2016). Por su parte, el aceite de Sacha inchi, obtenido de las semillas de esta planta oleaginosa (Plukenetia volubilis L.), se caracteriza por alto porcentaje de ácidos grasos poli-insaturados, principalmente, linolénico y linoléico, los cuales, representan el 82% del contenido total de aceite (Fanali et al. 2011).
Las propiedades fisicoquímicas de las moléculas tensoactivas son de gran interés, porque determinan la estabilidad de las emulsiones. Los fosfolípidos, como la Lecitina (LC) y los monoglicéridos, como el Monoesterato de glicerilo (ME), son ejemplos comunes de emulsificantes de bajo peso molecular, utilizados en la estabilización de diferentes productos alimenticios, ya que son compuestos muy activos en la superficie (Moran-Valero et al. 2017).
La LC y el ME son emulsionantes que se necesitan para aumentar la estabilidad coloidal y proporcionar interacciones interfaciales entre los componentes alimentarios, que son factores importantes para mejorar aún más la estabilidad de la emulsión y la vida útil en muchos alimentos. Estas aplicaciones, incluyen formulaciones de alimentos tradicionales, como productos de panadería, confitería o productos cárnicos, entre otras o nuevas formulaciones, como los alimentos instantáneos y bajos en grasa, formulaciones alimenticias de alto o bajo contenido en alcohol, alimentos funcionales (Moran-Valero et al. 2017).
El objetivo del presente trabajo fue estudiar el efecto de la adición del tipo de emulsificante y la relación de aceite sobre las propiedades fisicoquímicas de emulsiones estructuradas, a partir de aceite de aguacate y sacha inchi, para la estructuración de un oleogel, como sustituto de grasas usadas en mesa y en cocina, libre de grasas trans.
MATERIALES Y MÉTODOS
El aceite de aguacate (P. americana) fue suministrado por Terravocado S.A., el aceite de sacha inchi (P. volubilis), por un productor local de la Amazonia colombiana y la grasa alimentaria de origen vegetal (shortening latino), de Tecnas S.A. Además, se utilizaron emulsificantes: Lecitina (LC) y monoesterato de glicerilo (ME) y conservantes de calidad alimentaria, como ácido cítrico, sal y Terbutil Hidroquinona (TBQH), estos últimos de Bell Chem Internacional S.A. (Medellín, Colombia).
Formulación de las emulsiones: En las preparaciones de las emulsiones (w/o), se inició con la fase lipídica: aceite de aguacate/aceite de sacha inchi, shortening latino y TBQH y, posteriormente, la fase acuosa. En esta fase, se le adicionó los conservantes, como el cloruro de sodio y el ácido cítrico, ingredientes con la particularidad de ser solubles en agua. Se homogenizó térmicamente, a temperatura de 50°C, para favorecer la mezcla. La proporción de cada uno de los componentes del sistema oleoestructurado se midió en peso, para evitar errores, debidos a la variación de volumen por la temperatura.
En este estudio, se estableció una relación (w/o) de 20/80, donde un 30% de la fase oleosa en todas las muestras corresponde a la grasa de origen vegetal (shortening latino). Adicionalmente, la concentración de los aditivos y de los conservantes, como ácido cítrico y cloruro de sodio, fue establecido en 1% p/p. La homogenización de las dos fases, se realizó mediante el agitador Ultaturrax T25y, proceso, en el cual, previamente, se realizaron ensayos para determinar los valores óptimos de las variables, que se dejaron fijas en la preparación de las emulsiones: temperatura de homogenización (50°C), la velocidad de agitación (4000rpm) y tiempo (10 minutos).
Estructuración sólida del oleogel: Para favorecer el proceso de cristalización y formar los oleogeles, las emulsiones estructuradas fueron sometidas a un proceso de enfriamiento durante 12h, a una temperatura de 4°C ± 1. Una vez obtenido el sistema solidificado, las muestras continuaron en refrigeración, a esta temperatura.
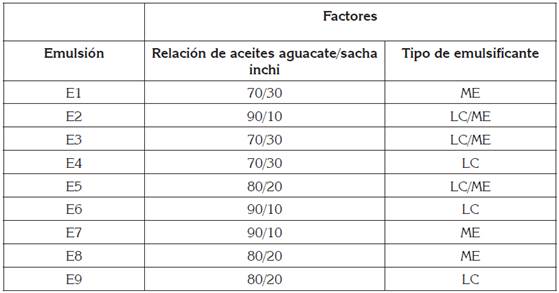
Diseño experimental: Se estableció un diseño factorial 3x3 completamente aleatorizado, para un total de 9 tratamientos. Los factores y los niveles establecidos en el estudio, se encuentran en la tabla 1. Se analizaron los datos experimentales estadísticamente, con un nivel de significancia del 5%, por medio de análisis de varianza (ANAVA), pruebas de diferenciación de medias, usando Statgraphics Centurion XVII software (versión 17.1.12, USA).
Determinación del color: El aspecto visual de los alimentos es una serie de características físicas, que incluyen el color, la turbiedad, la transparencia, entre otros y que, en conjunto muestran un panorama de la calidad del producto, razón por la cual, el color se puede usar como indicador de las transformaciones naturales o de los cambios ocurridos en el proceso de preparación de la emulsión. El color es definido como un haz de radiaciones luminosas, con una distribución espectral; los alimentos transparentes transforman la luz que les llega y la transmiten, a través de sus cuerpos, mientras que, los alimentos opacos, la reflejan. Esta transformación de la luz emitida incide en la retina del ojo y es la que, finalmente, conlleva a la evaluación final del producto. La evaluación colorimétrica, se realizó a través el sistema de coordenadas CIELAB, dado por un sistema cromático, mediante las coordenadas L, a* y b* (Moyano et al. 2008). Para este propósito, se utilizó el colorímetro X-RITE, modelo SP60, iluminante D65 y ángulo visual de 10°. A partir de los espectros, se obtuvo las coordenadas de color del CIEL*a*b*, donde L* es un indicador de la luminosidad a* (cromaticidad verde [-] a rojo [+]) y b* (cromaticidad azul [-] a amarillo [+]).
Firmeza: La medición de la fuerza máxima de penetración en los oleogeles, se llevó a cabo en el analizador de textura TA-XT2i. El espesor de la muestra fue de 4 cm; la sonda del equipo utilizada fue cónica, con ángulo de penetración de 30° (P/30C); la celda de carga fue 50kgf; la velocidad de deformación de 1mm/s y máxima profundidad de penetración de 1cm. La fuerza de firmeza fue considerada como la máxima de la curva de flujo del material (fuerza vs deformación). Se realizaron tres réplicas, donde la muestras a analizar fue el sistema oleo-estructurado solidificado durante refrigeración, a 4°C ± 1.
Determinación del índice de acidez (IA): El contenido de ácidos grasos libres, se determinó mediante la norma AOCS Official Method Ca, de 1997, expresado en porcentaje de ácido oleico.
Determinación del contenido de humedad: Para determinar la humedad en las muestras, se pesaron 3,00 ± 0,01g, que fueron sometidos a una temperatura de 105ºC, en un horno de convección forzada, durante 24h, hasta alcanzar un peso constante. La humedad, se determinó por diferencia de peso, de acuerdo con la norma AOCS Official Method 930.15, de 1990.
Determinación del índice de peróxidos: El análisis, se llevó a cabo mediante la norma AOCS Official Method cd 8-53, de 2003. Este método permite cuantificar la presencia peróxidos provenientes de la oxidación primaria de los lípidos. Estos tienen la capacidad de oxidar los iones hierro (Fe+2 a Fe+3), en soluciones de bajo pH. La oxidación resultante se cuantifica con ayuda de tiocianato que acompleja los iones hierro (Fe+3), generando una coloración medible por espectrofotometría UV.
RESULTADOS Y DISCUSIÓN
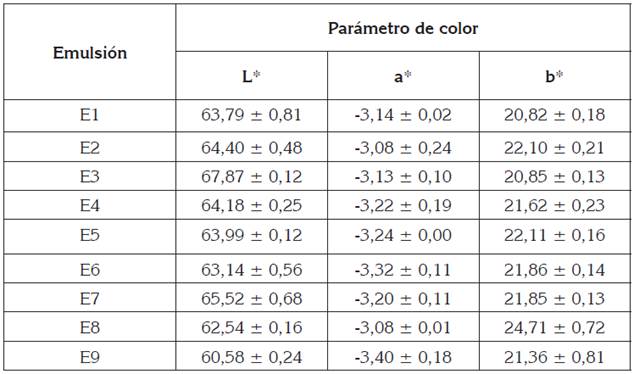
Color: La prueba ANAVA mostró diferencias significativas (p < 0,05), para el valor de la cromaticidad b* con respecto al tipo de emulsificante, donde los valores variaron entre 19,11 y 26,41, mientras que para los valores de la luminosidad L* y la cromaticidad a* no se presentaron diferencias significativas para ninguno de los factores ni su interacción (p > 0,05).
En la tabla 2, se muestras los valores de colorimetría, mediante el método CIELAB, para todas las formulaciones. Los valores a* negativos (coordenadas de verde a rojo), para las emulsiones, indican un ligero tinte verdoso, donde en la figura 1E, se puede observar que se obtienen valores más negativos, más tendientes al verde, cuando se usa una relación de aceite 90/10 y ME, como emulsificante, acorde con lo reportado para aceite de Sacha inchi, con valores de a* de -0,42 (Paucar-Menacho et al. 2015); para la oleína de palma, los valores de a* son alrededor de -6,86 (Vives, 2004) y los valores para la pulpa de aguacate variaba alrededor de -6,33 (Bi et al. 2015). El valor positivo de los valores de b * (coordenadas de azul a amarillo) indican que todas las emulsiones tenían un tinte amarillento, que aumentaba cuando se usaba la mezcla de LC/ME y una relación de aceite 90/10, como se muestra en las interacciones (Figura 1F). Estas diferencias en el color de la emulsión pueden ser atribuidas a diferencias en los colores intrínsecos de los tensioactivos, ya que, tanto ME como la LC, tenía un color amarillento. Estas diferencias concuerdan con lo reportado en emulsiones de café, donde se usó lecitina (Chung et al. 2017).
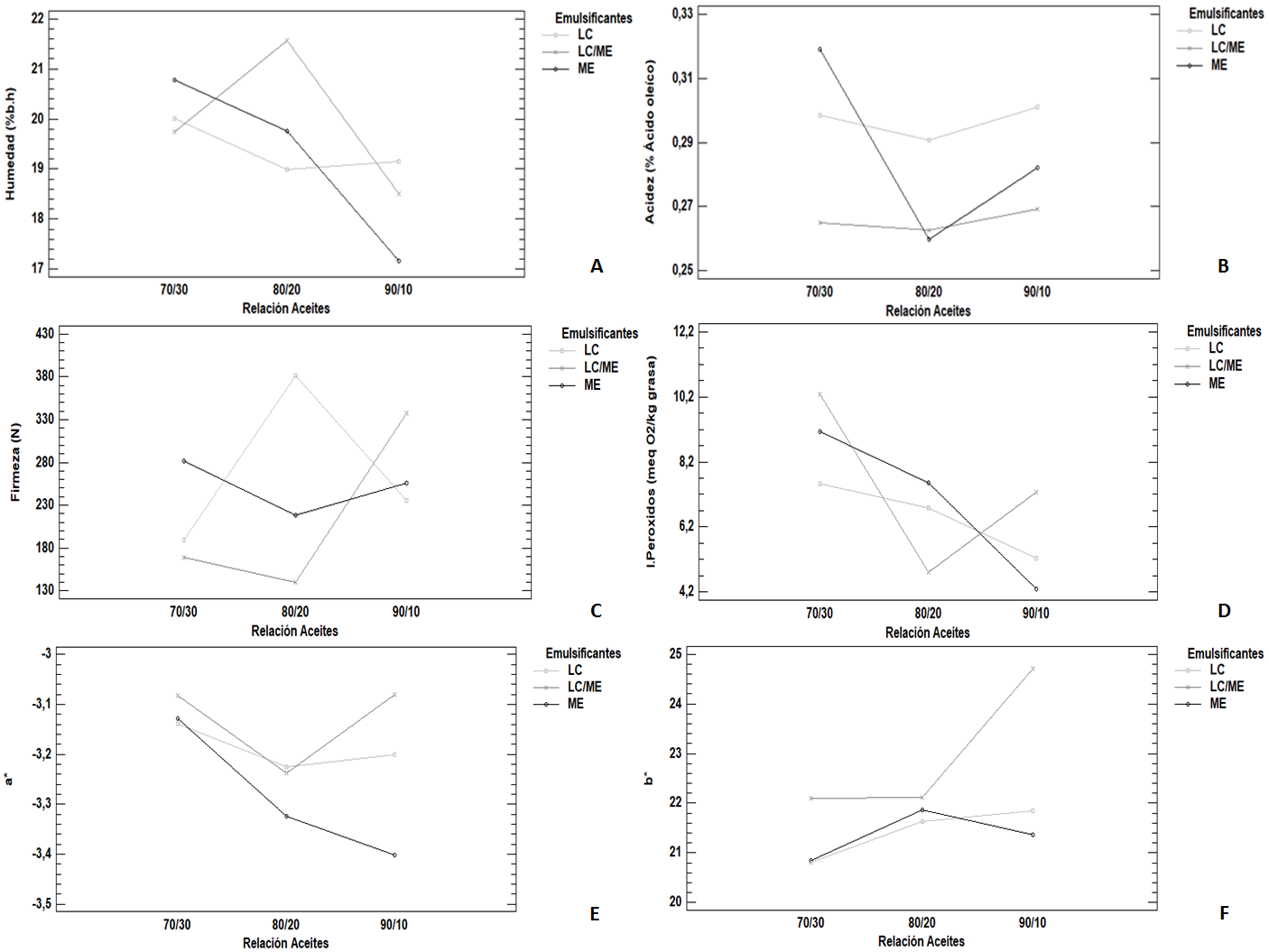
Figura 1 Interacciones de efectos para el tratamiento factorial: (A) Contenido de Humedad (%b.h); (B) Acidez (% ácido oleico); (C) Fuerza de Firmeza (N); (D) Índice de Peróxidos (meq O2/Kg de grasa); (E) Valor de la coordenada CIELAB a*; (F) Valor de la coordenada CIELAB b*
En cuanto a la luminosidad L*, sus valores alrededor de 63, muestran que las emulsiones son claras, mientras que en el reporte de aceite de aguacate, los valores fueron 11,52 (Castañeda-Antonio et al. 2015) y de 77,73 fueron obtenidos para aceite de Sacha inchi (Paucar-Menacho et al. 2015).De igual forma, el shortening latino está compuesto, principalmente, por oleína y por estearina de palma, cuyo valor de L* oscila alrededor de 80,72 (Rincón & Martínez, 2009), por lo tanto, la luminosidad de las emulsiones se puede atribuir, especialmente, al aceite de sacha inchi y al shortening latino.
Propiedades texturales de los oleogeles obtenidos: Esta evaluación, se hizo por penetrometría cónica, cuya sonda de medición es conducida en el oleogel cristalizado y la fuerza requerida para determinada profundidad de penetración total fue medida. Esta técnica ha sido ampliamente utilizada en la caracterización textural en productos alimenticios (Zúñiga et al. 2007).
Los valores de fuerza máxima de penetración para los oleogeles obtenidos oscilaron entre 0,89 y 4,79N, valores comparables con los obtenidos de aceite de girasol oleoestructurados con monoglicéridos y fitoesteroles, donde la fuerza máxima varió entre 1,3 y 6,0N (Kouzounis et al. 2017). De igual forma, se obtuvo oleogeles con aceite de girasol estructurado con monoglicéridos, cuya fuerza máxima varió de 0,40 y 2,95N (Palla et al. 2017). En el mismo estudio, se comparó con una margarina comercial, cuya media para la fuerza máxima de penetración fue de 1,60N, por lo tanto, es posible el desarrollo de un material con firmeza similar a las margarinas comerciales.
Al evaluar el efecto de la fuerza máxima, la prueba ANAVA, con un 5% de nivel de significancia, mostró que la interacción entre los factores tipo de emulsificantes y relación de aceites influye sobre la firmeza de los oleogeles y es estadísticamente significativa (p < 0,05). Por diferencia de medias, se obtiene que el valor de la mayor fuerza de firmeza fue para la formulación del oleogel preparado con una relación de aceites 80/20 y usando LC, como emulsificante (Figura 1C). Este resultado difiere de los resultados obtenidos para queso estructurado con almidón de tapioca y lecitina, donde se evidenció disminución de la firmeza, cuando se usó lecitina, por el debilitamiento de las estructuras creadas por las proteínas, a través de la hidratación, pero hubo una acción sinérgica que mejoraba la firmeza, cuando se usaba la combinación almidón de tapioca y lecitina. De igual forma, cuando se evalúa lecitina y triestearato de sorbitán, los dos componentes, individualmente en aceites vegetales, no dan estructura a concentraciones entre 6 y 20% p/p, mientras que se observa un efecto sinérgico con su mezcla, en relaciones específicas de lecitina: triesterato de sorbitan, entre 40:60 y 60:40, obteniéndose geles firmes (Pernetti et al. 2007); sin embargo, en estudios de caracterización de hidrogeles de emulsión oleo-estructurado a base de lecitina de soja con aceite de sésamo, se formaron geles en emulsión, cuando la concentración de lecitina de soja era mayor al 40% p/p (Singh et al. 2016); así mismo, se obtuvo sistemas oleoestructurados con aceite de girasol de dureza comparable con margarinas comerciales, cuando se usó 12% p/p, de monoglicéridos (Palla et al. 2017).
Índice de acidez: Con el índice de acidez, se determina la presencia natural de la acidez libre en las grasas, resultado de la hidrólisis o la descomposición lipolítica de algunos triglicéridos (Hidrólisis enzimática, tratamiento químico, o acción bacteriana). El índice de acidez, se define como el número de miligramos de KOH que se requieren para neutralizar los ácidos grasos libres, contenidos en un gramo de grasa. Debido a que la acidez de las sustancias grasas es muy variable, generalmente, las grasas frescas o recién preparadas no contienen ácidos grasos libres o, si los contienen, los tienen en muy pequeñas cantidades; al envejecer, principalmente, si no han estado protegidos de la acción del aire y la luz, su acidez crece lentamente, al principio y con cierta rapidez, después (Baldo et al. 2016).
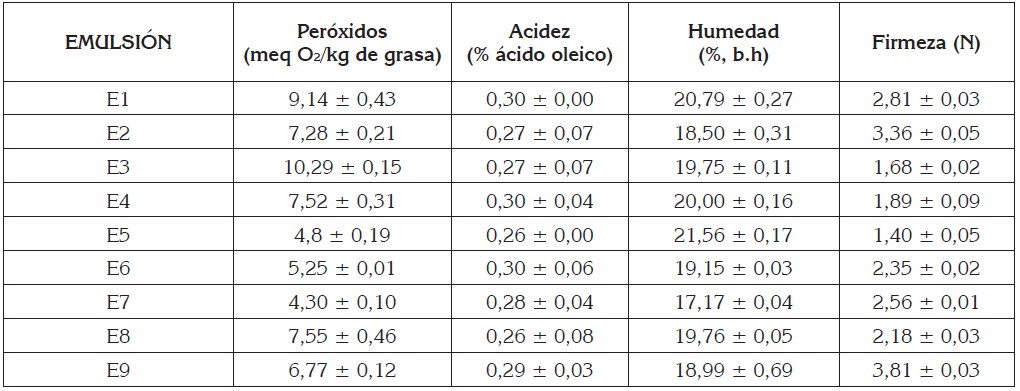
El análisis estadísticos para la acidez determinó que ninguno de los factores ni su interacción influyen sobre el índice de acidez, debido, posiblemente, a que en las formulaciones no varían en el contenido de grasa total sino la proporción entre los aceites de aguacate y de sacha inchi y, en ambos, predominan los ácidos grasos oleico y linoleico (Perez-Monterroza et al. 2014), por lo tanto, el contenido de los ácidos grasos libre no se ve modificado significativamente; lo anterior se observa en la Figura 1B. En la tabla 3, se muestra el valor de la acidez para todas las emulsiones, cuyo valores fueron iguales o inferiores a 0,3%, que es el máximo permitido, según lo indicado en la Norma Técnica Colombiana NTC 241, de 2002, para margarinas e, inferiores al 0,8 y 1%, que es el máximo permitido para aceite extra virgen de aguacate, según la Norma Técnica Colombiana NTC 199, de 2009 y para aceite de sacha inchi, según la Norma Técnica Peruana 151.400, de 2009, respectivamente. Valores de 0,16% fueron reportados para el aceite de aguacate, obtenido por fluidos súper críticos y de 0,48%, por métodos convencionales (Corzzini et al. 2017). Asimismo, se han reportado valores para aceite de sacha inchi, de 0,03 y 0,11%, mediante extracción soxhlet y fluidos súper críticos, respectivamente (Castaño T. et al. 2012) y de 1,14%, para aceite comercial (Paucar-Menacho et al. 2015). Valores en el índice de acidez se puede ver afectado por el tratamiento post-cosecha de la frutas o semillas, del método de extracción del aceite, exposición a la luz y a las altas temperaturas; de ahí, su variación en los valores reportados (Borges et al. 2017).
Contenido de humedad del sistema oleoestructurado: Para el contenido de humedad de las diferentes formulaciones, no se encontraron diferencias significativas (P>0,05) para los factores relación de aceite y tipo de emulsificante. El contenido de humedad varió entre 17,17 y 21,56% b.h, cumpliendo con el requisito de contenido de agua para los esparcibles de uso en mesa y en cocina. La norma colombiana NTC 241, de 2002, establece un porcentaje de humedad igual o superior al 16% b.h y en la figura 1A, se muestra las interacciones entre los factores.
Resultados similares en el contenido de humedad de 17,11 ± 0,41% b.h y 20,95 ± 0,49% b.h, se obtuvieron en margarinas preparadas con extracto hidro-etanólico de cáscaras de nopal (Opuntia ficus-indica) y vitaminas E, respectivamente (Chougui et al. 2015).
Índice de peróxidos: El índice de peróxido determina el contenido de peróxido de hidrógeno y proporciona una medida de la oxidación de los ácidos grasos insaturados. En la tabla 3, se observan los valores de índice de peróxido para todas las emulsiones, a excepción de una formulación, todos los valores se encuentran por debajo de la norma Mexicana, para aceite de aguacate, NMX-F-052-SCFI, de 2008 y de la Norma Técnica Peruana, para aceite de sacha inchi, de 2009, de 10meq O2/kg de aceite.
Se han reportado valores para el índice de peróxido en aceite de sacha inchi de 7,5meq O2/kg de aceite fresco (Vicente et al. 2015), mientras que para el aceite de aguacate se han reportado 5,26meq O2/kg de aceite fresco (Castañeda-Antonio et al. 2015); sin embargo, el valor del peróxido, se puede atribuir a muchos factores, como la variedad, las prácticas agrícolas y de las enzimas liberadas de las células de la fruta durante el proceso (Vargas-Ortiz et al. 2017).
Los resultados estadísticos mostraron efectos estadísticamente significativos (p < 0,05) para la relación de aceites, mientras que, el tipo de emulsificante no afecta el índice de peróxidos. Por diferencia de medias, se obtiene que una mayor proporción de aceite de sacha inchi favorece el proceso de oxidación o permite obtener valores más altos para el índice de peróxidos, como se observa en la figura 1D. En estudios realizados con aceites de ricino, de palma y de sacha inchi, se determinó que el aceite de ricino es el de menor grado de oxidación, lo que se explica por su bajo contenido ácidos grasos poliinsaturados, como linoleico y linolénico. Por el contrario, el aceite de sacha inchi es el de mayor grado de oxidación, debido a su alto contenido de ácidos linoleico y linolénico (Zuleta Suárez et al. 2012).
Es posible que el tipo de emulsificante no sea significativo en el índice de peróxido, debido a que, tanto la LC como el ME, actúan como conservantes y como modificadores de componente reológico; por su parte, la LC cumple función antioxidante, su actividad se debe principalmente a la acción de tocoferoles; la lecitina purificada puede ser menos activa como antioxidante primario, pero puede actuar como sinergista, en virtud de la capacidad de ligar iones metálicos. El monoestearato de glicerilo, por su parte, también es utilizado como agente conservador, debido a que actúa encapsulando las gotas de aceites presentes en la emulsión (Wang & Marangoni, 2016).
En conclusión, se obtienen oleogeles con valores de acidez y humedad, según lo establecido en la normatividad vigente colombiana. Adicionalmente, valores de peróxidos más altos son alcanzados cuando se usa mayor proporción de aceite de sacha inchi, debido al gran contenido de ácidos grasos poliinsaturados; a excepción del oleogel estructurado, con una relación de aceites 70/30 y LC como emulsificante, todos cumplen con el máximo permitido, para el índice de peróxido, de acuerdo con las normas reguladoras.
Se desarrollaron oleogeles con fuerza de firmeza comparable con margarinas comerciales para las emulsiones preparadas con una relación de aceites 80/20, usando como emulsificante Monoestertato de glicerilo o la mezcla lecitina -Monoesterato de glicerilo y la formulación con una relación de aceites 70/30, usando lecitina; sin embargo, dado que la emulsión preparada con una relación de aceite 70/30 y usando mezcla lecitina -Monoesterato de glicerilo-, no cumple en términos de índice de peróxidos, no se podría tomar como la mejor.
El tipo de emulsificante influyó en el color, específicamente, en la cromaticidad b*, que va del azul al amarillo, obteniéndose el valor máximo de cromaticidad, cuando se usa como emulsificante la mezcla LC/ME.