Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
TecnoLógicas
versión impresa ISSN 0123-7799versión On-line ISSN 2256-5337
TecnoL. no.28 Medellín ene./jun. 2012
Editorial
Interfaces electrohiladas para aplicaciones biomédicas
José María Lagaron
Consejo Superior de Investigaciones Científicas (CSIC) y BioInicia / FluidNatek S.L.
Valencia, España
El mercado médico constituye un sector dinámico dentro de las industrias de la salud que produce una amplia gama de dispositivos, equipamientos y consumibles para su empleo en el diagnóstico, prevención, monitorización y tratamiento de enfermedades o discapacidades en humanos. Se la considera como una industria relativamente joven, muy diversificada y poco cohesionada. La “European Medical Technology Trade Association” (Eucomed) estima la existencia de unas 7000 compañías médicas en Europa constituyendo un valor total de cerca de 54,8 billones de euros, alrededor del 30% de los ingresos mundiales del sector. Alemania es el país líder en tecnología médica europea con una cuota de mercado del 34,7% (19 billones), seguido de Francia con 16,4% (9 billones), Italia 11,2% (6 billones), Reino Unido 10,6% (5,8 billones) y España con el 5,5% (3 billones). Estos cinco países poseen el 78% del mercado, tal y como muestra la Fig. 1.
El segmento ortopédico es, junto al cardiovascular, comercialmente el más atractivo del sector médico por razones de tamaño, crecimiento y rentabilidad. Éste repercute aproximadamente en un 10% de los ingresos totales del mercado, siendo los llamados dispositivos reconstructivos, básicamente de rodilla y cadera, los tratamientos de mayor repercusión (Kruger, 2005). Específicamente, este tipo de implantes constituyen el 43% de los ingresos ortopédicos totales experimentando un crecimiento anual continuo de alrededor del 7,5%. De esta forma, según datos previstos para 2012, el segmento de los implantes ortopédicos podría llegar a unos ingresos anuales de 3,78 billones de euros (Frost & Sullivan, 2006). El aumento de la edad media de la población, la mayor práctica de actividades deportivas, el incremento de los accidentes de tráfico o laborales y la obesidad se encuentran entre los factores que favorecen el uso de estos implantes.
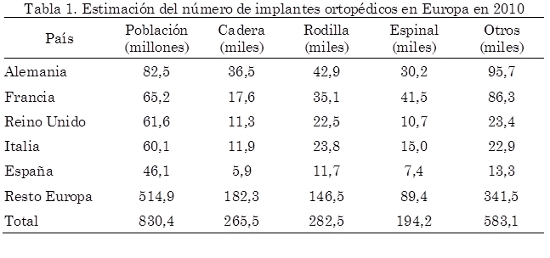
Otras previsiones del sector van todavía más lejos y aseguran que se prevé que las 250000 fracturas de cadera anuales que se producen en Europa en la actualidad pasen a 500000 en el 2050 (Gavrilov & Heuveline, 2003). Asimismo, cifras similares y con la misma tendencia se esperan para los implantes de rodilla. Según datos facilitados por la Eucomed, el número total de implantes de cadera, rodilla y espinal superaría las 750000 unidades anuales. La Tabla 1 presenta una estimación en 2010 del número anual de implantes ortopédicos presentes en Europa por países según la población censada.
Dentro del segmento ortopédico existen dos grandes grupos de dispositivos: los cementados y los no cementados. En los cementados un cemento adhiere el implante al hueso. Es el procedimiento que revolucionó el tratamiento de la artrosis de cadera a finales de la década de los 50, pero no es la solución total ni definitiva, como se creyó al comienzo de su aplicación. Este cemento, generalmente metilmetacrilato, no es adhesivo sino que al rellenar la cavidad fija los componentes protésicos. Los dos componentes, uno líquido (monómero) y otro en polvo (polímero), al juntarse hacen una masa que tras endurecerse ancla el implante al hueso. Por otra parte, se han confeccionado implantes no cementados, para eliminar el cemento, considerado como una de las causas involucradas en el aflojamiento.
Las prótesis no cementadas que se utilizan hoy en día empezaron a desarrollarse a partir de los años 70. Actualmente están indicadas para personas jóvenes o individuos que requieran una actividad física mayor. La experiencia ha demostrado que cuando se colocaba la prótesis cementada en personas más jóvenes, ésta era usada por ellas en forma indiscriminada, y el riesgo aflojamiento era mucho más alto. En algunos otros casos también puede optarse por una prótesis híbrida, en la que una parte del implante al requerir mayor movilidad se coloca sin cemento mientras el componente más estable es cementado. Se estima que alrededor de un 78% de las prótesis actuales llevan alguna parte no cementada, aunque en cualquier caso, la decisión final recae en el mismo cirujano. En ausencia de cemento, la unión es mecánica y el anclaje se produce mediante al menos uno de los siguientes métodos: fijación por diseño o presión, por superficie porosa que permite al hueso introducirse en los poros durante su crecimiento y, por último, un recubrimiento bioactivo con el que también el propio hueso efectúa la fijación, aunque a diferencia del caso anterior, éste es un concepto más biológico. Este último método de fijación requiere de la tecnología de superficies.
En la actualidad existen una gran variedad de prótesis no cementadas que presentan una superficie parcial o completamente recubierta con una superficie de material bioactivo, con variaciones en la composición del material, el espesor e incluso la pureza del recubrimiento. Desde los años 90, prácticamente la totalidad de estos recubrimientos están formados por capas superficiales de hidroxiapatita y otras cerámicas de fosfatos de calcio que pueden abarcar diferentes procesos, tanto físicos como químicos. El método industrial de recubrimiento más extendido de los implantes comerciales actuales se realiza mediante proyección térmica, en sus diferentes versiones, debido a su rapidez de aplicación y bajo coste de producción.
Si bien los resultados obtenidos demuestran un mejoramiento en la unión efectiva con el tejido óseo, que justifica su empleo con respecto a los implantes no recubiertos, aún persisten problemas relacionados con la uniformidad del recubrimiento, el agrietamiento de su superficie y la degradación térmica de las partículas. Estos factores han limitado en cierta forma las esperanzas inicialmente depositadas en esta técnica, implicando la realización de innumerables investigaciones para obtener un sistema alternativo de mayor calidad. Sin embargo, aunque los nuevos métodos solucionan algunos de estos problemas, actualmente éstos ofrecen una baja productividad y unos largos tiempos de procesamiento que restringen su aplicación en un proceso a gran escala. Adicionalmente, la tecnología basada en superficies cerámicas sigue ofreciendo dudas sobre una posible deslaminación del recubrimiento que pudiera provocar un aflojamiento aséptico de la prótesis y desgaste de las superficies de carga.
A causa de estas contrariedades, nuevos métodos basados en polímeros y sus composites con partículas duras están siendo desarrollados para ser aplicados en la tecnología de superficies. En este sentido, la tecnología del electroestirado posee la peculiaridad de procesar estructuras fibrilares que imitan la superficie ósea natural, lo que favorece la interacción del hueso con estos materiales. Los tejidos biomiméticos electroestirados pueden emplearse para recubrir las superficies de prótesis metálicas y de cualquier dispositivo biomédico en forma de interfaces hueso-implante. La base de estos materiales suele ser bioplásticos, es decir, polímeros de origen biológico que pueden ser resorbidos de forma natural por el organismo una vez hayan cumplido su función. Esto facilita la aplicación de las interfaces electroestiradas tanto para prótesis permanentes como para dispositivos temporales. Estas interfaces, a su vez, pueden incorporar las cerámicas bioactivas descritas anteriormente, lo que incrementa su rendimiento. Adicionalmente, pueden emplearse para la dosificación de fármacos y medicamentos, como por ejemplos anti-inflamatorios o antibióticos que faciliten el proceso post-operativo, lo que aumenta la funcionalidad final del producto. Por las ventajas citadas, las nuevas interfaces biomédicas electroestiradas suponen un nuevo producto funcional y tecnológicamente superior a los actuales.
En este contexto, nuestro grupo de investigación lleva trabajando en solucionar este tipo de problemas varios años y junto con la spin-off del CSIC, BioInicia S.L., ha desarrollado y patentado con éxito un nuevo recubrimiento altamente bioactivo con capacidad de liberación controlada de fármacos y también el equipamiento de laboratorio y planta piloto (marca FluidNatek) necesario para su fabricación para el sector biomédico.
Referencias
Frost & Sullivan, (2006). Advanced MedTech: Enabling Efficient and Outcomes-Oriented Healthcare Delivery, 2010 to 2012. [ Links ]
Gavrilov, L.A., Heuveline, P., (2003). Aging of population. In: Demeny P, McNicoll G (eds) The encyclopedia of population, Macmillan Reference USA, New York, 32-37. [ Links ]
Kruger, K., (2005). The medical devices sector. In L. R. Burns (Ed.), The business of healthcare innovation, United Kingdom: Cambridge University Press, 271-321. [ Links ]