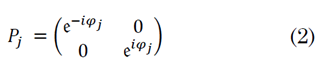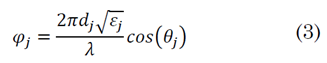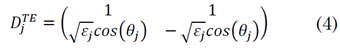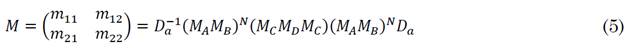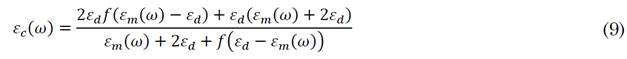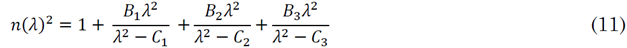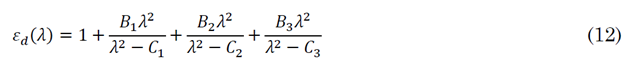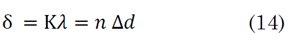1. INTRODUCCIÓN
Los cristales fotónicos (CF) son estructuras periódicas compuestas por capas alternadas de distinto nanomaterial, que afectan la propagación de la luz, dando origen a características ópticas únicas como las bandas fotónicas prohibidas (BFP). La luz dentro del BFP en determinados rangos de longitudes onda no se le tiene permitido propagarse, debido a la interferencia destructiva en las interfaces de las capas [1]. Sin embargo, al insertar ciertos defectos, la periodicidad del CF se rompe, permitiendo el paso de esta radiación [2], [3] [3]. Los CF’s pueden ser clasificados por la dimensionalidad de la periodicidad de la alternación del nanomaterial. Por tanto, podemos encontrarlos en una (1D), dos (2D) y tres (3D) dimensiones. Entre los materiales utilizados para construir estos cristales son los dieléctricos [4], semiconductores [5], superconductores [6], nanocompuestos [7], etc. Estas estructuras fueron estudiadas por primera vez en 1887 por Lord Rayleigh, quien descubrió que la propagación de la luz en medios estratificados unidimensionales puede ser totalmente reflejada dependiendo del ángulo de incidencia [8]. Luego, cien años más tarde en 1987, dos artículos por separado fueron publicados por Eli Yablonovitch y Sajeev John. Yablonovitch propuso que la BFP proporcionado por estructuras periódicas 3D podría suprimir la emisión espontanea [9], mientras que Sajeev propuso una super red dieléctrica desordenada para una fuerte localización de fotones [10].
Los cristales fotónicos unidimensionales (CF-1D), también conocidos como espejos de Bragg, han recibido considerable atención debido a su alta reflectividad, simplicidad en la fabricación en comparación con cristales fotónicos 2D y 3D, así como también a una gran cantidad de aplicaciones especialmente como reflectores [11], swtiches [12], controladores de polarización [13], sensores [14]-[15] y entre otros [16].
Recientemente, Francis et all., propusieron un CF-1D compuestos de capas alternadas de sílice fundida y agua marina, para la simultanea detección de salinidad y temperatura de determinadas muestras de agua. Ellos encontraron que, a medida que la temperatura aumentaba dejando la salinidad constante, el modo defectivo se corre a longitudes de ondas más cortas, y al mantener constante la temperatura aumentando la salinidad, el corrimiento se produce a longitudes de onda más largas [17].
El cáncer es actualmente una de las enfermedades con una alta tasa de mortalidad, debido a que la mayoría de los casos son diagnosticados en su etapa más avanzada (metástasis) [18], [19]. Según la organización mundial de la salud, en el 2012 el número de casos reportados globalmente fue de 14 millones y se estima que alcance 21.6 millones para el 2030 [20]. Por tanto, existe la necesidad de concebir nuevos dispositivos que sean asequibles y permitan su detección temprana, como biosensor [21]-[22].
Normalmente las células cancerígenas se han caracterizado por tener un índice de refracción mayor que las células normales que oscilan en un rango de 1.35-1.37, la gran acumulación de proteína en el núcleo es lo que origina la división incontrolable de estas células que destruyen los tejidos del cuerpo [23]-[24]. Los CF’s-1D, en virtud de sus propiedades ópticas, jugarían un papel decisivo como biosensor, ya que son bastantes sensibles a pequeños cambios de índice de refracción y su respuesta de detección es inmediata. Los analitos, cuando son infiltrados en forma de fluido en una nano cavidad defectiva dentro de la estructura periódica, proporcionan corrimientos únicos de longitudes de onda dentro del BFP, lo que permite caracterizar cada analito infiltrado con su respectiva sensibilidad.
Ramanujan et al. Propusieron un CF-1D para la detección de células cancerígenas, introduciendo una cavidad revestida de nanocompuestos con incidencia normal de la radiación. Ellos optimizaron el factor de relleno de las nanopartículas y el espesor de los nanocompuestos obteniendo una sensibilidad máxima de 43 nm/RIU [25].
En este trabajo optimizaremos la sensibilidad del dispositivo para la detección de cinco células cancerígenas diferentes, variando el ángulo de incidencia de la radiación y el espesor de la nano cavidad para la polarización TE y TM. El método de la matriz de transferencia (MMT) será implementado para el estudio de la propagación de esta radiación.
2. MODELO TEÓRICO
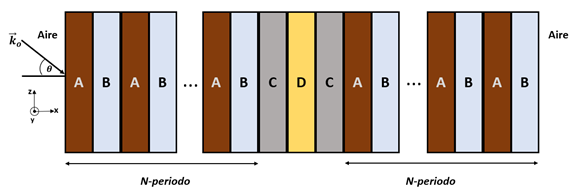
En la Fig. 1 se muestra la estructura del cristal fotónico unidimensional compuesto por la alternación de los materiales SiO2 (capa A) y aire (capa B) de espesores d1 y d2, respectivamente, con periodicidad N en el eje x. La simetría de translación se rompe al introducir la nano cavidad en el cual las muestras de las células son infiltradas (capa D) revestido por el nano compuesto de Ag/SiO2 (capa C) que se forma al mezclar las nanopartículas de plata con la sílice. El espesor para estos últimos materiales es denotado por d3 y d4, respectivamente.
Por medio del método de la matriz de transferencia [26] se estudiará la propagación de la luz con el ángulo incidente de la radiaciónθ para la localización de los modos de transmisión dentro del BFP con polarización TE y TM.
Se asume que los materiales del CF son isotrópicos y no magnetizados.
Para la polarización TE, la matriz para la j-ésima capa (=A, B, C y D) de espesores dj (d1, d2, d3 y d4) está representada por (1):
Donde P j es la matriz de propagación y está dada en (2):
La fase φ j se expresa como (3):
En (3) ε j es la constante dieléctrica, d j el espesor y θ j el ángulo de incidencia para la j-ésima capa (4).
D j es la matriz dinámica y está dada por (4):
Por lo tanto, la matriz de transferencia total para la estructura (AB)N(CDC)(AB)N puede ser calculada como se muestra en (5).
Donde D a es la matriz dinámica del aire que rodea al CF-1D defectivo,
La transmitancia es calculada con el elemento m 11 de la matriz M como (6).
De forma similar, para obtener la matriz para la j-ésima capa con polarización TM en (1), la matriz de propagación se mantiene intacta y el cambio se hace únicamente en la matriz dinámica que se encuentra dada en (7).
Por consiguiente, se calcula la matriz de transferencia total y la transmitancia utilizando (5) y (6).
La constante dieléctrica efectiva ε c (ω) del nanocompuesto es determinada usando (8) de Maxwell-Garnett [27]-[28].
Donde ε d es la constante dieléctrica de la sílice, ε m (ω) es la constante dieléctrica del metal en este caso plata, f es el factor de relleno de las nanopartículas y ω la frecuencia angular.
Ahora despejando (8) se obtiene ε c (ω) explícitamente como se muestra en (9).
La constante dieléctrica de las nanopartículas de metal ε m (ω) en este caso plata está dada por el modelo de Drude (10).
Donde ε o =5 es la constante dieléctrica relativa para la plata, ε p = 13.64 x 10 15 rad/s es la frecuencia del plasma de gases de electrones libres en un volumen infinito, y γ =3.03 x10 13 rad/s es la constante de amortiguamiento.
Finalmente, la constante dieléctrica de sílice ε d se obtiene por medio de la ecuación de Sellmeier [29] que relaciona el índice de refracción del material n con la longitud de onda λ está dada por (11). Teniendo en cuenta que n2 =ε, (12).
Donde B1=0.6961663, B2= 0.4079426, B3=0.8974794, C1=0.00467914826µm2, C2=0.0135120631µm2, C3= 97.9340025 µm2 son los coeficientes de Sellmeier determinados experimentalmente.
3. RESULTADOS Y DISCUSIÓN
Se considera que el medio de entrada y salida de la radiación es aire. Los espesores de las capas que componen el CF son: para la capa de sílice d1 = 268nm, capa de aire d2 = 388nm, capa del nano compuesto d3 = 90nm y el de la capa de la nano cavidad d4 = 90nm. Los espesores de las capas se eligieron un cuarto de longitud de onda cumpliendo con la relación nHdH=nL dL= λo/4 , donde λo es la longitud de onda con el cual se quiera trabajar. La periodicidad de las capas es N = 10 con un factor de relleno de las nano partículas de plata de 0.1.
El mecanismo de detección se debe a la aparición de picos de resonancia dentro de la banda fotónica prohibida que caracteriza a cada tipo de célula infiltrada por medio de biopsia líquida [30], [31], [32] en la nano cavidad, cuyas constantes dieléctricas se muestran en la Tabla 1. La sensibilidad del biosensor se determina teniendo en cuenta los corrimientos de los picos de resonancias de las células cancerígenas con respecto a la de una célula normal ∆λ, esto debido a los cambios de índice de refracción ∆n y es calculada en términos de nm/RIU de la siguiente forma (13):
Tabla 1 Constantes dieléctricas para una célula normal y distintas células cancerígenas

Fuente: [25].
En este trabajo se busca optimizar la sensibilidad del biosensor variando parámetros como el ángulo de incidencia, espesor de la nano cavidad y el factor de relleno para la polarización TE y TM.
Es decir, obtener la mayor respuesta óptica o separación de los picos de resonancia a pequeños cambios de índice de refracción.
La Fig. 2, muestra el espectro de transmitancia con incidencia normal de la radiación, al infiltrar distintos tipos de células en la nano cavidad. Se logró observar corrimientos de los picos de resonancia de las células cancerígenas hacia longitudes de onda más largas respecto a la célula normal. Este corrimiento se produce debido al incremento de la constante dieléctrica.
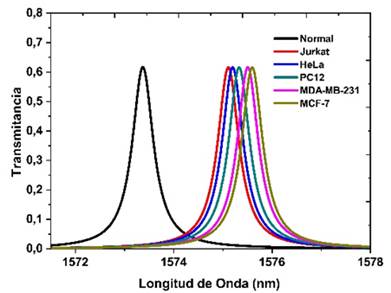
Fuente: elaboración propia.
Fig. 2 Picos de resonancia en presencia de distintas células con incidencia normal θ = 0°
En la Fig. 3, se muestra los efectos de incidencia oblicua de la radiación con polarización TE, consiguiendo corrimientos de los picos de resonancia hacia longitudes de ondas más largas, cuando se cambiaba de célula. Sin embargo, a medida que se incrementaba el ángulo de incidencia, los picos de resonancia se corrían a longitudes de ondas más cortas, con un decrecimiento en la transmitancia; esto se debe al aumento del camino geométrico que debe recorrer el haz de luz. Además, la separación entre los picos de resonancia de las células cancerígenas respecto a la célula normal se hacía mayor; esto se ve reflejado en la Tabla 2 con el cálculo de la sensibilidad. Para el caso de polarización TM, en la Fig. 4, de forma similar, se obtiene corrimientos a longitudes de onda más largas al cambiar la célula.
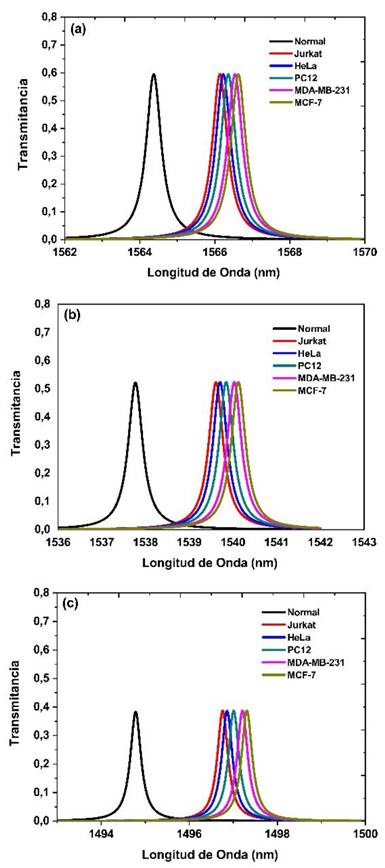
Fuente: elaboración propia.
Fig. 3 Transmitancia en función de la longitud de onda en presencia de distintas células para polarización TE a), b), c) con ángulo de incidencia θ = 25°,50°, 75°, respectivamente
Tabla 2 Sensibilidad del biosensor variando el ángulo incidente de la radiación para la polarización TE
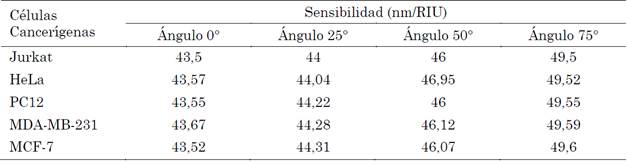
Fuente: elaboración propia.
Fuente: elaboración propia.
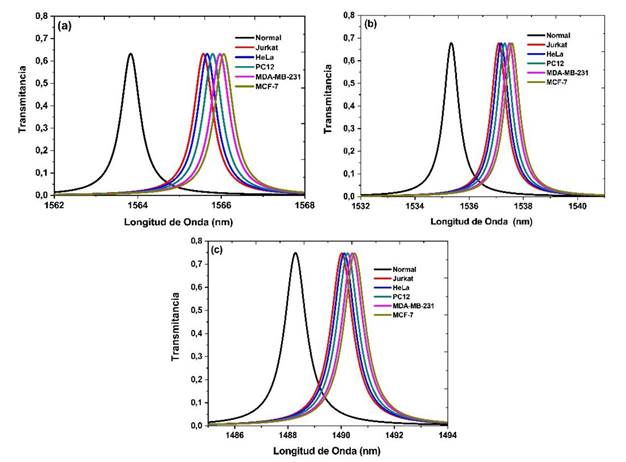
Fig. 4 Transmitancia en función de la longitud de onda en presencia de distintas células para polarización TM a), b), c) con ángulo de incidencia θ = 25°,50°, 75°, respectivamente
No obstante, el biosensor es mucho más sensible en el sentido de que los picos de resonancia se corren a longitudes de onda mucho más cortas que para el caso de la polarización TE. Adicionalmente, al aumentar el ángulo de incidencia la transmitancia aumenta y la separación de los picos de resonancia se mantiene casi constante. Esto se puede observar en la Tabla 3, cuando se calculó su sensibilidad en el cual solo existe un pequeño aumento a un ángulo de 50°.
Tabla 3 Sensibilidad del biosensor variando el ángulo incidente de la radiación para la polarización TM
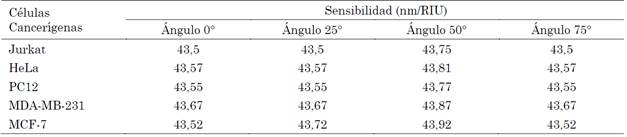
Fuente: elaboración propia.
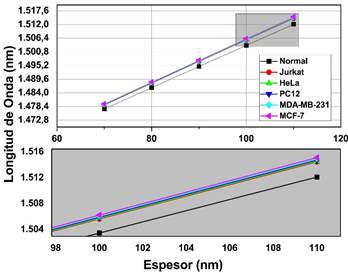
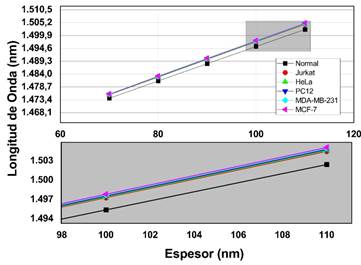
Ahora, se hace una optimización de la sensibilidad variando los espesores de la nano cavidad. Para ello se mantiene constante el ángulo de incidencia con el cual se obtuvo mayor sensibilidad, en este caso para polarización TE con ángulo de incidencia de 75° y para TM con ángulo de incidencia de 50°. La Fig. 5 muestra que para la polarización TE a medida que se incrementa el espesor de la nano cavidad los picos de resonancia se corren a longitudes de onda más largas para cada tipo de célula. Además, la separación de los picos entre la célula normal y las células cancerígenas aumenta. Así, obteniendo una mayor sensibilidad como se evidencia en la Tabla 4. De igual forma, ocurre el mismo efecto para la polarización TM donde existe un corrimiento de los picos de resonancia a longitudes de onda largas como se observa en la Fig. 6 y un aumento en la sensibilidad que se muestra en la Tabla 5.
Fuente: elaboración propia.
Fig. 5 Variación de los picos de resonancia en función del espesor de la nano cavidad TE con ángulo de incidencia 75°
Fuente: elaboración propia.
Fig. 6 Variación de los picos de resonancia en función del espesor de la nano cavidad TM con ángulo de incidencia 50°
Tabla 4 Sensibilidad del biosensor variando el espesor de la nano cavidad para la polarización TE con ángulo de 75°
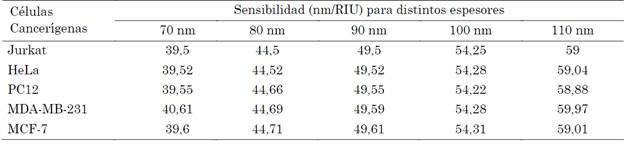
Fuente: elaboración propia.
Tabla 5 Sensibilidad del biosensor variando el espesor de la nano cavidad para la polarización TM con ángulo de 50°
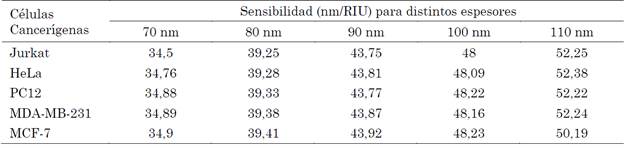
Fuente: elaboración propia.
Finalmente, se varía el factor de relleno de las nanopartículas de plata, manteniendo constante el espesor de la nano cavidad d4=90nm, y los ángulos de incidencia para polarización TE 75° y para la polarización TM 50°. Como se puede observar tanto en la Fig. 7 (a) para polarización TE como en la Fig. 7 (b) polarización TM para una célula normal, al aumentar el factor de relleno de las nanopartículas de plata, los picos de resonancia dentro del espectro de transmisión se acortan y hay corrimientos a longitudes de onda más largas. En el caso de infiltrar una célula cancerígena Jurkat ocurre el mismo fenómeno, como se muestra en la Fig. 8. El mismo efecto ocurre si se realiza la simulación para las células HeLa, PC-12, MDA-MB-231 y MCF-7.
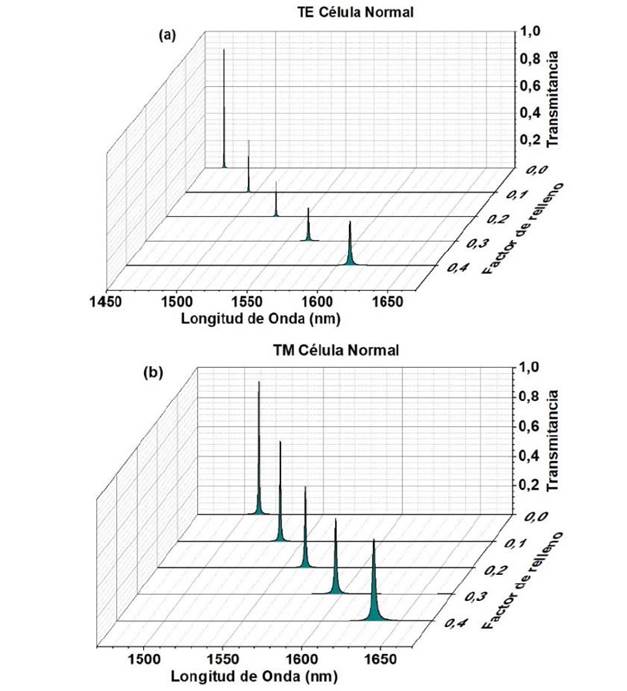
Fuente: elaboración propia.
Fig. 7 Picos de resonancia en función del factor de relleno para la célula normal con polarización a) TE con ángulo θ = 75° y b) polarización TM con ángulo θ = 50°
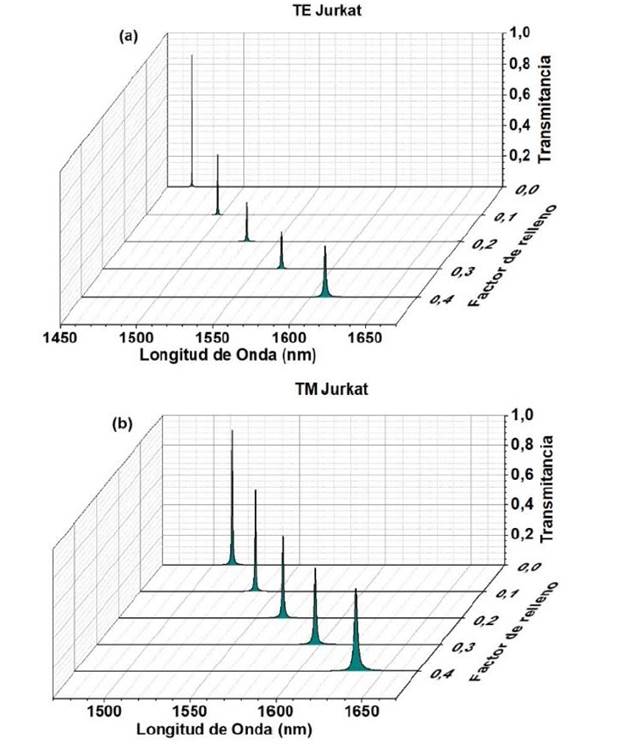
Fuente: elaboración propia.
Fig. 8 Picos de resonancia en función del factor de relleno para una célula cancerígena Jurkat con polarización a) TE con ángulo θ = 75° y b) polarización TM con ángulo θ = 50°
La Tabla 6 muestra los valores de la sensibilidad para la polarización TE con ángulo de incidencia de 75° para la célula normal y las células cancerígenas. Se pudo notar que existe una reducción de la sensibilidad al incrementar el factor de relleno de las nanopartículas de plata.
Tabla 6 Sensibilidad del biosensor variando el factor de relleno para la polarización TE con ángulo de 75°
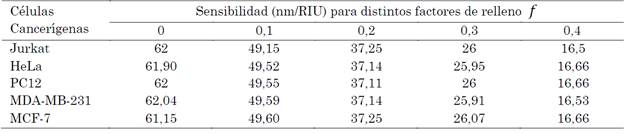
Fuente: elaboración propia.
De forma similar, la Tabla 7 muestra el mismo comportamiento para la polarización TM con ángulo de incidencia de 50°. En ambas, la mayor sensibilidad se consigue a un factor de relleno f=0. Es decir, cuando la sílice se encuentra en su forma pura. Sin embargo, los analitos preservan suscaracterísticas, debido a la mezcla de las nanopartículas de plata con la sílice. Por consiguiente, la mayor sensibilidad del biosensor se consigue a un factor de relleno de f=0,1.
Tabla 7 Sensibilidad del biosensor variando el factor de relleno para la polarización TM con ángulo de 50°
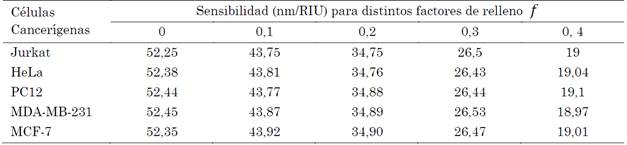
Fuente: elaboración propia.
Los corrimientos de los picos de resonancia ocurren debido al cumplimiento de la siguiente relación para ondas estacionarias (14) [33]:
Donde δ es la diferencia de camino óptico, K es un entero, λ es la longitud de onda de la radiación incidente, n el índice de refracción de cada célula y Δd es la diferencia de camino geométrico (espesor de la nanocavidad). Por tanto, al incrementar n debido al cambio de célula y manteniendo constante Δd y K, debe existir un incremento de λ.
4. CONCLUSIONES
Mediante el método de la matriz de transferencia se calculó el espectro de transmisión en un cristal fotónico unidimensional con la presencia de las células cancerígenas Jurkat, HeLa, PC-12, MDA-MB-231 y MCF-7. Se logró obtener la aparición de picos de resonancia que caracteriza a cada una de estas células, en el cual se corrían a longitudes de onda más largas cuando la constante dieléctrica de las células aumentaba. Se observó que para la polarización TE, al aumentar el ángulo de incidencia de la radiación, se obtuvo corrimientos de longitudes de ondas más cortas acompañado con el decrecimiento de la transmitancia y un aumento en la sensibilidad. Por otro lado, para la polarización TM se obtuvo corrimientos de longitudes de onda más cortas que en la polarización TE con un incremento en la transmitancia. Sin embargo, la sensibilidad se mantiene constante, excepto para el ángulo de 50° que tiene un pequeño aumento.
Finalmente, para una mayor optimización de la sensibilidad se variaron parámetros como: el espesor de la nano cavidad y factor de relleno de las nanopartículas de plata. Al aumentar el espesor de la nano cavidad encontramos corrimientos de los picos de resonancia a longitudes de más largas con un incremento en la sensibilidad, mientras que al aumentar el factor de relleno también se apreciaba corrimientos de los picos de resonancia a longitudes de onda más largas. Sin embargo, la sensibilidad decrecía. De esta forma, se logró obtener las condiciones necesarias para que la separación entre los picos de resonancia que caracterizan a cada célula cancerígena sea más distante respecto a la de una célula normal, de tal forma que permita una detección mucho más clara.