Introducción
La leucemia mieloide aguda (LMA) es una enfermedad heterogénea, para la cual, antes de los años setenta, fue difícil encontrar una estrategia de tratamiento eficaz, por esta razón la tasa global de curación tardó más tiempo en mejorar en comparación con las de las leucemias linfoblásticas agudas (LLA) 1,2.
Con el objetivo de mejorar los resultados, en 1978 el grupo Berlin-Frankfurt-Munster (BFM) inició estudios sucesivos de protocolos en LMA con la estrategia de incrementar sucesivamente la intensidad del tratamiento en cada uno. El estudio AML-BFM 93: administraba a los pacientes una terapia de inducción con ADE (arabinocido de citocina, daunorrubicina, etopósido), realizaba una clasificación de los pacientes en dos grupos de riesgo basado en las características genéticas y en la respuesta a la quimioterapia de inducción y usaba altas dosis de arabinocido de citocina y mitoxantrona (HAM por su sigla en inglés) antes y después de la consolidación en los pacientes de alto riesgo. Todos los pacientes recibieron intensificación con altas dosis de citarabina y etopósido y mantenimiento. El estudio mostró una supervivencia global de 5 años en el 57% de los tratados con HAM temprano y en el 54% de los pacientes en el brazo de HAM tardío 3-5.
En el Instituto Nacional de Cancerología de Colombia (INC) durante el periodo comprendido entre 1990 y 1994 se trataron 55 pacientes con protocolos diferentes a la estrategia BFM con una supervivencia a 5 años de 0%. En el periodo 1995 a 1997 se registraron 33 pacientes y la supervivencia lograda a 3 años de seguimiento fue del 3%. El 2 de febrero de 1998 se inició la aplicación del tratamiento basado en el protocolo BFM-93, conocido como BFM-93 modificado para MISPHO (Escuela Internacional de Hemato-Oncología Pediátrica de Monza). En los 23 pacientes incluidos entre 1998 y 2000 el 73,9% lograron la remisión completa y una supervivencia global de 20,4% con una mediana de supervivencia de 11 meses 6.
Con el propósito de mejorar la supervivencia libre de evento y la supervivencia global alcanzada con el esquema de tratamiento BFM-93 modificado para MISPHO, en mayo de 2004 se inició un protocolo de tratamiento basado en el esquema de tratamiento BFM-93 original 7,8 que se denominó LMA-INC 2004, donde se establecieron las bases para aplicar el tratamiento ajustado a una clasificación por grupos de riesgo. Un análisis inicial realizado en junio de 2008 con los primeros 18 pacientes mostró una supervivencia general del 44,7% (Ruiz VM, Suárez A, Venegas M. Evaluación del protocolo LMA-INC 2004. Trabajo de grado; Universidad Javeriana - Instituto Nacional de Cancerología. 2008).
El presente artículo tiene como finalidad mostrar los resultados logrados después de 10 años de instaurado el protocolo de tratamiento LMA-INC 2004.
Pacientes y métodos
Se realizó el estudio de una cohorte retrospectiva con análisis de supervivencia, en la que se incluyeron todos los pacientes menores de 18 años de ambos sexos que ingresaron a la clínica de oncología pediátrica del Instituto Nacional de Cancerología con diagnóstico de LMA tratados con el protocolo LMA-INC 2004 entre el 15 de mayo de 2004 y el 31 de diciembre de 2014 (tabla 1). Se excluyeron los pacientes con diagnóstico de LMA M3, LMA como segunda neoplasia, LMA realizado fuera del INC y que al ingreso hubieran recibido tratamiento de inducción a la remisión.
Tabla 1 Protocolo de tratamiento LMA-INC 2004
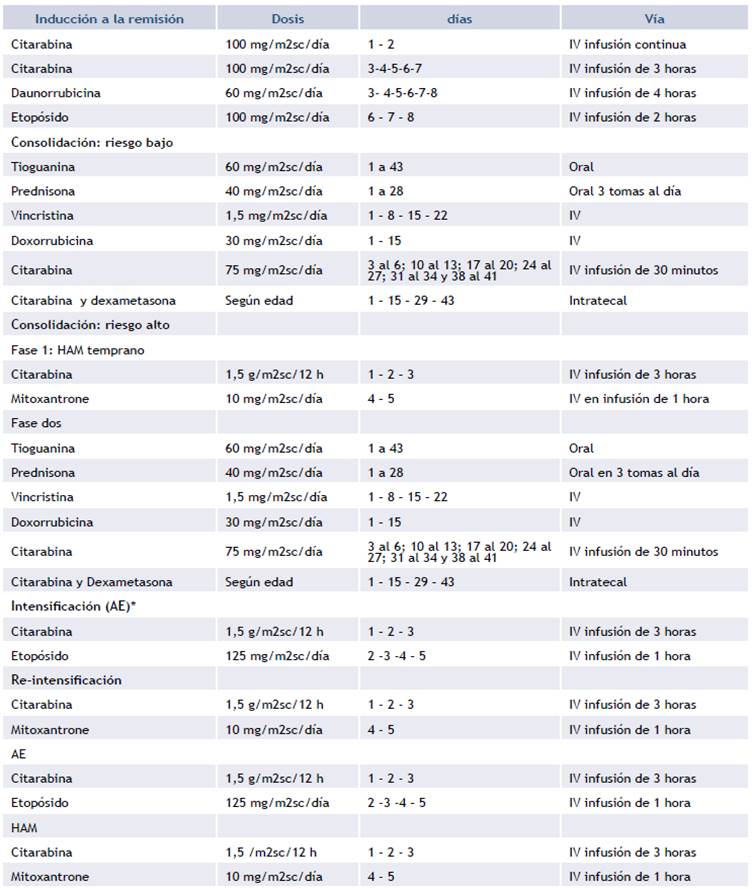
* Los pacientes de bajo riesgo reciben 4 bloques AE con intervalos de 21 días y los de alto riesgo un bloque de AE seguidos de reintensificación.
Todas las muestras de mielograma y biopsia de médula ósea fueron analizadas al momento del diagnóstico y en cada evaluación de respuesta por el Grupo de Hematopatología. Para el estudio morfológico se utilizó la clasificación French-American-British (FAB), se realizó inmunohistoquímica e inmunofenotipo por citometría de flujo y se practicó análisis de citogenética.
A todos los pacientes se les practicó punción lumbar para toma de líquido cefalorraquídeo (LCR) y la muestra enviada al grupo de patología y al laboratorio central para citología y citoquímico.
Los pacientes fueron clasificados al momento del diagnóstico en dos grupos de riesgo: el grupo de riesgo bajo abarcaba todas las LMA con morfología M1, M2 con bastones de Auer y M4 con eosinofilia y que documentaran menos del 5% de blastos en médula ósea en el día 15 de tratamiento de inducción a la remisión y la remisión completa al final de la inducción y el grupo de riesgo alto comprendía al resto de las LMA que no cumplieran las anteriores condiciones.
Los medicamentos y las dosis de los medicamentos del protocolo de quimioterapia son presentados en la tabla 1.
Todos los pacientes sin infiltración al sistema nervioso central (SNC 1: ausencia de blastos en líquido cefalorraquídeo) al diagnóstico recibieron quimioterapia intratecal durante la inducción a la remisión en el día 15 y en la consolidación los días 1, 15, 29 y 43 de tratamiento, ningún paciente recibió radioterapia como profilaxis. Los pacientes con infiltración del sistema nervioso central (SNC 2: presencia de blastos en líquido cefalorraquídeo con leucocitos mononucleares < 5 o SNC 3: presencia de blastos con leucocitos mononucleares > 5) recibieron quimioterapia intratecal con citarabina y dexametasona los días 2, 9, 15, 22 y 29 en la fase de inducción y los días 1, 15, 29, 43 y 50 durante la fase de consolidación y al terminar la fase de intensificación se enviaron a radioterapia con la propuesta de 1.800 cGy holoencéfalica en fracciones de 180 cGy cinco días a la semana.
Se realizó un análisis descriptivo mediante el uso de frecuencias absolutas y relativas para las variables nominales y ordinales. En las variables numéricas continuas que se distribuyeron de manera normal se utilizaron: la media como medida de tendencia central y la desviación estándar como medida de dispersión. Se estimaron funciones de supervivencia mediante el método de Kaplan Meier.
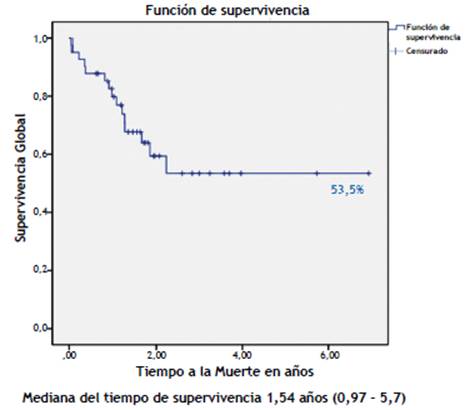
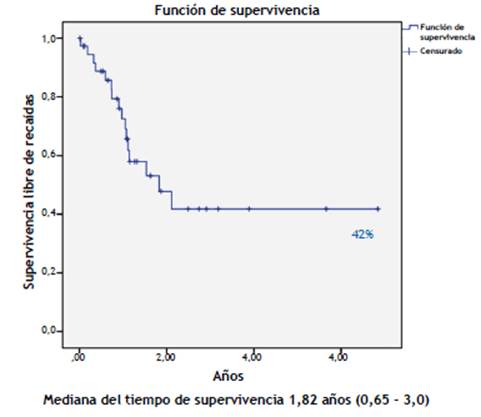
Para el cálculo de la función de supervivencia libre de recaída y supervivencia global, se definieron los siguientes tiempos: el tiempo a la recaída (supervivencia libre de recaída) como el tiempo transcurrido desde la fecha en que se documentó la remisión completa hasta la fecha de la primera recaída de la enfermedad y el tiempo a la muerte (supervivencia global) el tiempo transcurrido desde la fecha del diagnóstico a la fecha de la muerte por cualquier causa. Los pacientes que no presentaron evento a la fecha de la recolección de la información fueron censurados en la fecha del último control.
Los análisis estadísticos fueron realizados en el programa SPSS®.
Por tratarse de un estudio observacional retrospectivo este fue considerado como una investigación sin riesgos éticos para los pacientes y fue aprobado por el comité de ética en investigación del INC.
Resultados
Entre mayo de 2004 y diciembre de 2014 ingresaron a la clínica de oncología pediátrica del Instituto Nacional de Cancerología 90 pacientes con diagnóstico de LMA, de los cuales 24 eran LMA premieloicítica (M3) y 25 venían con diagnóstico establecido pero tratados en otras instituciones.
Cuarenta y un pacientes (n=41) cumplieron los criterios para LMA y recibieron el protocolo de tratamiento LMA-INC 2004; su edad promedio fue de 8,7 años (DE: ± 4,9) con predominio del sexo masculino (razón M:F=2,7); la mayoría residía en el área urbana, y el 87% (36/41) de los pacientes pertenecía al régimen de seguridad social subsidiado y el 13% (5/41) al régimen contributivo.
La LMA M2 fue la variante morfológica más frecuente, 19/41 (46,3%), seguida de la M5, 13/41 (31,7%). En 12 pacientes la presentación clínica inicial fue una masa sin compromiso de la médula ósea (sarcoma granulocítico).
No se pudo realizar el estudio de valoración citogenética en aproximadamente un tercio de los pacientes y en otro tercio el resultado fue de un cariotipo normal. En los 15 pacientes (36%) donde hubo una anomalía genética demostrada, la más frecuente fue la t(8,21). El 26,8% de los pacientes tenían infiltración del sistema nervioso central al diagnóstico y se demostró coagulación intravascular diseminada en el 12,2% de los casos al momento de su ingreso al hospital.
De los 41 pacientes tratados con el protocolo LMA-INC 2004, 19 (46,3%) fueron clasificados como riesgo estándar y el resto fueron clasificados y tratados dentro del grupo de riesgo alto, aunque en un paciente no fue posible su clasificación y fue tratado como riesgo alto. La tabla 2 muestra las características demográficas, clínicas y paraclínicas de la cohorte.
Tabla 2 Características demográficas, clínicas y paraclínicas de 41 pacientes con diagnóstico de LMA no LMA M3 tratados con el protocolo LMA-INC 2004 en el Instituto Nacional de Cancerología de Colombia.
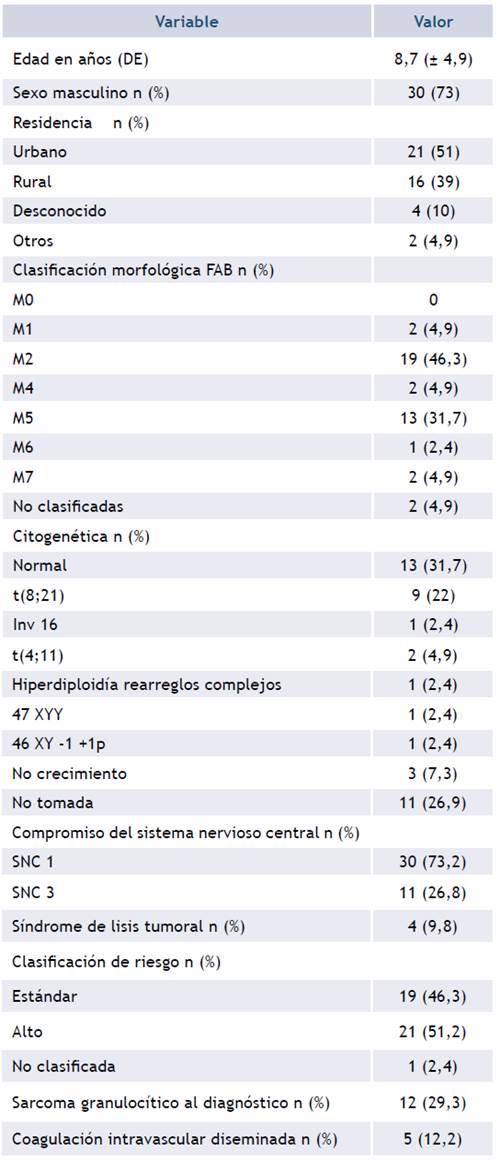
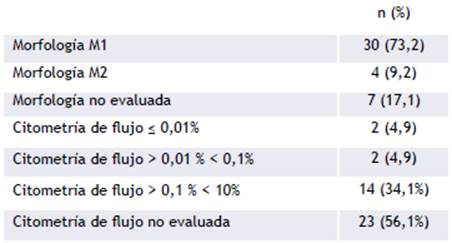
La remisión completa se obtuvo en 31 pacientes (75,6%). Dieciséis niños murieron, de los cuales, cinco muertes se presentaron como muerte temprana durante la inducción a la remisión (tabla 3). La evaluación de la médula ósea al día 15 de inducción a la remisión mostró que 30 pacientes (73,2%) lograron tener menos de 5% de blastos, aunque la cifra real de niños con más del 5% de blastos al día 15 de tratamiento no fue posible conocerla debido a que en el 17% de pacientes no fue posible realizar la evaluación. En la tabla 4 se muestra la respuesta morfológica y por citometría de flujo al día 15 de tratamiento.
Tabla 3 Curso clínico en 41 pacientes con diagnóstico de LMA no LMA M3 tratados bajo el protocolo LMA-INC 2004 durante 2004-2014 en el Instituto Nacional de Cancerología de Colombia.

Tabla 4 Características morfológicas y de citología de flujo en las médulas óseas al día 15 de tratamiento.
En la figura 1 y 2 se muestra que la supervivencia general acumulada a dos años fue de 60% y a cinco años fue de 53,5% con mediana de seguimiento de 1,54 años (0,97- 5,7 años) y la supervivencia libre de recaída a cinco años fue de 42% con mediana de 1,82 años (0,65 - 3,0 años).
Discusión
El grupo Berlin-Frankfurt-Munster (BFM) inició los estudios en LMA desde 1978 con estudios sucesivos (AML- BFM 78, AML-BFM 83, AML-BFM 93, AML-BFM 97) con un incremento de la intensidad del tratamiento en cada estudio 9. Desde 1983 se inició el protocolo de tratamiento AML-BFM 83 que introdujo la inducción a la remisión con el esquema ADE seguidos de 8 semanas de consolidación, profilaxis al SNC con radioterapia y mantenimiento, y se logró una mejoría en la supervivencia libre de evento desde 37% en el estudio AML-BFM 78 al 47% en AML-BFM 83 9.
En el estudio BFM 87 se mantuvo la terapia de inducción, pero se redujo la consolidación a 6 semanas y se administró dos ciclos posconsolidación con altas dosis de citarabina y etopósido (HAE); se mantuvo la radioterapia al SNC y el mantenimiento y se inició el trasplante de células progenitoras hematopoyéticas a los pacientes de alto riesgo. Los resultados mostraron una remisión completa al final de inducción de 75% con una supervivencia global del 49% 9,10.
Con el propósito de mejorar los resultados se implementó el AML-BFM 93 que mantuvo la inducción con ADE, clasificó los pacientes en los dos grupos de riesgo basado en las características genéticas y en la respuesta a la quimioterapia al día 15 y al final de la inducción se introdujo el uso de altas dosis de mitoxantrona antes y después de la consolidación (HAM temprano y HAM tardío) en los pacientes de alto riesgo. Todos los pacientes recibieron intensificación con HAE (altas dosis de citarabina y etopósido) y mantenimiento. El estudio mostró un incremento al 82% de la remisión completa al final de inducción, al 60% y 57% de supervivencia global y libre de eventos 5 años y al 61% libre de enfermedad 11,12.
Los resultados de la cohorte de pacientes incluidos en este trabajo muestran que una ligera mayoría pertenecían al grupo de alto riesgo (51%), lo cual es similar a lo mostrado en el trabajo original del AML-BFM 93 (65%).
También se pudo evidenciar baja frecuencia del subtipo M1 (4,9%) con respecto al 13% al 20% informado en otros grupos y por el contrario una elevada frecuencia del subtipo M2 (46%) contra el 26% al 30% de lo informado en los estudios BFM 13,14; esto podría ser resultado de una sobreclasificación del subtipo M2 basado en los criterios morfológicos debido a que el criterio del grado de maduración puede estar influenciado por la subjetividad en la interpretación.
La literatura refiere compromiso del sistema nervioso central al diagnóstico entre el 5% y el 15% 15 que contrasta con un incremento en su compromiso, de dos a cinco veces más (26%) en la serie presentada, pero que está muy cerca del reportado por el estudio del COG (Children Oncology Group) AAML0531 16 con el 29,2°% (SNC 2: 19,6°% y SNC 3: 9,6°%).
Con el protocolo LMA-INC 2004 la remisión completa al final de la quimioterapia de inducción fue del 75,6%; si bien es igual a los resultados del AML-BFM 87 (75%), no mostró una mejoría a lo logrado con el tratamiento administrado en años anteriores en el Instituto Nacional de Cancerología con el protocolo BFM 93 modificado para MISPHO 6 que obtuvo el 75% y es significativamente inferior al resultado del AML-BFM 93 original 11 que logró un 82%. Sin embargo, las muertes en inducción de todo el grupo estudiado fueron de aproximadamente un 5%, lo cual es comparable con los eventos fatales ocurridos en el BFM 93 que se presentaron en el 4% de los pacientes que recibieron HAM temprano y el 5% de los incluidos en el brazo del HAM tardío 11.
Los resultados en términos de supervivencia libre de evento y supervivencia global a cinco años del protocolo BFM 93 son significativamente mejores que los obtenidos en los estudios previos del AML-BFM y similares a los del United Kingdom Medical Research Council (MRC AML-10), que utilizando cuatro ciclos de quimioterapia intensiva logró como resultado una reducción de la mortalidad en inducción al 3% y supervivencia global a siete años del 56% y libre de evento de 48% 17.
Con el protocolo LMA-INC 2004 se encontró una supervivencia global a cinco años del 53,5% (media de seguimiento de 4,3 años) y una supervivencia libre de recaída del 43,2% (media de seguimiento 3,5 años); si bien estas cifras son inferiores a lo mostrado en los países desarrollados 18 es muy importante resaltar que con este protocolo de tratamiento se logró una mejoría del 30% en la supervivencia global y libre de recaída con relación al tratamiento con el protocolo anteriormente utilizado en el Instituto Nacional de Cancerología durante el final de los noventa y dramáticamente superior a lo observado a principios de esa década 6. Esta mejoría se debe a los procesos en cuanto a la precisión en los sistemas de diagnóstico y tipificación del riesgo y los tratamientos de soporte aunados a un tratamiento más intenso, que incluye la administración de altas dosis de citarabina y mitoxantrone en las fases de consolidación e intensificación.
Se reconocen como debilidades de este trabajo, en primer lugar, que el carácter retrospectivo del estudio impuso limitaciones por la presencia de datos faltantes en algunas variables y en segundo lugar que el tamaño de la muestra es pequeño y puede restar poder a las conclusiones del estudio y por la misma razón no es posible realizar análisis multivariables para factores pronósticos.
En conclusión, la gran mejoría observada en la supervivencia de los pacientes tratados con el protocolo LMA-INC 2004 es un logro importante que impone el reto de mejorar la estrategia de tratamiento de los niños con LMA para alcanzar las cifras de supervivencia de países más desarrollados.