Introducción
Gracias al impacto que la quimioterapia ha tenido sobre la supervivencia de las personas con cáncer, este es uno de los tratamientos más utilizados para dicha enfermedad. El uso de la quimioterapia se puede dar en cualquier etapa del tratamiento, desde la neoadyuvancia hasta el soporte paliativo 1,2. Sin embargo, la acción de los agentes antineoplásicos utilizados en quimioterapia no está limitada a las células tumorales, sino que afecta también a las células normales 3. En consecuencia, se observan efectos tóxicos importantes sobre diversos órganos. Los agentes quimioterapéuticos más tóxicos son los citostáticos, que afectan no solo a las células neoplásicas sino también a las de la médula ósea, el tracto digestivo y el folículo piloso, entre otras 4,5.
Más del 90% de los medicamentos de quimioterapia disponibles causa complicaciones de tipo gastrointestinal, y de estos, aproximadamente el 30% pueden causar síntomas gastrointestinales graves 6. Entre los síntomas más comunes, relacionados con el uso de agentes quimioterapéuticos, están náusea y vómito 4, disgeusia, mucositis, queilitis, glositis, estomatitis, esofagitis, diarrea, estreñimiento e íleo paralítico 4,5,7,8. Los síntomas de la toxicidad gastrointestinal no suelen ser duraderos, aunque algunos tratamientos de quimioterapia combinada ejercen efectos gastrointestinales intensos y prolongados 4.
Si bien los nuevos tratamientos quimioterapéuticos que bloquean dianas moleculares específicas han demostrado ser beneficiosos en el tratamiento de diferentes tipos de tumores, también ejercen actividad sobre las células normales, dando lugar a efectos adversos con un amplio espectro, como los gastrointestinales, debido a que el factor de crecimiento epidérmico (EGFR, por sus siglas en inglés) se sobreexpresa con frecuencia en la mucosa gastrointestinal normal 9.
Desde hace varias décadas se reconoce que el estado nutricional de los pacientes con cáncer se ve afectado no solo por la enfermedad, sino también por los diferentes tipos de tratamiento, entre ellos la quimioterapia y sus efectos secundarios 10. Síntomas gastrointestinales como vómito, náusea, mucositis, queilosis, glositis, estomatitis, esofagitis y estreñimiento, que son causados por diferentes agentes quimioterapéuticos, pueden disminuir o inhibir el consumo de alimentos en el paciente; la diarrea, otro síntoma secundario común, puede aumentar las pérdidas de nutrientes 5,11. Al parecer, otro síntoma que impacta de manera relevante la ingesta de alimentos es la sensación de saciedad temprana 12-14. Todos estos síntomas llevan a alteración del estado nutricional, que en el paciente oncológico implica estancias hospitalarias más prolongadas, menor respuesta terapéutica, mayores complicaciones asociadas al tratamiento para el cáncer 4,14 y aumento de la morbimortalidad 15.
Actualmente, el método utilizado para ajustar la dosis de los medicamentos antineoplásicos está basado en el área de superficie corporal (BSA, por sus siglas en inglés), que tiene en cuenta la altura y el peso de los pacientes, sin tomar en consideración las proporciones de masa grasa, masa libre de grasa y agua corporal total 9.
La evaluación de la toxicidad gastrointestinal posterior al tratamiento quimioterapéutico del paciente oncológico es esencial para instaurar medidas orientadas a evitar el deterioro del estado nutricional secundario a síntomas gastrointestinales y con ello favorecer la tolerancia y la adherencia al tratamiento para mejorar la calidad de vida del paciente 5. Dicha evaluación requiere del uso de instrumentos válidos y confiables, como una escala que permita determinar la presencia e intensidad de tales síntomas y que a la vez se constituya en una herramienta útil para los profesionales de la salud, para identificar de manera sencilla y objetiva la necesidad de intervención médica o nutricional.
En oncología no existe una escala diseñada exclusivamente para medir síntomas gastrointestinales. Son utilizados los cuestionarios EORTC QLQ-C30 (16) y FACIT-G 17, los cuales fueron desarrollados para evaluar calidad de vida en pacientes con cáncer y contienen pocos ítems relacionados con sintomatología gastrointestinal. Otras escalas como la ECOG y la escala de Karnofsky miden principalmente la capacidad funcional del paciente, mientras que la escala Rotterdam Symptom Checklist (RSCL, por sus siglas en inglés) es un cuestionario compuesto por 39 ítems, que dentro de los síntomas gastrointestinales solo evalúa náusea, vómito, boca seca, falta de apetito, acidez estomacal y estreñimiento 18. Finalmente, el Inventario de Síntomas MD Anderson (MDASI, por sus siglas en inglés) está compuesto por 19 ítems que se agrupan en dos escalas: afectación de los síntomas al estilo de vida (6 ítems) e intensidad de los síntomas (13 ítems), esta última únicamente para náusea, vómito y sequedad bucal 18,19. Por lo tanto, si se quiere aplicar un instrumento para evaluar de manera adecuada los efectos gastrointestinales secundarios a quimioterapia, se hace necesario generar una nueva escala a partir de la población objetivo o adoptar escalas disponibles en otros idiomas, lo cual exige efectuar su traducción y adaptación transcultural 20. Aunque es muy atractivo elaborar un instrumento nuevo, su construcción y validación consumen mucho tiempo y recurso humano. Es por ello que se recomienda, en la medida de lo posible, usar instrumentos ya existentes 21.
Actualmente, en Colombia no se dispone de instrumentos validados que permitan evaluar exclusivamente sintomatología gastrointestinal en pacientes oncológicos ambulatorios tratados con quimioterapia. El objetivo de este estudio fue realizar la traducción y adaptación transcultural del componente de síntomas gastrointestinales de la escala Terminología común para los eventos adversos en pacientes con cáncer (CTCAE, por sus siglas en inglés) versión 4.02 en pacientes ambulatorios que recibieron tratamiento quimioterapéutico en el Instituto Nacional de Cancerología en Bogotá. Los resultados de este estudio se enmarcan en un proyecto de investigación aprobado por el Comité de Ética en Investigaciones del Instituto Nacional de Cancerología, tal como consta en el acta N° 026 del 21 de septiembre de 2011.
Materiales y métodos
Selección de escalas disponibles
Se realizó una búsqueda manual en medios electrónicos de diferentes escalas en idioma inglés o español que evaluarán no solo la presencia de síntomas gastrointestinales en el paciente oncológico, sino también su frecuencia o intensidad. La mayoría de las escalas encontradas fueron diseñadas para la medición de calidad de vida en pacientes oncológicos y en general incluían pocos ítems relacionados con los síntomas de interés (EORTC QLQ-C30, ECOG, FACT-G, la escala de Karnofsky y el cuestionario RSCL) 16,18,19,22,23. En el proceso de búsqueda se encontró la escala desarrollada por el Instituto Nacional de Cáncer de los Estados Unidos, conocida como CTCAE versión 4.02 24, que se consideró la más completa pues contenía todos los ítems asociados al sistema gastrointestinal y a desórdenes metabólicos y nutricionales, por lo que esta evalúa tanto presencia como frecuencia o intensidad de los mismos.
Selección de los ítems
El objetivo de esta etapa fue identificar y seleccionar los ítems a incluir a partir de la escala CTCAE versión 4.02, la cual permite notificar la presencia y medir la frecuencia o gravedad de eventos adversos asociados al tratamiento antineoplásico.
La identificación y selección de los ítems se efectuó por medio de un consenso informal, realizado por un comité técnico conformado por seis profesionales con experiencia en el área clínica oncológica, siendo estos un médico epidemiólogo experto en validación de escalas, dos enfermeras especialistas en enfermería oncológica y tres nutricionistas dietistas. Los ítems fueron seleccionados teniendo en cuenta tres aspectos: a) la revisión de literatura sobre los principales síntomas gastrointestinales descritos en pacientes con cáncer sometidos a quimioterapia 4,5,8,11,13,25,26; b) la concordancia entre los síntomas gastrointestinales encontrados en la revisión de la literatura y los existentes dentro de la escala CTCAE versión 4.02 24, y c) la posibilidad de los síntomas de repercutir sobre el estado nutricional de los pacientes. El proceso finalmente resultó en la selección de 14 de 118 ítems o síntomas gastrointestinales secundarios o asociados al tratamiento con quimioterapia citotóxica, que cumplieron simultáneamente con los tres criterios de selección. Los síntomas seleccionados, en orden, fueron: náusea, vómito, diarrea, estreñimiento, xerostomía, disfagia, mucositis, queilitis, disgeusia, saciedad precoz, distensión abdominal, flatulencia, anorexia y dolor abdominal.
Traducción de ítems seleccionados
El proceso de la adaptación transcultural se realizó siguiendo los pasos y recomendaciones del manual ISPOR (por sus siglas en inglés) y del grupo de calidad de vida EORTC (por sus siglas en inglés) 27,28. Como primer paso se contactó a los desarrolladores del instrumento, quienes informaron que este era de uso libre, por tanto, se dio curso al proceso de traducción y adaptación del mismo.
Traducción directa:
De los ítems o síntomas seleccionados del documento original CTCAE versión 4.02, se realizaron dos traducciones del inglés (idioma original de la escala) al español, de manera independiente por dos personas calificadas para este fin (un traductor certificado por el Ministerio de Educación Nacional de Colombia y un nativo de país de habla inglesa). Luego de este proceso, el comité técnico analizó la equivalencia de las dos traducciones y generó por consenso una versión del documento en idioma español.
Traducción inversa:
La versión del documento en español, generada en la etapa previa, se tradujo nuevamente al inglés (idioma original de la escala) de manera independiente por dos personas expertas en traducciones científicas (un traductor oficial vinculado con el Instituto Nacional de Cancerología de Colombia y un experto en traducciones científicas). Estos traductores tenían desconocimiento de la estructura de la versión original.
Revisión de las versiones resultantes de la traducción inversa:
El comité técnico analizó ambas traducciones y procedió teniendo en cuenta dos criterios: 1. En caso de encontrar dos traducciones idénticas, no se efectuó ningún cambio. 2. En caso de identificar diferencias entre las dos traducciones, se eligió la traducción más ajustada a la versión original en inglés para asegurar la equivalencia semántica al contexto cultural colombiano. Como resultado de este paso, se generó por consenso una nueva versión del componente de sintomatología gastrointestinal de la escala CTCAE versión 4.02, adaptada al contexto cultural colombiano y equivalente a la versión original. Para facilitar la aplicación del instrumento en cada uno de los ítems, se incorporaron preguntas orientadoras para facilitar la manera de explorar cada uno de los síntomas.
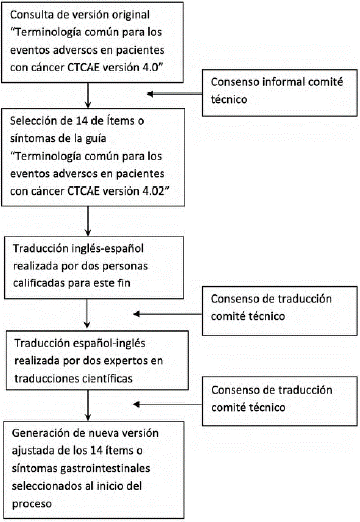
Todo el anterior proceso se ilustra en la figura 1.
Prueba piloto al instrumento
Selección de los participantes
En la fase preliminar o piloto de la adaptación transcultural del componente de síntomas gastrointestinales de la escala CTCAE Versión 4.02, se trabajó con una muestra de 25 pacientes que asistieron en forma ambulatoria al programa "Hospital Día" del Instituto Nacional de Cancerología (Bogotá, Colombia) entre noviembre de 2012 y enero de 2013. Estos fueron seleccionados con criterio no probabilístico, de conveniencia, entre quienes presentaban las siguientes características: a) tener diagnóstico confirmado de cáncer, b) ser mayor de edad, c) estar en tratamiento quimioterapéutico o próximo a iniciar quimioterapia, d) haber aceptado participar voluntariamente en este componente del estudio.
Realización de la prueba piloto
Los objetivos de la prueba piloto fueron: a) verificar que los ítems seleccionados sí reflejaran los síntomas gastrointestinales experimentados por los pacientes, b) determinar la comprensión de los ítems y la necesidad de explicación por parte del entrevistador, c) establecer el tiempo promedio empleado para contestar el total de preguntas, d) determinar la dificultad para responder las preguntas, e) evaluar el eventual grado de confusión, molestia u ofensa que pudieran generar los ítems, f) recibir sugerencias del paciente sobre la utilización de palabras más fácilmente comprensibles o el refraseo de ítems que facilitara la comprensión. Para documentar cada uno de los anteriores puntos se diseñó un formato que, para cada uno de los ítems, consideraba las respuestas y comentarios aportados por el paciente.
La aplicación, tanto del instrumento de medición de síntomas gastrointestinales como del formato de comprensión, fue efectuada por un profesional en salud nutricionista-dietista. El desarrollo de la prueba piloto se efectuó en cuatro momentos diferentes, así: 1) La primera prueba de aplicación de ambos componentes se realizó en 10 pacientes y generó la primera serie de modificaciones técnicas. 2) La segunda aplicación consistió en aplicar los formatos modificados a 10 pacientes diferentes (todos ellos para primera quimioterapia) y derivó en una segunda serie de ajustes técnicos. 3) La tercera aplicación se efectuó en 5 pacientes diferentes, en quienes se utilizaron los formatos doblemente modificados, la cual evidenció problemas de comprensión en dos síntomas. 4) La cuarta aplicación, efectuada en 5 pacientes (4 diferentes y 1 repetido), verificó y ajustó los problemas de comprensión evidenciados en la fase previa. Como resultado final de los cuatro pasos realizados se logró obtener la escala definitiva.
Resultados
Traducción de los ítems
Al realizar la traducción de los ítems solo se encontró una discordancia en el síntoma swelling, para el cual se propusieron los términos "hinchazón" o "saciedad precoz". Posterior a la aplicación de la prueba piloto, el comité técnico estableció para este síntoma la denominación "sentirse lleno rápidamente", como se muestra en el Anexo 1.
En la traducción inversa del español colombiano al inglés no se encontraron discordancias que hicieran necesaria la revisión de la traducción del cuestionario.
Caracterización de los pacientes
Trece (52%) de los pacientes eran del sexo masculino; con media de edad de 54,2 años (desviación estándar ± 15,3 años). Los cánceres más frecuentes entre los pacientes fueron: colorrectal (28%), estómago (16%), mama (12%), linfomas y cérvix (8% cada uno). El nivel de escolaridad mayormente observado fue el de educación básica primaria (68%); el 88% de los pacientes tenían tratamiento exclusivo con quimioterapia (tabla 1).
Tabla 1 Características sociodemográficas y clínicas de la muestra
| n | porcentaje | |
|---|---|---|
| Género | ||
| Masculino | 13 | 52 |
| Femenino | 12 | 48 |
| Edad | Media = 54,2 años (DE = 15,3 años) | |
| Nivel de escolaridad | ||
| Ninguno | 1 | 4 |
| Primaria | 17 | 68 |
| Secundaria | 6 | 24 |
| Universitario | 1 | 4 |
| Localización del tumor | ||
| Colorrectal | 7 | 28 |
| Estómago | 4 | 16 |
| Mama | 3 | 12 |
| Linfoma | 2 | 8 |
| Cérvix | 2 | 8 |
| Testículo | 1 | 4 |
| Óseo | 1 | 4 |
| Senos paranasales | 1 | 4 |
| Ovario | 1 | 4 |
| Próstata | 1 | 4 |
| Esófago | 1 | 4 |
| Sarcoma | 1 | 4 |
| Tipo de tratamiento | ||
| Quimioterapia | 22 | 88 |
| Quimioterapia más radioterapia | 3 | 12 |
Prueba piloto
Todos los síntomas gastrointestinales de la escala fueron experimentados en menor o mayor medida por todos los pacientes, es decir, ningún síntoma de la escala estuvo fuera del objeto de evaluación; así mismo, los pacientes no manifestaron algún otro síntoma gastrointestinal particular que ameritara su evaluación o inclusión en la escala. Adicionalmente, se reportaron los siguientes datos de importancia:
Para el 100% de los pacientes fueron comprensibles los términos referentes a los síntomas: náusea, vómito, estreñimiento, diarrea, anorexia y dolor abdominal.
Todos los encuestados necesitaron explicación por parte del entrevistador, debido al desconocimiento del significado de los términos referentes a los síntomas: xerostomía, disfagia, mucositis, queilitis y saciedad precoz. Debido a lo anterior, luego de la prueba piloto estos términos se reemplazaron por las palabras: boca seca; dificultad para pasar; inflamación, placas o llagas al interior de la boca; inflamación o grietas en los extremos de los labios; sentirse lleno rápidamente.
Dado que cada pregunta formulada para evaluar cada síntoma gastrointestinal indagaba por la presencia y por la frecuencia o intensidad de este, debido a que hubo confusión en algunos participantes respecto a la palabra "intensidad", como resultado de la prueba piloto se decidió eliminar esta palabra de la escala definitiva y centrar la pregunta en la presentación o en la frecuencia del mismo.
El 28% de los pacientes evaluados presentaban patología oncológica colorrectal y habían recibido quimioterapia como esquema adyuvante posterior a la realización de una colostomía. Derivado de lo anterior, como resultado de la prueba piloto se consideró pertinente adicionar en la escala definitiva, en la medición del síntoma de "diarrea", el número de veces que la bolsa colectora se llenaba.
Se determinó que el tiempo promedio de aplicación del instrumento fue de 5 minutos. Al 90% de los pacientes participantes les pareció adecuado el tiempo utilizado para responder la encuesta y al 10% les pareció muy largo.
Cabe aclarar que, tanto en la escala original como en la formulación inicial de la versión adaptada de la escala, seis de los síntomas gastrointestinales (vómito, diarrea, estreñimiento, disfagia, mucositis oral y anorexia) incluían la categoría de respuesta "muerte". Sin embargo, producto de la primera prueba de aplicación, el comité técnico acordó que la medición de los síntomas sería tipo Likert, con puntuación de cero hasta tres según la presencia o severidad del mismo, excluyendo a la categoría "muerte" debido a que las preguntas fueron reformuladas para ser aplicadas en primera persona a cada paciente. Las modificaciones realizadas a la escala luego de cada momento de aplicación durante la prueba piloto fueron las siguientes:
Momento 1. Se ajustaron las definiciones de los síntomas para hacerlos más comprensibles. Para la pregunta ¿Cuál es la intensidad de las náuseas? se retiraron de las opciones de respuesta las palabras "desnutrición o deshidratación". Para la pregunta ¿Cuál es la intensidad del vómito? se modificó en las opciones de respuesta la frase "separado por 5 minutos" por "separado por al menos 5 minutos". Adicionalmente, en seis de los síntomas se retiró la opción de respuesta "Muerte", dada la aplicación presencial del instrumento (lo cual se explicó antes). Para la pregunta "¿Ha presentado sequedad en la boca (xerostomía) en los últimos 7 días?" se retiraron de las opciones de respuesta los términos tendientes a cuantificar la cantidad de saliva en ml/min y se cambió la frase "saliva seca" por "boca seca". En la pregunta "¿Cuál es la intensidad de la mucositis oral?" se ajustó la opción de respuesta dejando "Presenta dolor" en lugar de "Presencia de dolor". En la pregunta relacionada con saciedad precoz, se modificaron la formulación del ítem y su estructura de medición (Anexo 1).
Momento 2. Los términos técnicos (xerostomía, disfagia, mucositis, queilitis, disgeusia y saciedad precoz) fueron reemplazados por su respectiva definición para facilitar su comprensión. Adicionalmente, el sistema utilizado para calificar la intensidad fue presentado de una manera más concreta (Anexo 1).
Momento 3. Se detectaron dos síntomas (estreñimiento y dolor abdominal) que fueron considerados como confusos por algunos pacientes. Por tal razón, estos síntomas fueron seleccionados para ser nuevamente evaluados en una fase posterior.
Momento 4. En este momento los participantes validaron la comprensión de los síntomas escogidos en el paso anterior y se generó la versión final del instrumento (Anexo 1).
Discusión
Existe la necesidad de disponer de escalas o cuestionarios de práctica clínica adaptados a nuestra cultura para evaluar diversos aspectos de salud en pacientes con cáncer. Hasta donde tenemos conocimiento, en nuestro país, en el área de nutrición en pacientes oncológicos, no existen instrumentos adaptados transculturalmente y validados para medir síntomas gastrointestinales asociados a tratamiento quimio-terapéutico. En 2017 se publicó la Guía de práctica clínica para la atención y el soporte nutricional del paciente oncológico adulto hospitalizado, pero esta no contempla la medición de síntomas gastrointestinales 29.
Este estudio sería el primero que se realiza en el país para disponer de un instrumento que permita medir de manera válida y confiable los síntomas gastrointestinales secundarios al tratamiento quimioterapéutico en pacientes ambulatorios.
En el diseño o adaptación de un instrumento de valoración en el ámbito clínico, el proceso de selección de ítems o síntomas es el primer paso, y es el más importante; luego, por medio de este, se efectúan las pruebas preliminares en sujetos con características muy similares a las de la población en la que se quiere aplicar el instrumento.
Después de realizar la adaptación transcultural del componente de síntomas gastrointestinales de la escala CTCAE versión 4.02 en pacientes ambulatorios tratados con quimioterapia, se considera que esta herramienta posee un gran potencial de uso en el ámbito clínico y de investigación, dado que los avances alcanzados respecto al tratamiento del cáncer indican la disminución de las tasas de mortalidad de los pacientes oncológicos y el incremento de los periodos libres de enfermedad o de recaída tumoral 30, sin que se logre evitar que los pacientes padezcan los efectos tóxicos y las secuelas asociadas con los tratamientos antineoplásicos suministrados.
Mejorar la calidad de vida de los pacientes con enfermedad oncológica es una prioridad de los cuidados integrales, que puede alcanzarse a través de evaluaciones sistemáticas y frecuentes, que permitan detectar oportunamente las necesidades y problemas del paciente. Tales evaluaciones deberán estar soportadas en la adecuada comunicación y monitorización de los cambios en la sintomatología gastrointestinal con potencial para repercutir en el estado nutricional y en las respuestas a los tratamientos contra el cáncer 31.
Además, durante el proceso de adaptación de esta escala, la participación de pacientes oncológicos sometidos a tratamiento con quimioterapia y de profesionales de la salud expertos en el tema fue un insumo valioso para asegurar la inclusión de los síntomas gastrointestinales más relevantes dentro de la escala que se estaba adaptando 4,5,8,11,13,15,25,26.
Durante el proceso, los pacientes pudieron comprender el significado de cada síntoma, dar cuenta de sus experiencias y de la frecuencia o intensidad de los mismos. Se cumplió entonces el objetivo planteado al ejecutar la prueba piloto, el de evaluar la pertinencia de la traducción y adaptación transcultural de una escala que pretende indagar de forma completa y sencilla sobre la sintomatología gastrointestinal que experimentan los pacientes oncológicos ambulatorios tratados con quimioterapia, empleando un lenguaje fácil de entender y adaptado a nuestro medio. Esto último se refuerza por el hecho de que más del 70% de los pacientes tenían niveles educativos bajos (básica primaria o ninguna).
El propósito de la prueba piloto de la escala de evaluación de síntomas gastrointestinales no solo consistió en establecer y cuantificar su presentación, sino también en promover una comunicación adecuada entre el paciente y el profesional de la salud, requerida para orientar un manejo médico y nutricional más acertado en este tipo de pacientes 32.
El hecho de haber trabajado con una muestra conformada principalmente por pacientes con bajo nivel educativo, lleva a pensar que en esta podrían coexistir variables socioculturales con una distribución diferente a la que presentarían en la población en la que se pretende aplicar la escala en un futuro, lo cual puede ser una limitación de este estudio.
Aunque este estudio se basó en la versión 4.02 de la escala CTCAE, la versión actualmente disponible (V 5.0) cuenta con los mismos ítems incluidos en la presente adaptación transcultural y solo cambian las categorías relacionadas con el manejo de un síntoma específico (vómito) 33.
Como se mencionó, no tenemos información de que en el país se hayan desarrollado o validado instrumentos para medir síntomas gastrointestinales secundarios al tratamiento quimioterapéutico en pacientes ambulatorios. En el contexto colombiano existen varios reportes de adaptaciones transculturales de instrumentos utilizados para medir diferentes dimensiones en pacientes con cáncer 34-40. En dichos estudios es un común denominador que, en el primer paso del proceso de adaptación transcultural (paso de traducciones), las discrepancias entre las traducciones, tanto directas como inversas, son escasas. Esto contrasta con la fase de estudio piloto, en la cual se suelen plantear ajustes especialmente relacionados con los términos técnicos asociados con síntomas 35,37. Comparado con lo publicado en otras adaptaciones transculturales en pacientes con cáncer en Colombia, resulta llamativo que en los estudios que no incorporan la exploración de síntomas clínicos 39, en la fase de estudio piloto los pacientes no refieren mayores dificultades en la comprensión de la escala; este hallazgo debe tenerse en cuenta al momento de diseñar instrumentos que incorporen características clínicas que, aunque en el ámbito del personal de salud se manejan utilizando términos técnicos aparentemente de fácil comprensión, al ser aplicados a los pacientes deben someterse a un proceso de ajuste para que estos los puedan comprender fácilmente.
El siguiente paso, correspondiente a la validación de la escala de evaluación y seguimiento de sintomatología gastrointestinal, requiere un proceso más complejo en cuanto al tamaño de la muestra y los procedimientos de análisis estadístico para determinar sus propiedades de medición