Introducción
El cáncer de mama ocupa el segundo lugar de incidencia de cáncer en Perú. En Estados Unidos, sólo en población de origen hispano, ocupa el primer lugar, con 19,800 casos al año 1. En el reporte de GLOBOCAN 2020 se diagnosticaron a nivel mundial 2 261 419 (11.7%) casos nuevos, ocupando el 1er lugar en incidencia y el 4to en mortalidad 2. En estudios de mujeres estadounidenses de origen latino, así como de países con etnia indígena (Colombia, Perú, México), existe una alta prevalencia de sobreexpresión de HER2 en cáncer de mama, asociada a variantes genéticas en estudio 3. En los últimos años se busca conocer la correlación de variables moleculares con la supervivencia. Esto definirá grupos con mayor probabilidad de beneficio terapéutico.
La clasificación clínica y molecular del cáncer de mama se basa en la presencia de receptores (proteínas), como estrógenos, progesterona y HER2/ neu (human epidermal growth 2/neuro glioblastoma). La inmunohistoquímica es un estudio histopatológico basado en la formación molecular de antígenos-anticuerpos 4. Este método determina los subtipos de cáncer de mama como parte de su expresión genética 5. La amplificación del receptor Her2/ neu se ha estudiado utilizando diferentes métodos analíticos, además de la inmunohistoquímica, como los métodos Southern, Western-blot, ELISA (enzyme-linked immuno assay) y FISH (Fluorescent In Situ Hybridization).
La clasificación molecular del cáncer de mama distingue 4 subtipos o categorías 5. El Luminal A presenta receptores de estrógenos y progesterona positivos, Her2 negativos y Ki67 bajos (para ser considerados altos o bajos, tiene un punto de corte del 20%). El subtipo Luminal B se divide en: Luminal B-Her2 negativo (receptores de estrógeno positivo y alto Ki67 o receptor de progesterona negativo o bajo) y Luminal B-Her2 positivo (receptores de estrógeno y Her2 positivo, independientemente de los niveles de Ki67 o progesterona). Los otros dos subtipos son Her2/ neu sobreexpresado y triple negativo.
Mundialmente, la aplicación de la Clasificación molecular se considera canónica para pacientes con cáncer. En algunas regiones de América Latina, como zonas rurales de Perú, no se pueden implementar por falta de tecnología local. La etnia indígena es un grupo vulnerable por tener menor capacidad adquisitiva para servicios de salud y por su negativa cultural a trasladarse a otras ciudades alejadas, donde sí se cuente con esta tecnología. Es relevante considerar extender el uso de la técnica de anticuerpos monoclonales, en un hospital cercano al lugar de residencia, lo cual evitaría la referencia del paciente a hospitales de Lima.
Este estudio tiene como objetivo aplicar la técnica de inmunohistoquímica en tumores de pacientes de etnia indígena nativa del sur de Perú, en un hospital cercano a su lugar de residencia. También se busca correlacionar la supervivencia global, según si se sobre expresa el receptor Her2/neu, en correlación al estadio clínico TNM (Tumor, nódulo y metástasis) 6. Conocer este escenario brinda un mayor rango de alternativas terapéuticas, dado que proporciona una base racional para el uso de anticuerpos monoclonales en este grupo de pacientes. La desventaja sobre otras técnicas es el alto costo, pero su implementación gratuita en el hospital donde fue realizado el estudio lo convertiría en un beneficio para las pacientes.
Pacientes y Métodos
Casos estudiados
Los criterios de inclusión fueron: tener diagnóstico anatomo-patológico de adenocarcinoma de mama, historia clínica completa y disponer de suficiente material biológico (muestra en parafina mayor a 5 mm), obtenidas de biopsias incisionales o muestras quirúrgicas, así como pertenecer a la etnia quechua. Los 3 principales criterios para considerarlos parte de este grupo étnico fue tener la lengua quechua como idioma materno, autoidentificarse como parte cultural de esta comunidad y rasgos físicos compatibles con la raza americana autóctona. El criterio de exclusión era no tener realización de prueba FISH. Este requisito era necesario sólo en pacientes Her2/neu 2 (+), debido al alto nivel de falsos positivos, lo cual requiere ser confirmado con una técnica validada 5 7 8 9.
Se identificaron 30 casos, siendo posteriormente reducidos a 23. Los 7 casos excluidos lo fueron por no cumplir con alguno de los criterios de inclusión. Las 23 pacientes pertenecían a la etnia indígena quechua, de la zona andina del sur de Perú, en la ciudad de Arequipa, localizada a una altitud de 2.235 metros sobre el nivel del mar. Las pacientes tuvieron un tiempo de seguimiento prospectivo de 3 años (36 meses), iniciando la inclusión desde noviembre del 2016, culminando el seguimiento en junio del 2020. No hubo datos censurados por pérdida de sujetos. El análisis por inmunohistoquímica de los tumores se realizó en el Hospital Carlos Seguín Escobedo, de la ciudad de Arequipa.
Para ser reportadas como 2 (+) las células deben retener el anticuerpo en la membrana celular, haciendo una tinción completa y cubriendo entre 10% y 30%, del componente citológico visto bajo el microscopio. Sólo este subgrupo requiere confirmación con FISH. Los reportes por inmunohistoquímica 3 (+), se consideran positivos para sobreexpresión y no requieren FISH.
Inmunohistoquímica
Se usó el Test comercial Dako HercepTest® para el proceso de inmunohistoquímica. Se realizaron cortes de muestras parafinadas, usando un micrótomo manual, con posterior montaje sobre portaobjetos. Tras someter a calor de 65°C, se sumergieron en xileno para eliminar la parafina. Los tejidos se rehidrataron sobre el portaobjetos y se lavaron con agua destilada, sumergiéndolos a continuación en una solución acuosa de peróxido al 3% durante 3 minutos. El tampón Tris se usó para enjuagar el tejido. La fase de recuperación de calor se realizó con tampón de citrato durante 40 minutos a 95°C. Luego se llevó a temperatura ambiente, colocando los portaobjetos en tampón Tris-Saline. El anticuerpo primario de ratón se añadió a la sección de tejido, durante 1 hora. Posteriormente, el tejido se lavó con tampón Tris y se procedió a incubar con anticuerpo biotinilado durante 10 minutos. La reacción primaria entre el antígeno y el anticuerpo para HER2/neu se amplifica con este anticuerpo secundario biotinilado. Después de nuevamente enjuagar con tampón Tris, se añadió una solución de cromógeno, 3,3'-diaminobencidina, tampón Tris y H2O2 (0,016%). La reacción química debe ser demostrada con la formación del complejo estreptavidina-peroxidasa, así como con la posterior adición del cromógeno de diaminobencidina. A continuación los portaobjetos se lavaron con agua destilada.
Al evaluar la muestra sobre el portaobjetos, a través del microscopio, se evidencia un patrón de tinción específico, de acuerdo al perfil molecular. El Gold stándar para calificar el resultado de inmunohistoquímica es la observación al microscopio hecha por un médico especialista (anatomopatólogo).
Análisis Estadístico
La validación de resultados técnicos se hizo con el Coeficiente kappa de Cohen. La prueba exacta de Fisher se utilizó para evaluar las variables categóricas. La supervivencia global se calculó utilizando el método de Kaplan-Meier y se comparó con la prueba de Logrank. Todos los datos se analizaron utilizando IBM® SPSS® versión 16.
Resultados
La evaluación de HER2/neu se realizó de acuerdo con las recomendaciones definidas y actualizadas por la Sociedad Americana de Oncología Médica 8. Se evaluaron treinta muestras biológicas, correspondientes a tumores del mismo número de pacientes. Se excluyeron siete (seis debido a un informe inmunohistoquímico incompleto y una debido a no tener antecedentes clínicos en el archivo). Los casos notificados como 2 (+) tuvieron confirmación por la técnica FISH, para disminuir la posibilidad de falsos positivos 9.
En nuestro estudio, la concordancia fue 100% respecto al realizado con la misma muestra, informada por uno o dos médicos especialistas (según protocolo del hospital, puede solicitarse una segunda opinión si un resultado no es concluyente para un solo anatomopatólogo). Las 23 muestras mostraron concordancia.
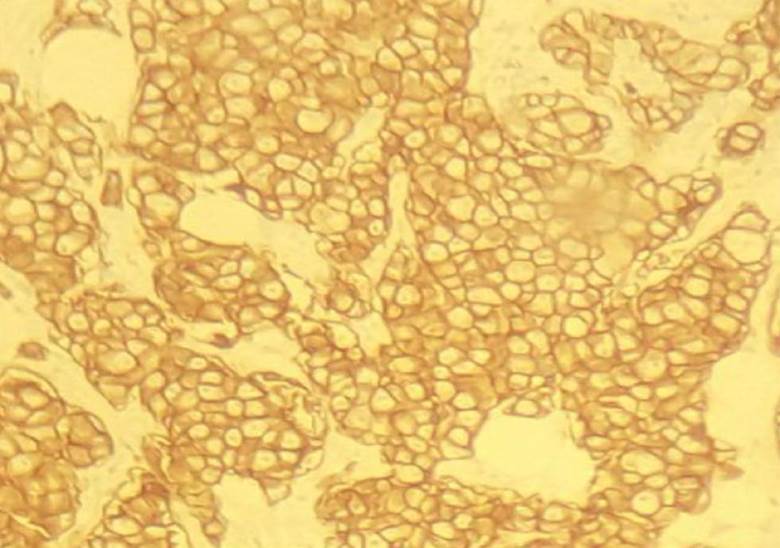
En la Figura 1 se presenta un caso con sobreexpresión del receptor Her2/neu. El anticuerpo monoclonal se deposita en más del 90% de la membrana celular, delimitando los espacios celulares, en los que no se observa el núcleo. Algunas células neoplásicas tienen formas gigantes con núcleos en división, lo cual es característico de la mayoría de las neoplasias indiferenciadas.
Fuente. elaboración propia
Figura 1 Muestra de tejido tumoral de mujer indígena de 48 años, con cáncer de mama EC IIIB, HER2/neu positivo. La tinción con inmunohistoquímica fue realizada con anticuerpos monoclonales de ratones (DAKO). La membrana celular está fuertemente teñida en más del 90%, solo en células tumorales. Amplificación: 10*40IAN: 0,95.
En la Tabla 1 se muestran los resultados considerando dos indicadores: estadio clínico y clasificación molecular. Cuando el resultado se informa como 0 y 1 (+), se consideran HER2 negativos. Las muestras con resultado 3 (+) califican como HER2/neu positivo.
Tabla 1 Características moleculares del tumor y estadio clínico de pacientes con Cáncer de Mama
| Indicador | Categoría | HER2/Neu | |
|---|---|---|---|
| Negativo n° (%) | Positivo | ||
| HER2/NEU | Sobreexpresión por anticuerpos monoclonales | 13 (56,6%) | 10 (43,4%) |
| Estadio TNM | -In situ | 1 (7,6) | 0 |
| -I | 5 (38,4) | 0 | |
| -II -III | 4 (30,7) 1 (7,6) | 3 (30) 4 (40) | |
| -IV | 2 (15,3) | 3 (30) | |
| TOTAL | 13 (100) | 10 (100) | |
| Clasificación Molecular | -Luminal A | 3 (23,1) | 0 |
| -Luminal B* | |||
| a) Her/neu (-) | 6 (46,2) | 0 | |
| b) Her/neu (+) | 0 | 6 (60) | |
| -Her/neu positivo | 0 | 4 (40) | |
| -Triple Negativo | 4 (30,7) | 0 | |
| TOTAL | 13 (100) | 10 (100) | |
* La categoría Luminal B se divide en dos subgrupos, dependiendo si son positivos para Her2/neu (6 casos) o negativos (6 casos).
Fuente. elaboración propia
Hubo 13 casos con receptor negativo Her2/neu (56,6%). La mayoría se presentan en estadio clínico in situ, I y II (10 casos), es decir, con buen pronóstico. Los casos positivos fueron 10 (43,4%). Estos pacientes fueron estadificados principalmente en las peores etapas de pronóstico (III y IV), con 7 casos.
El EC (estadio clínico) TNM se correlaciona con la probabilidad de muerte, dependiendo de la sobreexpresión del receptor HER2/NEU (Tabla 2). Este indicador clínico de pronóstico puede dividirse en dos subgrupos, según si tiene mejor sobrevida global. De este modo, el temprano incluye al cáncer in situ, EC I y II. El de peor pronóstico suele comprender el avanzado (EC III y IV).
El valor p para TNM fue 0.017. La regla de decisión es rechazar la hipótesis nula de correlación entre los casos positivos y el estadio clínico de mal pronóstico (III y IV), de acuerdo a si p<0.05. Debe evitarse cometer un error tipo I (falso positivo) si esta hipótesis nula se rechaza, siendo verdadera. Si el valor p es más bajo que el nivel de significancia, entonces puede ser rechazada. Con un p=0.017 (<0.05) la hipótesis nula puede ser rechazada.
Tabla 2 Estadio Clínico según Sobreexpresión del receptor HER2/Neu
| Indicador | Categoría | Neg n° (%) | HER2/Neu Positivo n° (%) | P |
|---|---|---|---|---|
| Estadio TNM* | Estadio clínico temprano | 10 (77%) | 3 (30) | |
| Estadio clínico avanzado | 3 (23%) | 7 (70) | 0.017 | |
| TOTAL | 13 (100) | 10 (100) |
* El estadio clínico TNM se puede dividir en dos subgrupos: temprano (incluye cáncer in situ, I y II) y avanzado (III y IV). Fuente. elaboración propia
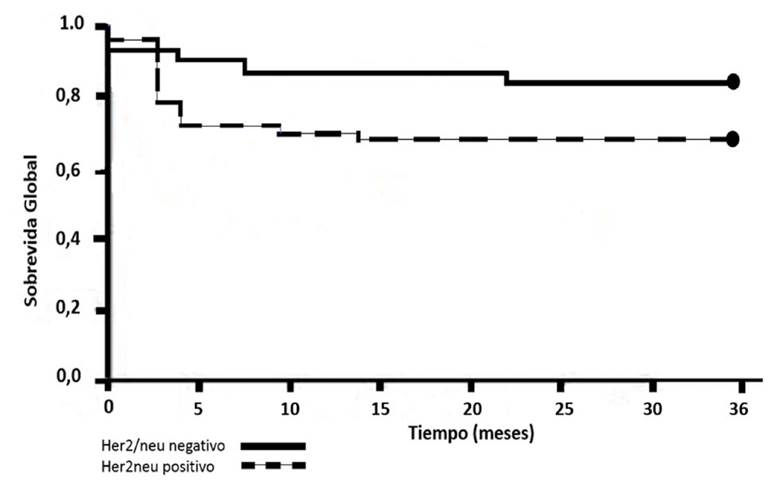
La evaluación de la supervivencia global, se realizó a través de las curvas de Kaplan-Meier (Figura 2). Se describe como un gráfico de curva de supervivencia, en la que el número de fallecidos están en el eje vertical y el tiempo en el horizontal. Cada escalera corresponde al evento "muerte". La curva superior de los casos negativos para sobreexpresión de Her2/ neu muestra una experiencia de supervivencia más favorable.
La supervivencia global a los 3 años fue del 69,9% para los HER2/neu positivos y 84,6% para los negativos. La diferencia es estadísticamente significativa (p=0,017).
Discusión
En este estudio, el 56,6% de tumores de pacientes con cáncer de mama de etnia indígena fueron negativos para sobreexpresión del receptor Her2/neu. La contraparte de pacientes con positividad tenía mayor tendencia a diagnosticarse en estadios clínicos avanzados. La inmunohistoquímica en tumores de este grupo de pacientes era necesaria para caracterizarlas adecuadamente.
El estudio del oncogén HER2/neu se evalúa mediante inmunohistoquímica, según protocolos y consensos mundiales 4 7 8 9. El costo económico de la técnica es elevado, lo cual la hace inaccesible para pacientes de bajos ingresos, como los grupos étnicos indígenas del Perú. Este inconveniente se ve aun más reforzado por las pocas instituciones que lo realizan, lo cual obliga a que las pacientes sean referidas a hospitales alejados. En Arequipa, antes de disponer de esta tecnología, las pacientes debían acudir a instituciones públicas de Lima o privadas. Según nuestra investigación, la técnica de inmunohistoquímica en Arequipa es factible, sin costo alguno para las pacientes ya que la institución donde se realizó el estudio está diseñada para personas con seguro laboral. De este modo se evita que deban ser referidas a otras ciudades o deban realizarlo en instituciones privadas.
Recientemente, se ha introducido un nuevo método basado en la amplificación cuantitativa de Her2 por PCR (polymerase chain reaction). Posiblemente se convierta en la prueba estándar en el futuro cercano, debido a su prontitud de realización y concordancia con inmunohistoquímica y FISH 10. Sin embargo, la mayoría de protocolos no lo incluyen rutinariamente 8 9.
El cáncer de mama es una enfermedad heterogénea, con una historia natural diferente para cada subtipo 7. La importancia de determinar la proteína Her2/ neu viene dada por su utilidad terapéutica. El tratamiento con anticuerpos monoclonales (terapia biológica) con o sin quimioterapia sistémica, ha mejorado la sobrevida global en oncología 11.
En nuestra investigación, el grupo de casos con sobreexpresión del receptor comprende 43,4%. Estas pacientes son las que podrían beneficiarse del uso de anticuerpos monoclonales. En mujeres estadounidenses de origen latino, así como en países latinoamericanos con etnias indígenas y mixtas (Colombia, México) y en la base de datos de Lima, la sobreexpresión de HER2 fue 30% 3. Estos resultados son mayores al reportado en un estudio australiano, con población mayormente caucásica, donde la sobreexpresión fue del 23,8% 12. En estudios previos realizados en Perú, sin mencionar el grupo étnico, se encontró un porcentaje similar al nuestro, con 41% de 117 casos estudiados, estando el 66% asociado con un grado histológico alto 13.
El mayor porcentaje de casos está representado por el grupo Her2/neu negativo, con 56,5%. Este resultado es consistente con las estadísticas de otros estudios, como el metaanálisis de Telli et al, donde las mujeres de origen chino representaban el 64%, las coreanas el 49% y las vietnamitas el 57% de los casos negativos 14. En Perú, este porcentaje alcanza el 82% de 280 pacientes evaluados, sin mencionar el grupo étnico 15. Las actualizaciones globales aconsejan identificar estas poblaciones, ya que tiene un impacto en la orientación terapéutica 5, en base a quimioterapia o terapia biológica hacia otros receptores no asociados al Her2/neu.
En otros países, con mínima población indígena nativa o migrante, el porcentaje de sobreexpresión es más bajo al de nuestro reporte, como en España, donde 1520% son casos positivos 16. En Cuba, el porcentaje es aun más bajo, con 198 muestras biológicas evaluadas, de las cuales sólo 10,6% fueron Her2/neu positivos 17. En un estudio realizado en China, este mismo grupo mostraba similitud con nuestros resultados, con 65,1% (762 casos) 18.
En nuestra evaluación, de acuerdo con el indicadorTNM, los pacientes Her2/neu positivos se correlacionaron con las etapas de pronóstico más desfavorables (III-IV). El único criterio de asociación fue la sobreexpresión del receptor, habiendo distribución uniforme con otras variables (lugar de residencia, edad, religión, edad de menarquía, índice de masa corporal y nivel de instrucción). En España, cuando se evaluaron todos los tipos moleculares, incluidos el luminal y el triple negativo, las tasas de mortalidad eran mayores para los que tenían sobreexpresado el receptor Her2/neu 19. En Colombia se reportaba la misma tendencia, independientemente si la evaluación molecular se realizaba por inmunohistoquímica o FISH 20. Lo mismo ocurre en Francia, donde canónicamente ya es considerado un factor de mal pronóstico, pero la importancia actual de identificar poblaciones específicas se da porque predice la respuesta al tratamiento con anticuerpos monoclonales 21. En México, los pacientes Her2/neu positivos (25,6% de 125 casos) representaron el grupo con mayor porcentaje de metástasis durante el seguimiento 22.
En Australia, país con población de origen europeo y aborígenes del Estrecho de Torres, la sobreexpresión de Her2/neu también se asocia con un peor pronóstico 23; sin embargo, tanto en este país como en todos los protocolos a nivel mundial, esta característica puede ser revertida con el uso de anticuerpos monoclonales. Esto explica la importancia de realizar la estadificación molecular. En Perú, los estadios clínicos III y IV tienden a tener más casos Her2/neu positivos, lo que explica porque la sobrevida global sea de 70 meses, en comparación con los mismos estadios en luminal A y B, con un poco más de sobrevida (72 meses) 15.
En países con poblaciones de origen caucásico e indígenas nativos, como Chile, evaluando muestras biológicas de 181 pacientes, los positivos para sobreexpresión mostraron mayor agresividad y menor supervivencia 24. En Colombia, país con poblaciones de origen africano, europeo, mestizos y nativos indígenas, se reportó que después de 46,6 meses de seguimiento, los pacientes con HER2 positivo, tenían peor pronóstico, identificando subgrupos clínicos y moleculares, como estadio III, menores de 40 años de edad, alto grado histológico y sin coexpresión de receptores hormonales 20.
En India, de 90 casos evaluados, el 30% correspondió a Her2/neu positivos y fueron los que mostraron el peor pronóstico 4. Incluso esta menor supervivencia afectó las primeras etapas clínicas. En Israel, de 58 casos evaluados, 21 fueron positivos para Her2/ neu (36%), y correspondieron principalmente a etapas metastásicas 25. En Perú, según el estudio de Medina, el grupo con la menor supervivencia fue el triple negativo, con 60 meses, seguido de Her2/ neu positivos, con 70 meses 15. En este mismo estudio, el grupo con el mejor pronóstico fue Luminal A, con sobrevida global de 72 meses (con diferencia significativa en la prueba LogRank, p=0.003).
Hay mayor porcentaje de casos con sobreexpresión HER2/neu en los tumores de mujeres indígenas evaluadas, con 43,4%, siendo el promedio mundial 20% 16. La falta de estudios específicos en este grupo de mujeres dificulta comparar porcentajes y definir como marco conceptual que la etnia tiene esta característica innatamente. La principal limitación del estudio fue el número de participantes. El único estudio en mujeres peruanas con resultado semejante (41%), no estadificó subgrupos que enmarcaran mujeres de etnia quechua 13. Este hallazgo requiere mayor ampliación de estudios antes de ser considerado un carácter biológico.
La importancia de los estudios en grupos específicos, como los étnicos, es identificar características que ayuden a pronosticar el status biológico. En última instancia, además del beneficio académico, lo importante es prever la terapéutica apropiada con base en la característica biológica. En cáncer de mama, los grupos que presentan mayor sobreexpresión del receptor HER2/neu son los que se benefician de aplicar anticuerpos monoclonales, incluso si es enfermedad avanzada. En Europa, el pronóstico mejora en las etapas metastásicas, cuando se aplica el tratamiento dirigido 26. En este último estudio de Witzel et al., realizado en población caucásica principalmente, la supervivencia general aumentó de 7,2 meses a 17,1 meses, cuando las pacientes recibieron anticuerpos monoclonales.
Conclusiones
La técnica de inmunohistoquímica con anticuerpos monoclonales puede ser realizada e implementada gratuitamente en biopsias o piezas quirúrgicas de tumores, de la población andina indígena de Arequipa. Este grupo étnico tiene poca disponibilidad económica de costearse el procedimiento, así como menor tendencia a desplazarse a ciudades alejadas de su lugar de residencia. Así mismo, este grupo de mujeres presentaba mayor porcentaje de tumores HER2 positivos que la población general, asociado posiblemente a una característica biológica innata, lo cual debe ampliarse con otros estudios. Al igual que poblaciones no andinas, también tenían mayor probabilidad de clasificarse en estadios clínicos III y IV, considerados de peor pronóstico